El aneurisma de la aorta abdominal es muy frecuente en nuestro medio y a nivel mundial, por lo que debe conocerse el manejo anestésico y sus implicaciones a largo plazo.
Objetivocomparar las técnicas anestésicas en pacientes con aneurisma de aorta abdominal llevados a reparación con prótesis endovascular entre enero 2009 a enero 2015 en el Hospital de San José de Bogotá.
Métodosestudio descriptivo retrospectivo de pacientes mayores de 18 años con aneurisma de aorta abdominal corregidos (EVAR) con prótesis endovascular excluyendo los rotos, los practicados de urgencia o con corrección de manera abierta.
Resultadosde 79 reparos endovasculares (EVARs) 58 (73,4%) fueron en hombres, los antecedentes más observados fueron hipertensión arterial (68,3%), enfermedad pulmonar obstructiva crónica (20,2%) y consumo de tabaco (15,1%). La técnica más utilizada fue anestesia local más sedación (50,6%), seguida de anestesia general (39,2%) y regional (10,1%); esta última mostró mayor estabilidad hemodinámica, menor requerimiento de vasopresores e inotrópicos. Hubo 33 (41,7%) complicaciones anestésicas.
Conclusionesla anestesia local más sedación fue la técnica más utilizada, con una mayor frecuencia en casos con comorbilidades. El tiempo anestésico y la estadía hospitalaria fue similar a la anestesia general, aunque con menores complicaciones; la regional requirió menor uso de vasopresores e inotrópicos.
Abdominal aortic aneurysm is very common in our country and worldwide, thus, an understanding of anesthetic management and anesthesia long-term implications is essential.
ObjectiveTo compare the anesthetic techniques used in patients who underwent prosthetic [stent-graft] endovascular abdominal aortic aneurysm repair between January 2009 and January 2015 at Hospital de San José in Bogotá.
MethodsA descriptive retrospective study including patients aged 18 years and older who had an EVAR. Those with ruptured aneurysms, who underwent emergency operations or open procedures, were excluded.
ResultsOut of 79 EVARs, 58 (73.4%) were performed in men, the most common antecedents were, hypertension (68.3%), chronic obstructive pulmonary disease (20.2%) and tobacco smoking (15.1%). Local anesthesia associated with sedation was the most frequently used technique (50.6%), followed by general anesthesia (39.2%) and regional anesthesia (10.1%); the latter provided greater hemodynamic stability and reduced need for vasopressor agents and inotropes. Thirty-three (41.7%) anesthesia complications were observed.
ConclusionsLocal anesthesia with sedation was the most frequently used technique predominantly in cases with concomitant comorbidities. Operating time and length of stay in hospital was similar to that of general anesthesia, with fewer complications; regional anesthesia required less use of vasopressor and inotropic support.
El aneurisma de la aorta abdominal (AAA) se define como una dilatación de la arteria con aumento de más del 50% de su diámetro original, es generado por procesos degenerativos y enfermedad aterosclerótica que llevan a degradación de las proteínas de la matriz extracelular del vaso ocasionando una pared aórtica frágil y susceptible de formar un aneurisma1. La importancia de los AAA se resalta debido a que son el 65% del total de los aneurismas de la aorta2.
Esta patología afecta principalmente a hombres de raza blanca, generando un aumento de su aparición a partir de los 50 años, llegando a tener una prevalencia de 78 por cada 100.000 habitantes en la octava década de vida1. Esta ha venido en aumento debido al incremento de la expectativa de vida, así como de enfermedades crónicas y el consumo de tabaco, se estima que el 90% de los pacientes con esta patología fuma o ha fumado alguna vez en su vida2.
Los factores de riesgo son similares a las enfermedades coronaria y arterial periférica: sexo masculino, raza blanca, tabaco (aumenta el riesgo de 20 a 25% del crecimiento del aneurisma y el cese del mismo reduce las complicaciones pulmonares y disminuye la morbimortalidad postoperatoria después de un reparo exitoso del aneurisma)1, hipertensión arterial (no solo se asocia con la formación de aneurismas, sino que aumenta el riesgo de rotura), tercera edad, dislipidemia, enfermedad pulmonar obstructiva crónica (EPOC) (siendo un factor de riesgo independiente) e historia familiar de aneurisma (pacientes con familiares de primer grado de consanguinidad tienen un riesgo 12 veces mayor de desarrollar un aneurisma y 18 veces entre hermanos)1. Cabe resaltar que algunas patologías congénitas aumentan la probabilidad de presentar un aneurisma aórtico como son los síndromes de Marfan, Ehlers-Danlos y de Loeys-Dietz3.
Entre las complicaciones más temidas está la rotura del aneurisma que lleva a una mortalidad que varía entre 80 y 90%1. Su presentación depende del diámetro y de su tratamiento oportuno2,4 con la realización de diferentes técnicas quirúrgicas, entre ellas la reparación con prótesis endovascular. La implementación de esta técnica ha disminuido los desenlaces fatales como la mortalidad temprana a 30 días, el tiempo de cirugía, el volumen de sangrado y los requerimientos de transfusión. Dado el avance quirúrgico se han implementado diferentes técnicas anestésicas con el fin de realizar un procedimiento, tanto desde la parte quirúrgica como anestésica, menos agresivo y con mejores resultados5,6.
La técnica de reparo endovascular (EVAR) de aneurisma aórtico fue practicada por primera vez por Dotter en 1969; pero fue en 1990 cuando se realizó con éxito por Volodos y Parodi7,8 y aprobado por la Food and Drug Administration en 19999, representando uno de los avances más importantes para el manejo de los aneurismas aórticos en la actualidad.
En el Hospital de San José como en otras partes del mundo se ha implementado el uso de prótesis endovascular, optando por la técnica abierta para casos muy específicos. Algo similar ocurre en el ámbito anestésico en el cual la anestesia general (AG), definida como la pérdida de la conciencia y amnesia del paciente, con una inducción estándar acompañada de manejo de la vía aérea con dispositivos infra- o supraglóticos, está siendo reemplazada por anestesia regional (AR), definida como administración de anestésico local en el neuroeje, ya sea en el espacio intratecal o en el espacio epidural, o por la anestesia local más sedación (AL+S), definida como un bloqueo de campo o de nervios circundantes en la región inguinal, con la administración de agentes intravenosos con propiedades sedantes.
Al utilizar otras opciones anestésicas se ha trasformado la idea de que la técnica anestésica exclusiva para el reparo de AAA es la AG. En este estudio se describen las técnicas empleadas en pacientes con AAA, llevados a reparación con prótesis endovascular entre enero 2009 y enero 2015 en el Hospital de San José de Bogotá.
Materiales y métodosSe llevó a cabo un estudio descriptivo retrospectivo. Se incluyeron todos los pacientes mayores de 18 años de edad diagnosticados con AAA que fueron llevados a corrección con prótesis endovascular desde enero 2009 hasta enero 2015, por el Servicio de Cirugía Vascular del Hospital de San José en Bogotá. Se excluyeron aquellos con aneurismas aórticos rotos, a quienes se les corrigió de urgencia, los aneurismas que comprometieran la vasculatura de la aorta torácica y/o femoral y cuando la corrección se hizo de manera abierta.
Los pacientes a los que se le realizó más de un procedimiento de corrección de AAA con prótesis endovascular se registraron y analizaron en forma independiente, teniendo en cuenta que fueron en momentos quirúrgicos, técnicas anestésicas y tiempos anestésicos diferentes.
Los registros de los pacientes con AAA tratados con prótesis endovascular fueron identificados mediante la base de datos de procedimientos realizados por el Servicio de Cirugía Vascular del Hospital de San José de Bogotá; los datos se obtuvieron a partir de la historia clínica, registro de anestesia y descripción quirúrgica. Se recolectaron variables sociodemográficas, antecedentes médicos y las relacionadas con la técnica anestésica (tiempo de anestesia, complicaciones, uso de vasopresores e inotrópicos) y tiempo de estancia hospitalaria.
Análisis estadísticoLa unidad de análisis correspondió a los procedimientos de corrección de AAA con prótesis endovascular. La estadística descriptiva se realizó en términos de frecuencias absolutas y relativas para las variables cualitativas y por medio de medianas y rangos intercuartílicos para las cuantitativas. Los datos se analizaron utilizando el programa Stata 13 ®. Este estudio fue considerado una investigación sin riesgo y aprobado por el comité de ética en investigaciones con seres humanos del Hospital de San José.
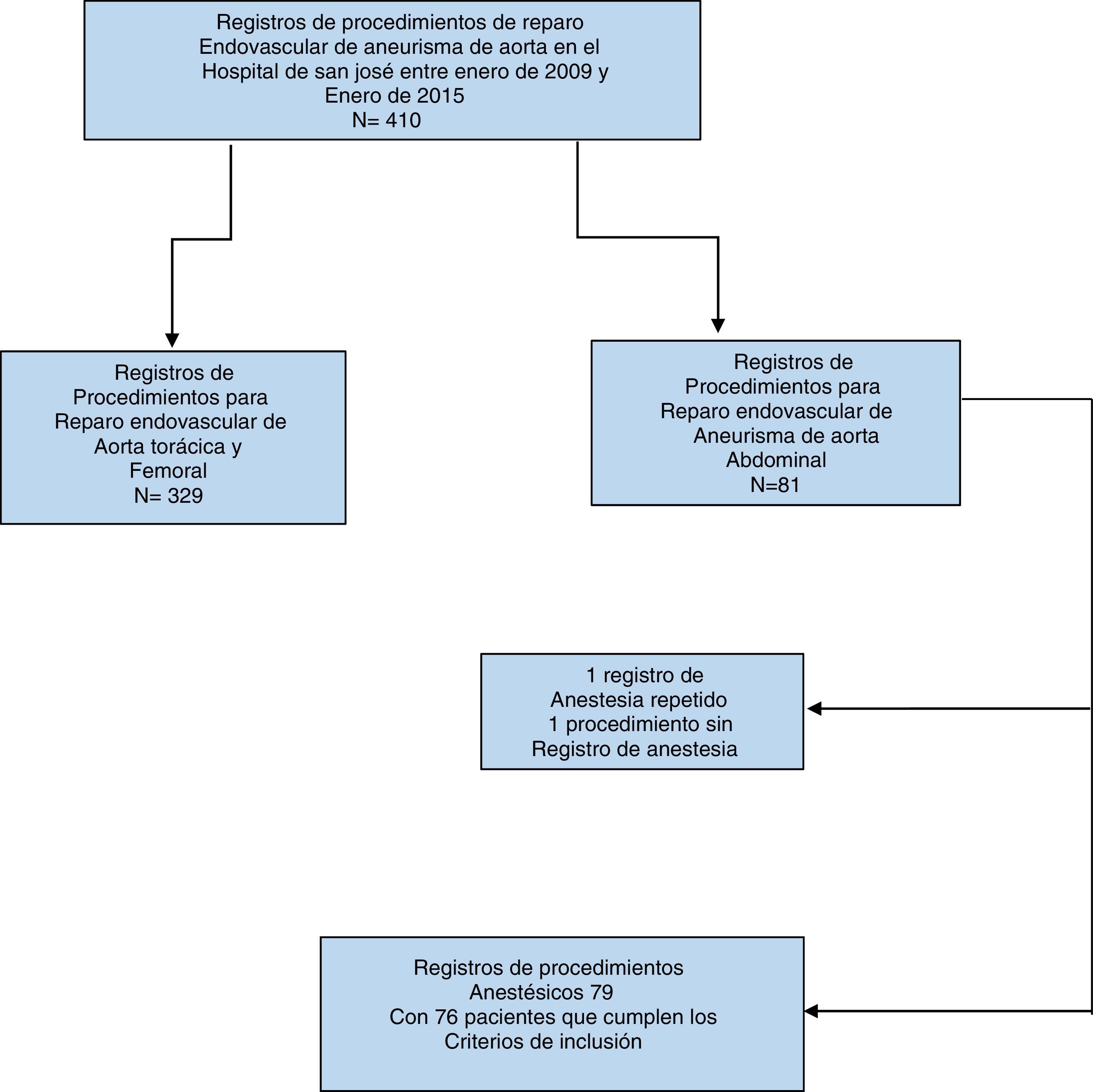
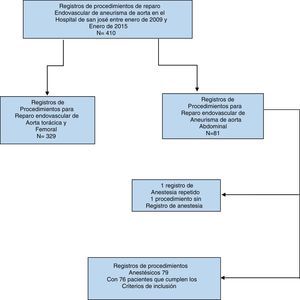
ResultadosUn total de 79 reparos endovasculares fueron identificados en los registros de historias clínicas que correspondieron a 76 pacientes que cumplieron los criterios de inclusión (fig. 1). De la información recolectada se muestra que el total de la población sometida a reparo endovascular eran en el momento de la intervención mayores de 50 años de edad, con una mediana de 73 años y rango intercuartílico de 69 a 81 años. Un total de 58 (73,4%) procedimientos fueron realizados en hombres, reflejando una mayor prevalencia de género (tabla 1).
Características generales de la población
| Femenino N= 21 | Masculino N= 58 | Todos N= 79 | |
|---|---|---|---|
| EDAD mediana(RIQ) | 77 (69 - 81) | 72 (69 -79) | 73 (69 - 81) |
| PESO mediana(RIQ) | 60 (50 - 65) | 69 (62 - 76) | 67 (60 - 75) |
| Antecedentes patológicos n (%) | |||
| Hipertensión arterial (HTA) | 17 (80,9%) | 37 (63,7%) | 54 (68,3%) |
| Enfermedad pulmonar obstructiva crónica (EPOC) | 8 (38,1%) | 8 (13,7%) | 16 (20,2%) |
| Tabaquismo | 2 (9,5%) | 10 (17,2%) | 12 (15,1%) |
| Diabetes | 0 | 5 (8,62%) | 5 (6,3%) |
| Infarto agudo de miocardio (IAM) | 1 (4,7%) | 9 (15,5%) | 10 (12,6%) |
| Falla cardíaca | 3 (14,2%) | 3 (5,1%) | 6 (7,5%) |
| Insuficiencia renal crónica (IRC) | 1 (4,7%) | 7 (12%) | 8 (10,1%) |
| Hipotiroidismo | 5 (23,8%) | 8 (13,7%) | 13 (16,4%) |
| Tuberculosis | 0 | 1 (1,7%) | 1 (1,27%) |
| Tromboembolismo pulmonar(TEP) | 0 | 1 (1,7%) | 1 (1,27%) |
| Técnica anestésica n (%) | |||
| General | 5 (23,8%) | 26 (44,8%) | 31 (39,2%) |
| Regional | 1 (4,7%) | 7 (12%) | 8(10,1%) |
| Local + sedación | 15 (71,4%) | 25 (43,1%) | 40(50,6%) |
Los antecedentes patológicos de mayor prevalencia fueron hipertensión arterial en un 68,3% (54/79) seguido por EPOC en un 20,2% (16/79) y en tercer lugar tabaquismo con 15,1% (12/79). El antecedente de hipertensión arterial fue prevalente en el sexo femenino con 80,9% (17/21) frente al 63,7% (37/58) de hombres.
En general, de las técnicas anestésicas empleadas, la AL+S fue la más usada cuando se comparó frente a la AG y la AR, utilizándose en 40 (50,6%), 31 (39,2%) y 8 (10,1%) pacientes respectivamente. Sin embargo, en hombres la técnica anestésica más empleada fue la AG, utilizada en 26 de 58 procedimientos (44,8%) (tabla 1).
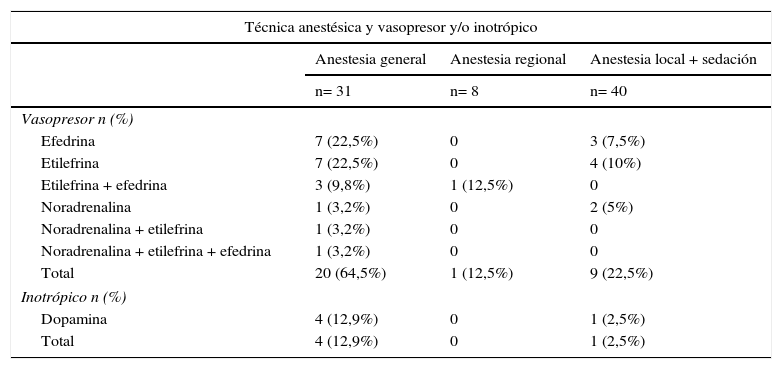
Solo 9 de los 40 procedimientos (22,5%) bajo AL+S requirieron del uso de vasopresores y en uno (2,5%) de inotrópicos. De estos fármacos los más empleados fueron etilefrina en cuatro procedimientos (10%) y dopamina en uno (2,5%). A su vez, de los 31 procedimientos ejecutados bajo AG, 20 (64,5%) requirieron vasopresores y 4 (12,9%) inotrópicos; en este grupo los vasopresores más utilizados fueron la efedrina y la etilefrina, y en todas las ocasiones el inotrópico de elección fue la dopamina, cuyo uso durante el procedimiento quirúrgico en todos los casos fue secundario a hipotensión arterial sostenida más bradicardia (tabla 2).
Relación entre la técnica anestésica y el vasopresor y/o inotrópico utilizado
| Técnica anestésica y vasopresor y/o inotrópico | |||
|---|---|---|---|
| Anestesia general | Anestesia regional | Anestesia local + sedación | |
| n= 31 | n= 8 | n= 40 | |
| Vasopresor n (%) | |||
| Efedrina | 7 (22,5%) | 0 | 3 (7,5%) |
| Etilefrina | 7 (22,5%) | 0 | 4 (10%) |
| Etilefrina + efedrina | 3 (9,8%) | 1 (12,5%) | 0 |
| Noradrenalina | 1 (3,2%) | 0 | 2 (5%) |
| Noradrenalina + etilefrina | 1 (3,2%) | 0 | 0 |
| Noradrenalina + etilefrina + efedrina | 1 (3,2%) | 0 | 0 |
| Total | 20 (64,5%) | 1 (12,5%) | 9 (22,5%) |
| Inotrópico n (%) | |||
| Dopamina | 4 (12,9%) | 0 | 1 (2,5%) |
| Total | 4 (12,9%) | 0 | 1 (2,5%) |
La técnica anestésica en la que menos se emplearon vasopresores fue la AR, con un solo procedimiento (12,5%) en el que se usó etilefrina más efedrina. En ningún procedimiento se administraron inotrópicos (tabla 2).
La mediana de tiempo de estancia intrahospitalaria relacionada con la AL+S y la AG fue de 2 días, con un rango intercuartílico de 1 a 4 días en ambos casos, mientras que para la AR se observó un menor tiempo de estancia con una mediana de 1,5 días con un rango intercuartílico de 1 a 2 días (tabla 3).
Relación entre tipo de técnica anestésica, antecedentes y complicaciones anestésicas
| Anestesia local + sedación n= 40 | Anestesia regional n=8 | Anestesia general n= 31 | |
|---|---|---|---|
| Edad | 73,5 (69 - 81) | 74,5 (70 - 84) | 73 (68 - 79) |
| Antecedentes n (%) | |||
| HTA | 31 (77,5%) | 3 (37,5%) | 20 (64,5%) |
| Tabaquismo | 6 (15%) | 3 (37,5%) | 3 (9,68%) |
| EPOC | 10 (25%) | 1 (12,5%) | 5 (16%) |
| Tiempo estancia en días, mediana (RIC) | 2 (1 - 4) | 1.5 (1 - 2) | 2 (1 - 4) |
| Duración anestesia en min, mediana (RIC) | 180 (165 - 210) | 212 (180 - 250) | 180 (150 - 240) |
| Complicaciones anestésicas n = 33 (41,7%) | |||
| Anestesia local + sedación n= 12 (36,4%) | Anestesia regional n=1 (3%) | Anestesia general n= 20 (60,6%) | |
| Conversión anestesia general | 1/12 (8,3%)* | 0 | 0 |
| Crisis hipertensiva | 2/12 (16,7%) | 0 | 0 |
| Hipotensión arterial sostenida + bradicardia | 1/12 (8,3%) | 0 | 4/20 (20%) |
| Hipotensión arterial sostenida | 1/12 (8,3%) | 0 | 3/20 (15%) |
| Hipotensión arterial | 7/12 (58,3%) | 1/1 (100%) | 13/20 (65%) |
La técnica anestésica que mostró mayor duración en minutos al realizar el procedimiento quirúrgico fue la AR con una mediana de 212 minutos con un rango intercuartílico de 180 a 250 minutos, la AG y la AL+S presentaron el mismo tiempo empleado en minutos con una mediana de 180 minutos (tabla 3).
Se presentaron 33 (41,7%) complicaciones anestésicas, siendo más frecuentes con la AG (60,6%). La hipotensión arterial fue la mayor, independiente de la técnica anestésica utilizada. Solo en una ocasión en la que se administró AL+S fue necesaria la conversión a AG debido a tiempo prolongado de cirugía. La crisis hipertensiva solo se presentó con AL+S, evidenciada en 2 ocasiones (16,7%) (tabla 3).
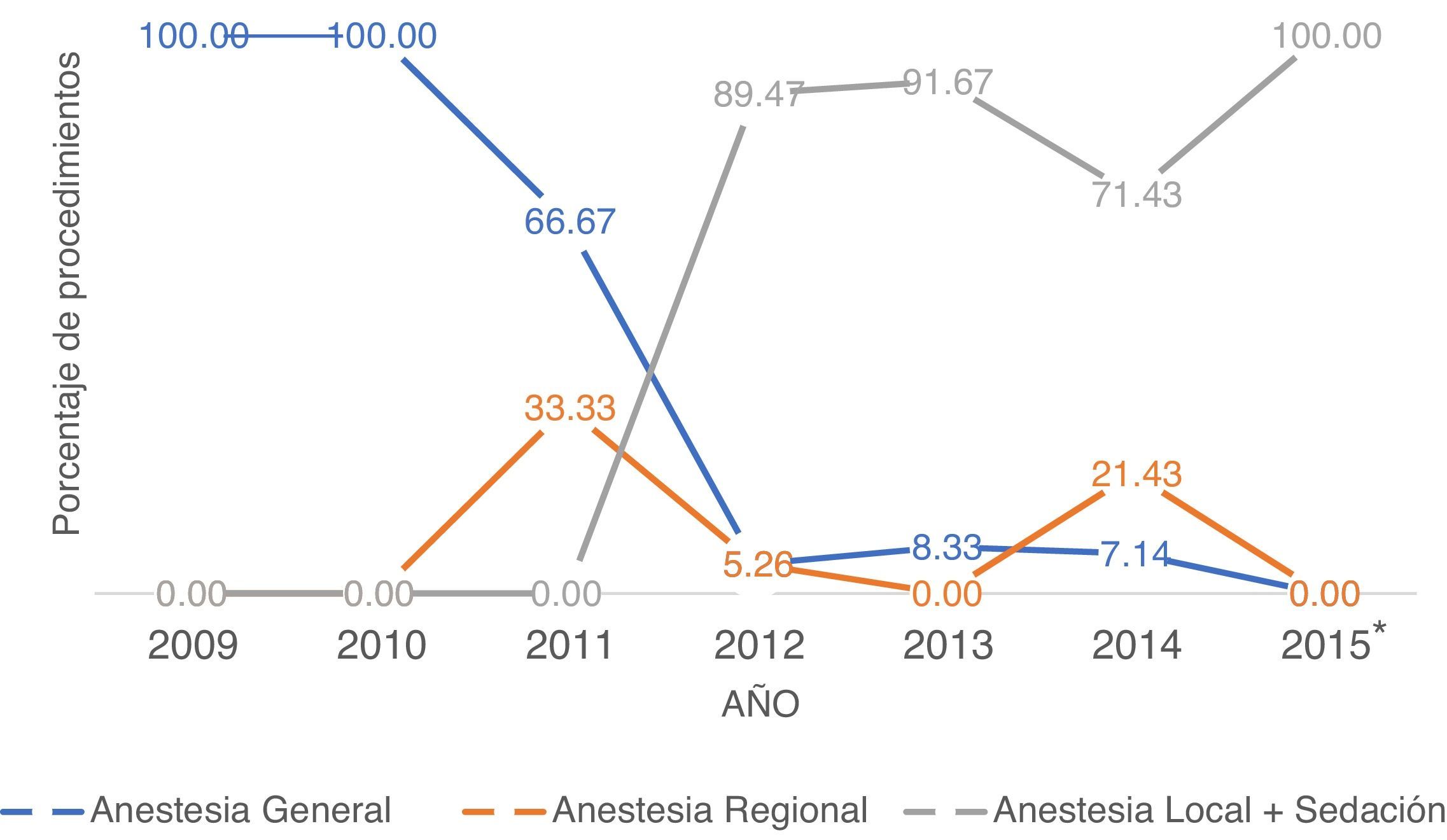
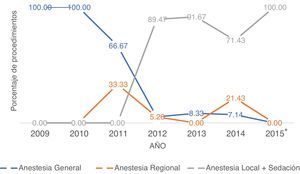
Al analizar el porcentaje de procedimientos realizados por año según la técnica anestésica empleada (fig. 2), la AG predominó en 100% en 2009 y 2010 respecto a la AR y a la AL+S. A partir de 2011 se evidenció un marcado aumento de 0% a 89,4% del uso de la AL+S, permaneciendo como la técnica anestésica más empleada en los años siguientes, aunque a partir de 2011 la AG presentó una disminución importante, teniendo el menor porcentaje del total de los procedimientos realizados en 2012 con un 5,26% y en enero de 2015 ningún paciente fue llevado a procedimiento endovascular bajo esta técnica anestésica.
DiscusiónDada la evolución en los últimos años de las opciones terapéuticas para el manejo de la enfermedad aneurismática aórtica, que va desde la corrección quirúrgica abierta hasta el reparo endovascular, la anestesia va de la mano con estos avances y se ha encaminado al uso de técnicas menos invasivas y mórbidas, así como más seguras para el paciente. Este estudio describe esta tendencia en pacientes con AAA, llevados a EVAR en el Hospital de San José, evidenciando un importante número de procedimientos ejecutados en años recientes bajo una anestesia menos invasiva, lo que le permite al lector deducir conclusiones críticas con los resultados obtenidos para la toma de decisiones en el momento de enfrentarse a un procedimiento de reparo endovascular.
Como se describe en la literatura, el presente estudio mostró similitudes en cuanto el uso y la administración de la AL +S, la cual corresponde a un bloqueo de campo o de nervios circundantes a la región inguinal realizado en nuestra institución por los cirujanos, asociado con la administración transoperatoria por parte del anestesiólogo de agentes anestésicos intravenosos con propiedades sedantes, ansiolíticas e incluso anestésico como el propofol, el remifentanil o la dexmedetomidina. Esto hace que al momento de su uso se tenga una variedad de medicamentos que están disponibles a nivel mundial y son de uso frecuente en nuestra institución, brindando de esta manera una opción interesante para la realización de EVAR en la sala de hemodinamia10. La AL+S fue la técnica anestésica más utilizada en el Hospital de San José teniendo un mayor auge a partir del año 2012, guardando una relación inversa respecto al empleo de la AG en este mismo periodo, con menores complicaciones cardiovasculares (bradicardia e hipotensión) cuando se compara con procedimientos realizados bajo AG11,12. De acuerdo con los hallazgos encontrados, los pacientes evaluados en quienes se empleó la AL+S y AR, mostraron una mayor estabilidad cardiovascular con cifras tensionales en rango de seguridad, lo cual coincide con lo reportado por otros autores.
Se ha descrito además que el uso de técnicas menos invasivas genera una disminución de atelectasias basales e infecciones respiratorias5–9,13–18. La AL+S ha sido considerada como una práctica anestésica bien tolerada y factible de realizar13, sobre todo en aquellos pacientes con comorbilidades representativas y transcendentales no solo para riesgo cardiovascular sino para el desarrollo de AAA11, como EPOC, HTA y tabaquismo, que se ve reflejado en nuestro estudio donde la mayoría de los pacientes a pesar de presentar antecedentes de importancia a la hora de ser llevados al procedimiento bajo AL + S, no desarrollaron complicaciones que amenazaran la vida o desencadenaran la muerte.
Las comorbilidades descritas siempre deben ser tomadas en cuenta a la hora de seleccionar la técnica anestésica a emplear, ya que el 92% de los pacientes con AAA tiene de base una enfermedad ateroesclerótica de todos los vasos del cuerpo, incluyendo el corazón (enfermedad coronaria)14, por lo que en el intraoperatorio pueden presentarse diferentes situaciones como el aumento del consumo de oxígeno, taquicardia, reducción de la fibrinólisis y el desbalance en el aporte y consumo de oxígeno, pudiendo desencadenarse infarto agudo de miocardio. Es por ello que la AL+S puede atenuar en mayor medida el estrés quirúrgico y las situaciones antes descritas, comparada con la AG y la AR19. A pesar de que en nuestro estudio ningún paciente presentó IAM, sí podemos resaltar que las complicaciones anestésicas se presentaron con mayor frecuencia al emplear la AG seguida de AL+S y la AR.
Teniendo en cuenta que la AL+S requiere el uso de medicamentos coadyuvantes para la sedación, como la dexmedetomidina que es uno de los fármacos más usados para la sedación consciente durante los procedimientos vasculares como fístulas arteriovenosas, endarterectomías y EVAR, los cuales permiten una sedación más segura, disminuyendo el riesgo de depresión respiratoria y generando una estabilidad cardiovascular, sin mayor impacto para el desenlace de los pacientes, incluso en los cortos periodos de clampeo y declampeo endovascular en los cuales las cifras tensionales pueden variar. Además de la generación de la vasodilatación periférica progresiva asociada con la disminución de la frecuencia cardíaca, garantiza el control de las cifras tensionales en la mayoría de los pacientes, con una ventaja adicional en el control del dolor por su efecto analgésico intrínseco20,21. A pesar de que en nuestro estudio no se recolectó información acerca de los fármacos empleados para la sedación y sin haberla tomado como una variable, podemos asegurar que es uno de los medicamentos más usados en nuestra institución. Esta limitación de no considerar qué medicación se usó en el EVA, puede ser una ventana para el diseño de nuevos estudios, tales como ensayos clínicos, para comparar el mejor perfil farmacológico en el manejo de la sedación en este procedimiento.
En el estudio EUROSTAR no hubo diferencias en la morbilidad respecto a la técnica anestésica empleada y el uso de cualquiera de ellos no interfirió en los segundos procedimientos endovasculares realizados en un mismo paciente, debido a que no se efectuaron en el mismo tiempo quirúrgico ni correspondían a una complicación secundaria de la técnica anestésica empleada primero22. En nuestro estudio podemos encontrar similitudes en tres de los pacientes descritos que fueron llevados a nuevos procedimientos endovasculares en otro tiempo quirúrgico, pues con ninguna de las técnicas anestésicas empleadas surgieron complicaciones que amenazaran la vida. Es importante dar a conocer que el American College of Cardiology/American Heart Association (ACC/AHA) no aboga por un modo de anestesia específico, pero respalda que la escogencia de la técnica sea dependiente del tipo de cirugía, de la experiencia del equipo quirúrgico y del estado premórbido del paciente, lo cual podemos evidenciar en nuestro estudio en el que desde 2009 hasta 2015, la práctica quirúrgica, la ganancia en la curva de aprendizaje de las técnicas y los resultados obtenidos de la técnica anestésica utilizada se basaron en la integralidad del equipo, además de tiempos quirúrgicos más cortos y mayor conocimiento de las técnicas anestésicas empleadas diferentes a la AG23. Por ello el anestesiólogo además de conocer los riesgos y complicaciones de las diferentes técnicas anestésicas, como la parálisis asociada con el hematoma espinal y la lesión medular, a la pobre tolerancia a los procedimientos largos con la AL+S y las complicaciones pulmonares con la AG entre otras, debe estar familiarizado con el cirujano, los tiempos quirúrgicos y cada paciente en particular24,25, para explorar otras opciones con diferentes medicamentos, lograr una sedación óptima y de esta manera poder usarlos como un adyuvante en alguna de las tres técnicas empleadas en la actualidad. Se puede concluir entonces que a pesar de existir divergencias a la hora de escoger la técnica anestésica para el manejo de EVAR, la AG no es la única opción y se deben tener presentes siempre las diferentes técnicas anestésicas descritas en la literatura.
Al ser el primer estudio realizado en el Hospital de San José enfocado en la descripción de las técnicas anestésicas empleadas en EVAR desde 2009 y teniendo en cuenta que a partir de 2011 el uso de la AL+S ha sido la técnica más empleada, le brinda al grupo de anestesia un enfoque objetivo al momento de seleccionar el tipo de anestesia para futuros procedimientos, lo cual constituye una fortaleza.
Existen algunas limitaciones al momento de analizar los resultados obtenidos por ser un estudio con una población pequeña, lo cual es susceptible de pérdida de registros clínicos con subregistro de los mismos ya que se basa solo en los datos que ya se encuentran escritos. Además al ser un estudio observacional y descriptivo, los datos obtenidos de las características de la población, signos vitales, complicaciones anestésicas y tiempos intraoperatorios entre otros, no permiten establecer relaciones ni asociaciones entre las variables ni estimar el riesgo de factores individuales de los pacientes o de los procedimientos realizados.
Por otro lado es importante la medición de la estabilidad hemodinámica con las diferentes técnicas anestésicas empleadas para considerar la morbimortalidad, pero para evaluar estos cambios son necesarias la monitoría del gasto cardíaco, la variabilidad del volumen sistólico y la medición de lactato, entre otros, con el empleo de dispositivos invasivos que no son usados en forma regular en este tipo de procedimientos.
ConclusionesEl artículo analiza las diferentes técnicas anestésicas para el manejo del EVAR, los resultados obtenidos, las complicaciones anestésicas, el uso de vasopresores e inotrópicos, el tiempo anestésico, el género y la edad promedio de presentación del aneurisma, para decidir el tipo de anestesia que debe emplearse en cada paciente. La literatura presenta diferentes pros y contras acerca de las diferentes técnicas anestésicas empleadas, pero es de vital importancia evaluar al paciente como individuo único, con comorbilidades importantes y antecedentes relevantes para la generación de aneurismas de la aorta abdominal y así proceder a la selección del procedimiento anestésico apropiado.
Es importante establecer que la técnica anestésica empleada debe ser la que presente una mayor estabilidad en los signos vitales, que sea menos mórbida, poco invasiva, segura y práctica para cada individuo en particular, que genere una disminución en las oscilaciones de los signos vitales, como hipotensión y bradicardia, las cuales son amenazantes en un tejido vascular ya lesionado. Por ello se puede concluir que la AG presenta con mayor frecuencia este tipo de complicaciones anestésicas al momento de compararlo con la AR y la AL + S.
La AL+S es la técnica más empleada en nuestra institución, no presenta diferencias en el tiempo de estancia hospitalaria ni en la duración anestésica, pero sí revela diferencias en el menor uso de vasopresores e inotrópicos al igual que la AR. Sin embargo, no podemos concluir que esta última técnica sea la ideal respecto a la AL+S y la AG, pues la población analizada es pequeña con solo 8 procedimientos de los 79 realizados y no se pueden hacer asociaciones.
Para demostrar el verdadero impacto en la morbimortalidad a corto y largo plazo de los pacientes con AAA sometidos a EVAR, se requiere realizar estudios analíticos con una adecuada muestra que puedan evaluar con mayor precisión cuál técnica anestésica es más efectiva y segura.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Agradecimientos al Servicio de Cirugía Vascular del Hospital de San José por colaborar con la base de datos en los procedimientos realizados de reparo endovascular.
Agradecimientos al Departamento de Investigación de la Fundación Universitaria de Ciencias de la Salud por la ayuda metodológica, y la colaboración en la escritura del manuscrito.