La dexametasona durante la extubación es útil en pacientes con intubación prolongada, además ayuda a disminuir la necesitad de reintubación.
ObjetivoEvaluar la formulación de corticoide intravenoso durante la extubación en recién nacidos hospitalizados en la Unidad de Cuidado Intensivo Neonatal del Hospital de San José, Bogotá D.C.
MétodoEstudio retrospectivo tipo serie de casos. Se describen las características de formulación de dexametasona para extubación, frecuencia de estridor, reintubación y estancia hospitalaria entre enero de 2013 y junio de 2015, con un análisis descriptivo de la información.
ResultadosSe incluyeron 316 pacientes con 322 eventos de intubación, 54,2% (n=171) sexo masculino, edad gestacional mediana 34 semanas (RIQ=30,5-37). La dexametasona se formuló en 26,7% (n=86 eventos). El 28,2% (n=24 eventos) recibió la primera dosis antes de 7 días de nacido y el 68,6% presentó criterios de intubación prolongada (n=89 eventos). En el 66,2% de intubación prolongada se utilizó dexametasona y en el 11,5% no hubo indicación clara. De los eventos que recibieron dexametasona el 13,2% (n=12) presentó estridor, 11,6% (n=10) con diagnóstico de displasia broncopulmonar, 2 cursaron con sangrado gastrointestinal y uno con hiporreflexia. La frecuencia de reintubación en las primeras 24h fue 1,9% (n=6 eventos), de ellos 4 recibieron dexametasona.
ConclusionesEl uso de dexametasona como profilaxis en la extubación de los pacientes hospitalizados es frecuente en la unidad, sin embargo, existe una importante variabilidad en su utilización. La frecuencia de eventos adversos fue baja.
Dexamethasone is useful during extubation in patients on prolonged intubation, as well as helping to reduce the need for re-intubation.
ObjectiveTo evaluate the use of intravenous corticosteroids during extubation in newborns admitted to the Neonatal Intensive Care Unit of San José Hospital, Bogota DC.
MethodA retrospective, case series study was conducted by recording the characteristics of the use of dexamethasone for extubation, stridor frequency, re-intubation, and hospital stay, between January 2013 and June 2015. A descriptive analysis of the information collected is presented.
ResultsA total of 316 patients, with a mean gestational age of 34 weeks (Inter-quartile range= 30.5–37), and 171 (54.2%) males, were included. There were 322 intubation events. Dexamethasone was used in 86 (26.7%) events. The first dose was given 7 days before birth in 24 (28.2%) of events, and 89 (68.6%) had prolonged intubation criteria. Dexamethasone was used in 66.2% of the prolonged intubations, and in 11.5% there was no clear indication. Of the events that received dexamethasone, 12 (13.2%) had stridor, 10 (11.6%) with a diagnosis of bronchopulmonary dysplasia, two suffered from a gastrointestinal bleed, and one with hyporeflexia. The frequency of re-intubation in the first 24hours was 1.9% (6 events), of which 4 of them received dexamethasone.
ConclusionsThe use of dexamethasone as prophylaxis in the extubation of patients admitted to the unit is common, however, there is a significant variation in its use. The frequency of adverse events is low.
La intubación orotraqueal (IOT), aunque vital para facilitar la ventilación mecánica en la unidad de cuidados intensivos neonatal (UCIN), se asocia con múltiples complicaciones, entre ellas el desarrollo potencial de edema glótico o subglótico, resultante en estridor y prolongación de la estancia en la UCIN1. Se han implementado estrategias para disminuir la frecuencia de aparición de estas complicaciones, como la utilización de corticoides intravenosos, en especial la dexametasona, buscando disminuir el edema reactivo que se desarrolla en la mucosa2 con resultados favorables3.
A pesar de su comprobada efectividad4,5 se han descrito múltiples eventos adversos con la utilización de los corticoides intravenosos, lo que se ha traducido en subutilización de la estrategia; entre las complicaciones se han descrito alteraciones al examen neurológico y parálisis cerebral, sangrado gastrointestinal, perforación intestinal, hiperglucemias, hipertensión, miocardiopatía hipertrófica y fallo del medro3,6–8. En la década pasada se llevó a cabo el estudio DART9, ensayo clínico aleatorizado, doble ciego en el cual se incluyeron 70 niños pretérmino en 11 centros de atención diferente, buscando conocer efectos adversos de la terapia con corticoide durante la extubación. El grupo de intervención estuvo compuesto por 35 niños, a quienes se administró dosis total de 0,89mg/kg de dexametasona, y un grupo control con igual número de participantes manejados con placebo. Este estudio concluyó que la formulación a bajas dosis en niños con 7 o más días de vida disminuye las complicaciones postextubación, así como el tiempo en días de intubación en neonatos pretérmino y/o bajo peso al nacer, sin presentar complicaciones a corto plazo.
En otro estudio realizado por el mismo autor, que incluyó a los sobrevivientes del estudio DART, se realizó seguimiento a 2 años, con una supervivencia de 56 pacientes al final del estudio; el grupo expuesto lo constituyeron aquellos con manejo con dexametasona (n=29) y control aquellos con placebo (n=27). Los autores no encontraron mayor proporción de parálisis cerebral (14% vs 22%; p=0,50), discapacidad mayor (41% vs 31%; p=0,41) o sordera (7,4% vs 14,8%; p=0,67) entre los grupos estudiados10. Sin embargo, estos resultados deben interpretarse con cautela por el bajo tamaño de la muestra.
En Colombia, en el año 2013, el Ministerio de Salud y de la Protección emite la guía de práctica clínica del recién nacido con trastorno respiratorio11, donde recomiendan el uso de periextubación de dexametasona IV para disminuir tanto la necesidad de reintubación, como la incidencia de estridor postextubación; sin embargo, no hace una recomendación específica acerca de la dosis y duración de la dexametasona, ni define cuáles son esos pacientes con alto riesgo de edema de la vía aérea.
A pesar de existir directrices nacionales, durante la práctica diaria observamos que no existe una unificación de criterios en la formulación de la dexametasona durante la extubación, con tiempos de inicio, posología y dosis diversas, por lo que se pretende con este estudio describir el uso de la dexametasona durante la extubación, así como las complicaciones secundarias descritas en la literatura, en la UCIN del Hospital de San José, Bogotá D.C. Colombia.
Materiales y métodosDiseñoEstudio observacional descriptivo longitudinal de recolección retrospectiva tipo serie de casos. Se describieron las características de prescripción de la dexametasona durante la extubación en recién nacidos que requirieron intubación orotraqueal en la UCIN del Hospital de San José entre enero de 2013 y junio de 2015.
ParticipantesFueron seleccionados del registro de atenciones del servicio de terapia respiratoria, quienes recogen el total de pacientes en quienes se realizó IOT. Se incluyeron todos los eventos con IOT (primera vez o reintubación) durante su estancia en la UCIN del Hospital de San José en el periodo de estudio. Un paciente pudo aportar datos en más de un momento, de acuerdo con el número de intubaciones que haya requerido, por lo que se seleccionaron los eventos de intubación y se analizaron las características de administración de dexametasona en cada evento.
La información fue extraída de manera manual de la historia clínica digital Vesalius®, y se procedió a diligenciar el instrumento de recolección de datos diseñado por los investigadores. Se incluyeron las características sociodemográficas de los participantes, la frecuencia, dosis y días de uso de la dexametasona, y se evaluó la frecuencia de estridor laríngeo, displasia broncopulmonar (definida como requerimiento de oxígeno por 28 o más días diagnosticada durante la estancia hospitalaria actual), intubación prolongada (IOT por 7 o más días), así como los días de estancia hospitalaria y los desenlaces de seguridad, como la frecuencia de hiperglucemia o hipertensión arterial y desenlaces neurológicos como hipotonía e hiporreflexia.
Análisis estadísticoSe realizó un análisis descriptivo de las variables a estudio. Las cualitativas se reportaron con frecuencias absolutas y porcentajes, y las cuantitativas con medidas de tendencia central y de dispersión. Se estratificaron los grupos de acuerdo con la dosis de administración de la dexametasona (menor de 0,25mg/kg de 0,25 a 0,5mg/kg y mayor de 0,5mg/kg) y se describen las frecuencias de las variables para cada subgrupo. Se tabuló la información en una base de datos Excel® 2010 y el análisis de los datos en el paquete estadístico Stata v13®. Se presentan los resultados en tablas 1 a 5 y figura 1.
Esta investigación, clasificada sin riesgo, fue aprobada por el Comité de Ética e Investigación de la Fundación Universitaria de Ciencias de la Salud.
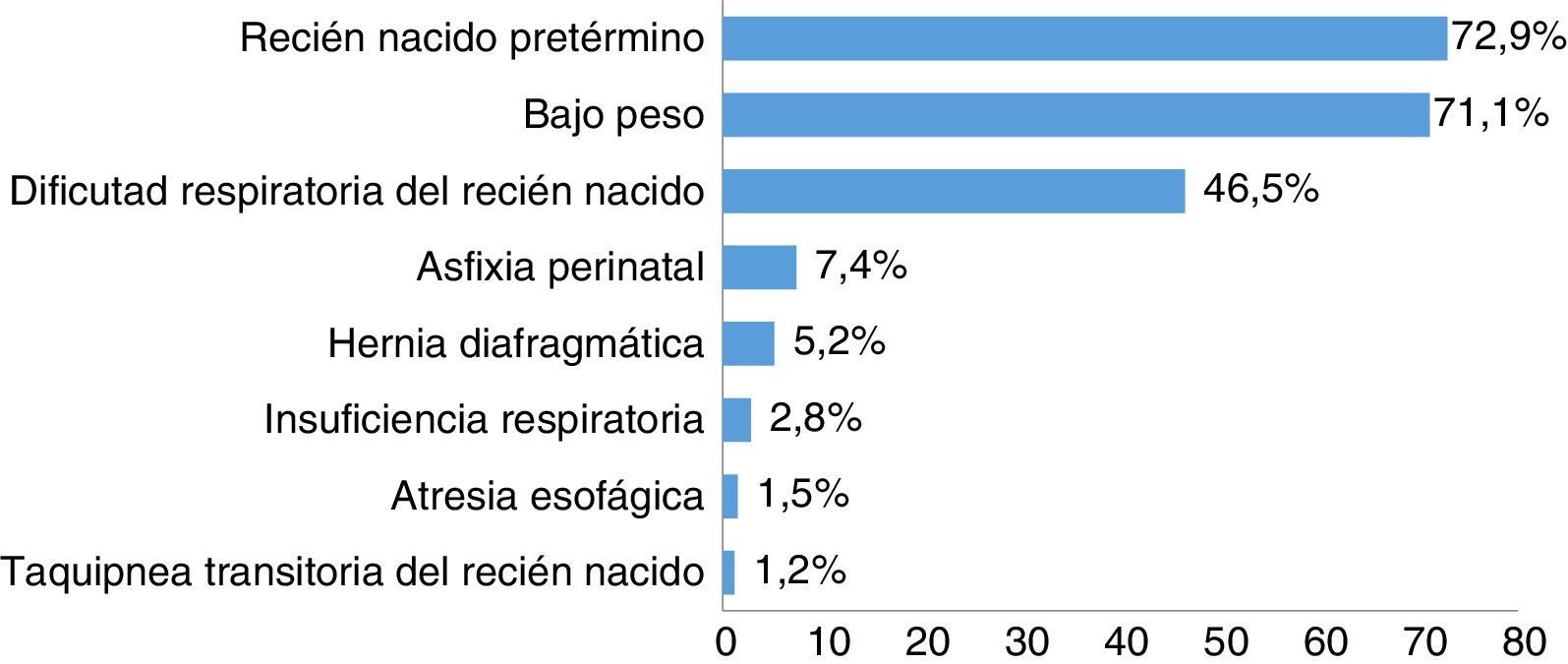
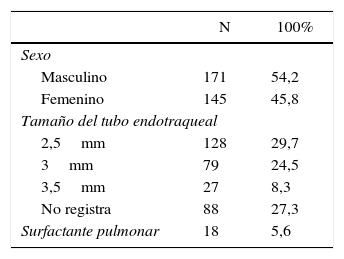
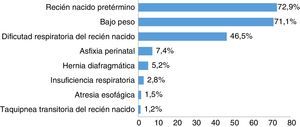
ResultadosIngresaron en la UCIN en el periodo de estudio 1.851 pacientes, 316 (17%) requirieron intubación orotraqueal para un total de 322 eventos. El 54,2% (n=171 eventos) fueron de sexo masculino. La edad gestacional en el momento del nacimiento estuvo entre 22,4 y 42,6 semanas, con una mediana de 34 (RIQ=30,5-37). La mediana de peso al nacer fue de 2.035g (RIQ=1.400-2.695) con un peso mínimo de 520g y máximo 4.020g (tabla 1). El proceso patológico de mayor frecuencia en los pacientes atendidos en la unidad fue la prematurez, seguido de bajo peso al nacer (fig. 1).
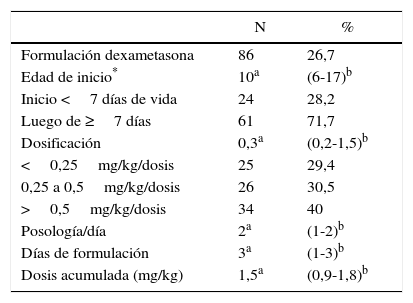
Se formuló dexametasona en el 26,7% (n=86) de los eventos, con una mediana de edad de la primera dosis a los 10 días de nacido (RIQ: 6-14), utilizando una dosis mediana de 0,3mg/kg/dosis (RIQ; 0,2-1,5), mínima de 0,1mg y máxima de 2mg. En cada evento se formuló dexametasona con una mediana de 2 días (RIQ: 1-2), mínimo uno y máximo 3 días. La dosis mediana acumulada fue de 1,5mg/kg/dosis (RIQ: 0,9-1,8), con una dosis mínima de 0,2 y máxima 14,4mg/kg/dosis. El 28,2% (n=24 eventos) recibió la primera dosis antes de los 7 días de nacido (tabla 2).
Características de formulación de la dexametasona
| N | % | |
|---|---|---|
| Formulación dexametasona | 86 | 26,7 |
| Edad de inicio* | 10a | (6-17)b |
| Inicio <7 días de vida | 24 | 28,2 |
| Luego de ≥7 días | 61 | 71,7 |
| Dosificación | 0,3a | (0,2-1,5)b |
| <0,25mg/kg/dosis | 25 | 29,4 |
| 0,25 a 0,5mg/kg/dosis | 26 | 30,5 |
| >0,5mg/kg/dosis | 34 | 40 |
| Posología/día | 2a | (1-2)b |
| Días de formulación | 3a | (1-3)b |
| Dosis acumulada (mg/kg) | 1,5a | (0,9-1,8)b |
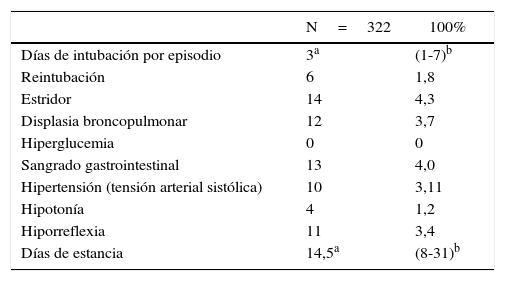
La mediana de intubación orotraqueal fue de 3 días (RIQ=1-7), con un mínimo de uno y un máximo de 60 días. El 27,6% (n=89 eventos) presentó intubación prolongada. El 1,9% (n=6 eventos) requirió reintubación. El 3,7% (n=12) de los casos fue diagnosticado con displasia broncopulmonar durante su hospitalización. De los que requirieron intubación prolongada en el 68,6% se empleó dexametasona. En el 11,5% se utilizó dexametasona en pacientes sin indicación. Como eventos no deseados el 4,35% (n=14) de extubación presentó estridor, y el 4% (n=13) sangrado gastrointestinal. Se evidenció hipertensión arterial en el 3,1% (n=10). La mediana de estancia hospitalaria fue 14,5 (RIQ: 8-31) días, mínimo uno y máximo 92 días (tabla 3).
Desenlaces
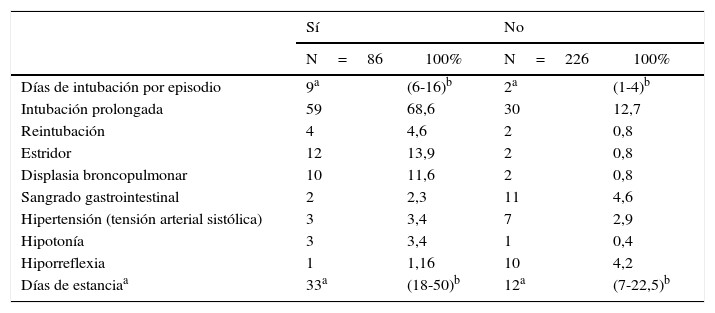
La mediana de aquellos formulados con dexametasona fue 9 días (RIQ: 6-16) con IOT, 4,6% (n=4) requirió reintubación, 13,2% (n=12) presentó estridor, 11,6% (n=10) displasia broncopulmonar, 2 sangrado gastrointestinal y uno hiporreflexia.
En los pacientes en quienes no se usó la dexametasona la mediana de días de IOT estuvo en 2 (RIQ=1-4), 0,85% (n=2) en displasia broncopulmonar, 4,6% (n=11) con sangrado gastrointestinal y 10 pacientes presentaron hiporreflexia. La mediana de estancia en la UCIN fue de 12 días (RIQ=7-22,5) (tabla 4).
Características de los pacientes con uso de dexametasona
| Sí | No | |||
|---|---|---|---|---|
| N=86 | 100% | N=226 | 100% | |
| Días de intubación por episodio | 9a | (6-16)b | 2a | (1-4)b |
| Intubación prolongada | 59 | 68,6 | 30 | 12,7 |
| Reintubación | 4 | 4,6 | 2 | 0,8 |
| Estridor | 12 | 13,9 | 2 | 0,8 |
| Displasia broncopulmonar | 10 | 11,6 | 2 | 0,8 |
| Sangrado gastrointestinal | 2 | 2,3 | 11 | 4,6 |
| Hipertensión (tensión arterial sistólica) | 3 | 3,4 | 7 | 2,9 |
| Hipotonía | 3 | 3,4 | 1 | 0,4 |
| Hiporreflexia | 1 | 1,16 | 10 | 4,2 |
| Días de estanciaa | 33a | (18-50)b | 12a | (7-22,5)b |
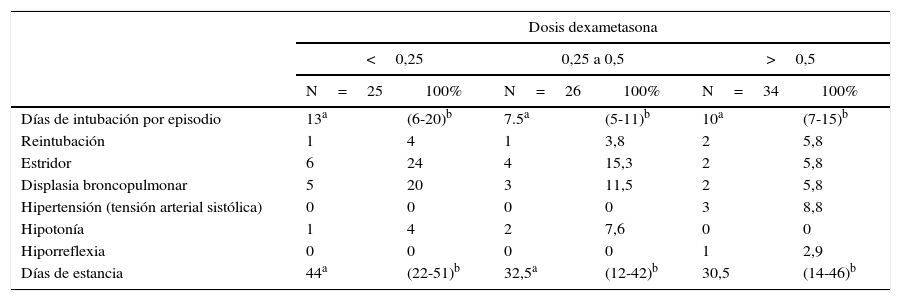
En los pacientes con dosis menores de 0,25mg/kg/dosis la mediana fue 13 días (RIQ=6-20) de IOT, 24% (N=6) presentaron estridor, uno manifestó hipotonía, ninguno presentó sangrado gastrointestinal y la duración de estancia estuvo en una mediana de 44 (RIQ=22-51) días.
En los pacientes con dosis entre 0,25 a 0,5mg/kg/dosis, la mediana de días de IOT fue de 7,5 (RIQ=7-11), 3,8% (n=1) requirió reintubación, 15,3% (n=4) estridor y la duración de estancia en la UCIN estuvo en una mediana de 22,5 días (RIQ=12-42).
Por último, con dosis mayores de 0,5mg/kg/dosis la mediana de días de intubación por episodio fue de 10 (RIQ=7-15), 5,8% (n=2) requirieron reintubación, 2 cursaron con estridor, uno sangrado gastrointestinal y 3 con cifras sistólicas elevadas, con una mediana de duración de estancia hospitalaria de 30,5 (RIQ=14-46) días (tabla 5).
Características de los pacientes de acuerdo con la formulación
| Dosis dexametasona | ||||||
|---|---|---|---|---|---|---|
| <0,25 | 0,25 a 0,5 | >0,5 | ||||
| N=25 | 100% | N=26 | 100% | N=34 | 100% | |
| Días de intubación por episodio | 13a | (6-20)b | 7.5a | (5-11)b | 10a | (7-15)b |
| Reintubación | 1 | 4 | 1 | 3,8 | 2 | 5,8 |
| Estridor | 6 | 24 | 4 | 15,3 | 2 | 5,8 |
| Displasia broncopulmonar | 5 | 20 | 3 | 11,5 | 2 | 5,8 |
| Hipertensión (tensión arterial sistólica) | 0 | 0 | 0 | 0 | 3 | 8,8 |
| Hipotonía | 1 | 4 | 2 | 7,6 | 0 | 0 |
| Hiporreflexia | 0 | 0 | 0 | 0 | 1 | 2,9 |
| Días de estancia | 44a | (22-51)b | 32,5a | (12-42)b | 30,5 | (14-46)b |
La utilización de la dexametasona durante la extubación ha demostrado ser útil en los pacientes recién nacidos con intubación prolongada, al disminuir el riesgo de estridor laríngeo, reintubación y displasia broncopulmonar3,12. El estudio muestra un uso frecuente para esta indicación con una frecuencia baja de reintubación y estridor.
Por el contrario, los estudios muestran que no hay beneficio de la prescripción rutinaria en prevenir desenlaces como mortalidad y displasia broncopulmonar, por lo que es importante que solo se utilice en situaciones específicas como en riesgo de edema laríngeo, como es la intubación prolongada11. El estudio muestra un porcentaje no despreciable de casos que no tiene una indicación muy clara para su uso, que se podría mejorar.
Las características demográficas como peso, etiologías y edad gestacional fueron similares a las reportadas en la literatura donde se ha utilizado este tipo de estrategias13,14. Las enfermedades que con mayor frecuencia se presentaron fueron la prematurez y el bajo peso al nacer, similar a los hallazgos de Méndez et al.15.
Acerca de la prescripción de dexametasona se encontró una evidente variabilidad en la formulación con dosis que oscilaron entre 0,1mg/kg/dosis hasta 2mg/kg/dosis, con una mayor formulación de dosis>0,5mg/kg/dosis, para una dosis acumulada promedio de 1,5mg/kg. Esto está acorde con el vacío actual del conocimiento en determinar qué dosis específica de dexametasona se requiere buscando la mejor efectividad del medicamento, y evitando así la presencia de eventos adversos a corto y a largo plazo16. En los primeros ensayos en la década de los 70 se utilizó dexametasona en dosis consideradas altas de 0,5mg/kg/día con evidencia de más eventos adversos17, pero estudios posteriores mostraron que dosis bajas como 0,2mg/kg/día son igualmente efectivas. El estudio DART9, que hasta la fecha es el de mejor calidad metodológica reportado, utilizó un régimen de dosificación que comienza con 0,15mg/kg/día por 3 días, luego 0,10mg/kg/día por 3 días, después 0,05mg/kg/día por 2 días y por último 0,02mg/kg/día por 2 días, para un total de 0,89mg/kg durante 10 días sin pérdida de eficacia y con baja presencia de eventos adversos. La dosis diaria y acumulada de este estudio está por encima de las del estudio DART9.
Otro motivo de controversia es el momento de seguridad para aplicar esta terapia. En el estudio DART9 y en otras revisiones sistemáticas18,19 recomiendan iniciar la primera dosis solo luego de los 7 días de vida para evitar eventos no deseados debido a la inmadurez del paciente. En el estudio se observa un porcentaje importante que recibió su primera dosis antes de los 7 días de vida, situación que se podría corregir en el futuro.
Los corticosteroides son medicamentos que pueden ayudar a romper el ciclo de la lesión pulmonar y la inflamación en los bebés con displasia broncopulmonar, y muchos estudios con esteroides posnatales han mostrado que son eficaces en la reducción de las necesidades de oxígeno y facilitan la extubación de recién nacidos prematuros17. El estudio realizado por Davis et al.4 evaluó dosis bajas de dexametasona para displasia broncopulmonar severa, iniciando con dosis de 0,05mg/kg/día, disminuyéndola por 9 días, con una dosis acumulada de 0,24mg/kg, presentando una extubación exitosa en 12 de los 16 bebés, lo que confirma la utilidad de los corticoides ante compromisos pulmonares severos. Nuestro estudio presentó una frecuencia de displasia del 11%, que es menor a la reportada en nuestro país, que es un 44% mayor, y la local que es tan alta como del 50%, e inclusive la referida para Latinoamérica, que es del 24,4%.
En este estudio la frecuencia de IOT y hospitalización en UCI fue similar entre los pacientes con y sin uso de dexametasona. Esto se puede deber a que no hay un efecto claro sobre estos desenlaces en la literatura, o a la alta variabilidad en la formulación de este medicamento, lo que llevó a que en algunos casos estuviera por debajo de las dosis recomendadas. Es importante y necesario realizar estudios con otras metodologías, que evalúen los desenlaces de acuerdo con la dosis administrada y su relación con la morbilidad del neonato.
Dentro de las limitaciones que encontramos en este estudio está la imposibilidad de realizar asociaciones causales, aunque nos da una idea global de la manera en la que es la formulación de la dexametasona en la UCIN del Hospital de San José. Otra limitación es que los resultados no son extrapolables a otras unidades, solo son representativos de esta población. Consideramos que las historias clínicas cuentan con la información suficiente y veraz con respecto a las demás variables evaluadas, y se encontró un nivel de registro más que adecuado, evitando así un sesgo en la información por la naturaleza retrospectiva del estudio.
ConclusionesLa profilaxis con dexametasona en la extubación de los pacientes hospitalizados en la UCIN del Hospital de San José es una estrategia común y frecuente, sin embargo existe una importante variabilidad en el uso y en la dosis formulada, por lo que se requiere la implementación de una estrategia que unifique los criterios de formulación, tanto en la fecha de inicio como en la dosis y duración.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.