La miocardiopatía periparto es un subtipo de miocardiopatía que se diagnostica al final del embarazo o durante los primeros meses posparto. De etiología poco conocida, se caracteriza por una disfunción sistólica ventricular izquierda y se manifiesta clínicamente en forma de insuficiencia cardíaca, con marcada retención hidrosalina y, en ocasiones, fallo ventricular severo que precisa soporte inotrópico, asistencia ventricular e incluso trasplante. El manejo anestésico obstétrico depende del grado de afectación cardíaca y debe orientarse a controlar y optimizar el estado hemodinámico y la función cardíaca durante la cirugía y el postoperatorio inmediato. Presentamos el caso de una gestante de 37 años diagnosticada de miocardiopatía periparto, sometida a cesárea urgente por inducción farmacológica fallida, en la que se realizó anestesia locorregional epidural de forma exitosa.
Peripartum cardiomyopathy is a cardiac disorder that occurs toward the end of pregnancy and the months following delivery. The etiology remains unknown in most cases and it is characterized by left ventricular impaired systolic function. The clinical course included heart failure symptoms and in many cases severe left ventricle failure. Usually it needs inotropic and ventricular support even transplantation. The anesthetic management depends of failure degree and may be orientated to control and optimize the hemodynamic and cardiac function during surgery and inmmediate post-partum period. The case is presented of a 37 years-old pregnant woman with peripartum cardiomiopathy who required emergency cesarean section due to failed pharmacologic induction. An epidural anesthesia was performed successfully.
La miocardiopatía periparto (MPP) es una forma de miocardiopatía dilatada considerada de origen idiopático. Se creen implicados factores inmunológicos, por sensibilización contra antígenos de células hematopoyéticas fetales, miocarditis e incluso el estrés hemodinámico que supone la gestación. Hay autores que la consideran una miocardiopatía de origen genético-familiar desencadenada por el embarazo. Existen otros factores como la edad materna tardía, la multiparidad, los embarazos múltiples, la raza afroamericana o la HTA durante el embarazo que también parecen favorecer esta complicación1. Sus criterios diagnósticos se basan en 3 condiciones2:
- 1.
Insuficiencia cardíaca (IC) de inicio en el último mes del embarazo hasta el quinto mes del puerperio.
- 2.
Reducción de la función sistólica, fracción de eyección (FE)<45% (generalmente medida con ecocardiograma).
- 3.
Ausencia de otras causa de insuficiencia cardíaca con FE deprimida.
En Estados Unidos, Canadá y Europa se trata de una enfermedad rara y la incidencia se estima en 1/2.500-4.000 nacimientos; en otros países es mucho más frecuente (1/1.000 en Sudáfrica y 1/300 en Haití). Estas diferencias pueden deberse a la dieta, al estilo de vida, a otras condiciones médicas o a la genética. Los estudios más recientes apuntan a un ligero ascenso en la incidencia motivada, en parte, por la mejora en los recursos diagnósticos y el mayor conocimiento del problema2,3.
Los síntomas de IC incluyen fatiga, disnea y retención hídrica. Debido a la superposición de síntomas debidos al embarazo, sobre todo en el tercer trimestre y el puerperio, el diagnóstico puede ser difícil y retrasarse.
El manejo de la MPP está basado en las guías de IC aguda y crónica4. A tener en cuenta que durante el embarazo están contraindicados los IECA, ARA-II y antagonistas de la aldosterona por su fetotoxicidad. Pueden utilizarse hidralazina o nitratos para disminuir la poscarga. También se pueden administrar bloqueadores beta, siendo el preferido el metoprolol, pero se debe supervisar al recién nacido para descartar efectos secundarios (hipoglucemia, bradicardia y otros). Los diuréticos solo se utilizan ante la presencia de síntomas de congestión pulmonar. Si la evolución es a IC aguda refractaria a tratamiento médico habrá que considerar el uso de agentes inotrópicos (dopamina y levosimendán), balón de contrapulsación intraaórtico, asistencias ventriculares o incluso el trasplante cardíaco.
También hay que considerar el riesgo embólico, pues es mayor que en otros tipos de miocardiopatía dilatada, siendo necesaria la anticoagulación en caso de trombo intracardíaco, embolia sistémica o fibrilación auricular. Si se utilizan anticoagulantes orales en la semana 36, estos deben ser sustituidos por heparina debido al riesgo de parto prematuro.
En cuanto al pronóstico se estima que el 50% de las pacientes con MPP recuperan una función cardíaca normal, un 25% persisten con FE deprimida, pero se mantienen estables, y otro 25% progresa a IC severa. Estudios recientes sugieren que el pronóstico ha mejorado con la medicación y los dispositivos actuales, con una supervivencia del 90-95%. El riesgo en embarazos sucesivos depende de la recuperación o no de la FE, en mujeres que no hayan recuperado la función cardíaca se desaconseja un nuevo embarazo.
La actuación anestésica en el momento del parto y durante el posparto inmediato debe orientarse a la optimización hemodinámica para evitar un agravamiento de la función miocárdica, seleccionando la técnica más adecuada según se trate de un parto vaginal o una cesárea. Esta indicación atenderá a criterios obstétricos.
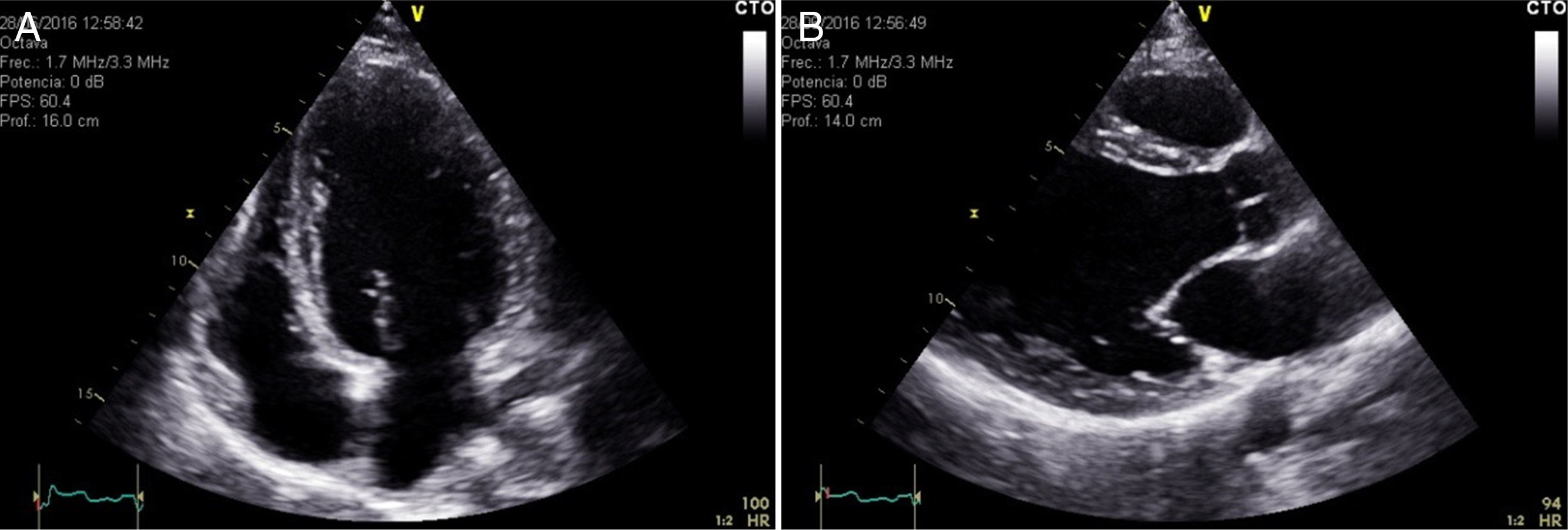
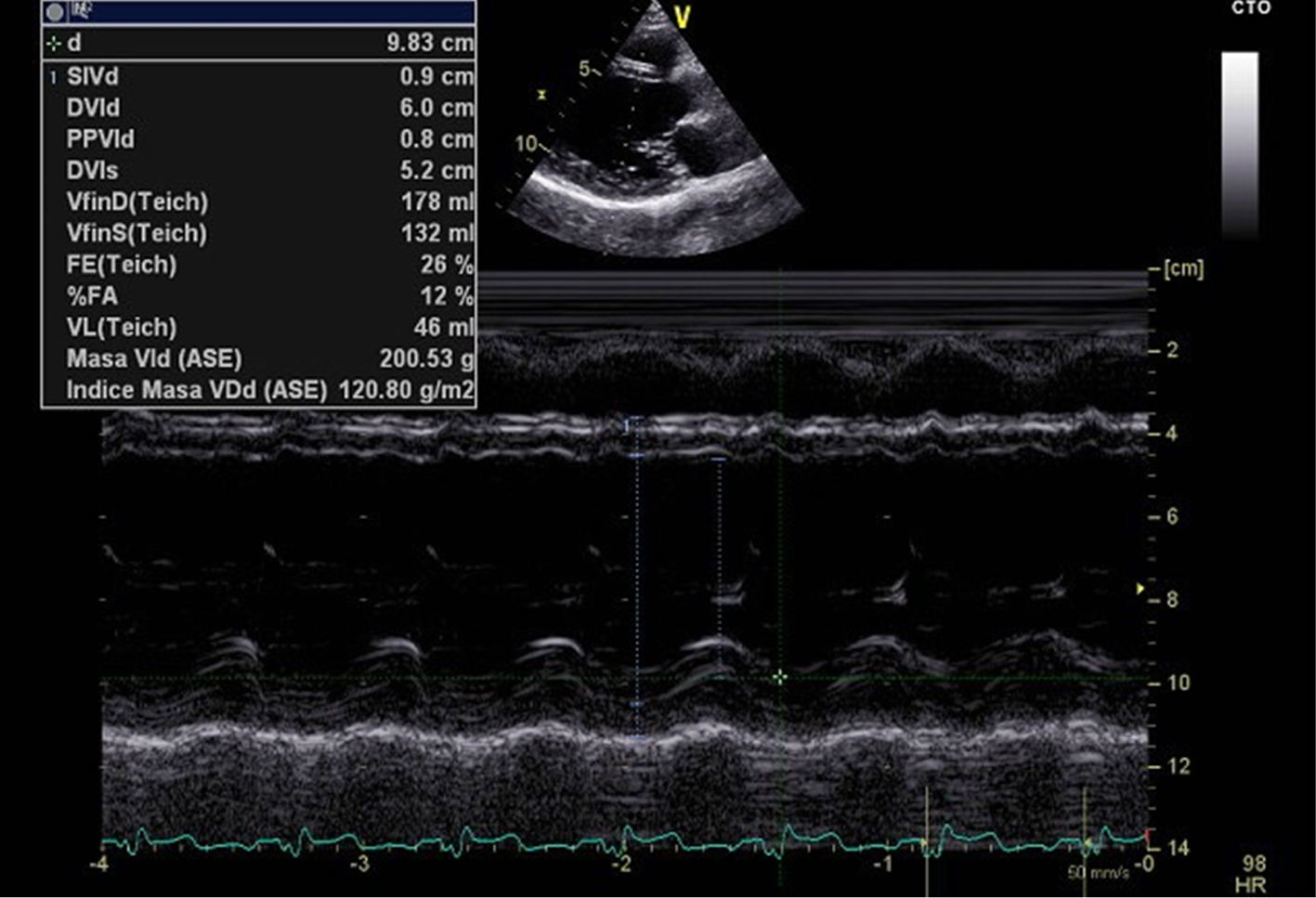
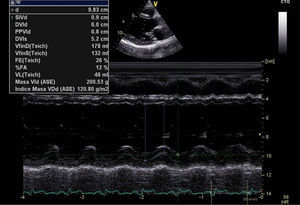
Caso clínicoMujer primípara de 37 años diagnosticada de MPP versus taquimiopatía por taquicardia sinusal inapropiada, presentando IC sistólica, con FE del 25% y bloqueo completo de rama izquierda (BCRIHH). Puntuación CARPREG 1 (riesgo de complicaciones 27%) y de la OMS III-IV. La paciente seguía revisiones cardiológicas desde la 18.ª semana de gestación, momento en el que se detectó una taquicardia sinusal>120 latidos por minuto (lpm). A medida que fue avanzando el embarazo, la paciente fue evolucionando hacia una IC sistólica, con dilatación progresiva del VI y deterioro de la FE (figs. 1 y 2). Sin otros antecedentes personales médicos ni quirúrgicos de interés; bajo tratamiento con bisoprolol 5mg/12h.
La paciente ingresó al servicio de obstetricia con 40 semanas de gestación para terminación de la misma mediante inducción farmacológica con oxitocina por detección de oligoamnios y parto de alto riesgo.
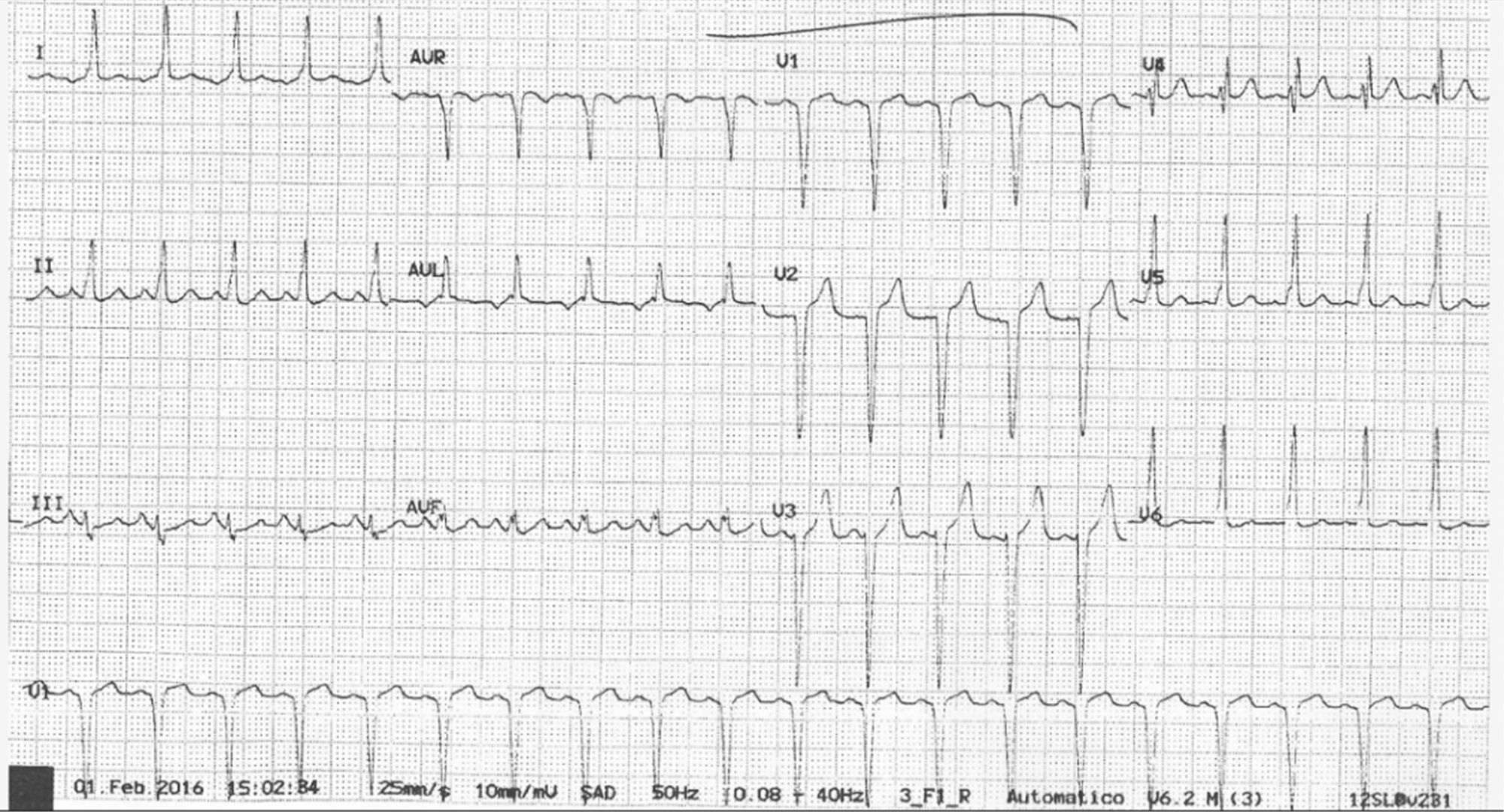
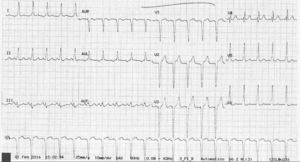
Se indicó analgesia epidural para el parto. Clínicamente la paciente estaba asintomática, sin presentar disnea, ortopnea, edemas significativos ni molestias torácicas de ningún tipo. La tensión arterial (TA) era de 95/65mmHg. El electrocardiograma (ECG) mostraba taquicardia sinusal a 114lpm y BCRIHH ya conocido (fig. 3). La técnica se realizó sin incidencias y siguiendo el protocolo habitual tras descartar contraindicaciones y previa información y firma de consentimiento informado. Se administró un bolo inicial de 5ml de levobupivacaína a 0,25% con 0,05mg de fentanilo, con posterior perfusión epidural continua de levobupivacaína 0,125%+fentanilo 1mcg/ml, a ritmo de 8ml/h.
El procedimiento se realizó bajo monitorización de ECG y oximetría capilar periférica, que se mantuvieron estables. La monitorización no invasiva con control de TA periódica cada 15-20minutos se mantuvo durante el tiempo que la paciente permaneció en la sala de dilatante. Se aplicó fluidoterapia restrictiva con cristaloides y control de diuresis horaria mediante sondaje. La paciente permaneció hemodinámicamente estable durante el tiempo de la inducción, sin presentar ningún tipo de descompensación clínica cardiológica.
Tras 12h de inducción con dinámica activa de parto y bolsa rota, la dilatación alcanzada fue de 2cm. La inducción se consideró fallida y se indicó una cesárea electiva.
A su llegada a quirófano la paciente mantenía TA 110/70mmHg, FC 100lpm y oximetría capilar del 100%. Se colocó cánula nasal a 2lpm con FiO2 100% y se monitorizaron los parámetros habituales (SatO2, ECG, FC, TA, capnografía). Se adoptó la posición en decúbito supino, con ligero decúbito lateral izquierdo. Se decidió realizar anestesia locorregional epidural por catéter normofuncionante que ya tenía insertado. Previamente se canalizó la arteria radial derecha bajo infiltración local de 1ml de lidocaína 2% para monitorización continua de TA intracesárea. Se optó por anestesia con mepivacaína bicarbonatada al 2% en dosis total de 240mg+0,15mg de fentanilo, administrándola de forma secuencial en bolus de 2-3ml cada 2minutos.
La incisión quirúrgica se inició 15 minutos después de completar la dosis epidural, y tras comprobar un nivel óptimo de calidad anestésica. La paciente no presentó alteraciones hemodinámicas significativas durante el procedimiento, manteniendo la TAS en torno a 95-130mmHg y la TAD 55-70, con FC 98-115lpm. No desarrolló ningún síntoma ni signo clínico de ICC, ni tampoco arritmia sobreañadida. Hemorragia intraquirúrgica dentro de los límites habituales, sin otras complicaciones.
Tras la intervención, la paciente fue trasladada a la UCI donde continuó vigilancia estricta durante 48horas. La evolución fue satisfactoria desde el punto de vista clínico, manteniéndose la tendencia a la taquicardia sinusal y la imagen de BCRIHH persistente en el ECG.
DiscusiónLas miocardiopatías que cursan con función sistólica deprimida se caracterizan por un fallo de la función contráctil de las fibras musculares, provocando una disminución del volumen sistólico y de la FE. Esto se acompaña habitualmente de una dilatación ventricular progresiva. A medida que la enfermedad va avanzando aumenta la dificultad para mantener un gasto cardíaco (GC) adecuado y aparecen los signos y síntomas característicos de la IC. La compensación fisiológica mediante la activación de determinados mecanismos neurohumorales y neuroendocrinos propicia que el GC se mantenga a expensas de mantener presiones de llenado anormalmente elevadas, lo cual, mantenido de una forma crónica, termina agravando la función miocárdica.
Desde un punto de vista anestésico, cualquier paciente con una miocardiopatía de este tipo deberá ser cuidadosamente tratada, teniendo como prioridad evitar el deterioro hemodinámico.
Además de todas las consideraciones previas, se tendrán en cuenta los cambios hemodinámicos propios del momento del parto. La situación de ansiedad y dolor aumentarán la FC y las cifras de TA, tanto sistólica como diastólica. Las contracciones uterinas no solo precipitan el dolor, también transfieren del orden de 300 a 400ml de sangre hacia la circulación sistémica, aumentando así el GC en cada contracción. En este sentido, la posibilidad de analgesia de parto mediante catéter epidural, siempre que no exista contraindicación, confiere una serie de ventajas que hacen que sea de uso fundamental en la mayoría de los casos. El control del dolor del parto y la reducción de la ansiedad contribuyen a la estabilidad de los parámetros hemodinámicos. El bloqueo progresivo de las fibras autonómicas simpáticas que permite la analgesia de parto, actuará reduciendo las resistencias periféricas, disminuyendo así tanto la pre como la poscarga. Este efecto terapéutico es similar al se pretende conseguir para prevenir la descompensación cardíaca mediante otro tipo de fármacos, aunque siempre debe evitarse que los cambios se produzcan de forma brusca5. La monitorización hemodinámica debe considerarse desde el inicio de la dilatación6.
En cuanto a la terminación de la gestación, en principio se prefiere el parto vaginal espontáneo para la mayoría de las afecciones cardíacas, sin que la MPP sea una excepción, usando analgesia de parto y un umbral bajo para la terminación mediante parto instrumental, evitando, en la medida de lo posible, los pujos. Parecen los métodos más seguros, ya que producen menos cambios hemodinámicos que en una cesárea, hay menor pérdida sanguínea, evita el estrés quirúrgico y el riesgo de infección también es menor7.
La indicación de cesárea suele obedecer a criterios obstétricos, pero existen ciertas condiciones maternas que también la recomiendan, siendo de especial interés en este caso el deterioro hemodinámico materno rápido cuando el parto vaginal no sea posible6–12 (tabla 1). En el caso que presentamos la inducción fallida fue el motivo de la cesárea.
Indicaciones de cesárea en pacientes con miocardiopatía (aparte de las indicaciones obstétricas)
| Síndrome de Marfan con dilatación aórtica>45mm En toda paciente en tratamiento con dicumarínicos en el momento del parto En casos de deterioro hemodinámico materno rápido en los que el parto vaginal no sea posible Algunos autores recomiendan la cesárea en mujeres con hipertensión pulmonar severa |
Fuente: Robertson et al.7.
Desde el punto de vista anestésico se han descrito casos de manejo tanto con anestesia general13 como con epidural14, si bien hay menos experiencia con esta última y, por tanto, ha de realizarse de forma cuidadosa y bajo control hemodinámico estricto. Debe evitarse el uso de anestesia intradural por sus rápidos efectos sobre el sistema cardiovascular.
Decidimos realizar anestesia mediante el catéter epidural, administrando el anestésico con pequeñas dosis de opiáceos y de forma secuencial para minimizar el impacto hemodinámico. La monitorización continua de la TA permitió un control intraoperatorio óptimo, sin que la paciente precisara ningún tipo de soporte vasoactivo ni tratamiento inotrópico.
La anestesia epidural, por tanto, resultó una medida eficaz y segura en esta paciente. Aunque la experiencia es menor que las cesáreas realizadas bajo anestesia general, consideramos que esta técnica también puede ser de elección siempre y cuando no existan contraindicaciones como la anticoagulación activa o la urgencia obstétrica.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran la no existencia de conflicto de intereses.