Definir un conjunto básico de indicadores de calidad de la atención hospitalaria del paciente con ictus, basados en la evidencia científica, a partir de la priorización consensuada por un panel de expertos representativo de los profesionales que realizan la atención hospitalaria en tres comunidades autónomas (Cataluña, Aragón y Baleares).
Material y métodoUn panel de 56 expertos, implicados en la atención hospitalaria de los pacientes con ictus, priorizaron mediante un método Delphi modificado en dos vueltas un set de indicadores de calidad de entre 70 indicadores identificados en la revisión de la literatura y utilizados en experiencias previas. Se consideró el consenso cuando el 75% o más de los panelistas puntuaron el indicador en el mismo tercil, en una escala de Likert 1-9.
ResultadosEl conjunto final de 29 indicadores comprende los mejor puntuados representativos de todas las áreas de atención hospitalaria. Un subgrupo de 5 indicadores es de aplicación únicamente en los Centros de Referencia de Ictus (Primary Stroke Centers, PSC). Los tres indicadores mejor puntuados y con el mayor consenso de los expertos son anticoagulación en la FA, antitrombóticos al alta y fisioterapia al alta gestionada.
ConclusionesA partir del método Delphi, se ha obtenido un set de indicadores actualizados, apoyados por la evidencia científica, considerados de elevada importancia y consensuados por los expertos que realizan la atención hospitalaria a los pacientes con ictus de los territorios participantes, que representan alrededor del 20% de la población española.
To define a core set of evidence-based performance indicators (PIs) for the assessment of in-hospital stroke care quality by means of consensus prioritisation by a panel of experts representing stroke care professionals in three Autonomous Communities (Catalonia, Aragon and Balearic Islands).
Material and methodsWe used a modified Delphi method in two rounds to prioritise a set of PIs from among 70 indicators identified by a review of the literature and those already used in previous experiences. Consensus on validity was reached when ≥75% of panellists rated a PI in the top tertile, using a 1-9 Likert scale. On the basis of the percentage distribution of annual stroke admissions in each one of the 3 regions, we configured a multidisciplinary panel of 56 experts involved in the hospital care of acute stroke patients.
ResultsTwenty-nine out of the 70 PIs initially put forward to the panel, have been prioritised after 2 rounds. The eventual core set of PIs consists of those with the highest scores and represent all areas of hospital-based stroke care. A subgroup of 5 PIs is applicable to Primary Stroke Centres only. The 3 highest rated PIs, which achieved the greatest consensus among the experts, are anticoagulants for AF, antithrombotics at discharge and continued physiotherapy planned at discharge.
ConclusionsThrough a Delphi method, we have obtained a core set of evidence-based PIs considered of high importance and agreed by a multidisciplinary panel of stroke care experts from the participating Communities, which represent over 20% of the Spanish population.
En la actualidad, disponemos de evidencia acerca del manejo efectivo del paciente con enfermedad cerebrovascular aguda1 y de su tratamiento2. Sabemos, además, que la prevención secundaria tras el ictus reduce significativamente el riesgo de recurrencia y la morbimortalidad vascular de estos pacientes3. Las guías de práctica clínica (GPC) estandarizan procesos y procedimientos4, y son un medio de traslación de la evidencia científica a la práctica, contribuyendo a la disminución de la variabilidad de la calidad de la atención. No obstante, la existencia de las GPC no garantiza su implementación, por lo que se han desarrollado múltiples métodos para asegurar la utilización de las mismas en la práctica clínica5. La realización de auditorías periódicas que registren la incorporación de recomendaciones específicas de una GPC y la comunicación activa de sus resultados son algunos de los métodos propuestos6,7. Diversas experiencias pueden servir de referencia, como el programa Get With The Guidelines-Stroke (GWTG-stroke), para la mejora de la adherencia a determinados estándares de calidad en los EUA8, o el National Sentinel Audit of Stroke que periódicamente evalúa la calidad de la atención hospitalaria del paciente con ictus en Gran Bretaña9.
A partir del modelo británico, el Plan Director de Enfermedades del Aparato Circulatorio/Enfermedad Vascular Cerebral (PDEAC/EVC), del Departamento de Salud de la Generalitat de Catalunya, impulsó dos auditorias (audits) del ictus tras la publicación de la GPC del Ictus a finales de 200510. En ambos audits11–13, se determinó el cumplimiento de una serie de recomendaciones seleccionadas, por un grupo reducido de expertos, de entre las más de 250 recomendaciones de la GPC del Ictus. Esta selección se hizo con base en la relevancia científica y/o clínica y fruto de ello se elaboró la herramienta Audit vs.1.0 que reunió 43 indicadores de proceso identificados por el grupo. Recientemente, se han publicado los resultados del Segundo Audit del Ictus13, que demuestran que, a pesar de la heterogeneidad interhospitalaria e intersectorial en el cumplimiento de determinados indicadores, el modelo impulsado por el PDEAC/EVC consigue mejorar de forma significativa la mayoría de los indicadores auditados. Esta experiencia, sin embargo, tiene algunas limitaciones: la ausencia de indicadores de resultado y un proceso de selección poco sistematizado llevado a cabo por un grupo reducido de expertos. Si tenemos en cuenta que la calidad asistencial es la característica de los servicios que permite aumentar la probabilidad de conseguir un resultado deseado siendo consistente con el conocimiento científico disponible14 y que los pilares de la calidad del proceso asistencial son la estructura, el proceso y los resultados15, la versión 1.0 de la herramienta audit del ictus es mejorable.
El método de consenso Delphi fue desarrollado por la industria de los Estados Unidos inicialmente con fines predictivos16, y se ha aplicado con diversas finalidades en todos los campos de la ciencia, así como en investigación médica y de servicios de salud17. Entre otras aplicaciones, se ha utilizado como herramienta para determinar prioridades de investigación18,19, para el desarrollo de instrumentos de medida20 y el desarrollo y selección de indicadores para la evaluación de la práctica clínica general y también en la atención de los pacientes con ictus21,22. Las características definitorias del método Delphi son el anonimato entre los expertos, la iteración y retroalimentación en, al menos, dos vueltas sucesivas, y el análisis estadístico explícito de las respuestas16.
En los sistemas sanitarios públicos es necesaria la implicación y el impulso de la administración en el desarrollo y utilización de herramientas para la evaluación periódica de la calidad de los servicios. En una enfermedad de relevancia epidemiológica indiscutible como el ictus, es imprescindible el desarrollo de un instrumento evaluativo único de la calidad asistencial basado en la evaluación del proceso, la estructura y el resultado a partir de un procedimiento sistemático basado en la evidencia científica y consensuado por la gran mayoría de los profesionales implicados en la asistencia23. Por todo ello, nos planteamos un proyecto con la participación de tres comunidades autónomas (Cataluña, Baleares y Aragón), cuyo objetivo principal fue definir un conjunto básico de indicadores de calidad de la atención hospitalaria del paciente con ictus a partir del consenso de un grupo de expertos representativo de los profesionales que realizan la atención hospitalaria al paciente con ictus en estos territorios. Y ello con el propósito de optimizar el sistema de información necesario para el seguimiento de la atención al ictus en su ámbito, mejorar la implicación de los profesionales involucrados y compartir los resultados y buenas prácticas, llegado el caso.
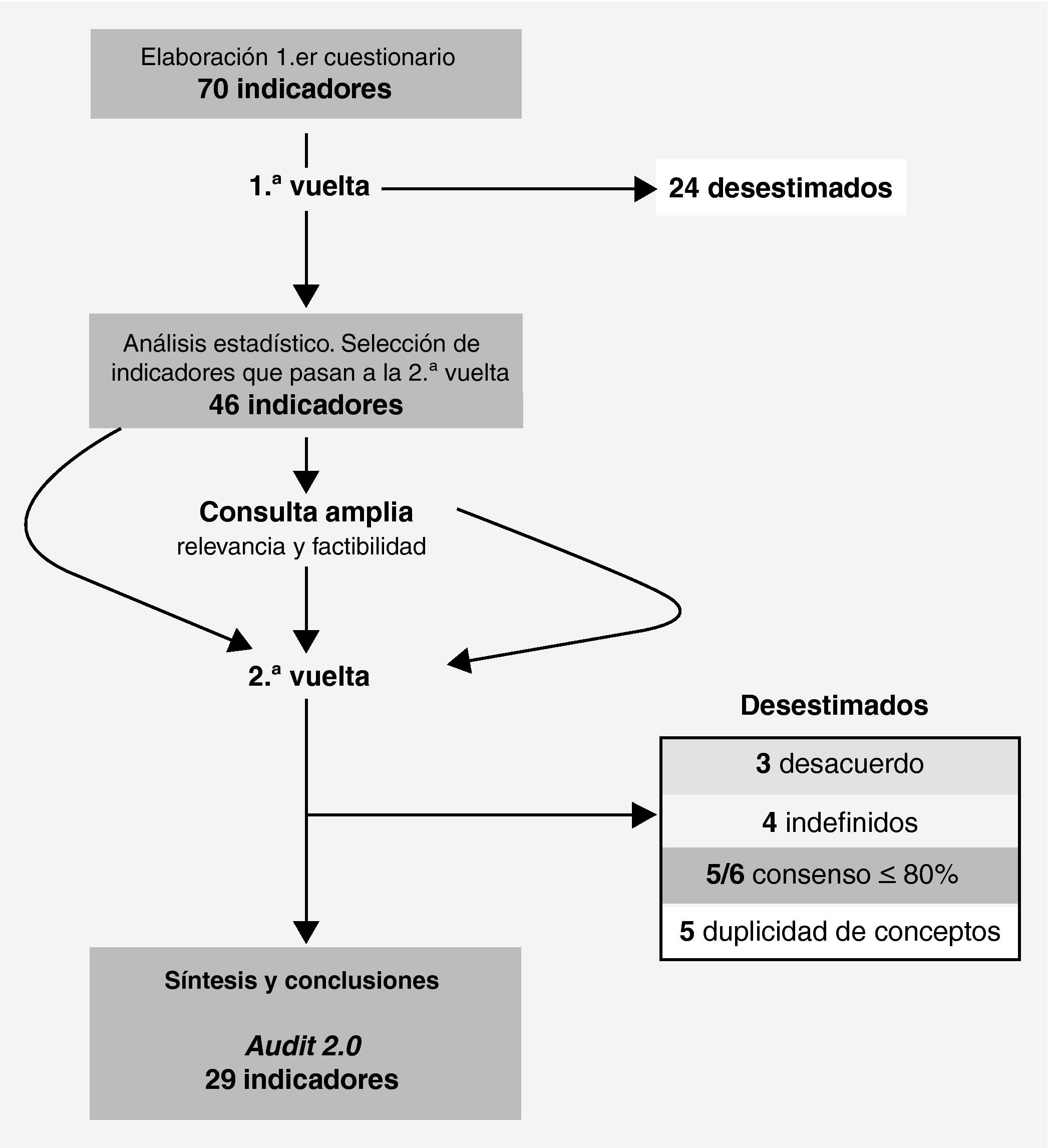
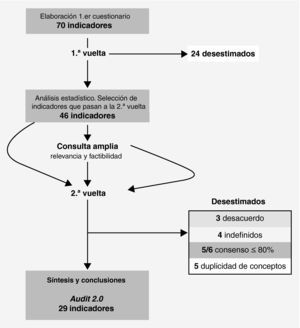
Material y métodoSe ha utilizado una técnica formal de consenso, el método Delphi, modificado en dos vueltas. Entre ambas vueltas se realizó una consulta a una muestra amplia de los profesionales implicados en la atención del ictus cuyo objetivo fue conocer su opinión acerca de la relevancia y la factibilidad de los indicadores de calidad priorizados tras la primera vuelta. El resultado de esta consulta se adjuntó, a modo de información adicional, a los resultados de la primera vuelta del Delphi y se remitió al panel de expertos (fig. 1).
Exploración del tema y selección de indicadoresSe realizó una revisión de la literatura sobre medidas de calidad utilizadas en proyectos publicados relacionados con la atención a los pacientes con ictus, GPC y potenciales revisiones sistemáticas de evidencia disponibles en la base de datos PubMed/MEDLINE y en fuentes de información disponibles hasta mayo de 2009. También se realizó una búsqueda en la web de las sociedades científicas de neurología e instituciones de alcance estatal e internacional. Se priorizó la literatura que ofrecía información sobre la calidad de la evidencia y aquella de procedencia relevante (GPC, sociedades científicas, agencias gubernamentales). Fueron aceptados 18 documentos donde se referían indicadores de calidad de la atención hospitalaria de los pacientes con ictus (consúltese el documento complementario online).
Tras la revisión de la literatura, se elaboró un documento inicial con los indicadores identificados, 300 en total, la mayoría de los cuales coincidentes o bien que exploraban recomendaciones iguales o similares de las GPC. El documento contenía la información necesaria (metodológica y sobre calidad de la evidencia) para la lectura, discusión y síntesis por el Grupo de Trabajo. Una vez valorados todos los indicadores y eliminados los redundantes, se confeccionó el primer cuestionario que se remitió a los panelistas en la primera vuelta. Este incluía 70 indicadores clasificados según diferentes áreas de atención y la información sobre cada uno de ellos para poder opinar: descripción del indicador, fórmula de cálculo del cumplimiento y referencia bibliográfica.
Panel de expertosLa configuración porcentual del panel de expertos se determinó según el número de contactos hospitalarios declarados al conjunto mínimo básico de datos del alta hospitalaria (CMBD-AH) de 2008 en cada una de las comunidades autónomas. De esta forma, se estableció que el 60% de los panelistas sería de Cataluña, el 25% de Aragón y el 15% restante de Baleares. Los miembros del grupo investigador seleccionaron el panel a partir del conocimiento de los profesionales de su comunidad autónoma y según los criterios establecidos: representación geográfica de los distintos sectores de cada comunidad, procedencia de diferentes categorías hospitalarias, balance de especialidades, prestigio reconocido y años de experiencia. Además, se buscó alcanzar un número adecuado de participantes, con la necesaria implicación y el compromiso para asegurar la cumplimentación de los sucesivos cuestionarios, e incrementar la fiabilidad del juicio.
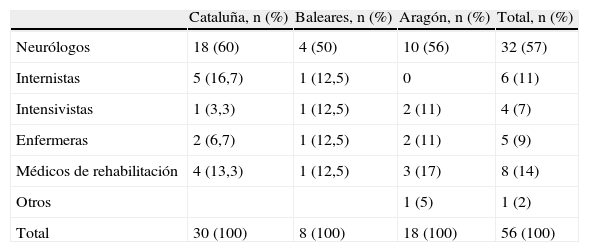
Los 56 expertos, informados por correo electrónico e invitados a participar en el proyecto, aceptaron la propuesta. En la configuración final del panel el 53,6% de los expertos fueron de Cataluña, el 14,3% de Baleares y el 32,1% de Aragón. En la tabla 1 se muestra la composición según especialidades.
Composición del panel de expertos del estudio Delphi
| Cataluña, n (%) | Baleares, n (%) | Aragón, n (%) | Total, n (%) | |
| Neurólogos | 18 (60) | 4 (50) | 10 (56) | 32 (57) |
| Internistas | 5 (16,7) | 1 (12,5) | 0 | 6 (11) |
| Intensivistas | 1 (3,3) | 1 (12,5) | 2 (11) | 4 (7) |
| Enfermeras | 2 (6,7) | 1 (12,5) | 2 (11) | 5 (9) |
| Médicos de rehabilitación | 4 (13,3) | 1 (12,5) | 3 (17) | 8 (14) |
| Otros | 1 (5) | 1 (2) | ||
| Total | 30 (100) | 8 (100) | 18 (100) | 56 (100) |
La priorización de los indicadores se realizó, en ambas vueltas, mediante una escala de importancia de Likert, donde cada indicador se valoró desde 1 (nada importante) a 9 puntos (muy importante). Según la puntuación concedida a cada indicador, se utilizó el valor de la mediana como aproximación al grado de importancia otorgado por el panel. Así, en función del tercil en el que se situó la mediana, el grado de importancia de los indicadores fue elevado (medianas entre 7 y 9), medio (4-6) o escaso (1-3).
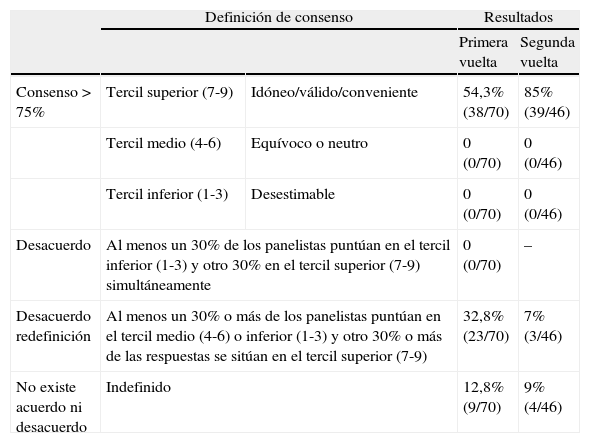
La definición de consenso varía de unos estudios a otros en función de los diferentes criterios utilizados para valorar los resultados18,24. En el presente estudio, se ha considerado el consenso cuando el 75% o más de las respuestas coincidían en alguno de los tres terciles25,26, definición ya utilizada en una experiencia previa21. De esta forma, los indicadores con un 75% o más de puntuaciones en el tercil superior fueron considerados válidos/idóneos/convenientes, los que alcanzaron consenso en el tercil medio se consideraron equívocos o neutros y cuando el consenso se situaba en el tercil inferior, se consideraron no válidos o desestimables. Cuando no hubo consenso ni desacuerdo, los indicadores se consideraron indefinidos (tabla 2).
Definición de consenso y resultados en ambas vueltas del estudio Delphi
| Definición de consenso | Resultados | |||
| Primera vuelta | Segunda vuelta | |||
| Consenso > 75% | Tercil superior (7-9) | Idóneo/válido/conveniente | 54,3% (38/70) | 85% (39/46) |
| Tercil medio (4-6) | Equívoco o neutro | 0 (0/70) | 0 (0/46) | |
| Tercil inferior (1-3) | Desestimable | 0 (0/70) | 0 (0/46) | |
| Desacuerdo | Al menos un 30% de los panelistas puntúan en el tercil inferior (1-3) y otro 30% en el tercil superior (7-9) simultáneamente | 0 (0/70) | – | |
| Desacuerdo redefinición | Al menos un 30% o más de los panelistas puntúan en el tercil medio (4-6) o inferior (1-3) y otro 30% o más de las respuestas se sitúan en el tercil superior (7-9) | 32,8% (23/70) | 7% (3/46) | |
| No existe acuerdo ni desacuerdo | Indefinido | 12,8% (9/70) | 9% (4/46) | |
El primer cuestionario fue enviado al panel de expertos en junio de 2009, acompañado de la descripción del estudio Delphi, las instrucciones para la puntuación y los plazos de respuesta. Tras la primera vuelta, se desestimaron los indicadores en los que había acuerdo acerca de su escasa importancia, y pasaron a la segunda vuelta aquellos en los que había acuerdo sobre su importancia o duda o desacuerdo.
Previamente a la segunda vuelta, los panelistas recibieron información pormenorizada de los resultados obtenidos globalmente e individualmente en la primera vuelta. En la segunda vuelta se solicitó a los panelistas que, en la medida de lo posible, tuvieran en cuenta la priorización de los indicadores que, en su opinión, deberían ocupar los 15-20 primeros puestos, ya que se pretendía finalizar con un máximo de 20-25 indicadores de calidad de la atención al ictus.
Después de la segunda vuelta, el conjunto final de indicadores se configuró a partir de los siguientes criterios de selección: a) selección de los indicadores mejor puntuados; b) representación de las diferentes áreas de atención; c) selección de un subgrupo de indicadores de aplicación específica en los hospitales o centros de referencia ictus (CRI), y d) selección del indicador con mayor puntuación, si había duplicidad de conceptos.
Consulta ampliaCon el objetivo de aportar información adicional a los panelistas en relación con los indicadores priorizados en la primera vuelta, se llevó a cabo una consulta amplia (CA) a los profesionales implicados en la atención a los pacientes con ictus en todo el territorio. Esta información adicional se concretaba en la opinión sobre la relevancia y factibilidad de dichos indicadores. Se definió relevancia como la cualidad según la cual el indicador tiene especiales significación o importancia y es pertinente al fin que se persigue, y factibilidad como la posibilidad de ser medible y realizable. En ambos casos la evaluación era subjetiva, con valores de respuesta sí/no. Las respuestas de la CA (porcentaje de consultados que valora el indicador como relevante y factible) se adjuntaron a los resultados de la primera vuelta y fueron remitidos a los panelistas. El grupo contactado incluyó una muestra amplia de profesionales, desvinculados de los panelistas, elegidos por cada miembro del grupo de trabajo, en todos los hospitales de la red pública de su comunidad.
ResultadosTras la primera vuelta, el 54,3% (38/70) de los indicadores obtuvo el consenso del panel sobre la validez/idoneidad/conveniencia. En ningún caso hubo desacuerdo ni consenso en los terciles medio e inferior, por lo que se procedió a la redefinición de desacuerdo (tabla 2). Así, pasaron a la segunda vuelta 46 indicadores. El indicador «Neuroimagen < 72 h» fue descartado, pese a ser indefinido, por encontrarse la mayor parte de las puntuaciones en los terciles medio e inferior.
La CA de opinión se remitió a 205 profesionales, de los que respondieron el 36,1% (n=74). El 54% (n=38) eran neurólogos; el 25% (n=18), enfermeras, y el 21% (n=15), médicos rehabilitadores. Procedían de Cataluña el 61% (n=45), el 16% (n=12) de Baleares y el 23% (n=17) restante de Aragón. El 79,7% de los consultados consideró relevantes los indicadores priorizados en la primera vuelta, y el 56,6% los consideró factibles. El indicador que un mayor porcentaje de consultados consideró relevante fue «rtPA 3 h» y el que menos, «LDL 100». El más factible, según opinaron los consultados, fue el indicador «Glucosa basal» y el menos factible, «Atención en urgencias por experto en ictus» (tabla 3). En la segunda vuelta, la mediana de puntuaciones de todos los indicadores se situó en el tercil superior, denotando que todos fueron considerados de importancia elevada. Existió consenso sobre su validez en el 85% (39/46) de los indicadores, y el 72% (33/46) obtuvo un consenso ≥ 80%. Entre los indicadores restantes, hubo desacuerdo en 3 (7%) y resultaron indefinidos 4 (9%). El indicador mejor puntuado, y en el que se alcanzó mayor consenso (el 98,2% de los expertos lo puntuaron en el tercil superior), fue «Anticoagulación en la FA», cuya puntuación media fue de 8,41±0,62. Otros indicadores que obtuvieron un elevado consenso fueron «Antitrombóticos al alta» (8,33±0,9) y «Fisioterapia al alta gestionada» (8,07±0,89), ambos con el 96,4% de las puntuaciones en el tercil superior. El indicador «rTPA 3 h» obtuvo acuerdo sobre su validez (el 94,6% de las puntuaciones en el tercil superior y una puntuación media de 8,4±1,07). Los indicadores con puntuaciones medias más bajas fueron «Manejo de hipertermia ≥ 38,5°C» (6,4±1,9) y «Atención en urgencias por experto en ictus» (6,9±1,8).
Relevancia y factibilidad de los indicadores que pasan a la segunda vuelta según la opinión expresada en la consulta amplia por los profesionales del ictus
| Indicador de calidad de la atención del paciente con ictus | Relevancia, % (sí)a | Factibilidad, % (sí)a |
| Puerta-aguja 60 minutos | 92% | 70% |
| rtPA 3 h | 93% | 84% |
| Trombólisis i.v. | 81% | 84% |
| Complicaciones rtPA | 84% | 86% |
| TC craneal < 25 min | 91% | 70% |
| rtPA i.v. | 72% | 77% |
| Atención en urgencias por experto ictus | 73% | 42% |
| rtPA 4.30 h | 84% | 89% |
| Atención en urgencias de pacientes candidatos | 81% | 57% |
| Neuroimagen < 24 h del ictus | 86% | 88% |
| Glucosa basal | 88% | 93% |
| ECG basal | 88% | 89% |
| Profilaxis TVP | 78% | 85% |
| Hipoxia | 82% | 86% |
| Coagulación basal | 88% | 92% |
| Test disfagia | 92% | 84% |
| Hemograma basal | 81% | 93% |
| Antitrombóticos precoces | 77% | 81% |
| Antiplaquetarios < 48 h | 65% | 70% |
| Evaluación tratamiento rehabilitador < 48 h | 78% | 59% |
| Evaluación tratamiento rehabilitador ingreso | 86% | 86% |
| Movilización precoz 48 h | 84% | 80% |
| Rehabilitación precoz (fisioterapia/terapia ocupacional) | 70% | 54% |
| Evaluación por trabajador social < 7 días | 69% | 74% |
| Objetivos del tratamiento rehabilitador consensuados por un equipo multidisciplinario | 80% | 54% |
| Educación ictus | 86% | 62% |
| Perfil lipídico | 86% | 86% |
| Imagen vascular en ictus isquémicos/AIT | 80% | 74% |
| Evaluación neurológica | 81% | 84% |
| Imagen vascular-carótida | 80% | 74% |
| Manejo hipertermia ≥ 37,5°C | 65% | 73% |
| Abandono tabaquismo | 70% | 53% |
| Manejo hipertermia ≥ 38,5°C | 66% | 69% |
| Antitrombóticos alta | 81% | 85% |
| Fisioterapia continuada al alta gestionada | 82% | 78% |
| Mecanismo ictus | 80% | 73% |
| Anticoagulación en la FA | 82% | 84% |
| Antihipertensivos al alta | 77% | 78% |
| Tratado en una UI durante el ingreso | 65% | 58% |
| LDL 100 | 64% | 68% |
| LDL 100 | 76% | 80% |
| Antidiabéticos | 68% | 81% |
| Situación neurológica alta | 86% | 82% |
| Mortalidad intrahospitalaria | 85% | 86% |
| Discapacidad alta | 88% | 84% |
| Neumonía intrahospitalaria | 76% | 74% |
AIT: accidente isquémico transitorio; ECG: electrocardiograma; FA: fibrilación auricular; i.v.: intravenoso; LDL: lipoproteína de baja densidad; rtPA: recombinant tissue plasminogen activator; TC: tomografía computarizada; TVP: trombosis venosa profunda; UI: unidad de ictus.
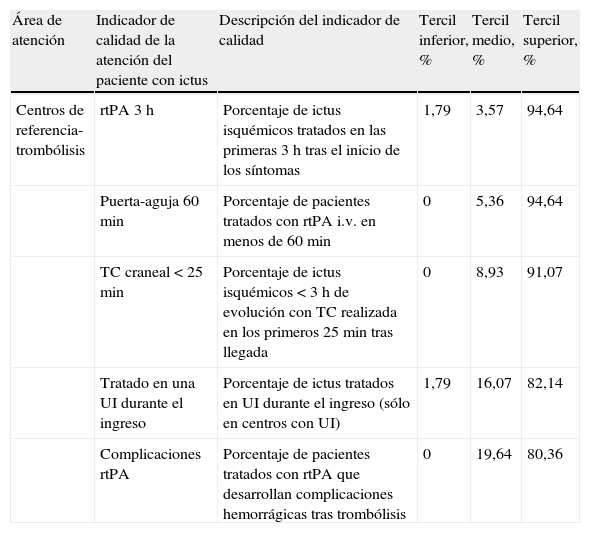
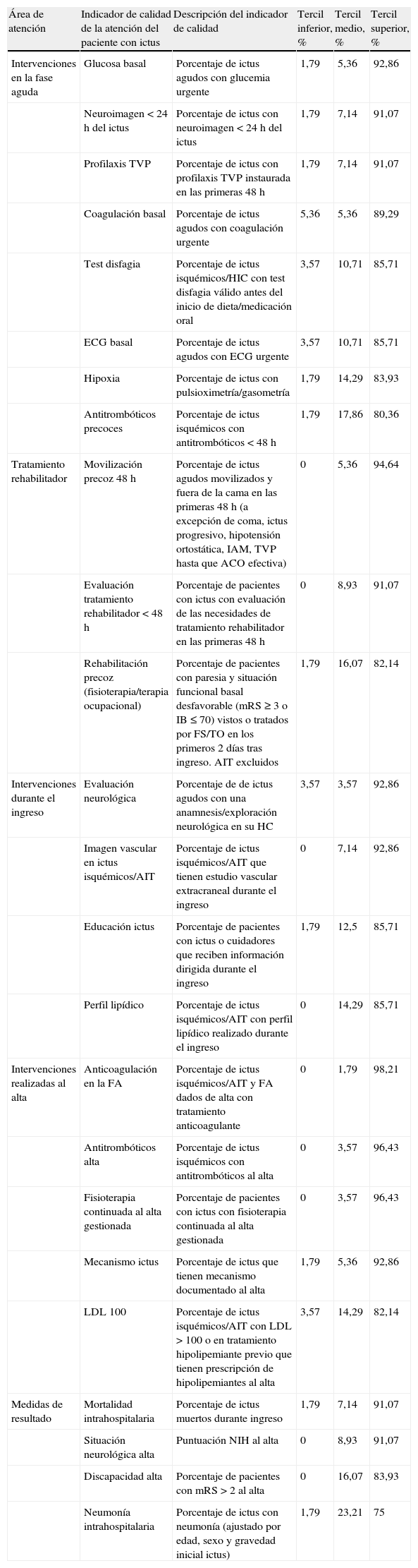
Según los criterios de selección definidos, fueron seleccionados 28 indicadores de los 33 de mayor puntuación y consenso superior al 80%. Los 5 indicadores restantes fueron desestimados por ser conceptualmente similares (fig. 1). El indicador «Neumonía intrahospitalaria», pese a haber obtenido el consenso del 75% de los panelistas, fue añadido por el grupo de trabajo. El conjunto final incluyó 29 indicadores, entre los cuales 5 configuraron un subgrupo que sólo se aplicará en los CRI (tablas 4 y 5).
Indicadores finales incluidos en el instrumento Audit vs. 2.0, específicos de los CRI
| Área de atención | Indicador de calidad de la atención del paciente con ictus | Descripción del indicador de calidad | Tercil inferior, % | Tercil medio, % | Tercil superior, % |
| Centros de referencia-trombólisis | rtPA 3 h | Porcentaje de ictus isquémicos tratados en las primeras 3 h tras el inicio de los síntomas | 1,79 | 3,57 | 94,64 |
| Puerta-aguja 60 min | Porcentaje de pacientes tratados con rtPA i.v. en menos de 60 min | 0 | 5,36 | 94,64 | |
| TC craneal < 25 min | Porcentaje de ictus isquémicos < 3 h de evolución con TC realizada en los primeros 25min tras llegada | 0 | 8,93 | 91,07 | |
| Tratado en una UI durante el ingreso | Porcentaje de ictus tratados en UI durante el ingreso (sólo en centros con UI) | 1,79 | 16,07 | 82,14 | |
| Complicaciones rtPA | Porcentaje de pacientes tratados con rtPA que desarrollan complicaciones hemorrágicas tras trombólisis | 0 | 19,64 | 80,36 |
CRI: centros de referencia ictus; i.v.: intravenoso; rtPA: recombinant tissue plasminogen activator; TC: tomografía computarizada; UI: unidad de ictus.
Indicadores finales incluidos en el instrumento Audit vs. 2.0, aplicables en todos los hospitales
| Área de atención | Indicador de calidad de la atención del paciente con ictus | Descripción del indicador de calidad | Tercil inferior, % | Tercil medio, % | Tercil superior, % |
| Intervenciones en la fase aguda | Glucosa basal | Porcentaje de ictus agudos con glucemia urgente | 1,79 | 5,36 | 92,86 |
| Neuroimagen < 24 h del ictus | Porcentaje de ictus con neuroimagen < 24 h del ictus | 1,79 | 7,14 | 91,07 | |
| Profilaxis TVP | Porcentaje de ictus con profilaxis TVP instaurada en las primeras 48 h | 1,79 | 7,14 | 91,07 | |
| Coagulación basal | Porcentaje de ictus agudos con coagulación urgente | 5,36 | 5,36 | 89,29 | |
| Test disfagia | Porcentaje de ictus isquémicos/HIC con test disfagia válido antes del inicio de dieta/medicación oral | 3,57 | 10,71 | 85,71 | |
| ECG basal | Porcentaje de ictus agudos con ECG urgente | 3,57 | 10,71 | 85,71 | |
| Hipoxia | Porcentaje de ictus con pulsioximetría/gasometría | 1,79 | 14,29 | 83,93 | |
| Antitrombóticos precoces | Porcentaje de ictus isquémicos con antitrombóticos < 48 h | 1,79 | 17,86 | 80,36 | |
| Tratamiento rehabilitador | Movilización precoz 48 h | Porcentaje de ictus agudos movilizados y fuera de la cama en las primeras 48 h (a excepción de coma, ictus progresivo, hipotensión ortostática, IAM, TVP hasta que ACO efectiva) | 0 | 5,36 | 94,64 |
| Evaluación tratamiento rehabilitador < 48 h | Porcentaje de pacientes con ictus con evaluación de las necesidades de tratamiento rehabilitador en las primeras 48 h | 0 | 8,93 | 91,07 | |
| Rehabilitación precoz (fisioterapia/terapia ocupacional) | Porcentaje de pacientes con paresia y situación funcional basal desfavorable (mRS ≥ 3 o IB ≤ 70) vistos o tratados por FS/TO en los primeros 2 días tras ingreso. AIT excluidos | 1,79 | 16,07 | 82,14 | |
| Intervenciones durante el ingreso | Evaluación neurológica | Porcentaje de de ictus agudos con una anamnesis/exploración neurológica en su HC | 3,57 | 3,57 | 92,86 |
| Imagen vascular en ictus isquémicos/AIT | Porcentaje de ictus isquémicos/AIT que tienen estudio vascular extracraneal durante el ingreso | 0 | 7,14 | 92,86 | |
| Educación ictus | Porcentaje de pacientes con ictus o cuidadores que reciben información dirigida durante el ingreso | 1,79 | 12,5 | 85,71 | |
| Perfil lipídico | Porcentaje de ictus isquémicos/AIT con perfil lipídico realizado durante el ingreso | 0 | 14,29 | 85,71 | |
| Intervenciones realizadas al alta | Anticoagulación en la FA | Porcentaje de ictus isquémicos/AIT y FA dados de alta con tratamiento anticoagulante | 0 | 1,79 | 98,21 |
| Antitrombóticos alta | Porcentaje de ictus isquémicos con antitrombóticos al alta | 0 | 3,57 | 96,43 | |
| Fisioterapia continuada al alta gestionada | Porcentaje de pacientes con ictus con fisioterapia continuada al alta gestionada | 0 | 3,57 | 96,43 | |
| Mecanismo ictus | Porcentaje de ictus que tienen mecanismo documentado al alta | 1,79 | 5,36 | 92,86 | |
| LDL 100 | Porcentaje de ictus isquémicos/AIT con LDL > 100 o en tratamiento hipolipemiante previo que tienen prescripción de hipolipemiantes al alta | 3,57 | 14,29 | 82,14 | |
| Medidas de resultado | Mortalidad intrahospitalaria | Porcentaje de ictus muertos durante ingreso | 1,79 | 7,14 | 91,07 |
| Situación neurológica alta | Puntuación NIH al alta | 0 | 8,93 | 91,07 | |
| Discapacidad alta | Porcentaje de pacientes con mRS > 2 al alta | 0 | 16,07 | 83,93 | |
| Neumonía intrahospitalaria | Porcentaje de ictus con neumonía (ajustado por edad, sexo y gravedad inicial ictus) | 1,79 | 23,21 | 75 |
ACO: anticoagulación oral; AIT: accidente isquémico transitorio; ECG: electrocardiograma; FA: fibrilación auricular; FS/TO: fisioterapeuta/terapeuta ocupacional; HC: historia clínica; HIC: hemorragia intracraneal; IAM: infarto agudo de miocardio; IB: índice de Barthel; LDL: lipoproteína de baja densidad; mRS: modified Rankin Scale; NIH: escala del National Institute of Health; TVP: trombosis venosa profunda.
En el presente estudio, la utilización de un método Delphi ha permitido evaluar y priorizar una selección de indicadores obtenidos mediante la revisión de la literatura y utilizados en experiencias previas. La iniciativa de definir un conjunto básico de indicadores de calidad de la atención hospitalaria del paciente con ictus responde, por un lado, a la necesidad de revisar y actualizar el modelo de audit ya existente en Cataluña y, por otro lado, a la voluntad de colaboración entre las tres comunidades autónomas, que compartirían metodología e indicadores en sus auditorías, enriqueciendo el análisis conjunto de resultados y favoreciendo así compartir estrategias y buenas prácticas en la atención al ictus. Para conseguirlo, se implicó en el proyecto al máximo número de expertos representativo de los profesionales que realizan la atención hospitalaria en estos territorios, cuya opinión fue consensuada mediante el uso de una técnica formal de consenso.
La definición, selección y priorización de indicadores de la calidad de la atención en los servicios sanitarios se han realizado, hasta el presente, mediante diferentes metodologías17, entre las que se incluye el método Delphi, del cual existen numerosas variaciones. En general, se considera suficiente e idónea la realización de tres vueltas para asegurar la estabilidad de las respuestas. Un número superior de vueltas no sólo no produciría grandes cambios, sino que podría disminuir la tasa de respuestas16. Un número inferior comprometería el consenso. A pesar de que en la primera vuelta se contempla la participación de los expertos en el desarrollo de las cuestiones que van a ser evaluadas y/o priorizadas17, entre las modificaciones del método27, se describe la selección previa de los ítems y la evaluación de un cuestionario cerrado predefinido21,25. En el presente estudio, se ha optado por esta modalidad de priorización de indicadores previamente definidos. Se ha utilizado pues un método Delphi modificado en dos vueltas en las cuales se obtuvo la respuesta del 100% de los panelistas.
Aunque la especialización y la experiencia son fundamentales en la elección del panel de expertos, en este proyecto el panel seleccionado es más representativo que experto, ya que el número de contactos hospitalarios por ictus en cada una de las comunidades autónomas ha sido el factor determinante en su composición. Además, se ha priorizado la inclusión de los diferentes perfiles profesionales implicados en la atención de los pacientes con ictus. No obstante, entre los panelistas se encuentra la mayoría de los expertos en patología cerebrovascular más reconocidos de cada comunidad. Se ha realizado una consulta amplia sobre la relevancia y factibilidad de los indicadores priorizados en la primera vuelta con el objetivo de involucrar también a un gran número de profesionales, además de ofrecer información suplementaria a los panelistas.
Los 46 indicadores evaluados en la segunda vuelta fueron considerados de importancia elevada (mediana de puntuaciones entre 7 y 9). En relación con el grado de consenso, alrededor del 85% (39/46) de los indicadores lo alcanzaron según la definición establecida (más del 75% de los panelistas puntúan 7, 8 o 9). En 33 (71,7%), el consenso fue incluso > 80%. Los dos indicadores mejor puntuados, y con mayor consenso, han sido «Anticoagulación en la FA» y «Antitrombóticos al alta». El indicador «rtPA 3 h» fue considerado el más importante, aunque obtuvo menor consenso que los anteriores. Estos resultados están en consonancia con los obtenidos en otras experiencias en las que también se había realizado una selección y priorización de indicadores21,22. Los indicadores priorizados en primero y segundo lugar en nuestra experiencia fueron también priorizados en las primeras dos posiciones en el estudio de Holloway et al21, siendo calificados como los más útiles. El conjunto final de 29 indicadores comprende los indicadores mejor puntuados de entre los que alcanzaron el consenso, son representativos de todas las áreas de atención hospitalaria, e incluyen un subgrupo de 5 indicadores que únicamente se aplicarán en los hospitales de referencia. Se desestimaron los indicadores que obtuvieron menor consenso y aquellos en los que no hubo consenso o fue indefinido.
El presente estudio tiene algunas limitaciones. Por un lado, a pesar de optar por el balance de especialidades, la selección de los panelistas fue desigual. Se consideró oportuna la inclusión de un número superior de neurólogos e internistas puesto que en ellos recae en mayor medida la toma de decisiones en la fase hospitalaria de la atención del paciente con ictus. Asimismo, dado que se trataba de seleccionar indicadores de calidad de la atención hospitalaria, no se incluyó a profesionales de otros ámbitos (atención primaria, larga estancia, etc.). Por otro lado, en la primera vuelta los expertos priorizaron indicadores procedentes de la revisión de la literatura y, por lo tanto, no participaron en su definición. Sin embargo, la decisión de partir de una selección de indicadores ya utilizados en la literatura posibilita la comparación de nuestros resultados y hace más consistente la definición de estos. Finalmente, considerar que la baja tasa de respuestas por parte de los profesionales encuestados en la CA (36%) podría no haber condicionado, como se pretendía, las puntuaciones del panel en la segunda vuelta. Sin embargo, es destacable la participación de un grupo amplio y representativo de expertos (56) que aportan la experiencia de diversas disciplinas y profesionales de la atención hospitalaria del paciente con ictus, así como la implicación de 3 comunidades autónomas, con lo que se consigue una mayor validez externa y, por lo tanto, que los resultados sean más generalizables.
En conclusión, mediante este proyecto se ha obtenido un conjunto mínimo básico de indicadores de calidad consensuados, actualizados y apoyados por la evidencia científica. Esta es la primera iniciativa de consenso en la priorización de indicadores de la atención hospitalaria del paciente con ictus que involucra a varias comunidades autónomas, abriendo la puerta a la participación de otras.
Conflictos de interesesSe declara que no hay conflictos de intereses de los autores en relación con el artículo que se remite para publicación. No existe relación financiera o ni con otras personas u organizaciones y que pudieran dar lugar a un conflicto de intereses.
Los autores agradecen la participación y sugerencias recibidas de los expertos del panel de consenso, así como la participación de los profesionales de la atención a los pacientes con ictus que respondieron la consulta sobre relevancia y factibilidad.
Este trabajo se ha realizado en el marco de colaboración previsto en el Plan de Calidad para el Sistema Nacional de Salud elaborado por el Ministerio de Sanidad y Política Social, al amparo del convenio de colaboración suscrito por el Instituto de Salud Carlos III, organismo autónomo del Ministerio de Ciencia e Innovación y la Agència d’Avaluació de Tecnologia i Recerca Mèdiques (AATRM) de Cataluña.