«Porque en cada adulto habita el niño que fue y en cada niño se encuentra el adulto que será»
El 11.° Día Mundial del Riñón se celebrará el 10 de marzo del 2016 en todo el mundo. Este evento anual, organizado conjuntamente por la Sociedad Internacional de Nefrología (ISN) y la Federación Internacional de Fundaciones del Riñón (IFKF), se ha convertido en un esfuerzo exitoso para informar a la población general y a los responsables de las políticas públicas de salud sobre la importancia y las consecuencias de la enfermedad renal. En esta ocasión el Día Mundial del Riñón será dedicado a la enfermedad renal en la infancia y a las enfermedades renales del adulto que pueden iniciarse a temprana edad.
Los niños que desarrollan daño renal agudo (DRA) secundario a una amplia variedad de causas, pueden tener secuelas a largo plazo que resulten en enfermedad renal crónica (ERC) muchos años después1–4. Además, la ERC en niños, en su mayoría de tipo congénita, así como las complicaciones renales secundarias a una gran variedad de enfermedades, no solo resultan en una importante morbimortalidad durante la infancia, sino también en complicaciones médicas más allá de la niñez. De hecho, las muertes infantiles asociadas a una larga lista de enfermedades infecciosas son vinculadas inextricablemente con compromiso de la función renal. Por ejemplo, niños que sucumben al cólera y otras infecciones diarreicas, comúnmente mueren a causa de DRA inducido por depleción de volumen y choque más que debido al proceso infeccioso. Además, un número importante de estudios indican que los adultos con hipertensión, proteinuria y ERC tenían antecedentes desde la infancia, tan tempranos como en la vida in-útero y perinatal (ver la tabla 1 para definiciones de la infancia). El Día Mundial del Riñón 2016 pretende concienciar a la población general de que muchas de las enfermedades renales del adulto se inician en la infancia. El entendimiento de los eventos y diagnósticos de alto riesgo que ocurren durante la infancia brindaría la oportunidad de identificar y realizar intervenciones preventivas en aquellas personas con alto riesgo de ERC durante su vida.
Definiciones de las etapas de la infancia
| Periodo perinatal | De las 22 semanas completas de gestación a 7 días de vida posnatal |
|---|---|
| Periodo neonatal | Del nacimiento al día 28 de vida posnatal |
| Infancia | Del nacimiento a 1 año de edad |
| Niñez | De 1 año a 10 años de edad |
| Adolescencia | De 10 años a 19 años de edad |
Los datos en esta tabla son definidos por la Organización Mundial de la Salud. El periodo perinatal es definido como 22 semanas de gestación completas hasta 7 días de vida; el periodo neonatal, hasta los 28 días de vida; la infancia hasta el año de vida; la niñez como 1 a 10 años de vida; y el adolescente desde los 10 a los 19 años de edad.
Estas definiciones varían en todo el mundo. Algunos definen como «persona joven» a aquellos con ≤24 años. En los Estados Unidos la niñez es considerada hasta los 21 años.
Actualmente los datos epidemiológicos a nivel mundial sobre el espectro del DRA y la ERC en niños son limitados, aunque cada vez se amplían más. La prevalencia de ERC en niños es rara, y varía desde 15 a 74,7 casos por millón3. Tales variaciones son debidas a la influencia de los factores culturales y regionales tanto como a la metodología usada para estimarla. La Organización Mundial de la Salud (OMS), recientemente agregó información sobre la mortalidad a nivel mundial de las enfermedades urológicas y renales, y se convertirá en una fuente importante de información; sin embargo, la OMS no reporta la información por grupos de edad5. Las bases de datos como las de los Estudios Colaborativos y Ensayos Renales Pediátricos de Norte América6, el Sistema de Datos Renales de Estados Unidos7 y el Registro EDTA8 incluyen datos de pacientes pediátricos con ERCT y algunos con ERC. Proyectos tales como los estudios ItalKid9 y Enfermedad Renal Crónica en Niños10, el Estudio Global de la Carga de Enfermedad 2013, así como los registros que ahora existen en muchos países proporcionan información importante, pero se requiere aún más11.
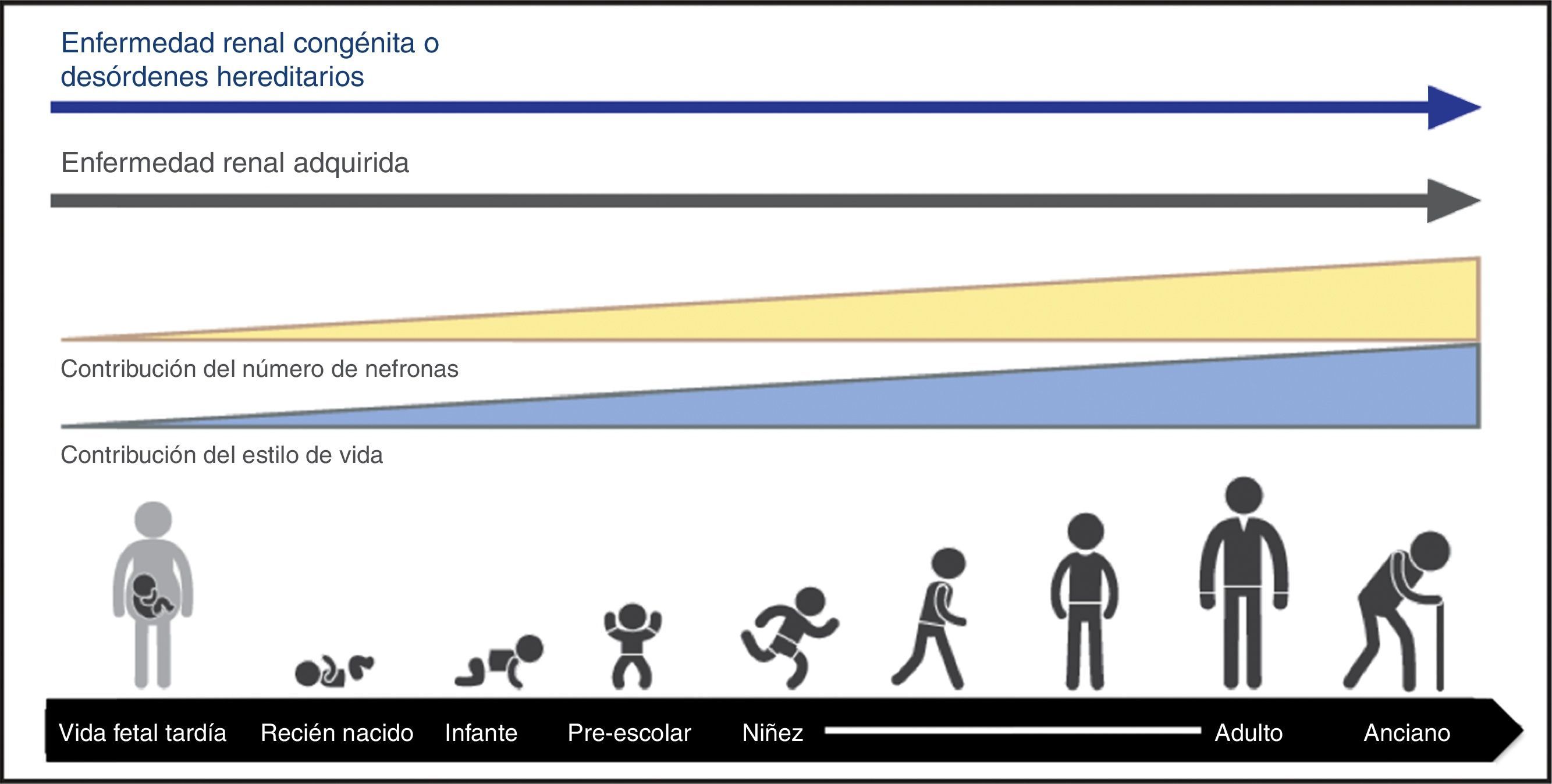
De acuerdo a algunos estudios seleccionados en población adulta, el DRA puede resultar en ERC12. La incidencia de DRA en niños admitidos en unidades de cuidados intensivos varía ampliamente, de 8% a 89%1, y los resultados dependen de los recursos disponibles. Se esperan también los resultados de proyectos como el AWARE, un estudio de niños con DRA en 5 países13. Estudios unicéntricos y de metaanálisis indican que tanto el DRA como la ERC en niños representan una minoría de pacientes con ERC en todo el mundo2,3. Sin embargo, es cada vez más evidente que la enfermedad renal del adulto es un legado de la infancia (fig. 1).
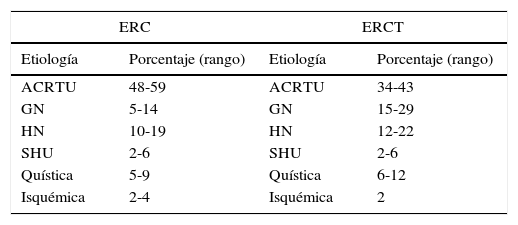
Espectro de las enfermedades renales pediátricasLas condiciones congénitas y hereditarias que predominan como causa de la ERC en la infancia difieren sustancialmente de aquellas observadas en los adultos. Hasta la fecha se han encontrado mutaciones en más de 150 genes que alteran el desarrollo renal o alguna función específica glomerular o tubular14. Muchos de estos desórdenes genéticos se presentan durante la infancia y pueden llevar progresivamente a ERC. Las anomalías congénitas del riñón o tracto urinario representan la mayor causa de ERC en la niñez (tabla 2), e incluyen hipoplasia/displasia renal y uropatía obstructiva. Un subgrupo importante de las displasias renales son las enfermedades quísticas, las cuales se originan en defectos genéticos en los cilios de las células túbulo epiteliales.
Etiología de la enfermedad renal crónica en niños
| ERC | ERCT | ||
|---|---|---|---|
| Etiología | Porcentaje (rango) | Etiología | Porcentaje (rango) |
| ACRTU | 48-59 | ACRTU | 34-43 |
| GN | 5-14 | GN | 15-29 |
| HN | 10-19 | HN | 12-22 |
| SHU | 2-6 | SHU | 2-6 |
| Quística | 5-9 | Quística | 6-12 |
| Isquémica | 2-4 | Isquémica | 2 |
Causas raras incluyen síndrome nefrótico congénito, enfermedades metabólicas, cistinosis.
Causas misceláneas dependen de cómo sean clasificadas.
ACRTU: anomalías congenitas del riñón y tracto urinario; GN: glomerulonefritis; HN: hipertensión; SHU: síndrome hemolítico urémico.
Fuente: Harambat et al.2. Datos de ERC obtenidos del NAPRTCS, Registro Italiano y Registro Belga. Datos de ERCT obtenidos de ANZDATA, ESPN/ERA-EDTA, Registro Renal del Reino Unido y el Registro Japonés.
Muchas glomerulopatías pediátricas son causadas por defectos genéticos o adquiridos en los podocitos, el tipo de célula especial que recubre los capilares glomerulares. Causas importantes, pero menos comunes, son los desórdenes metabólicos hereditarios, tales como la hiperoxaluria y la cistinosis, el síndrome hemolítico urémico atípico (una microangiopatía trombótica relacionada con alteraciones genéticas del complemento), alteraciones en la coagulación o en las vías metabólicas.
En varias clasificaciones no queda claro cómo categorizar a los niños que presentaron DRA con recuperación aparente, y si se incluyen, y cómo a aquellos niños que presentaron problemas perinatales que derivaron en un número de nefronas relativamente bajo. Entre los niños con ERC terminal (ERCT) de inicio en la infancia, las glomerulopatías son ligeramente más frecuentes y las alteraciones congénitas menos comunes (tabla 2), debido a que la pérdida de nefronas es típicamente mayor en enfermedades glomerulares. Sin embargo, la evidencia reciente sugiere que muchos pacientes con formas leves de anomalías congénitas del riñón o tracto urinario pueden progresar a ERCT durante la edad adulta, con un incremento en la cuarta década de la vida15.
Existen diferencias nacionales y regionales entre los tipos y el curso del DRA y la ERC durante y después de la infancia. La muerte por enfermedad renal es mayor en países en desarrollo, y las disparidades nacionales y regionales en los servicios de salud y sus resultados, deberán ser evaluados. Además, el acceso a la atención médica es variable, dependiendo de la región, el país y su infraestructura. Al centrarse en la enfermedad renal durante la infancia, se pueden alcanzar soluciones costo-efectivas, tales como el tratamiento preventivo o temprano de la enfermedad, que evite el desarrollo posterior de ERC avanzada. Las expectativas dependerán de la disponibilidad en la atención y en el tratamiento. Tratar a los niños que tienen DRA y ERC que requieren terapia de reemplazo renal puede ser eficaz para mitigar la carga de la enfermedad renal en los adultos. El lograrlo requiere que los recursos se enfoquen en lograr vías más rápidas y costo-efectivas para proporcionar tratamiento de reemplazo renal (TRR) en la infancia.
Enfermedad renal congénita, los orígenes del desarrollo en la salud y la enfermedad, reserva renal y sus implicacionesEn regiones donde los ultrasonidos fetales antenatales son rutinarios, muchos niños con malformaciones urológicas son identificados antes del parto, lo cual permite intervenciones tempranas. Sin embargo, en la mayor parte del mundo los niños con malformaciones estructurales no son identificados hasta mucho más tarde, cuando presentan síntomas. Mientras el tamizaje generalizado para proteinuria, hematuria e infecciones del tracto urinario se ha realizado en algunos países y regiones, existe una falta de consenso sobre su eficacia. Sin embargo, existe un acuerdo general de que los niños con estudios prenatales que indican posibles alteraciones genitourinarias, niños con una historia familiar de enfermedad renal y/o niños con signos tales como retraso en el crecimiento, historia de infección del tacto urinario recurrente, disfunción vesical o alguna alteración urinaria, deberán ser estudiados. El tamizaje inicial deberá incluir un examen físico dirigido, tira reactiva de orina, urianálisis completo y una química sanguínea básica, así como otros estudios más específicos según esté indicado.
Dependiendo del diagnóstico, el tratamiento definitivo estará indicado. La evidencia de que alguna terapia puede enlentecer la progresión de la ERC durante la infancia permanece siendo limitada. Los inhibidores de la enzima convertidora de angiotensina, los bloqueadores de los receptores de angiotensina, antioxidantes y posiblemente cambios en la dieta, pudieran estar indicados dependiendo del diagnóstico. Sin embargo, los cambios en la dieta necesitan permitir un adecuado crecimiento y desarrollo. El estudio ESCAPE proporcionó evidencia de que un control estricto de la presión arterial retarda la progresión de la ERC en el niño, independiente de la enfermedad renal de base16.
Algunos niños pueden requerir terapia de reemplazo renal en la primera infancia. Datos recientes extrapolados de registros en todo el mundo indican una buena sobrevida, aun cuando la diálisis sea requerida desde la edad neonatal2,17. El trasplante renal, la terapia de reemplazo renal de elección en los niños, es generalmente aceptable después de los 12 meses de edad, con una excelente sobrevida del paciente y del injerto, así como del crecimiento y desarrollo del niño.
Existe evidencia de que la ERC de inicio en la infancia lleva a una morbilidad cardiovascular acelerada y a una menor esperanza de vida. Se espera que los resultados de grandes estudios prospectivos, tales como el de Comorbilidad Cardiovascular en Niños con ERC(4C), informen sobre las causas y consecuencias de la enfermedad cardiovascular temprana en los niños con ERC18.
Además de los niños con enfermedad renal congénita, ahora se sabe que eventos perinatales pueden afectar la salud futura, aun en ausencia de enfermedad renal evidente durante los primeros años de vida19. En función de los estudios de cohorte observacionales y de reporte de casos, los bebés prematuros parecen tener mayor riesgo de presentar enfermedad renal mucho tiempo después del nacimiento.
Se está incrementando la sobrevida de los bebés prematuros, incluyendo bebés nacidos mucho antes de que la nefrogénesis se haya completado20. Los datos disponibles, aunque limitados, indican que durante la estancia en las terapias neonatales, los bebés reciben muchos nefrotóxicos, y aquellos que mueren previo a su egreso tienen glomérulos de mayor tamaño pero en menor cantidad21. Además, los niños que sobreviven tienen evidencia de algún grado de alteración renal que puede ser muy leve22. Aún más preocupante es la gran cantidad de evidencias que indican que aquellas personas nacidas a término, pero con peso bajo al nacer, pueden tener un riesgo alto de desarrollar hipertensión, albuminuria y ERC durante su vida23. Cuando se emplean medidas directas estas personas en la edad adulta pueden tener menor número de nefronas, y por lo tanto, una menor reserva cardiorrenal.
Al enfocar a los niños en el Día Mundial del Riñón queremos hacer hincapié en que es fundamental el seguimiento de la función renal y presión arterial a lo largo de la vida de aquellas personas nacidas prematuramente o pequeñas para su edad gestacional. Al hacerlo y evitar el uso de medicamentos nefrotóxicos durante su vida, es posible que se pueda evitar la ERC en muchas personas.
Recursos y tratamientos para niños. Diferencias con el tratamiento en el adultoExiste disparidad en la disponibilidad de recursos para el tratamiento del DRA en niños y personas jóvenes; en consecuencia muchos niños y jóvenes de países en desarrollo mueren al desarrollar DRA. Para resolver este problema la ISN ha iniciado el Proyecto Salvando Vidas Jóvenes, el cual trata de prevenir el DRA con el tratamiento oportuno de las infecciones y/o la administración oportuna de líquidos y electrolitos, así como tratar el DRA cuando este ocurra. En este proyecto que se lleva a cabo en el África subsahariana y el sudoeste de Asia participan por igual 4 fundaciones del riñón (IPNA, ISN, ISPD y SKCF)2, enfocándose en establecer y mantener centros para la atención del DRA, incluyendo el brindar tratamiento de diálisis peritoneal aguda. Este va de la mano con el proyecto del ISN «0 para 25», el cual hace la llamada a sus miembros para asegurar que en el 2025 nadie muera de DRA prevenible.
En vista del predominio de enfermedades congénitas y hereditarias, los recursos terapéuticos para niños con ERC han sido históricamente limitados a algunas condiciones inmunológicas. Muy recientemente el progreso en el desarrollo de nuevos fármacos, así como los avances en el conocimiento genético y la capacidad diagnóstica, han comenzado a superar la larga etapa del «nihilismo terapéutico» de la enfermedad renal pediátrica. El SHU atípico, considerado durante mucho tiempo ominoso, con alto riesgo de progresión a ERCT y recurrencia en el postrasplante, ha comenzado a ser una condición tratable con el advenimiento de un anticuerpo monoclonal que bloquea específicamente la activación de C524. Otro ejemplo es el uso de antagonistas del receptor de vasopresina para retardar el crecimiento quístico y preservar la función renal en la enfermedad renal poliquística25. Una vez demostrada su eficacia en adultos con enfermedad renal poliquística autosómica dominante, la terapia con vaptanos parece ser prometedora también para la forma recesiva de la enfermedad, la cual se presenta y comúnmente progresa a ERCT durante la infancia.
Sin embargo, el beneficio del paciente ante estos avances en la investigación farmacológica se pone en riesgo a nivel mundial, debido al costo elevado de algunos de los nuevos agentes terapéuticos. La búsqueda de terapias innovadoras asequibles para enfermedades raras será un objetivo clave para la nefrología pediátrica durante los próximos años.
La identificación de niños que se beneficien con abordajes terapéuticos novedosos puede ser facilitada por el desarrollo de registros clínicos que informen sobre el curso natural de la enfermedad, incluyendo correlaciones entre el genotipo y el fenotipo. Además de las bases de datos específicas de la enfermedad, también es necesario registros de tratamiento específico. Estos son particularmente relevantes en áreas donde los estudios clínicos son difíciles de realizar debido al pequeño número de pacientes y al desinterés de la industria, así como para las terapias que necesitan desarrollo o mejora global. Por ejemplo, actualmente existe una gran corriente internacional enfocada en la difusión y realización de diálisis y trasplante pediátricos. Mientras que las tasas de sobrevida del paciente pediátrico y la técnica son excelentes, incluso superiores a las de los adultos en muchos países industrializados, se estima que en cerca de la mitad de todos los niños del mundo no se ofrece terapia alguna de reemplazo renal. Facilitar el acceso a las TRR para todos los niños será un gran desafío para el futuro. Para obtener información fiable sobre datos demográficos y resultados de TRR pediátrica, la Asociación Internacional de Nefrología Pediátrica está a punto de lanzar un registro global basado en población. Si tiene éxito este registro podría ser un modelo para la recolección de datos a nivel mundial.
Transición de la atención pediátrica a la del adultoLa transición de la atención del adolescente con enfermedad renal hacia el grupo de los adultos es crítica para los pacientes y sus cuidadores. La falta de adherencia es una característica frecuente de la transición entre los cuidados pediátricos y los del adulto26–28. Por tanto, la combinación de procesos sistemáticamente definidos y soportados por vías de validación y guías creíbles deberán ser establecidos para asegurar resultados exitosos.
En el proceso de cambios de la atención pediátrica a la del adulto la «transición» deberá ocurrir gradualmente, y debe ser distinguida de la «transferencia», la cual es comúnmente un cambio abrupto y mecánico del médico tratante. La introducción del concepto de transición deberá ser preventivo, iniciarse meses a años previos al cambio, conforme el niño se vuelve adolescente y adulto. El objetivo final es fomentar una relación estrecha y una estructura personalizada que permita al paciente sentirse lo suficientemente cómodo como para informar la pérdida de adherencia y otros errores en el tratamiento.
Un plan de transición deberá reconocer que la madurez emocional del niño con enfermedad renal puede variar ampliamente. Evaluar al cuidador, su sobrecarga y la estructura familiar, así como los factores culturales, sociales y financieros en el momento de la transición es fundamental4. El tiempo apropiado y la forma de la transición puede variar ampliamente de acuerdo con el paciente y situaciones diferentes; por lo tanto, es preferible un proceso flexible, sin periodos de tiempo determinados, e incluso sin un formato definido.
Es importante destacar que la transición puede ser lenta, pausada o incluso retroceder temporalmente durante periodos de crisis, tales como exacerbaciones o progresión de la enfermedad, o si se presenta inestabilidad familiar o social. Recientemente la ISN y la Asociación Internacional de Nefrología Pediátrica publicaron un consenso donde proponen pasos consistentes con los puntos antes mencionados, con el objetivo de mejorar en la práctica clínica la transición en la atención de la enfermedad renal29,30.
Convocatoria para Generar información y acciones adicionalesTomando en cuenta la vulnerabilidad de los niños con enfermedad renal, incluyendo el impacto en el crecimiento y el desarrollo, así como su vida futura como adulto, y dada la mayor proporción de niños que enfrentan limitaciones en los países en desarrollo, es imprescindible educar a todos los involucrados con el fin de reordenar vías de comunicación y acciones a tomar31,32. Estos esfuerzos deberán fomentar colaboraciones regionales e internacionales y el intercambio de ideas entre fundaciones del riñón locales, sociedades de profesionales, otras organizaciones sin fines de lucro, estados y gobiernos, con el fin de involucrar a todas las partes para mejorar la salud, el bienestar y la calidad de vida de los niños con enfermedades renales y asegurar su longevidad durante la edad adulta.
Hasta hace poco el consenso de la OMS sobre enfermedades no transmisibles (ENT) incluía las enfermedades cardiovasculares, el cáncer, la diabetes y las enfermedades respiratorias, pero no la enfermedad renal33,34. Afortunadamente, y en parte debido a la campaña mundial realizada por la ISN, la declaración política de la Asamblea General de las Naciones Unidas incluyó en el 2011 la enfermedad renal en el apartado 1935.
El incrementar la educación y la concienciación acerca de las enfermedades renales en general, y la enfermedad renal en la infancia en particular, es consistente con los objetivos de la OMS para reducir la mortalidad de las ENT, con 10 años de iniciativas dirigidas a la población, enfocadas en cambios en el estilo de vida (incluyendo reducción en el consumo de tabaco, control en la ingesta de sal, control del aporte energético de la dieta y reducción en el consumo de alcohol) e intervenciones eficaces (incluyendo control glucémico, en la presión arterial y colesterol). Es necesario intensificar esfuerzos para realinear y expandir estas colaboraciones multidisciplinarias con un enfoque más efectivo en la detección temprana y manejo oportuno de la enfermedad renal en los niños. Mientras los datos relacionados con las enfermedades renales pueden ser opacados por otras ENT con un aparente mayor impacto en la salud pública, como es el caso de la diabetes, el cáncer y las enfermedades cardiovasculares, nuestros esfuerzos también deben dirigirse a incrementar la educación y concienciación sobre las interrelaciones que estos padecimientos puedan tener, como son las conexiones cardiorrenales, la naturaleza global de la ERC y ERCT como ENT, así como el papel de la enfermedad renal como agente multiplicador y factor de confusión para otras ENT. Los informes blanco, incluyendo artículos de consenso y proyectos de revisión por expertos de clase mundial, pueden servir para lograr estas metas36.
Conflicto de interesesEste trabajo cumple con los requisitos sobre consentimiento/asentimiento informado, comité de ética, financiación, estudios animales y sobre la ausencia de conflicto de intereses según corresponda.
Agradecemos la traducción al español del artículo original en inglés a la Dra. Luz María Alcantar Vallín.
Nota del editor: esta Nota editorial ha sido solicitada en el marco de la campaña Día Mundial del Riñón. Esta publicación ha sido enviada simultáneamente a una serie de revistas científicas. Se trata, por lo tanto, de una publicación duplicada, que Revista Chilena de Pediatría presenta como Nota editorial, dada la importancia que reviste para la salud pública en pediatría.
Miembros del Comité Directivo del Día Mundial del Riñón: Philip Kam Tao Li, Guillermo Garcia-Garcia, William G. Couser, Timur Erk, Julie R Ingelfinger, Kamyar Kalantar-Zadeh, Charles Kernahan, Charlotte Osafo, Miguel C. Riella, Luca Segantini, Elena Zakharova.
Los 4 grupos son (en orden alfabético): IPNA (Asociación Internacional de Nefrología Pediátrica), (ISN) Sociedad Internacional, (ISPD) Sociedad Internacional de Diálisis Peritoneal, (SKCF) Fundación Sustentable del Cuidado Renal.