Objetivos: Determinar la variabilidad entre el peso estimado (PE) y el peso real (PR) de los pacientes a los que se administra alteplasa como tratamiento del ictus isquémico agudo (IIA), según las fuentes de las que se obtiene (paciente, familia y personal sanitario), y su repercusión sobre la dosis de alteplasa administrada.
Métodos: Estudio prospectivo de pacientes con IIA tratados con alteplasa en nuestro hospital de mayo de 2010 a mayo de 2011. La dosis de alteplasa se calculó en función del PE. Se determinó el PR pesando a los pacientes en las 24 horas siguientes a la infusión de la medicación.
Resultados: Se incluyó a 72 pacientes. Globalmente, se sobreestimó el peso una media de 2,49 kg. El personal sanitario sobrevaloró el peso (estimación > 10% del PR) en el 45% de casos; los familiares en el 14%, mientras que ningún paciente sobreestimó su peso (p = 0,005). El paciente se aproximó más a su PR; sin embargo, fue la fuente menos empleada. La dosis real administrada (DRA) media de alteplasa fue de 0,932 mg/kg.
Conclusiones: El cálculo de dosis de alteplasa a partir del PE del paciente conlleva una variabilidad de la DRA, que podría afectar a la eficacia y la seguridad del tratamiento. Debemos considerar siempre que sea posible la información proporcionada por el paciente sobre su peso. Es necesario buscar una fórmula que permita obtener el PR del paciente, evitando recurrir a la estimación visual del peso.
Objectives: Our aim is to evaluate the variability between estimated patient weight (EPW) and actual patient weight (APW), depending on the source of weight estimation (patient, family or hospital staff) and the impact on the "true dose" (TD) of iv alteplase administered.
Methods: Prospective study of patients with acute ischemic stroke treated consecutively with iv tPA in our institution from May 2010 to May 2011. Alteplase dosing was calculated according to EPW. APW was determined in the 24 hours following iv alteplase treatment.
Results: A total of 72 patients were included. Globally, patient's weight was overestimated: mean=2.49 Kg. Hospital staff overestimated the patient's weight (estimation>10% of APW) in 45% of cases; the family overestimated in 14% of cases, while no patients overestimated their own weight (p=.005). The patients were the most accurate source to establish their actual weight, but also the least used source. The average TD of alteplase was 0.932 mg/Kg.
Conclusions: Dose calculation of alteplase according to EPW leads to variation of the TD, which may affect the safety and effectiveness of the treatment. Whenever possible, the patients' estimation of their own weight should be taken into consideration. A method to obtain the APW is needed, avoiding the use of visual weight estimation.
"Investigar significa pagar la entrada por adelantado y entrar sin saber lo que se va a ver".
Robert Oppenheimer (1904-1967)
Introducción
El ictus es un trastorno de la circulación cerebral que aparece de forma súbita y provoca una detención del aporte sanguíneo al cerebro, con lo que se produce un daño cerebral focal. Los síntomas son variables según el área cerebral afectada. Distinguimos dos tipos de ictus: isquémico y hemorrágico.
La administración intravenosa de alteplasa (rtp-a) o trombólisis intravenosa (TIV) permite restablecer el flujo sanguíneo cerebral, y ha demostrado ser un tratamiento eficaz en el ictus isquémico agudo. Con la TIV se mejora la supervivencia y se disminuye el grado de incapacidad del paciente. El tiempo es un factor importante en la eficacia de la TIV: cuanto más precozmente se reanude el flujo en la zona isquémica, menor será el área de necrosis. En estudios previos, se ha determinado la eficacia y la seguridad de la TIV si se realiza en las 4,5 horas tras el inicio del ictus, y se considera que la dosis óptima de alteplasa es de 0,9 mg/kg de peso hasta una dosis máxima de 90 mg (en pacientes con peso superior a 100 kg)1,2.
En la práctica habitual, la dosis de alteplasa se calcula en función de la estimación del peso del paciente. Como consecuencia de este hecho, la eficacia y la seguridad de la TIV pueden verse afectadas tanto en el caso de infravalorar el peso, ya que no alcanzamos la dosis terapéutica, y por tanto el tratamiento podría ser ineficaz, como en el caso de sobrevalorarlo, en cuyo caso aumenta el riesgo de presentar efectos secundarios, de los cuales el más importante es la transformación hemorrágica.
El objetivo del presente trabajo es describir la variabilidad en la determinación del peso del paciente y la dosis real administrada (DRA) de alteplasa a pacientes con ictus isquémico agudo, en función de la fuente que realiza la estimación del peso (el propio paciente, la familia o el personal sanitario) y la DRA de rtp-a.
Material y métodos
Se realizó un estudio prospectivo de los pacientes tratados con TIV en la Unidad de Ictus del Hospital General Universitario Gregorio Marañón durante un año (de mayo de 2010 a mayo de 2011). La dosis de alteplasa se calculó en función del peso estimado (PE) del paciente. La estimación se obtuvo de tres fuentes: a) el propio paciente; b) la familia del paciente, o c) el personal sanitario. Se determinó el peso real (PR) de los pacientes pesándolos en las 24 horas siguientes a la infusión de la medicación. Para ello, se utilizó una silla-peso calibrada (báscula digital seca, modelo 958). Se calculó la DRA de alteplasa al dividir la dosis de alteplasa administrada por el PR del paciente.
Se analizaron las diferencias y las correlaciones entre PE y PR, y se comparó la DRA en función de la persona que estimó el peso del paciente.
Se calcularon las frecuencias de las variables cualitativas. Para las variables cuantitativas, se calcularon medias con sus desviaciones estándar y medianas. Para la comparación de variables cuantitativas, se emplearon las pruebas de Kruskal-Wallis y de Mann-Whitney. Para la comparación de proporciones se diseñaron tablas de contingencia y se utilizó la prueba de la x2. La correlación entre PE y PR se determinó mediante el coeficiente de correlación lineal de Pearson y la prueba r2 lineal con intervalos de confianza del 95%. Se consideró que las diferencias detectadas alcanzaban la significación estadística cuando los valores de p fueron menores de 0,05. El análisis estadístico de los datos obtenidos se realizó mediante el programa SPSS (Statistical Package for Social Science) versión 15.0.
Resultados
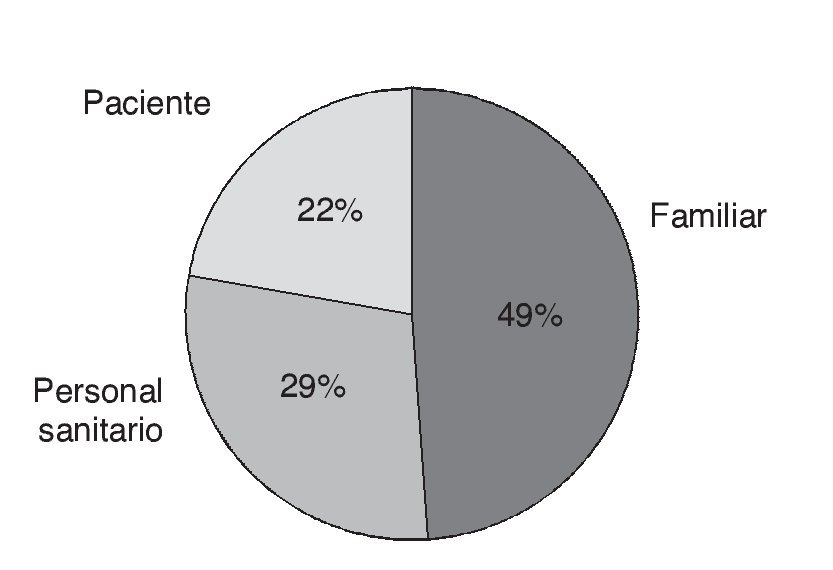
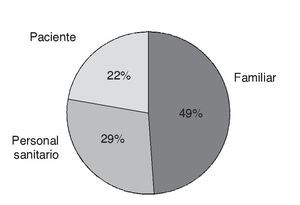
Durante el período estudiado se trató a 72 pacientes con TIV. El peso de 35 pacientes (49%) fue estimado por un familiar; en 21 casos (29%) el peso del paciente fue estimado por el personal sanitario, y sólo 16 pacientes (22%) informaron sobre su propio peso (fig. 1).
Figura 1 Porcentaje de la fuente de la que obtuvo el peso.
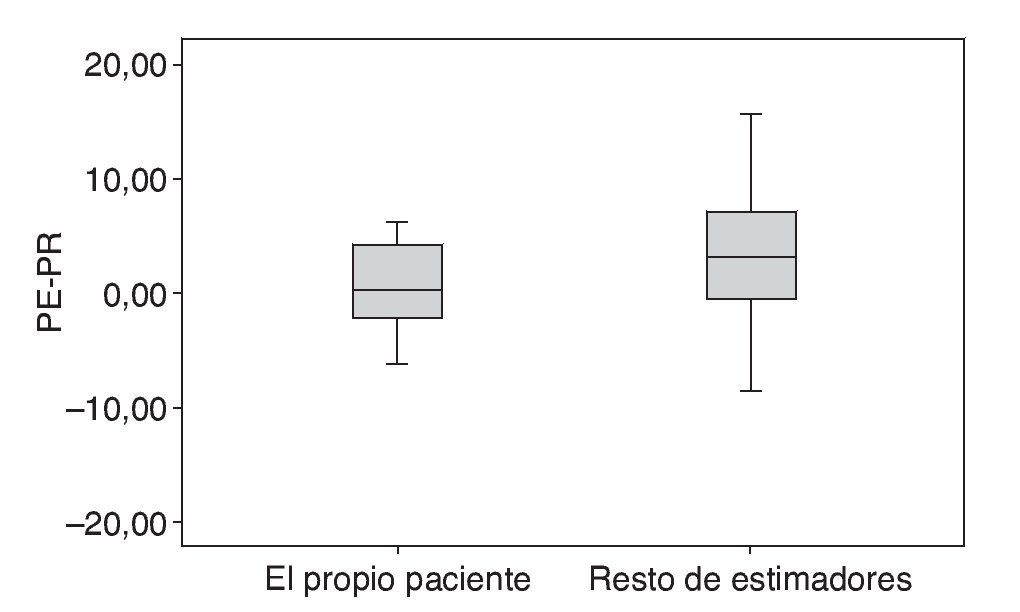
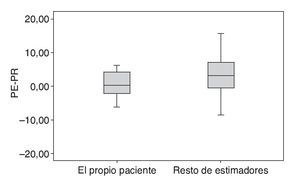
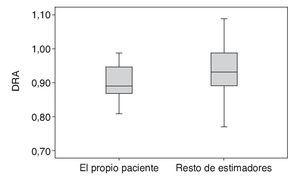
Globalmente, el peso fue sobreestimado una media ± desviación estándar (DE) de 2,49 ± 5,33 kg, oscilando desde los -12,9 a los +18,8 kg respecto al PR. La mayor diferencia entre PE y PR se observó cuando fue estimado por el personal sanitario (sobreestimación media de +3,6 kg, con una DE de 7,7 kg; rango: -12,9 a 18,8 kg). Cuando el PE fue calculado por los familiares, éste fue sobrevalorado una media de +2,25 kg (DE de 3,83 kg; rango: -6 a 8 kg). Quien más se aproximó a su PR fue el propio paciente, con una variabilidad media de +0,71 kg (DE de 3,43 kg; rango: -3 a 4,5 kg). La diferencias entre PE y PR según los tres grupos de estimadores (paciente, familiar o personal sanitario) no alcanzaron la significación estadística (p = 0,2). La diferencia entre PE y PR fue menor cuando la estimación la realizó el propio paciente frente al resto de estimadores (familiares y personal sanitario): sobreestimación de +0,47 frente a +3,12 kg (p = 0,06) (fig. 2).
Figura 2 Sobreestimación del peso según la fuente. PE: peso estimado; PR: peso real.
Se detectó una sobreestimación inferior al 10% del PR en el 22% de los pacientes estudiados. Cuando el estimador fue el personal sanitario, la sobreestimación alcanzó el 45% de los casos, mientras que cuando el peso lo estimaron los familiares, se sobreestimó sólo en el 14% de los casos. Ningún paciente sobreestimó su propio peso (p = 0,005) (fig. 3).
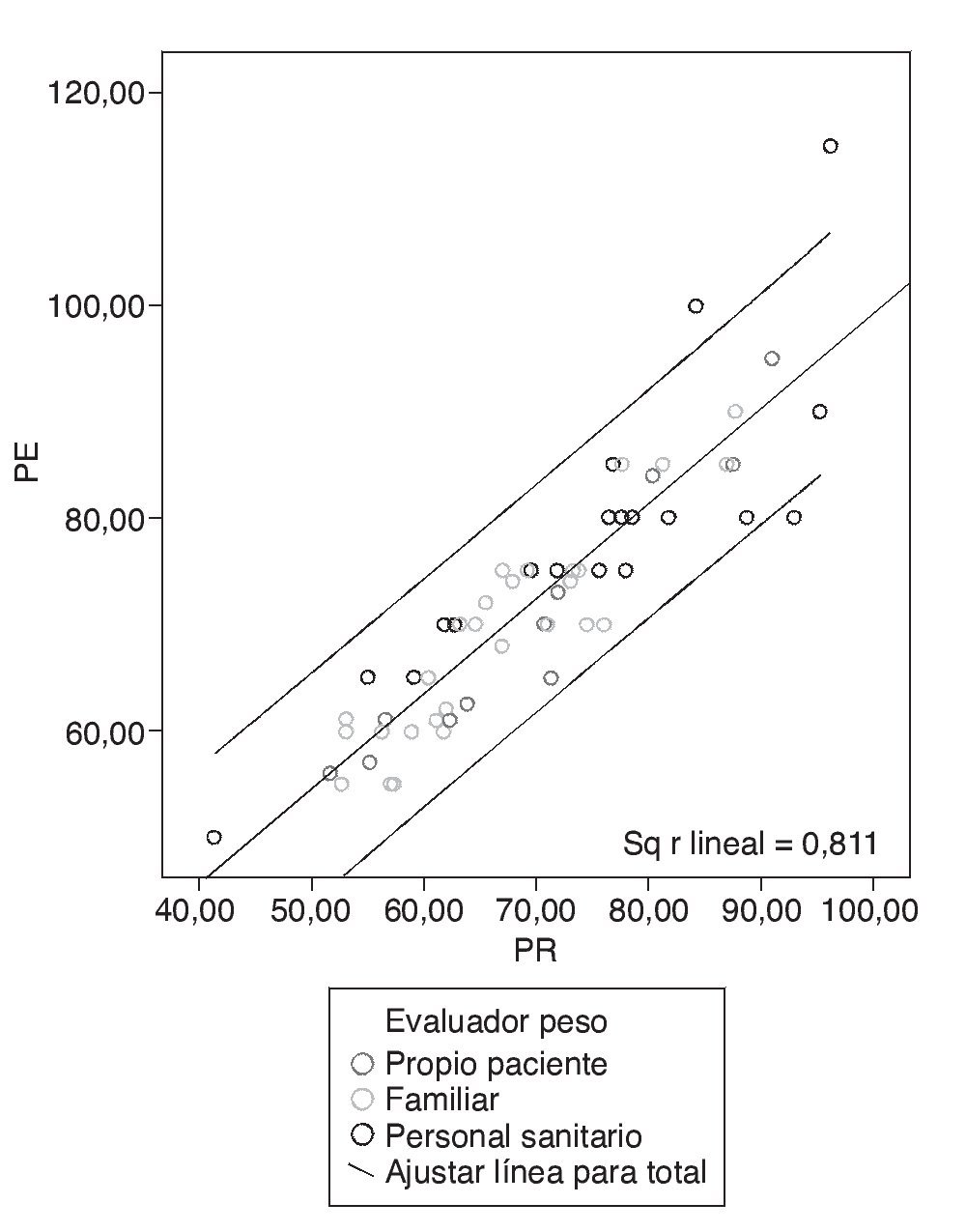
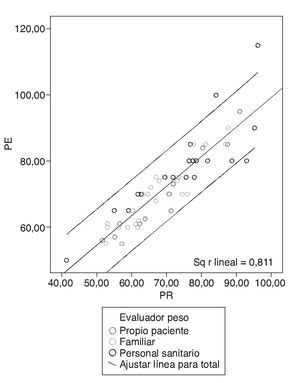
Figura 3 Correlación entre el peso real (PR) y el peso estimado (PE) en función de la fuente que lo estime.
La correlación entre PE y PR fue elevada, con un coeficiente de correlación de Pearson de 0,900 (prueba r2 lineal = 0,811). El valor del coeficiente de correlación de Pearson entre el PR y el PE por el propio paciente fue de 0,947 (prueba r2 lineal = 0,897), por el personal sanitario fue de 0,847 (prueba r2 lineal = 0,717), y entre el PR y PE por la familia fue de 0,924 (prueba r2 lineal = 0,872) (fig. 3).
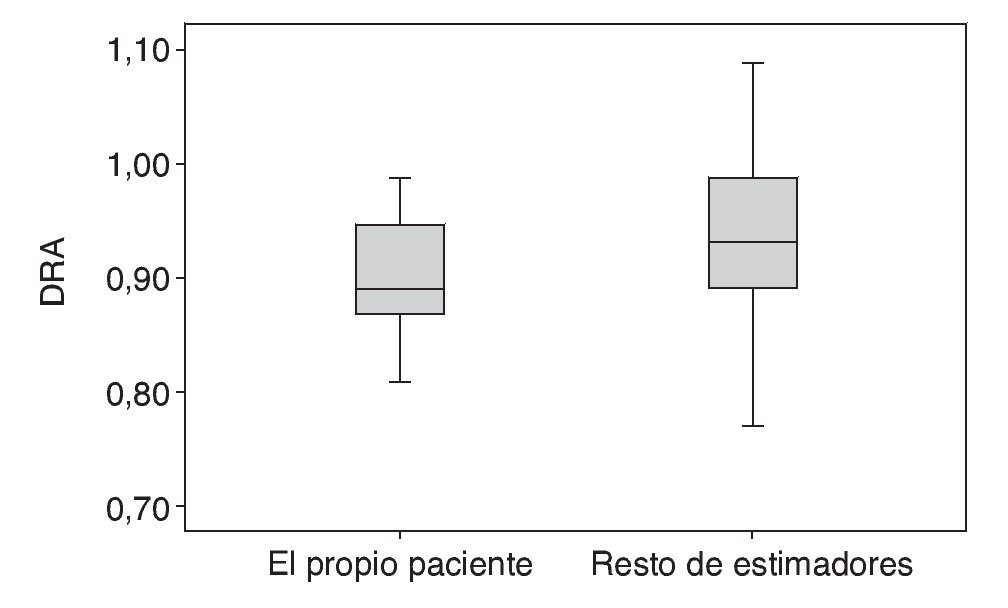
Como consecuencia de la sobreestimación del peso del paciente, la DRA superó la dosis recomendada de 0,9 mg/kg (media 0,932 mg/kg; DE de 0,07 kg; rango: 0,77-1,09 mg/ kg). La DRA media de los pacientes cuyo peso fue estimado por el personal sanitario fue de 0,943 (DE de 0,09 kg; rango 0,77-1,09 mg/kg); cuando el PE lo determinó la familia del paciente, la DRA media fue de 0,934 (DE de 0,05 kg; rango de 0,83-1,04 mg/kg) y cuando el propio paciente calculó su peso la DRA media fue 0,904 (DE de 0,05 kg; rango 0,81-0,97 mg/kg). Tampoco se observaron diferencias significativas (p = 0,3) al comparar los valores de las DRA obtenidos por cada uno de los 3 estimadores. Al comparar la DRA obtenida a partir de la información del propio paciente frente a las DRA obtenidas a partir del PE por la familia o el personal sanitario, se observaron diferencias significativas (0,899 frente a 0,942 mg/kg; p = 0,048) (fig. 4).
Figura 4 Dosis real administrada (DRA) según el paciente frente al resto de estimadores.
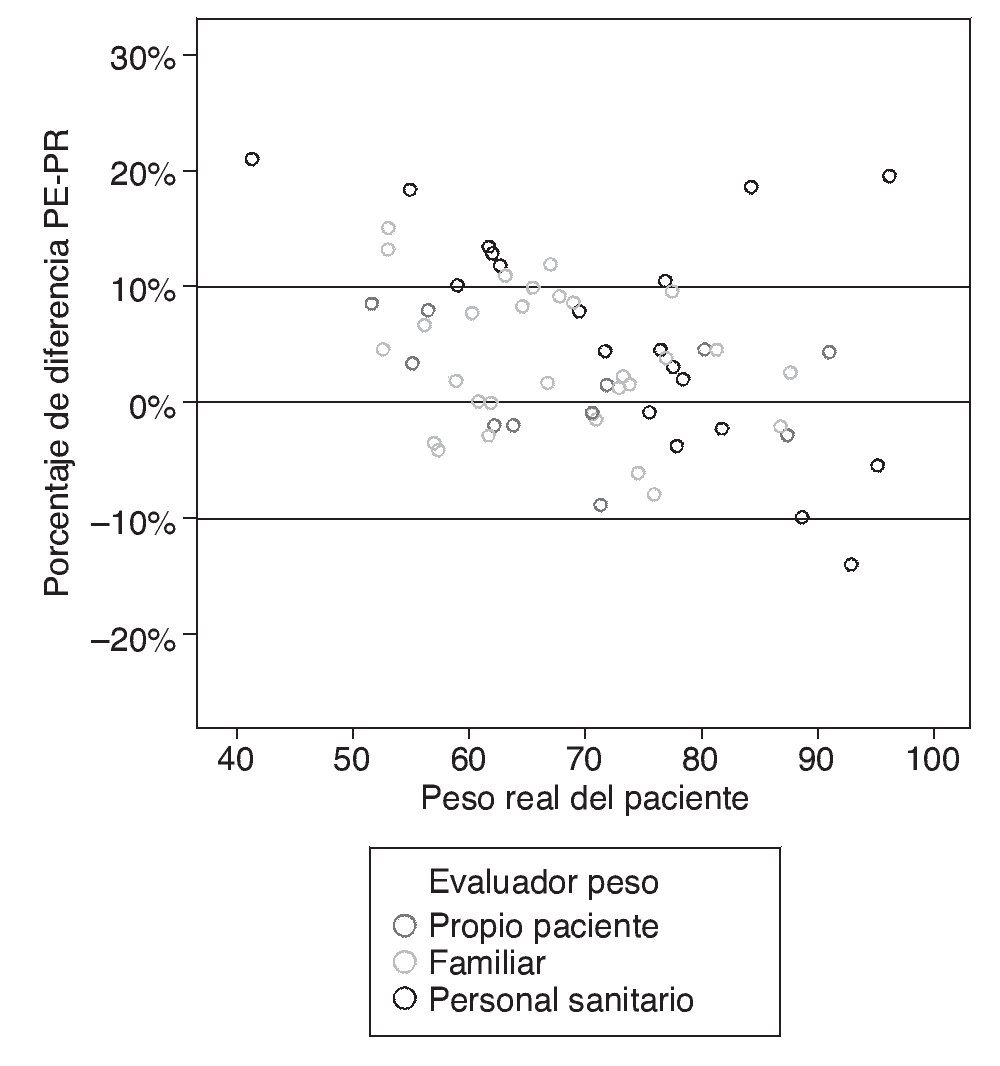
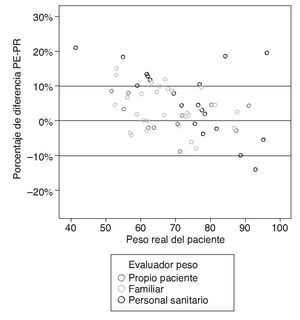
La correlación entre PE y PR fue elevada, con un coeficiente de correlación de Pearson de 0,899 (prueba r2 lineal = 0,808), el valor del coeficiente de correlación de Pearson entre el PR y el PE por el personal sanitario fue de 0,847 (prueba r2 lineal = 0,717), y entre el PR y PE por la familia fue de 0,924 (prueba r2 lineal = 0,872) (fig. 5).
Figura 5 Porcentaje de la diferencia entre el peso real (PR) y el peso estimado (PE) según el evaluador.
Discusión
La dosis de 0,9 mg/kg de peso de alteplasa hasta una dosis máxima de 90 mg se determinó como eficaz y segura para el tratamiento del ictus isquémico agudo a partir de los resultados de pequeños estudios piloto realizados a principios de la década de 19903-5. Dosis inferiores pueden resultar ineficaces, mientras que dosis más altas (en especial por encima de 0,95 mg/kg) se han relacionado con transformación hemorrágica5.
En la práctica habitual, el cálculo de la dosis de alteplasa para el tratamiento del ictus isquémico agudo resulta problemático, debido a la dificultad para conocer el PR del paciente. En muchas ocasiones, el paciente no se encuentra en condiciones de informar sobre su propio peso debido a los síntomas producidos por el ictus (presenta alteración del lenguaje o bajo nivel de consciencia) o porque el déficit motor impide pesar al paciente en una balanza tradicional. Además, debido a la rapidez con la que debe administrarse la medicación, no se considera recomendable perder tiempo en pesar al paciente.
Los resultados de nuestra investigación muestran que hay una variabilidad importante entre el PE y el PR (que llega a ser de 18,8 kg). Esta variabilidad resultó significativamente superior cuando el peso lo estimó personal sanitario. En cambio, cuando la fuente del peso fue el propio paciente, la estimación fue mucho más acertada. Como consecuencia de la variabilidad en el peso, la DRA de alteplasa en algunos casos fue superior a la considerada como segura, o inferior a la dosis considerada eficaz.
Varios estudios han analizado los errores en la estimación del peso de los pacientes y su repercusión en el cálculo de dosis de diferentes fármacos. En todos ellos se observaron importantes imprecisiones cuando el peso lo estimó personal sanitario, mientras que el PE por el propio paciente resultó mucho más preciso6-8.
En un estudio7 realizado en pacientes cardiológicos, a los que se administraba heparina de bajo peso molecular, se observó también una importante disparidad entre el PE y el PR de los pacientes que afectaba a la dosis de fármaco administrada. En este estudio, además, se detectó una sobreestimación del peso en pacientes más delgados y una infraestimación en los pacientes obesos, resultado que no se observa en nuestro estudio.
En el estudio WAIST, que analizó la variabilidad del PE y de la DRA de alteplasa en pacientes con ictus agudos, se observó que un 12% de los pacientes fue infradosificado (recibió una dosis un 10% menor a la recomendada) y un 17% recibió dosis mayores al 10% de dosis la recomendada. La mayor diferencia entre PE y PR se observó cuando los estimadores fueron los médicos o el personal de enfermería que atendieron al paciente. Además, la infradosificación se asoció de forma independiente a una eficacia menor del tratamiento, con una tasa mayor de dependencia o muerte tras el ictus9.
En otro estudio que también analizó los errores de dosis de alteplasa en pacientes con ictus, se observó un riesgo mayor de complicaciones hemorrágicas intracerebrales en los pacientes que recibieron dosis más elevadas de alteplasa10.
Se han propuesto diferentes métodos para el cálculo del peso basado en parámetros antropométricos (altura, perímetro abdominal, de cintura, muslo, tobillo, etc.), con resultados aceptables, pero que en ningún caso superaron la estimación del paciente de su propio peso11,12. Consideramos que la aplicación de estos métodos para el cálculo del peso en el contexto del paciente con ictus agudo resultaría poco factible, porque implicaría entorpecer y retrasar la aplicación de los cuidados pertinentes para la TIV (seguimiento del paciente, canalización de vía venosa, preparación de la medicación, etc.).
Otros autores proponen la dotación de camas con peso en el Servicio de Urgencias (cuartos de parada, mesa de la tomografía computarizada craneal) para obtener el PR del paciente13.
Un hallazgo llamativo de nuestro estudio fue que tan sólo en el 22% de los casos se calculó la dosis de alteplasa en función del PE por el propio paciente. Suponemos que una proporción mayor de pacientes se encontraba en condiciones de proporcionar dicha información. Por tanto, consideramos que la estrategia adecuada a seguir es tratar de conseguir el PE por el propio paciente como primera opción, pese a las limitaciones que a priori puedan hacernos pensar que no puede proporcionarnos esta información.
Conclusiones
El cálculo de dosis de alteplasa a partir del PE del paciente conlleva una variabilidad de la DRA, que en ocasiones resulta llamativa y podría afectar a la eficacia y la seguridad del tratamiento. Debemos considerar, siempre que sea posible, la información proporcionada por el paciente sobre su peso. Se hace necesario buscar una fórmula que permita obtener el PR del paciente, evitando recurrir a la estimación visual del peso.
Conflicto de intereses
Los autores declaran no tener ningún conflicto de intereses.
Agradecimientos
A todo el personal del Servicio de Neurología, médicos, personal de enfermería y auxiliares de obras y servicios, sin los que no se hubiera podido realizar el estudio.
Recibido el 5 de diciembre de 2011; aceptado el 25 de septiembre de 2012
qEste trabajo ha obtenido el Premio SEDENE 2011 al mejor Póster en la XVIII Reunión Anual de la SEDENE. Barcelona 2011.
* Autor para correspondencia.
Correo electrónico:
carmen.funesmolina@gmail.com (C. Funes Molina).