Con posterioridad a la introducción de la máscara laríngea en los años 1980 se han venido desarrollando varios dispositivos similares, los cuales han cambiado el manejo de la vía aérea pediátrica en anestesia. Este artículo de reflexión describe y examina los distintos dispositivos supraglóticos para la vía aérea pediátrica disponibles actualmente en el Reino Unido.
MetodologíaEste artículo de opinión se basa en una revisión de los artículos que tratan el tema de los dispositivos supraglóticos para la vía aérea pediátrica, realizada en las bases de datos Cochrane, Medline, Ovid y PubMed y también en los libros de texto.
ResultadosA medida que se desarrollan dispositivos nuevos con indicación clara de pertinencia clínica y ventajas genuinas, se necesitarán también estudios de alta calidad a fin de mejorar las características de dichos dispositivos.
Following the introduction of the laryngeal mask in the 1980's, several similar devices have been developed, changing paediatric airway management under anaesthesia. This reflective article describes and examines the different paediatric supraglottic airway devices currently available in the U.K.
MethodologyThis perspective article is based on a narrative review of articles that discussed paediatric supraglottic airway devices using Cochrane, Medline, Ovid and PubMed databases as well as text books.
ResultsAs new devices continue to be developed with a clear indication of clinical relevance and genuine advantages, so high quality research will also continue to be required in order to improve features in new devices.
El manejo de la vía aérea es una habilidad esencial en anestesia pediátrica. Una vía aérea difícil manejada de manera subóptima o sin preparación adecuada puede ser un factor determinante de morbimortalidad en anestesia pediátrica. La vía aérea con máscara laríngea (LMA) y otros dispositivos supraglóticos han abierto el camino para cambios importantes en el manejo de la vía aérea tanto en los procedimientos de rutina como en los casos de urgencia.
Antes de la introducción de la LMA en 1988 había solamente dos alternativas para el manejo de la vía aérea en niños y adultos por igual: el tubo endotraqueal o la máscara facial.
A veces puede ser difícil mantener una ventilación adecuada con la máscara facial, y cuando esta es ineficaz, puede llevar a hipoxia e hipercapnia. Las distintas características anatómicas, y también los hábitos corporales, pueden dificultar una buena ventilación a través de la máscara facial tanto en los adultos como en los niños.
Si bien el tubo endotraqueal proporciona una vía segura y definitiva, tiene sus desventajas. La intubación endotraqueal es una habilidad avanzada que se debe adquirir, y entraña el riesgo de lesiones de los dientes, la laringe y la tráquea, además del riesgo de hipoxia cuando es inesperadamente difícil o imposible intubar la tráquea.
En 1981, el Dr. Archie Brain realizó experimentos en modelos de yeso de laringes de cadáveres1 y observó que cuando se hacía un sello hermético alrededor de la laringe posterior con un balón de forma elíptica inflado en la hipofaringe, se podía llevar el aire a la vía aérea2.
Al conectar una sección de manguera al balón de caucho de una máscara dental de Goldman, desarrolló el primer prototipo de la LMA que se utilizó por primera vez en un paciente en 1981. Ya en 1983, Brain pudo informar sobre el primer ensayo del uso clínico de la LMA en 23 pacientes, incluidas 16 mujeres sometidas a cirugía laparoscópica ventiladas exitosamente a través de la máscara laríngea estando paralizadas3,4. Experimentó con varios materiales, realizó estudios con 700 pacientes y utilizó más de 200 prototipos, antes de lanzar el dispositivo en 1988. La primera máscara laríngea se introdujo en Gran Bretaña en 1988 y después en los Estados Unidos de América en 1991.
Para 2006, la máscara laríngea se había utilizado en cerca de 200 millones de pacientes y se habían publicado más de 2.500 trabajos académicos1. En 2003 venció la patente de la máscara laríngea clásica, siendo 2008 la fecha de vencimiento de la patente estatutaria. Varias compañías comenzaron a diseñar y desarrollar diferentes dispositivos con base en la máscara laríngea clásica pero como dispositivos de uso único. Aparte de los factores comerciales, la preocupación por el riesgo de infección por un prion (agente causante de la nueva variante de la enfermedad de Creutzfeldt-Jakob [vCJD]) fue el factor determinante que impulsó el desarrollo de los dispositivos de uso único a finales de los años 19901.
El costo, la ley de esterilización del Reino Unido, la forma de disponer de los materiales y los factores ambientales, entre otras cosas, han influido en los distintos dispositivos supraglóticos para la vía aérea (SGAD) producidos durante los últimos 10 años. Con el vencimiento de la patente de la máscara laríngea clásica y tras un verdadero alud de nuevos dispositivos, tal parece que se han estabilizado los nuevos diseños.
En este artículo de opinión examinamos los distintos dispositivos supraglóticos para vía aérea disponibles actualmente en pediatría, e incluimos una descripción de sus funcionalidades y características específicas. Se basa en una revisión narrativa de los artículos sobre el tema de los dispositivos supraglóticos pediátricos, utilizando las bases de datos de Cochrane, Medline, Ovid y PubMed además de libros de textos.
AntecedentesContrario a lo que sucede con el tubo endotraqueal, el sello de la vía aérea que se logra con la máscara laríngea es menos seguro y, por tanto, su uso se ve limitado en ciertas situaciones, incluidos los casos de pacientes con alto riesgo de regurgitación y pacientes que requieren presiones ventilatorias elevadas o ventilación prolongada. Sin embargo, para el manejo de rutina de la vía aérea, la máscara laríngea se ha convertido en una herramienta esencial. Para mediados de los años 1990, se calculaba que la máscara laríngea se utilizaba hasta en un 30% de todas las anestesias generales en el mundo3-7. La máscara laríngea tiene una función importante en el manejo de la vía aérea difícil, tanto esperada como imprevista. Se puede utilizar como canal para la intubación traqueal con un tubo endotraqueal sobre un broncoscopio de fibra óptica, al igual que como dispositivo de rescate cuando otros mecanismos para lograr la ventilación fallan o no son posibles. Hay varios estudios grandes que reportan la eficacia y el uso seguro en neonatos8,9, víctimas de trauma8,10, mujeres sometidas a cesárea8,11, situaciones de paro cardíaco y urgencias extrahospitalarias8,12. La Sociedad de Vía Aérea Difícil (Reino Unido), la Sociedad Americana de Anestesiólogos y el Colegio de Anestesia de Australia y Nueva Zelanda incluyen la máscara laríngea en sus guías para la vía aérea difícil12-14.
La primera máscara laríngea pediátrica fue una versión más pequeña de la LMA producida para adultos15, en la cual no se tomaron en consideración las diferencias anatómicas de la vía aérea de los lactantes y los niños. Sin embargo, la máscara laríngea funcionó bien en esta población, con una tasa de éxito reportada del 95-98% en términos de permitir una ventilación adecuada en los niños9,16.
Clasificación y tamaño de la máscara laríngeaDependiendo de la presencia o ausencia de un canal gástrico, los dispositivos supraglóticos disponibles para vía aérea se clasifican en uno de dos grupos (dispositivos de primera o de segunda generación). Los dispositivos de primera generación carecen del canal de acceso gástrico, la máscara descansa encima de la glotis con el tubo de vía aérea conectado a ella. Por otra parte, los dispositivos de segunda generación incorporan un canal para acceso gástrico que permite un desfogue y a la vez la posibilidad de insertar un tubo gástrico.
La selección de una máscara laríngea del tamaño correcto se determina con base en el peso del paciente. El tamaño1 se recomienda para neonatos y lactantes de hasta 5kg de peso, pero también se ha utilizado en prematuros de menos de 1kg15. Es importante señalar que en el subgrupo de neonatos y prematuros la incidencia de los problemas de la vía aérea parece más alta (obstrucción tardía de la vía aérea y desplazamiento)15. Los estudios con fibrobroncoscopio sugieren que la epiglotis se puede plegar sobre la máscara laríngea, en particular en los lactantes pequeños, ocluyendo la laringe15. Sin embargo, a pesar de esto, al parecer no hay interdependencia entre la visualización a través de la vía aérea y la vía área clínicamente permeable15. Esto sugiere que a pesar de la compresión de la glotis ejercida por la máscara laríngea, el área remanente podría ser lo suficientemente grande para permitir un flujo satisfactorio del gas.
En el grupo de 10-20kg, el tamaño recomendado es 2, pero en algunos pacientes el tamaño de 2.5 podría proporcionar un mejor sello. Sin embargo, esto es a expensas de una presión más alta de sellado del balón, lo cual podría comprometer el drenaje venoso17,18.
El tamaño de 2.5 se recomienda en pacientes de entre 20-30kg, mientras que para los pacientes de entre 30-50kg se recomienda el tamaño3.
Con el aumento de la incidencia de la obesidad infantil, es mayor el número de niños que llegan para cirugía de rutina. En estos casos puede ser difícil escoger la máscara laríngea del tamaño correcto. En niños de más de 40kg, la selección del tamaño de la máscara laríngea solamente con base en el peso puede traducirse en unas presiones de sellado excesivamente altas8, y podría ser más apropiado determinar el tamaño del dispositivo con base en la edad y la predicción del peso.
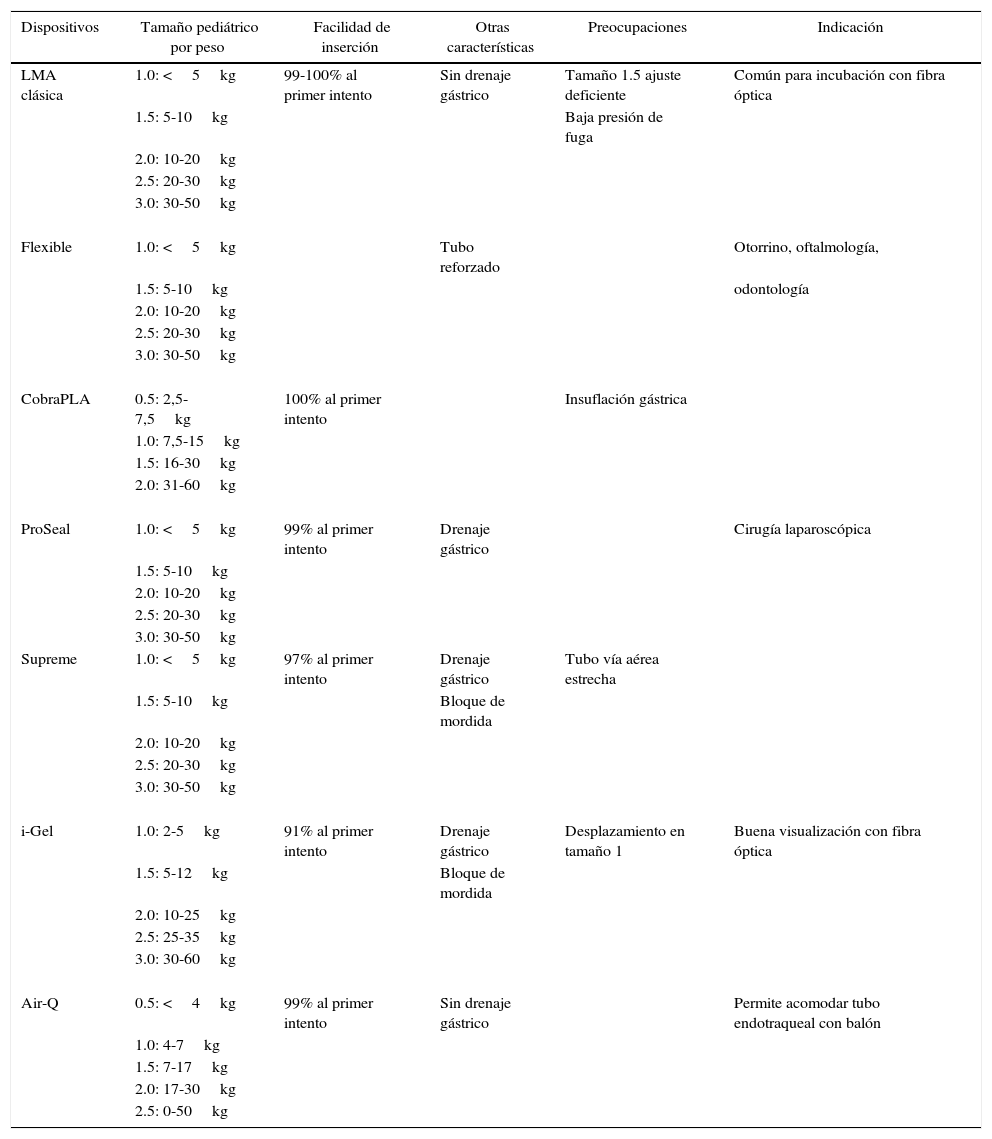
Para cada tamaño de la máscara laríngea hay una recomendación del fabricante en cuanto al volumen de insuflación. En todos los tamaños, el exceso de insuflación del balón por encima de lo recomendado por el fabricante puede generar compresión de las estructuras que rodean la faringe. Hay casos pediátricos documentados de parálisis de los nervios hipogloso y laríngeo recurrente15. Esto también puede ocurrir cuando se infla más de la cuenta para compensar una fuga en los casos en que la máscara laríngea utilizada es demasiado pequeña para un niño (tabla 1).
Resumen de las características de los dispositivos supraglóticos de vía aérea disponibles para pacientes pediátricos
| Dispositivos | Tamaño pediátrico por peso | Facilidad de inserción | Otras características | Preocupaciones | Indicación |
|---|---|---|---|---|---|
| LMA clásica | 1.0: <5kg | 99-100% al primer intento | Sin drenaje gástrico | Tamaño 1.5 ajuste deficiente | Común para incubación con fibra óptica |
| 1.5: 5-10kg | Baja presión de fuga | ||||
| 2.0: 10-20kg | |||||
| 2.5: 20-30kg | |||||
| 3.0: 30-50kg | |||||
| Flexible | 1.0: <5kg | Tubo reforzado | Otorrino, oftalmología, | ||
| 1.5: 5-10kg | odontología | ||||
| 2.0: 10-20kg | |||||
| 2.5: 20-30kg | |||||
| 3.0: 30-50kg | |||||
| CobraPLA | 0.5: 2,5-7,5kg | 100% al primer intento | Insuflación gástrica | ||
| 1.0: 7,5-15kg | |||||
| 1.5: 16-30kg | |||||
| 2.0: 31-60kg | |||||
| ProSeal | 1.0: <5kg | 99% al primer intento | Drenaje gástrico | Cirugía laparoscópica | |
| 1.5: 5-10kg | |||||
| 2.0: 10-20kg | |||||
| 2.5: 20-30kg | |||||
| 3.0: 30-50kg | |||||
| Supreme | 1.0: <5kg | 97% al primer intento | Drenaje gástrico | Tubo vía aérea estrecha | |
| 1.5: 5-10kg | Bloque de mordida | ||||
| 2.0: 10-20kg | |||||
| 2.5: 20-30kg | |||||
| 3.0: 30-50kg | |||||
| i-Gel | 1.0: 2-5kg | 91% al primer intento | Drenaje gástrico | Desplazamiento en tamaño 1 | Buena visualización con fibra óptica |
| 1.5: 5-12kg | Bloque de mordida | ||||
| 2.0: 10-25kg | |||||
| 2.5: 25-35kg | |||||
| 3.0: 30-60kg | |||||
| Air-Q | 0.5: <4kg | 99% al primer intento | Sin drenaje gástrico | Permite acomodar tubo endotraqueal con balón | |
| 1.0: 4-7kg | |||||
| 1.5: 7-17kg | |||||
| 2.0: 17-30kg | |||||
| 2.5: 0-50kg |
Fuente: Autores.
La máscara laríngea permite ventilación con presión positiva en la vía aérea debido a la baja presión que ejerce sobre la laringe. Cuando la presión inspiratoria es superior a los 20cmH2O aumenta el riesgo de insuflación gástrica y regurgitación15. Este riesgo aumenta todavía más si la máscara laríngea está mal posicionada. La ventilación con control de presión puede producir presiones inspiratorias más bajas en comparación con la ventilación con control de volumen en la cual no se regula la presión, particularmente en lactantes y niños17.
El uso de relajantes musculares facilita la ventilación mecánica efectiva al aumentar la distensibilidad torácica, pero se ha demostrado, si bien en estudios con animales, que períodos prolongados de ventilación mecánica (más de 5h) a través de la máscara laríngea producen efectos indeseables tales como edema lingual y deterioro capilar y epitelial18.
Retiro de la máscara laríngeaAunque inicialmente se sugirió que la máscara laríngea se debía retirar una vez restablecidos los reflejos de la vía aérea y cuando el paciente estuviera en capacidad de obedecer órdenes, es decir, abrir la boca al pedírselo, en pediatría es práctica reconocida retirar la máscara laríngea en estado «profundo» (con los reflejos laríngeos ausentes)15. Los anestesiólogos que están a favor de este método describen menos complicaciones como laringoespasmo, tos, mordida apretada y desaturación. Las secreciones se pueden succionar antes de que se recuperen los reflejos laríngeos15. Sin embargo, no hay evidencia disponible para respaldar esta técnica.
Dispositivos supraglóticos para la vía aérea pediátricaActualmente en el Reino Unido hay 7 dispositivos supraglóticos para la vía aérea pediátrica.
LMA clásica (cLMA™).
LMA flexible (fLMA™).
LMA-Unique™.
LMA-ProSeal (PLMA™).
i-Gel™.
LMA Supreme™.
Cobra Perilaryngeal Airway (CobraPLA™).
Air-Q™.
En la práctica de la anestesia pediátrica hay pocos ensayos aleatorizados controlados de calidad y con el poder adecuado para detectar las diferencias en los desenlaces.
De acuerdo con la Organización Mundial de la Salud, en el mundo se administran anualmente 250millones de anestesias8. La incidencia de broncoaspiración durante la anestesia general es difícil de establecer. La mayor parte de la evidencia proviene de estudios en adultos (no aplicables directamente a la población pediátrica), series de casos, y del uso continuo en lugar de evidencia de alta calidad. Esto crea un sesgo contra los nuevos dispositivos y, por tanto, toda afirmación con respecto a la seguridad y la eficacia se debe tomar con cautela. Los estudios aleatorizados futuros se deben centrar en los desenlaces durante distintos tipos de procedimientos.
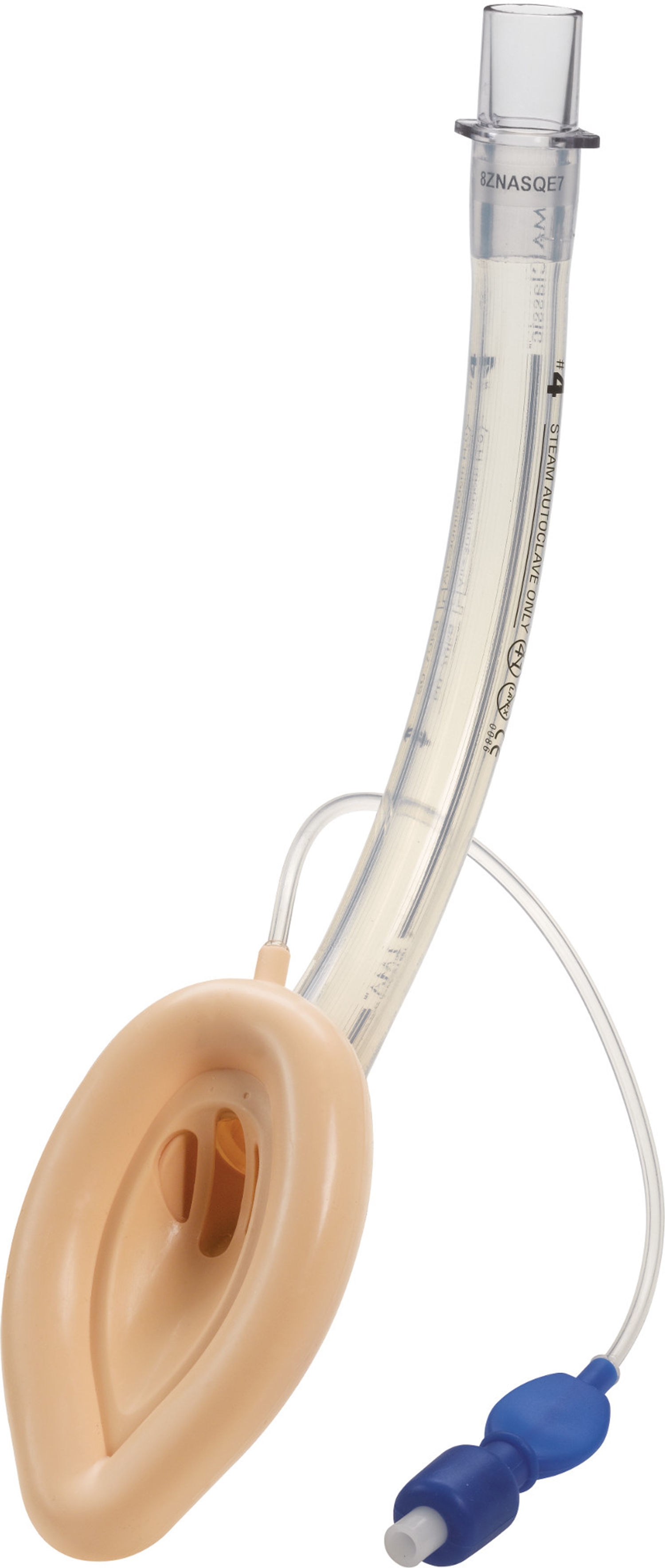
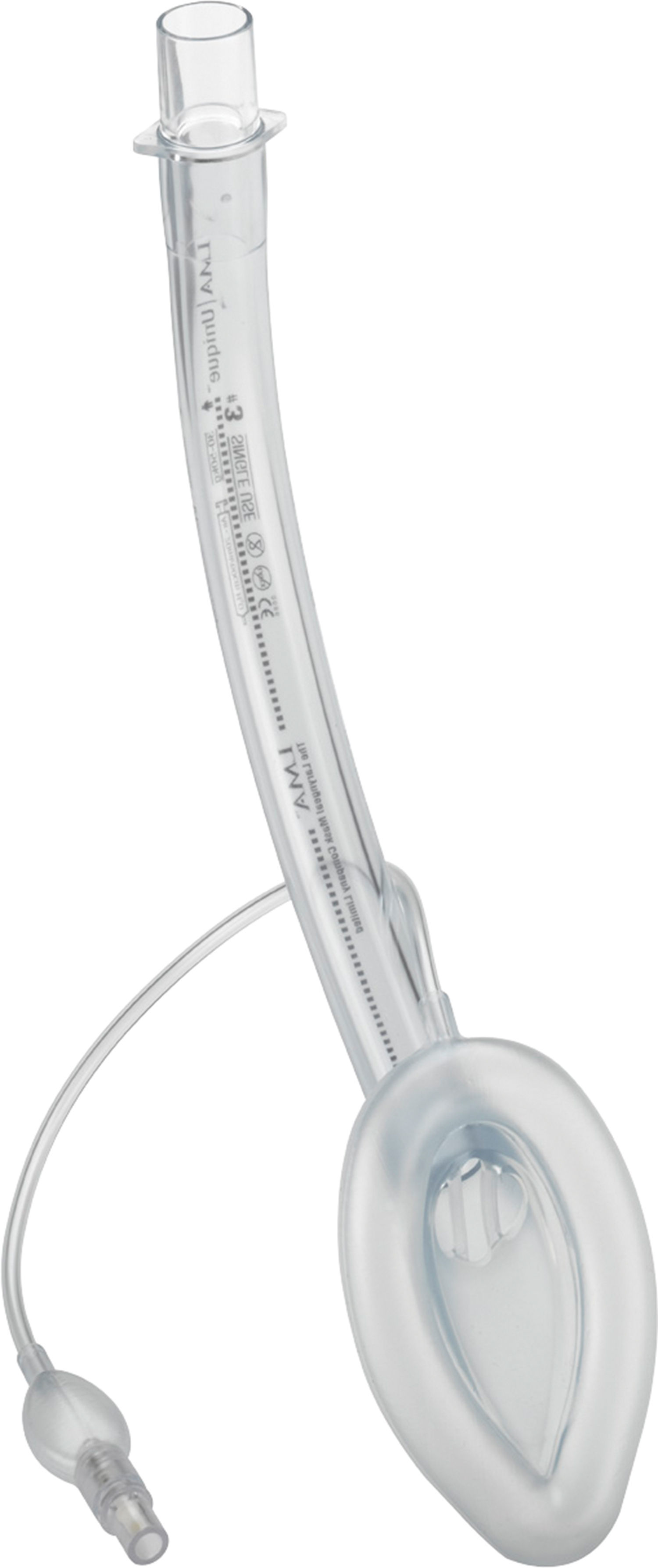
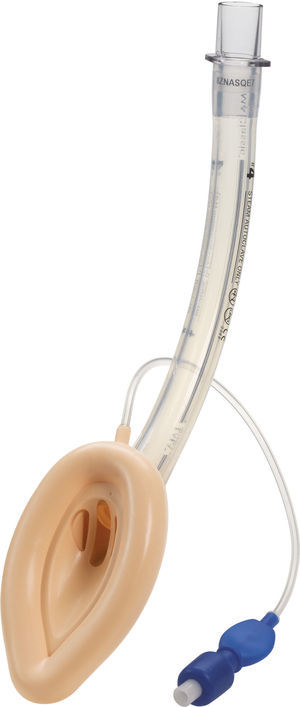
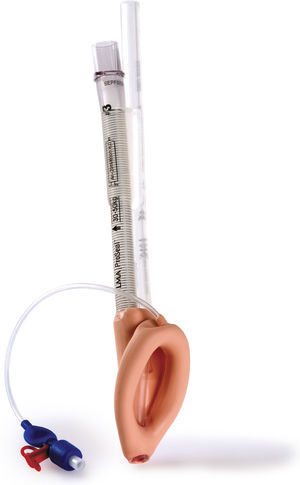
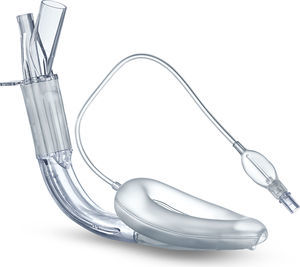
Máscara laríngea clásica (cLMA)La máscara laríngea clásica (cLMA) (figs. 1 y 2) consta de una máscara de silicona blanda que se asienta sobre la laringe, con un vástago integrado que se extiende para permitir la conexión con el circuito de anestesia. Tiene dos barras (rejillas) gruesas de silicona diseñadas para impedir que descienda la epiglotis y ocluya la luz. Puesto que están hechas de caucho de silicona, las máscaras laríngeas clásicas se pueden esterilizar en autoclave y reutilizar19.
En los pacientes pediátricos, el uso de dispositivos supraglóticos puede ofrecer una ventaja sobre los tubos endotraqueales durante la anestesia en niños que han tenido infecciones recientes de las vías respiratorias altas. En un ensayo aleatorizado, Tait et al. compararon el uso de la máscara laríngea clásica con el tubo endotraqueal y demostraron que el grupo en el cual se utilizó la máscara laríngea clásica tuvo un número significativamente menor de complicaciones respiratorias en comparación con el grupo en el cual se utilizó el tubo endotraqueal20.
Las principales complicaciones reportadas con el uso de la máscara laríngea clásica son el laringoespasmo y la obstrucción causada por el plegado de la epiglotis. Al parecer, la tasa de complicaciones en los lactantes pequeños es más alta, alcanzando el 47%9-11,20.
En los niños, la presión de fuga de la vía aérea es más alta que en los lactantes21,22, lo cual podría despertar dudas con respecto a la posibilidad de proporcionar una ventilación con presión positiva de manera segura con la máscara laríngea clásica en este grupo. La fuga alrededor del balón podría provocar distensión gástrica y aumentar el riesgo de broncoaspiración.
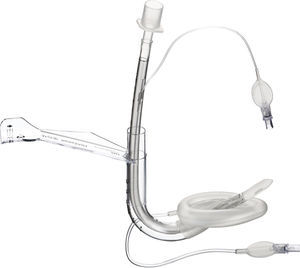
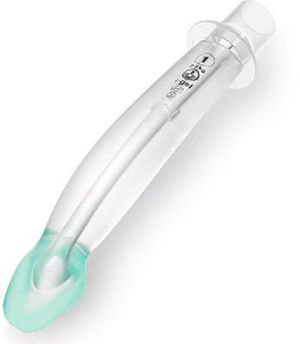
Máscara laríngea flexible (fLMA™)La máscara laríngea flexible (o reforzada) (fig. 3) es similar a la máscara laríngea clásica pero tiene un tubo de respiración más delgado, más estrecho y más largo reforzado con una espiral de alambre de acero para impartir mayor flexibilidad y reducir el riesgo de acodadura19.
La máscara laríngea flexible (fLMA) se utilizó por primera vez en 1990. Se desarrolló específicamente para anestesia en otorrinolaringología y en procedimientos odontológicos. Su función se ha ampliado a muchos otros campos, entre ellos los de anestesia para cirugía oftalmológica y de cabeza y cuello. Se han realizado algunos estudios grandes en pediatría para evaluar su eficacia22,23, los cuales han demostrado que, en casos de adenoamigadalectomía, se desempeña igual o mejor que los tubos endotraqueales en lo que se refiere a mejorar el acceso quirúrgico y prevenir la contaminación de la vía aérea24-26.
Webster et al.26 estudiaron el prototipo de la máscara laríngea flexible y lo compararon con intubación endotraqueal en 99 niños sometidos a adenoamigdalectomía. Este estudio concluyó que la máscara laríngea flexible era una alternativa segura a la intubación traqueal en los casos de adenoamigdalectomía. La máscara laríngea flexible no limitó el acceso quirúrgico y protegió las vías respiratorias bajas contra contaminación con la sangre aspirada. Los autores también concluyeron que hubo una menor necesidad de ventilación asistida y que la respuesta hemodinámica a la laringoscopia se redujo en este grupo. La incidencia de complicaciones después de la extubación se redujo pero no se eliminó en el grupo de la máscara laríngea.
Williams y Bailey25 aleatorizaron a 104 niños ASA grados 1 y 2, llevados a amigdalectomía y/o adenoidectomía electiva. En un grupo se utilizó la máscara laríngea flexible y en el otro se utilizó el tubo endotraqueal RAE. Concluyeron que la máscara laríngea flexible brinda una vía aérea segura hasta el momento en que se recuperan por completo los reflejos laríngeos.
A pesar de la evidencia existente, en anestesia pediátrica para otorrinolaringología el uso de tubos endotraqueales sigue siendo la práctica más común22,23.
Las máscaras laríngeas clásica y flexible han transformado radicalmente la práctica de la anestesia pediátrica y suelen ser los dispositivos supraglóticos utilizados más comúnmente en esa población. Tienen evidencia concluyente derivada de varios estudios de buena calidad, son seguras y eficaces, y son punto de referencia para el estudio de dispositivos nuevos. Tienen un papel invaluable en el manejo de la vía aérea de los niños con infecciones de la vía respiratoria, y en los casos de vía aérea difícil tanto prevista como imprevista. Su principal limitación es en lactantes pequeños, en quienes puede ocurrir un sellado deficiente con insuflación gástrica o fuga del contenido gástrico21,22.
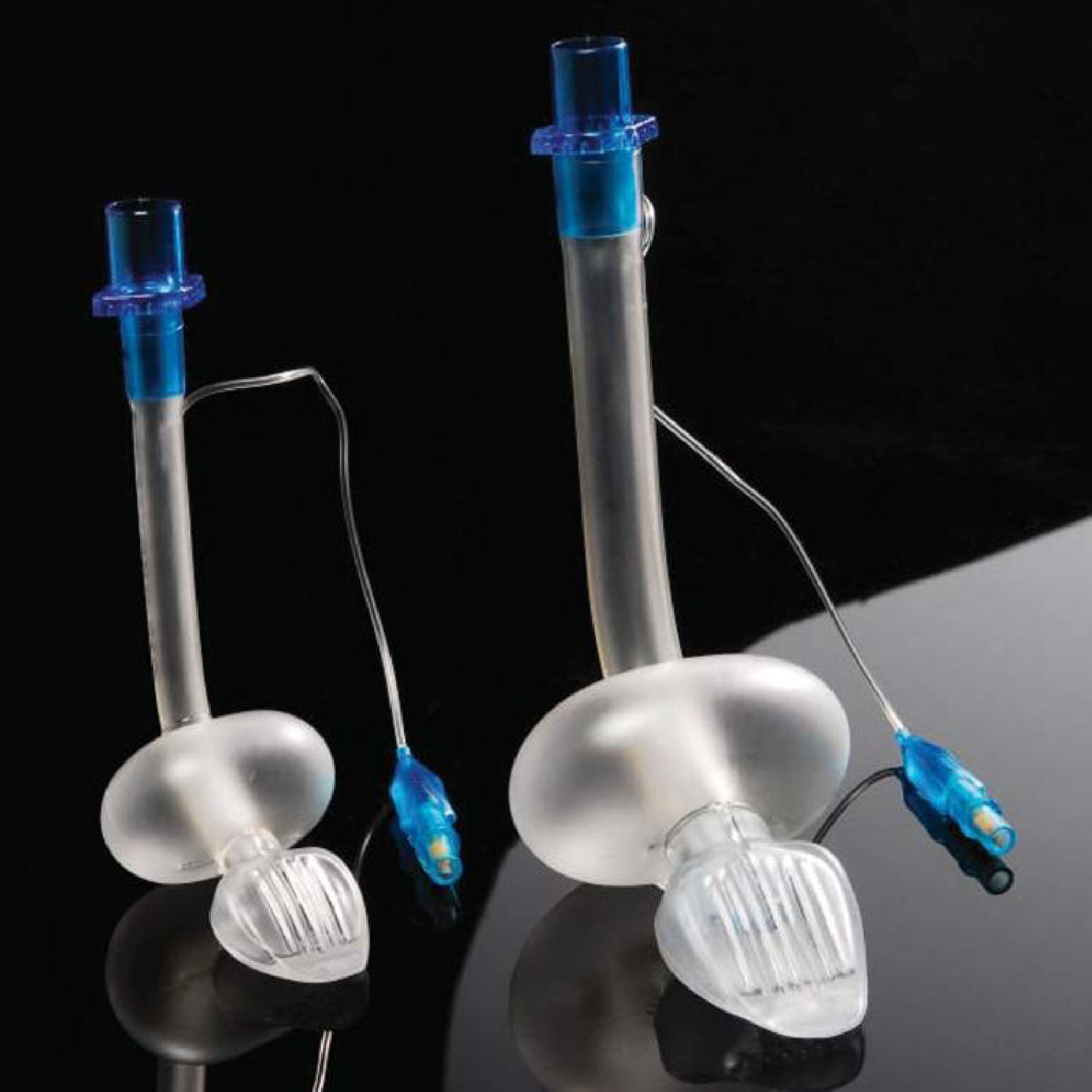
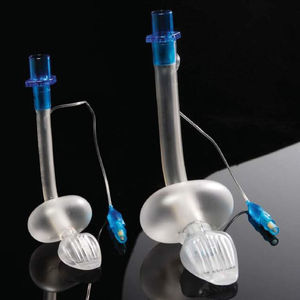
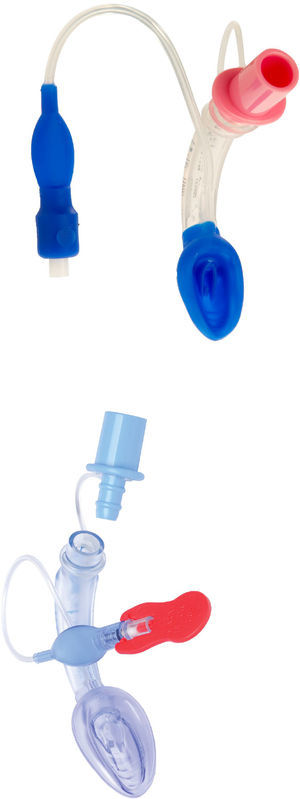
CobraPLA™La vía aérea perilaríngea Cobra (CobraPLA) (fig. 4) salió al mercado en 2003. Tiene una punta distal flexible cuya forma le da el nombre al dispositivo. Es un dispositivo de uso único y viene en 8 tamaños para usar en neonatos y hasta en pacientes de más de 140kg de peso.
Tiene una cabeza de plástico blando diseñada para asentarse en la hipofaringe y sellarla, y su superficie anterior queda al nivel de la entrada de la laringe. En su parte proximal dispone de un balón inflable que eleva la base de la lengua y ayuda a sellar la orofaringe19.
Un estudio en adultos adelantado por Cook y Lowe27 se debió suspender prematuramente puesto que hubo dos casos de broncoaspiración durante cirugías de bajo riesgo. Sin embargo, hay otros estudios en adultos que demostraron un desempeño similar al comparar el dispositivo Cobra con la máscara laríngea clásica28-30.
En la práctica pediátrica, la CobraPLA se ha comparado con la máscara laríngea Unique en estudios realizados por Szmuk5,25 y por Gaitini et al.31 con 200 y 80 niños, respectivamente. No se reportaron diferencias con respecto a la facilidad de inserción de los dos dispositivos, pero Gaitini et al.31 reportaron el uso de presiones de fuga más elevadas con la CobraPLA en comparación con la máscara laríngea Unique. Passariello et al. estudiaron a 40 niños entre uno y 10años de edad con pesos de entre 10 y 35kg y grados ASA 1 o 2 programados para procedimientos quirúrgicos menores32. Para el grupo en el cual se utilizó la CobraPLA se reportaron tasas de insuflación gástrica del 21%, a pesar de unas presiones ventilatorias de 20cmH2O o menos.
No hay evidencia para sustentar una ventaja clara de la CobraPLA frente a la máscara laríngea clásica8.
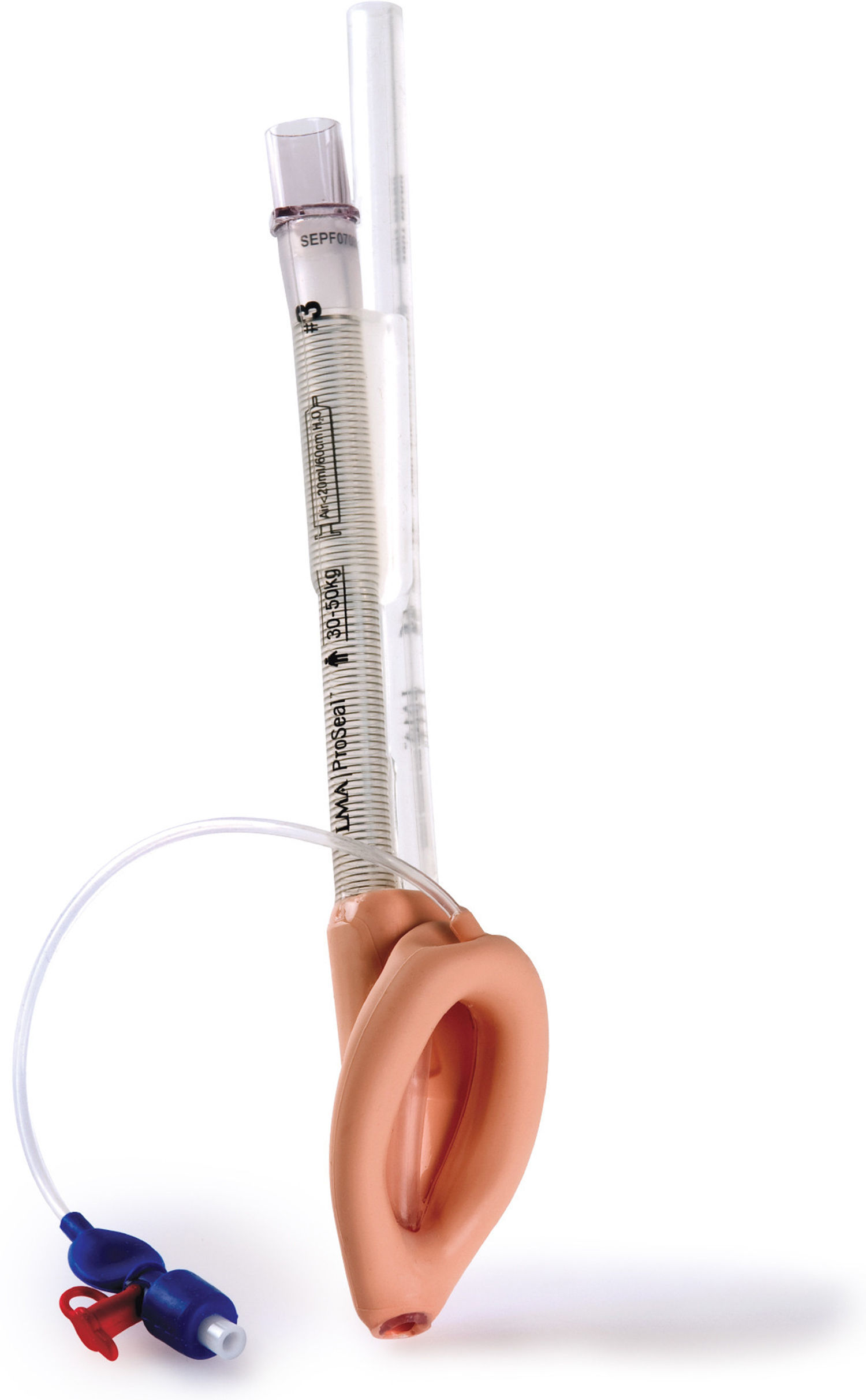
Máscara laríngea ProSeal (PLMA™)La máscara laríngea ProSeal (PLMA) (fig. 5) se utilizó por primera vez en el Reino Unido en 2000 y se comercializó para uso en pediatría en 2007, con modificaciones de diseño encaminadas a mejorar el desempeño durante la ventilación controlada, mejorar la seguridad reduciendo el riesgo de broncoaspiración, y facilitar el diagnóstico del posicionamiento equivocado de la punta19.
La principal característica que la diferencia de la máscara laríngea clásica es la presencia de un canal gástrico adosado al tubo de la vía aérea, el cual puede utilizarse para pasar una sonda gástrica. Trae un bloque de mordida incorporado y la forma de la máscara es más grande que la de la máscara laríngea clásica.
Los tamaños pediátricos y neonatales no llevan el balón dorsal adicional que traen los tamaños 3-58.
La máscara laríngea ProSeal también ejerce menos presión contra la mucosa que la máscara laríngea clásica, reduciendo la posibilidad de trauma y daño de la mucosa33,34.
Son muchos los estudios que respaldan la utilización de la máscara laríngea ProSeal35-37. Todos estos estudios concuerdan en que es fácil de insertar al primer intento en el 84-94% de los casos, ofrece una ventilación efectiva en el 99-100% de los casos y facilita una buena visualización de la laringe a través del fibrobroncoscopio en el 86-92%36,37.
Sinha et al. compararon la máscara laríngea ProSeal con el tubo endotraqueal en 60 niños entre las edades de 6meses y 8años33 llevados a cirugía laparoscópica con una duración del carboperitoneo inferior a 60min. En el estudio no se incluyeron pacientes con infecciones activas de las vías respiratorias ni niños con vía aérea difícil previamente reconocida o con riesgo de broncoaspiración. Se encontró que la máscara laríngea ProSeal y el tubo endotraqueal fueron igualmente eficaces desde el punto de vista ventilatorio, sin una diferencia estadísticamente significativa en cuanto a saturación de oxígeno o mediciones de dióxido de carbono al final de la espiración. La tasa de inserción exitosa al primer intento fue del 88% para la máscara laríngea.
El estudio fue pequeño y otros estudios adicionales deberán incluir diversos procedimientos y períodos más prolongados de carboperitoneo antes de poder recomendar el uso de la máscara laríngea ProSeal durante cirugía laparoscópica electiva y cirugía abdominal en pacientes pediátricos.
Se han realizado varios ensayos aleatorizados controlados para comparar la máscara laríngea ProSeal con la clásica21,22,38-40. Estos estudios confirmaron que la máscara laríngea ProSeal es fácil de insertar y mantiene una buena posición anatómica, pero también sugieren que requiere una presión de fuga orofaríngea más elevada en comparación con la máscara laríngea clásica. Goldman et al.22 realizaron exámenes con fibra óptica en 30 lactantes anestesiados no paralizados entre las edades de 2 y 30meses y con un peso de entre 5 y 12kg. Aunque se trató de un estudio relativamente pequeño, determinó que en 3 de cada 5 pacientes que presentaron una reducción del volumen corriente máximo, hubo confirmación por fibra óptica de compresión de la laringe con el uso de la máscara laríngea ProSeal en comparación con la clásica.
Lopez et al.36 estudiaron a 60 lactantes y neonatos sometidos a cirugía electiva. Los dividieron en dos grupos, en uno de los cuales se utilizó la máscara laríngea ProSeal de tamaño1 y en el otro la máscara laríngea clásica también de tamaño1. Concluyeron que la máscara laríngea ProSeal ofreció una ventilación segura y efectiva permitiendo al mismo tiempo la ventilación con presión positiva.
Para resumir, la PLMA podría tener mejores características de desempeño en comparación con las máscaras laríngeas estándar, en particular en los casos en que se requiere ventilación controlada. Hay menos volumen de evidencia que sustenta el uso de la máscara laríngea ProSeal en comparación con la clásica, pero su uso en pediatría podría estar indicado particularmente cuando se requiere ventilación controlada41.
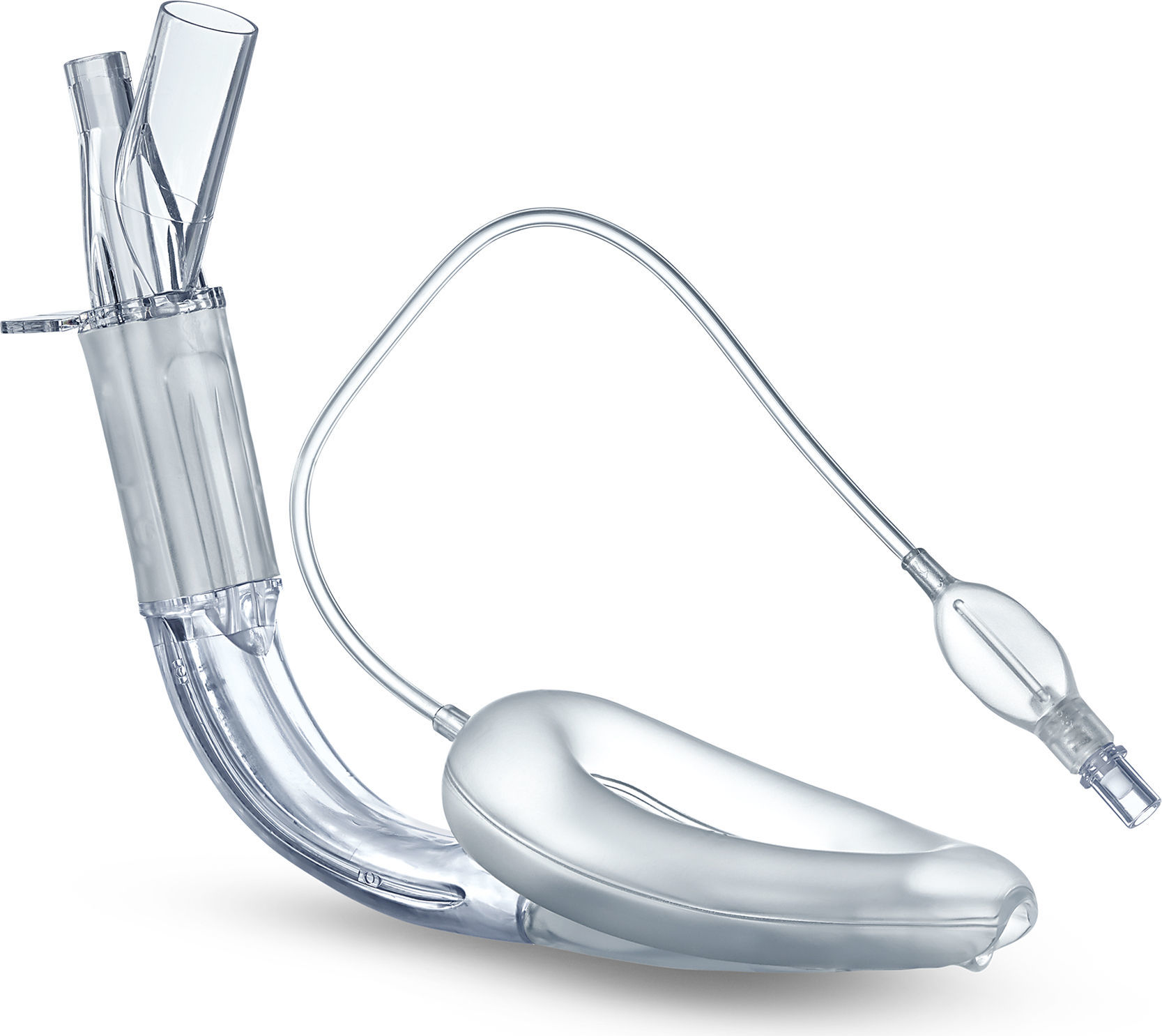
Máscara laríngea Supreme™La máscara laríngea Supreme (fig. 6) se utilizó por primera vez en 2009. Este dispositivo de PVC para uso único se desarrolló con el propósito de fusionar las características más ventajosas de la PLMA (mejor sello, tubo de drenaje, bloque de mordida incorporado) con mayor facilidad de inserción considerando que es más curva y rígida. Los orificios de ventilación se encuentran en la parte lateral de la máscara, y para evitar atrapamiento de la epiglotis tiene unas aletas que se apoyan sobre esta19.
En dos estudios aleatorizados, Jagannathan et al. compararon la máscara laríngea Supreme con la máscara laríngea Unique (una versión desechable de la máscara laríngea clásica). La conclusión de esos estudios fue que la máscara laríngea Supreme proporcionaba un puerto adecuado para el acceso gástrico reduciendo la insuflación del estómago al utilizar presiones de fuga de la vía aérea comparables con las de la máscara laríngea Unique o más altas42-44.
Al comparar la i-Gel con la Supreme, la i-Gel tiene mayor fuga de la vía aérea42. Sin embargo, los dos dispositivos son adecuados para proporcionar ventilación con presión positiva intermitente y no hubo diferencias en su desempeño clínico.
No hay evidencia suficiente disponible para evaluar a fondo el desempeño de la máscara laríngea Supreme en pediatría. Trevisanuto et al.45 realizaron un estudio observacional con 40 anestesiólogos y el uso de las máscaras laríngeas Supreme, clásica y ProSeal. Evaluaron de manera subjetiva las características y la naturaleza de la ventilación, al igual que la presión máxima de insuflación. Este estudio demostró que los clínicos percibieron que la calidad de la ventilación era superior con el uso de la máscara laríngea Supreme. Jagannathan et al.46 evaluaron la tasa de éxito con la inserción al primer intento en un estudio observacional con 100 niños. Utilizaron los tamaños 1.0, 2.0 y 3.0 de la máscara laríngea Supreme. Se logró la inserción exitosa en el 100% de los casos, con una tasa de éxito al primer intento del 97%.
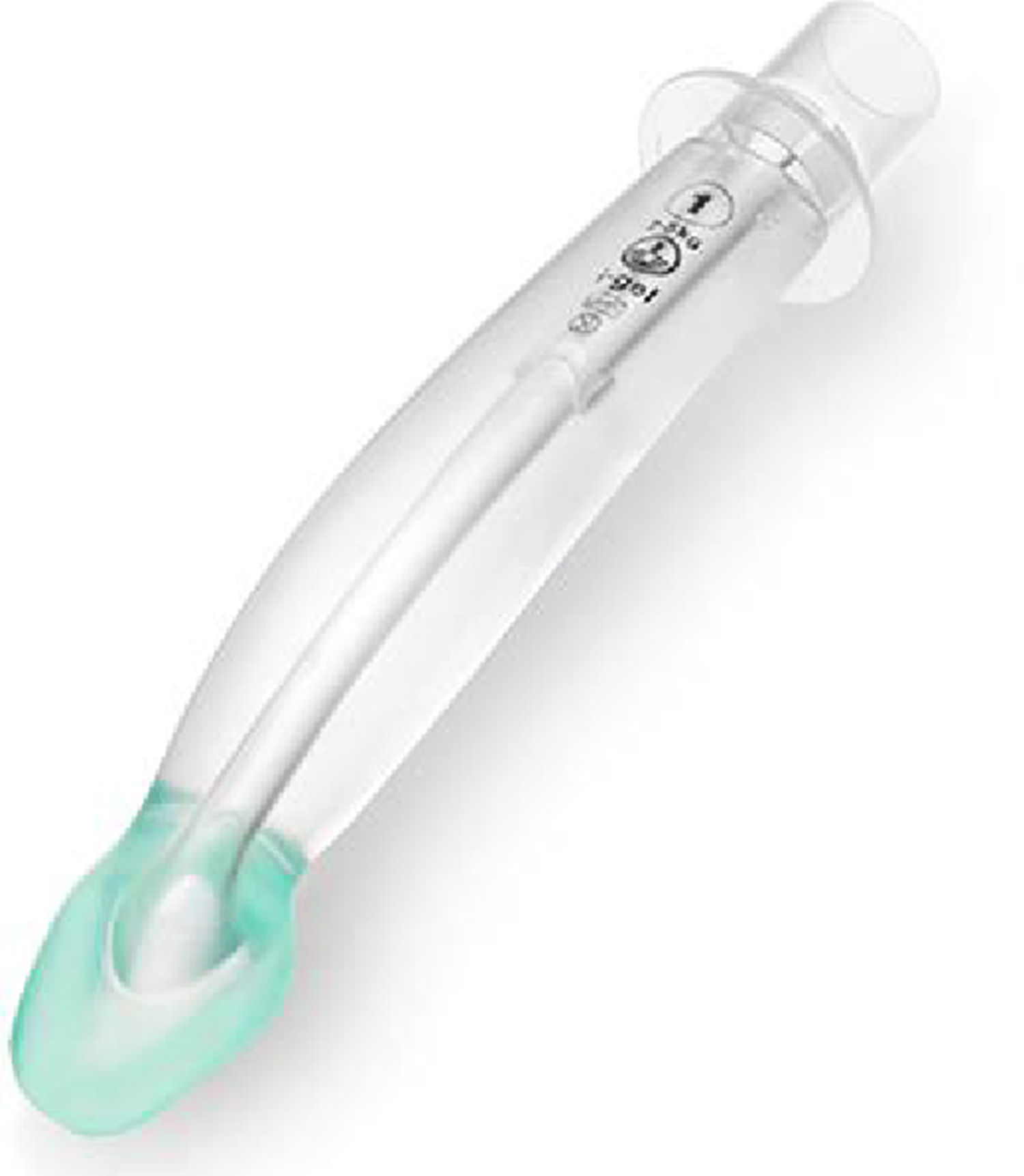
i-Gel™La i-Gel (fig. 7) es un dispositivo supraglótico sin balón, hecho de gel elastomérico (estireno-etileno-butadieno-estireno). Su forma se parece a la de la máscara laríngea ProSeal inflada. Tiene un tubo corto de calibre ancho para la vía aérea, sin rejillas, un vástago de forma elíptica, un recipiente de forma «anatómica», un bloque de mordida incorporado, y un canal de acceso gástrico en todos los tamaños salvo el 1. Estas características hacen que haya poca resistencia al flujo del gas, estabilidad, mejor sello de la faringe y un conducto adecuado para la intubación traqueal. El gel elastomérico se calienta a la temperatura del cuerpo, mejorando el sello de la máscara alrededor de la vía aérea. La máscara i-Gel se incorporó a la práctica de anestesia pediátrica en 200919.
Hay muchas descripciones publicadas del uso de la i-Gel en pacientes pediátricos con estudios observacionales, ensayos aleatorizados controlados y metaanálisis en los cuales se ha evaluado su desempeño46-50.
Dos estudios51,52 en los cuales se comparó la máscara laríngea clásica con la i-Gel concluyeron que, especialmente en la población de lactantes, el tiempo requerido para la inserción fue menor en el caso de la i-Gel que en el de la clásica. Se ha reportado que en este grupo en particular hay riesgo de movimiento y desplazamiento del dispositivo supraglótico.
El tubo de forma elíptica se diseñó para mejorar la estabilidad y prevenir la rotación. Sin embargo, Jagannathan et al. reportaron que en caso de necesitar ajustar la i-Gel para garantizar la permeabilidad de la vía aérea, en particular en los niños más pequeños, era útil y recomendable fijar con cinta a los dos maxilares en este grupo de edad a fin de prevenir mayor movimiento del dispositivo46.
La i-Gel podría ser más fácil de usar porque se inserta rápidamente sin necesidad de inflar el balón, y su perfil de ventilación y seguridad es semejante al de la máscara laríngea clásica pero en un dispositivo desechable. Su diseño y sus características de funcionamiento hacen de esta máscara laríngea una alternativa frente a la clásica. Con la i-Gel se facilitan el rescate de la vía aérea y la intubación guiada por fibra óptica53.
Ha habido 2 metaanálisis recientes42,54 en los cuales se incluyeron 9 ensayos aleatorizados controlados en los que se comparó la máscara laríngea i-Gel con otros dispositivos supraglóticos para vía aérea en pediatría. La conclusión de estos metaanálisis fue que la i-Gel no solamente tenía presiones más altas de fuga de la vía aérea comparada con otros dispositivos supraglóticos, sino que permitía mejor visualización con fibra óptica. Sin embargo, no se encontró diferencia con respecto a la tasa de éxito de la inserción y la tasa de complicaciones.
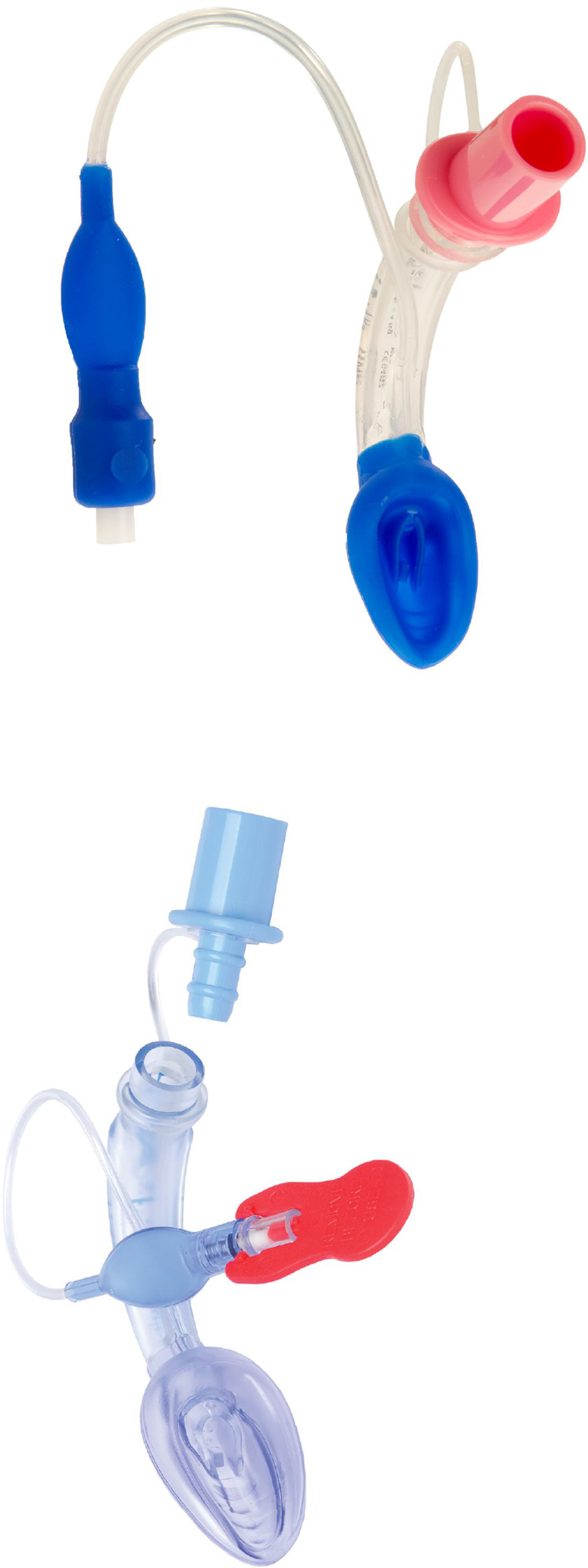
Air-Q™La vía aérea Air-Q (fig. 8) salió al mercado en el Reino Unido en 2012. Este dispositivo supraglótico consta de una máscara ovalada y un tubo curvo y corto para la vía aérea. También tiene un orificio diseñado para prevenir el plegamiento de la epiglotis19.
La Air-Q viene en 3 versiones producidas para varios usos o para un solo uso:
- 1.
Estándar - con balón.
- 2.
Autopresurizada (Air-Q; sin balón inflable).
- 3.
Air-Q con bloqueador esofágico. Este dispositivo tiene un canal gástrico pero no viene en tamaños pediátricos.
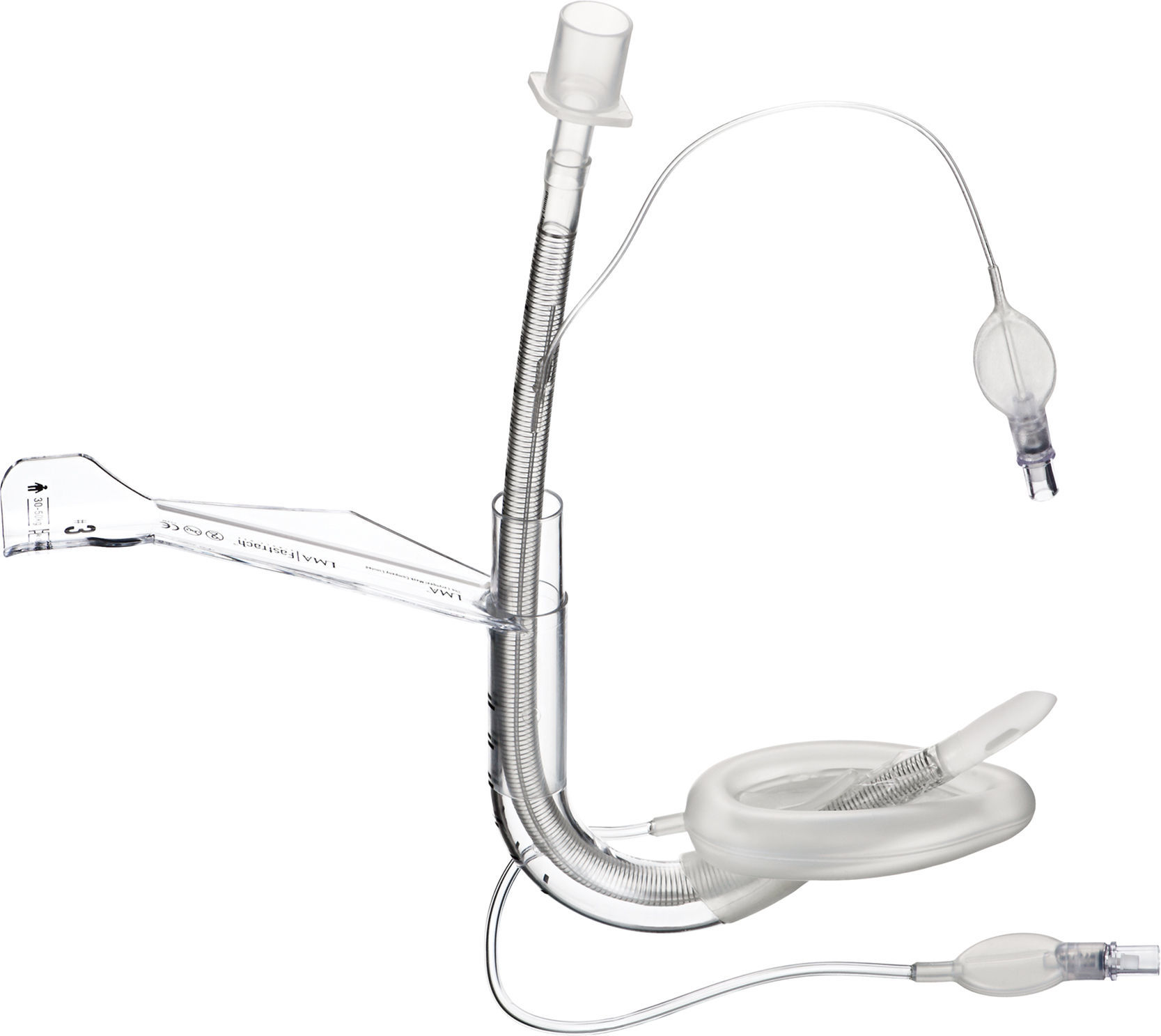
Una de las características principales de la Air-Q (fig. 8) es su tubo para la vía aérea, el cual es más ancho y corto. Estas características pueden facilitar el paso de tubos endotraqueales con balón a través de este dispositivo tanto en lactantes como en niños. La Air-Q se puede retirar de manera segura después de intubar46,55-57.
Jagannathan et al. concluyeron, después de una serie de casos de niños con vía aérea difícil prevista debido a anomalías craneofaciales y apertura reducida de la boca, que la ventilación con la Air-Q fue satisfactoria incluso cuando se utilizaron tamaños más pequeños, y que el dispositivo también fue adecuado al intentar la intubación endotraqueal con el tubo del tamaño correcto57.
La Air-Q se ha utilizado para facilitar la oxigenación y al mismo tiempo facilitar la intubación guiada por fibrobroncoscopio en la vía aérea difícil tanto prevista como imprevista46.
En un estudio reciente en el que Jagannathan et al. compararon la Air-Q con la i-Gel58, la conclusión fue que los dos dispositivos supraglóticos podrían utilizarse de manera segura y efectiva como conductos para la intubación endotraqueal guiada por fibroscopio. También señalaron que la i-Gel de 1.5 fue el dispositivo supraglótico que presentó más movimiento y desplazamiento durante el estudio.
En una revisión sistemática para evaluar la eficacia de la Air-Q, Ahn et al.59 concluyeron que la Air-Q era más difícil de insertar que cualquiera de los otros dispositivos, pero que la visualización con el fibrobroncoscopio era mejor que con cualquier otro dispositivo supraglótico, mejorando las tasas de éxito de intubación a través de los dispositivos supraglóticos.
DiscusiónDesde que se diseñara y utilizara inicialmente la máscara laríngea clásica hace más de 35años, son muchos los dispositivos supraglóticos que se han desarrollado. Aunque en la actualidad hay muchos dispositivos disponibles para uso en pediatría, la decisión de cuál elegir en una determinada situación puede ser difícil. No existe el dispositivo perfecto que cumpla con todos los requisitos.
La máscara laríngea clásica es la que más se ha estudiado y la que cuenta con la base de evidencia más fuerte que demuestra que proporciona condiciones excelentes en la mayoría de las situaciones. Mientras se realiza un estudio grande, pensamos que en niños sanos sometidos a procedimientos en los cuales es apropiada la ventilación espontánea, la máscara laríngea clásica o su versión desechable puede ser el dispositivo de elección.
En cirugías otorrinolaringológica, odontológica, oftalmológica y algunos procedimientos de cabeza y cuello, la máscara laríngea flexible puede ser ventajosa, debido a su tubo de respiración flexible y reforzado.
Las máscaras laríngeas con puerto gástrico y presiones de fuga más altas, como es el caso de la ProSeal o la i-Gel, pueden ser las más apropiadas cuando se utiliza ventilación con presión positiva intermitente y en cirugía laparoscópica, si bien la base de evidencia es limitada.
En los casos de vía aérea difícil conocida, o en la situación de un dispositivo de rescate para una intubación fallida, la i-Gel al parecer permite una buena visualización a través del fibrobroncoscopio. La Air-Q también se diseñó para este propósito y permite el paso de un tubo endotraqueal de tamaño apropiado incluso con una Air-Q de menor tamaño. Además, puede ser más fácil de retirar una vez asegurada la vía aérea con un tubo endotraqueal.
Tanto la máscara laríngea clásica como los dispositivos más nuevos se han utilizado en medicina prehospitalaria y en situaciones de urgencia tales como paro cardiorrespiratorio. Todavía es insuficiente la evidencia para respaldar el uso de un determinado dispositivo por encima de otro. Las características del paciente, los requerimientos de la cirugía y la preferencia personal determinan la decisión sobre la utilización de un determinado dispositivo supraglótico.
A medida que se desarrollen nuevos dispositivos con una indicación clara de pertinencia clínica y ventajas genuinas se seguirá necesitando la investigación de alta calidad. Es solo tras una evaluación rigurosa de la seguridad y la eficacia que se podrá recomendar el uso generalizado de cualquier nuevo dispositivo supraglótico en anestesia pediátrica.
FinanciaciónNo se utilizó financiación.
Conflicto de interesesNo hay conflicto de interés.