La espasticidad es desencadenada por una alteración en el sistema nervioso central; puede presentarse de manera local o generalizada. La severidad de los síntomas —entre ellos, limitación funcional, deformidad, dolor, trastorno del sueño, depresión y múltiples incapacidades— depende de las zonas comprometidas. El tratamiento de la enfermedad se basa en la terapia física y es complementado con correctores de postura, algunas intervenciones quirúrgicas y terapia farmacológica. El baclofeno es un medicamento útil en esta patología. La vía de administración inicial siempre es oral, sin embargo por su baja biodisponibilidad o mala tolerancia en algunos pacientes se requiere la vía intratecal.
ObjetivoEl objetivo del presente artículo es presentar una revisión de la literatura aprovechando el reporte de un caso de una paciente con diagnóstico de tetraparesia espástica que recibió tratamiento con baclofeno intratecal mediante la implantación de una bomba de terapia intratecal (BTI).
Métodos y materialesSe realizó una búsqueda en las bases de datos EBSCO, MEDLINE y OVID, que incluyó artículos de revisiones sistemáticas, ensayos clínicos, revisiones narrativas y series de casos, entre 1995 y 2012, para la realización de una revisión narrativa no sistemática y reporte de un caso.
ResultadosSe tuvieron en cuenta un total de 35artículos para la realización de la actualización en el tema propuesto.
ConclusionesEl uso del baclofeno mediante la implantación de BTI es una alternativa eficaz y segura para el tratamiento de los pacientes con espasticidad severa y refractaria al tratamiento oral convencional.
Spasticity is triggered by a central nervous system disorder and may be local or generalized. The severity of symptoms, including functional limitation, deformity, pain, sleep disorders, depression and multiple disabilities, depends on the areas involved. The treatment of the disease is based on physical therapy and complemented with posture correcting devices, a few surgical interventions and drug therapy. Baclofen is a useful drug for this pathology and is usually administered orally; however, due to its low bioavailability or poor tolerance some patients require intrathecal administration.
ObjectiveThe purpose of this article is to present a literature review based on a case report of a patient with a diagnosis of spastic tetraparesis, receiving intrathecal baclofen treatment through an implantable intrathecal therapy pump (ITP).
Methods and materialsA database search was conducted in EBSCO, MEDLINE and OVID that included systematic review articles, clinical trials, narrative reviews and case series between 1995 and 2012, for a non-systematic narrative review and a case report.
Results35 articles were considered in total for an update on the topic suggested.
ConclusionsBaclofen use through an implanted ITP is an effective and safe option for treating patients with severe spasticity refractory to conventional oral therapy.
La espasticidad se define como un trastorno motor caracterizado por un aumento del tono muscular dependiente de la velocidad, con reflejos de estiramiento exagerados, como un componente del síndrome de neurona motora superior1. En Estados Unidos se presenta en la mitad de los pacientes con esclerosis múltiple, parálisis cerebral, accidente cerebrovascular, traumatismo encefálico o lesión medular. La espasticidad severa puede asociarse con gran limitación funcional, deformidad, dolor, síntomas depresivos, alteraciones del sueño, empeoramiento de la calidad de vida e incapacidades prolongadas2.
Puede ser una característica de algún trastorno que afecte al tracto corticoespinal, lo cual puede ocurrir en muchas enfermedades del sistema nervioso central. Puede ser focal o generalizada, dependiendo de la localización y de la extensión de la lesión neurológica responsable. Dicha extensión va a determinar el grado de limitación funcional, y la intensidad del dolor dependerá de la severidad de la espasticidad3.
El diagnóstico es clínico, apoyado en escalas de medición, como la de Ashworth (0: no hay aumento del tono; 1: leve aumento del tono; 2: mayor aumento del tono muscular, pero la extremidad se deja flexionar fácilmente; 3: tono muscular aumentado, dificultad para la movilización pasiva; 4: rigidez completa de la extremidad, en flexión o extensión), la de Penn (0: ningún espasmo; 1: leve espasmo con la estimulación; 2: espasmos fuertes irregulares, menores de uno por hora; 3: más de un espasmo por hora; 4: más de 10 espasmos por hora) o la de Tardieu4 y pruebas funcionales, como por ejemplo la medida de independencia funcional para niños conocida como WeeFIM5. Sin embargo, se debe tratar de encontrar la causa de base. El tratamiento implica mejorar la actividad funcional, la movilidad y el alivio del dolor. Se logra mediante la terapia física, el uso de correctores de posturas, procedimientos quirúrgicos y terapia farmacológica6.
El baclofeno es el fármaco más ampliamente empleado para el tratamiento de la espasticidad; es un agonista del receptor de ácido gamma-aminobutírico (GABA) en la médula espinal, aprobado por la FDA. Disminuye la liberación de neurotransmisores excitatorios con la consecuente disminución de los reflejos medulares. Controla la espasticidad en el 70 al 87% de los pacientes y disminuye la frecuencia de espasmos durante el día. La vía de administración de elección es la oral, sin embargo su biodisponibilidad es baja, por lo que algunos pacientes presentan poca respuesta o mala tolerancia, lo que obliga a utilizar la ruta intratecal, que logra una concentración en el sitio efector 100veces mayor que la oral. El baclofeno intratecal tiene una vida media de 6h, y por lo tanto su administración debe realizarse de manera continua. Por lo anterior, se utilizan las bombas de terapia intratecal (BTI)7.
El objetivo de este artículo es presentar una revisión de la literatura aprovechando el reporte de un caso de una paciente con diagnóstico de tetraparesia espástica que recibió tratamiento con baclofeno intratecal mediante la implantación de una BTI.
Caso clínicoMujer de 37años de edad con historia de espasticidad en hemicuerpo izquierdo de 22años de evolución y de etiología no filiada. Se inició en el pie izquierdo, con alteración para la marcha y caídas múltiples, con progresión ascendente solo hasta la rodilla. En los últimos 6años se reactivó la espasticidad, con compromiso del miembro superior izquierdo (codo y mano) y articulación temporomandibular.
Fue evaluada por múltiples especialistas, incluyendo neurología, neurocirugía, neuropsicología, junta médica de neurología, junta médica de movimientos anormales y, finalmente, junta médica de dolor.
Se le realizaron múltiples exámenes de laboratorio, que incluyeron citoquímica de líquido cefalorraquídeo, resonancia total de columna simple y contrastada, resonancia cerebral, niveles séricos de vitamina B12, ácido fólico, VDRL, anticuerpos antinucleares, VIH, HTLV-1, y todos fueron normales. Nunca se encontró una causa clara de su espasticidad; por lo tanto, el tratamiento recibido se dirigió a controlar la rigidez, disminuir la frecuencia de los espasmos y controlar el dolor.
Recibió múltiples tratamientos con ácido valproico, duloxetina, gabapentina, tizanidina, toxina botulínica, clonazepam, pregabalina, tramadol, hidrocodona, oxicodona y baclofeno oral con dosis iniciales de 10mg cada 12h con incrementos semanales de 10mg, hasta llegar a una dosis de 80mg diarios, sin lograr el control de los síntomas.
En los últimos 6meses de su enfermedad la paciente presentó un franco deterioro, con compromiso de las 4extremidades que le impide la deambulación; precisa silla de ruedas y posteriormente termina encamada dada la severidad de la espasticidad, que le impide sentarse en la silla. Hay pérdida del control de los esfínteres, empeoramiento de los síntomas depresivos y aumento en la intensidad del dolor. La espasticidad era la causa de la limitación funcional y del dolor. Fue hospitalizada en una institución de cuarto nivel, donde fue evaluada por la junta médica de dolor, y se le propuso tratamiento con baclofeno intratecal.
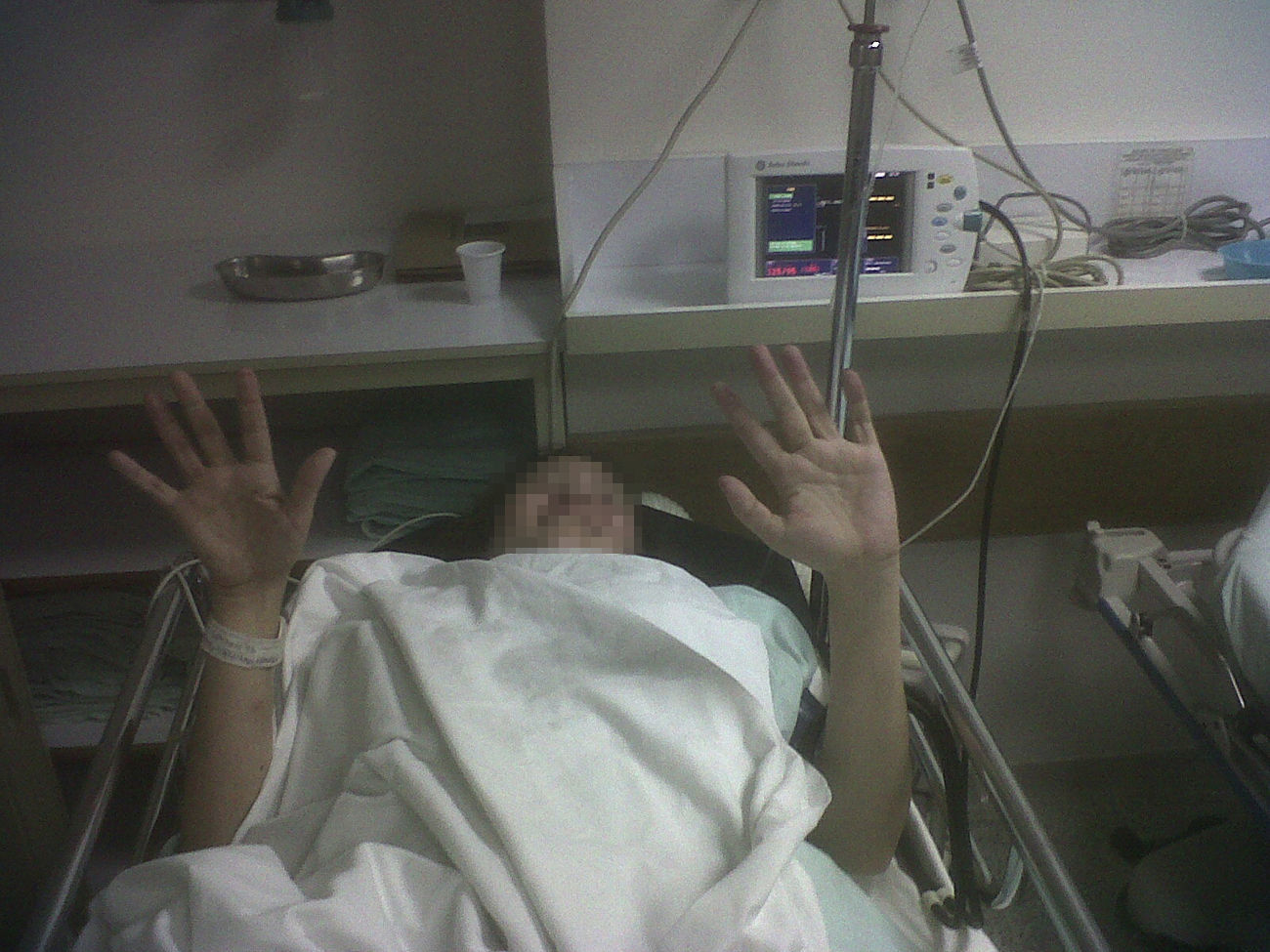
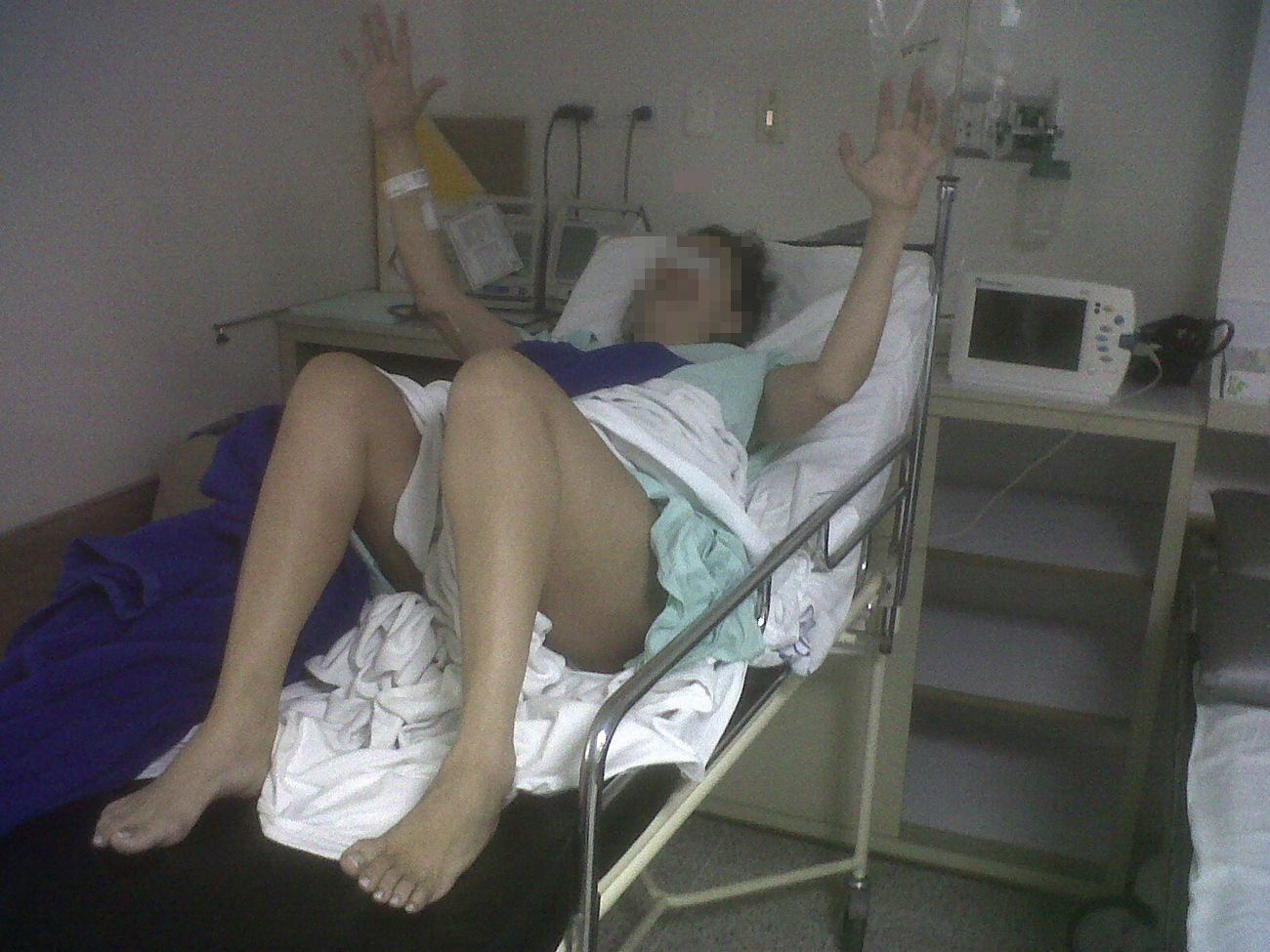
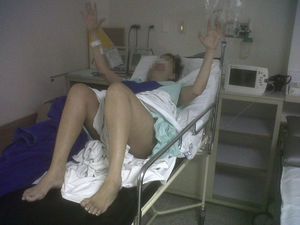
El protocolo realizado comenzó con las sesiones de dosis de prueba. La primera dosis recibida fue de 50μg de baclofeno intratecal, con la que se obtuvo mejoría de 2puntos en la escala Ashworth, principalmente en las manos y el miembro inferior derecho (fig. 1). La segunda dosis se le realizó 24h después. Se le administraron 75μg, con una mejoría de 4puntos en la escala de Ashworth en ambas extremidades derechas, 3puntos en el miembro superior izquierdo y 2puntos en el miembro inferior izquierdo. Incluso se logró sentar a la paciente, luego de haber estado acostada en cama durante 3meses (fig. 2). También recuperó el control de los esfínteres. Ambas dosis de prueba se realizaron en decúbito lateral derecho, a nivel de L3-L4, técnicamente difíciles por las características clínicas de la paciente. No se presentaron efectos adversos.
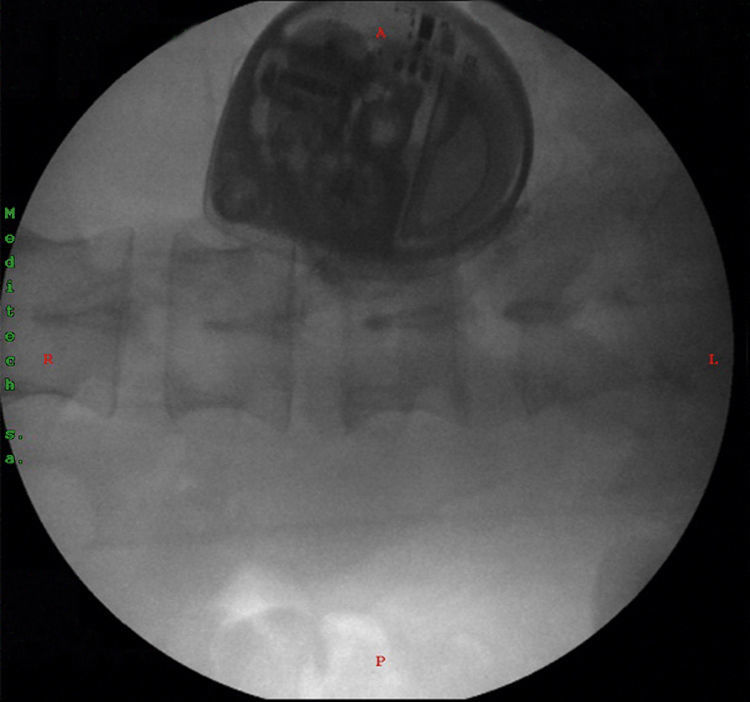
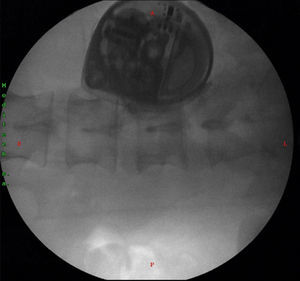
No hubo necesidad de realizar más pruebas y se programó para la inserción definitiva de la BTI, la cual se realizó bajo anestesia general, en decúbito lateral izquierdo. Se realizó un abordaje del espacio L3-L4 guiado por fluoroscopia, se encontró retorno de líquido cefalorraquídeo, se avanzó el catéter intratecal hasta la región de T1-T2, donde se dejó definitivamente. Posteriormente se tunelizó el catéter desde la región lumbar hasta la región abdominal paraumbilical derecha, donde se realizó el bolsillo para el implante definitivo de la bomba (fig. 3).
Se implantó una bomba (Synchromed II, Medtronic®), se llenó con una ampolla de baclofeno de 10mg en 20ml (Lioresal®, Novartis Farmacéutica) y se programó en modo simple continuo para pasar a una velocidad de 50μg diarios.
El procedimiento fue ambulatorio, con una duración de 90min y una recuperación de 2h. Se suspendió el baclofeno oral, y el resto de medicamentos se continuaron en iguales dosis. Se realizó una evaluación a las 24h, en la que la paciente ya presentaba una mejoría parcial de sus síntomas. Se realizó una segunda evaluación a las 72h, y en ella la paciente ingresó caminando al consultorio, con una mejoría significativa de la espasticidad, disminución de la frecuencia de espasmos (un punto en la escala de Penn) y disminución de la intensidad del dolor. Se inició fisioterapia intensiva durante las primeras 4semanas. Se realizaron evaluaciones cada semana durante un mes, cada mes durante 3meses y cada 3meses durante un año (fig. 4).
Las dosis de baclofeno permanecieron estables; solo requirió aumento de 50 a 60μg el primer mes y de 60 a 75μg el sexto mes.
El único efecto adverso observado fue un aumento de la espasticidad en el sexto mes, secundaria a una infección urinaria, que necesitó un reajuste de la dosis y tratamiento antibiótico durante 10días, después de los cuales recuperó de nuevo su estado funcional.
En cuanto al tratamiento analgésico, se desmontó la oxicodona y se realizó rotación a hidrocodona. La pregabalina permaneció con dosis de 75mg cada 8h.
La calidad del sueño mejoró, con lo que se logró suspender el clonazepam.
La calidad de vida mejoró hasta el punto de poder retornar a la universidad para continuar sus estudios.
DiscusiónLa espasticidad es una alteración motora caracterizada por aumento de la resistencia pasiva muscular al estiramiento seguido por incremento del tono muscular, incremento que depende de la velocidad del estiramiento. Se acompaña de hiperreflexia y un grado variable de debilidad muscular. El tono muscular es controlado por vías motoras descendentes. Es el resultado de un balance entre vías facilitadoras sobre el tono extensor, mediado por el tracto reticuloespinal medial y vestibuloespinal medial, y efectos inhibitorios mediados por el tracto reticuloespinal dorsal. Cuando este último se encuentra alterado se da la espasticidad. Adicionalmente se presentan cambios en la configuración del sistema nervioso central que explican otros hallazgos clínicos8.
Para el manejo de la espasticidad existen múltiples opciones terapéuticas por vía oral9:
Dantroleno. Actúa directamente en el músculo esquelético bloqueando la contracción por inhibición de la liberación de calcio del retículo endoplásmico, con la dificultad que puede desencadenar una hepatotoxicidad grave10. Se inicia con una dosis de 25 a 50mg diarios y se incrementa 25mg cada 4días hasta una dosis máxima de 400mg diarios. No se encuentra disponible en Colombia.
Ciproheptadina. Inhibe la liberación de acetilcolina, de histamina y principalmente de la serotonina, en diferentes regiones del sistema nervioso central. Se inicia con una dosis de 4mg y se aumenta cada 5días hasta una dosis máxima de 16mg diarios. Se puede utilizar para el tratamiento del síndrome de abstinencia por baclofeno11.
Benzodiacepinas. La más utilizada es el diazepam. Actúan en los receptores GABAA aumentando el influjo de calcio a la neurona, hiperpolarizándola e inhibiendo la actividad aferente motora. Por sus efectos adversos, principalmente la somnolencia, no se consideran terapia de primera elección. Para el tratamiento de los espasmos nocturnos también se ha utilizado el clonazepam12.
Canabinoides. Actúan en los receptores CB1 y CB2, y además, en los receptores de N-metil-D-aspartato (NMDA). Se han utilizado el dronabinol y la nabilona en pacientes con esclerosis múltiple. El dronabinol se inicia con una dosis de 2,5 a 5mg diarios, con incrementos cada 5días hasta una dosis máxima de 20mg13,14.
Glicina. Es uno de los aminoácidos inhibitorios más abundantes en la médula espinal. La treonina en dosis entre 6 a 7,5g diarios ha demostrado disminuir el tono muscular en pacientes con esclerosis múltiple y trauma medular.
Alfa-2 adrenérgicos. Se ha demostrado que la clonidina inhibe la liberación del glutamato y disminuye la espasticidad por inhibición presináptica de los receptores alfa-2 en vías aferentes.
Tizanidina. Inhibe la liberación de neurotransmisores excitatorios y facilita la acción de la glicina. Se ha demostrado su eficacia en pacientes con esclerosis múltiple, infarto cerebral, trauma raquimedular y trauma encefálico15.
4-aminopiridina. Inhibe los canales de potasio en áreas desmielinizadas en pacientes con esclerosis múltiple y mejora la actividad cortical central y espinal en pacientes con trauma espinal. Puede producir trombocitopenia, convulsiones, vasoespasmo arterial distal, fallo hepático, náuseas y mareo.
Otras terapias. Se han utilizado otros medicamentos para disminuir los espasmos, con resultados variables: piracetam, progabide e ivermectina. Ensayos clínicos aleatorizados han demostrado beneficio con la gabapentina en dosis entre 1.200 y 2.700mg diarios16.
La paciente del presente caso había recibido tizanidina, gabapentina y diazepam, con efectividad parcial. El último año recibió clonazepam por el aumento de los espasmos nocturnos. Finalmente se inició un esquema de baclofeno oral, con una dosis máxima de 80mg diarios, con mala respuesta.
Además del tratamiento de la espasticidad, se debe realizar control del dolor crónico. El dolor en pacientes con espasticidad es tratado con terapia física de base y una variedad de alternativas farmacológicas, cuya elección depende de la enfermedad desencadenante, de la severidad y del número de extremidades afectadas. Cuando la espasticidad es focal, las inyecciones de toxina botulínica suelen ser efectivas, especialmente en pacientes con diagnóstico de esclerosis múltiple o en espasticidad posterior a enfermedad cerebrovascular17,18. En la espasticidad focal también se han usado los bloqueos de nervio periférico con sustancias neurolíticas como alcohol19 o fenol en concentraciones menores al 5% para evitar un daño nervioso definitivo, con mejoría por periodos de 3 a 6meses20. Estos bloqueos tienen mayor éxito y seguridad cuando son guiados por electromiografía o ultrasonografía21,22.
Si el compromiso es generalizado se recomiendan terapias sistémicas, entre ellas nuevamente las benzodiacepinas (diazepam, clonazepam), con efectos adicionales como sedación, somnolencia y riesgo de adicción, y los alfa-2 agonistas (clonidina, tizanidina), con la posibilidad de generar hipotensión, somnolencia y constipación. Los canabinoides también han demostrado beneficio como antiespasmódico y analgésico, pero con múltiples efectos adversos23. También hay reportes del uso de fenol en concentración neurolítica en bloqueos nerviosos. Para el tratamiento del dolor severo se pueden utilizar opiáceos fuertes24.
El medicamento más ampliamente utilizado en pacientes con espasticidad es el baclofeno. Se indica en pacientes con esclerosis múltiple, trauma de cráneo, lesión medular y distonías25. En niños se ha reportado ampliamente su utilidad en alteraciones neurológicas postraumáticas y parálisis cerebral26,27.
El baclofeno tiene baja liposolubilidad, lo que disminuye su biodisponibilidad cuando es administrado por vía oral y tiene una baja capacidad para cruzar la barrera hematoencefálica. La vida media con dosis únicas intratecales es corta, por lo que se requiere su administración de forma continua mediante la implantación de un catéter en el espacio subaracnoideo espinal, conectado a una bomba de infusión continua implantada en el abdomen y con control externo del software28.
El baclofeno oral es efectivo en el 55 al 96% de los pacientes. La incidencia de efectos adversos es del 10 al 75%. Los más comunes son somnolencia, debilidad excesiva, vértigo, alteraciones psicológicas, cefalea, náuseas, vómito, astenia, depresión, diarrea e hipotensión. El principal riesgo del tratamiento oral es el síndrome de abstinencia que produce convulsiones, alteraciones psiquiátricas e hipertermia. En casos severos puede producir rabdomiólisis e incluso la muerte29. El mayor efecto adverso referido por la paciente fue la somnolencia y las alteraciones psicológicas. Debido a su ineficacia clínica, se inició tratamiento a través de la ruta intratecal.
El baclofeno intratecal actúa por medio de los receptores GABAB de la médula espinal; fue aprobado en Estado Unidos para uso subaracnoideo en pacientes con espasticidad de origen espinal en 1992, y para espasticidad de origen cerebral en 1996. Está indicado en pacientes que no responden al tratamiento con baclofeno oral o que presentan efectos adversos no tolerables.
Una revisión sistemática publicada en la base de datos Cochrane apoya la efectividad del baclofeno intratecal en pacientes con espasticidad y la baja respuesta terapéutica con la tizanidina30.
Para la administración continua de medicamentos intratecales se utilizan, desde hace más de 20años, las BTI. Permiten una dosificación continua de medicamentos para el tratamiento de la espasticidad, el dolor crónico benigno y el dolor en el cáncer31.
El baclofeno intratecal se indica en pacientes que respondan favorablemente a las dosis de pruebas. En la paciente del presente caso se realizaron únicamente 2pruebas, debido a la mejoría tan significativa de la espasticidad. La dosis de prueba usualmente está en el rango de 25 a 100μg en adultos y de 10 a 50μg en niños, administrada en dosis única o en infusión continua mediante punción lumbar. El test con infusión continua precisa de la colocación de un catéter intratecal y una bomba externa, de manera que se modifica la dosis de manera más precisa y puede dejarse hasta un tiempo aproximado de 7días, durante los cuales podemos modificar la dosis y comprobar su efectividad.
Las BTI deben ser implantadas en un quirófano con todas las técnicas de asepsia. La bomba es colocada en el tejido subcutáneo en la pared abdominal en adultos y subfacial en los niños, con el paciente en decúbito lateral. El uso del fluoroscopio puede ayudar a controlar el sitio exacto de colocación de la punta del catéter, que varía según el sitio anatómico comprometido. En pacientes con tetraparesia la punta del catéter debe ubicarse en la región cervicotorácica, tal y como se utilizó en la paciente.
La infusión del baclofeno puede ser en bolos, en infusión continua o una combinación de ambas. El seguimiento debe realizarse de manera periódica para poder establecer la dosis requerida, de acuerdo con la evaluación clínica de las escalas de espasticidad. La frecuencia de las recargas es determinada por la dosis y la concentración del medicamento; en promedio es cada 3meses, máximo cada 6meses.
Las complicaciones con la implantación de la bomba son más frecuentes en los niños, tales como formación de seromas, hematomas, infección, rotura de la bomba o del catéter, migración o fractura del catéter y formación de pseudomeningocele. El mal funcionamiento de la bomba o el retardo en la recarga puede llevar a un síndrome de abstinencia, produciendo síntomas potencialmente peligrosos como disfunción respiratoria, rabdomiólisis, hipertensión o hipotensión y alteraciones de la coagulación. Se pueden producir granulomas en la punta del catéter, ocurriendo más comúnmente con otros medicamentos32,33. Un estudio retrospectivo en 126pacientes con terapia intratecal con baclofeno observó una prevalencia de delirio en el 9,5% de la muestra; de este 9,5%, el delirio era secundario a intoxicación en el 66,6% y a abstinencia en el 33,3%. Ningún paciente falleció como consecuencia de efectos adversos neurológicos34. En un año de seguimiento, la paciente no presentó complicaciones neurológicas.
La tolerancia al baclofeno se observa en el 15 al 20% de los pacientes durante los primeros 12meses de implantada la BTI. Heetla et al.35 realizaron un seguimiento a 10años en 37pacientes con terapia intratecal. Todos requirieron aumento en la dosis de baclofeno durante los primeros 18meses, y se mantuvieron con una dosis promedio de 350μg diarios. El 22% de los pacientes desarrollaron tolerancia, definida como un aumento de la dosis mayor de 100μg por año. La paciente presentada comenzó con una dosis de 50μg durante 4semanas, al cabo de las cuales requirió un aumento a 60μg. Permaneció con esta dosis durante 6meses, se aumentó a 75μg y permaneció con la dosis estable durante el primer año.
ConclusionesEl uso del baclofeno mediante la implantación de bombas de terapia intratecal es una alternativa eficaz y segura para el tratamiento de los pacientes con espasticidad severa y refractaria al tratamiento oral convencional, y logra mejorar de manera significativa la calidad de vida.
FinanciaciónLa financiación de esta revisión es con recursos propios y con la asesoría de la Universidad CES, Medellín, Colombia.
Conflicto de interesesLos autores declaran que no existe ningún conflicto de intereses.