El desarrollo de técnicas para la realización de una traqueostomía percutánea por dilatación (TPD) ha facilitado su implementación en las unidades de cuidados intensivos (UCI).
ObjetivoDescribir las complicaciones tempranas intra y postoperatorias en pacientes de cuidados intensivos que requirieron traqueostomía percutánea por dilatación utilizando la técnica Ciaglia Blue Rhino y que se realizaron sin la asistencia de fibrobroncoscopio.
Pacientes y métodosSe revisaron de forma retrospectiva los registros cínicos de 80 pacientes durante un periodo de 3 años. Se registraron las variables demográficas, de severidad, días de ventilación mecánica antes del procedimiento y las complicaciones intraoperatorias y postoperatorias tempranas.
ResultadosSe incluyeron 80 pacientes con una edad media de 61,5 (15-89) años (29 mujeres). La media de puntuación APACHEII fue 17,9. Los pacientes requirieron en promedio 11,6 días de ventilación mecánica antes de la TPD. El 11,6% presentó complicaciones intraoperatorias y el 9,1% complicaciones postoperatorias tempranas. En 2 pacientes se puncionó accidentalmente el tubo endotraqueal y 3 pacientes presentaron sangrado autolimitado del sitio de traqueostomía. Ninguna de las complicaciones representó un riesgo vital para los pacientes.
ConclusionesLa TPD mediante la técnica Ciaglia Blue Rhino sin la asistencia de fibrobroncoscopio es un procedimiento con baja incidencia de complicaciones.
The development of percutaneous dilatational tracheostomy techniques (PDT) has facilitated the procedure in Intensive Care Units (ICU).
ObjectiveTo describe the early intra and post-operative complications in ICU patients requiring percutaneous dilatational tracheostomy using the Ciaglia Blue Rhino technique, without fiber optic bronchoscopy.
Patients and methodsWe collected data from eighty ICU patients during three years. The demographic variables were recorded, in addition to severity, number of days in mechanical ventilation prior to the procedure and intraoperative as well as early postoperative complications.
ResultsEighty patients included, mean age 61.5 (15-89) years old (29 females). The mean APACHE II score was 17.9. In average, the patients required 11.6 days of mechanical ventilation prior to the PDT. 11.6% had intraoperative complications and 9.1% experienced early postoperative complications. In two patients the endotracheal tube was accidentally punctured and three patients had self-limiting bleeding at the tracheostomy site. None of the complications was life-threatening to the patients.
ConclusionsPDT using the Ciaglia Blue Rhino technique, without fiber optic bronchoscope is a procedure with low incidence of complications.
La traqueostomía es un procedimiento frecuente en las unidades de cuidados intensivos (UCI) indicado en el tratamiento del paciente críticamente enfermo que requiere ventilación mecánica de forma prolongada1.
La traqueostomía percutánea por dilatación (TPD) fue introducida en 1985 y desde entonces ha sufrido varias modificaciones. Actualmente se describen 3 técnicas para su realización: la técnica Ciaglia (y su modificación Blue Rhino), la técnica Griggs y la técnica Howard Kelly modificada2-7.
En los últimos años, la TPD ha ganado amplia aceptación. Es un procedimiento mínimamente invasivo que aporta numerosas ventajas entre las que destacan el presentar un alto grado de seguridad, ser una técnica de fácil realización y aprendizaje, presentar menor tamaño de la incisión cutánea limitando daño de los tejidos, bajo riesgo de sangrado, tiempo quirúrgico corto, bajos costos y que no precisa traslado a quirófano por lo que disminuye la morbilidad derivada del transporte a salas de cirugía (en caso de traqueostomía abierta)3,8-11.
La TPD tiene algunas limitaciones y riesgos, entre ellos la decanulación y la obstrucción de la vía aérea, la canulación traqueal a ciegas, sangrado perioperatorio, infecciones, estenosis traqueal, neumotórax, perforación esofágica, enfisema subcutáneo y fractura del anillo traqueal12.
El objetivo del presente estudio, fue determinar las complicaciones intra y postoperatorias tempranas en pacientes de cuidado intensivo que requirieron TPD utilizando la técnica Ciaglia Blue Rhino y que se realizaron sin la asistencia de fibrobroncoscopio.
Pacientes y métodosMediante un diseño observacional-retrospectivo y tras aprobación del comité de ética institucional, se revisaron los registros de todos los pacientes médicos o quirúrgicos ingresados a la UCI de la Clínica La Estancia de la ciudad de Popayán (Colombia), a los que se les realizó TPD durante un periodo de 3 años (diciembre de 2006 a diciembre de 2009). Fueron excluidos los menores de 18 años y los pacientes con alguna distorsión de la anatomía cervical o infección de tejidos cervicales. Este grupo de pacientes se llevaba a traqueostomía abierta de forma convencional.
Todas las TPD fueron electivas y se realizaron por el equipo de la UCI de manera estandarizada de acuerdo a un protocolo institucional y empleando el equipo Ciaglia Blue Rhino Percutaneous Tracheostomy Introducer set (Cook Critical Care, Bloomington, IN, USA).
Técnica quirúrgicaEn primer lugar se verificaron todos los implementos requeridos para el procedimiento. Se evaluaron los signos vitales. Se optimizó la posición de tal manera que se expusieran con mayor facilidad las estructuras anatómicas cervicales. Se realizó asepsia del cuello, colocación de campos quirúrgicos y se proporcionó sedación y analgesia (fentanilo, remifentanilo, midazolam o propofol).
Tras la identificación por palpación del segundo anillo traqueal, se infiltró la piel suprayacente con lidocaína sin epinefrina al 2%. Bajo visión laringoscópica se retiró cuidadosamente el tubo orotraqueal hasta visualizar el balón traqueal en el estrecho glótico. La aguja introductora del catéter se ensambló en una jeringa de 10ml que contenía el anestésico local y se puncionó entre el primero y segundo anillo traqueal o entre el segundo y tercer anillo, de acuerdo a las facilidades anatómicas de cada caso y en forma perpendicular hasta obtener pérdida de la resistencia. Se aspiró con la jeringa confirmando la extracción de aire, lo cual es indicativo de la presencia de la punta en la luz traqueal. Al alcanzar esta posición, se avanzó un catéter de polivinilo en un ángulo de 45° caudal y se retiró la jeringa y la aguja metálica. A través del catéter se pasó la guía de alambre con punta en J atraumática y se retiró el catéter dejando la guía en posición.
A cada lado de la guía metálica se realizó una incisión transversal de 0,5cm de longitud que comprometía piel y tejido celular subcutáneo (esta es una modificación propia de nuestro servicio con la cual hemos observado menor trauma de incisión para la inserción; primero se realiza la punción luego la incisión). Posteriormente se pasó el primer dilatador corto hasta que se deslizó fácilmente y luego se retiró dejando la guía de alambre adentro. A continuación se avanzó la guía blanca del catéter sobre la de alambre hasta que sus extremos coincidían con las marcas distal y proximal. Sobre las dos guías se pasó el dilatador único hasta que el extremo proximal coincidió con la marca de la guía del catéter en una inclinación de 45° respecto a la piel y en dirección caudal. Se introdujo el dilatador con movimientos firmes y avanzando un poco cada vez hasta que se llegó a la marca de posicionamiento del dilatador (línea negra). La ventilación mecánica se suspendía cuando el dilatador entraba en la luz traqueal.
En ese momento se retiró el dilatador y se introdujo la cánula de traqueostomía lubricada, ensamblada y con el balón desinflado en el cargador sobre los catéteres guía. Finalmente se retiró el catéter cargador y las 2 guías (del catéter dilatador y de alambre), se fijó la cánula con puntos a la piel y con la cinta de tela alrededor del cuello y se reinició el proceso de ventilación. A todos los pacientes se les tomó una radiografía del tórax de control.
La técnica en detalle puede ser apreciada en el enlace web «Traqueostomía Percutánea en Cuidado Intensivo»13.
Recolección y análisis de la informaciónPara la recolección de la información se utilizó un formato que incluía las variables edad, sexo, diagnóstico de ingreso a la UCI, APACHEII, diagnóstico para la realización de la TPD, modo de ventilación mecánica y parámetros al momento de realizar el procedimiento, tiempo de ventilación mecánica (VM) antes de la TPD, medicamentos utilizados para sedación, personal que realizó el procedimiento, complicaciones intraoperatorias y complicaciones postoperatorias. El tiempo de realización de la TPD se clasificó de acuerdo a lo reportado por otros autores como temprana (menor a 4 días desde la intubación orotraqueal) y tardía (mayor a 10 días)14.
Los datos se analizaron con el paquete estadístico SPSS versión 15.0 mediante estadística descriptiva (Statistical Package for the Social Sciences, Chicago, IL, USA). Las variables categóricas se presentan como proporciones y frecuencias. Las variables continuas se resumen con medias o medianas. La dispersión de los datos se cuantificó utilizando la desviación estándar o el rango intercuartílico (RIQ) dependiendo de cada distribución y su proximidad a la normalidad. Para explorar independencia entre algunas variables y el tiempo de realización del procedimiento se utilizó el test de χ2 y el test de Mann-Whitney para muestras independientes para variables categóricas y continuas, respectivamente. Se consideró como significante un valor de p inferior a 0,05.
ResultadosEl procedimiento TPD se realizó a un total de 80 pacientes durante el periodo en estudio. El 64% de ellos fueron hombres (n=51) y el 36% mujeres (n=29). La edad promedio fue de 61,5 años, con un rango comprendido entre 15 y 89 años.
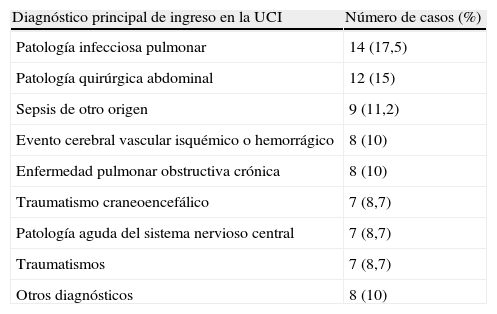
Las patologías por las cuales se ingresaron los pacientes a la UCI se detallan en la tabla 1. La media de la puntuación de severidad APACHE II al ingreso fue de 17,9 (DE=6,4; RIQ=14-21; recorrido=3-37). La indicación para la realización de la TPD fue ventilación mecánica prolongada en el 72% de los pacientes y secundaria a patología del sistema nervioso central o periférico en el 28%. Los pacientes permanecieron con intubación orotraqueal previa al procedimiento un promedio de 11,6 días (DE=7,1; RIQ=7,9-11).
Principales diagnósticos de ingreso en la UCI en pacientes que requirieron TPD (n=80)
| Diagnóstico principal de ingreso en la UCI | Número de casos (%) |
| Patología infecciosa pulmonar | 14 (17,5) |
| Patología quirúrgica abdominal | 12 (15) |
| Sepsis de otro origen | 9 (11,2) |
| Evento cerebral vascular isquémico o hemorrágico | 8 (10) |
| Enfermedad pulmonar obstructiva crónica | 8 (10) |
| Traumatismo craneoencefálico | 7 (8,7) |
| Patología aguda del sistema nervioso central | 7 (8,7) |
| Traumatismos | 7 (8,7) |
| Otros diagnósticos | 8 (10) |
Fuente: autor.
La TPD se realizó de forma temprana (menor a 4 días) en un 15% (n=12) y de forma tardía (mayor a 10 días) en el 67,5% (n=54). En un 15% (n=12) se realizó después de 18 días de intubación orotraqueal.
Los medicamentos más utilizados para la realización del procedimiento fueron fentanilo (62%), remifentanilo (18%), midazolam (86%) y rocuronio (29%).
El 49% de las TPD fueron realizadas por un residente de anestesiología o cirugía general con la asistencia directa de un intensivista, el 40% por un médico intensivista y el 10% por especialistas de otras áreas.
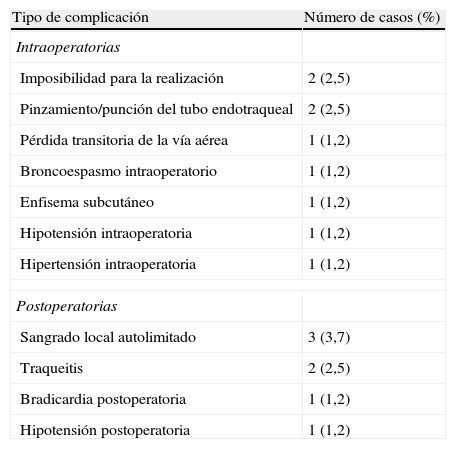
Se presentaron complicaciones intraoperatorias en 9 pacientes (11,6%) y complicaciones postoperatorias en 7 pacientes (9,1%) (tabla 2). Ninguna de las complicaciones representó un riesgo vital para los pacientes.
Complicaciones intra y postoperatorias tempranas del procedimiento TPD (n=80)
| Tipo de complicación | Número de casos (%) |
| Intraoperatorias | |
| Imposibilidad para la realización | 2 (2,5) |
| Pinzamiento/punción del tubo endotraqueal | 2 (2,5) |
| Pérdida transitoria de la vía aérea | 1 (1,2) |
| Broncoespasmo intraoperatorio | 1 (1,2) |
| Enfisema subcutáneo | 1 (1,2) |
| Hipotensión intraoperatoria | 1 (1,2) |
| Hipertensión intraoperatoria | 1 (1,2) |
| Postoperatorias | |
| Sangrado local autolimitado | 3 (3,7) |
| Traqueitis | 2 (2,5) |
| Bradicardia postoperatoria | 1 (1,2) |
| Hipotensión postoperatoria | 1 (1,2) |
Fuente: autor.
La tabla 3 presenta una comparación entre el tiempo de realización de la TPD en el total de los pacientes y la frecuencia de complicaciones encontradas. Se encontraron diferencias estadísticamente significativas en la presentación de complicaciones globales e intraoperatorias entre los 2 tiempos de realización (temprana vs. tardía). No se encontraron diferencias significativas entre otras variables como edad, sexo o puntuación APACHE II al ingreso.
DiscusiónLa TPD es un procedimiento ampliamente aceptado, y su utilización ha venido en aumento en los últimos años15,16. Una de las modificaciones a la técnica es la asistencia del fibrobroncoscopio para la visualización directa del procedimiento por vía endotraqueal. Sin embargo, esta implica la disponibilidad del equipo, requiere de personal entrenado en su realización y puede incrementar los costos del procedimiento17.
Algunos autores han documentado que la asistencia con fibrobroncoscopio altera el intercambio gaseoso con retención de dióxido de carbono. Reilly et al. demostraron incrementos en la presión intracraneana con el uso del fibrobroncoscopio debido al incremento de presión de dióxido de carbono18. Nawaz et al. reportan que la ausencia de asistencia con broncoscopio en el procedimiento no incrementa la morbilidad pero sí el tiempo en la realización19. Su uso rutinario en el procedimiento ha demostrado reducir la incidencia de complicaciones y en la actualidad su utilización está recomendada20-22, aunque en muchos sitios aún no está completamente disponible.
Nuestro estudio contrasta sus resultados con los reportados por Romero et al., que utilizaron asistencia con fibrobroncoscopio en 100 pacientes23. Dichos autores reportan una incidencia de complicaciones tempranas globales de 12% (8% intraoperatorias y 4% postoperatorias). Al igual que nuestros resultados, ninguna complicación resultó en desenlaces fatales para el paciente.
En nuestra práctica diaria no disponemos de asistencia con fibrobroncoscopio para la realización de las TPD, pero este estudio muestra que la incidencia de complicaciones tempranas globales no presenta diferencias sustanciales sin la asistencia del equipo y en comparación con el estudio de Romero et al.23. Adicionalmente, nuestros resultados se apoyan en los recientemente publicados por Jackson et al. en el año 2011. En su estudio retrospectivo demostraron que la incidencia de complicaciones tempranas o tardías del procedimiento no presentó diferencias con y sin la utilización de fibrobroncoscopio24. Es importante resaltar que 2 de nuestras complicaciones tempranas estuvieron dadas por pinzamiento o punción del tubo endotraqueal a pesar de su extracción hasta el estrecho glótico durante la punción. Eventualmente, estas complicaciones podrían haber sido prevenidas con la visualización directa del procedimiento por vía endotraqueal. Por supuesto, esto no descarta la posibilidad de puncionar el fibrobroncoscopio, lo cual ha sido reportado como complicación intraoperatoria por Ramirez et al.12.
El American College of Chest Physicians recomienda la traqueostomía para los pacientes en quienes se anticipa la necesidad de una vía artificial por más de 21 días25. Aunque no se ha definido el día exacto para su realización, sabemos que la ventilación mecánica por vía endotraqueal por un periodo inferior a 7 días cuenta con una baja incidencia de secuelas, las cuales son casi siempre reversibles. El lapso de 7 a 10 días es un tiempo de transición que requiere evaluación cuidadosa, pues se observa un 12% de incidencia de estenosis laringotraqueales26. Whited et al. reportan que el riesgo de complicaciones a largo plazo de la vía aérea se incrementa de forma sustancial después del décimo día de intubación endotraqueal9. En nuestro estudio el tiempo promedio de realización de la TPD fue de 11,6 días. El estudio de Romero et al. reportó un tiempo de 16,7 días. Esta diferencia se podría explicar por el tipo de pacientes manejados en cada sitio, su indicación particular para la realización de traqueostomía y los protocolos de cada institución.
Las complicaciones del procedimiento varían de acuerdo al sitio de estudio, el equipo quirúrgico y la severidad de la enfermedad del paciente. Diversos estudios reportan complicaciones entre el 2 y el 60%27,28, con mortalidad asociada de entre el 0 y el 5%29,30. El sangrado del sitio de punción ha sido reportado con una frecuencia del 1,2%, la estenosis traqueal en el 0,8% y la aparición de neumotórax en el 0,4%3,31. Hill et al. reportan una mortalidad del 0,3% y un índice global de complicaciones del 19%32.
En nuestro estudio retrospectivo encontramos una incidencia de complicaciones tempranas de 11%, la cual es inferior a la reportada por otros estudios33,34. Una de las complicaciones intraoperatorias más frecuente fue la imposibilidad de realizar la TPD. Estos pacientes requirieron una traqueostomía abierta.
Hemos documentado diferencias significativas en la proporción de complicaciones en relación al tiempo de realización de la TPD. El momento ideal para la realización de la traqueostomía es un tema que continua en discusión. Evidencias recientes sugieren que el uso de la traqueostomía debe ser individualizado, basado en las posibilidades futuras de extubación y en la evaluación del riesgo y beneficio de su utilización. En pacientes que han sufrido de traumatismo craneoencefálico severo se ha planteado el posible beneficio si se realiza de forma temprana (dentro de 3 a 4 días desde el inicio de la intubación orotraqueal)35. El ensayo clínico aleatorizado Tracheostomy Management in Critical Care (TracMan) fue diseñado para evaluar las diferencias entre pacientes que reciben el procedimiento antes de 4 días o después de 10 días a partir del inicio de la intubación orotraqueal (temprana vs. tardía)14. A pesar de que la técnica para la traqueostomía no fue estandarizada en el protocolo del estudio, la mayoría la realizaron de forma percutánea y en la cama del paciente. Sus autores han reportado la inclusión de más de 900 pacientes en múltiples unidades de cuidado intensivo del Reino Unido. Adicionalmente han presentado muy pocos casos de complicaciones intraoperatorias y ninguna muerte relacionada al procedimiento. Demostraron menor tiempo de sedación en el grupo de traqueostomía temprana. Sin embargo, el tiempo de estancia en las UCI o en el hospital no fue diferente entre los grupos. El reporte final del estudio aún no ha sido publicado. Las diferencias encontradas en nuestro estudio en relación al tiempo de realización del procedimiento deben ser analizadas con precaución por el tamaño de la muestra y las posibilidades de error tipoI. Otras complicaciones se presentaron en similitud con las reportadas por otros autores.
Este estudio fue diseñado para evaluar únicamente las complicaciones intra y postoperatorias tempranas de la realización de la traqueostomía en nuestro centro mediante la técnica de múltiples dilatadores. Por supuesto, esta estimación depende directamente de las complicaciones que se consideren en la definición de este desenlace compuesto —el cual no es estándar entre diversos estudios—. Una de sus limitaciones es la evaluación de los pacientes a corto plazo únicamente sin tener en cuenta otros desenlaces importantes relacionados con el uso de la traqueostomía en el paciente crítico. Por sus características metodológicas retrospectivas, este estudio está sujeto a posibles sesgos de información. Sin embargo, sus resultados son una fuente importante de hipótesis para nuestro grupo y para la comunidad médica. Adicionalmente, evidencias recientes sugieren fuertemente que la técnica de dilatación única presenta mejores condiciones de seguridad y de éxito36,37.
En conclusión, este estudio demuestra que nuestro grupo ha desarrollado una curva de aprendizaje sin la asistencia de fibrobroncoscopio que ha permitido abordar el procedimiento con una incidencia de complicaciones tempranas baja y similar a la reportada en la literatura.
Fuente de financiaciónRecursos propios de los autores.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Trabajo ganador del segundo puesto en el concurso Jorge Colmenares, XXIX Congreso Colombiano de Anestesiología y Reanimación 2011.