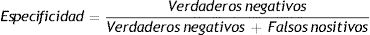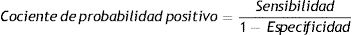Evaluar la calidad de la muestra de orina de 24 horas (orina-24h) es un desafío en el laboratorio de análisis clínicos. Para la detección de las muestras mal recogidas se han propuesto diferentes estrategias basadas en la excreción urinaria de creatinina. El objetivo de este estudio fue evaluar el desempeño de 2 de ellas: una basada en el intervalo de referencia de la excreción urinaria de creatinina (estrategia-IR) y otra propuesta por el Swiss Survey on Salt Group (estrategia-S).
Materiales y métodosEl estudio se realizó en el año 2016 en una población de Argentina. Participaron 69 sujetos adultos. Se obtuvieron muestras de orina-24h mal recogidas (N=69) y bien recogidas (N=69) que a su vez se clasificaron como mal y bien recogidas según las 2 estrategias evaluadas. Se calculó el coeficiente kappa, la proporción de muestras clasificadas incorrectamente y el cociente de probabilidad (CP) positivo y negativo. Se consideró la diferencia como estadísticamente significativa para un valor de p<0,05. El estudio fue aprobado por un Comité de Bioética local y se obtuvo el consentimiento informado de cada participante.
ResultadosEstrategia-IR vs. estrategia-S: coeficiente kappa: 0,26 (IC-95%: 0,10-0,42; p=0,020) vs. 0,51 (IC-95%: 0,37-0,64; p=0,000); muestras clasificadas incorrectamente: 37 vs. 25% (p=0,000); CP positivo: 1,7 (IC-95%: 1,2-2,4) vs. 9,8 (IC-95%: 3,7-25,8); CP negativo: 0,6 ((IC-95%: 0,4-0,8) vs. 0,5 ((IC-95%: 0,4-0,6).
ConclusiónLa estrategia-S presentó mejor desempeño que la estrategia-IR para detectar las muestras de orina-24h mal recogidas.
Assessment of the quality of the 24-hour urine sample (urine-24h) is a challenge in the clinical laboratory. Different strategies based on urinary creatinine excretion have been proposed for the detection of poorly collected samples. The objective of this study was to evaluate the performance of two of these strategies: one based on the reference interval of urinary creatinine excretion (IR-Strategy), and the other one proposed by the Swiss Survey on Salt Group (S-Strategy).
Materials and methodsThe study was carried out in the year 2016 with a population from Argentina. A total of 69 adult subjects were included in the study. Complete urine samples (N=69) and incomplete samples (N=69) were obtained. These were classified as poor, and well collected, according to the two strategies evaluated. Kappa coefficient, proportion of incorrectly classified samples, and positive and negative likelihood ratios (LR) were calculated. The difference was considered statistically significant for a P<.05. The study was approved by a local Bioethics Committee, and the informed consent was obtained from each participant.
ResultsStrategy-IR vs. Strategy-S: Kappa coefficient: 0.26 (95% CI; 0.10-0.42; P=.020) vs. 0.51 (95% CI; 0.37-0.64; P=.000); incorrectly classified samples: 37% vs. 25% (P=.000); positive LR: 1.7 (95% CI; 1.2-2.4) vs. 9.8 (95% CI; 3.7-25.8); negative LR: 0.6 (95% CI; 0.4-0.8) vs. 0.5 (95% CI; 0.4-0.6).
ConclusionThe S-Strategy showed a better performance than the IR-Strategy in the detection of poorly collected urine samples.
La excreción urinaria de algunas magnitudes biológicas presenta variabilidad a lo largo del día por lo que la medición cuantitativa de las mismas requiere disponer de una muestra de orina de 24 horas (orina-24h)1–3. Si bien en muchos casos dicha excreción es evaluada utilizando los índices obtenidos a partir de la relación «sustancia/creatinina» en muestras de orina recogidas al azar, existen limitaciones para su aplicación, por lo que la orina-24h sigue siendo solicitada en el laboratorio de análisis clínicos a pesar de las dificultades que representa su recogida4,5.
La obtención de un resultado válido a partir de esta muestra implica que el individuo evaluado realice una correcta recogida de la orina-24h, y es responsabilidad del laboratorio clínico proporcionar instrucciones claras, simples y fáciles de comprender para lograr tal objetivo6. No obstante, a pesar de recibir instrucciones adecuadas, existe baja adherencia de los individuos a cumplir con las pautas para la recolección debido a lo engorroso que resulta este procedimiento5,7. Por tal motivo es habitual observar que el paciente recoja inadecuadamente el volumen completo de orina durante las 24h, que pierda volumen por frascos mal cerrados o que extienda la recolección a más de 24horas y por ello recoja un exceso de orina; todas estas situaciones representan errores de la etapa preanalítica5. Esto puede tener influencia directa en los resultados de laboratorio, produciendo errores diagnósticos y/o terapéuticos.
En consecuencia, la calidad de la muestra de orina-24h depende en gran medida de la participación voluntariosa y honesta de los individuos evaluados; y detectar muestras inadecuadas representa un desafío para el laboratorio clínico. Con este propósito, el personal del laboratorio debe indagar sobre el procedimiento de recogida que realizó el individuo y si este fue inadecuado debe rechazar la muestra y solicitar que se repita el procedimiento. Sin embargo, utilizar solo esta estrategia para detectar muestras inapropiadas es subjetivo y puede conducir a la aceptación de muestras sin la calidad necesaria para su análisis.
Para solucionar este problema, se han propuesto 2 marcadores que permiten comprobar si la recogida de la muestra de orina-24h fue completa: la recuperación urinaria del ácido p-aminobenzoico previamente ingerido y la excreción urinaria de creatinina (EUC)8 calculada como:
La recuperación urinaria del ácido p-aminobenzoico es una práctica compleja y costosa por lo que su aplicación diaria es limitada9.
En base a las características de la creatinina10 y dado que la determinación de la EUC es una práctica simple y sencilla de llevar a cabo en el laboratorio, se han desarrollado estrategias en función de esa excreción para detectar las muestras de orina-24h recogidas inadecuadamente9,10, 2 de las cuales se seleccionaron para ser evaluadas en este estudio.
La primera estrategia seleccionada es comúnmente utilizada en la práctica clínica y se basa en comparar la EUC del individuo con el intervalo de referencia poblacional (estrategia-IR) (tabla 1)10. Su desventaja radica justamente en la problemática asociada a la determinación de los intervalos de referencia poblacionales10.
Excreción urinaria de creatinina estimada para adultos según las 2 estrategias
| EUC (mg/kg/24h) | Hombres | Mujeres |
|---|---|---|
| IR poblacional (estrategia-IR) | 20-25 | 15-20 |
| Fórmula S (estrategia-S) | (266,16−2,33×IMC+0,66×edad−0,017×edad2)/8,84 | (266,16−47,71−2,33×IMC+0,66×edad×0,017×edad2)/8,84 |
EUC: excreción urinaria de creatinina; IMC: índice de masa corporal; IR: intervalo de referencia; S: Swiss Survey on Salt Group.
La segunda estrategia seleccionada en este estudio fue recientemente publicada por Forni Ogna et al. (2015) en representación del Swiss Survey on Salt Group (estrategia-S) y se basa en una ecuación validada para predecir la EUC (tabla 1), de la cual derivan nomogramas con aplicabilidad clínica10. Su ventaja reside en que fue desarrollada en los años recientes, en una gran población sin enfermedad renal. Su desventaja es que hasta el momento solo fue validada en una población europea.
En este estudio se planteó la hipótesis de que la estrategia-S es mejor que la estrategia-IR para detectar muestras de orina-24h mal recogidas. En este contexto, el objetivo fue evaluar el desempeño de estas 2 estrategias basadas en la EUC para detectar las muestras de orina-24h mal recogidas por pérdida de la última micción correspondiente al periodo de recogida de 24horas.
Materiales y métodosEl presente estudio se realizó en el mes de agosto del año 2016, en la Universidad Nacional del Sur y el Hospital Municipal de Agudos, ambos situados en la ciudad de Bahía Blanca, Argentina. Se obtuvo el consentimiento informado de los individuos y la aprobación del Comité de Bioética del mencionado hospital.
Se invitó a participar voluntariamente del estudio a bioquímicos y a alumnos del último año de la carrera de Bioquímica de dicha universidad, a quienes se les explicó el objetivo y protocolo del mismo. Se les aclaró que quienes estaban comprendidos entre los criterios de exclusión se abstuvieran de participar.
Criterios de exclusión: uso de diuréticos, uso de suplementos dietarios, embarazo o lactancia, diabetes mellitus o enfermedad renal, donación de sangre o plasma durante (o menos de 4 semanas antes) el estudio, pérdida excesiva de peso en el último mes.
Aceptaron participar 69 individuos adultos (13 hombres y 56 mujeres) aparentemente sanos. Todos ellos fueron instruidos detalladamente sobre el protocolo a seguir, tanto de manera oral como escrita, declararon entenderlo y se comprometieron a cumplirlo.
Se indicó no modificar el estilo de vida durante el periodo de recogida de la muestra de orina-24h, incluyendo alimentación e hidratación, y evitar la realización de actividad física 48h antes de la toma de muestra y durante la misma.
A cada participante se le entregaron 2 recipientes plásticos nuevos de boca ancha y sin aditivos para la recolección de la muestra, uno con capacidad para 3L y otro para 0,75L.
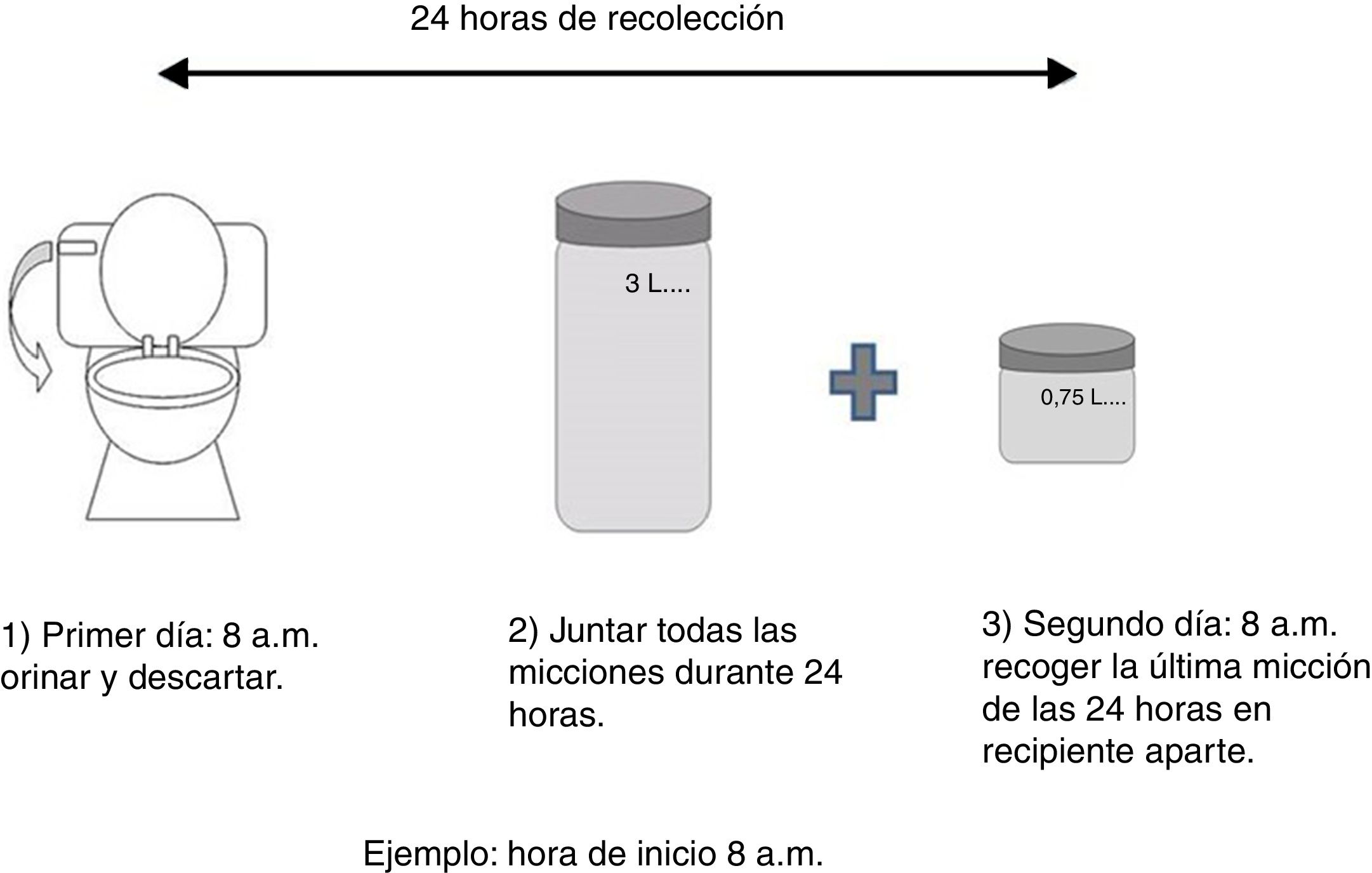
Las instrucciones proporcionadas para recoger la muestra de orina-24h fueron (fig. 1):
- -
Descartar la micción correspondiente a la hora de inicio del periodo de 24h.
- -
Registrar dicho horario.
- -
Recolectar cada micción emitida luego del horario de inicio en el recipiente de 3L, excepto la última micción correspondiente a la hora de finalización del periodo de 24horas.
- -
Recolectar la última micción en el recipiente de 0,75L.
- -
Conservar las muestras en frigorífico durante el periodo de recolección.
- -
Remitir las muestras recolectadas al laboratorio luego de finalizar el procedimiento.
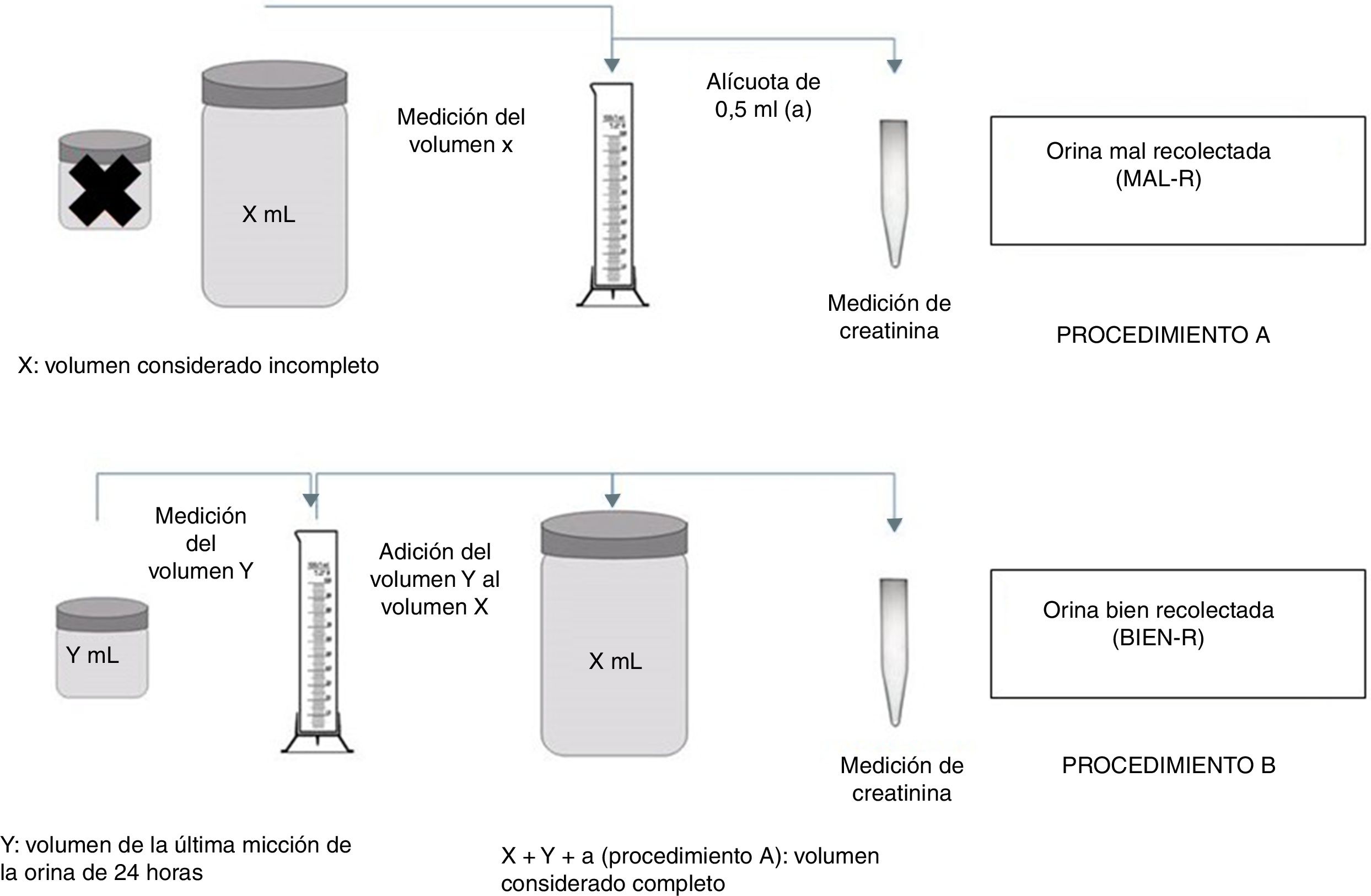
En la figura 2 se observan los 2 procedimientos llevados a cabo para obtener las orinas bien y mal recogidas de cada individuo. En el procedimiento A, se midió el volumen (X) de orina recolectado en el recipiente mayor, sin la última micción, del cual se separó una alícuota de 0,5mL (a) para la medición de creatinina. Se obtuvieron así 69 alícuotas consideradas mal recogidas (MAL-R). En el procedimiento B, se midió el volumen (Y) de orina recolectado en el recipiente de 0,75L y luego se añadió a su correspondiente recipiente de 3L con el volumen (X) de orina. Se sumaron los respectivos volúmenes (+Y+a) para obtener así el volumen real de la muestra de 24h. Se consideró que dicho volumen correspondía a las muestras bien recogidas (BIEN-R). Se obtuvieron 69 alícuotas correspondientes a muestras BIEN-R para la medición de creatinina.
Todas las alícuotas, en total 138, se mantuvieron refrigeradas hasta su procesamiento.
La clasificación de las muestras en MAL-R y BIEN-R se consideró el gold standard o clasificación de referencia y se basó en la declaración de certeza de los sujetos de haber cumplido estrictamente con el protocolo del estudio.
Se evaluó el desempeño, por comparación con la clasificación de referencia, de las 2 estrategias basadas en la EUC:
Estrategia-IR: una muestra de orina-24h se consideró bien recogida (Bien-IR) cuando la EUC (mg/kg/24h) se encontraba dentro del IR, de lo contrario, se consideró mal recogida (Mal-IR)10.
Estrategia-S: basada en 3 nomogramas obtenidos y validados en una población europea que permiten obtener el percentil (P) poblacional en que se ubica la EUC (mg/kg/24h) de un individuo según su sexo, edad e índice de masa corporal (IMC). La muestra de orina-24h se consideró bien recogida (Bien-S) si la EUC se encontraba entre los P10 y P90 sugeridos en esta estrategia, de lo contrario, se consideró mal recogida (Mal-S)10.
La medición de creatinina (mg/L) se realizó por un método enzimático en un autoanalizador Vitros® 4600 (Ortho Clinical Diagnostics, New Jersey, EE. UU.) con un error total del 4,8% (coeficiente de variación analítico: 1,9%; bias: 1,7%). Todas las muestras se procesaron con el mismo lote de reactivos. Se registraron los datos de altura (m) y peso corporal (kg) de los individuos. La EUC (mg/kg/24h) para cada alícuota de orina se obtuvo multiplicando la concentración de creatinina por el respectivo volumen de la muestra (MAL-R o BIEN-R) y se dividió por el peso corporal del individuo, según la fórmula descripta previamente. Se calculó el IMC como peso (kg)/altura (m2).
El análisis estadístico se realizó con los programas Statistical Package for Social Science 15,0 (SPSS, Chicago, IL, EE. UU.) y Epidemiologic Analysis of Tabulated Data 3,1 (Epidat, Xunta de Galicia, HDA, OPS, OMS). Como el número de hombres incluidos en el estudio fue menor a 30, las características de los sujetos y de las muestras estratificadas por sexo se compararon con la prueba Mann-Whitney U para variables no paramétricas. Para comparar las proporciones se utilizó la prueba de χ2.
Para evaluar el desempeño de ambas estrategias en la detección de las muestras bien y mal recogidas, respecto de la clasificación de referencia, se calculó el coeficiente de concordancia kappa. Este coeficiente se interpretó según la escala de Landis y Koch (<0: sin acuerdo; 0,0-0,20: acuerdo insignificante; 0,21-0,40: acuerdo discreto; 0,41-0,60: acuerdo moderado; 0,61-0,80: acuerdo considerable; 0,81-1: acuerdo casi perfecto)11. Asimismo, se calculó la proporción de las muestras clasificadas incorrectamente por cada estrategia como: la suma del número de muestras MAL-R pero clasificadas como bien por la estrategia evaluada y el número de muestras BIEN-R pero clasificadas como mal por la estrategia evaluada, dividido el total de muestras.
Para cada estrategia se calculó la sensibilidad, especificidad y cocientes de probabilidad12, como:
Siendo:
Verdaderos positivos: muestras MAL-R clasificadas como mal recogidas por la estrategia evaluada (Mal-IR o Mal-S).
Verdaderos negativos: muestras BIEN-R clasificadas como bien recogidas por la estrategia evaluada (Bien-IR o Bien-S).
Falsos positivos: muestras BIEN-R pero clasificadas como mal recogidas por la estrategia evaluada (Mal-IR o Mal-S).
Falsos negativos: muestras MAL-R pero clasificadas como bien recogidas por la estrategia evaluada (Bien-IR o Bien-S).
Se consideró la diferencia como estadísticamente significativa para un valor de p<0,05. Para evaluar la magnitud de la diferencia se calculó el tamaño del efecto para las variables no paramétricas con la delta de Cliff. La delta de Cliff es un parámetro complementario al valor de p, que permite inferir el tamaño o importancia clínica de la diferencia estadística observada. Este parámetro estadístico toma valores entre −1 y +1. Un valor de±1 indica ausencia de solapamiento entre los 2 grupos estudiados, mientras que un valor 0 indica la completa superposición de los mismos. Un valor positivo indica que las observaciones del primer grupo son mayores que las del segundo grupo y un valor negativo lo contrario. Para interpretar la delta de Cliff se utilizó la siguiente escala de valores: 0,15 tamaño del efecto pequeño; 0,33 tamaño del efecto mediano; 0,47 tamaño del efecto grande. Se calculó la delta de Cliff con el software libre Cliff's Delta Calculator13.
ResultadosLas características de la población y de las muestras estratificadas por sexo (hombres/mujeres: 13/56; p=0,225) se enumeran en la tabla 2. Entre ambos sexos no se observó una diferencia estadísticamente significativa en la edad, el IMC y el volumen de orina-24h. En la tabla 3 se observa que la diferencia de las diuresis entre las muestras BIEN-R y MAL-R no fue estadísticamente significativa, sin embargo la EUC medida en las muestras MAL-R fue estadísticamente menor respecto de las muestras BIEN-R. El tamaño del efecto de esa diferencia, evaluado a través de la delta de Cliff resultó ser grande.
Características de la población estudiada
| Hombres (N=13) | Mujeres (N=56) | p | |
|---|---|---|---|
| Edad (años) | 25 (24-26) | 25 (23-26) | 0,488 |
| Peso (kg) | 75 (63-84) | 58 (51-63) | 0,000 |
| Altura (m) | 1,78 (1,72-1,80) | 1,63 (1,60-1,68) | 0,000 |
| Índice de masa corporal (kg/m2) | 22,8 (21,2-26,5) | 21,4 (19,4-23,3) | 0,050 |
| EUC medida (mg/kg/24h) | 23 (21-27) | 19 (17-20) | 0,000 |
| Volumen de 24h (mL/24h) | 1.680 (1.230-2.085) | 1.530 (1.205-1.981) | 0,570 |
EUC: excreción urinaria de creatinina.
Datos expresados como mediana (percentil 25-percentil 75). Diferencia estadísticamente significativa: p<0,05.
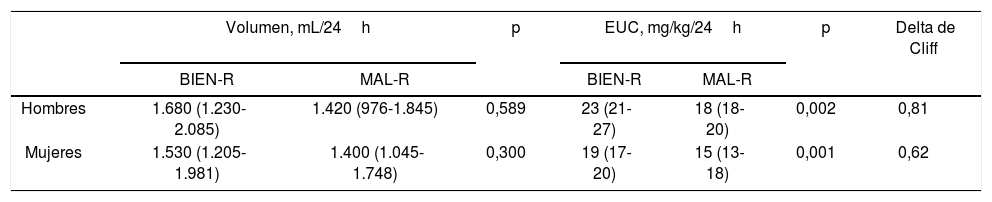
Evaluación de las muestras de orina de 24horas bien y mal recogidas
| Volumen, mL/24h | p | EUC, mg/kg/24h | p | Delta de Cliff | |||
|---|---|---|---|---|---|---|---|
| BIEN-R | MAL-R | BIEN-R | MAL-R | ||||
| Hombres | 1.680 (1.230-2.085) | 1.420 (976-1.845) | 0,589 | 23 (21-27) | 18 (18-20) | 0,002 | 0,81 |
| Mujeres | 1.530 (1.205-1.981) | 1.400 (1.045-1.748) | 0,300 | 19 (17-20) | 15 (13-18) | 0,001 | 0,62 |
BIEN-R: muestras de orina de 24h bien recogidas según la clasificación de referencia; EUC: excreción urinaria de creatinina; MAL-R: muestras de orina de 24horas mal recogidas según la clasificación de referencia.
Datos expresados como mediana (percentil 25-percentil 75). Diferencia estadísticamente significativa: p <0,05. Delta de Cliff>0,47, tamaño del efecto grande.
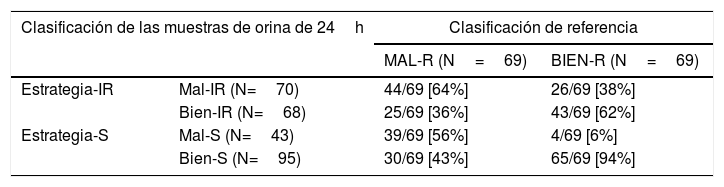
En la tabla 4 se observa la clasificación de las muestras de orina-24h obtenida por la estrategia-IR y la estrategia-S, respecto de la clasificación de referencia. De las muestras MAL-R, la estrategia-IR clasificó como tal al 64% de las mismas y la estrategia-S al 56%. De las muestras BIEN-R, la estrategia-IR clasificó como tal al 62% de las mismas y la estrategia-S al 94%.
Tabla de contingencia obtenida para la clasificación de las muestras de orina de 24h según la estrategia-IR y la estrategia-S respecto de la clasificación de referencia
| Clasificación de las muestras de orina de 24h | Clasificación de referencia | ||
|---|---|---|---|
| MAL-R (N=69) | BIEN-R (N=69) | ||
| Estrategia-IR | Mal-IR (N=70) | 44/69 [64%] | 26/69 [38%] |
| Bien-IR (N=68) | 25/69 [36%] | 43/69 [62%] | |
| Estrategia-S | Mal-S (N=43) | 39/69 [56%] | 4/69 [6%] |
| Bien-S (N=95) | 30/69 [43%] | 65/69 [94%] | |
IR: intervalo de referencia; S: Swiss Survey on Salt Group.
Datos expresados como proporción.
MAL-R o BIEN-R: muestras mal o bien recogidas según clasificación de referencia.
Mal-IR o Bien-IR: muestras mal o bien recogidas según la estrategia-IR.
Mal-S o Bien-S: muestras mal o bien recogidas según la estrategia-S.
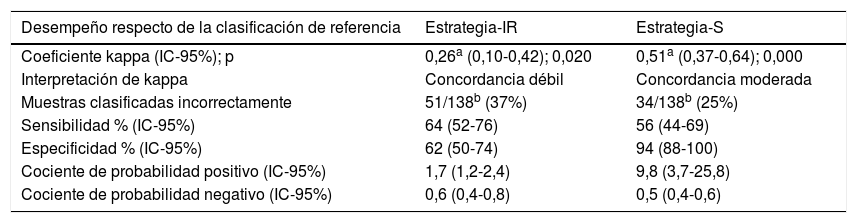
El desempeño obtenido por ambas estrategias en la clasificación de las muestras de orina-24h se describe en la tabla 5.
Desempeño obtenido de la estrategia-IR y la estrategia-S en la clasificación de las muestras de orina de 24h respecto de la clasificación de referencia
| Desempeño respecto de la clasificación de referencia | Estrategia-IR | Estrategia-S |
|---|---|---|
| Coeficiente kappa (IC-95%); p | 0,26a (0,10-0,42); 0,020 | 0,51a (0,37-0,64); 0,000 |
| Interpretación de kappa | Concordancia débil | Concordancia moderada |
| Muestras clasificadas incorrectamente | 51/138b (37%) | 34/138b (25%) |
| Sensibilidad % (IC-95%) | 64 (52-76) | 56 (44-69) |
| Especificidad % (IC-95%) | 62 (50-74) | 94 (88-100) |
| Cociente de probabilidad positivo (IC-95%) | 1,7 (1,2-2,4) | 9,8 (3,7-25,8) |
| Cociente de probabilidad negativo (IC-95%) | 0,6 (0,4-0,8) | 0,5 (0,4-0,6) |
IC-95%: intervalo de confianza del 95%; IR: intervalo de referencia; S: Swiss Survey on Salt Group.
Entre los resultados obtenidos se observa que la estrategia-S presentó mejor concordancia con la estrategia de referencia (kappa: 0,51; p=0,000; concordancia moderada), mientras que la estrategia-IR clasificó mayor cantidad de muestras de manera errónea. En definitiva, la estrategia-S presentó menor tendencia a clasificar incorrectamente las muestras en comparación con la estrategia-IR (25 vs. 37%), respecto de la clasificación de referencia.
La estrategia-S presentó mayor especificidad que la estrategia-IR, es decir, tuvo mayor capacidad de clasificar correctamente las muestras Bien-R. Según el cociente de probabilidad positivo de la estrategia-S, es 10 veces más probable que esta estrategia clasifique como Mal-S una muestra Mal-R que una muestra Bien-R, en cambio para la estrategia-IR esta probabilidad fue menor.
DiscusiónEn este trabajo se observó que la pérdida de la última micción de la muestra de orina-24h produjo una disminución estadística y clínicamente significativa en el valor de la EUC. Esta observación evidencia que este error preanalítico debe ser detectado para evitar que el laboratorio comunique resultados erróneos que afecten su interpretación clínica y que es necesario establecer una estrategia de control óptima para evaluar si el volumen de orina-24h fue recolectado en su totalidad.
Con los años se ha intentado establecer los indicadores que permitan validar la integridad de una muestra de orina-24h, como el uso de los intervalos de referencia para creatininuria en adultos14, el índice de creatininuria15, las fórmulas de estimación de la EUC16, etc. No obstante las poblaciones evaluadas para establecer estos indicadores presentan diferencias en términos de edad, etnia, factores ambientales y nutricionales9.
En este trabajo la estrategia-S demostró un mejor desempeño que la estrategia-IR, en la clasificación de muestras de orina-24h como bien y mal recogidas por pérdida de la última micción. Los resultados obtenidos evidenciaron que aplicando la estrategia-S es casi 10 veces más probable que una muestra mal recogida se clasifique como tal; en cambio, aplicando la estrategia-IR la probabilidad de dicha clasificación es mucho menor, aproximadamente 2 veces.
Forni Onga et al. (2015) concluyeron que el intervalo de referencia poblacional de la EUC, históricamente utilizado, no es representativo de la población europea y que esta sería la causa por la cual la estrategia-IR condujo al rechazo de más de la mitad de las muestras de orina-24h evaluadas en esa población10. Siguiendo esta línea de razonamiento es esperable que ninguna de las 2 estrategias sea totalmente representativa de la población argentina estudiada en este trabajo.
Otra causa que evidencia diferencias entre las estrategias, además de las poblacionales, podría ser el hecho de que la estrategia-IR tiene en cuenta solo el peso del paciente mientras que la estrategia-S contempla el IMC. En la era en que la obesidad crece de manera exponencial en el mundo, es fundamental tener en cuenta que en los individuos con sobrepeso u obesidad, el aporte del peso en kg en cualquiera de las fórmulas que permiten calcular la EUC no siempre será representativo de su masa muscular sino, probablemente, de su tejido graso. Por tal motivo es de interés emplear fórmulas que tengan en cuenta el IMC, como la que utiliza la estrategia-S.
Otro aspecto a tener en cuenta es que los intervalos de referencia sugeridos para la EUC en el periodo de 24horas (estrategia-IR) se basan en estudios realizados en la década de los 6010, pero la información que se detalla en esos trabajos es escasa. Por ejemplo, no indican con qué método se realizó la medición de la creatinina, aunque seguramente no emplearon métodos trazables, lo cual limitaría su uso en la actualidad. Esas diferencias metodológicas podrían influir en los resultados obtenidos puesto que los métodos no trazables impiden que los datos sean conmutables. Es interesante tener en cuenta que tanto en el presente trabajo como en el realizado por Forni Onga et al. (2015)10, la creatinina urinaria se cuantificó por métodos trazables a espectrofotometría de masa por dilución isotópica, lo cual los haría comparables. Quizás por este motivo, la estrategia-S fue mejor que la estrategia-IR en nuestra población.
Una limitación de este trabajo fue la ausencia de un método gold standard, como el método del ácido p-aminobenzoico, para evaluar si una muestra de orina-24h se recolectó en forma completa. No obstante cabe destacar que todos los participantes, por ser profesionales del laboratorio clínico o alumnos avanzados de la carrera de Bioquímica, tenían pleno conocimiento sobre el procedimiento y el riesgo que implica recoger inadecuadamente la muestra de orina-24h, lo cual se consideró garantía suficiente de calidad de la muestra recogida. Otra limitación del estudio fue que solo se contempló como causa de muestra mal recogida la pérdida de la última micción; este hecho introduce un sesgo por tener todas las muestras mal recogidas menor volumen que las muestras bien recogidas.
En conclusión, la estrategia-S fue mejor que la estrategia-IR para detectar las muestras de orina-24h mal recogidas por pérdida de la última micción correspondiente al periodo de 24h, en una población adulta de Argentina. La estrategia-S podría ser de utilidad en el laboratorio clínico para evaluar el procedimiento de recogida de la muestra de orina-24h, siempre acompañado de la realización de un interrogatorio minucioso al paciente sobre el cumplimiento de las instrucciones recibidas para tal fin. Deberían efectuarse estudios en diferentes poblaciones para validar su utilidad en la aceptación y/o rechazo de la muestra de orina-24h, un desafío de crucial importancia que enfrenta el laboratorio clínico para asegurar la calidad preanalítica de este espécimen biológico.
FinanciaciónEl presente trabajo ha sido financiado a través de un subsidio (PGI 24/B225) otorgado por la Universidad Nacional del Sur, Bahía Blanca, Argentina.
Conflicto de interesesLas autoras declaran no tener ningún conflicto de intereses.