La concentración sérica de 25-hidroxivitamina D (25[OH] vitamina D) es el parámetro que mejor refleja el estado de suficiencia de vitamina D de un individuo.
El objetivo de este estudio fue comparar los resultados de 25-hidroxivitamina D obtenidos mediante 3 métodos automatizados comerciales utilizando muestras de pacientes y siguiendo el protocolo establecido en la guía CLSI (Clinical Laboratory Standards Institute) EP09-A2-IR.
Material y métodosSe determinaron las concentraciones de 25[OH] vitamina D en 40 muestras de suero mediante 3 inmunoensayos: LIAISON® (Diasorin), ARCHITECT (Abbot) y Elecsys Vitamin D total (Roche). Se siguió el protocolo EP09-A2-IR (2.ª edición 2010) del CLSI.
ResultadosEn el estudio de reproducibilidad ningún duplicado superó el límite de aceptabilidad y ninguno de los métodos presentó valores extremos. Los 3 métodos mostraron una alta correlación entre sí. Se observaron diferencias constantes y proporcionales entre los resultados de LIAISON®-ARCHITECT® y ARCHITECT -Elecsys, mientras que entre LIAISON®- Elecsys solo existieron diferencias constantes. La mediana del coeficiente de variación (CV) obtenido en el ARCHITECT fue significativamente inferior a la obtenida con el LIAISON® (p<0,01) pero no difirió significativamente de la del Elecsys (p=0,204). Tampoco existieron diferencias significativas entre las medianas del CV de LIAISON® respecto a Elecsys (p=0,308).
ConclusiónLos 3 métodos presentan una buena reproducibilidad y una alta correlación entre sí, aunque los resultados de 25[OH] vitamina D obtenidos no son intercambiables. Todos parecen adecuados para su utilización, aunque deben ser valorados por cada laboratorio para seleccionar la metodología que más se ajuste a sus necesidades.
Serum concentration of 25-hydroxyvitamin D (25[OH]vitamin D) is the best parameter for assessing vitamin D status in patients. The aim of this study is to compare the results of vitamin D in patient samples using three different automated methods, following the CLSI (Clinical Laboratory Standards Institute) EP09-A2-IR (2nd edition 2010) guideline.
MethodsConcentrations of 25-hydroxyvitamin D (25[OH]vitamin D) in 40 patient serum samples were determined, using three different immunoassays: LIAISON® (Diasorin), ARCHITECT (Abbot) and Elecsys Vitamin D total (Roche). The CLSI (Clinical Laboratory Standards Institute) EP09-A2-IR (2nd edition 2010) guideline was used.
ResultsIn the reproducibility study no duplicate was outside the acceptability limit and there were no outliers in any of the methods. The three methods showed a good correlation with each other. Constant and proportional differences were observed between the results of LIAISON®-ARCHITECT® and ARCHITECT -Elecsys®, whereas only constant differences were observed between LIAISON®- Elecsys. The median CV obtained with ARCHITECT was significantly lower than with LIAISON® (P<.01), but was not significantly different from that of the Elecsys (P=.204). No significant difference between the median CV of LIAISON® and Elecsys (P=.308) was observed, either.
ConclusionThe three methods show a good reproducibility and a good correlation between each other, although the results obtained are not interchangeable. All of them are appropriate for their use in clinical laboratories, although in each case an evaluation should be performed in order to choose the best method for the fulfilling of the laboratories requirements.
La vitamina D es una vitamina liposoluble cuyas fuentes principales son la síntesis cutánea y la ingesta de determinados alimentos. Su acción principal está relacionada con el metabolismo fosfocálcico y el metabolismo óseo. Sin embargo, recientemente se han demostrado acciones antiproliferativas, inmunomoduladoras y de estimulación de la diferenciación celular que la relacionan con múltiples efectos fisiopatológicos1. El mejor parámetro para valorar el estado de suficiencia de la vitamina D de un individuo es la medida de las concentraciones séricas de 25-hidroxivitamina D (25[OH] vitamina D)2. La mayor parte de la 25[OH] vitamina D en suero corresponde a la forma D3, mientras que la forma D2 alcanza niveles mensurables en pacientes en tratamiento o en personas tomando suplementos o alimentos fortificados con esta vitamina1,3.
Aunque se han propuesto candidatos a métodos de referencia como la dilución isotópica cromatografía líquida/espectrometría de masas (ID-LC-MS/MS)4, los métodos de referencia para la determinación de la 25[OH] vitamina D (D2 y D3) son la cromatografía líquida-tándem por espectrometría de masas y la cromatografía líquida de alta eficacia (HPLC). Ambos métodos presentan una alta sensibilidad pero son lentos, requieren de infraestructura de alto coste, gran volumen de muestra y personal cualificado, por lo que en la mayoría de laboratorios clínicos se utilizan inmunoensayos que permiten el análisis rápido de gran volumen de muestras. Desde la aparición de estos inmunoensayos se han desarrollado diferentes métodos comerciales que utilizan anticuerpos o proteínas de unión como ligandos, quimioluminiscencia (CMIA) o electroquimioluminiscencia (ECLIA) como marcador de señal, y se procesan en analizadores de inmunoensayos multiparamétricos. Entre ellos, el método comercial de LIAISON® (DiaSorin) lleva años en el mercado y la validez de sus resultados ha sido repetidamente evaluada5,6.
Recientemente ha aparecido en el mercado un método mejorado de determinación de vitamina D por el analizador Modular E170 (Roche) que permite medir tanto la 25[OH] vitamina D3 como la 25[OH] vitamina D2 y, por primera vez, un método implementado en el analizador ARCHITECT (Abbot).
A menudo resulta difícil seleccionar un procedimiento para comparar la medición de un mismo analito mediante distintos métodos. Existen diferentes protocolos validados y conviene escoger aquel que se adapte a nuestro ámbito de trabajo en relación a su manejabilidad y coste económico. El Clinical Laboratory Standards Institute (CLSI) es un organismo interdisciplinar internacional que elabora guías consensuadas y estándares de buenas prácticas en el laboratorio. En el año 2010 edita una revisión de la guía EP09-A2-IR (2.ª edición 2010) en la que se detalla cómo comparar diferentes métodos y cómo estimar el sesgo mediante la utilización de muestras de pacientes7. Hasta la fecha no tenemos conocimiento de ningún estudio en el que se comparen los resultados de 25[OH] vitamina D obtenidos por estos 3 inmunoensayos comerciales utilizando la guía CLSI.
El objetivo de este estudio es comparar las concentraciones de 25[OH] vitamina D obtenidas mediante 3 métodos automatizados comerciales utilizando muestras de pacientes siguiendo el protocolo establecido en la guía CLSI, EP09-A2-IR.
Material y métodosSe seleccionaron 40 muestras de suero de pacientes del Hospital Germans Trias i Pujol (HGTiP). La totalidad de las muestras fueron recogidas en tubos de suero sin anticoagulante y con gel separador. Tras su centrifugación, se realizaron 2 alícuotas que fueron conservadas a -20°C hasta su procesamiento. Todas las muestras correspondieron a adultos caucásicos (edad media: 63,44 años) de los cuales el 70% fueron mujeres y el 30% hombres.
El criterio de selección fue que las concentraciones de 25[OH] vitamina D obtenidas mediante el método empleado en la práctica diaria (LIAISON®25 OH Vitamina D TOTAL Assay [Diasorin]) estuvieran distribuidas abarcando todo el rango de linealidad de dicho método. Se escogieron 10 muestras con concentraciones de 25[OH] vitamina D <20ng/mL, 20 muestras con concentraciones entre 20 y 40ng/mL y 10 muestras con concentraciónes >40ng/mL.
Métodos analíticosEn todas las muestras se determinó por duplicado la concentración de 25[OH] vitamina D mediante los 3 métodos comerciales automatizados. Todos ellos reconocen 25[OH] vitamina D total (D2 y D3) en diferentes tipos de muestra (suero y plasma).
LIAISON®25 OH Vitamina D TOTAL Assay. Referencia 310600 (DiaSorin,Inc, Stillwater, MN, EE. UU.) (LIAISON®)8 es el método utilizado en nuestra práctica diaria y se tomó como referencia. Consiste en un inmunoensayo competitivo con detección por quimioluminiscencia. Presenta una imprecisión intraensayo con un coeficiente de variación (CV) ≤5,5% y una sensibilidad funcional de 4ng/mL. Su intervalo de medición es de 4-150ng/mL, de modo que las muestras por encima de esta concentración deben diluirse manualmente utilizando el diluyente LIAISON®25 OH Vitamina D TOTAL Specimen Diluent Set. La especificidad analítica reflejada a través del porcentaje de reactividad cruzada con otros metabolitos es de 104% para 25[OH] vitamina D2, 100% para 25[OH] vitamina D3 y <1% para 3-epi-25[OH] vitamina D38.
ARCHITECT 25-OH Vitamin D assay. Ref. 3L52. (Abbot, Wiesbaden, Germany) (ARCHITECT)9 utiliza un inmunoensayo competitivo con detección por quimioluminiscencia fue el método tomado como referencia en la comparación ARCHITECT - Elecsys. El método presenta una imprecisión intraensayo con un CV ≤3,7% y una sensibilidad funcional de=8ng/mL. Su intervalo de medición es de 8-160ng/mL de modo que las muestras por encima de esta concentración deben ser diluidas utilizando una muestra de baja concentración de 25[OH] vitamina D (≤10,7ng/mL). La especificidad analítica reflejada a través del porcentaje de reactividad cruzada con otros metabolitos es de 52% para 25[OH] vitamina D2, 105% para 25[OH] vitamina D3 y 2,7% para 3-epi-25[OH] vitamina D39.
Elecsys Vitamin D total (Modular E170. Ref.05894913 190 (Roche Diagnostics GMBH, Mannheim.Germany.) (Elecsys)10 utiliza un inmunoensayo de unión competitiva a la proteína de fijación, con detección por electroquimioluminiscencia (ECLIA). Presenta una imprecisión intraensayo con un CV ≤ 6,8% y un límite de detección de 3ng/mL. Su intervalo de medición es de 3-70ng/mL de modo que las muestras por encima de esta concentración deben ser diluidas utilizando el diluyente Elecsys Diluent Universal o un suero con concentración de 25[OH] vitamina D baja. La especificidad analítica reflejada a través del porcentaje de reactividad cruzada con otros metabolitos es de 81% para 25[OH] vitamina D2, 98% para 25[OH] vitamina D3 y 93% para 3-epi-25[OH] vitamina D310.
ProtocoloSe siguió la guía «Comparación de métodos y estimación del sesgo utilizando muestras de pacientes» del CLSI EP09-A2-IR, aunque en este estudio no se ha realizado la estimación del sesgo. Todas las muestras se determinaron por duplicado mediante los 3 métodos a analizar siguiendo el protocolo de cada analizador. Todos los resultados se expresaron en ng/mL. Para su conversión a unidades del sistema internacional (SI): ng/mL x 2,5=nmol/L. Los duplicados se realizaron en una misma serie y por los 3 analizadores en el mismo día, realizando la totalidad del estudio en 5 días. En todos los métodos los resultados correspondieron a la misma calibración.
- 1.
Se estudió la reproducibilidad de los duplicados. Para cada método se calculó el promedio de los duplicados ([xi1+xi2]/2) y las diferencias absolutas de estos (DXi=|xi1–xi2|). Los límites de aceptabilidad entre duplicados correspondieron al promedio de las diferencias multiplicado por 4. Si alguna diferencia absoluta individual excedía este valor límite se calculaba el límite de aceptabilidad para la diferencia absoluta normalizada (relativa) (promedio DX’i=|xi1–xi2|/media del duplicado (xi) multiplicado por 4). Si se sobrepasaba también este límite ese duplicado se debía eliminar de la base de datos. En caso de tener que excluir uno o ningún duplicado se podía continuar el estudio sin realizar ninguna acción adicional.
- 2.
Estudio de los valores extremos (outliers). Para cada muestra se calculó la diferencia absoluta entre el primer duplicado del método en comparación y el primer duplicado del método considerado de referencia (Eij=yij - xij). Se realizó el mismo cálculo para el segundo duplicado, y así sucesivamente. Se sumaron las diferencias para cada duplicado. El límite de aceptabilidad correspondió al promedio de las diferencias (∑ de las diferencias/2N) multiplicado por 4. Si algún valor excedía este límite se calculaba el límite normalizado. Si se sobrepasaba también este límite ese duplicado se debía eliminar de la base de datos. En caso de tener que excluir solo uno o ningún duplicado se podía continuar el estudio sin realizar ninguna acción adicional.
- 3.
Cálculo de la adecuación del rango de la variable X, siendo la variable X el método de referencia en la comparación. Se realizó un análisis de regresión. Si el coeficiente de correlación r era superior a 0,975 (coeficiente de determinación, r2 ≥ 0,950) el error asociado a la variable X quedaba compensado por el rango de datos y se podía utilizar la regresión lineal simple para calcular la pendiente y la intersección en el origen.
- 4.
Cálculo de la pendiente, la intersección en el origen y la recta de regresión mediante el método de regresión de Passing-Bablok. Para cada método se calculó la pendiente, la intersección en el origen y el intervalo de confianza del 95% (IC=95%).
Si el intervalo de confianza de la intersección no incluía el cero existía una diferencia sistemática de tipo constante entre los 2 métodos. Si el IC de la pendiente no incluía el uno indicaba la existencia de una diferencia sistemática de tipo proporcional entre los métodos. Se repitió el análisis para las muestras con una concentración de 25[OH] vitamina D por el método LIAISON® ≤ 20ng/mL (n=21) y para las muestras con una concentración de 25[OH] vitamina D por el método LIAISON®>20ng/mL (n=19).
Estudio combinado de la precisión. Para cada duplicado se calculó el coeficiente de variación (CV). Se promedió este coeficiente para cada método. Se calcularon y compararon (Prueba de Wilcoxon) las medianas del CV de los distintos métodos.
Los valores de los duplicados de la concentración de 25[OH] vitamina D que se obtuvieron por los 3 métodos se muestran en la tabla 1.
- 1.
En el estudio de reproducibilidad de los duplicados, tanto el método LIAISON® como el método Elecsys presentaron un duplicado por encima del límite de aceptabilidad para la diferencia absoluta individual, aunque estos duplicados no superaron el límite de aceptabilidad al calcular la diferencia absoluta normalizada o relativa, por lo que no fueron excluidos de la comparación (tabla 2) y fue posible continuar con el estudio.
- 2.
En el estudio de los valores extremos (outliers) entre métodos se observó que varios duplicados en las 3 relaciones (LIAISON®- ARCHITECT, LIAISON® - Elecsys y ARCHITECT - Elecsys) superaban el límite de aceptabilidad absoluto pero en ningún caso superaron el límite de aceptabilidad normalizado por lo que no se excluyó ningún duplicado de la comparación (tabla 3) y fue posible continuar con el estudio.
- 3.
Coeficientes de correlación y de determinación entre métodos. En la correlación de LIAISON® con ARCHITECT el coeficiente de correlación de Pearson fue r= 0,976 y el coeficiente de determinación r2=0,953 por lo que el rango de datos de la variable X se consideró adecuado. La correlación de los resultados obtenidos con el método LIAISON® frente a Elecsys y ARCHITECT frente a Elecsys fue estadísticamente significativa aunque los coeficientes de correlación y de determinación, r= 0,967, r2=0,937, p<0,001 y r= 0,943, r2=0,89, p<0,001 respectivamente, no alcanzaban el r=0,975 requerido para cumplir con la adecuación del rango de la variable X. Por este motivo el estudio de las rectas de regresión se realizó mediante la prueba de Passing-Bablock, la cual no tiene requerimientos especiales con respecto a la distribución de las muestras y los errores de medición.
- 4.
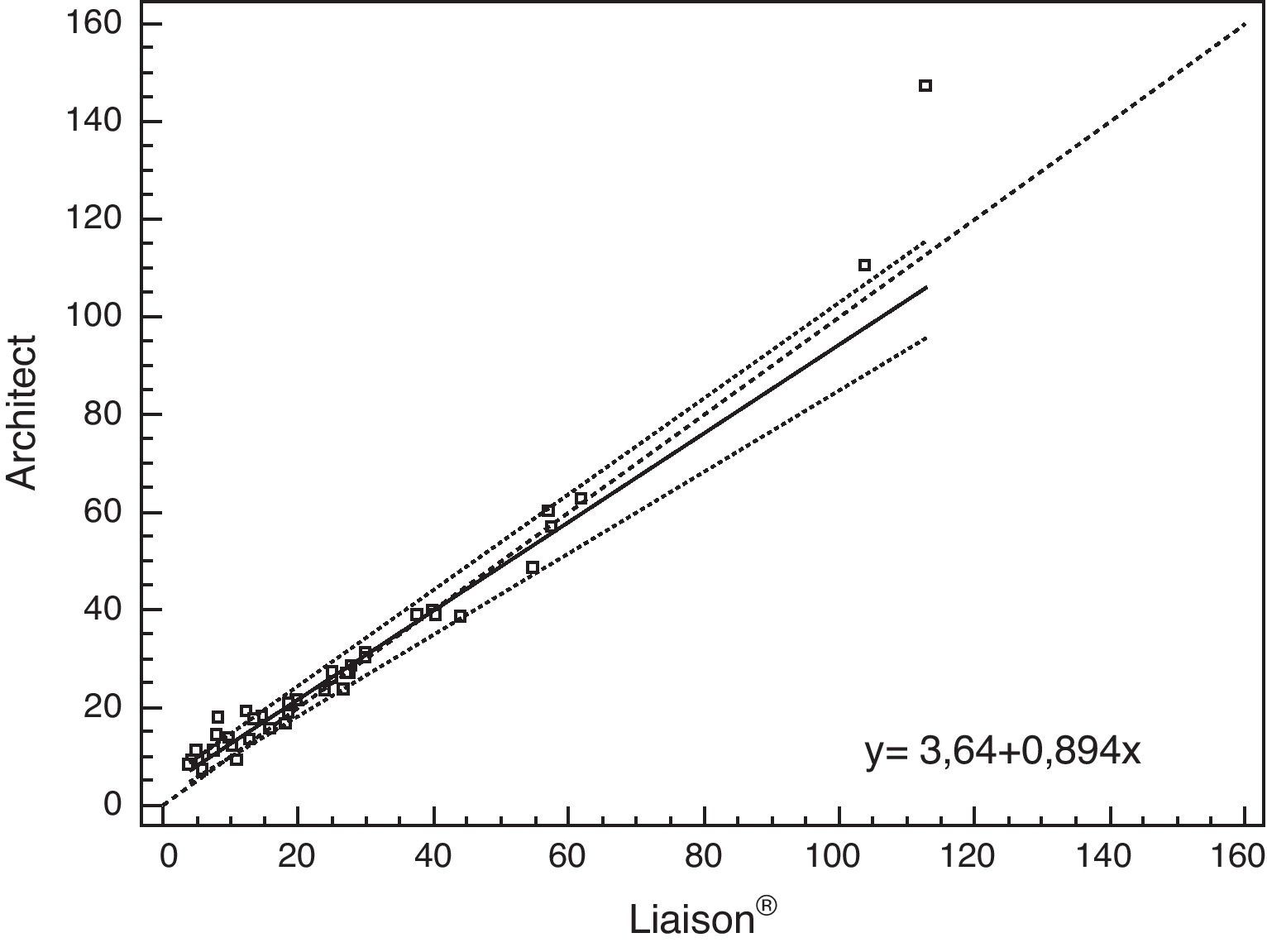
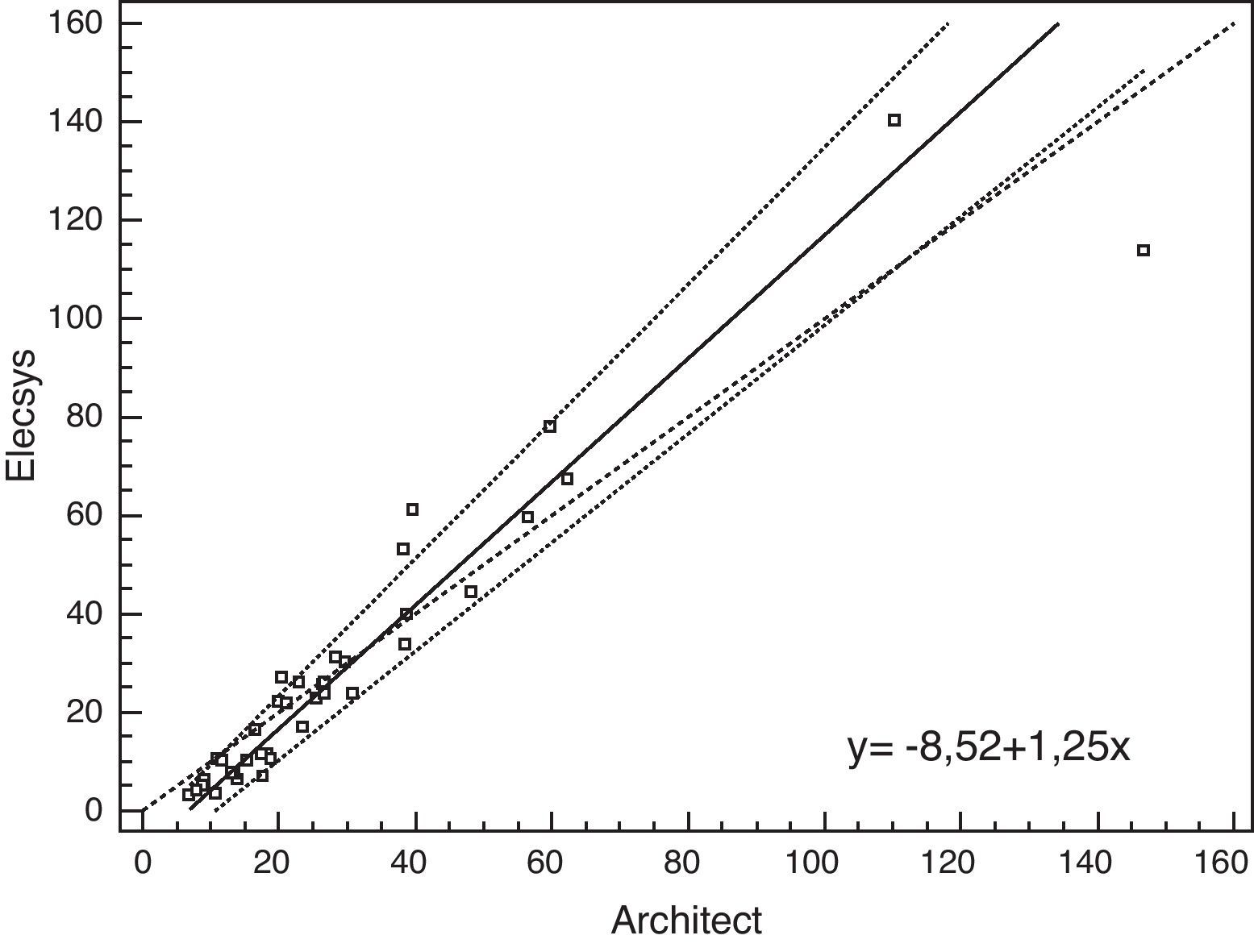
En la tabla 4 se resumen las rectas de regresión obtenidas mediante Passing-Bablok (figs. 1–3), con la pendiente, la ordenada en el origen y los correspondientes intervalos de confianza 95% calculados.
Tabla 4.Rectas de regresión, pendiente e intersección en el origen calculadas mediante el método de Passing-Bablok en todas las muestras, muestras con concentración de 25[OH] vitamina D ≤ 20ng/mL y muestras con concentración de 25[OH] vitamina D >20ng/mL
X LIAISON® 25 OH Vitamina D TOTAL Assay ARCHITECT 25-OH Vitamin D assay Y Todas las muestrasN=40 ARCHITECT 25-OH Vitamin D assay y= 3,64+0,894xIC 95% A: 1,65 - 5,08IC 95% B: 0,82 - 0,97 Elecsys Vitamin D total y= -2,59+1,08xIC 95% A: (-5,18) - (-1,17)IC 95% B: 0,98 -1,22 y= -8,52+1,25xIC 95% A: (-11,65) - (-4,43)IC 95% B: 1,10 -1,39 Muestras con concentración 25[OH] vitamina D ≤ 20ng/mLN=21 ARCHITECT 25-OH Vitamin D assay y= 4,99+0,82xIC 95% A: 2,49-7,37IC 95% B: 0,59-1,06 Elecsys Vitamin D total y= -1,07+0,94xIC 95% A: (-5,33)- 1,44IC 95% B: 0,66-1,38 y= -7,13+1,32xIC 95% A: (-16,75) - (-1,95)IC 95% B: 0,75-1,85 Muestras con concentración 25[OH]vitamina D>20ng/mLN=19 ARCHITECT 25-OH Vitamin D assay y= -1,80+1,04xIC 95% A: (-5,04)-2,11IC 95% B: 0,93-1,15 Elecsys Vitamin D total y= -12,03+1,37xIC 95% A: (-22,64) - (-1,62)IC 95% B: 1,05-1,7 y= -11,55+1,32xIC 95% A: (-19,93) - (-1,4)IC 95% B: 1,04-1,61 Ecuaciones de regresión (y=A+Bx) e intervalos de confianza del 95% (IC 95%) para la intersección en el origen (A) y para la pendiente (B) obtenidos por el método de Passing-Bablok.
Resultados de 25[OH] vitamina D obtenidos por los 3 métodos comparados
| Número muestra | LIAISON® 25 OH Vitamina D TOTAL Assay | ARCHITECT 25-OH Vitamin D assay | Elecsys Vitamin D total | |||
| Resultado 1 (ng/mL) | Resultado 2 (ng/mL) | Resultado 1 (ng/mL) | Resultado 2 (ng/mL) | Resultado 1 (ng/mL) | Resultado 2 (ng/mL) | |
| 1 | 10,20 | 11,80 | 9,8 | 8,5 | 5,83 | 5,97 |
| 2 | 8,70 | 8,12 | 17,5 | 18,2 | 6,64 | 6,59 |
| 3 | 5,43 | 4,88 | 11,4 | 10,3 | 3,68 | 3,00 |
| 4 | 7,90 | 7,17 | 10,3 | 11,8 | 10,76 | 9,88 |
| 5 | 5,54 | 5,20 | 9,6 | 8,7 | 6,93 | 5,29 |
| 6 | 8,37 | 7,70 | 14,1 | 14 | 7,07 | 5,48 |
| 7 | 10,20 | 9,61 | 13,5 | 13,7 | 7,42 | 7,29 |
| 8 | 4,30 | 4,66 | 9,1 | 9,1 | 5,60 | 4,22 |
| 9 | 4,90 | 7,16 | 6,8 | 7,1 | 3,00 | 3,00 |
| 10 | 4,00 | 4,00 | 7,7 | 8,6 | 4,99 | 3,00 |
| 11 | 57,60 | 57,60 | 55,8 | 57,6 | 59,80 | 58,66 |
| 12 | 40,30 | 39,70 | 39,3 | 40,2 | 61,34 | 60,29 |
| 13 | 117,00 | 109,00 | 144,9 | 149,3 | 120,70 | 106,12 |
| 14 | 40,20 | 41,00 | 38,3 | 39 | 34,49 | 32,52 |
| 15 | 57,20 | 57,40 | 60,9 | 59,2 | 76,48 | 79,22 |
| 16 | 61,00 | 63,20 | 62,5 | 62,4 | 68,52 | 65,46 |
| 17 | 43,90 | 44,50 | 38,1 | 38,6 | 54,14 | 51,68 |
| 18 | 38,40 | 37,10 | 38,8 | 38,8 | 40,08 | 39,33 |
| 19 | 104,00 | 104,00 | 109 | 111,7 | 140,00 | 140,00 |
| 20 | 54,40 | 55,50 | 47,3 | 49,3 | 45,49 | 42,77 |
| 21 | 15,20 | 14,30 | 18,4 | 17,9 | 11,77 | 10,82 |
| 22 | 17,40 | 20,10 | 18,9 | 18,2 | 11,99 | 10,63 |
| 23 | 28,00 | 28,00 | 28,9 | 28,1 | 31,96 | 30,28 |
| 24 | 26,50 | 29,10 | 26 | 27,4 | 25,23 | 25,68 |
| 25 | 14,60 | 17,30 | 14,9 | 16 | 10,17 | 9,97 |
| 26 | 20,10 | 18,20 | 20,1 | 20,4 | 22,38 | 21,70 |
| 27 | 16,80 | 19,90 | 17,3 | 15,9 | 16,44 | 16,08 |
| 28 | 12,30 | 12,50 | 18 | 19,9 | 10,71 | 10,08 |
| 29 | 18,90 | 20,80 | 21,8 | 20,9 | 22,42 | 20,63 |
| 30 | 22,90 | 25,40 | 24,1 | 22,4 | 26,83 | 24,98 |
| 31 | 11,40 | 14,60 | 12,2 | 14,2 | 8,23 | 6,87 |
| 32 | 23,60 | 26,70 | 26,1 | 25,3 | 23,04 | 21,84 |
| 33 | 24,10 | 26,20 | 27,3 | 26,6 | 23,73 | 23,46 |
| 34 | 29,50 | 30,90 | 31,4 | 30,6 | 23,63 | 23,15 |
| 35 | 19,10 | 18,50 | 19,4 | 21,6 | 27,59 | 26,15 |
| 36 | 30,50 | 29,60 | 30,5 | 29,4 | 30,79 | 29,17 |
| 37 | 25,20 | 28,70 | 24,2 | 23,1 | 17,25 | 16,13 |
| 38 | 10,10 | 10,80 | 10,9 | 12,8 | 9,76 | 10,26 |
| 39 | 27,60 | 27,20 | 26,7 | 26,8 | 26,50 | 24,88 |
| 40 | 13,20 | 14,30 | 16,9 | 18,2 | 11,31 | 11,24 |
Cuando se utilizaron todas las muestras se observó que existían diferencias constantes y proporcionales entre los resultados de 25[OH] vitamina D obtenidos entre LIAISON® - ARCHITECT y ARCHITECT® - Elecsys, mientras que entre LIAISON® - Elecsys solo existían diferencias constantes.
Al analizar separadamente los resultados de 25[OH] vitamina D de concentración elevada y los de concentración baja, utilizando como punto de corte una concentración de 25[OH] vitamina D=20ng/mL, se observó que cuando la concentración de 25[OH] vitamina D era ≤20ng/mL (tabla 4) los resultados obtenidos entre LIAISON® - ARCHITECT y ARCHITECT - Elecsys presentaban diferencias constantes aunque no proporcionales mientras que entre LIAISON® y Elecsys no existían diferencias de ningún tipo.
Cuando la concentración de 25[OH] vitamina D era>20ng/mL (tabla 4), los resultados obtenidos entre LIAISON® - Elecsys y ARCHITECT - Elecsys presentaban diferencias constantes y proporcionales mientras que entre LIAISON® y ARCHITECT no existían diferencias de ningún tipo.En la tabla 5 se muestran las medianas, rango intercuartílico y rango 95% de los CV de los 40 duplicados para cada método. La mediana del CV obtenida en ARCHITECT fue significativamente inferior a la obtenida con LIAISON® (p<0,01) pero no difirió significativamente de la de Elecsys (p=0,204). Tampoco se hallaron diferencias significativas entre las medianas del CV de LIAISON® respecto a Elecsys (p=0,308).
Estudio combinado de la precisión
| LIAISON® 25 OH Vitamina D TOTAL Assay | ARCHITECT 25-OH Vitamin D assay | Elecsys Vitamin D total | |
| Mediana del CV (%) | 5 | 2,66 | 3,78 |
| Rango intercuartílico | 2,25-7,31 | 1,6-5,96 | 1,4-5,94 |
| Rango 95% | 0-26,5 | 0-11,33 | 0-35,22 |
Medianas, rango intercuartílico y rango 95% de los CV de los 40 duplicados para cada método.
Los 3 métodos muestran una correlación estadísticamente significativa entre sí, como demuestran los elevados coeficientes de correlación hallados. Sin embargo, a pesar de mostrar una buena reproducibilidad y no presentar valores extremos entre ellos, los resultados de 25[OH] vitamina D obtenidos no son intercambiables, ya que también existen diferencias constantes y proporcionales entre los 3 métodos.
La reactividad cruzada referida por los diferentes fabricantes8–10 para las principales formas moleculares de vitamina D (25[OH] vitamina D2, 25[OH] vitamina D3 y 3-epi-25[OH] vitamina D) es variable, lo cual podría explicar las diferencias proporcionales observadas entre los métodos comparados en este estudio, aunque estas diferencias también podrían explicarse por diferencias en la calibración lo cual debería analizarse en futuros estudios. Por otro lado, las diferencias constantes halladas podrían ser debidas a las diferencias en la sensibilidad de los diferentes métodos, lo cual no se ha podido evaluar en este estudio. Al analizar separadamente las muestras con concentraciones de 25[OH] vitamina D ≤20ng/mL y aquellas con concentraciones de 25[OH] vitamina D >20ng/mL se observa que por debajo de este límite solo existen diferencias constantes entre los resultados obtenidos por LIAISON®-ARCHITEC y ARCHITECT- Elecsys. Probablemente esto sea debido a las diferencias en la sensibilidad de los diferentes métodos como hemos especificado anteriormente.
Al analizar el grupo en el que la concentración de 25[OH] vitamina D es >20ng/mL se encuentran diferencias constantes y proporcionales entre los resultados obtenidos entre LIAISON® - Elecsys y ARCHITECT-Elecsys. Esto puede ser explicado en parte porque la linealidad de Elecsys es más baja, de manera que 3 de las muestras fueron diluidas manualmente utilizando un diluyente y no una muestra con concentración baja de 25[OH] vitamina D, introduciéndose de esta forma otra posible fuente de error.
En el estudio de la imprecisión valorada a partir de los CV de los duplicados de cada método la menor imprecisión se obtiene en los resultados obtenidos por ARCHITECT, seguido de Elecsys y LIAISON® (2,66, 3,78 y 5% respectivamente) aunque las diferencias solamente son significativas entre LIAISON® y ARCHITECT.
Una fuente conocida de variabilidad entre diferentes métodos es la falta de una estandarización común internacionalmente aceptada. Hasta la fecha los métodos utilizados para la cuantificación de 25[OH] vitamina D no están calibrados frente a un mismo estándar11–13. Al igual que sucede con los resultados obtenidos en el presente estudio, diferentes autores han observado la existencia de una gran variabilidad en los resultados de 25[OH] vitamina D obtenidos en las mismas muestras tanto entre métodos como entre laboratorios14,15 y se ha demostrado que dicha variabilidad mejoraría notablemente con el uso de un único calibrador estándar16,17. Se ha reportado que la variabilidad entre métodos es tal que un mismo paciente podría ser clasificado como normal o deficitario en función del laboratorio que hubiese determinado esa concentración de 25[OH] vitamina D12,18.
Recientemente el National Institute of Standars and Technology (NIST) ha desarrollado materiales de referencia basados en suero para la medida de 25[OH] vitamina D2 y D3 denominado SRM (972 y 2972)19–21. En 2010 el National Center for Environmental Health (NCEH) propone el uso del SRM 2972 a base de solventes de calibración como material de referencia para la comparación y el ajuste de los calibradores de las casas comerciales así como el uso del suero SRM 972 para la verificación de la calibración a intervalos regulares, lo cual mejoraría no solo la comparabilidad entre los resultados obtenidos entre diferentes inmunoensayos sino también entre estos y los métodos de referencia (HPLC y espectrometría de masas)4,22,23.
Las limitaciones de este estudio incluyen por un lado el pequeño tamaño de la muestra, aunque se han utilizado 40 muestras por duplicado, tal y como indicaba el protocolo CLSI y por otro, que no se ha realizado una evaluación extensa de los 2 métodos que se han comparado con el utilizado en nuestra práctica diaria, ya que queda fuera de los objetivos y posibilidades de este estudio.
En conclusión, la comparación realizada deja patente que los 3 métodos pueden ser utilizados en la práctica diaria aunque cada laboratorio, de manera individual, debe valorarlos a la hora de seleccionar la metodología que más se ajuste a su laboratorio, tipo de muestras y a sus necesidades.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Los autores agradecen a las casas comerciales Roche y Abbot la donación de los reactivos necesarios para poder realizar esta comparación.