La posible falta de correlación entre la concentración de HbsAg del virus de la hepatitis B y la carga viral observada en nuestro hospital, y la gran controversia existente en torno a este aspecto, ha motivado el presente estudio. Adicionalmente, se realizan estudios de eficiencia diagnóstica de la cuantificación de HbsAg para verificar la utilidad real de la introducción de esta determinación en nuestro laboratorio.
MétodosSe han usado 150 muestras de portadores crónicos del virus. Los individuos HbeAg negativos se dividen en 4 grupos: (HbsAg < 1.000 UI/mL [subgrupo 1], HbsAg > 1.000 UI/mL [subgrupo 2], DNA < 2.000 UI/mL [subgrupo 3], DNA > 2.000 UI/mL [subgrupo 4]). Tanto la cuantificación de HbsAg como la determinación cualitativa de HbeAg se han realizado mediante inmunoanálisis quimioluminiscente en el analizador Architect® i2000SR (Abbott Laboratories, Sligo, Irlanda). La carga viral se ha cuantificado mediante PCR a tiempo real (RT-PCR) (Cobas Ampliprep/Cobas TaqMan® de Roche Diagnostics) (Manheim, Alemania). Los estudios de correlación se han realizado mediante la prueba de Spearman utilizando el programa estadístico MedCalc®.
ResultadosLos coeficientes de correlación obtenidos han sido: grupo total HbeAg negativo (r=0,322; p=0,0002); subgrupo 1 (r=0,501; p=0,0001); subgrupo 2 (r=-0,105; p=0,362); subgrupo 3 (r=0,275; p=0,0052); subgrupo 4 (r=0,299; p=0,092).
ConclusiónSe ha observado una modesta pero significante correlación entre las concentraciones séricas de HbsAg y los valores de DNA-VHB en individuos HbeAg negativos.
Possible lack of correlation observed among serum hepatitis B surface antigen (HbsAg) concentration results and viral load in our hospital, and the great controversy surrounding this aspect in the literature, has motivated this study. Additionally, diagnostic efficiency analysis of quantitative HbsAg measurement are done in order to verify the real usefulness of the introduction of this test in our laboratory.
Methods150 hepatitis B chronic carriers samples have been used. Negative HbeAg individuals were divided in four groups (HbsAg < 1,000 UI/mL [subgroup 1], HbsAg > 1,000 UI/mL [subgroup 2], DNA < 2,000 UI/mL [subgroup 3], DNA > 2,000 UI/mL [subgroup 4]). Both quantitative HbsAg and qualitative HbeAg have been performed by a chemiluminiscent immunoassay from Architect® i2000SR analyzer (Abbott Laboratories, Sligo, Ireland). Viral load has been quantified by real time polymerase chain reaction (RT-PCR) (Cobas Ampliprep/Cobas TaqMan® from Roche Diagnostics) (Manheim, Germany). Correlation studies have been performed by the Spearman test. Statistical analysis have been performed using MedCalc® software.
ResultsCorrelation coeficients obtained in this study have been: Total negative HbeAg group (r=0.322; p=.0002); subgroup 1 (r=0.501; p=.0001); subgroup 2 (r=-0.105; p=.362); subgroup 3 (r=0.275; p=.0052); subgroup 4 (r=0.299; p=.092).
ConclusionModest but significant correlation between HbsAg levels and VHB-DNA values in negative HbeAg individuals has been observed.
La infección por el virus de la hepatitis B (VHB) ha evolucionado en los últimos años hasta ser considerada un serio problema de salud pública. Se calcula que una tercera parte de la población mundial ha estado en contacto con el virus y alrededor de 350 millones de personas han desarrollado cronicidad de la infección. Aproximadamente un 30% de estos enfermos crónicos sufrirán una cirrosis o un carcinoma hepatocelular1.
Con el fin de evitar el desarrollo de estas complicaciones, es de vital importancia el seguimiento estricto de estos portadores crónicos. Tradicionalmente, este seguimiento se ha llevado a cabo mediante determinaciones periódicas de la carga viral, pero las amplias y frecuentes fluctuaciones de los valores de DNA del VHB obligan a la realización de diversas determinaciones separadas por intervalos de meses con tal de poder realizar un diagnóstico definitivo que permita diferenciar los portadores crónicos activos de los inactivos. Además, a pesar de que esta técnica se ha automatizado totalmente en los últimos años, continúa teniendo un coste elevado.
Por otro lado, la determinación del antígeno de superficie del virus de la hepatitis B (HbsAg), es considerada como la piedra angular en el diagnóstico de la infección, motivo por el que ha sido ampliamente utilizada durante décadas.
Numerosos estudios sugieren que la cuantificación de HbsAg es un potente marcador en el seguimiento de estos pacientes y, por este motivo, se están desarrollando nuevos métodos capaces de cuantificar el antígeno de superficie en sangre.
La introducción de esta determinación ha cambiado completamente el panorama de estos pacientes. Diversos autores afirman que, la combinación en una sola determinación de concentraciones de HbsAg < 1.000 UI/mL y valores de DNA-VHB < 2.000 UI/mL es capaz de identificar los portadores inactivos de la enfermedad de forma comparable con un estrecho seguimiento a largo plazo2–4, lo que supone una importante reducción del gasto, dado que evita un gran número de determinaciones analíticas así como de visitas a consultas externas.
Una primera revisión de los resultados obtenidos al introducir la determinación cuantitativa de HbsAg en nuestro hospital, pone de manifiesto una posible falta de correlación entre esta medida y la determinación de la carga viral del VHB. La posterior revisión bibliográfica, derivada de esta observación, permite evidenciar la gran controversia existente en torno a este aspecto5–8, motivo por el cual se plantea el presente estudio.
De manera adicional, se realizan estudios de la eficiencia diagnóstica de esta nueva determinación con el fin de verificar la utilidad real de la introducción de esta prueba en nuestro laboratorio.
Material y métodosPara la realización de este estudio se han utilizado 150 muestras de pacientes, en seguimiento por la Unidad de Hepatología del Hospital Parc Taulí de Sabadell, todos ellos portadores crónicos de la enfermedad, el 91% presentaban el antígeno e del VHB (HbeAg) negativo.
En cada muestra se determina la concentración de HbsAg mediante un inmunoanálisis quimioluminiscente en el analizador automatizado Architect® i2000SR (Abbott Laboratories, Sligo, Irlanda), con un intervalo de medida comprendido entre 0,05–250 UI/mL. En este mismo analizador, se determina cualitativamente la positividad o negatividad de HbeAg mediante un inmunoanálisis quimioluminiscente.
Paralelamente, se determina la carga viral mediante una reacción en cadena de la polimerasa a tiempo real (RT-PCR) en el analizador automatizado Cobas Ampliprep/Cobas TaqMan® de Roche Diagnostics (Manheim, Alemania) (intervalo de medida: 20 – 17*108 UI/mL).
Tras haber analizado la distribución de los datos mediante la prueba de Kolmogorov-Smirnov, se realizan estudios de correlación no paramétricos mediante la prueba de Spearman.
Para la realización de los diferentes análisis de correlación, se agrupan los individuos según si presentan HBeAg negativo o positivo y, dentro del grupo con HbeAg negativo, se realizan diferentes subgrupos según cuál sea su concentración de HBsAg y su carga viral.
Siempre y cuando la correlación sea significativa (p < 0,05), se considerará que existe una correlación perfecta con valores del coeficiente rho cercanos a 1 y una correlación mínima o nula con valores de rho cercanos a 0.
Todos estos cálculos se realizan mediante el programa estadístico Medcalc®.
La eficiencia diagnóstica de la interpretación conjunta de las mediciones de la concentración de HbsAg y de DNA del virus B, se calcula dividiendo el número de determinaciones en las que se cumple el criterio de que cuando la concentración de HbsAg es < 1.000 UI/mL, el valor de DNA es < 2.000 UI/mL y cuando la concentración de HbsAg es > 1.000 UI/mL el valor de DNA es > 2.000 UI/mL, por el número total de determinaciones. De manera adicional, también se calcula la eficiencia diagnóstica en el grupo de individuos con DNA < 2.000 UI/mL, dado que este grupo es candidato a ser portador inactivo de la enfermedad.
ResultadosDe los 150 pacientes, 78 eran hombres y 72 mujeres, con edades comprendidas entre 25 y 86 años (media de edad de 49 años).
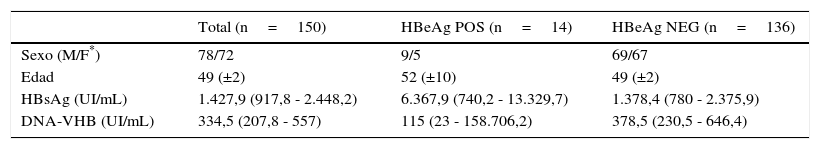
En el grupo de 136 individuos con el HBeAg negativo, las concentraciones de HBsAg han oscilado entre 0,2 y 43.070 UI/mL (mediana=1.378,4 UI/mL) y los valores de DNA entre 20 y 2.094.907 UI/mL (mediana=334,5 UI/mL). En el grupo de 14 individuos HBeAg positivo en cambio, las concentraciones de HBsAg han oscilado entre 108 y 15.725 UI/mL (mediana=6.367,9 UI/mL) y los valores de DNA entre 20 y 1.684.715 UI/mL (mediana=115 UI/mL) (tabla 1).
Población incluida en el estudio según sexo, edad y medianas de concentración de HbsAg y DNA-VHB con un intervalo de confianza del 95%
| Total (n=150) | HBeAg POS (n=14) | HBeAg NEG (n=136) | |
|---|---|---|---|
| Sexo (M/F*) | 78/72 | 9/5 | 69/67 |
| Edad | 49 (±2) | 52 (±10) | 49 (±2) |
| HBsAg (UI/mL) | 1.427,9 (917,8 - 2.448,2) | 6.367,9 (740,2 - 13.329,7) | 1.378,4 (780 - 2.375,9) |
| DNA-VHB (UI/mL) | 334,5 (207,8 - 557) | 115 (23 - 158.706,2) | 378,5 (230,5 - 646,4) |
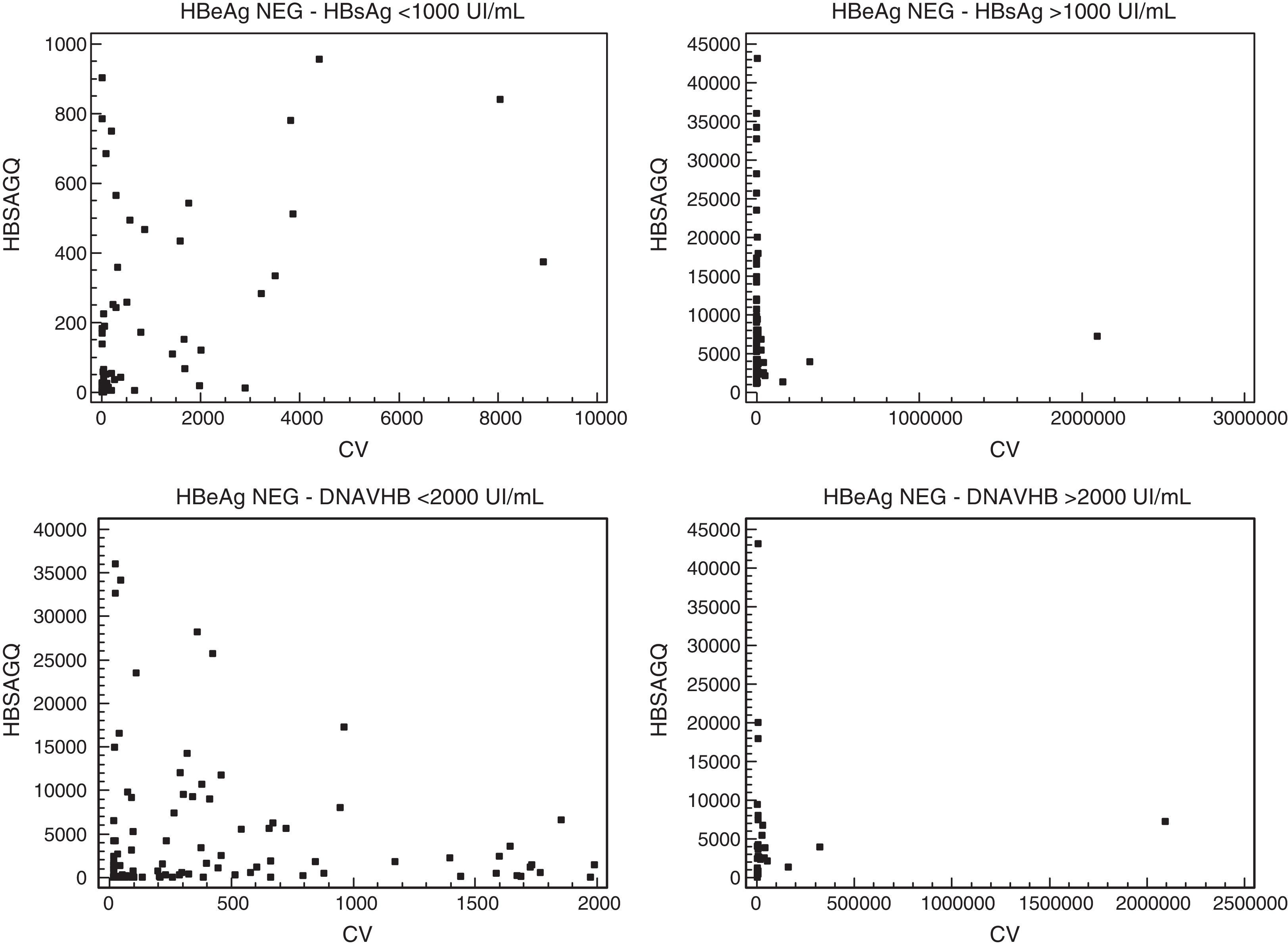
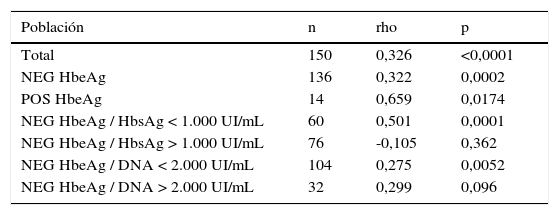
Tal y como se puede observar en la tabla 2, existe una baja correlación entre HbsAg y DNA en el grupo total de individuos incluidos en el estudio (r=0,326; p<0,0001). Dentro del grupo de individuos HbeAg negativo, la correlación obtenida es similar (r=0,322; p=0,0002), no siendo así en el grupo HbeAg positivo, en los que se observa una buena correlación (r=0,659; p=0,0174). Debido al reducido número de individuos integrantes en este último grupo, el estudio se ha centrado en el grupo que presenta HbeAg negativo. Dentro de este grupo, la correlación obtenida en el subgrupo de individuos con concentración de HbsAg < 1.000 UI/mL ha sido moderada (r=0,501; p=0,0001) pero en el subgrupo con concentración de HbsAg > 1.000 UI/mL, ha sido inexistente (r=-0,105; p=0,362). Finalmente, también se ha clasificado a los individuos según sus valores de DNA, y se ha observado únicamente correlación (débil) en el grupo con DNA < 2.000 UI/mL (r=0,275; p=0,0052 vsr=0,299; p=0,092) (fig. 1).
Resultados de correlación entre la determinación cuantitativa de HbsAg y la carga viral del virus de la hepatitis B en los diferentes grupos del estudio
| Población | n | rho | p |
|---|---|---|---|
| Total | 150 | 0,326 | <0,0001 |
| NEG HbeAg | 136 | 0,322 | 0,0002 |
| POS HbeAg | 14 | 0,659 | 0,0174 |
| NEG HbeAg / HbsAg < 1.000 UI/mL | 60 | 0,501 | 0,0001 |
| NEG HbeAg / HbsAg > 1.000 UI/mL | 76 | -0,105 | 0,362 |
| NEG HbeAg / DNA < 2.000 UI/mL | 104 | 0,275 | 0,0052 |
| NEG HbeAg / DNA > 2.000 UI/mL | 32 | 0,299 | 0,096 |
La eficiencia diagnóstica obtenida para la interpretación conjunta de la concentración de HbsAg y de los valores de DNA del virus B en la población total del estudio ha sido de 53,30%. La eficiencia diagnóstica en el grupo que presenta valores de DNA < 2.000 UI/mL ha sido de 46,15%.
DiscusiónLos resultados obtenidos concuerdan con los publicados por diferentes autores que afirman haber observado una correlación modesta pero significativa entre las concentraciones de HbsAg del virus B y los valores de DNA del mismo virus en individuos con HbeAg negativo5,8–13 y están en contraposición con aquellos estudios que niegan la existencia de dicha correlación6,7,14,15.
Cabe decir que, a pesar de que la correlación observada entre estas dos determinaciones es muy pobre, se ha observado una correlación más fuerte en el grupo de individuos que presentaba concentraciones de HbsAg < 1.000 UI/mL. Este hecho contrasta con la ausencia total de correlación existente en el grupo de individuos con concentraciones de HbsAg > 1.000 UI/mL.
Probablemente, la controversia existente en la bibliografía pueda ser debida a la diferente estratificación de las poblaciones estudiadas (diferentes estadios de la enfermedad, grado de fibrosis, etc.) o bien, tal y como sugieren algunos estudios16, esta correlación pueda estar ligada a un determinado genotipo del virus.
Teniendo en cuenta la correlación tan pobre obtenida en los individuos con valores de DNA < 2.000 UI/mL y nula en aquellos con valores de DNA > 2.000 UI/mL, se plantea la duda sobre la utilidad real de la cuantificación del antígeno de superficie del virus B en la detección de portadores crónicos inactivos de la enfermedad. Los resultados de nuestro estudio, muestran una eficiencia diagnóstica únicamente del 46,15% en el grupo de pacientes con DNA < 2.000 UI/mL, que es el grupo en el que clínicamente se tendrán realmente dudas en la clasificación como portadores activos o inactivos.
Probablemente, sería conveniente estratificar mejor a los pacientes antes de solicitar la cuantificación del antígeno de superficie al laboratorio, si lo que se desea obtener es una información clínicamente útil para realizar el seguimiento de estos pacientes.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.