La enfermedad de Von Willebrand (EVW) constituye la diátesis hemorrágica hereditaria más frecuente, con una prevalencia estimada del 0,6-1,3% en la población general1,2, cifras que se elevan al 2% según algunos autores3. Fue descrita en 1926 por Erik Von Willebrand4. Solo uno de cada 10.0002 pacientes presenta trastornos hemorrágicos importantes. Se muetra un caso de una paciente de 48 años y 60kg de peso con antecedentes personales de EVW tipo 2B, episodios de rectorragia y menorragia y, como antecedentes quirúrgicos, 2 cesáreas. Precisó intervención quirúrgica urgente por dolor abdominal con signos de irritación peritoneal. En el estudio realizado por Hematología se observaron valores normales de antígeno del factor de Von Willebrand (FVW:Ag), capacidad del plasma de aglutinar plaquetas utilizando la ristocetina como cofactor (FVW: CoR) de 22,6UI/dL (50-150), actividad del factor de Von Willebrand (FVW) de 27,6% (50-200%)2 y factor VIII (FVIII) de 52UI/dL (50-150). El resto de los estudios fueron normales. Tras valoración del caso conjuntamente por hematólogos, ginecólogos y anestesiólogos se decidió la administración preoperatoria de 3.000UI de concentrado de FVW/FVIII (Fandhi®, Instituto Grifols S.A., Barcelona, España) y 500mg de ácido tranexámico, que fue continuado cada 6h el día de la intervención quirúrgica. En el quirófano se monitorizó la presión arterial no invasiva, la saturación periférica de oxígeno y el electrocardiograma. Se canalizaron 2 vías periféricas de grueso calibre. Tras inducción intravenosa con 140mg de propofol, 150μg de fentanilo y 50mg de rocuronio e intubación orotraqueal, se realizó una laparotomía exploradora que mostró un folículo hemorrágico y requirió una salpingooforectomía izquierda. La anestesia se mantuvo con sevoflurano 1CAM y remifentanilo en infusión continua según requerimientos analgésicos, presentando un sangrado intraoperatorio de 400mL. Tras finalizar el procedimiento se administraron 150μg de fentanilo y 1g de paracetamol para mantener un adecuado nivel de analgesia, siendo revertido el bloqueo neuromuscular con 0,6mg de atropina y 2,5mg de neostigmina, extubándose sin incidencias. Se mantuvo un buen control hemodinámico en el periodo postoperatorio, realizándose determinaciones según protocolo de niveles plasmáticos de FVW:CoR y de FVIII, y terapia con 2.000UI de concentrado de FVW/FVIII cada 24h en los 5 días siguientes a la intervención quirúrgica, sin observarse episodios hemorrágicos. Se inició una profilaxis tromboembólica con heparina de bajo peso molecular.
El FVW es una glucoproteína segregada por las células endoteliales y los megacariocitos, que circula en el plasma en multímeros de alto peso molecular. Presenta importantes implicaciones en la hemostasia2, fijándose al complejo receptor glucoproteico plaquetario glucoproteína 1b/IX, iniciando la adherencia plaquetaria al subendotelio lesionado y la posterior activación plaquetaria, ocasionando la exposición del receptor integrina glucoproteína 2b/3a a través del cual el FVW y el fibrinógeno intervienen en la agregación plaquetaria2. Por otro lado, el FVW se encarga del trasporte del cofactor procoagulante FVIII2. Los niveles bajos del FVW o una fijación defectuosa del FVW al FVIII disminuyen los niveles del FVIII porque se acelera su proteolisis2. Clínicamente se manifiesta de forma variable en función de su severidad, oscilando desde sangrado mucocutáneo y hematomas, estando presente hasta en el 20% de los casos de pacientes con menorragia5, hasta un cuadro clínico indistinguible de la hemofilia con hemartros y hematomas musculares5. Se asocia a hemorragia excesiva en intervenciones quirúrgicas4. Esta afección puede estar producida por un déficit cuantitativo del FVW (tipos 1 y 3) o cualitativo (tipo 2). El tipo 1 es el más frecuente (70-80% de los casos), consistente4 en una disminución en los niveles del FVW del 20 al 50%. Los niveles plasmáticos habituales de FVW son de 10μg/mL (100%)2. El tipo 2 se subdivide en 2A, 2B, 2M y 2N2. En la EVW el patrón de herencia es autosómico dominante en todos los casos, excepto en el tipo 2N y 34. El diagnóstico de la EVW se basa en un riguroso interrogatorio preoperatorio, investigando sangrado mucocutáneo, menorragia, epistaxis, hemorragias posparto o posquirúrgicas previas, etc., y en pruebas de laboratorio específicas e inespecíficas. Dentro de las pruebas inespecíficas podemos observar un tiempo de hemorragia prolongado y de tromboplastina parcial activado discretamente prolongado si existe una disminución del FVIII, pero unos valores normales en estas determinaciones no excluyen la enfermedad2,4. Para un diagnóstico definitivo se precisan 3 tests diagnósticos específicos5, la medida de la actividad del FVIII, y medición de los niveles plasmáticos del FVW:Ag y de la capacidad funcional del FVW en el plasma, determinada por el FVW:CoR. Mientras que en la EVW tipo 1 y tipo 3 existe un déficit cuantitativo con valores bajos de FVW:Ag y FVW:CoR, en nuestro caso, un tipo 2, existe un déficit cualitativo, de modo que se observaron niveles normales de FVW:Ag, pero marcada disminución de los niveles de FVW:CoR4. Ante la sospecha de un tipo 2 de EVW, se recomienda la determinación de la relación FVW:CoR/FVW:Ag, que será menor de 0,64 (tabla 1). La EVW tipo 2B es una forma infrecuente de la enfermedad, que solo supone el 1% de los casos6, presentando una serie de peculiaridades que la diferencian del resto de los tipos1,5. Se trata de un defecto de «ganancia de función»2,4 con una mayor fijación del FVW a la glucoproteína 1b plaquetaria y mayor aclaramiento de este complejo2,7, por lo que se poduce trombocitopenia por formación de agregados plaquetarios4 circulantes, así como una depleción de los multímeros de alto peso molecular que componen al FVW7. La historia familiar suele ser claramente positiva, a diferencia del tipo 12. Este subtipo de EVW presenta una serie de peculiaridades en su estrategia terapéutica y un manejo perioperatorio que la diferencian de los demás tipos. El abordaje terapéutico sigue las siguientes estrategias: aumentar los niveles o la actividad del FVW intrínseco, administrar concentrados exógenos de FVW/FVIII y optimizar las vías alternativas protrombóticas o disminuir la fibrinólisis4. Las estrategias para prevenir o controlar el sangrado en pacientes con EVW se realizan en caso de cirugía mayor, traumatismos y hemorragias con riesgo vital e incluyen la desmopresina, los concentrados de FVW y FVIII, el crioprecipitado, los fármacos antifibrinolícos y los concentrados de plaquetas, que solo están indicados cuando el trastorno de coagulación persiste a pesar de valores de FVIII normales1. Aunque el tratamiento con desmopresina está indicado en la EVW tipo 1 y 2A por estimular la liberación de FVW por las células endoteliales2, en el subtipo 2B está contraindicada por aumento del riesgo de trombocitopenia transitoria tras la liberación del FVW mutado2. La administración de concentrados derivados plasmáticos de FVW y FVIII, sometido a técnicas de inactivación viral, a dosis de 50UI/kg−1 el día de la cirugía y los días posteriores en función del riesgo hemorrágico, constituye el tratamiento de elección4. Se aconseja una monitorización plasmática de la actividad del FVIII y FVW:CoR cada 12h el día de la intervención quirúrgica y cada 24 h los días posteriores4, manteniendo una actividad plasmática de FVIII entre 80 y 100% (50UI/dL) el primer día postoperatorio y mayor del 50% durante los 5-10 siguientes1,4, y de FVW:CoR de 30UI/dL4. La actividad del FVIII es el determinante más importante de hemorragia quirúrgica en la EVW, siendo su medida de vital importancia para reducir el riesgo de tromboembolismo venoso asociado a valores elevados e instaurar una terapia profiláctica con heparina de bajo peso molecular1. El fármaco antifibrinolítico ácido tranexámico ha sido empleado como terapia adyuvante, inhibiendo la conversión de plasminógeno en plasmina y manteniendo la estabilidad del coágulo1. El crioprecipitado no constituye la primera elección por su alto riesgo de transmisión viral2,7. En los pacientes con EVW refractaria a esta primera línea de tratamiento está indicada la realización de plasmaféresis4. Aunque se recomienda un abordaje multidisciplinar y la valoración por un hematólogo previa a un procedimiento quirúrgico electivo, no siempre es factible en los casos urgentes4, por lo que se deberían establecer estrategias terapéuticas4 adaptadas al subtipo de esta afección para reducir las pérdidas sanguíneas intraoperatorias y evitar la administración de productos recombinantes derivados del plasma y hemoderivados, reduciendo, por tanto, los costes asociados al uso de estos productos, así como la exposición innecesaria a agentes infecciosos7.
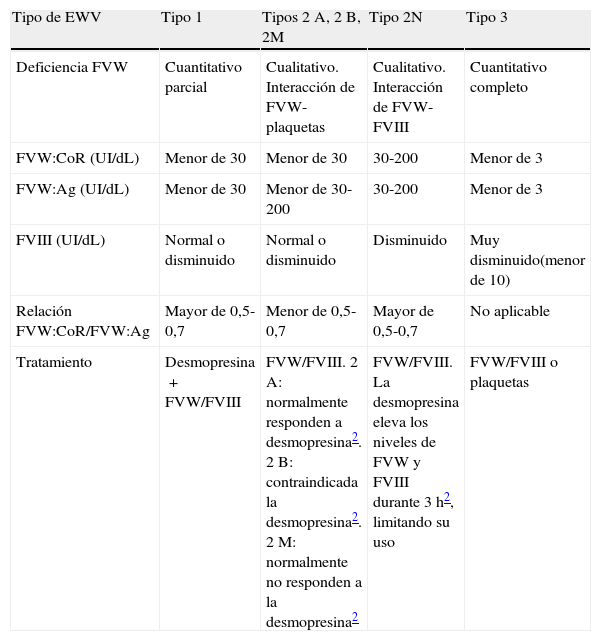
Diagnóstico diferencial entre los distintos subtipos de enfermedad de Von Willebrand y enfoque terapéutico
| Tipo de EWV | Tipo 1 | Tipos 2A, 2B, 2M | Tipo 2N | Tipo 3 |
| Deficiencia FVW | Cuantitativo parcial | Cualitativo. Interacción de FVW-plaquetas | Cualitativo. Interacción de FVW-FVIII | Cuantitativo completo |
| FVW:CoR (UI/dL) | Menor de 30 | Menor de 30 | 30-200 | Menor de 3 |
| FVW:Ag (UI/dL) | Menor de 30 | Menor de 30-200 | 30-200 | Menor de 3 |
| FVIII (UI/dL) | Normal o disminuido | Normal o disminuido | Disminuido | Muy disminuido(menor de 10) |
| Relación FVW:CoR/FVW:Ag | Mayor de 0,5-0,7 | Menor de 0,5-0,7 | Mayor de 0,5-0,7 | No aplicable |
| Tratamiento | Desmopresina+FVW/FVIII | FVW/FVIII. 2A: normalmente responden a desmopresina2. 2B: contraindicada la desmopresina2. 2M: normalmente no responden a la desmopresina2 | FVW/FVIII. La desmopresina eleva los niveles de FVW y FVIII durante 3h2, limitando su uso | FVW/FVIII o plaquetas |
EVW: enfermedad de Von Willebrand; FVW: factor de Von Willebrand; FVW:Ag: antígeno del factor de Von Willebrand; FVW:CoR: ristocetina como cofactor para test de aglutinación plaquetaria; FVIII: factor de coagulación VIII.
Modificada de Maquoi et al.1.