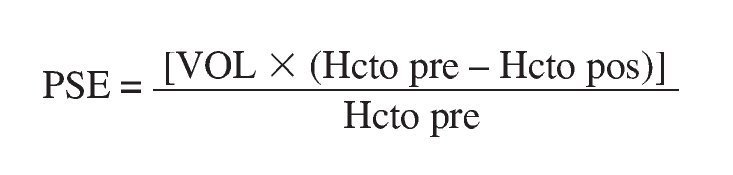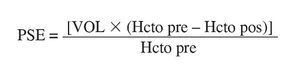La cirugía sin sangre es una propuesta terapéutica, que consiste en minimizar el uso de la transfusión sanguínea alógena. Ott y Cooley1 publicaron en el año 1977 su experiencia de veinte años en cirugía cardíaca abierta con 542 Testigos de Jehová. Esta idea fue seguida posteriormente por otros cirujanos y ampliándose de forma progresiva con múltiples referencias en la literatura sobre el tratamiento de estos pacientes en las diversas especialidades médicas y quirúrgicas.
Actualmente se donan cada año 75 millones de unidades de sangre a nivel mundial. El término "sangre segura" es relativo, ya que la transfusión sanguínea en los países del primer mundo también supone un riesgo de contraer una enfermedad.
Probablemente los riesgos mayores son los relacionados con el virus de la inmunodeficiencia humana (VIH) (1:1,5-2 millones), virus de la hepatitis B (VHB) (1:100.000) y virus de la hepatitis C (VHC) (1:60.000). Por otra parte, nos encontramos con otras enfermedades de las que todavía hoy no conocemos con exactitud cuál es su incidencia de transmisión en las transfusiones (Creutzfeld-Jakobs, citomegalovirus, simian foamy virus [SFV], West Nile virus [WNV], etc.).
Para poder calcular las necesidades transfusionales de cada paciente se realizaron en los años noventa diversos estudios valorando diversas variables. Así, por ejemplo, Nelson et al sugirieron la siguiente fórmula:
Donde PSE es la pérdida de sangre estimada, VOL el volumen total de sangre y Hcto el hematocrito.
En otro estudio, Larocque clasificó a los pacientes valorando una serie de variables como los niveles de hemoglobina (Hb) preoperatoria, el peso, el tipo de cirugía (rodilla, cadera), la uni o bilateralidad y si era cirugía primaria o de revisión para, de esta manera, intentar predecir la posibilidad de transfusión en prótesis de rodilla y cadera realizando un sistema de puntuación. Asimismo se sabe que la transfusión alógena produce inmunomodulación2. Esto fue descrito por Opelz, que demostró una mejora en la supervivencia de los pacientes a los que se les trasplantó un riñón y se les había realizado una transfusión.
Esto, que sin duda es beneficioso para algunas enfermedades, es perjudicial para otras3. De hecho, se ha visto un aumento de la recurrencia del cáncer colorrectal en pacientes operados con resección y que habían recibido una transfusión alógena.
No obstante, en lo único que hay unanimidad en todos los estudios publicados es que el principal valor predictivo de la necesidad de transfusión es el nivel de Hb preoperatoria4,5. Todos los demás (peso, talla, edad, sexo) están muy cuestionados.
En nuestra especialidad se ha empezado a observar que los pacientes que reciben una transfusión alógena presentan un mayor índice de infección postoperatoria (nosocomial y posquirúrgica)6. La donación de sangre en nuestro país es totalmente altruista, así como en otros 80 países, entre los que se encuentran prácticamente todos los europeos y el número de donantes activos se sitúa en unos 90 millones en todo el mundo.
Los objetivos de este trabajo han sido los siguientes:
1) Objetivo general: intentar disminuir el índice transfusional obtenido en la cohorte histórica (57,3%), aplicando métodos de ahorro de sangre. Consideramos un objetivo realista conseguir un índice transfusional por debajo del 10%.
2) Objetivos operativos: a) valorar la eficacia de cada uno de los métodos de ahorro de sangre utilizados: eritropoyetina (EPO), autotransfusión-predonación y Redon recuperador, umbral de transfusión; y b) valorar coste/beneficio de las técnicas de ahorro de sangre en un hospital terciario.
MATERIAL Y MÉTODO
Se ha realizado un estudio de cohortes, que consta de una cohorte actual y otra histórica de control. La cohorte histórica la forman 193 pacientes, a los que se les colocaron 197 prótesis totales de rodilla durante el año 2002. Todos los pacientes fueron operados en el Hospital Donostia. La cohorte actual la forman 105 pacientes, a los que se les colocaron 107 prótesis totales de rodilla desde mayo de 2004 hasta agosto de 2005. Todos los pacientes fueron operados en el Hospital Donostia. El estudio se realizó con la aprobación del Comité Ético de nuestro hospital.
Se fijaron criterios de inclusión y de exclusión en ambos grupos. En el grupo histórico se incluyeron todos los pacientes que acudieron a la consulta del Servicio de Cirugía Ortopédica y Traumatología (COT) del Hospital Donostia y se les indicó prótesis total de rodilla y fueron operados en el año 2002. En el grupo actual se incluyeron todos los pacientes vistos en la consulta por los cirujanos participantes en el estudio y que fueron operados desde mayo del 2004 hasta agosto de 2005.
Los criterios de exclusión fueron: mayores de 80 años y pacientes en tratamiento con dicumarínicos.
Se han colocado tres modelos de prótesis: Duracon, Génesis II y LCS (en 5 casos y sólo en el grupo actual). En ambas cohortes, la profilaxis antibiótica se realizó con cefazolina IV, administrando 2 g previamente a la inducción anestésica (monodosis). La profilaxis tromboembólica se realizó en ambas cohortes con enoxaparina 40 mg por vía subcutánea (sc) cada 24 horas durante 4 semanas.
En la cohorte histórica, el tipo de prótesis utilizadas ha sido el siguiente: Duracon: 152 implantes (134 conservando el LCP [88,1%] y 18 sin conservar el LCP [11,9%]); y Génesis: 45 implantes (26 conservando el LCP [57,7%] y 19 sin conservar el LCP [22,3%]).
En la cohorte actual se han utilizado las siguientes prótesis: Duracon: 79 implantes (43 conservando el LCP [54,4%] y 36 sin conservar el LCP [45,6%]); Génesis: 23 implantes (8 conservando el LCP [34,8%] y 5 sin conservar el LCP [65,2%]); y LCS: 5 implantes, todos ellos conservando el LCP.
En la cohorte histórica, 190 prótesis fueron cementadas y 7 sin cementar. En la cohorte actual, las 107 prótesis fueron cementadas.
Variables estudiadas
1) Variables de identificación: nombre, apellidos y número de historia clínica.
2) Variables cuantitativas: nivel de Hb (g/dl), nivel de presión arterial (mmHg), estudio de anemia (ácido fólico [ng/ml], hierro μg/dl], transferrina [mg/dl], ferritina [ng/ml], vitamina B12 [pg/dl], saturación de transferrina [%]) y edad.
3) Variables categóricas: sexo (hombre: 0, mujer: 1), tipo de enfermedad previa (sí: 0, no: 1), administración de EPO (sí: 0, no: 1), transfusión alógena (sí: 0, no: 1), transfusión predonación (sí: 0, no: 1), incidencias en la cirugía (sí: 0, no: 1), incidencias en el Redon recuperador (sí 0, no: 1), incidencias en la evolución (sí: 0, no: 1), tipo de patología (artrosis: 1, artritis reumatoide: 2, otras: 3), tipo de anestesia (regional + sedación: 1, regional + sedación + catéter epidural: 2, general: 3), clasificación según la American Society of Anesthesiology (ASA I: 1, ASA II: 2, ASA III: 3, ASA IV: 4, ASA V: 5).
Distribución por grupos
Siendo la Hb preoperatoria el factor predictivo más importante conocido para valorar la probabilidad de transfusión alógena, hemos dividido a los pacientes de cada cohorte en tres grupos.
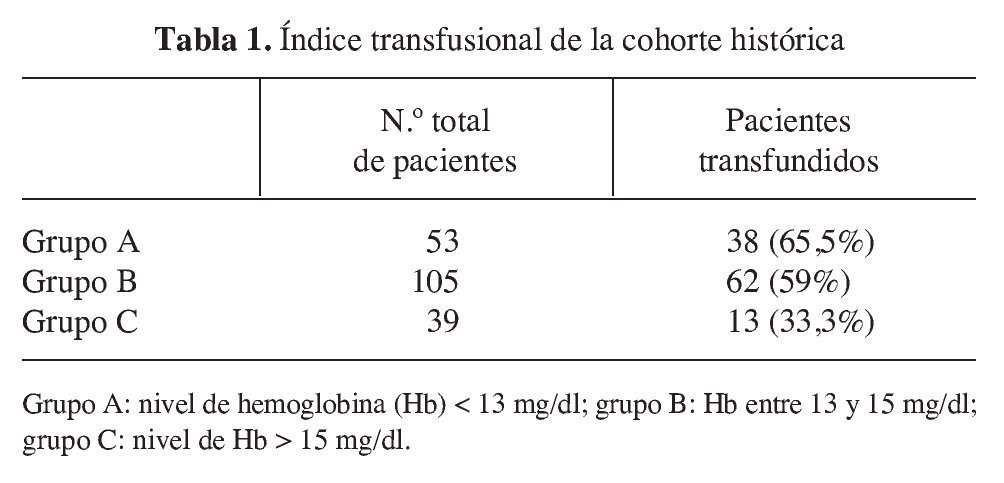
1) Grupo A: nivel de Hb < 13 mg/dl.
2) Grupo B: nivel de Hb entre 13-15 mg/dl.
3) Grupo C: nivel de Hb > 15 mg/dl.
Para cada uno de los tres grupos de la cohorte actual se ha diseñado un protocolo de actuación en la fase preoperatoria, así como en la intraoperatoria y en la posoperatoria7,8.
Fase preoperatoria
1) Grupo A: debido a que la probabilidad de transfusión en este grupo de pacientes es muy elevada, se les suministraba EPO. Si había alguna contraindicación para su uso, no se le hacía el tratamiento, pero se le incluía en el estudio. La dosificación fue de 40.000 UI/sc en 4 administraciones semanales, que comenzaron el día 21 preoperatorio, siguieron los días 14 y 7 preoperatorio, y la última dosis fue el mismo día de la cirugía. En el caso de que se hubieran superado los 15 g/dl de Hb y quedara alguna dosis por poner, ésta se suspendería. Durante todo el tratamiento el paciente se complementaba con 240 mg de sulfato ferroso diarios.
2) Grupo B: estos pacientes se encuentran en un nivel medio de probabilidad de transfusión y se les ha protocolizado para entrar en un programa de autotransfusión-predonación. Una vez visto el nivel de Hb en el estudio preoperatorio, se fijaba la fecha de la intervención y, con un mínimo de tres semanas previas a dicha fecha, los pacientes eran enviados al banco de sangre para la extracción de dos unidades de sangre completa. Además, tenían que tomar 240 mg de sulfato ferroso diarios.
3) Grupo C: a estos pacientes, al ser de baja probabilidad de transfusión, no se les ha indicado ningún tipo de actuación en esta fase.
Fase quirúrgica
En esta fase se protocolizó el uso de la isquemia de principio a fin de la intervención en todos los pacientes. La isquemia se retiró una vez colocado el drenaje de Redon recuperador9,10.
Se recomendó el uso de bisturí eléctrico, una vez hecha la incisión de la piel, y realizar la incisión quirúrgica lo más pequeña posible en todos los pacientes. En ningún caso se realizó una técnica mínimamente invasiva (MIS).
Fase postoperatoria
En esta fase todos los grupos tenían que seguir la misma pauta de protocolo.
1) Redon recuperador: se protocolizó el uso del modelo Consta VacTM CBC II Stryker®. El recuperador aporta un filtro para retransfundir la sangre, que es el convencional de 200 micras, y se ha sustituido por uno de 40 micras por mayor seguridad para recuperar y transfundir la sangre drenada durante las primeras 4-6 horas posoperatorias9.
2) Umbral de transfusión: los márgenes adecuados se sitúan entre 7-10 g/dl de Hb y luego, en función de la situación clínica de cada paciente11, se tomó la decisión de transfundir. El estado de salud se clasifica según la ASA12. Todos los pacientes tomaron 240 mg del sulfato ferroso diarios en ayunas (dos comprimidos en el desayuno y uno en la cena), durante las tres semanas siguientes a la cirugía.
Métodos estadísticos
Los datos incluidos en el editor del paquete estadístico Systat fueron evaluados mediante un análisis preliminar para detectar incongruencias, valores fuera del rango lógico, alteraciones de los criterios de reclutamiento, etc. La detección de los errores y la posterior corrección se realizó acudiendo a la historia clínica.
Las variables categóricas se describen mediante frecuencia absoluta y frecuencia relativa en porcentaje. Las variables cuantitativas se describen mediante media y desviación estándar.
Se comparó la distribución de las variables cualitativas en los diferentes grupos mediante la prueba de χ2, colapsando categorías si los efectivos calculados eran inferiores a 5, o mediante prueba de Fischer, si ello era necesario.
Se comparó la distribución de las variables cuantitativas en los diferentes grupos mediante prueba de t de Student o ANOVA si el número de grupos era superior a dos.
En todos los casos se estableció el nivel de significación en α = 0,05. Los análisis estadísticos se realizaron mediante el paquete estadístico STATA versión 8, en entorno Windows XP.
RESULTADOS
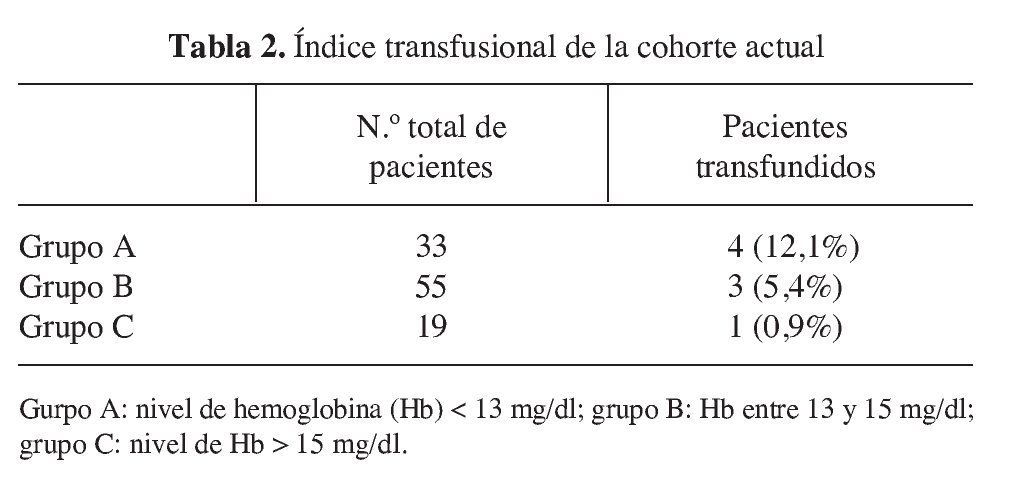
Índice transfusional
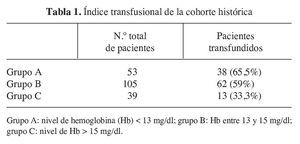
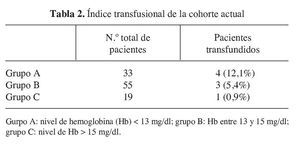
El resultado obtenido una vez analizados los datos de las dos cohortes ha sido el de lograr disminuir el índice transfusional. En la cohorte histórica se situaba en un 57,3% (113 pacientes) y en la cohorte actual ha pasado a ser de un 7,5% (8 pacientes). Esta diferencia es estadísticamente significativa (χ2 = 34,4, df = 1, p < 0,05). Si lo analizamos en función de los niveles de Hb y por lo tanto de cada uno de los grupos establecidos, hemos observado las variaciones en el índice transfusional que aparecen en las tablas 1 y 2.
Sexo
Hemos encontrado un claro predominio de mujeres sobre hombres en ambas cohortes, salvo en ambos grupos C, en los que se invierte la relación mujer/hombre.
1) Cohorte histórica: 142 mujeres/55 hombres (72,1/27,9%).
2) Cohorte actual: 76 mujeres/31 hombres (71,1/28,9%).
No hay diferencia estadísticamente significativa en la distribución por sexos en ambas cohortes.
Edad
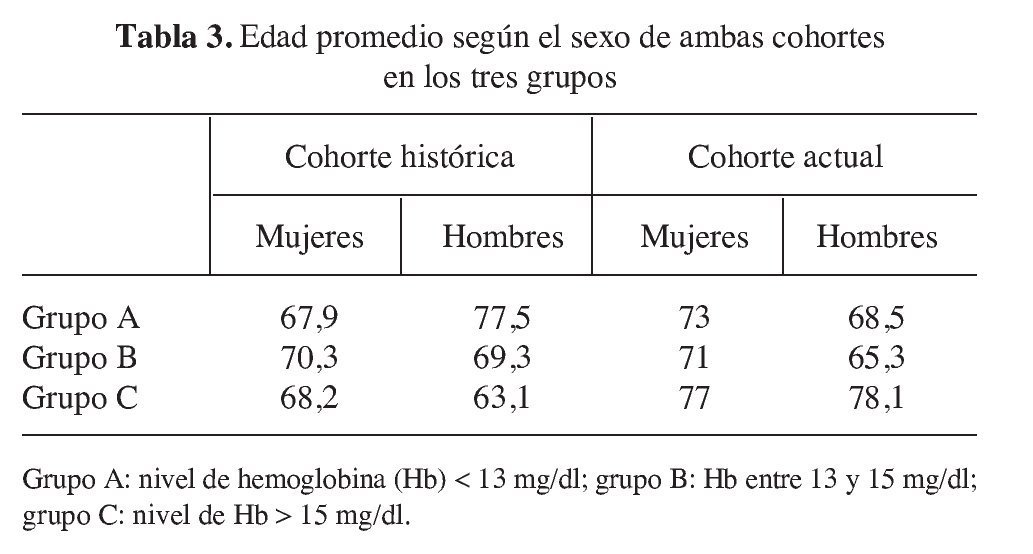
En este estudio no se han incluido pacientes mayores de 80 años (suponían el 9,3% de la cohorte histórica). Lo que hemos observado es que en un intervalo de dos años, la edad de los pacientes ha aumentado en 5,1 años para las mujeres y en 3,2 para los hombres. Sin embargo, nos encontramos que la diferencia no es estadísticamente significativa. El promedio de edad en ambas cohortes fue:
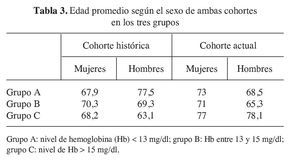
1) Cohorte histórica: mujeres 67,9 años, con un rango entre 40 y 79. Hombres 65,3 años, con un rango entre 49 y 79 (tabla 3).
2) Cohorte actual: mujeres 73 años, con un rango entre 50 y 79. Hombres 68,5 años, con un rango entre 58 y 79.
Evaluación de la ASA
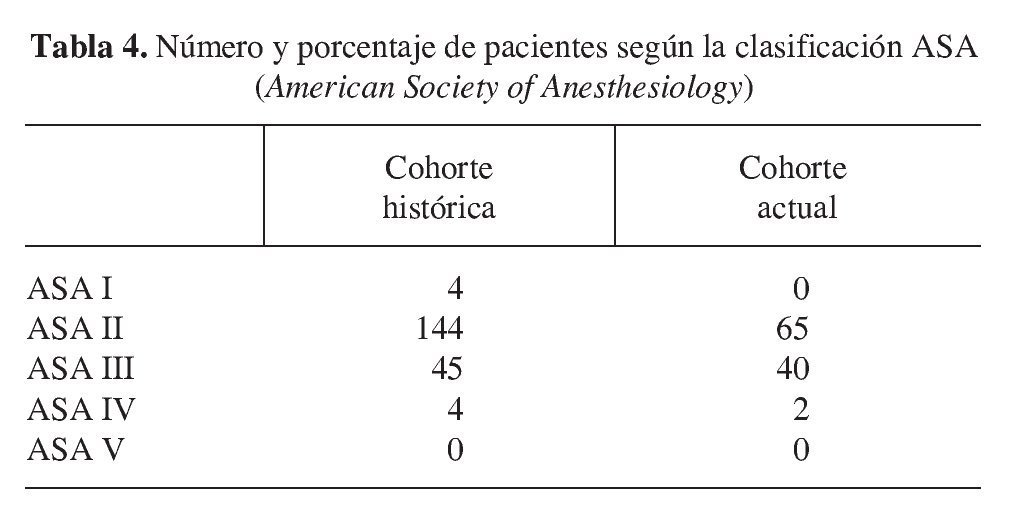
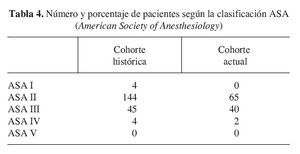
La valoración del estado de salud del paciente desde un punto de vista anestésico se realizó según la ASA y podemos observar que en ambas cohortes la mayoría de los pacientes está en el nivel ASA II y III; como ya vimos en las patologías previas, los pacientes de la cohorte actual tienen un estado de salud más deteriorado (tabla 4).
Si realizamos una comparación de las dos cohortes y valoramos por un lado los pacientes ASA I y II, y por otro lado, los pacientes ASA III, IV y V nos encontraríamos con que el índice de gravedad de los enfermos es mayor en la cohorte actual, lo que supone una diferencia estadísticamente significativa (χ2 = 6,16, df = 1, p < 0,05).
ERITROPOYETINA
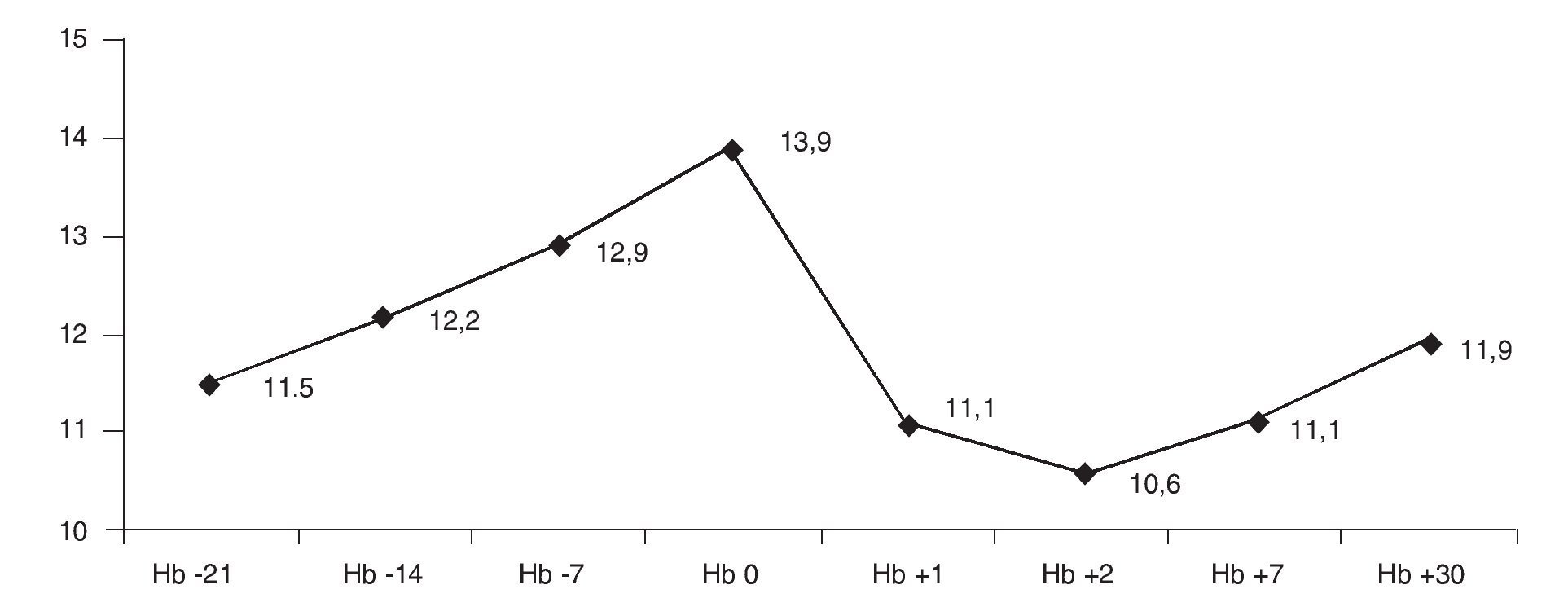
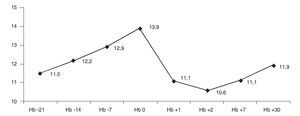
Los pacientes tratados con EPO son aquellos cuyo nivel de Hb preoperatoria es inferior a 13 g/dl, es decir, los pacientes encuadrados en los dos grupos A. El tratamiento con EPO ha conseguido una mejoría notoria en el aumento de los niveles de Hb preoperatorios, situándolos en un promedio de 2,3 g/dl por encima del nivel inicial. Una semana después de la intervención, el nivel promedio de Hb es 0,4 g/dl menor al que tenían los pacientes antes de la intervención. Al mes postcirugía el nivel de Hb se situó en un promedio de 0,3 g/dl por encima del nivel inicial (fig. 1).
Figura 1.Evolución del nivel de hemoglobina (Hb) con el tratamiento de eritropoyetina.
Autotransfusión-predonación
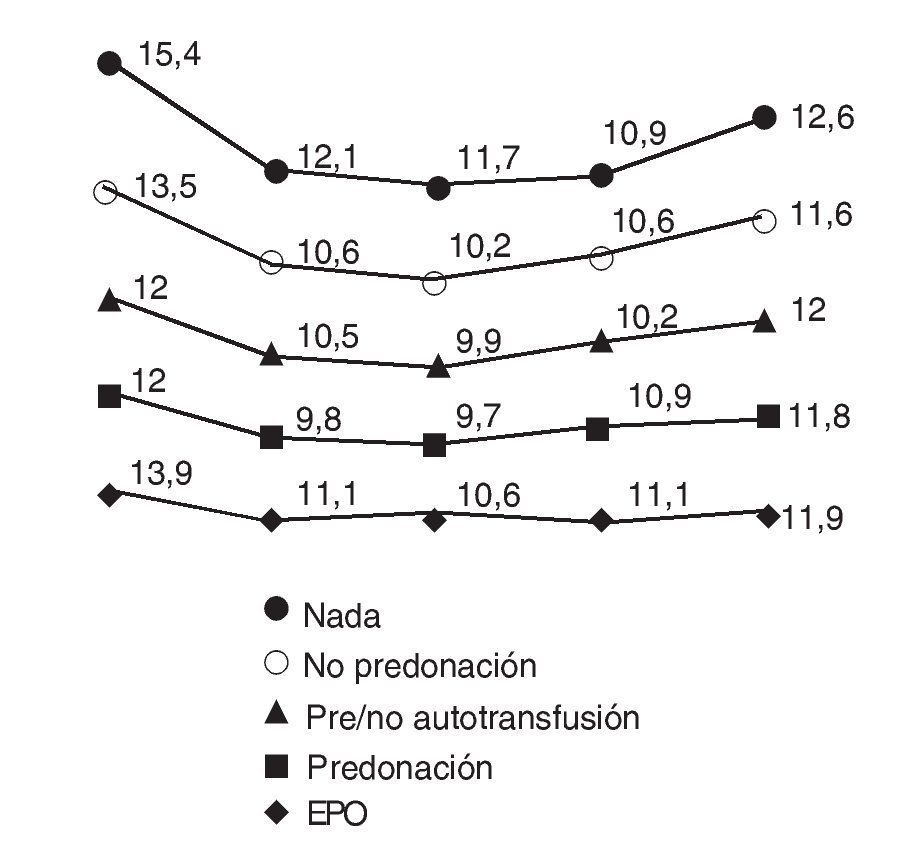
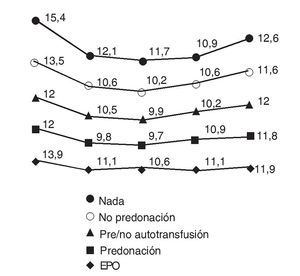
En este grupo están incluidos los pacientes con un nivel de Hb preoperatorio situado entre 13-15 g/dl. Por lo tanto, son los candidatos a entrar en un programa de autotransfusión y se encuadran en ambos grupos B. En la cohorte histó-rica, 3 pacientes entraron en un programa de predonación. En el grupo B actual, siguieron el protocolo de predonación 34 pacientes (61,8%) de los 55 que formaban el grupo. El promedio del nivel de Hb preoperatoria de los pacientes que siguieron el protocolo de predonación fue de 13,9 g/dl, con un rango entre 13 y 14,9 g/dl, y pasó a 12 g/dl el día de la cirugía, después de la extracción de las dos bolsas de sangre, con un rango entre 10,6 y 13,6 g/dl. De las 67 bolsas de sangre extraídas, sólo han sido utilizadas 45 (67,1%) y 22 se han desechado (32,9%) (fig. 2).
Figura 2.Evolución del nivel de hemoglobina (Hb) en cada uno de los grupos (A, B y C) y en los tres subgrupos del grupo B desde el día de la cirugía, los días 1, 2 y 7, y al mes poscirugía. EPO: eritropoyetina. Grupo A: nivel de Hb < 13 mg/dl; grupo B: Hb entre 13 y 15 mg/dl; grupo C: nivel de Hb > 15 mg/dl.
Redon recuperador
1) Cohorte histórica: se utilizó en 79 pacientes (40,1%) y no se utilizó en 118 (59,9%); precisaron transfusión alógena 13 de ellos (24,5%).
2) Cohorte actual: se ha utilizado en 100 de los 107 pacientes (93,5%).
El valor promedio de recuperación de sangre de los drenajes colocados fue de 608 cc, con un rango entre 150 y 1.575 cc.
Si valoramos por grupos la cantidad de sangre recuperada observamos que: grupo A: 714 cc, grupo B: 589 cc y grupo C: 687 cc (promedio: 663 cc).
Si comparamos las dos cohortes, vemos que el porcentaje de utilización ha pasado de un 40,1% en la cohorte histórica a un 93,5% en la actual, lo que supone una diferencia estadísticamente significativa (χ2 = 84,3, df = 1, p < 0,05). El promedio de sangre recogida ha aumentado de 383 a 608 cc.
Umbral de transfusión
En la cohorte histórica, los 113 pacientes fueron transfundidos con sangre alógena y 8 pacientes de la cohorte actual han necesitado transfusión alógena.
Incidencias de la evolución clínica
En la cohorte histórica sólo se han podido recoger los datos de las infecciones protésicas, por lo que será el único dato que se va a comparar.
En cuanto a infecciones, en la cohorte histórica hubo tres pacientes (1,5%), y en la cohorte actual, un paciente (0,9%).
Una paciente padeció una trombosis venosa profunda en la pierna no operada. Pertenecía al grupo B y no fue transfundida con su sangre predonada.
Se han encontrado dos infecciones nosocomiales: una infección respiratoria en un paciente con antecedentes de cardiopatía e hipertensión arterial (HTA), que pertenecía al grupo C y no precisó transfusión, y una infección urinaria en un paciente con antecedentes de cardiopatía e HTA, que pertenecía al grupo B y al que no se le realizó la predonación por sus antecedentes y fue transfundido con dos unidades de sangre alógena.
Hierro oral
Ningún paciente en la cohorte histórica tenía protocolizada la ingesta de hierro. El hierro oral lo tomaron de forma preoperatoria los pacientes del grupo A que recibieron EPO (30 pacientes) y aquellos que realizaron la predonación en el grupo B (34 pacientes).
DISCUSIÓN
La probabilidad de incidencias relacionadas con la transfusión de una unidad de hematíes es de 1,71/1.000 y además puede haber incidentes de mayor gravedad, con una gran morbilidad para el paciente y que incluso pueden llevarle al fallecimiento (0,74% de todos los ingresos por reacción transfusional [IRT]).
La donación de sangre en nuestro país es totalmente altruista; no obstante, existe un coste relacionado con la transfusión sanguínea tal como demostraron en una revisión sistemática Amin et al13. Estos mismos investigadores realizaron un estudio posterior en Canadá sobre los costes generados en los años 2002-200314 y calcularon que el coste medio de una bolsa de sangre en ese país era de 264,81 $.
Durante la fase preoperatoria es donde en función de los niveles de Hb podremos actuar sobre ella para mejorarla. Para ello, hoy en día fundamentalmente disponemos de la EPO. Pero, además, también podemos empezar a usar técnicas de ahorro de sangre como la autotransfusión, bien en forma de predonación o mediante la hemodilución normovolémica aguda y la utilización de hierro endovenoso.
Las indicaciones de la EPO son para un nivel de Hb entre 10-13 g/dl, ya que es el grupo en el que la posibilidad de transfusión es mayor. Puede ser utilizada de forma única (cirugía primaria) o como coadyuvante en programas de autotransfusión15. Sin embargo, existe una serie de contraindicaciones: HTA no controlada, infarto agudo de miocardio reciente, angor inestable, enfermedades vasculares periféricas graves y accidente cerebrovascular reciente. Son asimismo inconvenientes: la necesidad de coordinación intrahospitalaria de los diferentes servicios implicados, monitorización de los niveles de Hb para no pasar de 15g/dl, fecha fija de la intervención y su elevado coste.
Cuando nos referimos a la autotransfusión, estamos hablando de tres técnicas diferentes:
1) Autotransfusión predonación.
2) Hemodilución normovolémica aguda.
3) Recuperador de sangre (intra o postoperatorio). De esta técnica se hablará más adelante, ya que aquí estamos hablando de la fase preoperatoria.
La primera referencia publicada en relación a esta técnica se debe a Milles et al, ya en el año 1962. La autotransfusión-predonación se podría considerar como el "patrón oro" dentro de las técnicas de ahorro de sangre, si bien para algunos presenta algunos inconvenientes: los pacientes se encuentran anemizados en el momento de la cirugía, un porcentaje elevado de las bolsas extraídas no se utiliza, aumenta el número de transfusiones, con los riesgos y gastos que conlleva16, presenta el mismo número de errores administrativos (confusión con la bolsa adecuada) que la transfusión alógena, su coste-efectividad es escaso en las cirugías primarias7 y supone un incremento de trabajo organizativo e incomodidad para el paciente.
Sin embargo, existen argumentos en su favor: la transfusión alógena disminuye significativamente17,18, la infección postoperatoria es menor que con la transfusión alógena, ahorra "la sangre que otros no pueden darse a sí mismos", la anemización de los pacientes y la escasa utilización de las bolsas predonadas se debe a un incorrecto cálculo de las necesidades del paciente17,18, disminuye el riesgo de fenómenos tromboembólicos en la cirugía protésica de rodilla y cadera19. Lo que es indudable es que en nuestro país la predonación se encuentra en un nivel de utilización muy bajo en relación con el número total de donaciones20.
La cirugía mayor produce una respuesta inflamatoria sistémica, cuyos mediadores humorales (factor de necrosis tumoral [TNF], interleucina [IL]-1, interferón [INF]) inhiben la eritropoyesis mediante la supresión del crecimiento de la colonia eritroide y, por lo tanto, inhibiendo indirectamente la producción de EPO endógena. Estas citoquinas, además, inducirían un déficit funcional de hierro, aunque los depósitos de hierro se encuentren en situación de norma-lidad21. Actualmente, y para poder actuar sobre esa respuesta inflamatoria sistémica, disponemos del hierro sacarosa. No obstante, su uso en nuestro país fue aprobado en el año 2002 y la bibliografía publicada en nuestra especialidad es escasa y se relaciona fundamentalmente con el manejo de la anemia en las fracturas de cadera22.
En la fase quirúrgica hemos de intentar disminuir las pérdidas sanguíneas y procurar que la hemostasia sea lo más adecuada posible. En caso de cirugía de cadera y columna, los recuperadores de sangre intraoperatorios tienen una gran utilidad, no así en la cirugía de rodilla. Para mejorar la hemostasia podemos utilizar agentes hemostáticos sistémicos, utilizar sellantes de fibrina, utilizar una técnica quirúrgica adecuada y evitar la hipotermia en el paciente quirúrgico.
Actualmente, y en concreto en la cirugía de prótesis de rodilla y cadera, se han comenzado a emplear técnicas MIS, que, entre otros beneficios teóricos, tendrían el de una menor pérdida hemática23. Por el momento esto no se ha podido demostrar en las prótesis totales de rodilla, ya que el sangrado es similar, en parte debido a que la movilización pasiva comienza a las 6 horas postoperatorias y esto contribuye a que el sangrado sea mayor24.
En la fase postoperatoria solamente disponemos de dos opciones: recuperador de sangre postoperatorio y utilizar un umbral de transfusión adecuado. El primero de ellos tiene muchos detractores ya que no hay evidencia científica que justifique la utilización de un drenaje de Redon postoperatorio25 y se confirmó más tarde, también, en un metaanálisis realizado en Inglaterra por Parker et al en 200426. Las necesidades transfusionales son mayores si se usan redones postoperatorios. La sangre que se transfunde no es de buena calidad. Pero también tiene muchos defensores que justifican su uso ya que el Redon recuperador de sangre disminuye la transfusión alógena. En un metaanálisis realizado por la ISPOT (International Study of perioperative transfusion) en 1999 se observó que el Redon recuperador disminuye el riesgo relativo de transfusión alógena en un 39%. Posterior-mente, en 2004, la librería Cochrane27 concluyó también que usando recuperador el riesgo relativo de transfusión alógena disminuye un 42%. Es un método de autotransfusión que no presenta los inconvenientes del predepósito. La calidad de la sangre recuperada es de absoluta garantía. Para que estas condiciones se den, es fundamental que se recupere la sangre de las 4 primeras horas y se transfunda antes de que se cumplan 6 horas9. Además, no es conveniente pasar más de 1.000 cc para evitar problemas de hipervolemia. Actualmente está demostrado que la sangre filtrada y no lavada es de una seguridad equiparable a la lavada8,28.
Cuando se utiliza el término "umbral de transfusión", se está hablando de las circunstancias clínicas que rodean a un paciente en el momento de decidir si se tiene o no que transfundir sangre. Hoy en día, el nivel aislado de Hb solo no es suficiente para decidir una transfusión sanguínea. Por lo tanto, es imprescindible valorar otros parámetros clínicos. Adams y Lundy en el año 1942 recomendaron la regla 10/30 como valores aconsejables para realizar una transfusión sanguínea y de esta manera evitar posibles riesgos en los pacientes. Esta regla se mantuvo casi de manera uniforme hasta finales de los años ochenta. Sin embargo, con la aparición del VIH y su transmisión entre otros medios por la transfusión sanguínea, su idoneidad comenzó a ser cues-tionada. En el año 1988, en Estados Unidos se realizó una conferencia de consenso y se recomendó que la transfusión se realizara con unos niveles de Hb entre 7 y 10 g/dl29.
En un estudio prospectivo y aleatorizado realizado en Canadá por Herbert et al se vio que en los pacientes de Unidad de Cuidados Intensivos menores de 55 años y con un APACHE (Acute Physiology and Chronic Health Evaluation) < 20, que mantenían una Hb entre 7-9 g/dl, los resultados obtenidos sin transfundir eran iguales o incluso mejores que en un grupo similar, cuyos niveles de Hb eran mayores de 10 g/dl, siempre que los pacientes estuvieran en situación de normovolemia. Sin embargo, en pacientes con un síndrome coronario isquémico activo, si no se mantenían niveles de Hb superiores a 10 g/dl, la morbimortalidad aumentaba. En otro estudio, Bak et al realizaron una hemodilución normovolémica aguda preoperatoria en 8 pacientes sanos (entre 13 y 61 años). Posteriormente, se les realizó cirugía de escoliosis y durante todo el proceso estuvieron monitorizados mediante ecocardiografía transesofágica y se comprobó que un nivel de Hb de 8 g/dl era tolerado sin ningún problema por dichos pacientes.
Donde mejor se ha podido estudiar el efecto de la anemia aguda postquirúrgica es en los pacientes Testigos de Jehová. En un estudio retrospectivo de cohortes sobre 2.083 pacientes, Carson et al observaron en 300 de ellos, en los que su nivel de Hb estaba entre 7-8 g/dl, que su mortalidad fue del 0% y su morbilidad del 9,5%. Sin embargo, si los niveles bajaban a 5 g/dl, la mortalidad a los 30 días era del 34%.
No obstante, actualmente no hay ningún estudio que pueda definir cuál es el nivel de Hb a partir del que hay que transfundir. Como ya se ha comentado al principio de este apartado, la decisión de transfundir se debe tomar en función de la situación clínica general del paciente11,29.
En realidad, cuando hablamos de sustitutos de la sangre estamos hablando de sustituir los hematíes, ya que son los que suministran el O2 al organismo, mientras que la volemia, como ya se ha comentado anteriormente, se puede reemplazar con los cristaloides y/o los coloides. Los sustitutos de hematíes de que disponemos hoy en día son las soluciones de Hb y los perfluorocarbonados.
De los dos tipos de sustancias, de momento hay pocos estudios y con pocos pacientes, y no parece que hoy en día sea generalizable su utilización, salvo en usos militares o en catástrofes civiles, como resucitadores hasta llegar al hospital más cercano.
Teniendo en cuenta nuestros resultados, podemos extraer las siguientes conclusiones:
1) El valor predictivo más importante para la posible necesidad de transfusión alógena es el nivel de Hb preoperatoria. Según los resultados obtenidos, parece razonable utilizar el nuevo protocolo de ahorro de sangre propuesto por nosotros.
2) La EPO ha resultado ser un medicamento muy eficaz y muy seguro. Se utiliza en los pacientes con mayor probabilidad de recibir una transfusión alógena y, aunque su coste sea elevado, es la única técnica de que disponemos actual-mente para ese grupo de pacientes. Por otra parte, no en todos los casos es necesario usar 4 dosis para evitar la transfusión alógena.
3) La autotransfusión-predonación es muy eficaz. En esta serie ningún paciente transfundido con su sangre predonada ha precisado transfusión alógena. Sin embargo, su eficiencia ha sido baja ya que no hemos utilizado un 32,9% de las bolsas predonadas.
4) El Redon recuperador usado en este estudio, Consta VacTM CBC II Stryker®, ha demostrado ser muy seguro. Ello confirma que no es necesario en este tipo de cirugía lavar la sangre filtrada con este sistema. Su eficacia es alta, ya que hemos visto que el promedio de sangre recuperada es equivalente al menos a una bolsa de concentrado de hematíes y, según hemos visto, su coste es similar al de dicha bolsa.
5) Es importante tener en cuenta que la organización de un sistema de ahorro de sangre supone un gran esfuerzo organizativo, que necesariamente tiene que implicar a los servicios de Hematología, Anestesia y al de Cirugía correspondiente.
6) Todo esto no nos debe hacer olvidar que la transfusión de sangre alógena sigue siendo un procedimiento terapéutico esencial en nuestra práctica médica cotidiana.
Declaración de conflicto de intereses
Los autores han declarado no tener ningún conflicto de intereses.
Correspondencia:
M. Echenique Elizondo.
Universidad del País Vasco.
Paseo Dr. Begiristain, 105.
20014 San Sebastián. España.
Correo electrónico: gepecelm@sc.ehu.es
Recibido: febrero de 2007.
Aceptado: septiembre de 2007.