Las nuevas técnicas de fijación ósea y los avances en el conocimiento de la biología de la cicatrización ósea permiten conseguir resultados satisfactorios en el tratamiento de las fracturas de los huesos largos. Ocasionalmente, un pequeño porcentaje evoluciona de un modo desfavorable hacia la pseudoartrosis1,2. De éstas, la mayoría se consolidan aplicando métodos convencionales (injerto y síntesis rígida)1,3-7 pero existe un grupo de pseudoartrosis que por distintas causas no curan a pesar de este tipo de tratamiento. Se define como pseudoartrosis recalcitrante, aquélla que no se consolida tras tres o más intervenciones, si bien no existe un consenso sobre el número exacto de intentos quirúrgicos necesarios para ser considerada como tal8. Así mismo, se han definido una serie de factores de mal pronóstico (infección, traumatismo de alta energía, fractura abierta y pérdi-da de cobertura) cuya coexistencia aumenta las posibilidades de que la fractura no cure8.
Cuando se interviene una pseudoartrosis recalcitrante, el cirujano debe enfrentarse a la necesidad de cambiar el material de osteosíntesis y, posiblemente, corregir una deformidad, lo que deteriorará aún más la vascularización local ya dañada previamente. Ante esta situación, el tratamiento debería ir acompañado de un gesto adicional, distinto a los practicados con anterioridad, fundamentalmente encaminado a mejorar las condiciones vasculares locales. Los colgajos libres permiten traer tejido sano a un área desvascularizada.
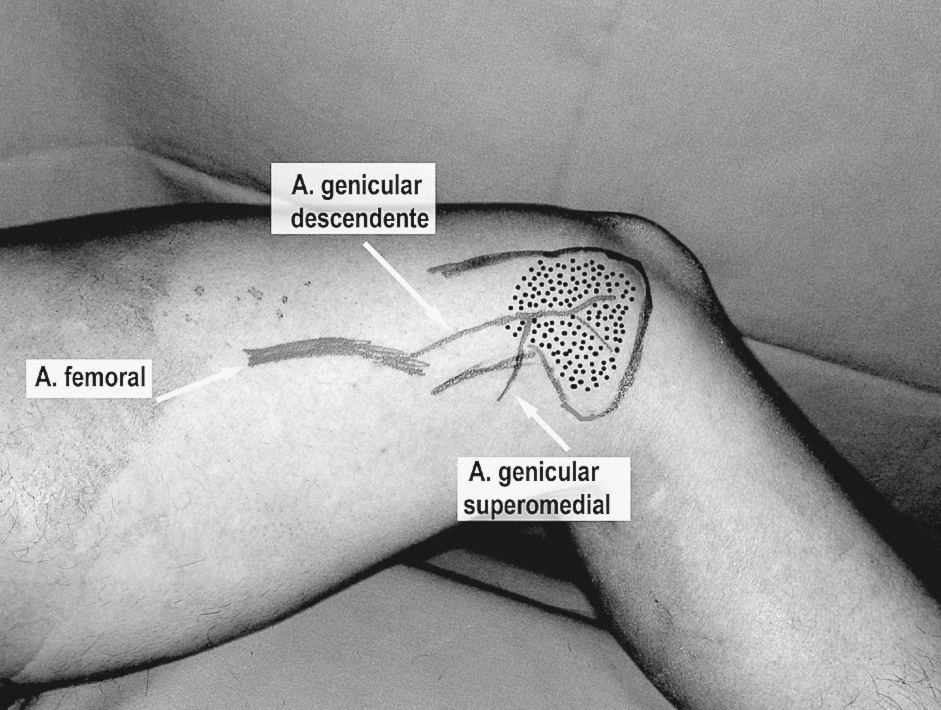
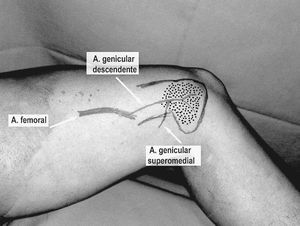
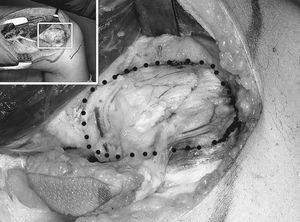
En el tratamiento de la pseudoartrosis con grandes defectos óseos el empleo de injertos óseos vascularizados está ampliamente aceptado8. Sin embargo, ante defectos de menor tamaño es habitual el uso de técnicas clásicas (desbridamientos seriados, estabilización interna e injerto óseo no vascularizado). Basándonos en el concepto anteriormente expuesto (necesidad de tejido vascularizado), consideramos que en las pseudoartrosis recalcitrantes con defectos menores la combinación de periostio vascularizado y la fina cortical del cóndilo del fémur con su propio aporte vascular es la solución biológicamente ideal. El colgajo corticoperióstico (CP) del cóndilo femoral9 reúne estas características (fig. 1).
Figura 1. Diseño del colgajo corticoperióstico del cóndilo femoral medial. En puntos se ha marcado el área donante de hueso y periostio.
En este trabajo, presentamos nuestra experiencia en el tratamiento de pseudoartrosis recalcitrantes de huesos largos de la extremidad superior con defectos óseos menores de 3 cm mediante colgajos CP del cóndilo medial del fémur.
MATERIAL Y MÉTODO
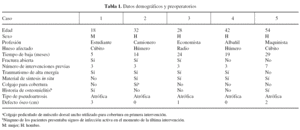
Se presentan cinco pacientes con pseudoartrosis recalcitrantes de los huesos largos de la extremidad superior tratados entre 2003 y 2004: 2 húmeros, 2 cúbitos y 1 radio (tabla 1). La serie consta de 4 varones y 1 mujer con edades comprendidas entre los 18 y 54 años.
El traumatismo inicial había sido una fractura abierta en 3 casos, una fractura conminuta de húmero y una fractura cerrada posteriormente infectada. En 2 pacientes había historia previa de osteomielitis, pero no había signos de infección activa cuando se presentaron para tratamiento en nuestra unidad. Una de las fracturas abiertas fue tratada con una plastia local en otro centro para su cobertura. Todos fueron intervenidos en tres o más ocasiones (rango 3-7). En nuestra primera valoración, en 4 casos persistía el material de osteosíntesis in situ; el quinto paciente llevaba un fijador externo tras la retirada del material como intento de controlar la infección. Los pacientes presentaban dolor, impotencia funcional, inflamación y sensación de inestabilidad. Los factores desfavorables asociados están reflejados en la tabla 1.
En todos los pacientes se abordó el foco a través de la incisión previa. Se retiró el material de osteosíntesis y se desbridó el tejido fibroso y desvitalizado. Tras la realineación del hueso, se calculó el defecto óseo cuando existía. Mientras se procedía a la síntesis rígida con placas LCP (locking compression plate) (cuatro casos) y una placa DCP (dynamic compression plate) para un cúbito, de 3,5 mm para el antebrazo y 4,5 mm para el húmero, otro equipo elevaba el colgajo.
Anatomía quirúrgica
El periostio y la cortical del cóndilo medial femoral están irrigados a través de vasos muy finos que proceden de una arcada que se forma en su superficie (fig. 1). A esta arcada llegan entre otras la rama articular de la arteria genicular descendente y la arteria geniculada superomedial. Estas dos arterias vascularizan esta región de forma competitiva, de tal forma que cuando una está desarrollada la otra es hipoplásica y viceversa. La arteria genicular descendente proporciona un pedículo de 8-10 cm y un vaso de una calibre de 1,5-2 mm. Es el pedículo ideal y es dominante en el 80% de los casos9. La geniculada superomedial cuando es dominante tiene un calibre similar, pero el pedículo que se consigue es mucho menor 3-4 cm, y su disección más difícil.
Técnica quirúrgica
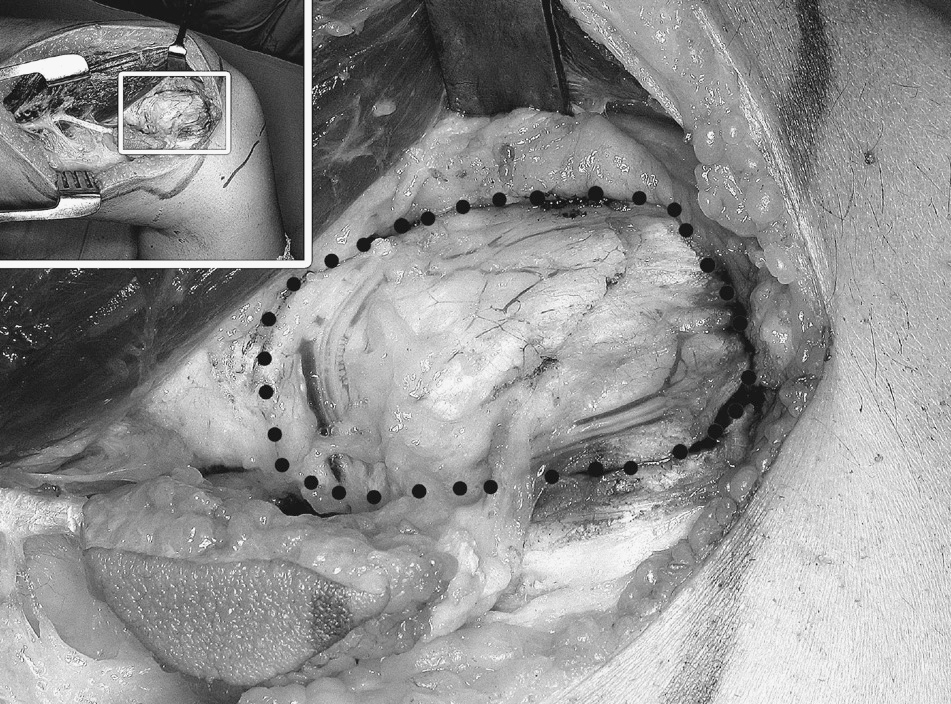
La técnica de disección empleada es la descrita por Sakai-Doi, et al9. Mediante una incisión en la cara medial del muslo, se aborda el fémur a través del hiato fascial entre el vasto medial y el sartorio. Anterior al tabique intermuscular interno, posterior al vasto medial, se encuentra el hiato con la rama articular de la arteria genicular descendente. En este hiato se encuentran las perforantes que hay que disecar si se desea incluir una isla cutánea (dos de los cinco casos). Tras este paso debe quedar expuesta toda la anatomía vascular del colgajo y el cóndilo femoral donante (fig. 2). A continuación se aísla el pedículo de la arteria genicular descendente. En caso de que ésta sea hipoplásica, se prosigue la disección hacia posterior hasta el origen de la arteria genicular supero-medial en la poplítea. Se puede incluir un pequeño colgajo de piel, basado en perforantes de los vasos geniculares descendentes, para la monitorización postoperatoria.
Figura 2. Detalle durante la elevación del colgajo, en el que se puede apreciar la gran riqueza de vasos periósticos sobre el cóndilo femoral medial. Los límites del colgajo están premarcados con un osteotomo (puntos). En el recuadro arriba a la izquierda: vista panorámica.
Se delimita mediante un osteotomo fino el área de colgajo que se quiere incluir (preservando la arcada vascular), y a continuación mediante un osteotomo fino de hoja ancha se eleva el colgajo que incluye el periostio, la cortical y una fina lámina de esponjosa. Esta maniobra se hace casi a mano, progresando poco a poco desde todos los lados y sin apalancar para no romper el colgajo.
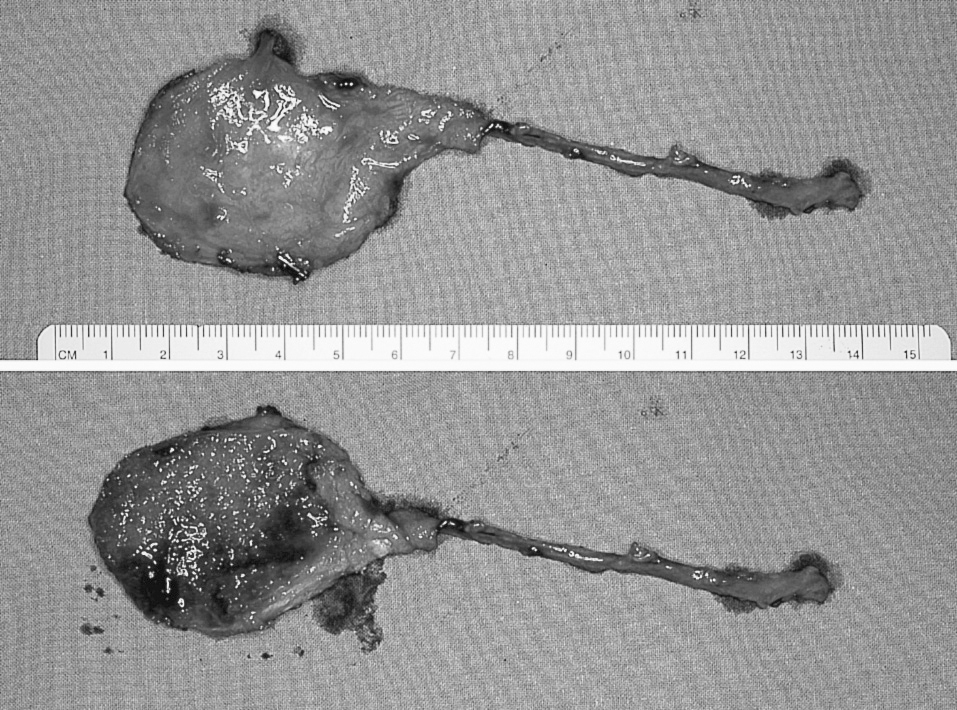
Tras retirar la isquemia se comprueba el sangrado del periostio y de la superficie de la esponjosa. El colgajo es transferido tras la osteosíntesis (fig. 3). La pastilla CP se moldea para abrazar el defecto óseo. Doi aconseja simplemente doblarla, pero en nuestra experiencia hemos encontrado esta maniobra arriesgada para los finos vasos periósticos. Por este motivo hacemos una serie de muescas a modo de línea discontinua con una sierra oscilante en la cara profunda del colgajo (esponjosa) sin llegar al periostio, con lo que se debilita la cortical y se dobla sin dificultad (fig. 4). El colgajo se sutura al lecho donante en el lado contrario a la placa y se rellena el espacio entre la placa y el colgajo con injerto de esponjosa tomado del mismo cóndilo femoral. Las anastomosis arteriales se realizaron término-laterales a la arteria local dominante (braquial, radial o cubital) y las venosas término-terminales a venas subcutáneas o concomitantes.
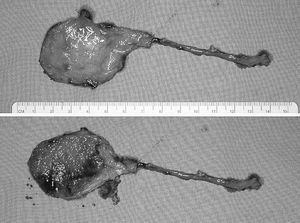
Figura 3. Colgajo corticoperióstico elevado con el pedículo largo (dependiente de la arteria y venas geniculadas descendentes). Arriba: cara perióstica. Abajo: cara profunda, donde se puede apreciar la esponjosa expuesta. El colgajo consta de periostio, cortical medial y 2-3 mm de esponjosa del cóndilo femoral.
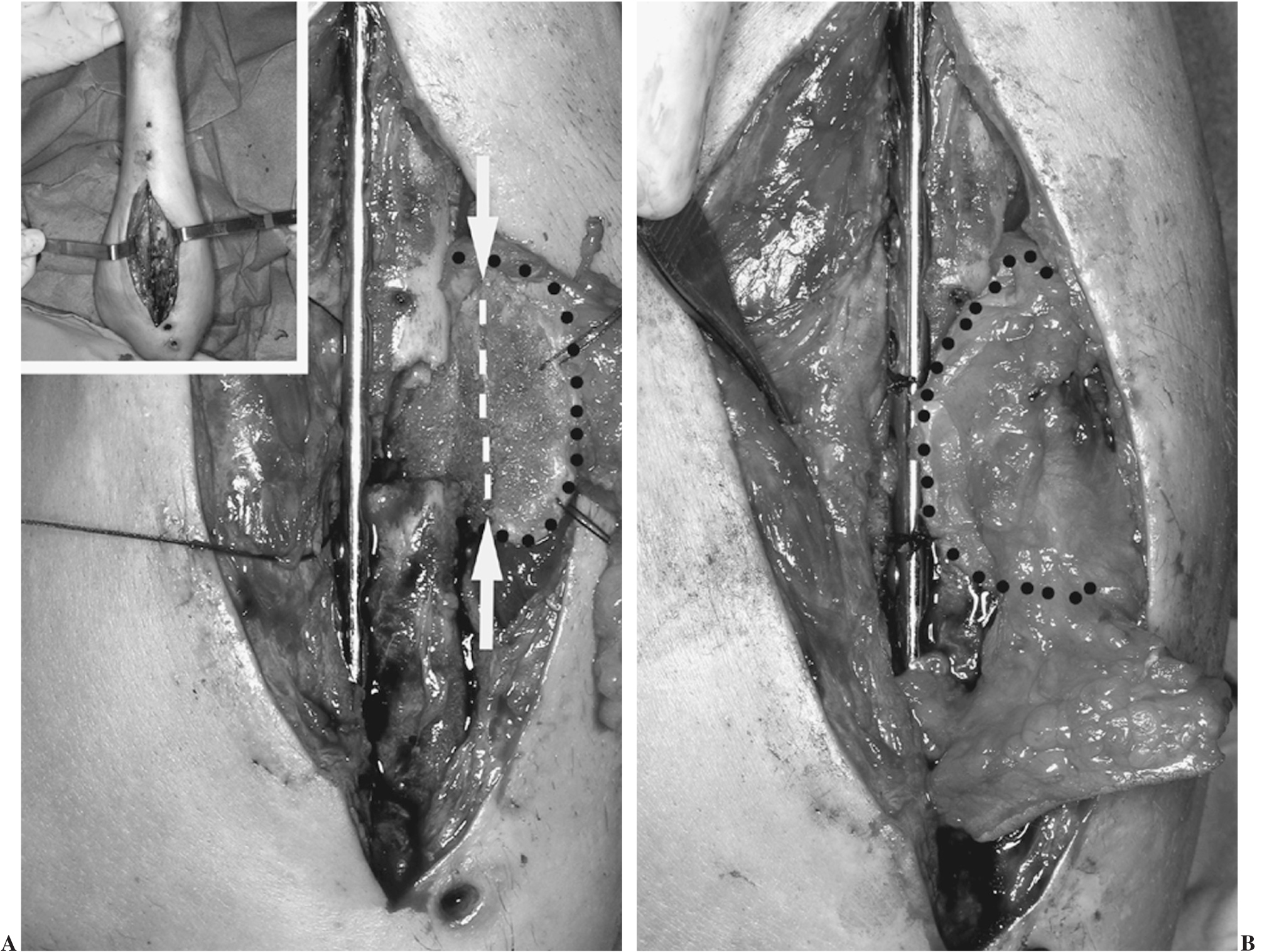
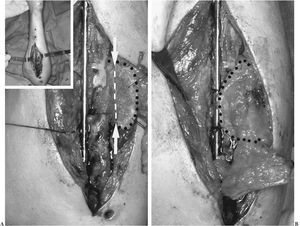
Figura 4. Técnica de adaptación del colgajo corticoperióstico en un cúbito (caso 1). Izquierda (A): el colgajo (marcado con puntos) está ya fijado y adaptado a las caras anterior y medial de cúbito y levantado por hilos antes de aplicarlo sobre la cara posterior del cúbito. Las flechas blancas y la línea de puntos marcan la osteotomía en la porción corticoesponjosa del colgajo por donde se pliega 90° para cubrir la cara posterior del cúbito (derecha). Derecha (B): el colgajo cubriendo el defecto en el cúbito y suturado a la placa (debajo del colgajo se rellena de injerto esponjoso). En el recuadro (arriba a la izquierda): vista panorámica.
Una vez realizado el cierre de la herida por planos, se coloca un vendaje blando con una ventana en el mismo para controlar la perfusión de la isla cutánea y/o para el control del colgajo con una sonda doppler. En la zona donante se dejó un drenaje aspirativo y se aplicó un vendaje blando permitiendo la carga a las 24 horas sin restricciones. Se empleó medicación hemorreológica intravenosa hasta el alta hospitalaria al quinto día y profilaxis antitrombótica hasta la deambulación sin restricciones (2-3 semanas).
En el postoperatorio inmediato se comenzó la movilización sin férula de la extremidad. Se realizaron controles con radiología simple cada mes. El tiempo de seguimiento varió entre 8 y 24 meses (promedio de 14 meses).
RESULTADOS
El tiempo de disección del colgajo varió (45-90 minutos) en función de las variaciones anatómicas y de la inclusión de la isla cutánea, realizándose simultáneamente la síntesis por otro equipo de cirujanos. En 3 casos de esta serie el pedículo era corto. En 2, con un pedículo de 3 cm, la arteria dominante era la geniculada súpero-medial, fue necesario recurrir a un injerto venoso en un caso y a cambiar el área receptora de anastomosis en el otro. En otro caso, aunque había arteria genicular descendente, existía una variación anatómica de la arteria femoral en el hiato de los aductores, que se tradujo en un pedículo anormalmente corto de la arteria genicular descendente (aproximadamente 4 cm de arteria). El calibre de las arterias fue de aproximadamente de 1-1,5 mm para los casos de pedículo corto y de 1,5-2,5 mm cuando se empleó la variante larga con la arteria genicular descendente.
Todos los colgajos sobrevivieron y en todos los casos se consiguió la consolidación radiológica entre el segundo y tercer mes postoperatorio, observándose un puente óseo yuxtacortical (figs. 5 y 6).
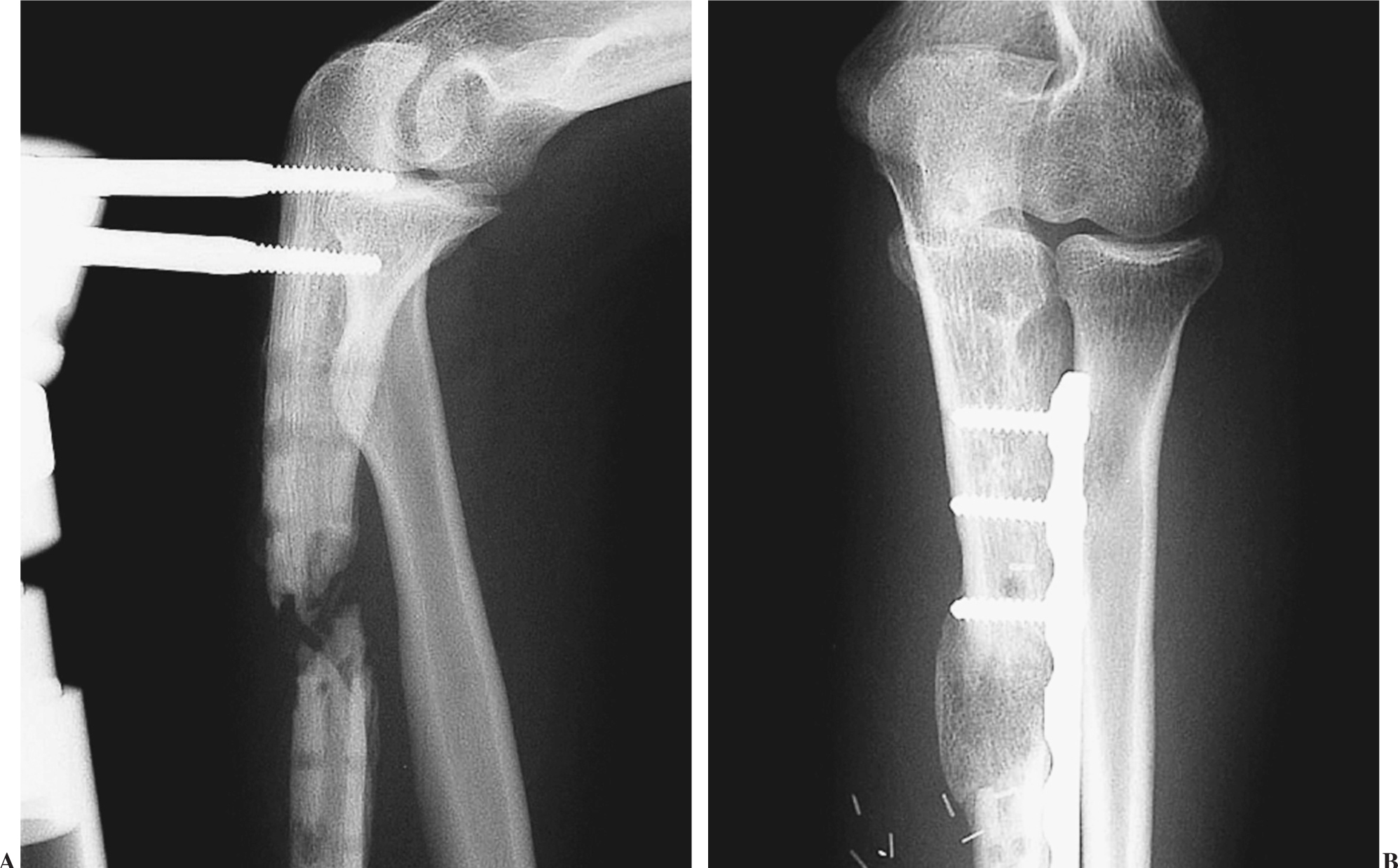
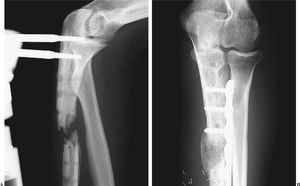
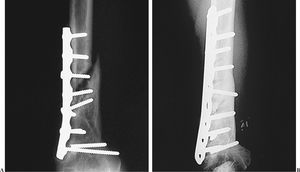
Figura 5. Caso 1. Pseudoartrois recalcitrante de cúbito. Radiografía preoperatoria (A) y postoperatoria (B) a los 2 meses. El resultado fue satisfactorio tras realizar el colgajo microvascular.
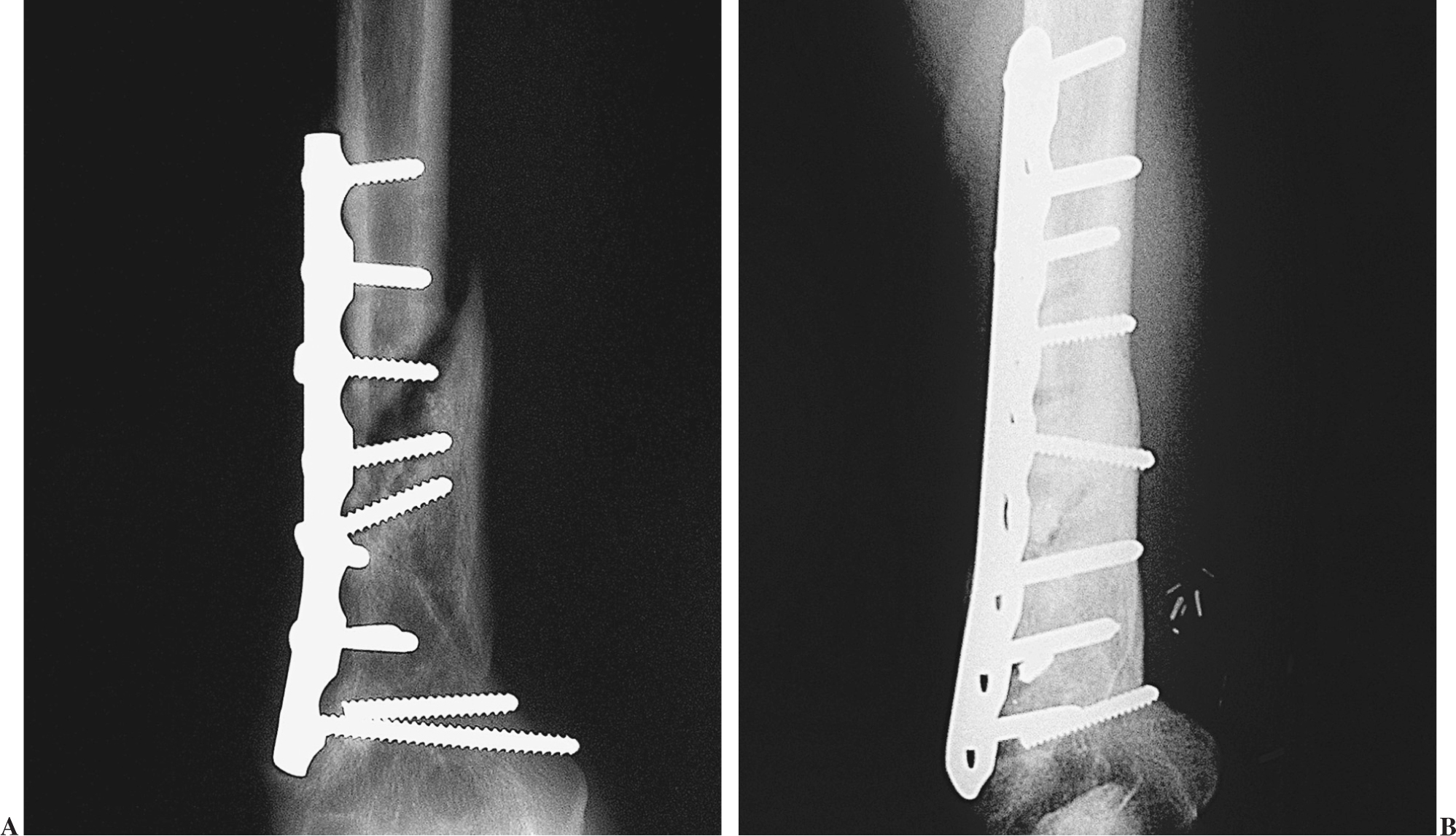
Figura 6. Caso 4. Radiografía preoperatoria (A) de una pseudoartrosis recalcitrante de húmero distal. Se puede apreciar un fragmento en mariposa que ha consolidado en su porción distal, pero que en la proximal no ha consolidado tras dos intentos con cambio de osteosíntesis y aporte de injerto óseo. Radiografía a los 3 meses del colgajo microvascular (B). El resultado fue satisfactorio.
Todos refirieron la mejoría de la sintomatología clínica preoperatoria, con desaparición de las molestias. No hubo casos de recidiva de infección ósea. El rango de movilidad de las articulaciones vecinas fue del 100% en tres casos. Una paciente (caso 1) quedó con una limitación de la supinación que mejoró tras la extracción del material al año. En la última revisión la pronación y la flexo-extensión del codo eran completas, persistiendo una limitación de la supinación a 60° (activa).
Al caso 4, que había sufrido una pérdida de 12 cm del nervio radial, se le realizó una transferencia tendinosa paliativa a los seis meses de la reconstrucción ósea. Al paciente 2, un economista con alta demanda deportiva, le hemos aconsejado la extracción del material de osteosíntesis, que por ahora él prefiere diferir. No es previsible cirugía adicional en ningún otro paciente.
En la zona donante, fueron frecuentes las molestias locales en la rodilla con la deambulación en etapas iniciales. En todos los casos cedieron espontáneamente en un plazo inferior a los dos meses. En la última revisión los pacientes no refirieron ningún problema con la zona donante.
DISCUSIÓN
La actitud terapéutica habitual ante una pseudoartrosis es la de intentar una osteosíntesis estable con aporte de injerto óseo autólogo, consiguiéndose con este método unas tasas de consolidación altas3,4,7. Sin embargo, el problema es muy distinto en los casos de pseudoartrosis recalcitrantes (o potencialmente recalcitrantes). González del Pino et al8 definen como recalcitrante a aquéllas intervenidas al menos en tres ocasiones y define una serie de factores de mal pronóstico que van a condicionar una alta tasa de no unión: infección previa, fractura abierta, mecanismo lesional de alta energía, material de osteosíntesis in situ y pérdida de sustancia con necesidad de cobertura. Ante una pseudoartrosis intervenida previamente, en la que coincidan estos factores de mal pronóstico y sospechando la elevada posibilidad de tener problemas de consolidación, el cirujano debería añadir algún procedimiento adicional a los realizados por cirujanos previos (osteosíntesis más injerto óseo).
Es bien conocido que cualquier parte del cuerpo puede aislarse en un pedículo dado (arteria y vena) y ser trasplantado de una parte a otra del cuerpo, sin perder sus propiedades biológicas, si se restablece su nutrición mediante anastomosis vasculares. Taylor et al10,11 demostraron que tanto el peroné como la cresta ilíaca podían ser trasplantados manteniendo el hueso sus propiedades biológicas y mecánicas. Este hueso trasplantado llega incluso a hipertrofiarse, adaptándose a las necesidades funcionales del lecho receptor10. El trasplante de hueso vascularizado es un procedimiento ampliamente aceptado para la reconstrucción de grandes defectos óseos. Cuando los defectos son muy pequeños o irregulares los colgajos óseos clásicos no están indicados porque es muy complicado aislar las arterias que vascularizan el segmento dado y hay riesgo de que el fragmento trasplantado quede avascular. Además, abultan demasiado en áreas con pocas partes blandas. En el miembro superior, las pseudoartrosis con frecuencia poseen estas características: defectos pequeños en zonas que aceptan mal grandes incrementos de volumen12. En estas situaciones es donde el colgajo CP tiene su indicación principal9,12-18.
El colgajo CP se ha utilizado para necrosis avascular del astrágalo12, pero su mejor indicación es la de la pseudoatrosis recalcitrante de los huesos largos de la extremidad superior con pequeños defectos óseos9,12. Las ventajas del colgajo vienen dadas por su forma ligeramente cóncava del córtex medial del cóndilo femoral, la ausencia de cobertura muscular, que reduce el peligro de dañar a los vasos periósticos y la posibilidad de incluir una isla cutánea.
Independiente de la duración de la pseudoartrosis, su curación puede ser proporcionada utilizando los métodos clásicos: osteosíntesis estable en la presencia de ambiente bien vascularizado y adición de injerto de hueso autólogo1,5,7. Aunque en nuestra opinión todos los casos eran pseudoartrosis complejas que requerían gestos «excepcionales», hemos de reconocer que este trabajo podrá ser criticado, porque «se podía haber solucionado con métodos convencionales». La respuesta lógicamente no puede ser categórica en ninguno de los sentidos, pero incluso los autores más optimistas desaconsejan métodos convencionales cuando el lecho donde se va a poner el injerto es inelástico-cicatrizado y/o con pérdida de la envoltura muscular4. Nosotros nos hemos decantado por el uso de colgajos CP en este grupo de pacientes, dado que las alternativas tradicionales ya habían sido realizadas anteriormente, y consideramos que era importante no volver a repetirlas sin modificar el ambiente biológico para la consolidación. Además, a la presencia de tres o más factores de mal pronóstico presentes en todos los casos, se añadía el factor socioeconómico (bajas prolongadas en pacientes en edad productiva), factores estos que nos inducían a poner todos los medios para favorecer la consolidación.
El colgajo CP se ha demostrado eficaz en los casos aquí presentados. Destaca la presencia de un notable puente óseo evidente en las radiografías tan sólo dos meses después del procedimiento (fig. 6). Esta hipertrofia del callo óseo puede ser explicada por la alta capacidad osteogénica, osteoinductiva y osteoblástica del colgajo19. Gracias a su elasticidad, permite cubrir con facilidad parte del foco de pseudoartrosis. Por otra parte, del mismo cóndilo femoral se puede obtener abundante injerto esponjoso sin añadir morbilidad.
En cuanto a las desventajas, cabe destacar el mayor tiempo quirúrgico frente a un injerto no vascularizado, la necesidad de técnicas de microcirugía y de un riguroso control postoperatorio. La elevación del colgajo dura entre 45 y 90 minutos, pero la cirugía añade poco más al procedimiento, por la posibilidad de hacer dos campos. El tiempo requerido para las anastomosis puede suponer entre 40 minutos y un máximo dos horas (en el caso del injerto de interposición). Lógicamente, cualquier colgajo microquirúrgico requiere un equipo de cirujanos entrenados y un buen control postoperatorio de enfermería. Los vasos que se manejan en el colgajo CP son bastante más pequeños que los de los colgajos libres «más utilizados» (radial, dorsal ancho y peroné). Además, hay que considerar la posibilidad de variaciones anatómicas20 que transforman una operación relativamente sencilla (cuando el pedículo depende de la genicular descendente) en una compleja (cuando la arteria es la genicular súpero-medial, o variaciones de la femoral, como en tres de nuestros casos), donde pueden ser necesarios injertos venosos o recurrir a recursos que desconoce el microcirujano ocasional. No obstante, creemos que este colgajo tiene un papel clave en las pseudoartrosis de los huesos largos de la extremidad superior, por su mínima morbilidad y su alta tasa de éxitos.
Finalmente, el procedimiento no supone un grave daño para el paciente, ni anula ninguna alternativa, ya que no es necesaria la resección amplia de hueso potencialmente sano para poder interponer el injerto vascularizado convencional (peroné o cresta ilíaca). Por el contrario, combina una intervención clásica (síntesis rígida más injerto autólogo de esponjosa), con una que sanea el lecho (por añadir tejido vascularizado) y que genera más hueso (el colgajo CP vascularizado). En caso de fracaso, todas las ventajas de la intervención clásica están presentes, y no se habrá creado un defecto para la interposición de un injerto óseo vascularizado convencional.
En conclusión, el colgajo CP vascularizado constituye una atractiva opción terapéutica para el tratamiento de las pseudoartrosis recalcitrantes con defectos óseos menores en la extremidad superior, incluso en casos con antecedentes de infección. Destaca la existencia de un evidente puente óseo en las radiografías 2 meses después del tratamiento.
Conflicto de intereses. Los autores no hemos recibido ayuda económica alguna para la realización de este trabajo. Tampoco hemos firmado ningún acuerdo por el que vayamos a recibir beneficios u honorarios por parte de alguna entidad comercial. Por otra parte, ninguna entidad comercial ha pagado ni pagará a fundaciones, instituciones educativas u otras organizaciones sin ánimo de lucro a las que estemos afiliados.
Correspondencia:
F. del Piñal.
C/ Calderón de la Barca 16-entlo.
39002 Santander.
Correo electrónico: drpinal@drpinal.com
Recibido: agosto de 2005.
Aceptado: marzo de 2006.