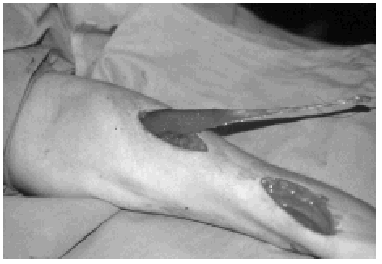
La compleja estructura del plexo braquial es muy vulnerable a las lesiones traumáticas tanto en el adulto como en el recién nacido, en este último después de accidentes obstétricos. Estas lesiones comprometen gravemente la función del miembro superior produciendo parálisis sensitiva, motora, vegetativa y se acompaña con frecuencia de un dolor intenso neuropático. La disfunción que origina en un paciente generalmente joven y los dolores de difícil tratamiento repercuten en la psicología del afectado, pudiendo producir además estados depresivos que precisen de apoyo psicoterápico.
En nuestro país, estas lesiones no son tan infrecuentes ya que el uso de la motocicleta está muy extendido. Según datos de la Dirección General de Tráfico (DGT) del año 2000, circulan 1.445.644 motocicletas y 408.159 ciclomotores. En un estudio sobre los accidentados de motocicleta que acudían a nuestro servicio de urgencias se observó que la edad media era de 23,5 años y que el paciente tipo era varón y conducía una motocicleta de baja cilindrada1. Las lesiones del miembro superior aparecían en un 20% de los pacientes y había una incidencia del 2 por 1.000 de lesiones del plexo braquial. Otras causas son los accidentes de automóvil, laborales, heridas por arma blanca o de fuego. En un estudio epidemiológico de Midha2, las lesiones del plexo braquial aparecen en el 4,2% de los accidentes de motocicleta y afectan al 1,2% de los politraumatizados.
Según Narakas3 el 70% de las lesiones del plexo braquial traumáticas se producen por accidentes de tráfico y el 70% de éstas se deben a accidentes de motocicleta o ciclomotor. Según datos de la DGT en el año 2000 se produjeron 40.093 heridos entre conductores y pasajeros de motocicletas y ciclomotores en España, lo que permite realizar una estimación aproximada de entre 80 a 160 lesionados de plexo por accidentes de moto anualmente, que suponen aproximadamente la mitad del total de los lesionados de plexo braquial de nuestro país. La incidencia de parálisis braquial obstétrica oscila entre el l y el 2 por 1.000 nacidos en los países industrializados4-7. En nuestro hospital el número de nacimientos vivos en los últimos 4 años es de 9.770 y se han registrado 11 casos de parálisis obstétrica, lo que supone un 1,1 por 1.000. En España, según datos del Instituto Nacional de Estadística la tasa de natalidad actual es de 400.000 niños por año, lo que nos lleva a estimar una frecuencia aproximada de entre 400 a 800 parálisis obstétricas al año.
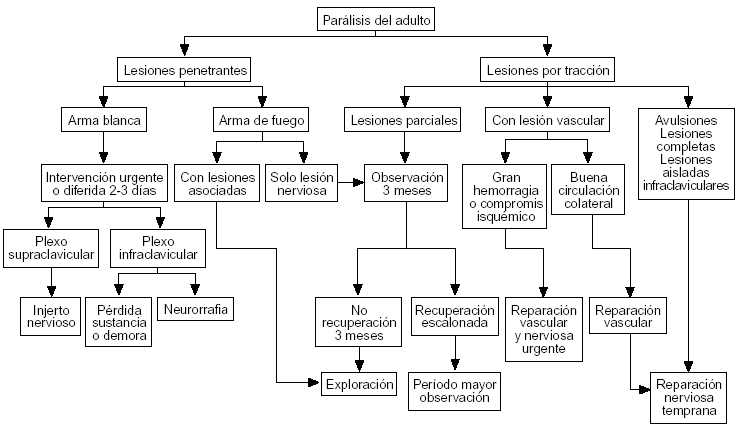
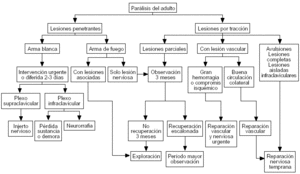
El diagnóstico de estas lesiones es complejo y se basa en la determinación de la extensión, es decir el número de raíces y nervios afectados. También hay que tener en cuenta la localización del nivel de lesión, si las lesiones se sitúan antes del ganglio raquídeo (preganglionares) o después (postganglionares) y dentro de estas últimas es útil situarlas en la zona supraclavicular o infraclavicular; por último es determinante conocer la gravedad de la lesión neurológica desde una neuroapraxia transitoria a una ruptura o arrancamiento nervioso irrecuperable (fig. 1). El pilar del diagnóstico de estas lesiones es la exploración del paciente, que debe quedar recogida en un esquema sistemático sobre la función sensitiva y motora y signos clínicos8-11.
Figura 1. Algoritmo de tratamiento de las lesiones del plexo braquial en el adulto.
El análisis de la evolución clínica ofrece una información diagnóstica muy valiosa, especialmente en lesiones parciales y obstétricas, a la hora de decidir si un paciente precisa de una reparación del plexo braquial temprana o de un período de mayor observación. El estudio debe completarse con las pruebas complementarias que consisten en estudios electroneurofisiológicos10,12 y pruebas de imagen. Entre estas últimas, las que han mostrado mayor utilidad en el diagnóstico son la mielografía y mielo tomografía axial computarizada (TAC)13,14, aunque el desarrollo de mejores aparatos de resonancia magnética (RM) con técnicas 3D y efectos mielográficos permite obtener diagnósticos con resultados iguales o mejores15-18.
La bibliografía sobre el tratamiento de estas lesiones muestra una larga historia de esfuerzos de reparación quirúrgica con fases de optimismo y pesimismo e incluso se ha considerado la amputación, acompañada o no de una artrodesis del hombro, como indicación de elección en los casos más graves19-21. En la actualidad, los avances en microcirugía, el uso de pegamentos biológicos y las técnicas de diagnóstico intraoperatorias han mejorado los resultados quirúrgicos en fases tempranas de la lesión. En un reciente metaanálisis de la bibliografía, de 965 transferencias para la restauración de la flexión del codo, un 71% de las transferencias al nervio musculocutáneo, independientemente del nervio donante, alcanzan ≥ M3 y un 37% llegan a ≥ M422. De 123 transferencias de diferentes autores para la restauración de la abducción del hombro, el 73% de los pacientes alcanzan ≥ M3 y un 26% llegan a ≥ M422. Sin embargo, para que la cirugía nerviosa sea efectiva debe ser lo más precoz posible y los malos resultados se correlacionan con la demora en el tratamiento.
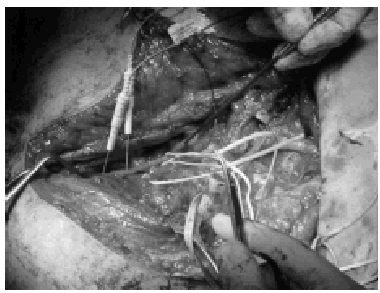
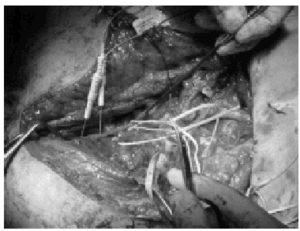
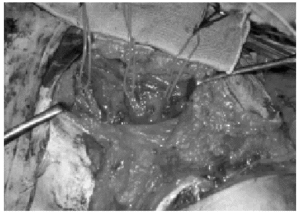
Existen algunas circunstancias en estos pacientes que retrasan la cirugía y por lo tanto empeoran los resultados. En primer lugar es una patología que se suele acompañar de graves lesiones asociadas relacionadas con el plexo (vasculares, óseas, medulares), traumatismos craneoencefálicos, viscerales (abdominales o torácicas) u otras lesiones esqueléticas. El tratamiento inicial de las lesiones más graves que comprometen la vida y posteriormente el tratamiento de otras lesiones esqueléticas de más accesible manejo en cualquier centro, deja en segundo plano la afectación del plexo braquial cuyas lesiones a menudo permanecen olvidadas hasta que el paciente se recupera de las otras. Por otra parte, la estructura del plexo braquial es muy compleja, requiere un abordaje quirúrgico muy amplio y de gran dificultad técnica y precisa de conocimiento de técnicas microquirúrgicas, experiencia en cirugía nerviosa y la disposición de equipos experimentados en el diagnóstico intraoperatorio electrofisiológico, con estudios de potenciales evocados para comprobar la conexión de los muñones radiculares a la médula y estudios de conducción nerviosa para conocer si existen fibras funcionantes atravesando un neuroma (fig. 2)9,10, 12, 23,24. A veces es necesario recurrir a estudios anatomopatológicos intraoperatorios para localizar los axones motores de los sensitivos25 y para reconocer la calidad del tejido nervioso en el lugar de la reparación y, por lo tanto, determinar el nivel apropiado del injerto26 e incluso la exploración endoscópica para una valoración macroscópica de las raíces dentro del canal medular27. Todo esto hace que muchas lesiones irrecuperables sin cirugía evolucionen sin darles la oportunidad de la reconstrucción microquirúrgica o bien este procedimiento quirúrgico quede incompleto. Esto elimina la única oportunidad que tiene el afectado de conseguir una mejoría y perpetúa la creencia de muchos médicos de que las lesiones del plexo braquial van mal se haga lo que se haga.
Figura 2. Imagen del campo quirúrgico con electroneurografía intraoperatoria con estimulación antes del neuroma y registro postneuroma en el nervio musculocutáneo.
En estos pacientes en que la disfunción es muy grave, cualquier ganancia funcional por pequeña que parezca conduce a una satisfacción del paciente y a una mejora en su calidad de vida. Debido a que las posibilidades de tratamiento son muy variadas y dependen del momento en que nos enfrentemos con esta patología, deben estar muy claras las indicaciones y localizadas en el tiempo. El conocimiento de la cronología en las indicaciones quirúrgicas de estas lesiones permite abordar esta patología de la forma más precoz posible, no demorando más allá de lo necesario la recuperación y mejorando los resultados. El propósito de este artículo es actualizar las indicaciones de cómo afrontar estas lesiones, si precisan de una reparación quirúrgica y cuándo es el momento ideal de intervenir, basándonos en nuestra experiencia y la revisión de la bibliografía (fig. 1).
INDICACIONES DE CIRUGÍA INMEDIATA
Lesiones penetrantes
Existen circunstancias en las que las lesiones traumáticas del plexo precisan de una intervención de extrema urgencia. Se trata de las lesiones penetrantes por arma blanca o arma de fuego, con lesión vascular (arteria carótida, yugular, vasos subclavios o axilares), lesiones esofágicas, traqueales o de la cúpula torácica. Estas lesiones requieren una intervención urgente de estas estructuras que comprometen la vida del paciente. Las secciones nerviosas por este mecanismo son postganglionares. Si son por herida incisa o punzante (cuchillo) o incisocontusa (machete), la reparación nerviosa epineural término-terminal puede ser posible cuando se interviene de forma urgente. Sin embargo no es aconsejable realizarla en el plexo supraclavicular, porque existe una incidencia muy elevada de dehiscencia de sutura nerviosa en los primeros días del postoperatorio con los movimientos de lateralización de la cabeza y por la existencia de necrosis o fibrosis intraneural en los extremos que precisa de una adecuada resección de los tejidos dañados28-30.
En todas las lesiones supraclaviculares se deben utilizar injertos cuya longitud se calcula midiendo el defecto creado con la colocación de la cabeza y el hombro en distracción. Se puede considerar la reparación término-terminal directa en las lesiones infraclaviculares, si no existe defecto y si no queda ninguna tensión de la sutura inmovilizando el brazo pegado al cuerpo durante 6 semanas. Si no se dispone de experiencia en este tipo de reparaciones o la situación del paciente no lo permite, se puede diferir la reparación nerviosa pero, preferentemente, no más de dos o tres días para evitar la formación de tejido cicatricial y la retracción de los extremos nerviosos. Las lesiones que más se benefician de una reparación inmediata son las secciones parciales, porque se pueden determinar claramente cuáles son los fascículos lesionados y hacer una reparación selectiva. Si se dejan evolucionar, la fibrosis se extiende y engloba los fascículos intactos, por lo que su identificación es mucho más difícil. Si se marcan los cabos nerviosos debe ser con los tejidos adyacentes, evitando todo tipo de traumatismo del tejido nervioso que obligue a la utilización de injertos más largos.
Los injertos nerviosos se obtienen de los nervios surales de ambas piernas, pero también se puede recurrir a los nervios braquial y antebraquial cutáneo interno del brazo lesionado. También se pueden utilizar injertos vascularizados del nervio radial superficial, del sural o del cubital. Los nervios no vascularizados libres se vascularizan en un plazo de entre 3 y 7 días en un lecho normal y por lo tanto tienen muy pocas diferencias en cuanto a resultados clínicos. No obstante, los injertos nerviosos vascularizados pueden tener su indicación en lechos receptores isquémicos, como después de quemaduras o para reconstrucción con grandes injertos para los troncos en los casos de lesiones del plexo braquial con avulsiones de las raíces C8 y T1 usando el nervio cubital31-33.
Las lesiones por arma de fuego con parálisis nerviosa se deben intervenir de urgencias si existe una lesión asociada que comprometa la vida del paciente (esofágica, traqueal, vascular). Las lesiones nerviosas por arma de fuego dependen de la masa y sobre todo de la velocidad del proyectil. Las heridas por proyectil de alta velocidad originan lesiones en todos los nervios cercanos al trayecto de la bala, debido a la onda de choque periférica que deforma las estructuras periféricas y originan un amplio abanico de lesiones nerviosas, muchas de ellas de buen pronóstico. En ocasiones es necesario realizar una estabilización ósea urgente de clavícula, húmero proximal o escápula; sin embargo, en los proyectiles de alta velocidad es aconsejable dejar evolucionar la lesión nerviosa y esperar la recuperación durante un período de tres meses. Por el contrario, los proyectiles de baja velocidad sólo originan lesión en los nervios sobre los que impactan directamente y por lo tanto se puede plantear una cirugía precoz para reparar estos nervios divididos.
Lesiones cerradas
Las lesiones del plexo braquial por tracción en el adulto con frecuencia se acompañan de lesiones vasculares en el segmento subclavio-axilar, sobre todo en las lesiones infraclaviculares (30%)28,34. La lesión vascular puede originar situaciones urgentes, en las que es preciso intervenir para el control de la hemorragia o para revascularizar un miembro isquémico. Las lesiones del plexo con lesión vascular asociada se caracterizan porque, con mucha frecuencia, se presentan con una parálisis más extensa de la que corresponde a las raíces dañadas en los hallazgos quirúrgicos29. Esto se debe a que se produce una compresión del plexo por un gran hematoma, un pseudoaneurisma expansivo o una fístula arteriovenosa, que provoca una parálisis progresiva en los nervios adyacentes. Estos casos pueden mejorar mucho si se realiza una neurolisis de todo el plexo con descompresión o evacuación del hematoma y se debe hacer precozmente, antes de que se instaure la fibrosis28.
El tratamiento ideal de la lesión nerviosa asociada a lesión vascular es la reparación vascular y nerviosa simultánea. Esto permite una disección adecuada de las lesiones, una reparación término-terminal o con injertos cortos y se disminuye el tiempo de recuperación del paciente. Si se realiza la reparación secundaria de los nervios tras la cirugía vascular inicial, la disección es muy complicada por la fibrosis existente y se corre el riesgo de lesionar el injerto vascular. En situaciones de extrema urgencia a veces no es posible contar con la presencia de un cirujano del plexo braquial e incluso de un cirujano vascular; en estos casos es mejor realizar un control de la hemorragia y una estabilización del paciente, y mandarlo a un centro especializado en el tratamiento de este tipo de lesiones. Siempre se debe realizar reparación vascular para evitar la fibrosis isquémica y la gangrena del miembro.
Para la reparación arterial se deben emplear injertos venosos invertidos de vena safena magna y se deben evitar las prótesis vasculares, especialmente en los pacientes jóvenes en los que se espera mayor recuperación funcional. Las prótesis no se adaptan a los cambios de calibre en los puntos de unión y pueden producir fugas pequeñas o grandes hemorragias que aumentan la fibrosis alrededor de los troncos, y se pueden producir obstrucciones al cruzar una zona de tanta movilidad como es el hombro34,35 Las lesiones de las venas subclavia y axilar deben de ser reparadas antes que la arteria con injertos cortos de vena safena magna35.
Las luxaciones glenohumerales pueden ser la causa de lesión nerviosa por compresión o estiramiento, y exigen una reducción urgente bajo anestesia general, evitando maniobras que puedan lesionar más los nervios afectados o interpuestos. En las lesiones esqueléticas con lesión nerviosa y vascular simultánea a veces hay que realizar una estabilización ósea inmediata, para descomprimir y permitir la reparación de las estructuras vasculonerviosas. Las fracturas humerales, y de codo o antebrazo ipsilaterales deben ser intervenidas, para evitar contracturas e inestabilidades, permitir las exploraciones necesarias y una rehabilitación precoz, y para evitar la evolución a pseudoartrosis, ya que la denervación produce una pérdida de la cubierta estabilizante de las partes blandas proporcionada por las contracciones activas de los músculos36.
INDICACIONES DE CIRUGÍA TEMPRANA EN LESIONES AGUDAS
Existen circunstancias en que conviene realizar la cirugía tan pronto como sea posible, es decir cuando la situación del paciente lo permita y exista un equipo con experiencia en la reparación de estas lesiones. Idealmente la cirugía es más sencilla en los primeros 7 días desde el accidente, aunque consideramos cirugía temprana en las tres primeras semanas. La experiencia demuestra que la disección es mucho más rápida y más fácil de realizar, permite evaluar las lesiones antes de que la fibrosis se extienda, y antes de que se retraigan los muñones, y por lo tanto los injertos necesarios son más cortos. Por último, se acorta el tiempo de recuperación, no demorando la reparación cuando está indicada.
La existencia de avulsiones radiculares o arrancamientos preganglionares implica lesiones irrecuperables si se dejan evolucionar. Aunque las avulsiones pueden afectar a todo el plexo, los tejidos que soportan las raíces inferiores (C8, T1) al foramen vertebral son más débiles que las raíces superiores (C5, C6 y C7) y por lo tanto las hace más vulnerables a la tracción. Para recuperar la función perdida de la raíz avulsionada podemos recurrir a reimplantaciones medulares radiculares y a transferencias nerviosas hacia ciertas funciones esenciales de la parte distal del plexo avulsionado. La primera reimplantación medular de raíces avulsionadas fue realizada por George Bonney en 1977 en un paciente con avulsión de las 5 raíces, a las 48 horas del accidente, con sutura directa, sin evidencias de recuperación28.
Posteriormente Carlstedt ha demostrado cierta recuperación motora después de reimplantaciones radiculares con injerto interpuesto en monos37 y en seres humanos38; aunque cierta regeneración es posible, se necesitan mayores investigaciones en este campo. Las transferencias nerviosas pueden ser intraplexuales o extraplexuales; ambas se basan en la utilización de nervios funcionantes del plexo o de fuera del plexo para reinervar los nervios que estimulan uno o varios músculos específicos. Neurotización es el crecimiento de axones nuevamente desde una estructura inervada a una estructura denervada después de una reparación o una lesión axonal.
De los nervios del propio plexo disponibles, se puede utilizar, en primer lugar, como describieron Harris y Low en 1903, los muñones proximales de otras raíces no avulsionadas (neurotización intraplexual)39-41, pero deben realizarse injertos largos a segmentos distales a los troncos para prevenir el fenómeno de dispersión axonal (figs. 2 y 3). También se ha recurrido a verdaderas transferencias intraplexuales con nervios como el toracodorsal para el axilar8, subescapular para el axilar o para el torácico largo, nervio torácico largo para el musculocutáneo o el supraescapular42, parte del nervio mediano para el musculocutáneo32, y la popular utilización de parte del nervio cubital para el musculocutáneo introducida por Oberlin43,44. Los nervios donantes extraplexales del mismo lado son el accesorio del espinal descrita por Tuttle en 191340,41,45,46, los intercostales (fig. 4)32,40,41,47, el frénico47,48, ramas motoras del plexo cervical e hipogloso8. Pero también se están utilizando nervios contralaterales como la raíz C747,49-51 o la rama anterior del pectoral52. Cuanto más precoz se realicen las transferencias nerviosas más posibilidades de alcanzar la neurotización al músculo o músculos más distales y mejor es el pronóstico. Por tanto, si se sospecha la existencia de avulsiones con los signos clínicos y las pruebas complementarias de imagen y electroneurofisiológicas se debe intervenir tan pronto como sea posible.
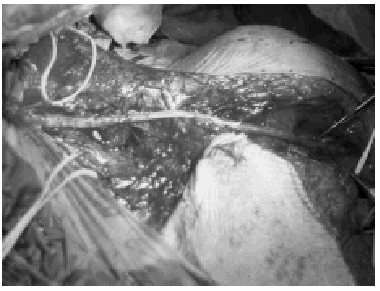
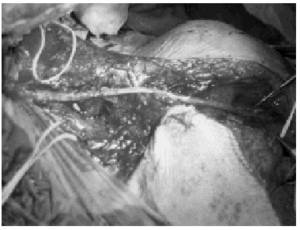
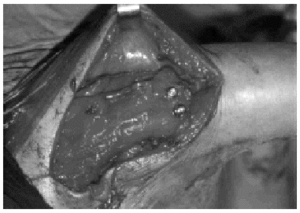
Figura 3. Imagen del campo quirúrgico de paciente con rotura postganglionar de la raíz C5 y avulsión de la raíz C6; se observa la realización de injerto de sural polifascicular de 20 cm desde muñón de raíz C5 hasta nervio musculocutáneo, para evitar la dispersión axonal. Se asoció transferencia de nervio accesorio del espinal para nervio supraescapular y otro injerto monofascicular desde raíz C5 a nervio axilar.
Figura 4. Imagen del campo quirúrgico en la que se observa la obtención de nervios intercostales.
Las lesiones completas del plexo braquial, con parálisis de todas las raíces, son las más frecuentes pues constituyen el 75% de las lesiones traumáticas del adulto53. Las parálisis completas del plexo braquial implican un amplio espectro de lesiones graves con rupturas y avulsiones y en ocasiones a dos niveles (15%), de las que no se espera mejoría si se dejan evolucionar espontáneamente28,53. Las ventajas de una intervención precoz son una exposición más fácil, una rápida identificación de las lesiones irrecuperables (como rupturas y avulsiones) y una realización de injertos interpuestos y transferencias nerviosas tempranas (cuando el potencial de crecimiento de los nervios es mayor). La desventaja es que una demora de la cirugía de unos tres meses permite observar la mejoría de las lesiones potencialmente recuperables y por tanto candidatas exclusivamente a una neurolisis. Las ventajas claramente compensan este inconveniente y existe actualmente consenso mundial para intervenir estas lesiones precozmente.
A la hora de establecer prioridades de las funciones a recuperar se deben valorar cuáles son las más importantes y el potencial de recuperación, y se debe tratar de neurotizar funciones específicas, sobre todo en el adulto, evitando la dispersión de las fibras. En el adulto, el hombro es la función más importante que se puede recuperar junto con la flexión del codo. Otras prioridades son, por ese orden, la sensibilidad en el territorio del mediano, la extensión de la muñeca y la flexión de los dedos. En el niño, sin embargo, la función de la mano es el punto primordial, porque su uso es lo que va a llevar al desarrollo de todo el miembro.
Las lesiones del plexo braquial del adulto con lesión vascular a veces llegan pasados unos días desde el accidente, sin ningún compromiso isquémico y buenos pulsos distales debido a circulación colateral. Aunque la parálisis sea parcial, si coexiste una lesión vascular no isquémica hay que realizar una exploración quirúrgica tan pronto como sea posible. En primer lugar, porque es necesario llevar a cabo siempre la reparación vascular para mantener la troficidad muscular necesaria para la regeneración nerviosa. Y en segundo lugar, es imperativa una exploración temprana de los nervios, ya que una lesión vascular implica siempre la asociación de ruptura o avulsión de los nervios menos elásticos.
Las lesiones aisladas infraclaviculares del nervio supraescapular, axilar y musculocutáneo son frecuentes y de buen pronóstico si el paciente es joven y la reparación se realiza precozmente. En estos casos de lesión nerviosa localizada, las pruebas electroneurofisiológicas (electromiografía, electroneurografía) nos orientan con fiabilidad de la importancia de la lesión. En los casos en que existan potenciales de denervación y bloqueo de la conducción axonal en los músculos inervados por estos nervios a las tres semanas del traumatismo, la lesión es grave y no es necesario demorar la reparación. Por tanto, en estos casos está indicada la exploración quirúrgica temprana.
INDICACIONES DE CIRUGÍA DIFERIDA
Llamamos cirugía diferida a la que se realiza a partir de los tres meses de la lesión. Durante este período se evalúa al paciente, se le realizan todas las pruebas complementarias necesarias y se espera a que las lesiones menos graves (grados I, II y III de Sunderland) (tabla 1) puedan recuperarse. El ejemplo más frecuente en nuestro medio, donde esta actitud es más conveniente, son las lesiones parciales del plexo braquial. Estas lesiones son menos graves y presentan una amplia gama de lesiones, muchas de ellas potencialmente recuperables. Si a los tres meses no se obtiene recuperación de la parálisis de los músculos más proximales, en estas lesiones incompletas se debe realizar una exploración del plexo. Otra indicación de cirugía de las afectaciones parciales es la recuperación de la parálisis en segmentos distales, sin mejoría en los segmentos proximales. Esto indica lesión más grave de las primeras raíces que, por otra parte, tienen más potencial de recuperación y por lo tanto mejor pronóstico si se realiza una reparación. Las parálisis disociativas, es decir con afectación motora pero sin déficit sensitivo, aunque afecten a todos los músculos del brazo, se incluyen en este grupo de lesiones incompletas en el que la evolución es uno de los pilares del diagnóstico y por lo tanto se aconseja una observación de tres meses para comprobar su progresión. Todas las lesiones parciales en que exista una progresión favorable con mejoría escalonada de proximal a distal se deben dejar evolucionar, no siendo precisa la exploración.
Otro supuesto donde esta actitud es imperativa son las lesiones por arma de fuego con proyectiles de alta velocidad, no complicadas, en las que gran parte de la parálisis es originada por la onda de choque y sólo en una mínima parte del plexo se originan verdaderas secciones nerviosas (grados IV y V de Sunderland). La observación de la evolución de los primeros tres meses permite conocer y delimitar la existencia de lesiones graves.
En la parálisis obstétrica la evolución desempeña un papel esencial, aunque la exploración clínica es complicada por la difícil valoración del balance muscular en el neonato54,55. La mayoría de las parálisis obstétricas tienen un buen pronóstico y entre el 80% y el 90% recuperan espontáneamente, debido a que muchas lesiones son leves y a la gran capacidad de regeneración de los tejidos en las primeras semanas de vida7. Sin embargo queda un pequeño grupo de niños a los que si se les deja evolucionar espontáneamente van a tener una función del miembro muy mala56-58. Existen controversias en lo referente a cuándo indicar la cirugía en los casos en que la progresión no sea buena. Los estudios de Gilbert52 y los de Boome y Kaye54 demuestran que si en los bebés de 3 meses de vida se observa inicio de la recuperación del deltoides o del bíceps, el resultado funcional final va a ser normal o bueno. Si la recuperación de estos músculos comienza después de los tres meses, los resultados son muy malos y aleatorios; sin embargo, si a estos pacientes se les interviene precozmente, se mejoran los resultados54,58-62. Como la valoración del deltoides a veces es dificultosa, Gilbert establece el bíceps como músculo guía para la indicación del tratamiento quirúrgico; si a los 3 meses en el niño no se observa contracción de este músculo se debe realizar una exploración quirúrgica sin demorar más del cuarto o quinto mes.
Por último, a veces se observan lesiones del plexo en personas mayores por un traumatismo de baja energía, y se pueden acompañar de una luxación glenohumeral o una fractura de la extremidad proximal de húmero; son generalmente de buen pronóstico y es imperativa la observación de la evolución clínica; se suele percibir una mejoría importante en los 3 primeros meses de la lesión.
INDICACIONES DE CIRUGÍA TARDÍA
En muchas ocasiones los pacientes llegan a la consulta pasados varios meses de producirse la lesión. La experiencia nos demuestra que los resultados son mucho peores cuando la exploración y reparación nerviosa se realiza después de los 6 meses. No obstante ésta es posible realizarla hasta el año de producirse la lesión. Después de este momento los resultados son peores y es mejor plantear una cirugía de secuelas, basada fundamentalmente en las transferencias tendinosas para recuperar funciones esenciales del brazo paralizado como es la abducción del hombro (fig. 5), flexión del codo (fig. 6) o la extensión de la muñeca28,63. A veces después de la cirugía nerviosa es necesario recurrir a este tipo de cirugía con el mismo objetivo. El control voluntario del hombro después de la cirugía nerviosa se consigue a los 12 meses, pero la flexión del codo a veces lleva más de 18 meses.
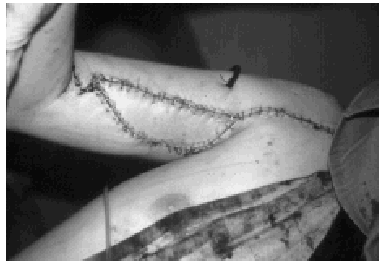
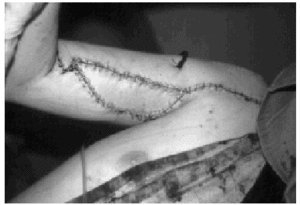
Figura 5. Transferencia de músculo trapecio para la realización de la abducción y estabilización del hombro. Fotografía intraoperatoria en la que se observa el anclaje del acromion con dos tornillos al húmero
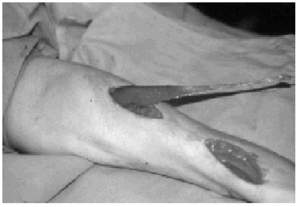
Figura 6. Transferencia de músculo dorsal ancho para la realización de la flexión de codo. Fotografía después del cierre de la herida, en la que se observa la perfecta perfusión de la isla cutánea.
Según Narakas42, la cronología de la secuencia de recuperación muscular y sensitiva, si todo va bien, después de una transferencia de nervios intercostales al nervio musculocutáneo es la siguiente: a los 6 meses se observan contracciones simples del bíceps sincrónicas con la tos o la respiración profunda, y la electromiografía muestra una respuesta de baja amplitud en las unidades motoras; a los 8 meses se pueden registrar contracciones voluntarias y actividad espontánea sincrónica con la respiración normal y durante la tos o la respiración profunda se puede ver el primer vestigio de flexión del codo; a los 10 meses el paciente puede ser capaz de flexionar 90º, pero se fatiga rápidamente y las contracciones involuntarias con la respiración van desapareciendo; al mismo tiempo aparece una sensación de protección en el territorio proximal del nervio musculocutáneo, pero referido a la axila o al pecho; entre los 12 y 14 meses aumenta la fuerza y la sensación se extiende por la parte lateral del antebrazo, y entre los 18 y los 24 meses aumenta la fuerza y la sensación de protección (térmica, nociceptiva y de presión), permaneciendo abolida la extereoceptiva42.
Cuando se ha realizado reparación de las raíces inferiores (C7, C8 y T1) la neurotización de los músculos del antebrazo puede tardar 36 meses, y más de 50 meses para alcanzar la sensibilidad de la mano. Se han constatado mejorías más tardías, aunque estos períodos pueden servir de referencia, para si existe un estancamiento de la recuperación plantear las transferencias tendinosas correspondientes. Cuando no existen músculos para transferir sólo se puede recurrir a los trasplantes de uno o varios músculos libres47,49,64. Otras opciones de tratamiento son la osteotomía desrotadora, la artrodesis, la tenodesis y la liberación de contracturas.
La cirugía generalmente se debe plantear desde distal a proximal, para evitar que una artrodesis de hombro o una contractura en flexión del codo impidan colocar la mano en la posición adecuada para su intervención. Pero cuando se espera mayor recuperación de la mano se puede plantear la cirugía del hombro o el codo. Generalmente hay que esperar hasta que haya terminado la recuperación nerviosa del segmento que se va a intervenir, excepto en la cirugía profiláctica. La recuperación de una función esencial como es la extensión de la muñeca, se puede plantear precozmente, si existen músculos transferibles, aunque exista un potencial de recuperación. En los niños la recuperación después de la realización de injertos nerviosos comienza a los 7 meses de la intervención y se considera que a los 24 meses se alcanza el máximo de reinervación compatible con la recuperación útil de la función muscular. Luego continúa una mejoría debido al proceso de aprendizaje central hasta más de 3 años. La cirugía paliativa también está indicada en la parálisis obstétrica en fase de secuelas y ésta debe plantearse en este último período entre los dos y tres años de vida del niño56-59,61,65,66.
Las lesiones de las raíces C8-T1 o de Déjerine Klumpke suponen un 3% de las supraclaviculares en el adulto53. Se producen por tracción hacia arriba del brazo, originando casi siempre un arrancamiento de las raíces C8 y T1 no recuperable. Las neurotizaciones en estas dos raíces o del tronco primario inferior no han dado ningún resultado en el adulto y los injertos, en las raras lesiones postganglionares, sólo se realizan con el propósito de conseguir una escasa sensibilidad de protección y mitigar el dolor. La escasa recuperación funcional de la musculatura inervada por estas raíces se puede explicar por la larga distancia que tienen que recorrer los axones, por la gran dispersión de las fibras y porque los músculos que inervan son de pequeño tamaño y de una función muy compleja, cuya recuperación sólo es posible en el niño. Por esta razón, no se espera mejoría de las lesiones preganglionares aisladas de las raíces inferiores y la cirugía se plantea para paliar las secuelas. El objetivo es conseguir cierta función en la mano, con la flexión y extensión de los dedos y oposición del pulgar y no es necesario demorarla (fig. 7).
Figura 7. Paciente con lesión de raíces C8 y T1 en fase de secuelas, al que se ha realizado transferencias para la motorización de la mano en dos tiempos. Fotografía intraoperatoria en el primer tiempo quirúrgico, en el que se ha realizado artrodesis de articulación trapeciometacarpiana para mantener la oposición y transferencia de músculo braquioradialis a extensores de los dedos y extensor largo del pulgar.
Después de la aplicación de radioterapia y más frecuentemente después de cáncer de mama se puede producir fibrosis del plexo braquial, que origina parálisis y dolor intenso. Este problema hay que diferenciarlo de una recurrencia tumoral o metástasis, para lo cual son útiles la RM y los estudios electroneurofisiológicos. La cirugía está indicada en los casos de dolor intenso, pérdida de función rápidamente progresiva y en los casos de diagnóstico incierto para descartar afectación tumoral28. La técnica de elección es la neurolisis selectiva, completada con el aporte de tejido vascularizado como un músculo dorsal ancho vascularizado28 o el trasplante libre de omentum67. Los resultados funcionales son malos y como mucho pueden detener la progresión de la parálisis, pero pueden ser efectivos para el control del dolor.
El dolor en las lesiones del plexo braquial es un grave problema y de muy difícil tratamiento. El dolor aparece en las lesiones preganglionares, especialmente en las raíces C8 y T1; es un dolor constante, quemante intenso y en la mayoría de los casos se acompaña de ataques paroxísticos de dolor muy intenso. Se origina por desaferenciación de las células de la zona de reentrada dorsal (DREZ), al producirse el arrancamiento de la raicilla sensitiva del asta posterior de la médula espinal. La amputación no debe considerarse nunca para resolver el dolor al ser éste de origen central20,45, y por otra parte desaparece o disminuye, en la mayoría de los pacientes, hasta un nivel soportable en los tres primeros años68. El tratamiento farmacológico con analgésicos habituales suele ser insuficiente y para controlarlo se precisan fármacos anticonvulsivantes como la carbamacepina, la gabapentina o el ácido valproico. Otras medidas consisten en apoyo psicológico, rehabilitación y técnicas de distracción y estimulación nerviosa transcutánea, aunque es muy resistente al tratamiento28,68. Se ha demostrado el efecto beneficioso de la cirugía nerviosa con injertos y transferencias69, pero en los casos más refractarios al tratamiento está indicado el procedimiento neuroquirúrgico de Nashold, consistente en la termocoagulación de las astas dorsales desaferenciadas o zona DREZ70. Este procedimiento ha demostrado su efectividad, aunque no está exento de complicaciones70,71 y debe reservarse a los casos incontrolables por las medidas anteriores y que no han tenido la mejoría espontánea después de los tres años o incluso hayan empeorado28,68,71.