La infección es una de las complicaciones locales más importantes en el paciente con fractura del cuello femoral tratada con una artroplastia. El objetivo del presente estudio es describir y analizar posibles factores de riesgo que podrían estar implicados en la infección periprotésica del paciente con fractura del cuello femoral.
Material y métodosSe realizó un estudio de casos y controles retrospectivo que incluye a pacientes con fractura del cuello femoral tratada con una artroplastia en el periodo comprendido entre enero de 2015 y diciembre de 2017. Se definieron como casos a los pacientes con fractura del cuello femoral que tras someterse a una artroplastia (hemiartroplastia o artroplastia total de cadera) tuvieron como desenlace una infección periprotésica, cuyo diagnóstico se llevó a cabo atendiendo a los criterios mayores y menores descritos en el Consenso Internacional de Infecciones Musculoesqueléticas (Philadelphia 2018). Con la intención de atenuar la influencia de variables que podrían considerarse confusoras, se realizó un análisis multivariante.
ResultadosSe apreció una asociación estadísticamente significativa entre infección periprotésica y determinadas variables presentes en el momento del ingreso, entre las que se encuentran la presencia de anemia moderada o severa (OR: 10,91; IC95%: 1,07-111,50; p=0,007), trombocitopenia (OR: 27,72; IC95%: 3,48-221,01; p=0,002), el antecedente tromboembólico (OR: 8,80; IC95%: 1,31-59,38; p=0,026), el trastorno ansioso-depresivo en tratamiento con 2 o 3 fármacos (OR: 21,36; IC95%: 3,65-125,12; p=0,001) y la hepatopatía (OR: 32,04; IC95%: 2,59-396,29; p=0,007).
ConclusionesLa infección periprotésica en el paciente con fractura del cuello femoral tratado con una artroplastia podría relacionarse con la presencia de determinadas variables en el momento del ingreso hospitalario, entre las que se encuentran la anemia moderada o severa, la trombocitopenia, el antecedente de evento tromboembólico, el trastorno ansioso-depresivo en tratamiento con 2 o 3 fármacos o la hepatopatía.
Infection is one of the most important local complications in the patient with femoral neck fracture treated with arthroplasty. The aim of the present study is to describe and analyze possible risk factors that could be involved in periprosthetic infection in the patient with femoral neck fracture.
MethodsA retrospective case-control study was performed including patients with femoral neck fractures treated with arthroplasty in the period between January 2015 and December 2017. Cases were defined as patients with femoral neck fracture who after undergoing arthroplasty (hemiarthroplasty or total hip arthroplasty) had a periprosthetic infection, whose diagnosis was carried out according to the major and minor criteria described in the International Consensus on Musculoskeletal Infections (Philadelphia 2018). In order to mitigate the influence of variables that could be considered confounding variables, a multivariate analysis was carried out.
OutcomesA statistically significant association was found between periprosthetic infection and certain variables present at the time of admission, including the presence of moderate or severe anaemia (OR: 10.91; 95%CI: 1.07-111.50; P=.007), thrombocytopenia (OR: 27.72; 95%CI: 3.48-221.01; P=.002), history of thromboembolism event (OR: 8.80; 95%CI: 1.31-59.38; P=.026), anxious-depressive disorder in treatment with two or three drugs (OR: 21.36; 95%CI: 3.65-125.12; P=.001) and liver disease (OR: 32.04; 95%CI: 2.59-396.29; P=.007).
ConclusionsPeriprosthetic infection in the patient with femoral neck fracture treated with arthroplasty could be related to the presence of certain variables at the time of hospital admission, including moderate or severe anaemia, thrombocytopenia, history of thromboembolic event, anxious-depressive disorder in treatment with two or three drugs or liver disease.
El aumento en la esperanza de vida se acompaña de un incremento en la incidencia de la fractura de cadera, considerada una de las principales causas de mortalidad e incapacidad en el paciente anciano. Mientras que en 1990 se diagnosticaron en torno a 1,66 millones de fracturas de cadera en todo el mundo, se estima que estas cifras alcanzarán los 4,5 millones en el año 20501.
Desde un punto de vista anatómico y fisiológico pueden diferenciarse dos grandes grupos: las fracturas intracapsulares y las extracapsulares. Las intracapsulares incluyen las fracturas de la cabeza y del cuello femoral, siendo este último el grupo más numeroso2. Así pues, en dicho grupo la mayor parte se corresponden con fracturas desplazadas del cuello femoral, que suelen precisar una hemiartroplastia (HA) o una artroplastia total de cadera (ATC)3.
La artroplastia de cadera no está exenta de complicaciones4, entre las que destaca la infección periprotésica, que puede acompañarse de reingresos y reintervenciones, largos periodos con antibioterapia y un deterioro funcional del paciente. La incidencia de dicha complicación se sitúa en torno al 1,3% en la artroplastia de cadera electiva; sin embargo, esta cifra podría alcanzar hasta el 4,7% en la artroplastia de cadera realizada por fractura5. Dada su importancia, resulta fundamental identificar qué factores de riesgo podrían estar involucrados en su aparición, pues la optimización o eliminación de estos puede contribuir a disminuir su incidencia. En este sentido, Breznicky et al.6 sugieren que entre los factores de riesgo clave podrían encontrarse el índice de masa corporal (IMC), la diabetes y la enfermedad renal o hepática. También se ha analizado la influencia de variables como el índice de comorbilidad de Charlson, la duración de la estancia hospitalaria o la tasa de transfusión perioperatoria7.
El objetivo del presente trabajo es describir y analizar factores de riesgo que podrían estar implicados en la infección periprotésica del paciente con fractura del cuello femoral.
Material y métodosSe realizó un estudio de casos y controles, retrospectivo, en el que se incluyeron pacientes con fractura del cuello femoral tratada con una artroplastia, HA o ATC, en el periodo comprendido entre enero de 2015 y diciembre de 2017. Se excluyó del estudio a los pacientes que presentaban un trastorno del metabolismo óseo distinto a la osteoporosis (osteomalacia, osteodistrofia renal o enfermedad de Paget), pacientes con menos de 50años, pacientes intervenidos en otros hospitales, pacientes intervenidos en nuestro centro hospitalario con domicilio en otra área sanitaria (realizaron el seguimiento postoperatorio en su hospital de referencia) y aquellos que no dieron su consentimiento para participar en el estudio.
En todos los casos, el procedimiento (HA o ATC) se realizó o supervisó (cuando operó un residente) por un cirujano experimentado. La decisión de utilizar una HA o una ATC se llevó a cabo atendiendo a la puntuación alcanzada en el índice de comorbilidad de Charlson (edad y comorbilidades fundamentales) y en el índice de Barthel (grado de autonomía). No obstante, aunque dichas puntuaciones suponen una herramienta muy útil, no se establecieron criterios rígidos, siendo necesario individualizar cada caso. Cuando se optó por una HA, se usó una prótesis bipolar en los menores de 85años y una monopolar en los pacientes más añosos, con edades superiores a los 85años. En la HA se utilizó un vástago cementado. Por el contrario, en la ATC se utilizó un vástago cementado en la mayoría de los casos, a excepción de algunos pacientes en los que, tras valorar de forma intraoperatoria la densidad ósea, se consideró la no cementación. Cuando se llevó a cabo cementación se utilizó cemento sin antibióticos. Asimismo, en la ATC se implantó un componente acetabular no cementado. En todos los pacientes se realizó un abordaje lateral de Hardinge y se llevaron a cabo las siguientes medidas perioperatorias: profilaxis antibiótica preoperatoria con cefazolina 2g (salvo alergia a la penicilina, en cuyo caso se administró vancomicina), tromboprofilaxis con heparina de bajo peso molecular, raquianestesia y protocolo de rehabilitación, que comenzó en el postoperatorio inmediato.
Se definieron como casos a los pacientes con fractura del cuello femoral que tras someterse a una artroplastia (HA o ATC) tuvieron como desenlace una infección periprotésica, cuyo diagnóstico se llevó a cabo atendiendo a los criterios mayores y menores descritos por Parvizi et al.8. Por el contrario, se consideraron controles todos los pacientes que tras el tratamiento con una artroplastia de cadera por fractura del cuello femoral no presentaron una infección periprotésica. Todos los controles se extrajeron de la misma cohorte de donde surgieron los casos. Los criterios de inclusión y exclusión se aplicaron de forma semejante en la selección de los casos y los controles.
Todos los pacientes (o sus representantes legales autorizados) firmaron consentimiento informado. Durante todo el proyecto se siguieron los principios éticos dispuestos en la Declaración de Helsinki, con su última revisión en Fortaleza, Brasil, 2013. Se obtuvo el visto bueno del Comité de Ética de la Investigación Provincial de Málaga en la sesión celebrada el 30 de julio de 2020.
En el momento del ingreso hospitalario se recogieron variables demográficas (sexo, edad e IMC), diversos índices preoperatorios (Barthel, comorbilidad de Charlson, American Society of Anesthesiologists [ASA]), hábitos tóxicos (consumo de tabaco y alcohol), comorbilidades (obesidad, HTA, dislipemia, gota, insuficiencia venosa periférica, diabetes, inmunosupresión, patología tiroidea, respiratoria, cardiaca, hematológica, mental, renal, hepática, oncológica y neurológica), lateralidad, grado de desplazamiento de la fractura (clasificación de Garden), tipo de procedimiento (HA o ATC), tiempo quirúrgico, perfil del cirujano que realiza el procedimiento (facultativo vs. MIR y traumatólogo general vs. traumatólogo de la unidad de cadera), parámetros analíticos preoperatorios (hemoglobina, plaquetas, urea, creatinina y filtrado glomerular) y postoperatorios (hemoglobina), necesidad de transfusión (preoperatoria o postoperatoria), estancia hospitalaria (preoperatoria y postoperatoria). Atendiendo a la clasificación de la Organización Mundial de la Salud (OMS), se estableció el diagnóstico de anemia leve ante la presencia de niveles de hemoglobina entre 12 y 10g/dl, y anemia moderada o severa con valores inferiores a 10g/dl. De la misma manera, la trombocitopenia se diagnosticó con niveles de plaquetas inferiores a 100.000/mm3, lo que incluye a las trombocitopenias moderadas y graves. En el postoperatorio se registraron las complicaciones locales, entre las que se incluyó la infección periprotésica (clasificación de Tsukayama9 y germen causal), la luxación, la fractura periprotésica, el aflojamiento aséptico, la dismetría, la insuficiencia glútea y la cojera. También se registraron las complicaciones sistémicas (anemia moderada o severa, evento tromboembólico, neumonía, problema cardiaco, delirium, infección del tracto urinario, hemorragia digestiva o descompensación multiorgánica), los reingresos y las reintervenciones, la mortalidad, el dolor (escala visual analógica [EVA]), la función (escalas Harris, Oxford y WOMAC), la calidad de vida (EuroQol-5D) y la satisfacción del paciente (insatisfecho, parcialmente satisfecho y satisfecho).
Los datos se recogieron en el momento del ingreso, durante la estancia en el hospital y en las revisiones ambulatorias, que se realizaron al mes, a los 3meses y a los 12meses del procedimiento. Durante el seguimiento se identificaron y describieron las pérdidas.
Se identificaron y abordaron los posibles sesgos. Los casos se definieron de forma precisa, con la intención de evitar falsos casos (sesgo de selección). Se clasificó de forma exhaustiva y homogénea tanto a los casos como a los controles, con el fin de evitar una clasificación errónea (sesgo de clasificación). Los datos se extrajeron siguiendo un protocolo estandarizado, similar en todos los participantes, con las mismas fuentes de información en ambos grupos (sesgo de información). Asimismo, con el fin de atenuar el sesgo de recuerdo, se minimizó el tiempo entre la exposición y la realización del estudio.
Los datos recogidos se introdujeron en una base de datos Excel (Microsoft® Excel® 2016 MSO, versión 2202 compilación 16.0.14931.20118) y se analizaron con el programa Statistical Package for Social Sciences (IBM SPSS® Statistics, versión 25). Desde el punto vista de la estadística descriptiva, las variables cuantitativas se expusieron como medidas de tendencia central (media aritmética, mediana y moda) y medidas de dispersión (desviaciones típicas y rangos). Las variables cualitativas se describieron mediante frecuencias y porcentajes. El análisis cualitativo se realizó con el test chi-cuadrado de Pearson. Tras corroborar que las variables cuantitativas no seguían una distribución normal, el análisis cuantitativo se llevó a cabo con la prueba U de Mann-Whitney (muestras independientes). Las diferencias apreciadas se consideraron estadísticamente significativas cuando el valor de p fue inferior a 0,05.
Se realizó un análisis por subgrupos con la intención de identificar variables con una distribución diferente en los casos y los controles. Además, tras realizar un análisis estadístico bivariado, se llevó a cabo un análisis multivariante.
Con la intención de reflejar la fuerza de asociación entre la variable de resultado principal (infección periprotésica) y las diferentes variables independientes, se calcularon los diferentes odds ratio (OR).
ResultadosEl presente estudio incluyó a pacientes con fractura del cuello femoral tratada con una artroplastia entre enero de 2015 y diciembre de 2017. Se apreció un seguimiento medio de 4,48±0,89años (rango: 2,97-5,98). La muestra preliminar fue de 543 pacientes; sin embargo, se excluyeron 36 que se trataron mediante osteosíntesis y 15 tratados de forma conservadora. También se excluyeron 16 pacientes que cambiaron su domicilio a otra área sanitaria, por lo que no pudieron realizar el seguimiento postoperatorio. Con todo ello, el tamaño muestral final fue de 476 pacientes.
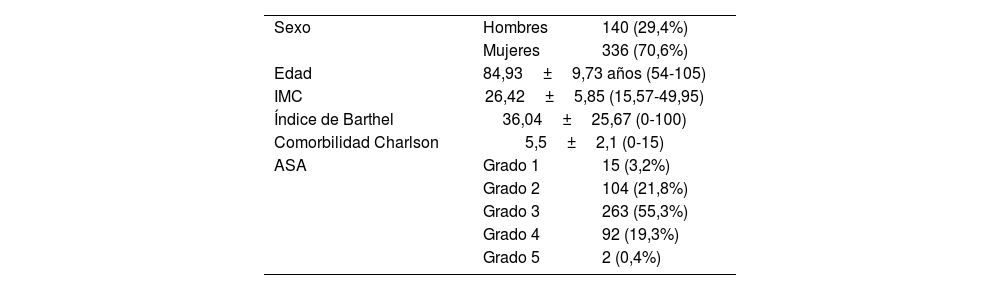
Las variables sociodemográficas e índices preoperatorios se exponen en la tabla 1.
Variables sociodemográficas e índices preoperatorios
| Sexo | Hombres | 140 (29,4%) |
| Mujeres | 336 (70,6%) | |
| Edad | 84,93±9,73 años (54-105) | |
| IMC | 26,42±5,85 (15,57-49,95) | |
| Índice de Barthel | 36,04±25,67 (0-100) | |
| Comorbilidad Charlson | 5,5±2,1 (0-15) | |
| ASA | Grado 1 | 15 (3,2%) |
| Grado 2 | 104 (21,8%) | |
| Grado 3 | 263 (55,3%) | |
| Grado 4 | 92 (19,3%) | |
| Grado 5 | 2 (0,4%) | |
Se identificaron 226 fracturas con lateralidad derecha (47,5%), frente a 250 con lateralidad izquierda (52,5%). Se registraron 59 fracturas Garden2 (12,4%), 183 Garden3 (38,4%) y 234 Garden4 (49,2%).
Respecto al tipo de procedimiento, 310 pacientes (65,1%) se trataron con una HA y 166 (34,9%) con una ATC. Atendiendo al perfil del cirujano, 177 fracturas (37,2%) fueron operadas por residentes y 299 (62,9%) por facultativos especialistas de área. Asimismo, 95 fracturas (20%) se operaron por la unidad de cadera, frente a 381 fracturas (80%) que se intervinieron por el resto de unidades, incluida la unidad de trauma.
La infección periprotésica, considerada variable de resultado principal, fue la complicación local postoperatoria más frecuente. El grupo de los casos, compuesto por aquellos pacientes que tuvieron como desenlace una infección periprotésica, incluyó un total de 15 pacientes (3,2%), frente al grupo de los controles, constituido por 461 pacientes (96,8%) que no presentaron infección periprotésica.
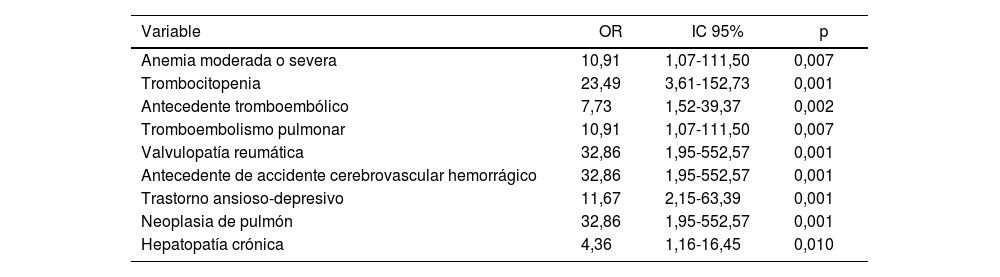
La realización de un análisis cualitativo mediante el test chi-cuadrado de Pearson puso de manifiesto que la infección periprotésica fue más frecuente entre los pacientes que en el momento del ingreso hospitalario presentaban anemia moderada o severa (25% vs. 2,9%, p=0,035), trombocitopenia (40% vs. 2,8%, p=0,001), antecedente tromboembólico (18,2% vs. 2,8%, p=0,043), valvulopatía reumática (50% vs. 2,9%, p<0,001), antecedente de accidente cerebrovascular de tipo hemorrágico (50% vs. 2,7%, p=0,011), trastorno ansioso-depresivo en tratamiento con 2 o 3fármacos (25% vs. 3,2%, p=0,044), neoplasia de pulmón (50% vs. 3%, p=0,001) o hepatopatía crónica (20% vs. 2,7%, p=0,028). Como medida de asociación se calculó la OR, que se muestra en la tabla 2.
Medidas de asociación entre infección periprotésica y comorbilidad presente al ingreso. Cálculo de la odds ratio (OR), intervalo de confianza del 95% (IC95%) y valor de p
| Variable | OR | IC 95% | p |
|---|---|---|---|
| Anemia moderada o severa | 10,91 | 1,07-111,50 | 0,007 |
| Trombocitopenia | 23,49 | 3,61-152,73 | 0,001 |
| Antecedente tromboembólico | 7,73 | 1,52-39,37 | 0,002 |
| Tromboembolismo pulmonar | 10,91 | 1,07-111,50 | 0,007 |
| Valvulopatía reumática | 32,86 | 1,95-552,57 | 0,001 |
| Antecedente de accidente cerebrovascular hemorrágico | 32,86 | 1,95-552,57 | 0,001 |
| Trastorno ansioso-depresivo | 11,67 | 2,15-63,39 | 0,001 |
| Neoplasia de pulmón | 32,86 | 1,95-552,57 | 0,001 |
| Hepatopatía crónica | 4,36 | 1,16-16,45 | 0,010 |
La infección periprotésica también fue más frecuente entre los pacientes que en el postoperatorio sufrieron una luxación (25% vs. 2,8%, OR: 11,67, IC95%: 2,15-63,39, p=0,023). No se apreciaron diferencias estadísticamente significativas respecto a otras complicaciones locales ni sistémicas (37,5% vs. 33,3%, p=0,485).
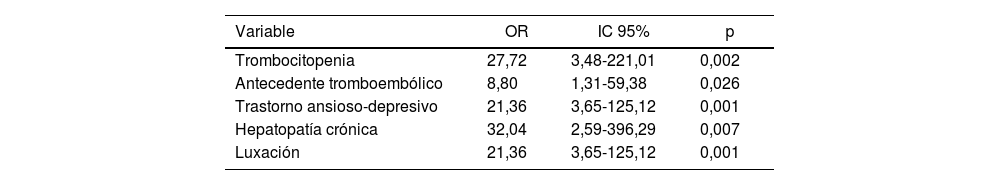
Se realizó un análisis multivariante, cuyos resultados se presentan en la tabla 3.
Análisis multivariante. Odds ratio (OR), intervalo de confianza del 95% (IC95%) y valor de p
| Variable | OR | IC 95% | p |
|---|---|---|---|
| Trombocitopenia | 27,72 | 3,48-221,01 | 0,002 |
| Antecedente tromboembólico | 8,80 | 1,31-59,38 | 0,026 |
| Trastorno ansioso-depresivo | 21,36 | 3,65-125,12 | 0,001 |
| Hepatopatía crónica | 32,04 | 2,59-396,29 | 0,007 |
| Luxación | 21,36 | 3,65-125,12 | 0,001 |
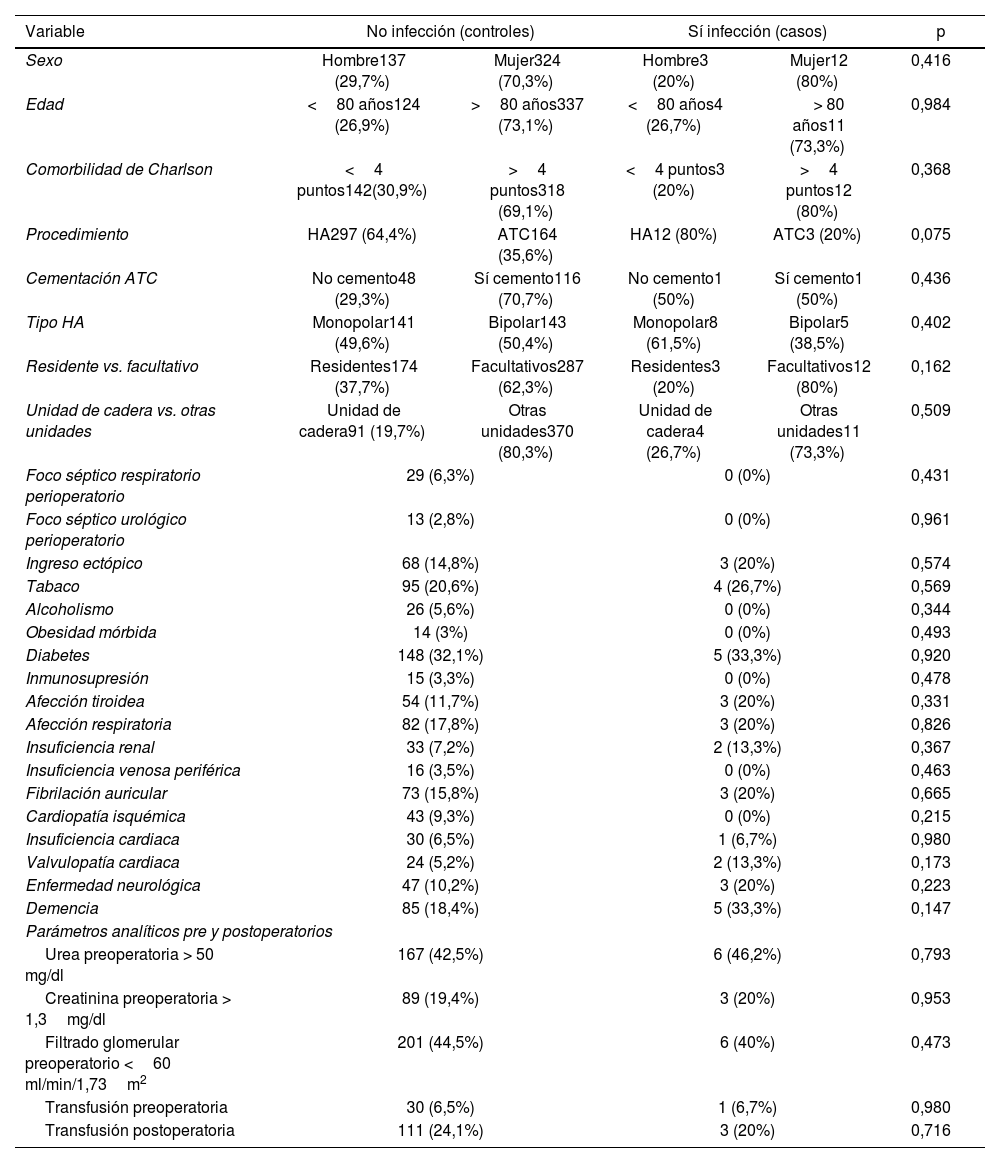
En la tabla 4 se expone un resumen con factores de riesgo analizados que no presentaron una asociación estadísticamente significativa con la variable infección.
Variables de la exposición que no presentaron asociación estadísticamente significativa con la variable infección
| Variable | No infección (controles) | Sí infección (casos) | p | ||
|---|---|---|---|---|---|
| Sexo | Hombre137 (29,7%) | Mujer324 (70,3%) | Hombre3 (20%) | Mujer12 (80%) | 0,416 |
| Edad | <80 años124 (26,9%) | >80 años337 (73,1%) | <80 años4 (26,7%) | > 80 años11 (73,3%) | 0,984 |
| Comorbilidad de Charlson | <4 puntos142(30,9%) | >4 puntos318 (69,1%) | <4 puntos3 (20%) | >4 puntos12 (80%) | 0,368 |
| Procedimiento | HA297 (64,4%) | ATC164 (35,6%) | HA12 (80%) | ATC3 (20%) | 0,075 |
| Cementación ATC | No cemento48 (29,3%) | Sí cemento116 (70,7%) | No cemento1 (50%) | Sí cemento1 (50%) | 0,436 |
| Tipo HA | Monopolar141 (49,6%) | Bipolar143 (50,4%) | Monopolar8 (61,5%) | Bipolar5 (38,5%) | 0,402 |
| Residente vs. facultativo | Residentes174 (37,7%) | Facultativos287 (62,3%) | Residentes3 (20%) | Facultativos12 (80%) | 0,162 |
| Unidad de cadera vs. otras unidades | Unidad de cadera91 (19,7%) | Otras unidades370 (80,3%) | Unidad de cadera4 (26,7%) | Otras unidades11 (73,3%) | 0,509 |
| Foco séptico respiratorio perioperatorio | 29 (6,3%) | 0 (0%) | 0,431 | ||
| Foco séptico urológico perioperatorio | 13 (2,8%) | 0 (0%) | 0,961 | ||
| Ingreso ectópico | 68 (14,8%) | 3 (20%) | 0,574 | ||
| Tabaco | 95 (20,6%) | 4 (26,7%) | 0,569 | ||
| Alcoholismo | 26 (5,6%) | 0 (0%) | 0,344 | ||
| Obesidad mórbida | 14 (3%) | 0 (0%) | 0,493 | ||
| Diabetes | 148 (32,1%) | 5 (33,3%) | 0,920 | ||
| Inmunosupresión | 15 (3,3%) | 0 (0%) | 0,478 | ||
| Afección tiroidea | 54 (11,7%) | 3 (20%) | 0,331 | ||
| Afección respiratoria | 82 (17,8%) | 3 (20%) | 0,826 | ||
| Insuficiencia renal | 33 (7,2%) | 2 (13,3%) | 0,367 | ||
| Insuficiencia venosa periférica | 16 (3,5%) | 0 (0%) | 0,463 | ||
| Fibrilación auricular | 73 (15,8%) | 3 (20%) | 0,665 | ||
| Cardiopatía isquémica | 43 (9,3%) | 0 (0%) | 0,215 | ||
| Insuficiencia cardiaca | 30 (6,5%) | 1 (6,7%) | 0,980 | ||
| Valvulopatía cardiaca | 24 (5,2%) | 2 (13,3%) | 0,173 | ||
| Enfermedad neurológica | 47 (10,2%) | 3 (20%) | 0,223 | ||
| Demencia | 85 (18,4%) | 5 (33,3%) | 0,147 | ||
| Parámetros analíticos pre y postoperatorios | |||||
| Urea preoperatoria > 50 mg/dl | 167 (42,5%) | 6 (46,2%) | 0,793 | ||
| Creatinina preoperatoria > 1,3mg/dl | 89 (19,4%) | 3 (20%) | 0,953 | ||
| Filtrado glomerular preoperatorio <60 ml/min/1,73m2 | 201 (44,5%) | 6 (40%) | 0,473 | ||
| Transfusión preoperatoria | 30 (6,5%) | 1 (6,7%) | 0,980 | ||
| Transfusión postoperatoria | 111 (24,1%) | 3 (20%) | 0,716 | ||
Con la realización del test U de Mann-Whitney tampoco se apreciaron diferencias estadísticamente significativas respecto al número de unidades transfundidas en el preoperatorio (0,12±0,49 vs. 0,13±0,52, p=0,973) y en el postoperatorio (0,52±1,02 vs. 0,40±0,83, p=0,697).
La estancia hospitalaria global fue de 12,0±9,7 días (HA: 12,0±5,9 días vs. ATC: 11,0±14,3 días). Asimismo, la estancia hospitalaria en los casos fue de 13,0±2,6 días, frente a 12,0±9,9 días en los controles (p=0,053).
Con el tratamiento mediante HA (100% cementadas) se registró un tiempo quirúrgico medio de 39±8minutos, frente a 58±11minutos con la ATC (70,5% cementadas vs. 29,5% no cementadas), sin poder apreciarse diferencias estadísticamente significativas entre la variable tiempo quirúrgico y la variable infección periprotésica (p>0,05).
En la tabla 5 se exponen los microorganismos identificados en función del tipo de procedimiento (HA vs. ATC) y el tipo de infección según la clasificación de Tsukayama, considerándose significativos cuando se aislaron en al menos 3 muestras intraoperatorias.
Distribución de los microorganismos causales atendiendo al tipo de procedimiento y la clasificación de Tsukayama
| Procedimiento | Clasificación de Tsukayama | Microorganismo | Frecuencia y porcentaje |
|---|---|---|---|
| HA: 12 (80%) | Aguda: 9 (75%) | Staphylococcus aureus | 2 (22,2%) |
| Polimicrobiana (S. aureus y S. epidermis) | 2 (22,2%) | ||
| Escherichia coli | 1 (11,1%) | ||
| Pseudomonas aeruginosa | 4 (44,4%) | ||
| Crónica: 2 (16,7%) | Staphylococcus aureus | 1 (50%) | |
| Enterobacter cloacae | 1 (50%) | ||
| Hematógena: 1 (8,3%) | Pseudomonas aeruginosa | 1 (100%) | |
| ATC: 3 (80%) | Aguda: 1 (33,3%) | Klebsiella pneumoniae | 1 (100%) |
| Crónica: 2 (66,7%) | Staphylococcus epidermidis | 2 (100%) |
Durante los 12 meses posteriores al procedimiento fallecieron 52 pacientes (10,9%), que deben considerarse pérdidas durante el seguimiento. De los 52 pacientes, 32 (6,7%) fallecieron durante el ingreso hospitalario y 20 (4,2%) tras al alta hospitalaria. No se apreciaron diferencias estadísticamente significativas respecto a la mortalidad intrahospitalaria (31 [6,7%] vs. 1 [6,7%], p=0,733) ni en el primer año (51 [11,1%] vs. 1 [6,7%], p=0,498) entre los casos y los controles.
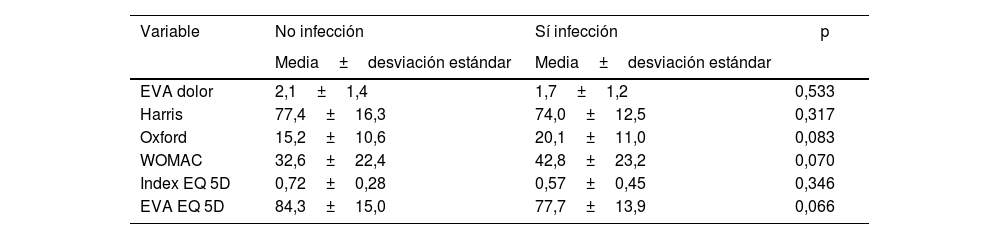
A los 12 meses de la fractura, los resultados funcionales y de calidad de vida no presentaron diferencias estadísticamente significativas respecto a la variable infección periprotésica; sin embargo, sí se apreció que los pacientes con infección presentaban resultados funcionales y de calidad de vida inferiores (tabla 6).
Resultados funcionales y de calidad de vida a los 12 meses de la fractura
| Variable | No infección | Sí infección | p |
|---|---|---|---|
| Media±desviación estándar | Media±desviación estándar | ||
| EVA dolor | 2,1±1,4 | 1,7±1,2 | 0,533 |
| Harris | 77,4±16,3 | 74,0±12,5 | 0,317 |
| Oxford | 15,2±10,6 | 20,1±11,0 | 0,083 |
| WOMAC | 32,6±22,4 | 42,8±23,2 | 0,070 |
| Index EQ 5D | 0,72±0,28 | 0,57±0,45 | 0,346 |
| EVA EQ 5D | 84,3±15,0 | 77,7±13,9 | 0,066 |
La infección periprotésica se relacionó con una mayor insatisfacción del paciente (5,6% vs. 3,1%); sin embargo, dicha diferencia no resultó estadísticamente significativa (p=0,782).
DiscusiónLa infección es una de las principales complicaciones en el paciente con fractura del cuello femoral tratado con una artroplastia. En nuestra serie fue la complicación local postoperatoria más frecuente. Dada su importancia, diversos autores han tratado de identificar qué factores de riesgo podrían estar implicados en su aparición. Noailles et al.10 presentaron una revisión sistemática que relacionó la infección periprotésica con la presencia de comorbilidad (obesidad, enfermedad hepática o edad avanzada), con aspectos relacionados con el procedimiento quirúrgico (realización por un cirujano junior, uso de vástagos no cementados o retraso en la programación quirúrgica) y con el manejo perioperatorio (estancia hospitalaria prolongada, presencia de hematoma, drenaje persistente a través de la herida o sondaje urinario). A este respecto, en el presente trabajo los hallazgos más relevantes fueron la asociación estadísticamente significativa entre infección periprotésica y la presencia de determinadas variables en el momento de ingreso, entre las que se encuentran la anemia, la trombocitopenia, el antecedente de evento tromboembólico, el trastorno ansioso-depresivo y la hepatopatía crónica.
La anemia moderada o severa es un factor de riesgo de infección en el paciente intervenido de fractura de cadera, que se incrementa cuando dicho paciente precisa la transfusión de hemoderivados alogénicos. Este hecho parece estar relacionado con cambios inmunitarios que se producen tras recibir una transfusión, entre los que destacan el descenso en los niveles de IL-2, la inhibición de las células natural killer (NK) y la disminución de la respuesta de hipersensibilidad. También se han apreciado cambios en la inmunomodulación, que conllevan una reducción en la respuesta inmunitaria ante la presencia de bacterias en el lecho quirúrgico, lo que podría favorecer el desarrollo de una infección11.
La presencia de trombocitopenia moderada o grave en pacientes que se operan de fractura del cuello femoral incrementa el riesgo de sangrado durante la cirugía, lo que puede llevar a la formación de hematomas, un «caldo de cultivo» para la proliferación bacteriana y, en consonancia con lo apreciado en nuestra serie, el desarrollo de una infección. En la misma línea, los pacientes con antecedentes de tromboembolismo en tratamiento con terapia anticoagulante también presentan un aumento en el riesgo de infección, motivado por la formación de hematomas perioperatorios que pueden favorecer el crecimiento bacteriano12.
En nuestro análisis se apreció una mayor incidencia de infección entre los pacientes con trastorno ansioso-depresivo. Así pues, se ha descrito que en estos pacientes se producen alteraciones en la angiogénesis y la inmunomodulación, así como una supresión de las células NK y de las células presentadoras de antígenos, que resultan fundamentales para generar la respuesta inmunitaria13,14.
Los pacientes con hepatopatía crónica en fase evolucionada presentan un aumento de la hipertensión portal, una circulación hiperdinámica y una situación de inmunosupresión secundaria a la disfunción hepática, circunstancias que incrementan el riesgo de infección. Asimismo, en pacientes con hepatopatía crónica suele producirse una traslación bacteriana intestinal secundaria a la hipertensión portal, una disfunción de los polimorfonucleares (PMN), una disminución del complemento y alteraciones en el sistema reticuloendotelial, aspectos que afectan negativamente a la respuesta inmunitaria15.
En relación con factores de riesgo considerados clásicos, como la diabetes mellitus, a diferencia de lo descrito por Park et al.16, en nuestra serie los pacientes diabéticos presentaron una incidencia de infección periprotésica discretamente superior (3,8% vs. 3,1%); sin embargo, dicha diferencia no resultó estadísticamente significativa (p=0,559). Tampoco se apreciaron diferencias respecto a otros factores de riesgo clásicos, entre los que se encuentra el IMC (p=0,493)17.
Respecto al tipo de procedimiento, en consonancia con lo descrito en el metaanálisis de Peng et al.18, nuestro análisis no identificó diferencias estadísticamente significativas entre los pacientes tratados con HA y ATC (p=0,075); sin embargo, sí se apreció una incidencia de infección superior en los pacientes en los que se utilizó una HA frente a una ATC (13 [4,2%] vs. 2 [1,2%]).
Diferentes autores, como DeAngelis et al.19, sugieren que la incidencia de infección periprotésica podría reducirse cuando la intervención es llevada a cabo por cirujanos con fellowship en artroplastia de cadera (p=0,01). También se ha descrito que la infección es más frecuente entre los cirujanos que realizan menos artroplastias de cadera/año (p=0,042)20. A este respecto, en nuestra serie no se observaron diferencias estadísticamente significativas entre los pacientes intervenidos por la unidad de cadera y los operados por otras unidades, que suelen realizar menos artroplastias de cadera/año.
La infección periprotésica también se ha relacionado con estancias hospitalarias más prolongadas10. En este sentido, nuestro análisis puso de manifiesto un discreto incremento en la estancia total en el grupo de pacientes que tuvo como desenlace una infección; sin embargo, no resultó estadísticamente significativo (p>0,05).
En el presente estudio el microorganismo causal más frecuente fue Pseudomonas aeruginosa, aspecto que difiere de lo descrito en el trabajo de Guren et al.21, en el cual los hallazgos microbiológicos más frecuentes fueron Staphylococcus aureus y la infección polimicrobiana. Asimismo, dichos autores informan que la presencia de infección polimicrobiana podría relacionarse con una tasa de fracaso superior y una mayor mortalidad al año de la cirugía.
Respecto a la función y a la calidad de vida del paciente tratado con una artroplastia por una fractura del cuello femoral, se observó que los pacientes que tuvieron como desenlace una infección periprotésica presentaban resultados funcionales y de calidad de vida inferiores. Dichos hallazgos coinciden con lo expuesto por Wildeman et al.22.
Entre las limitaciones del presente trabajo se encuentran las propias del estudio de casos y controles: tiene un carácter retrospectivo, no permite estimar incidencias y puede presentar sesgos, que en nuestro estudio trataron de minimizarse mediante una definición precisa de los casos (sesgo de selección) y con una extracción de datos semejante y estandarizada en ambos grupos (sesgo de información). Otra limitación es que hasta 177 procedimientos (37,2%) fueron realizados por residentes, pues nuestro centro es un hospital universitario.
ConclusionesLa infección periprotésica en el paciente con fractura del cuello femoral tratado con una artroplastia podría relacionarse con la presencia de determinadas variables en el momento del ingreso hospitalario, entre las que se encuentran la anemia moderada o severa, la trombocitopenia, el antecedente de evento tromboembólico, el trastorno ansioso-depresivo en tratamiento con 2 o 3 fármacos o la hepatopatía.
Nivel de evidenciaNivel de evidencia 2.
FinanciaciónLa presente investigación no ha recibido ayudas específicas provenientes de agencias del sector público, sector comercial o entidades sin ánimo de lucro.
Contribuciones de los autoresTodas las personas firmantes han contribuido en el diseño del trabajo, en la recogida y el análisis de los datos, en la interpretación de los resultados, así como en la redacción y la revisión del manuscrito definitivo.
Declaración de transparenciaEl autor para la correspondencia, en nombre del resto de las personas firmantes, garantiza la precisión, transparencia y honestidad de los datos y la información contenida en el estudio; que ninguna información relevante ha sido omitida; y que todas las discrepancias entre autores/autoras han sido adecuadamente resueltas y descritas.
Conflicto de interesesNo existen conflictos de intereses relacionados directa o indirectamente con el contenido del estudio.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
Aprobación del comité de éticaAprobado por el Comité de Ética Asistencial de Málaga.