La atención médica a los pacientes politraumatizados en nuestro país, en ausencia de centros especializados, recae en los hospitales de referencia de las principales ciudades. En muchos casos el enfoque y tratamiento de cada una de las lesiones que presenta el paciente se realiza de manera individual, y sin una correcta organización y coordinación de las diferentes especialidades. En este contexto no es infrecuente que las lesiones ortopédicas queden relegadas al último escalón de tratamiento, lo que en muchas ocasiones conlleva el ingreso con métodos de estabilización que no permiten la movilización adecuada del paciente, como tracciones transesqueléticas, durante días o semanas, implicando una morbilidad que, ante la evidencia disponible, podría ser evitada.
La evolución clínica después de sufrir un traumatismo múltiple está influenciada, fundamentalmente, por factores clínicos y de tratamiento, siendo los primeros la magnitud y extensión inicial de las lesiones que abocan a una importante respuesta inflamatoria sistémica, y a la gravedad del traumatismo torácico1. En este contexto la estabilización primaria de las fracturas de los huesos largos se hace determinante para asegurar un cuidado respiratorio adecuado e intensivo, limitar la respuesta inflamatoria sistémica y disminuir la incidencia e intensidad de las complicaciones que presentan estos pacientes.
IMPORTANCIA DEL PROBLEMA EN NUESTRO MEDIO
La Organización Mundial de la Salud ha calificado el politraumatismo como «la enfermedad del próximo milenio»2. Es conocido por todos que los accidentes de tráfico son la cuarta causa general de muerte en Occidente, y la primera en personas menores de 40 años. Constituyen, además, la primera causa de invalidez y de tetraplejias en jóvenes2.
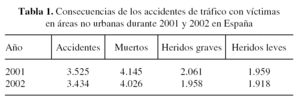
En España los datos que nos aporta la Dirección General de Tráfico3, en cuanto a morbimortalidad causada por los accidentes en carretera, ponen de manifiesto la gravedad del problema en nuestra sociedad. En la tabla 1 se describen las consecuencias de los accidentes de tráfico con víctimas ocurridos en las áreas no urbanas de nuestro país durante los años 2001 y 2002. Es importante resaltar que los datos que se refieren al número de fallecidos se han obtenido tras un seguimiento únicamente de las primeras 24 horas después el accidente, por lo que no se tienen en cuenta las muertes que ocurren pasado ese tiempo, y que precisamente son las teóricamente evitables con la actuación médica pertinente.
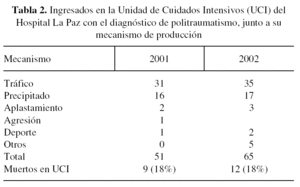
En la comunidad de Madrid los muertos en accidente de tráfico en regiones extraurbanas fueron, en el año 2001, 240 y en 2002, 216 muertos3. La tabla 2 muestra el número de pacientes ingresados en la Unidad de Cuidados Intensivos (UCI) del Hospital Universitario La Paz, con el diagnóstico de politraumatismo, y que al menos presentó alguna de las siguientes lesiones: traumatismo de extremidades superiores, inferiores, pelvis o raquis. Además, se refleja su mecanismo de producción y la mortalidad durante su ingreso en la Unidad.
DEFINICION, CARACTERISTICAS Y COMPLICACIONES DEL PACIENTE POLITRAUMATIZADO
Un paciente politraumatizado es aquel que presenta dos o más lesiones traumáticas graves, periféricas o viscerales, que repercuten negativamente sobre una o varias de sus funciones, amenazando su supervivencia4. Suele tratarse de un individuo previamente sano de cualquier edad, aunque más frecuentemente joven, que sufre una agresión traumática externa habitualmente de alta energía. Ésta puede provocar una serie de lesiones de localización diversa, tanto viscerales (intracraneales, torácicas o abdominales) como esqueléticas (raquis, pelvis, miembros superiores o inferiores), que lo convierten en un paciente extremadamente frágil, con alto riesgo de complicaciones y con peligro de perder la vida.
La mortalidad de estos pacientes se distribuye en el tiempo de la siguiente manera4: el 50% fallece en la primera media hora a consecuencia de lesiones orgánicas incompatibles con la vida; el 30% muere en las primeras cuatro horas, principalmente por la pérdida masiva de sangre y/o complicaciones respiratorias; el 20% restante fallece días o semanas después del traumatismo a consecuencia de fracaso multiorgánico, condicionado principalmente por complicaciones inflamatorias e infecciosas. En la tabla 3 se resumen las principales complicaciones que pueden derivarse de las lesiones ortopédicas4,5.
Ante la presencia de shock en estos pacientes, asumiremos que es hipovolémico, salvo que se demuestre lo contrario. La mayoría ingresa con cierto grado de hipotermia (menos de 35 ºC); con menos de 30 ºC se producen alteraciones del ritmo cardiaco que originan la muerte. Los 32 ºC se asocian con una mortalidad del 100%; por debajo de los 34 ºC se produce acidosis, aumento de la viscosidad sanguínea, disminución del metabolismo de los fármacos y alteraciones de la coagulación por disfunción de los factores y secuestro plaquetario. Por ello se hace prioritario controlar la temperatura de estos pacientes.
El síndrome de respuesta inflamatoria sistémica se caracteriza por dos o más de las siguientes circunstancias: más de 90 pulsaciones por minuto y de 20 respiraciones minuto, temperatura superior a 38º o inferior 36º, y más de 12.000 leucocitos, menos de 4.000, o más de 10% de formas inmaduras. El fracaso multiorgánico es el fallo consecutivo de dos o más órganos debido a la respuesta inflamatoria sistémica que provoca fenómenos de hipermetabolismo y daño endotelial difuso. La coagulopatía aguda traumática, al contrario de lo que se creía, no tiene relación con la cantidad de líquidos infundidos. Se ha visto que su incidencia es proporcional a la intensidad del traumatismo inicial, y que se correlaciona positivamente con la mortalidad6.
El síndrome de embolia grasa se caracteriza por la tríada clásica de insuficiencia respiratoria, alteraciones neurológicas del comportamiento y el nivel de conciencia, y un rash macular de predominio en tórax, axilas, cuello y conjuntivas. En la placa de tórax veremos el típico patrón en tormenta de nieve. El síndrome de distrés respiratorio agudo (SDRA) es una insuficiencia respiratoria de rápida instauración por lesión inflamatoria de la membrana alveolo-capilar, cuya definición gasométrica es una PO2 menor de 55 mmHg con una FiO2 mayor del 50%. La placa de tórax presenta infiltrado alveolo-intersticial difuso sin cardiomegalia.
Las complicaciones infecciosas tienen una importancia extraordinaria en los pacientes politraumatizados tanto por su elevada frecuencia como por su gravedad.
Por último, las complicaciones ortopédicas están condicionadas por la complejidad e intensidad de las lesiones y la dificultad de aplicar los tratamientos más adecuados en el momento que son necesarios debido a la presencia de lesiones viscerales y al mal estado general del paciente, que lleva a hacer prioritarias otras actuaciones terapéuticas.
Las complicaciones son las que condicionan el pronóstico de estos pacientes y las secuelas que van a padecer en caso de sobrevivir, por lo que se hace fundamental entender sus mecanismos fisiopatológicos de producción, con el fin de intentar evitarlos o paliarlos en la medida de lo posible.
FISIOPATOLOGIA DEL POLITRAUMATISMO
Los mecanismos fisiopatológicos básicos que acontecen tras un traumatismo importante han sido actualizados recientemente en diversas publicaciones6-10 que profundizan en los mecanismos de respuesta tisular al traumatismo, y permiten ir encontrando las bases que nos ayuden a comprender cómo y por qué se desencadenan las respuestas inflamatorias frente al traumatismo y se manifiestan los diferentes síndromes traumáticos y sus complicaciones.
Las consecuencias clínicas tras un traumatismo de alta energía vienen condicionadas, fundamentalmente, por la naturaleza e intensidad de las lesiones provocadas, pero también es cierto que dos individuos diferentes no responden igual a la misma lesión. Los trabajos de Schroedeor8 y su equipo ilustran que la genética influye en la respuesta, evidenciándose que los diferentes alelos de las proteínas de shock térmico HSP70 se correlacionan con los niveles de citocinas proinflamatorias circulantes (factor de necrosis tumoral [TNF], interleucina 6 [IL-6]), la incidencia de fallo hepático y la incidencia de complicaciones.
Cuando el paciente sobrevive a las consecuencias orgánicas viscerales directas del impacto y la pérdida de sangre (a veces agravada por la denominada coagulopatía aguda traumática6), que por sí solas son capaces de provocar su muerte, comienzan los procesos inflamatorio-reparativos, cuyo último objetivo es la curación de los daños infligidos. A consecuencia del traumatismo tisular pueden penetrar cuerpos extraños o microorganismos, y se liberan componentes intracelulares y de la matriz extracelular que provocan una respuesta inflamatoria local aguda (primeras 24-48 horas). Ésta corre a cargo de los leucocitos polimorfonucleares, que migran a los lugares de la lesión y liberan proteasas, radicales libres y micropartículas9. Estas sustancias son capaces de activar a las células macrofágicas y endoteliales locales, y preceden a la expresión de grandes cantidades de moléculas de adhesión y citocinas, predominantemente entre el segundo y quinto día, que provocan la quimiotaxis de células inflamatorias a los lugares de la lesión, con el fin de iniciar la respuesta inmune frente a los microorganismos que hayan penetrado y limpiar los detritus celulares. Esta respuesta inflamatoria, cuando se produce de manera masiva desde varias y extensas localizaciones, da lugar a la producción de cantidades significativas de citocinas proinflamatorias sistémicas (TNFα e IL-6, entre otras) al torrente sanguíneo, instaurándose a lo que podríamos denominar un estado inflamatorio sistémico, que se manifiesta bajo múltiples síndromes, tanto locales como generales, entre los que están el síndrome de distrés respiratorio agudo o el síndrome de respuesta inflamatoria sistémica. La activación general inflamatoria y las grandes demandas metabólicas, añadidas a los daños viscerales directos pueden abocar a la lesión vascular endotelial masiva y al fracaso orgánico progresivo, produciéndose el temido fallo multiorgánico y la muerte del paciente, en casos extremos.
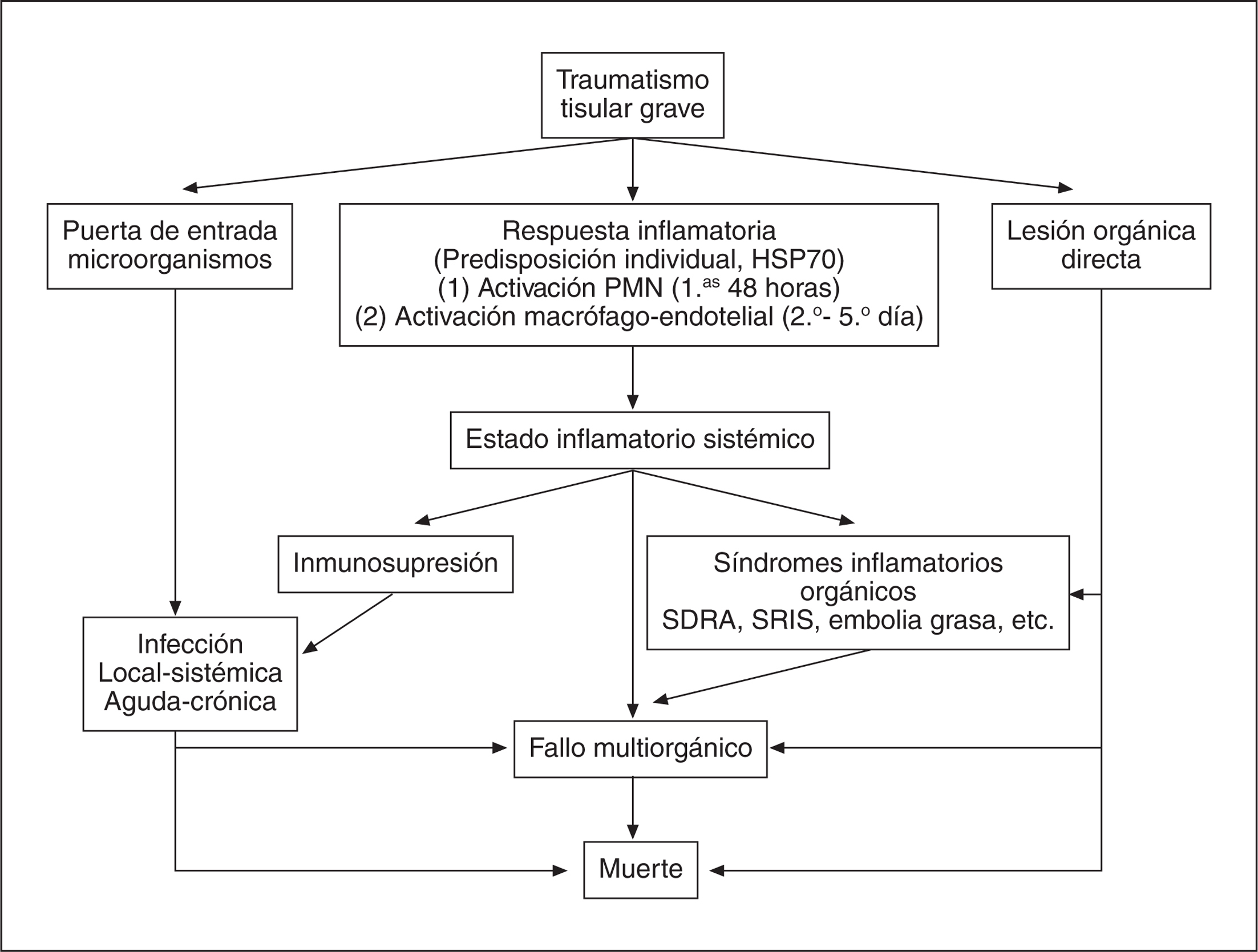
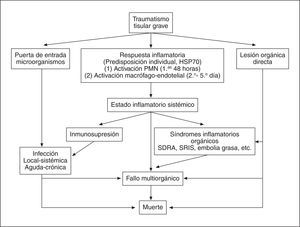
La infección en los pacientes politraumatizados es un problema frecuente y de importancia vital. Las lesiones traumáticas y los medios diagnóstico-terapéuticos invasivos se convierten en puertas de entrada de microorganismos que pueden desencadenar infecciones locales y sistémicas (infecciones de heridas, neumonías, sepsis). Esto es agravado por un estado de inmunosupresión7, que se produce en el individuo politraumatizado, caracterizado por una alteración de la inmunidad celular y humoral, con disminución de la actividad citotóxica de las celulas natual killer (NK) y disminución de la actividad presentadora de antígenos por parte de los macrófagos, de etiología no bien aclarada. La figura 1 muestra un resumen de los mecanismos expuestos.
Figura 1. Fisiopatología del politraumatismo. PMN: leucocitos polimorfonucleares; SDRA: síndrome de distrés respiratorio agudo; SRIS: síndrome de respuesta inflamatoria sistémica.
En este contexto las fracturas de huesos de gran tamaño, aparte de ser en sí mismas un mecanismo causal, tienen una influencia específica en la evolución de los procesos fisiopatológicos. Por un lado, perpetúan en el tiempo el traumatismo y el estímulo inflamatorio sistémico, facilitando además la infección, ya que la movilidad de los focos de fractura produce daño tisular progresivo e imposibilita la eliminación de detritus. Por otro lado, condicionan la inmovilidad del paciente en una cama, lo cual dificulta la ventilación y los cuidados respiratorios, aumentando el riesgo de trombosis venosa profunda, tromboembolismo pulmonar y complicaciones respiratorias. En estas circunstancias también se hacen más frecuentes los síndromes por decúbito, y se dificultan de manera importante los cuidados de enfermería. Por todo ello, la existencia de focos de fractura sin estabilizar supone una importante fuente adicional de morbilidad, que pueden llegar a condicionar la supervivencia del paciente.
PERSPECTIVA HISTORICA
Los pacientes con traumatismos múltiples importantes han sido tratados siguiendo criterios diversos. Hasta el siglo pasado, no era infrecuente ver que la actitud preferente ante las fracturas femorales era muchas veces la amputación del miembro, con el fin de evitar largos periodos de complicaciones y sufrimiento e incluso la muerte del paciente. El tratamiento de las fracturas femorales con la férula de Thomas a principios del siglo XX puso de manifiesto la importancia de la estabilización de las fracturas para la supervivencia y la viabilidad del miembro11, pero no fue hasta los años 50, con la introducción del tratamiento quirúrgico estandarizado de las fracturas, el momento que se puede considerar el punto de inflexión en el cuidado del paciente politraumatizado. Según se iban adquiriendo conocimientos en los años 70 sobre la fisiopatología de estas lesiones, se iba cambiando el concepto de «demasiado enfermo para operarle» por «demasiado enfermo para no operarle», surgiendo el tratamiento precoz definitivo (early total care) en los años 80, que abogaba por una fijación definitiva, en menos de 24 horas, de todas las fracturas que presentara el paciente, con el fin de disminuir la mortalidad y morbilidad. En los años 90 se evidenció una evolución desfavorable cuando se aplicaba este protocolo en algunos pacientes con lesiones torácicas graves o con una puntuación alta en el índice de gravedad de lesiones (injury severity score, [ISS]), siendo entonces cuando aparece el concepto de cirugía ortopédica de control de daños (damage control orthopedic surgery), que recomienda una estabilización inicial rápida provisional, mediante fijador externo, seguida de una osteosíntesis secundaria definitiva de las fracturas importantes, en aquellos pacientes con riesgo de padecer complicaciones sistémicas. En la actualidad las mayores controversias en cuanto a la forma de tratamiento de estas lesiones están en aquellos pacientes que presentan traumatismos craneales importantes, en los que la hipotensión e hipoxia que pueden acompañar a la cirugía definitiva de las fracturas de huesos largos pueden tener consecuencias en la progresión del proceso encefálico que presente.
VENTAJAS DEL TRATAMIENTO PRECOZ DE LAS FRACTURAS
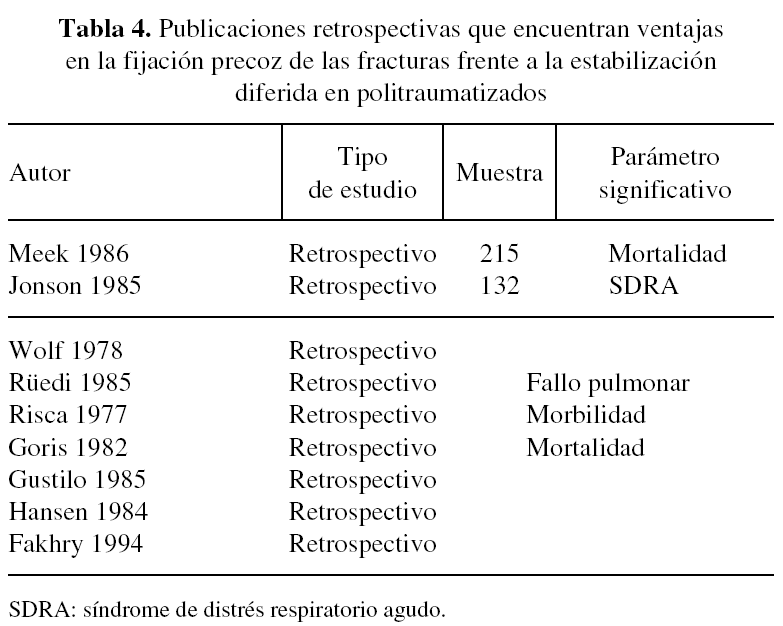
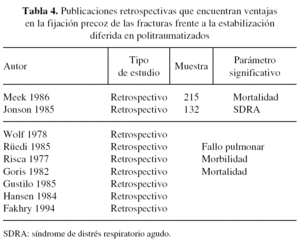
Como se ha señalado anteriormente, fue en la década de los 80 cuando empezó a ponerse en boga la fijación precoz de las fracturas de los pacientes con múltiples traumatismos. Durante estos años, en los Trauma Center de Estados Unidos, Canadá y algunos países europeos (Alemania entre los más destacados) se desarrollan protocolos de estabilización inmediata y se llevan a cabo estudios que pretenden averiguar si este tipo de actuación resulta beneficiosa o no. Son multitud los trabajos retrospectivos que demuestran que la fijación precoz de las fracturas ofrece mejores resultados que su tratamiento diferido, tanto en morbilidad como en mortalidad. En la tabla 4 se muestran algunos de los más importantes12-20.
Pero de todos los estudios publicados, merece la pena resaltar cuatro por las consecuencias que se derivan de sus resultados.
El primero es el publicado por Seibel R et al21, en 1985. En él se analiza la mayor incidencia de complicaciones que sufren las personas que no son intervenidas precozmente: cuando los pacientes permanecen 10 días con tracción transesquelética, doblan la duración del fallo pulmonar, multiplican por 10 los hemocultivos positivos, por 2 el uso de opiáceos y por 3,5 las complicaciones locales en la fractura. Cuando son 30 días, se multiplica el fallo pulmonar por 4, los hemocultivos positivos por 74, el uso de opiáceos por 2 y las complicaciones fractuarias por 17.
Bone LB22 en 1989, en un estudio prospectivo, concluye que cuando se retrasa la estabilización quirúrgica de las fracturas femorales, la incidencia de complicaciones pulmonares (síndrome de distrés respiratorio agudo, tromboembolismo pulmonar, síndrome de embolia grasa y neumonía) aumenta de manera significativa, pasando del 2,2% cuando se realizaba la cirugía en las primeras 24 horas, al 38% cuando se retrasaba más de 48 horas. En el grupo estabilizado después de los 2 días se objetivaba un aumento de los días de ingreso en UCI, de la estancia media en el hospital y de los costes.
También Bone LB23 publica en 1994 un estudio que analiza la mortalidad, mostrando los resultados de una revisión multicéntrica con dos grupos de pacientes: 676 incluidos en el protocolo de early total care, frente a 906 no incluidos. Se concluye que hay una reducción significativa de la mortalidad, mayor del 50%, en los menores de 50 años (del 11,8% al 5,1% cuando presentan un ISS entre 18 y 34, y del 25,8% al 11,5% cuando el ISS es de 35 a 45). En pacientes de edad más avanzada, las disminuciones eran similares, aunque con una mortalidad mayor en todos los grupos.
En el año 2001 Dunham publica un metaanálisis24, en el que se hace una crítica y exhaustiva revisión de los originales publicados entre los años 1980 y 1998, intentando reunir toda la evidencia disponible hasta la fecha acerca del momento óptimo de fijación de las fracturas de huesos largos, y conciliar los diferentes resultados obtenidos por los autores. De un total de 1.813 artículos se seleccionaron aquellos que cumplían los siguientes criterios de inclusión: mecanismo de producción de alta energía, que los individuos de los estudios presentaran fracturas de «huesos largos», que además padecieran alguna lesión importante traumática no ósea, y que se incluyeran dos grupos: fijación precoz y tardía. Se aplica un segundo filtro con unos estrictos criterios de selección tanto positivos como negativos, excluyéndose una parte importante de las publicaciones. Los artículos se agruparon según las lesiones que presentaran en su muestra, clasificándose en: pacientes con lesión torácica, pacientes con lesión cerebral, y un grupo mixto que engloba estudios en los cuales los individuos no habían sido segregados según la localización de las lesiones que tenían. En función de la calidad de la evidencia científica que ofrecen, los resultados fueron incluidos en dos niveles distintos de recomendación.
El resumen de las conclusiones es el siguiente:
1) En el grupo mixto de pacientes no se observa una mejoría en los resultados de supervivencia entre los estabilizados en las primeras 48 horas y los estabilizados después. No obstante, tras la estabilización precoz queda demostrada una menor morbilidad (días de ventilación mecánica y UCI, estancia hospitalaria, incidencia de SDRA, complicaciones pulmonares, neumonía e infección sistémica). No hay ningún dato a favor de que la estabilización temprana produzca una peor evolución. Es preferible realizar una estabilización precoz de las fracturas de huesos largos en pacientes politraumatizados.
2) En los pacientes con lesión cerebral, no hay evidencia de que la fijación precoz de las fracturas de huesos largos mejore o empeore el pronóstico en pacientes con lesiones cerebrales leves, moderadas o graves. Deberá individualizarse el tratamiento, teniendo en cuenta las siguientes consideraciones: gravedad del traumatismo craneoencefálico (escala de Glasgow), estado hemodinámica, gravedad de la disfunción pulmonar (PaO2/FiO2, distensibilidad pulmonar, y necesidad de presión positiva al final de la espiración), tiempo estimado de la intervención quirúrgica, pérdida de sangre estimada y presencia de fracturas abiertas o cerradas.
3) En los pacientes con lesión torácica, tampoco hay evidencia suficiente para demostrar que la estabilización quirúrgica temprana produzca una mejor o peor evolución. El momento de la estabilización de las fracturas también debe ser individualizado, según los criterios expuestos en el grupo anterior.
Las pocas pautas que el trabajo anterior es capaz de ofrecer ponen de manifiesto la escasa calidad de la evidencia científica que hasta ahora se ha podido conseguir, pues sus recomendaciones quedan lejos de lo que se puede inferir de la lectura aislada de los artículos en los que se basa. Esto probablemente sea así por la gran dificultad que supone realizar ensayos clínicos prospectivos aleatorizados en este tipo de pacientes, lo cual se corrobora al observar que no hay ninguna publicación con nivel uno de recomendación de evidencia terapéutica. La mayoría de los trabajos son retrospectivos. Algunos tienen grupos controles históricos o tratados en otras instituciones. Otros no especifican el tiempo que consideran «precoz» para la estabilización, o los medios empleados para realizarla. Es por ello que muchos de los estudios que ofrecían unos resultados más abultados, por ejemplo en cuanto a mortalidad8, fueron excluidos. El hecho de que el punto de corte para considerar «precoz» la cirugía sea de 48 horas, también puede haber tenido algo que ver en que no se hayan encontrado diferencias en cuanto a mortalidad, porque, como se verá más adelante, cuando se realizan intervenciones de estabilización definitiva entre los dos y los cinco días, la evolución de los pacientes puede ser peor de lo esperado.
DEL TRATAMIENTO PRECOZ TOTAL A LA CIRUGIA DE CONTROL DE DAÑOS
Tras el comprensible entusiasmo inicial que llevó a la introducción de todos los pacientes politraumatizados en los protocolos basados en el early total care, en los años 90 los responsables de los equipos de trauma de urgencias de los centros especializados1,25,26, principalmente los del área germano-parlante, observaron que hay un subgrupo de pacientes, precisamente los de mayor gravedad por presentar traumatismos viscerales, torácicos y craneales, y un ISS elevado, en los que tras la agresión que supone la estabilización quirúrgica por fijación interna, la evolución y los resultados eran desfavorables25,27-29. A partir de entonces los esfuerzos se dirigieron a intentar discriminar en qué pacientes se podía mantener el protocolo de fijación precoz definitiva, y en cuáles era mejor optar por una estabilización provisional, para, en un segundo tiempo, proceder al tratamiento definitivo de las fracturas cuando la situación del paciente lo permitiera: había nacido la cirugía ortopédica de control de daños.
Bajo este contexto encontramos los trabajos de Bone LB30 y de Carlson DW31, publicados en 1998, en los cuales se señala que la incidencia de SDRA y de fallo pulmonar en pacientes que sufren una contusión pulmonar y se fijan las fracturas precozmente es menor del 3%, que es independiente del método de fijación empleado, destacando incluso que el uso de clavos intramedulares fresados no incrementa la morbilidad pulmonar, y que esta incidencia es debida a la propia contusión pulmonar.
Brundage SI32 publica un estudio retrospectivo que incluye 1.362 pacientes, donde se obtienen interesantes resultados; el SDRA y la neumonía tienen menor incidencia en los individuos tratados en las primeras 24 horas, siendo en ellos también menor la estancia en UCI y la estancia media hospitalaria. Sin embargo, los pacientes con traumatismo torácico fijados entre los 2 y 5 días presentaban un incremento de la incidencia de SDRA, neumonía y embolismo graso (p < 0,0001). En cuanto al traumatismo craneoencefálico, se observó también que la estabilización en menos de 24 horas no empeoraba el pronóstico de la lesión craneal. Como conclusión apunta que la fijación de las fracturas femorales en menos de 24 horas mejora la evolución de los pacientes, incluso en aquellos con lesiones coexistentes torácicas o encefálicas; que entre los 2 y 5 días incrementa las complicaciones pulmonares, especialmente en presencia de traumatismo torácico o craneal, y que los pacientes que presentan estas lesiones no tienen contraindicación específica para la fijación intramedular de las fracturas de fémur
En el mismo sentido, Pape H33 señaló en 1999, tras realizar un estudio que incluía 4.314 pacientes, que las operaciones de duración mayor a 3 horas deben ser evitadas en los pacientes con lesiones traumáticas graves entre los días 2 y 4, puesto que se vio que bajo estas circunstancias los pacientes sufrían con mayor frecuencia fallos orgánicos graves. El mismo autor en el año 200310 publica un estudio que analiza el impacto de las actuaciones quirúrgicas de estabilización de fracturas sobre las citocinas proinflamatorias, encontrando que los niveles de citocinas en sangre, incluyendo la IL-6, aumentan de manera significativa tras la fijación intramedular precoz (primeras 24 horas), pero no si esta estabilización se realiza con métodos de fijación externa. Además, tampoco se objetiva un incremento de la respuesta inflamatoria tras la conversión de fijación externa a interna.
En cuanto a la lesión encefálica, Giannouidis PV et al34 y Bhandari et al35, señalan que el principal predictor de mortalidad en estos pacientes es la escala de Glasgow, reconocen que la literatura y las investigaciones realizadas hasta la fecha no aclaran todavía cuál es el mejor momento para estabilizar quirúrgicamente estas fracturas, pero que la mejor opción es considerar que estos pacientes se van a recuperar totalmente de sus lesiones encefálicas y que se cree, según los estudios que van apareciendo, que los mejores resultados se obtienen cuando se procede a una fijación temprana de las fracturas femorales.
A la hora de evaluar los resultados de los protocolos en los que se contempla la cirugía ortopédica de control de daños, debemos referirnos a un estudio retrospectivo de cohortes realizado en la escuela médica de Hannover36, en el que se evaluaron los medios empleados y el curso clínico de los pacientes con fractura de fémur atendidos en el Trauma Center de nivel 1 de dicha región, durante un periodo de 20 años, tiempo durante el cual se pasó de la filosofía del early total care, al damage control orthopedic surgery. Los individuos se clasificaron en diferentes grupos, según al periodo que pertenecieran (early total care, periodo intermedio o damage control orthopedic surgery) y según el tipo de fijación que se había practicado (enclavado intramedular, osteosíntesis con placa o fijador externo). Los resultados muestran que se reducía el número de complicaciones generales, dependiendo del tratamiento al que habían sido sometidas las fracturas de fémur, disminuyendo significativamente la incidencia de fallo multiorgánico en aquellos pacientes que seguían los protocolos «más modernos» en cuanto al tratamiento de dicha fractura, independientemente de otras posibles mejoras introducidas. Se observó también que la incidencia de SDRA era mayor en pacientes que habían sido tratados con fijación intramedular (15%), que en aquellos tratados con fijación externa (9,1%). Por otro lado, no se vieron diferencias estadísticamente significativas en cuanto a la incidencia de complicaciones locales según el método de fijación empleado. Con la evolución de los periodos, la osteosíntesis con placa pasó de ser el 23% de todos los tratamientos al 7%. El uso de la fijación externa, sin embargo, aumentó del 16% al 35%, y además se optaba por este tipo de estabilización precoz más a menudo cuando se trataba de pacientes con ISS elevado o cuando existían lesiones torácicas o abdominales. La osteosíntesis con clavo intramedular fresado también disminuyó a favor de un tratamiento con clavos no fresados. Aparte de la introducción de los protocolos de la cirugía de control de daños para los pacientes más afectados, otras variables que se identificaron como corresponsables de la mejor evolución de los politraumatizados fueron: el rescate aéreo, pasar del enclavamiento fresado al no fresado y el mejor manejo de los traumatismos torácicos o abdominales.
PROTOCOLOS DE FIJACION DE FRACTURAS DE HUESOS LARGOS EN PACIENTES POLITRAUMATIZADOS
La valoración retrospectiva de los artículos hace aflorar una cuestión fundamental: discriminar más escrupulosamente los grupos de pacientes a los cuales aplicar unos protocolos de estabilización quirúrgica concretos, según la gravedad y localización de las lesiones que presente. Además, también parece que existe un periodo para los pacientes más graves, con lesiones torácicas y neurológicas, en los cuales debe ser evitada la fijación quirúrgica32, 33, y que podría haber condicionado los resultados en estudios que no lo hayan tenido en cuenta. En este sentido, Nast-Kolb D1 señala que el enclavado intramedular supone un traumatismo importante por sí mismo, favoreciendo el shock hemorrágico, el embolismo pulmonar y el desarrollo de una mayor respuesta inflamatoria sistémica. Así su grupo de la Universidad de Munich propone un punto de corte que separará los pacientes en dos protocolos quirúrgicos de estabilización de fracturas: politraumatismos graves, definidos por un ISS mayor de 29 o traumatismos torácicos grave AIS (abbreviated injury scale) mayor de 3, que serán estabilizados en las primeras 24 horas mediante fijación externa provisional, y los politraumatizados con puntuaciones menores a éstas, que serán tratados mediante fijación precoz intramedular definitiva, recomendando los clavos no fresados frente a los fresados.
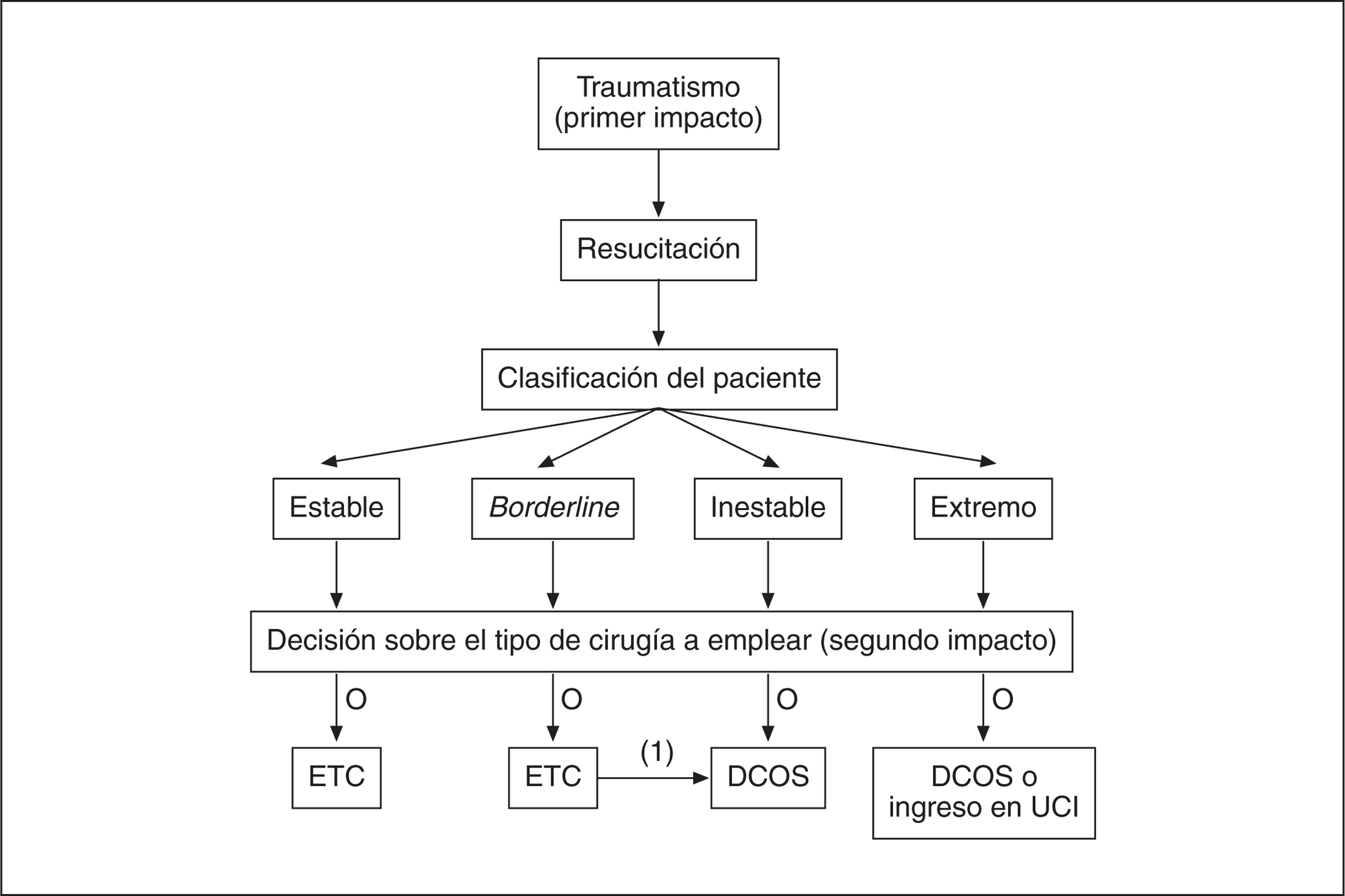
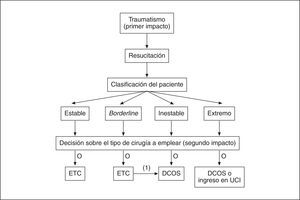
Pero a la hora de establecer unos protocolos, es la reciente revisión publicada por Giannoudis PV37 la que más luz arroja en cuanto a las definiciones, tiempos y modos de actuación adaptados a la situación de cada paciente. Empieza definiendo el concepto de cirugía ortopédica de control de daños: en un primer paso se procedería al control de la hemorragia, a la descompresión de las lesiones craneales cuando estuviera indicado y a la estabilización temporal temprana de las fracturas inestables. La segunda fase consistiría en la recuperación del paciente en la UCI, y la tercera el tratamiento diferido definitivo de las fracturas cuando el estado general del paciente lo permita. Clasifica a los enfermos en cuatro grupos principales: estables, límite o Borderline, inestables y extremos, y recomienda la actuación en función de esta clasificación, como indica la figura 2.
Figura 2. Clasificación y algoritmo terapéutico para pacientes politraumatizados37. ETC: cuidado total precoz; DCOS: cirugía ortopédica de control de daños; (1): el cirujano debe poder cambiar en todo momento de actitud desde ETC a DCOS, si la situación así lo aconseja; UCI: unidad de cuidados intensivos.
El paciente estable para el que el protocolo de cuidado precoz definitivo (early total care) es seguro y ofrece beneficios demostrados en cuanto a morbimortalidad y recursos empleados, queda ahora definido por las características que se muestran en la tabla 5. El grupo límite queda definido por la presencia de alguna de las características de la tabla 6.
Las actuaciones a llevar a cabo en los pacientes inestables o extremos, se engloban dentro de los protocolos de cirugía ortopédica de control de daños, y deben consistir en actuaciones rápidas y eficaces dirigidas a salvar la vida del paciente, evitando protocolos, reglas fijas y tiempos de decisión que retrasen las actuaciones y pongan aún más en peligro su supervivencia.
La técnica de elección para conseguir la estabilización temporal de la pelvis o de un «hueso largo» es la fijación externa. La técnica de elección para la conversión a fijación definitiva de estas fracturas, en particular en la fractura de fémur, es el enclavado intramedular, que se llevará a cabo cuando la situación del paciente lo permita, con la intención de disminuir las consecuencias del «segundo impacto» que supone esta fijación. Recomienda, al igual que vimos en otros estudios, que la cirugía definitiva debe realizarse después de pasados cuatro días del traumatismo inicial. Los riesgos de infección después de la conversión de fijación externa femoral a enclavado intramedular oscilan entre el 1,7 y el 3%38,39, y son similares a los riesgos tras un enclavado primario del fémur. Sin embargo, en la tibia, la incidencia de infección podría ser considerablemente mayor (17-65%). Giannoudis concluye basándose en estos estudios que la conversión de fijación externa a enclavado intramedular puede llevarse a cabo de una manera segura y con bajo riesgo de infección, en las dos primeras semanas tras el traumatismo.
El resumen de los objetivos a cumplir por el cirujano ortopédico ante el politraumatizado con fracturas son: control de la hemorragia, evitar el desarrollo de una respuesta inflamatoria sistémica excesiva, eliminación del tejido necrótico, prevención de la lesión por isquemia-reperfusión, control del dolor y facilitación de los cuidados de enfermería. Todo ello puede lograrse mediante la estabilización de las fracturas y el desbridamiento y realización de fasciotomías, cuando esté indicado.
De todo lo expuesto anteriormente se pueden extraer una serie de conclusiones que merece la pena tener en cuenta:
1) Se hace patente la necesidad de ensayos de mayor calidad científica, que ofrezcan una evidencia de mayor peso que lo publicado hasta ahora, con estudios longitudinales prospectivos controlados y aleatorizados que apoyen los datos que parecen vislumbrarse con las publicaciones que tenemos hasta ahora. Es necesario realizar una correcta evaluación de los resultados terapéuticos, sobre todo de aquellos pacientes con lesiones craneales y torácicas, de la aplicación de los nuevos protocolos de cirugía de control de daños, que sean capaces de encontrar diferencias no sólo en cuanto a morbilidad y costes, sino en cuanto a mortalidad.
2) Debe potenciarse la investigación básica en este campo para conocer mejor los mecanismos íntimos de la respuesta inflamatoria sistémica, con el fin de buscar tratamientos coadyuvantes que mejoren la situación clínica del paciente y para comprender mejor los riesgos y beneficios de nuestra actuación terapéutica quirúrgica.
3) La utilización de métodos de tracción esquelética, mientras se espera a una optimización de la situación general del paciente, parecen aportar más complicaciones que beneficios a la luz de los artículos publicados hasta la fecha.
4) La fijación precoz de las fracturas de fémur, raquis, pelvis, tibia y húmero (en las primeras 24 horas) disminuyen las tasas de complicaciones y secuelas, los costes y la estancia hospitalaria, y podría disminuir también la mortalidad, en pacientes seleccionados.
5) Se hace necesaria una evaluación individual y completa de cada caso para poder aplicar el mejor tratamiento de las fracturas de huesos largos, para lo cual es necesaria una correcta clasificación de la gravedad de la totalidad de las lesiones (clasificaciones ISS, TRISS [Trauma Score/Injuri Severity Score], AIS) y una meditada red de protocolos quirúrgicos, en función del resultado de esta valoración, que incluya la fijación definitiva inmediata (menos de 24 horas) para los pacientes menos graves, y la estabilización provisional segura y rápidamente ejecutada (menos de 24 horas) para los pacientes más graves, y con sus tiempos más adecuados de conversión a fijación definitiva salvando el periodo «peligroso» señalado en la literatura (segundo-quinto día). A este respecto, la búsqueda ya iniciada de parámetros analíticos inflamatorios (i.e. IL-6) o de gravedad (coagulopatía aguda traumática), que se correlacionen con la situación clínica del paciente podrá arrojar más luz en cuanto a la mejor actuación individual.
6) Evidentemente, para la consecución de estos protocolos se hace indispensable la colaboración multidisciplinar específica y los medios apropiados para llevarlos a cabo, tanto desde el punto de vista material como humano.
AGRADECIMIENTOS
A la Unidad Docente de Cirugía Ortopédica y Traumatología del Hospital Universitario La Paz, por su esfuerzo en incentivar y facilitar la realización de revisiones y estudios científicos dentro del programa docente de médicos especialistas en formación, y fomentar la formación continuada de los médicos especialistas.
Al Dr. E.C. Rodríguez-Merchán, por su gran interés y participación en la consecución de actividades formativas complementarias dentro del estudio del politraumatismo.
A la Unidad de Cuidados Intensivos del Hospital Universitario La Paz, en especial al Dr. Yus, por colaborar en la facilitación de datos relacionados con los pacientes politraumatizados en nuestro Hospital, y su aliento en la progresión de nuestro interés sobre este tema.
Conflicto de intereses. Los autores no hemos recibido ayuda económica alguna para la realización de este trabajo. Tampoco hemos firmado ningún acuerdo por el que vayamos a recibir beneficios u honorarios por parte de alguna entidad comercial. Por otra parte, ninguna entidad comercial ha pagado ni pagará a fundaciones, instituciones educativas u otras organizaciones sin ánimo de lucro a las que estemos afiliados.