Al referirme a este tema, es mi propósito señalar brevemente las características clínicas e histológicas fundamentales del tumor óseo maligno que con mayor frecuencia vemos en la clínica.
En la presente comunicación recojo los datos del material disponible en nuestro Servicio del Hospital Provincial y de los casos estudiados en el departamento de Anatomía Patológica del Instituto de Investigaciones Médicas del Prof. Jiménez Díaz, que hacen un total de veintidós casos, cifra muy pequeña para hacer consideraciones estadísticas. Por lo tanto, nuestro material se utiliza únicamente para la ilustración de datos anatomoclínicos que se desprenden de una revisión de las publicaciones recientes, más importantes, sobre este tema.
Un tumor extraesquelético puede llegar a implantarse en el hueso por dos diversos mecanismos: 1.o Mediante la extensión del proceso neoplásico primitivo, que por asentar cerca del hueso lo invade por crecimiento infiltrativo. 2.o Porque las células cancerosas llegan a él por vía linfática o hemática.
La estirpe celular capaz de implantarse en el hueso puede ser conjuntiva o epitelial, y de estas dos nos parece de mayor interés y utilidad estudiar los tumores epiteliales, porque los sarcomas que asientan secundariamente en el hueso son más difíciles de sistematizar y muchas veces cabe la duda de si el sarcoma con localizaciones múltiples en uno o varios huesos, es en realidad una metástasis o un crecimiento plurifocal.
Frecuencia. -- Los tumores óseos secundarios a procesos cancerosos aparecen en la clínica con mucha frecuencia, siendo posible que no tengamos en cuenta el elevado porcentaje de cánceres que en un estado más o menos avanzado del proceso primitivo se implantan en el hueso, porque en las autopsias, generalmente, no se hace un estudio cuidadoso de las lesiones óseas.
Abrams y col.1, en mil autopsias realizadas en casos de cánceres generalizados, encontraron que había localizaciones óseas en el 27 por 100. En las necropsias de cáncer de mama las lesiones óseas aparecían en las dos terceras partes; en las autopsias por cáncer de pulmón, en una tercera parte; los cánceres renales originaban metástasis óseas en la cuarta parte de los casos; los pancreáticos, en el 3 por 100; los del recto, en el 13 por 100; los del estómago, en el 11 por 100; los del colon, en el 9 por 100; los del ovario, en el 9 por 100, y, por último, los cánceres prostáticos daban lugar a metástasis esqueléticas en más del 50 por 100 de los fallecidos por esta causa.
Localización. -- Las localizaciones metastáticas epiteliales más frecuentes son en aquellos huesos que conservan la médula ósea roja, cuya vascularización es más rica y en los que su actividad hematopoyética está conservada. Así comprobamos la mayor participación del ilíaco, los cuerpos vertebrales, las costillas y el esternón, siguiendo a éstos las regiones escápulo-humeral y femoral. Se ha considerado clásicamente que las localizaciones óseas de los carcinomas eran infrecuentes en los huesos por debajo de las rodillas y codos. Nosotros7, en un caso de epitelioma espino-celular desarrollado sobre una fístula osteomielítica de peroné izquierdo, vimos a los siete meses de la amputación una metástasis en un metatarsiano del pie contrario. También Sierra Cano12 ha descrito una localización tarsiana por cáncer uterino.
El cráneo es localización bastante frecuente de las diseminaciones neoplásicas, sobre todo del cáncer de tiroides y de mama. A veces las lesiones redondeadas, líticas y de tamaño variable, pueden ser el primer síntoma de un tumor del tiroides. En algunas ocasiones pueden ser estas lesiones circulares, radioopacas, múltiples, muy difíciles de diferenciar radiográficamente de la mielomatosis.
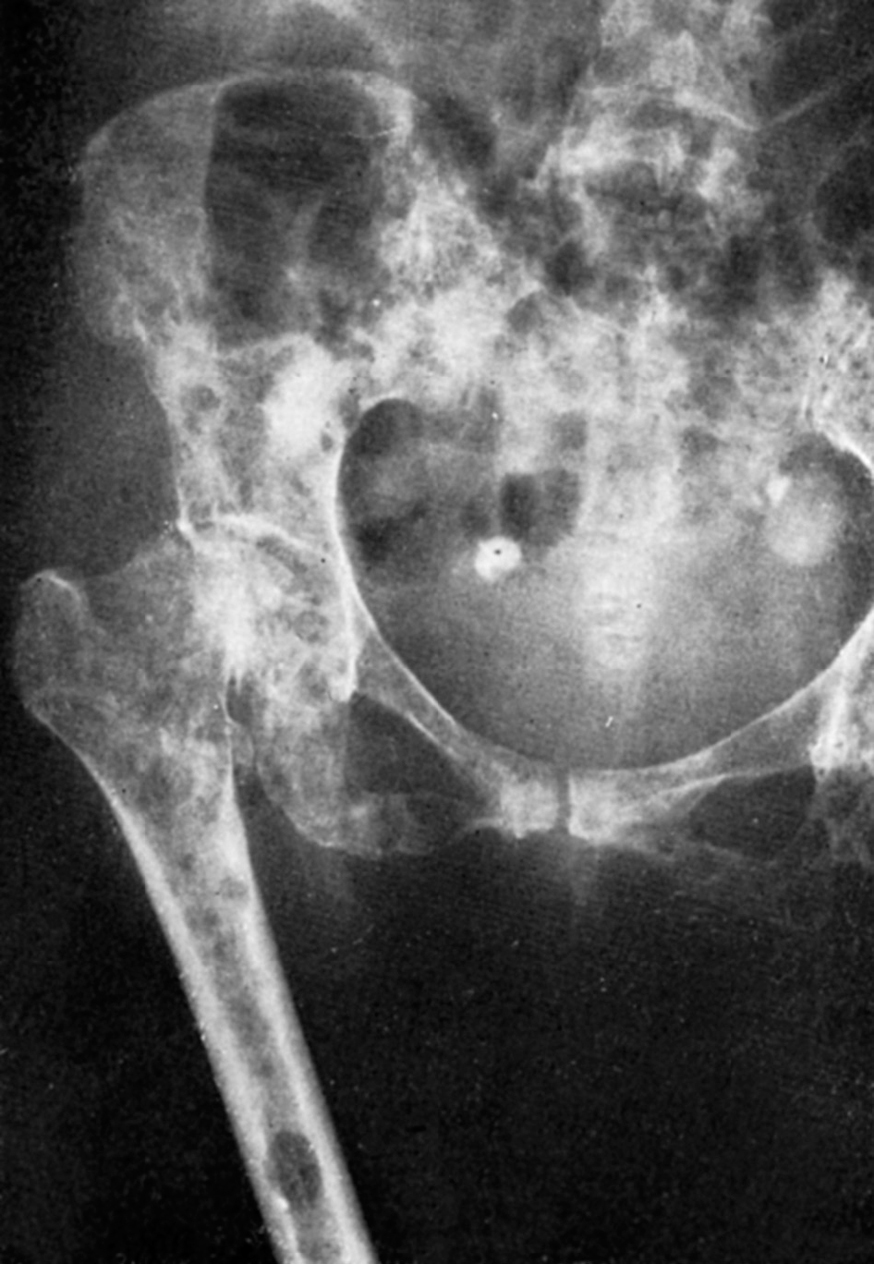
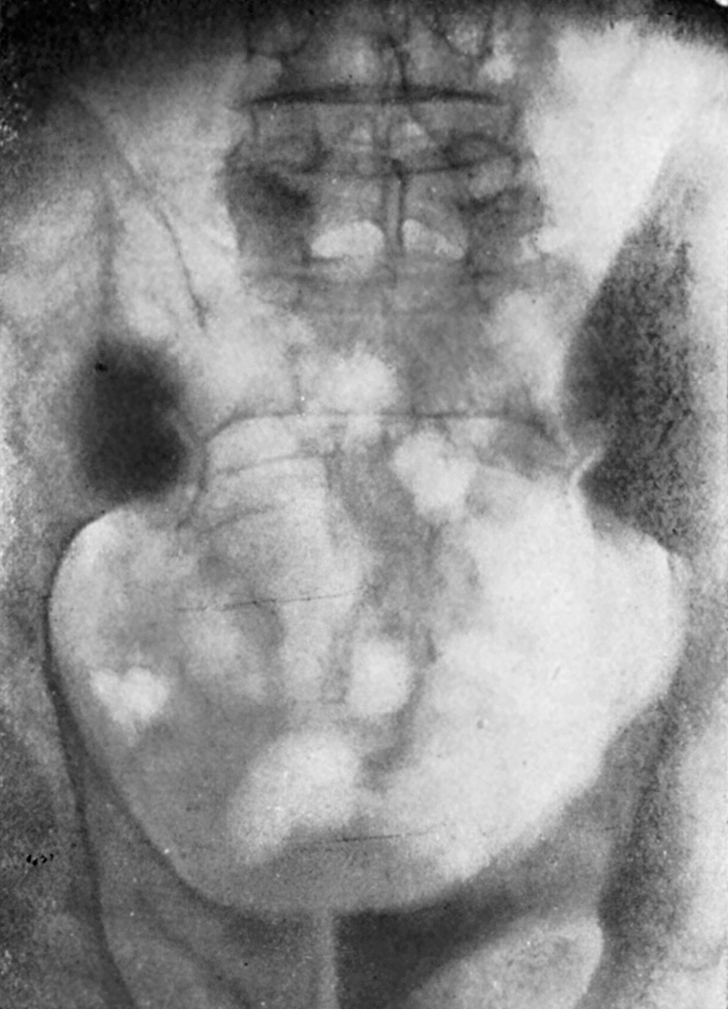
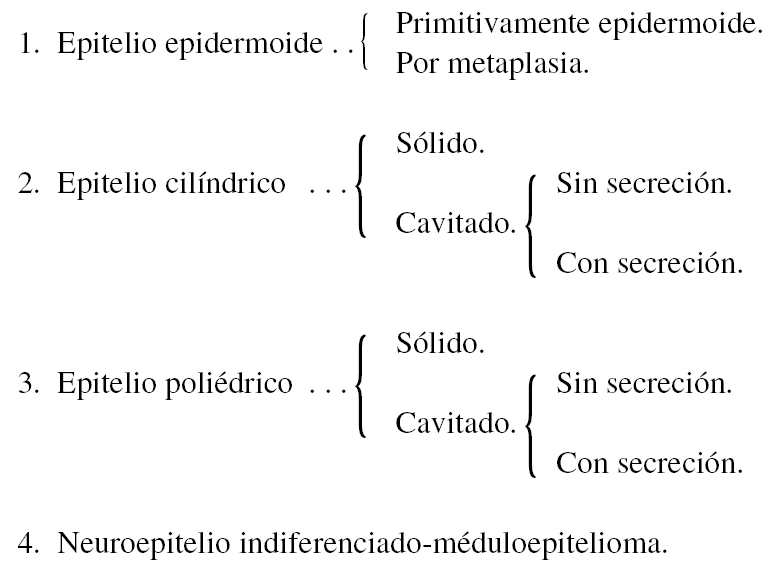
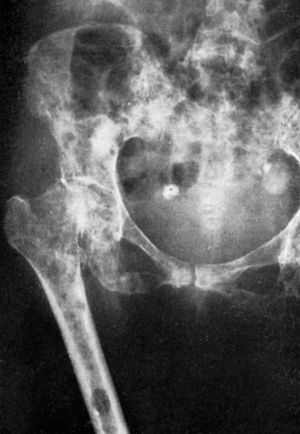
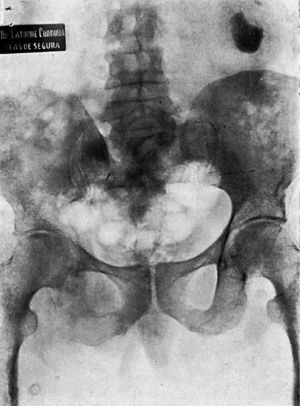
Radiográficamente las metástasis de estirpe epitelial pueden dar imágenes más o menos circulares de rarefacción (fig. 1.a), pero en algunos casos pueden ser radioopacas (fig. 2.a), y esta es una propiedad característica de las lesiones por el cáncer de próstata, que por su localización, generalmente en los cuerpos vertebrales lumbares y en el ilíaco, así como por el carácter condensante de las lesiones óseas, ofrece un cuadro radiológico bastante característico.
Figura 1. Mujer, cuarenta y siete años. Siete años antes operada de un tumor de mama. Carcinomatosis difusa, radiográficamente caracterizada por focos osteolíticos y osteocondensantes.
Figura 2. Carcinoma de próstata. Varón, de setenta y cinco años. Disuria dos años antes de los «dolores reumáticos». Metástasis osteocondensante.
Inicialmente, en algunos casos, antes de perfilarse netamente las lesiones osteolíticas, aparecen zonas de osteoporosis más o menos difusas, sobre todo cuando el sector afectado es la columna vertebral, en la que un número variable de cuerpos vertebrales puede mostrar imágenes de rarefacción uniforme. Cuadros inicialmente considerados como de osteomalacia senil o postmenopáusica, por presentar radiológicamente imágenes de porosis difusas se deben en un elevado número a localizaciones metastáticas, que únicamente en fases más avanzadas del proceso, aparecen como zonas líticas bien delimitadas. La opacificación de una lesión primitivamente osteolítica supone la regresión por calcificación o por reposición del foco por tejido óseo.
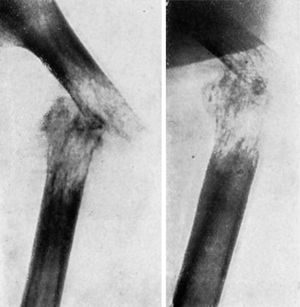
Con alguna frecuencia, el síntoma que primero puede llamar la atención en una metástasis cancerosa localizada en el hueso es una fractura patológica, caracterizada radiológicamente porque la línea de fractura corta una superficie muy decalcificada, en la mayoría de los casos de decalcificación moteada (fig. 3.a).
Figura 3. Mujer, cuarenta y siete años. Fractura patológica de fémur por metástasis de carcinoma de mama, operado nueve meses antes.
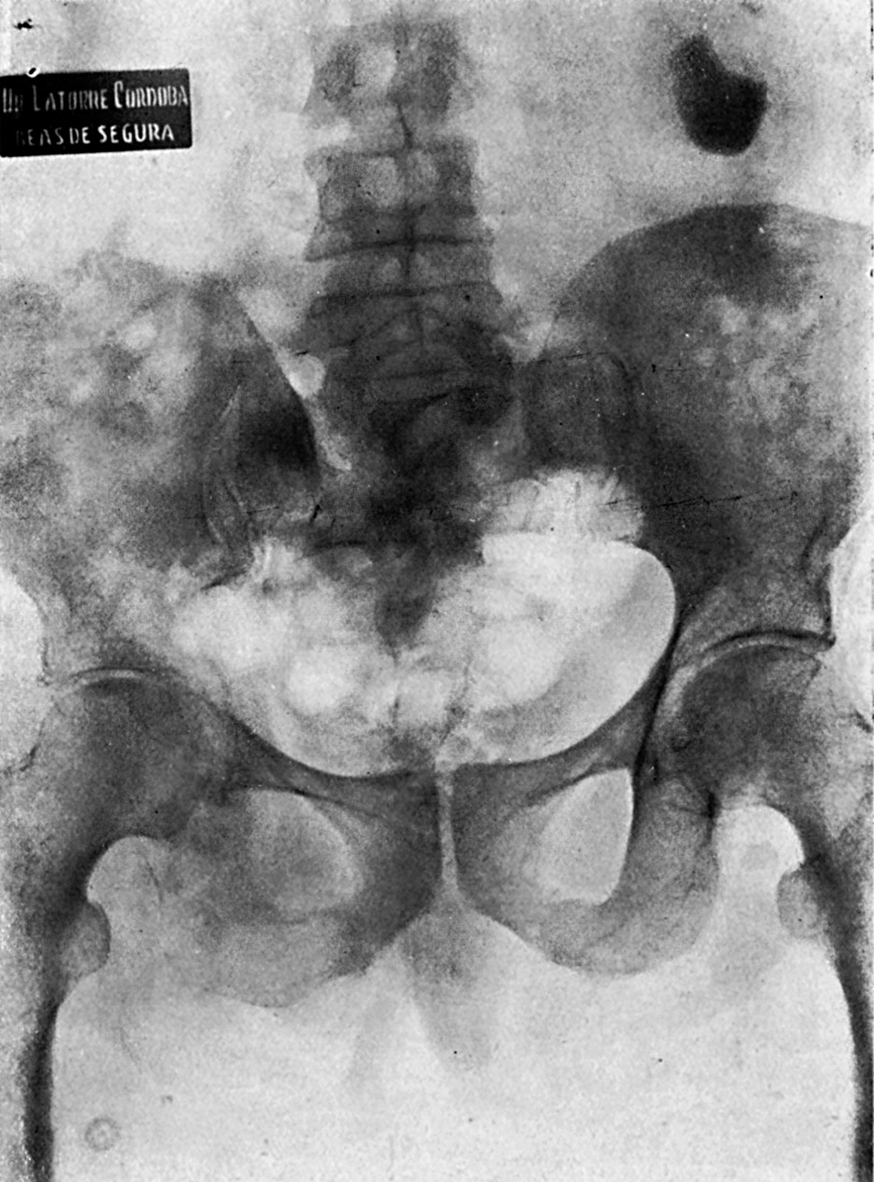
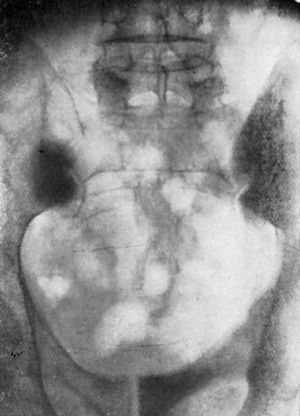
Figura 4. Enfermo, de cincuenta y seis años de edad. Aquejaba un proceso «inflamatorio» a nivel de la región isquiática derecha. Intervención y biopsia, extrayéndose una materia puriforme. A pesar del cuidadoso estudio clínico y radiológico no fue posible identificar el tumor primitivo.
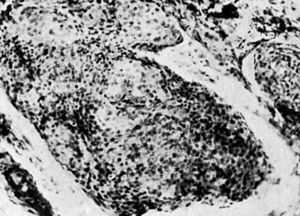
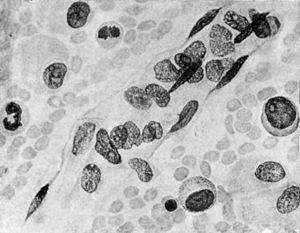
Figura 5. Microfotografía de una preparación correspondiente a la biopsia del caso de la figura 4.a. Se observa un cordón de epitelio epidermoide.
Histopatología. -- La identificación del tejido neoplásico epitelial, que constituye la metástasis ósea, no es en la gran mayoría de los casos difícil de lograr; únicamente en algunos casos de carcinoma muy indiferenciados, con mayor frecuencia de pulmón, cabe la posibilidad de confusión con un sarcoma de células redondas.
Sin embargo, la identificación del origen del tumor, o sea el órgano de que parte, es mucho más difícil de determinar, y en un gran número de casos, ni aun después de la necropsia es posible identificar el órgano de partida. De nuestro material, un caso que dió como síntoma inicial una localización en costilla, histológicamente un carcinoma epidermoide, no pudo ser comprobado su origen aun después de la autopsia.
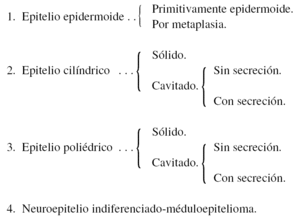
Nosotros utilizamos para la identificación y clasificación histológica de estos procesos un esquema que nos es útil para darnos una idea del órgano de partida.
Clasificación histológica de las metástasis epiteliales:
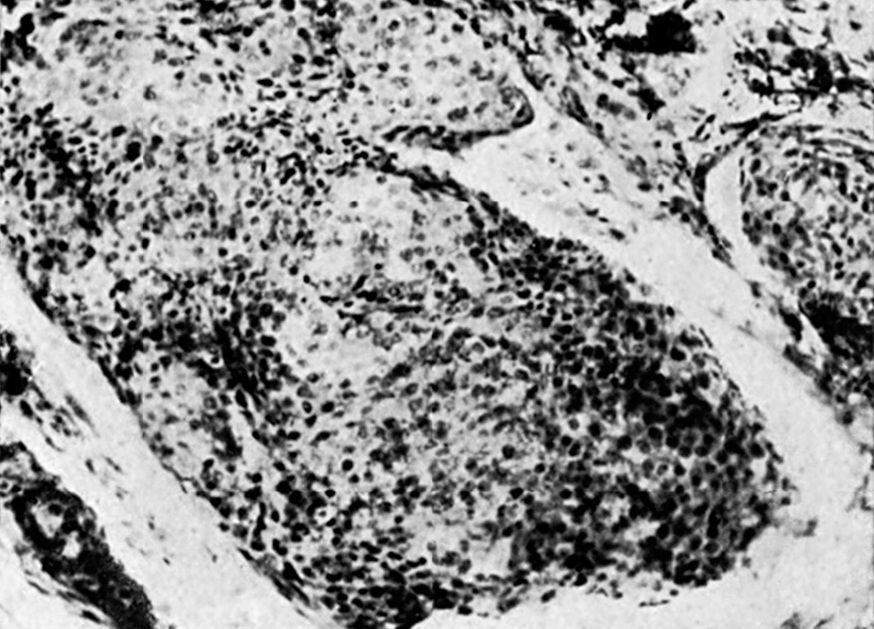
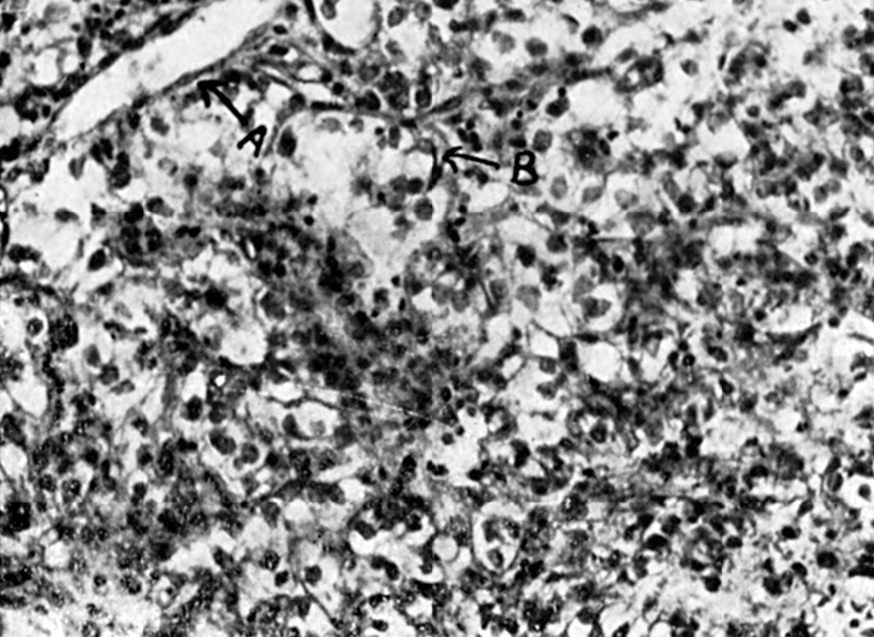
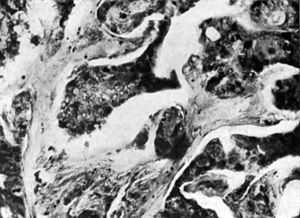
El epitelioma epidermoide (fig. 6.a) se caracteriza por la presencia de células con epiteliofibrillas, de aspecto más o menos globuloso, o por la presencia de globos córneos. El epitelio epidermoide se deriva de procesos neoplásicos cutáneos, o de regiones de transición, como sucede en la boca, ano y fosas nasales.
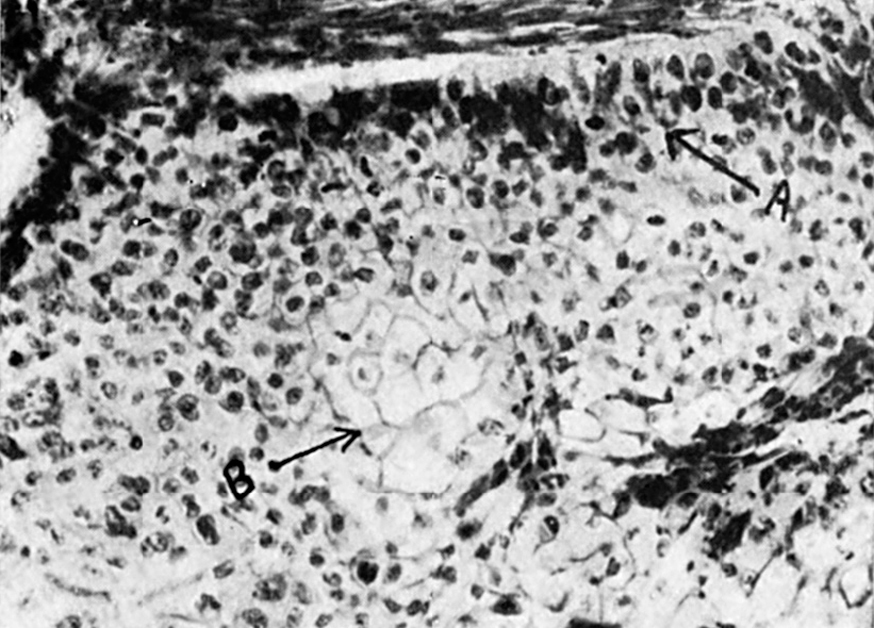
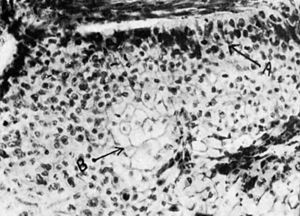
Figura 6. Detalle de un cordón neoplásico en el que se puede observar la transición o metaplasia de tejido cilíndrico (A) a epitelio epidermoide caracterizado por células globulosas conteniendo substancia queratínica (B).
Sin embargo, el epitelio de algunas estructuras constituidas por un tipo no epidermoide pueden mediante un proceso de metaplasia transformarse en epidermoide, y así ocurre con algunos cánceres de conductos biliares y nasofaringe.
El epitelio cilíndrico correspondería con mayor frecuencia a procesos neoplásicos del tracto digestivo, principalmente adenocarcinomas, conteniendo una secreción mucoide. Si consideramos al adamantinoma, como sugieren algunos autores, «carcinoma de restos de los gérmenes dentarios», entraría dentro de esta clasificación. La estructura cilíndrica de las células con el núcleo situado en la parte superior, es de aspecto sumamente típico.
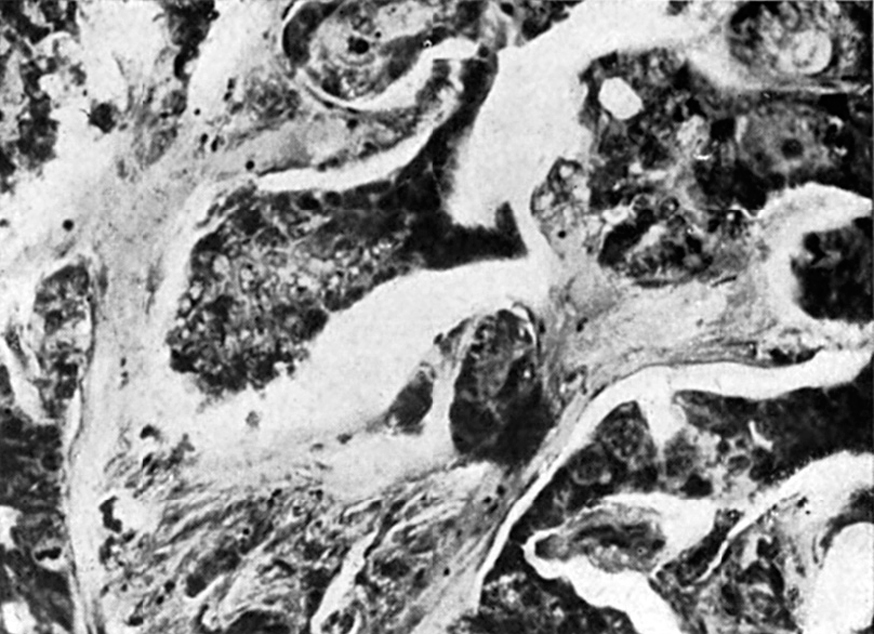
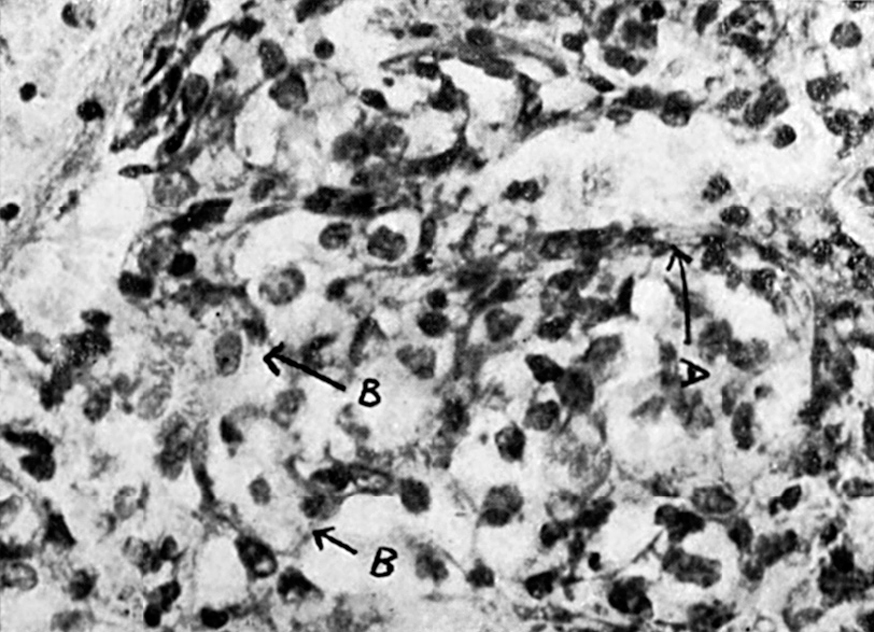
El epitelio poliédrico o cuboideo (fig. 7.a), cuando se encuentra en un foco de metástasis puede partir de numerosos órganos. En la mayoría de los casos procedería de cánceres mamarios, cuya estructura, generalmente, se caracteriza por cordones de células de este tipo dispuestas en cordones sólidos o con disposición adenomatosa. Histológicamente algunos cánceres constituidos por células cuboideas, tienen características que permiten su fácil identificación. El cáncer de tiroides, por ejemplo, tiene generalmente una estructura glandular típica y sus vesículas ocasionalmente contienen substancia coloide (fig. 8.a). El hipernefroma o tumor de Grawitz (figs. 9.a y 10), que consideramos invariablemente como tumor renal, originado en la porción secretora, tiene como estructura característica grandes células claras, generalmente dispuestas alrededor de vasos neoformados y que dan una reacción positiva a las tinciones para el glucógeno y las grasas, puesto que están repletas de estas substancias.
Figura 7. Cordón de tejido epitelial cuboideo sólido, procedente de un tumor de mama.
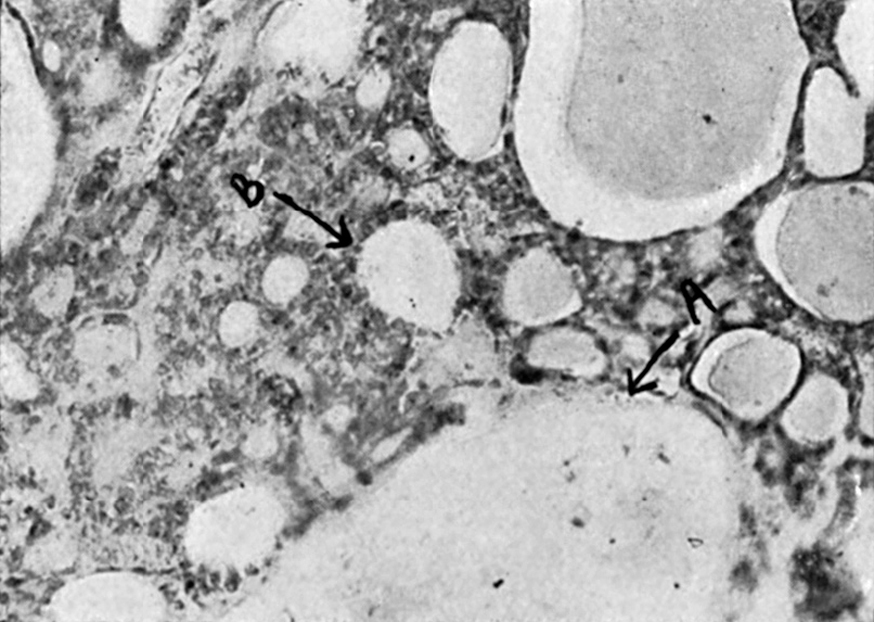
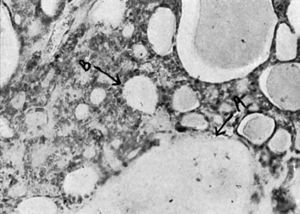
Figura 8. Metástasis de carcinoma de tiroides. La estructura típica de estos procesos, caracterizada por la agrupación alveolar de las células de epitelio plano, en cuyo seno se encuentra substancia coloidea. (A), trabécula ósea, y (B), alvéolo conteniendo substancia coloide.
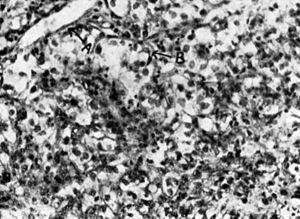
Figura 9. Estructura típica del hipernefroma, caracterizada por células grandes, claras, dispuestas en forma alvéolo-papilar y adosadas a la pared de vasos neoformados. (A), pequeño vaso con células del hipernefroma adosadas; (B), aspecto característico de las células.
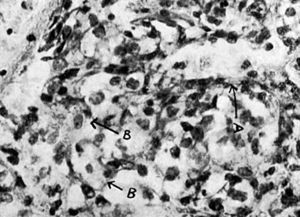
Figura 10. Microfotografía a mayor aumento en la que se ve: (A), estructura del vaso neoformado, y (B), células del hipernefroma.
En cuanto a los tumores nerviosos, que por su origen ectodérmico puede discutirse su inclusión dentro de una clasificación de los tumores epiteliales, por su diferenciación a partir de epitelio, creemos que solamente el méduloepitelioma, por su grado de indiferenciación, puede ser considerado dentro de este grupo, pero las metástasis a hueso de este tumor son muy raras.
El puntualizar con datos estadísticos las características histológicas, radiológicas y de localización de los distintos tipos de cánceres que se diseminan en el hueso no reportaría demasiada utilidad, porque al revisar la literatura y tratar de hacer una síntesis de ella podemos decir que por su cuadro clínico, morfología radiográfica y localización, los tumores cancerosos del hueso no tienen ninguna característica capaz de que su generalización nos haga valorar con más probabilidad de certeza los casos individuales. Incluso histológicamente muchas veces una metástasis de cáncer de estómago o pulmón, por su gran indiferenciación y parquedad de síntomas clínicos referentes a la neoplasia primitiva, pueden ser difíciles de filiar e incluso a menudo se incluyen equívocadamente dentro del cajón de sastre de los sarcomas de Ewing.
Este carácter inespecífico de la carcinomatosis ósea es importante y debemos tenerlo siempre presente. Un caso con lesiones óseas, sea cual fuera su localización, cuando se presenta en una persona después de los treinta años, debe despertarnos la sospecha de una metástasis ósea y únicamente descartaremos esta posibilidad tras una intencionada exploración clínica y valiéndonos de una serie de procedimientos o pruebas que nos ayudarán a determinar el diagnóstico. Ellos son:
1.o La biopsia: Esta puede realizarse a cielo abierto o por punción. Para Coley4 y Pique y Schajowicz9 el procedimiento preferible es la punción y aspiración. Nosotros personalmente preferimos, siempre que sea posible, la biopsia a cielo abierto, obteniendo una muestra amplia del tejido.
2.o La punción esternal: Muchas veces es útil el estudio citológico de la médula ósea esternal, cuando por algún motivo no pueda realizarse la biopsia del foco, así como si hay que establecer el diagnóstico diferencial con el mieloma múltiple.
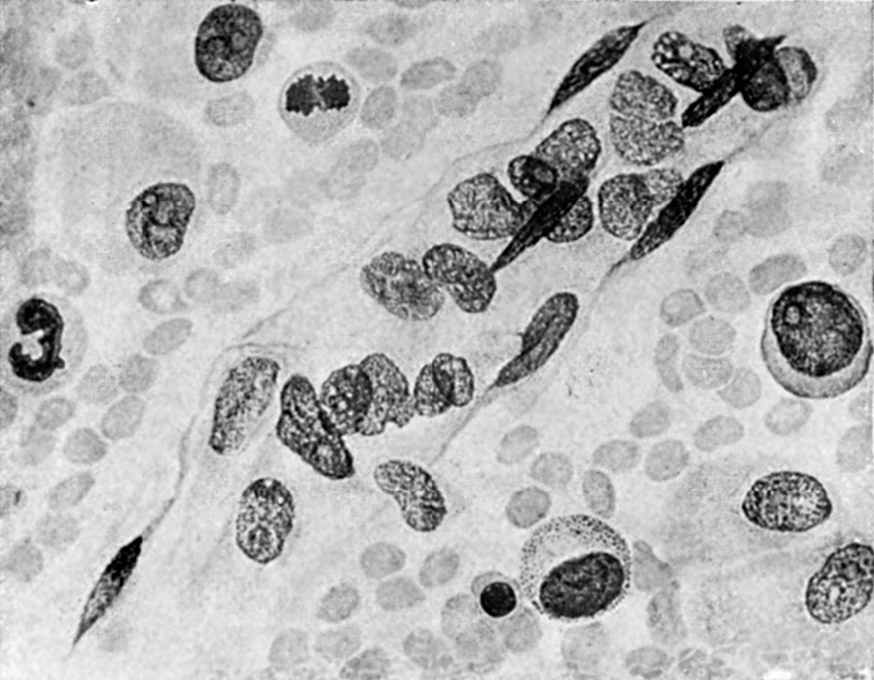
En numerosas ocasiones es posible encontrar células neoplásicas (figura 11) en la médula esternal, pero aun si esto no fuera posible, el estudio realizado por un citólogo podría identificar lo que Panigua8 considera como «síndrome de malignidad inducida», fundamentándose en las alteraciones morfológicas de la médula ósea en los casos de una generalización neoplásica.
Figura 11. Carcinosis ósea metastática de páncreas. Punción esternal: vaso capilar de la médula ósea que contiene un trombo de células neoplásicas de cromatina laxa con destacados nucléolos (dibujo de microfotografía; cortesía del Dr. Paniagua).
3.o Determinación de los valores de calcio y fósforo en sangre: La invasión del hueso por el tejido neoplásico provoca la movilización de sales cálcicas, lo que puede acusarse por el aumento en la sangre y la consecuente reducción proporcional de la cifra de fósforo.
4.o Determinación de la fosfatasa alcalina y ácida: Cuando se produce una neoformación compensadora o reactiva del tejido óseo alrededor de la metátasis o cuando se han producido fracturas en los huesos lesionados y existe un intento de formación de callo, las cifras de la fosfatasa alcalina pueden encontrarse elevadas. La fosfatasa alcalina se eleva considerablemente en un gran porcentaje de casos de cáncer de próstata, y esta determinación es también de gran valor para detectar una recidiva después de haber resecado la próstata.
Para diferenciar la fosfatasa ácida derivada de la próstata de aquella que procede de otros procesos (pancreáticos, insuficiencia hepática, etcétera), Bonner3 y colaboradores utilizan como reactivo el levotartrato. Prueba extremadamente útil y de fácil realización.
5.o Prueba del yodo radiactivo: En ciertos tipos de cánceres tiroideos, cuando existe substancia coloide con apetencia para el yodo, si inyectamos yodo radiactivo, éste puede acumularse en las zonas de metástasis, que se detectan entonces con un contador de Geiger.
Tratamiento. -- Las posibilidades terapéuticas de las metástasis cancerosas óseas dependen tanto de su multiplicidad y extensión cuanto de las características anatómicas y funcionales del órgano afectado primitivamente.
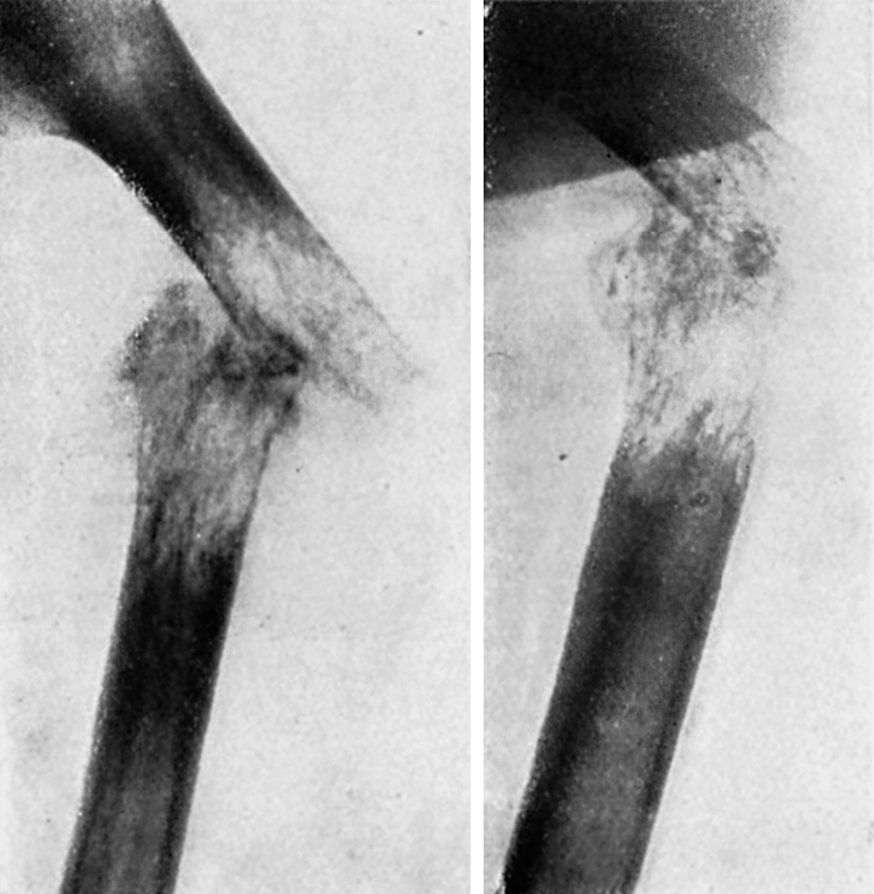
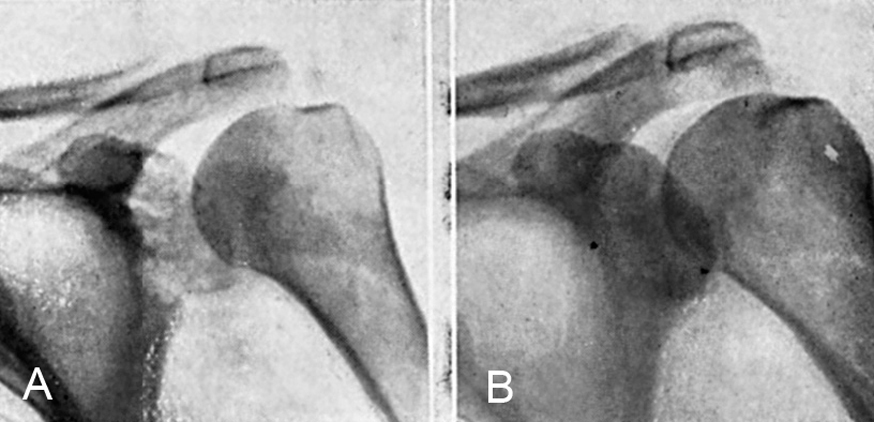
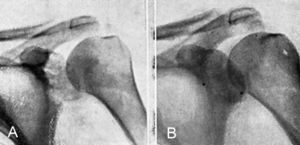
En las localizaciones óseas de los cánceres de mama el tratamiento, en la mayoría de los casos, parece que debiera ser la castración quirúrgica o por radiación, con o sin la administración de la hormona masculina. Sylven y Hallberg13 insisten sobre el efecto beneficioso de la testosterona, a la cual atribuyen la acción de atenuar el dolor, mejorar el estado general e incluso favorecer la calcificación de los focos líticos óseos. Ahora bien, no mejoran la metástasis linfáticas ni viscerales. Estos autores creen que aquella hormona, al crear un balance de nitrógeno positivo, favorece el aumento de peso y la sensación subjetiva de bienestar, acción que es más evidente cuando se aplica este tratamiento a personas debilitadas (fig. 12). Paradójicamente, Coste, Galmiche y Basset5 comunican el efecto igualmente favorable del tratamiento con estrógenos sobre las metástasis óseas en las mujeres menopáusicas, y explican que la acción del estrógeno en estos casos sería la de frenar la eliminación de hormona gonadotrópica hipofisaria. Para ellos sería la secreción perturbada de esta hormona u otra substancia somatotropa de la hipófisis anterior la que actuaría como favorecedora del crecimiento tumoral. Albright2 considera que en los casos tratados de esta forma, la mejoría aparente de las lesiones óseas sería debida a la acción osteoblástica de los estrógenos.
Figura 12. (A), metástasis de carcinoma de mama. Mujer, de cuarenta y seis años. No menopáusica. Tratamiento con andrógenos y radioterapia. (B), dos meses después de iniciado el tratamiento, densificación del foco metastásico.
Treves y col.14, en seis casos de tumores de mama en varones con metástasis esqueléticas hallaron un franca mejoría mediante la castración quirúrgica (orquiectomía); en dos casos, además de la calcificación de los focos óseos, se obtuvo una notable regresión del tumor primitivo, sobre el que no se hizo ninguna intervención quirúrgica.
En las metástasis de los cánceres de próstata el tratamiento de elección parece ser la castración y la administración de estrógenos. Riches10, en la revisión de cuarenta casos, encuentra que mediante la administración de estrógenos los dolores disminuyen y se produce una desaparición parcial de los fosos metastáticos osteoblásticos, mejorando también las metástasis viscerales.
En los cánceres de tiroides la resección del tumor primitivo y la administración de yodo radiactivo sería el único tratamiento a nuestro alcance.
La única posibilidad de resección quirúrgica del tumor primitivo y de la metástasis ósea se presenta en los hipernefromas (tumor de Grawitz), tumores que en ocasiones tienen la peculiaridad de producir una metástasis ósea solitaria, como señala Lichtenstein6.
En las restantes localizaciones del tumor primitivo sólo queda la radioterapia como tratamiento paliativo.
En lo que se refiere a las fracturas producidas por las metástasis óseas, el tratamiento ortopédico incruento está justificado en las localizaciones de la columna vertebral y miembro superior. En las fracturas del fémur la osteosíntesis metálica suprime los dolores producidos por la movilidad de los fragmentos, facilita el tratamiento hormonal o radioterápico, así como las necesidades de aseo y cuidado del enfermo, importante detalle que obstaculiza el vendaje enyesado. En alguna de estas fracturas patológicas se puede producir un callo perióstico suficiente cuando la proliferación carcinomatosa no es demasiado rápida, y con mayor razón si es frenada con el tratamiento radioterápico y hormonal. En las lesiones diafisarias deberá utilizarse el clavo intramedular (Sierra Cano y Rodríguez Valdés)11, y en las metafisarias, un clavo de placa.
(*)Comunicación a las IV Jornadas Nacionales de la S.E.C.O.T. Asturias, julio de 1955.