Evaluar retrospectivamente los resultados clínico-funcionales, las tasas de cicatrización, las complicaciones y el tiempo quirúrgico en pacientes tratados con reconstrucción capsular superior (RCS) usando autoinjerto de porción larga de bíceps (PLB) y aloinjerto de Aquiles (AA).
Materiales y métodosEstudio retrospectivo que incluyó 24 pacientes con roturas irreparables del supraespinoso e infraespinoso tratados con RCS. Se conformaron 2 grupos de tratamiento: uno con 12 casos utilizando AA y otro con 12 casos utilizando PLB. Todos los pacientes fueron seguidos durante un mínimo de 2 años.
ResultadosEl SSV fue de 73,7±25,3 vs. 86,0±8,7 (p=0,26), la escala de Constant fue de 76,8±20,1 vs. 83,7±4,6 (p=0,12) y la EVA de 1,6±2,3 vs. 1,7±0,5 (p=0,9) para los grupos PLB y AA, respectivamente. La cicatrización tendinosa fue del 66,7% en AA y del 100% en PLB (p=0,001). Las complicaciones fueron del 50% en AA y del 0% en PLB. El tiempo quirúrgico promedio fue de 127,7±37,6minutos para AA y 84,3±14,3 minutos para PLB (p=0,01).
ConclusionesLa RCS con PLB ha mostrado mejores resultados en términos de cicatrización tendinosa, menos complicaciones y un tiempo quirúrgico reducido al compararlo con la utilización de AA.
To retrospectively evaluate the clinical–functional outcomes, healing rates, complications, and surgical time in patients treated with superior capsular reconstruction (SCR) using long head of the biceps autograft (LHB) and Achilles allograft (AA).
Materials and methodsThis retrospective study included 24 patients with irreparable rotator cuff tears of the supraspinatus and infraspinatus, treated with SCR. Two treatment groups were formed: one with 12 cases using AA and another with 12 cases using LHB. All patients were followed for a minimum of 2 years.
ResultsThe SSV was 73.7±25.3 vs. 86.0±8.7 (p=0.26), the Constant score was 76.8±20.1 vs. 83.7±4.6 (p=0.12), and the VAS was 1.6±2.3 vs. 1.7±0.5 (p=0.9) for the LHB and AA groups, respectively. Tendon healing was 66.7% in AA and 100% in LHB (p=0.001). Complications were 50% in AA and 0% in LHB. The average surgical time was 127.7±37.6minutes for AA and 84.3±14.3min for LHB (p=0.01).
ConclusionsSCR with LHB showed better results in terms of tendon healing, fewer complications, and reduced surgical time compared to the use of AA.
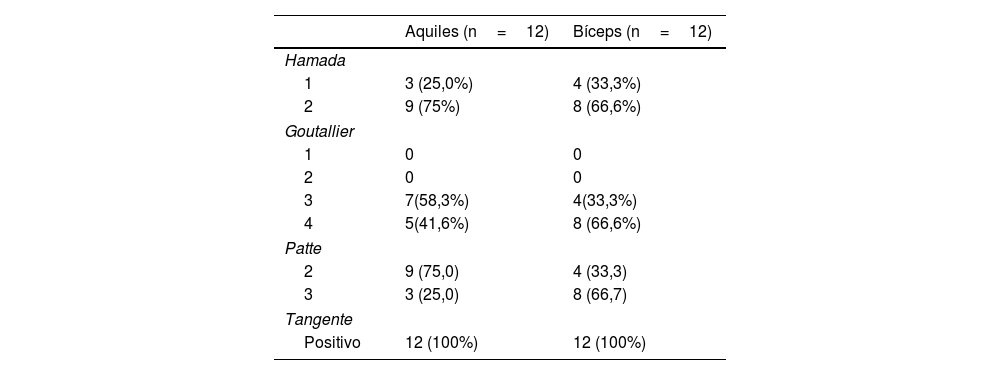
Las lesiones masivas e irreparables del manguito rotador presentan un desafío clínico significativo, especialmente en pacientes jóvenes sin artrosis glenohumeral. Se considera una lesión masiva cuando afecta a más de 2 tendones, y se clasifica como irreparable en presencia de al menos uno de los siguientes factores: degeneración grasa de grado 3 o 4, según la clasificación de Goutallier, retracción del cabo tendinoso al nivel de la glena (Patte 3), o atrofia muscular severa del supraespinoso con signo de la tangente positivo1–3.
Estas lesiones han sido abordadas mediante diversas técnicas quirúrgicas, que incluyen el desbridamiento y la tenotomía del tendón del bíceps, reparaciones parciales del manguito rotador, transferencias tendinosas y la artroplastia reversa de hombro4–8. Aún no existe un consenso sobre el tratamiento quirúrgico ideal9.
Mihata publicó en 2012 la técnica de reconstrucción capsular superior (RCS), que busca restaurar la estabilidad superior del hombro en pacientes con lesiones irreparables del supraespinoso, utilizando autoinjerto de fascia lata, que se fija en la parte superior de la glena y la huella de inserción del supraespinoso. Esta técnica presentó resultados clínicos y funcionales alentadores, junto con una tasa de cicatrización del 83,3%, lo que rápidamente la convirtió en una opción terapéutica10. Sin embargo, este procedimiento incrementa la morbilidad en el sitio dador, por lo que surgieron alternativas de injerto, como el aloinjerto dérmico acelular (AIDA), aloinjerto de tendón de Aquiles (AA) y el autoinjerto de tendón de la porción larga del bíceps (PLB)11–14.
El AA se destaca por su estructura robusta, versátil y resistente. Lee et al. han reportado buenos resultados con respecto a la movilidad activa, escalas funcionales y disminución el dolor en un seguimiento a corto plazo15. No obstante, también se han registrado tasas significativamente elevadas de complicaciones, como el fracaso de cicatrización tendinosa (83,3%), re-operaciones e infecciones16.
Por otra parte, la utilización de PLB como injerto consiste en preservar la inserción proximal del mismo, mientras que se realiza una tenotomía distal y se fija con un anclaje al nivel de la huella de inserción del tendón del supraespinoso, posterior a la entrada de la corredera biciptal. Este injerto está disponible en la mayoría de los pacientes, permitiendo un procedimiento menos costoso, con una tasa de cicatrización comparable con la técnica original de Mihata, mejorando las escalas de dolor, movilidad y función14,17.
ObjetivoEl objetivo de este estudio es realizar una evaluación retrospectiva de los resultados clínico-funcionales, tasas de cicatrización, complicaciones y tiempo quirúrgico en 2 series de pacientes tratados con PLB y AA. Dado que aún no se ha determinado el injerto óptimo, este trabajo busca aportar información valiosa en la comparación de estas alternativas para la RCS.
HipótesisSe plantea como hipótesis de que la utilización de PLB en la RCS podría generar resultados clínicos y funcionales comparables a las reparaciones con AA, pero con menor incidencia de complicaciones y un tiempo quirúrgico reducido.
Materiales y métodosSe realizó un análisis retrospectivo de nuestra base de datos para identificar a todos los pacientes con lesiones masivas e irreparables del supraespinoso e infraespinoso, tratados consecutivamente mediante la técnica de RCS utilizando AA y PLB. Estas técnicas se aplicaron en 2 períodos distintos: inicialmente se utilizó el AA desde enero de 2020 hasta junio de 2021. Posteriormente, debido a la preferencia del cirujano, los resultados obtenidos y la bibliografía disponible, se decidió comenzar a tratar a estos pacientes con PLB desde julio de 2021 hasta diciembre de 2022. El grupo AA incluyó a todos los pacientes tratados durante el primer período, mientras que el grupo PLB comprendió los primeros 12 pacientes tratados en el segundo período. Las roturas se clasificaron según la clasificación de Collin18, y todos los pacientes incluidos presentaron roturas tipo D que afectan tanto al tendón del supraespinoso como al del infraespinoso, sin compromiso del subescapular. Se seleccionaron pacientes con diagnóstico de rotura irreparable del supraespinoso e infraespinoso, sin artrosis glenohumeral (Hamada≤2), y con edades entre 40 y 70 años, para asegurar la comparabilidad entre los grupos y evitar sesgos en la recuperación y los resultados funcionales. Los criterios de exclusión fueron lesiones irreparables del tendón del músculo subescapular, artrosis glenohumeral, antecedentes de infección en el hombro y limitaciones neurológicas.
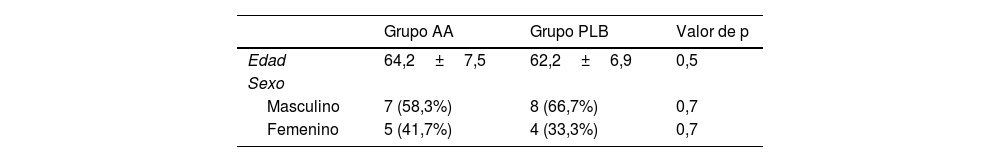
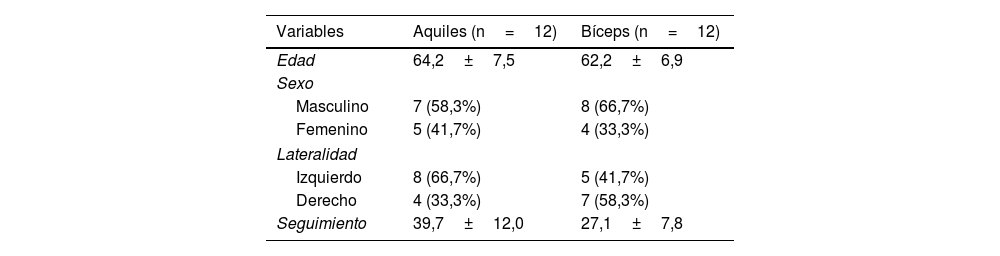
Se identificaron 12 pacientes tratados con RCS utilizando AA; de ellos 5 eran mujeres (41,7%) y 7 eran hombres (58,3%), con una edad media de 64,2±7,5años. El período de seguimiento para el grupo AA fue de 39,7±12meses. El emparejamiento se realizó con 12 pacientes, incluyendo 8 hombres (66,7%) y 4 mujeres (33,3%), con una edad media de 62,2±6,9 años y un período de seguimiento para el grupo PLB de 27,1±7,8 meses tratados con PLB, según se describió anteriormente (tabla 1).
El rango de movilidad del hombro fue evaluado clínicamente por el cirujano tratante antes de la cirugía y en los controles postoperatorios periódicos. Los parámetros de evaluación clínica incluyeron la movilidad activa del hombro realizando: elevación anterior en el plano de la escápula, rotación externa con el hombro en aducción y el codo en flexión de 90 grados y rotación interna estimada según el máximo nivel alcanzado por el pulgar. Además, se utilizó la escala visual analógica (EVA) para determinar la presencia e intensidad del dolor, y se evaluó la función mediante la escala de Constant-Murley y el Subjective Shoulder Value (SSV).
Evaluación radiológicaSe revisaron las radiografías de hombro en proyecciones anteroposterior y axiales de la escápula preoperatorias y a los 2 años postoperatorios. Se midió el intervalo acromiohumeral (IAH), determinado por la distancia entre el ápex de la cabeza humeral y el borde inferior del acromion, y se registró la presencia preoperatoria de artropatía de manguito rotador según la clasificación de Hamada.
Se llevó a cabo una evaluación por resonancia magnética (RM) preoperatoria y posoperatoria a los 2 años. La evaluación preoperatoria por RM incluyó la clasificación de Goutallier para la infiltración grasa del músculo, Patte para el grado de retracción tendinosa y el signo de la tangente, que se midió en cortes sagitales T1 trazando una línea tangente al borde superior de la apófisis coracoides hasta el borde superior de la espina, en un corte sagital al nivel de la escápula1–3. Se consideró irreparable un músculo con infiltración grado 3 y 4, retracción tendinosa grado 3, o signo de la tangente positivo, siendo la confirmación definitiva intraoperatoria según criterio del cirujano. Adicionalmente, se identificó en las imágenes postoperatorias el estado del injerto como continuo o discontinuo mediante el uso de la clasificación de Sugaya y la lectura de un especialista en imágenes diagnósticas independiente, sin conocimiento del tipo de injerto utilizado19. En concordancia con Bernstein et al.20 se consideró que el injerto estaba continuo cuando presentaba un aspecto homogéneo de baja intensidad en T1, sin evidencia de interposición de líquido entre el injerto y su anclaje óseo. El fracaso de cicatrización se definió como cualquier discontinuidad del tendón a lo largo de su trayecto, desde la inserción en la glena hasta su inserción en el troquíter, o la presencia de líquido en la interfase injerto-anclaje que indique falta de integración. En los tendones cicatrizados se realizó la medición del espesor del injerto para evaluar su comportamiento.
Se registró en la historia clínica la presencia de complicaciones intraoperatorias y reintervenciones durante el seguimiento. Además, se identificó el tiempo quirúrgico empleado tanto para el grupo AA como para el grupo PLB, medido en minutos.
Análisis estadísticoLas variables continuas se describieron como media y desviación estándar, y las variables cualitativas como porcentaje. Se compararon los 2 grupos de análisis mediante una prueba «t» para las variables cuantitativas y la prueba de Fisher para las variables cualitativas. Se consideró estadísticamente significativa una diferencia<0,05. Se utilizó el programa Graph Pad Prism 8.0.
Técnica quirúrgicaTodos los pacientes fueron intervenidos quirúrgicamente en nuestro centro, por el mismo equipo quirúrgico, bajo anestesia general previo bloqueo regional interescalénico. Se colocaron en posición de silla de playa. Se practicó una artroscopia exploradora. Después de realizar una bursectomía amplia, se realizó una movilización del muñón del infraespinoso, realizando en todos los casos una reparación parcial del mismo.
Técnica con aloinjerto de Aquiles (fig. 1)Acorde con la descripción original de la técnica quirúrgica planteada por Mease et al.21, se realizó el cruentado y decorticación de la cara superior de la glena, resecando el labrum y la inserción bicipital, realizando una tenomía del mismo. Se colocaron 2 anclajes Subpunch 3.0mm (South America Implants S.A, Canning, Buenos Aires, Argentina) en hora 11 y 13, a través del portal anterior, y un portal de Neviaser al menos 5mm mediales al borde articular. Posteriormente se procedió a medir con un palpador graduado la distancia mediolateral desde el borde articular superior de la glena hasta el comienzo de la huella de inserción del supraespinoso. A esta medición se le agregó 1cm por el lado de la glena y 15mm por el lado del troquíter; el injerto se coloca fijando la parte distal del tendón de Aquiles en la glena y la parte proximal en el húmero. Esta orientación se elige porque el tendón es más ancho en su porción proximal y más angosto en la distal, lo que permite una mejor adaptación anatómica y una fijación más segura en los puntos de contacto óseo. La medición anteroposterior se realizó desde el margen anterior del infraespinoso, tras realizar la reparación parcial, hasta el borde superior del subescapular. Puesto que el AA presenta en promedio un grosor máximo de 8mm no es necesario plegarlo para aumentar su tamaño. Sus bordes se suturaron con una sutura continua de alta resistencia para obtener un constructo uniforme y resistente21. En el borde medial del injerto se pasaron los 8 cabos de sutura provenientes de los anclajes; con 4 se realizó un anudado con técnica de doble polea, lo que permitió facilitar el ingreso y la correcta ubicación del injerto. Con las suturas remanentes se fijó el borde anterior y posterior con nudos colchoneros. En la cara lateral se realizó una fijación con técnica de doble hilera equivalente transóseo. La fijación en la cara lateral se realizó en 30° de abducción y 20° de rotación externa. En todos los casos se realizó un cierre lado a lado entre el injerto y el infraespinoso con 2 suturas HS Fiber USP2 M5 (South America Implants S.A, Canning, Buenos Aires, Argentina)(fig. 2).
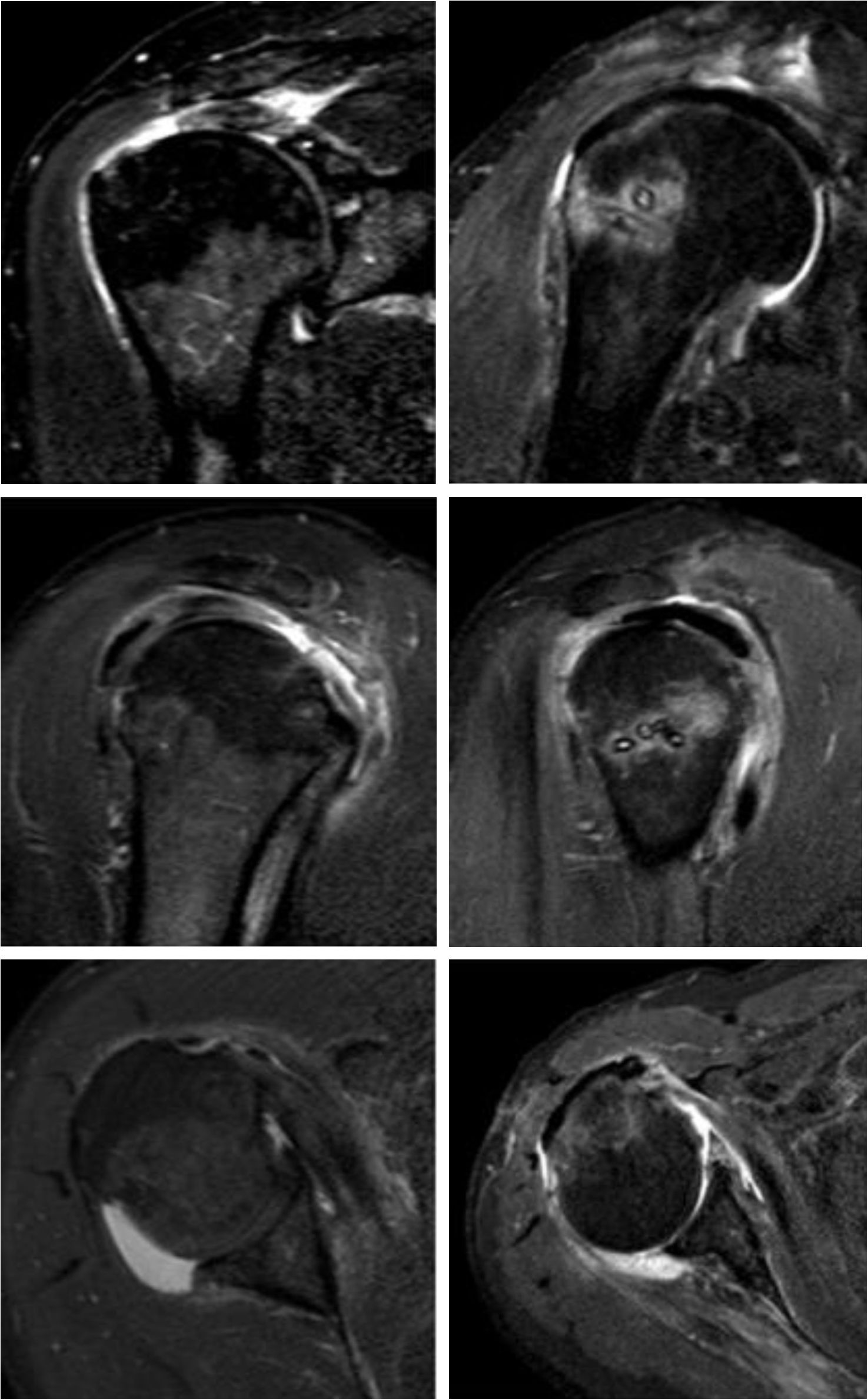
Resultado de imágenes de aloinjerto de Aquiles (AA).
Resultado postoperatorio de reconstrucción capsular superior (RCS) con AA. A y B. Se muestran imágenes preoperatorias de resonancia magnética nueclear (RMN) con una lesión masiva e irreparable. Cy D. Imágenes postoperatorias de RMN, pasados 2 años de la reconstrucción con AA.
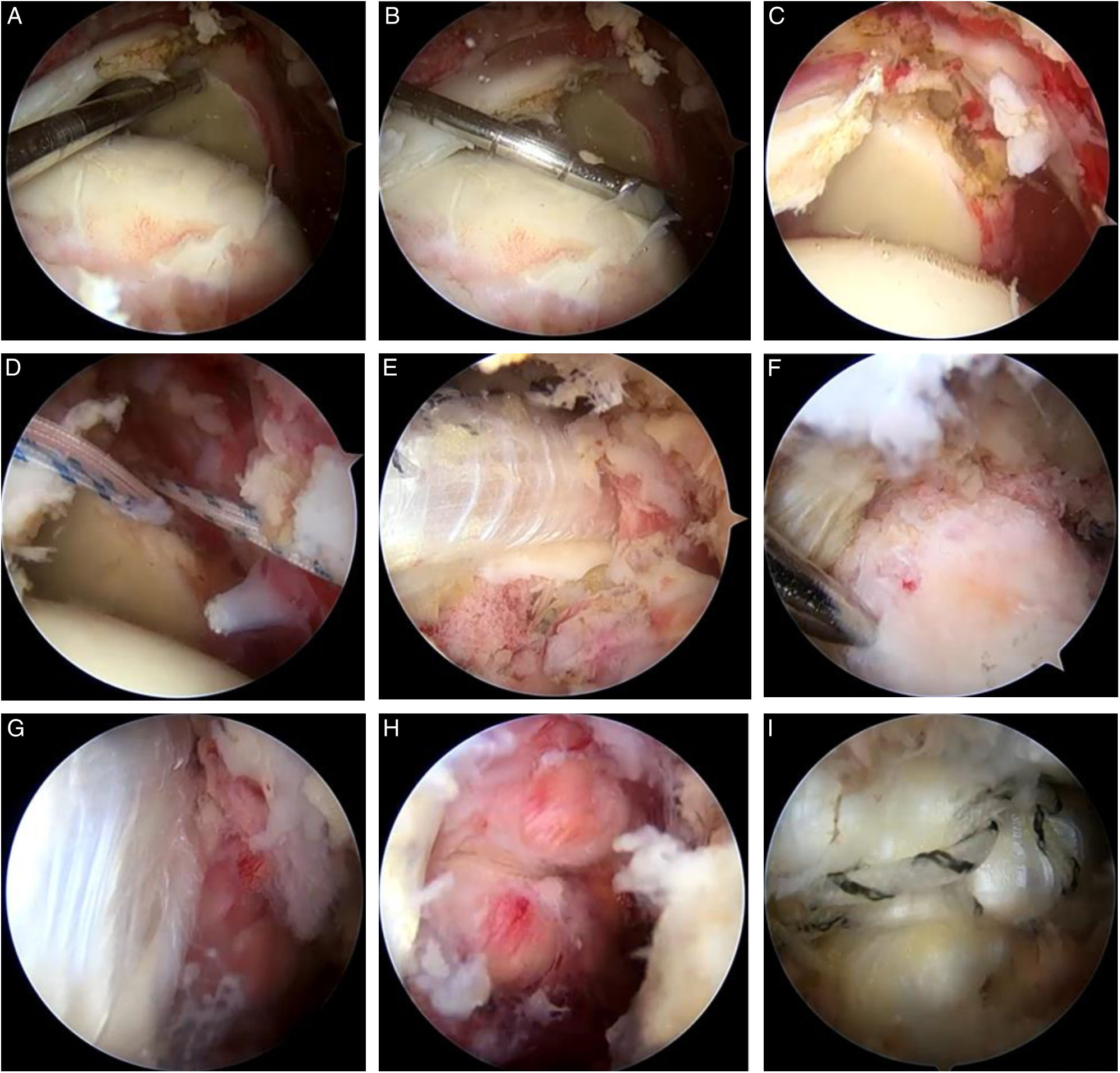
Resultado intraoperatorio con aloinjerto de Aquiles (AA).
Resultado final intraoperatorio de una reconstrucción capsular superior (RCS) con AA. A y B. Mediciones intraoperatorias para la confección del aloinjerto de Aquiles. C. Preparación de la glena en las posiciones de las 11 y las 13 horas para la colocación de los anclajes. D. Colocación de los anclajes con doble sutura. E. Deslizamiento del aloinjerto mediante el sistema de doble polea. F. Fijación lateral en la huella de inserción del supraespinoso. G. Visualización del aloinjerto fijado y del manguito posterosuperior remanente. H. Reparación parcial del manguito posterosuperior. I. Cobertura completa de la cabeza humeral con el AA.
Durante la artroscopia diagnóstica se evaluó la integridad del tendón del bíceps desde el portal posterior. No se encontraron lesiones de SLAP mayores o iguales al grado 2, y los cambios degenerativos observados en el labrum superior, compatibles con la edad de los pacientes, no representaron una contraindicación para proceder con la RCS. A continuación se procedió a cruentar y decorticar la huella de inserción del tendón del supraespinoso, posteriormente se introdujeron 2 suturas de alta resistencia en la porción larga del bíceps, justo antes de su entrada en la corredera bicipital, con un mínimo de 4 pasos de sutura que atravesaron el tendón. Luego se procedió a la apertura del ligamento transverso en la corredera bicipital, seguido de una tenotomía en la porción distal del bíceps, distal de la zona de sutura. El tendón se movilizó y se ancló con un arpón knotless Subtwist de 4,5mm en el centro del troquíter (justo detrás de la corredera bicipital) (South America Implants S.A.®, Canning, Buenos Aires, Argentina), siguiendo la descripción de Boutsiadis et al.14. Esta ubicación optimiza la tensión lograda para que el tendón adopte una posición adecuada al nivel del cable anterior del manguito rotador. No se realizó en ningún caso una tenodesis en la porción distal remanente del tendón bicipital. Finalmente, se verificó la tensión mediante palpación. En todos los casos se agregó a esto una reparación parcial del manguito posterosuperior remanente(fig. 4).
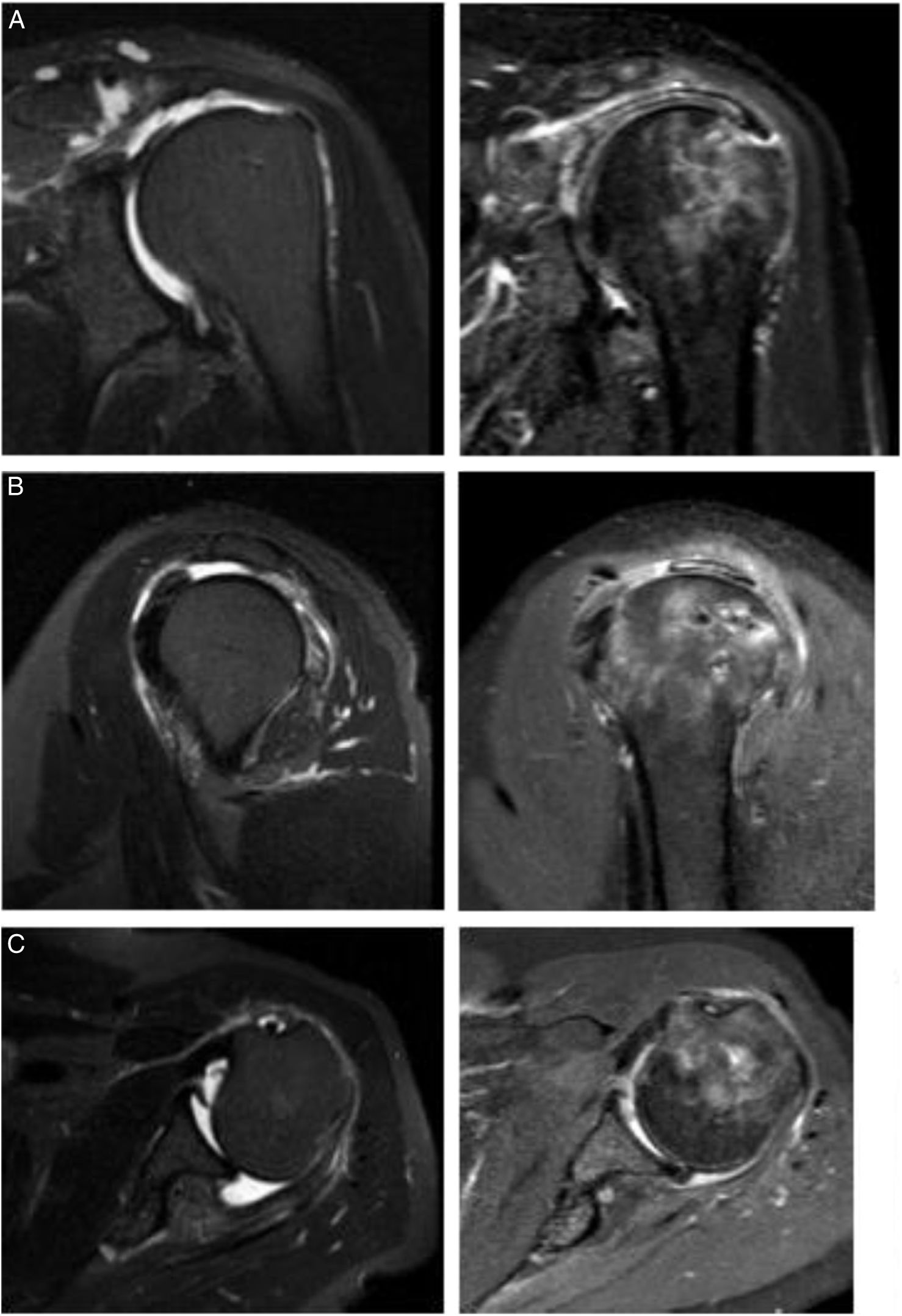
Resultado de imágenes con autoinjerto de porción larga del bíceps (PLB).
El resultado postoperatorio de reconstrucción capsular superior con PLB se ilustra en las siguientes imágenes. A. Muestra un corte coronal de resonancia magnética nuclear (RMN) con una lesión Patte 3 del tendón del supraespinoso y su resultado postoperatorio con PLB. B. Corte sagital de RMN con una lesión posterosuperior del manguito rotador y su resolución con PLB. C. Lesión posterior del manguito rotador en un corte axial de RMN y su resolución con PLB. Todas las imágenes postoperatorias fueron tomadas a los 2 años después de la reconstrucción con PLB.
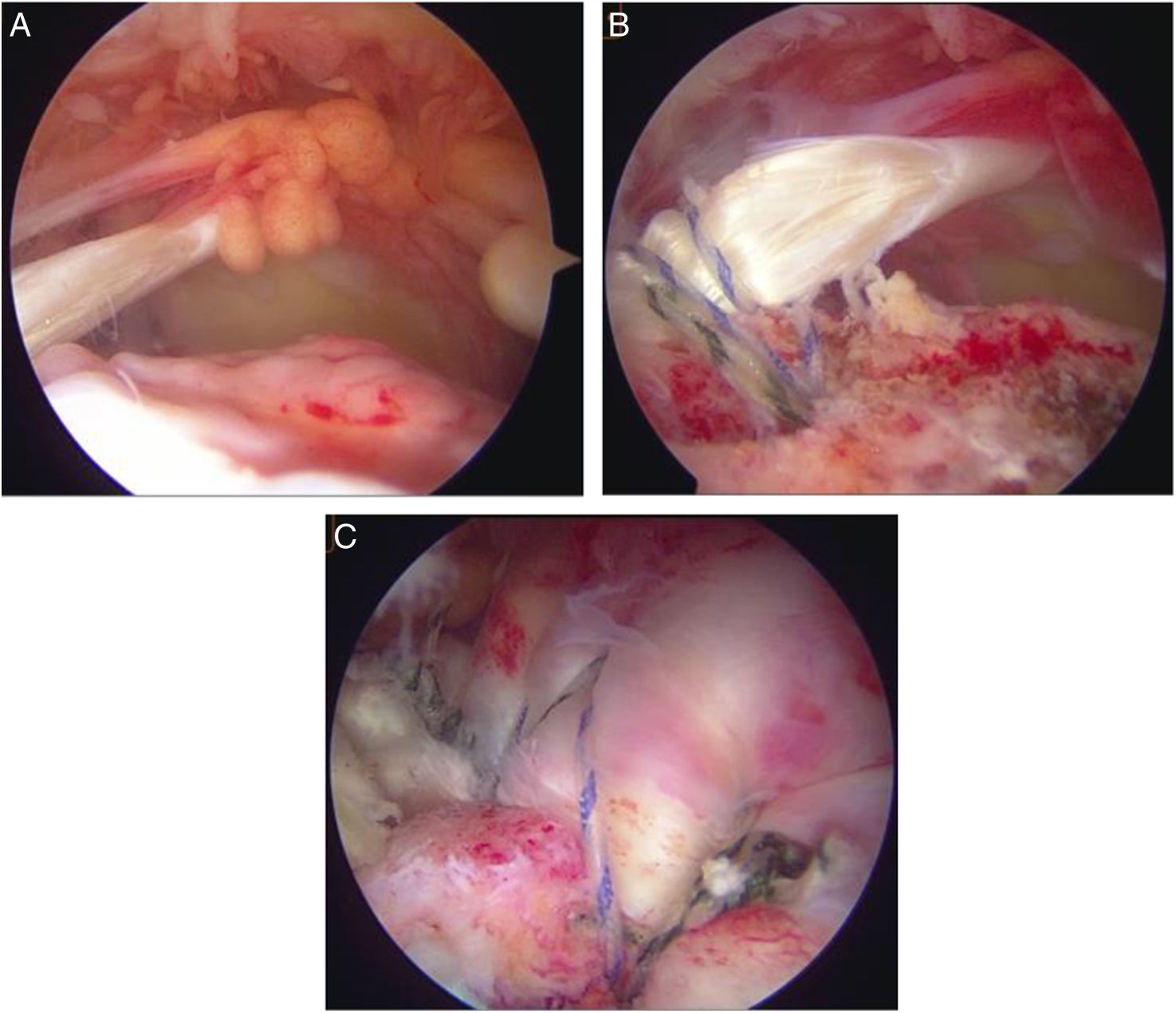
Técnica autoinjerto de porción larga del bíceps (PLB).
A. Identificación de una lesión masiva del manguito rotador, visualizando claramente el área desprovista de los tendones supraespinoso e infraespinoso desde el portal lateral. B. Anclaje tendinoso de la PLB en el centro del troquíter. C. Reparación parcial del manguito remanente unido al PLB.
Todos los pacientes siguieron el mismo protocolo de rehabilitación, utilizando un cabestrillo tipo Velpeau durante 6 semanas. La rehabilitación kinésica comenzó a los 30 días postoperatorios, con ejercicios de movilidad pasiva. La movilidad activa sin resistencia se indicó a las 6 semanas. Las actividades de fuerza se restringieron hasta el tercer mes, y se permitieron actividades deportivas o el retorno a trabajos de fuerza al sexto mes, según la evolución clínica de cada paciente.
ResultadosLos datos demográficos de la muestra se detallan en la tabla 2.
Tanto el grupo AA como el PLB evidenciaron mejoras en los resultados clínicos y funcionales posoperatorios (tabla 3). El grupo PLB mostró una ligera superioridad sobre el grupo AA en el SSV, siendo 86,0±8,7 vs. 73,7±25,3 y en la escala de Constant de 83,7±4,6, vs. 76,8±20,1, pero sin demostrar que esto fuera estadísticamente significativo (p=0,26) y (p=0,12) respectivamente. Con respecto a la evaluación de la EVA se reportaron valores de 1,6±2,3 vs. 1,7±0,5 (p=0,9) para el grupo AA y el grupo PLB.
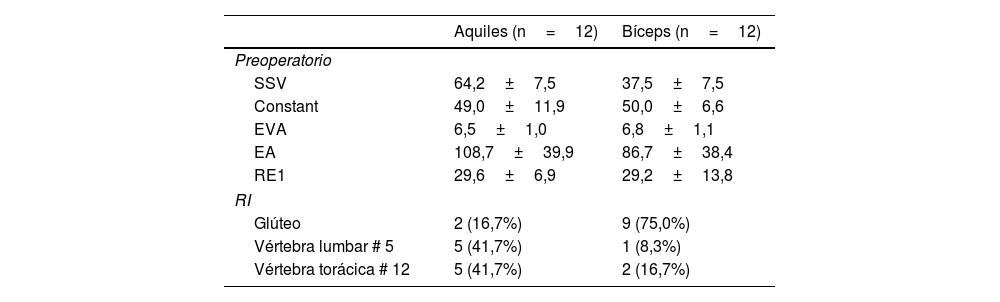
Comparativa de resultados clínico-funcionales
| Aquiles (n=12) | Bíceps (n=12) | |
|---|---|---|
| Preoperatorio | ||
| SSV | 64,2±7,5 | 37,5±7,5 |
| Constant | 49,0±11,9 | 50,0±6,6 |
| EVA | 6,5±1,0 | 6,8±1,1 |
| EA | 108,7±39,9 | 86,7±38,4 |
| RE1 | 29,6±6,9 | 29,2±13,8 |
| RI | ||
| Glúteo | 2 (16,7%) | 9 (75,0%) |
| Vértebra lumbar # 5 | 5 (41,7%) | 1 (8,3%) |
| Vértebra torácica # 12 | 5 (41,7%) | 2 (16,7%) |
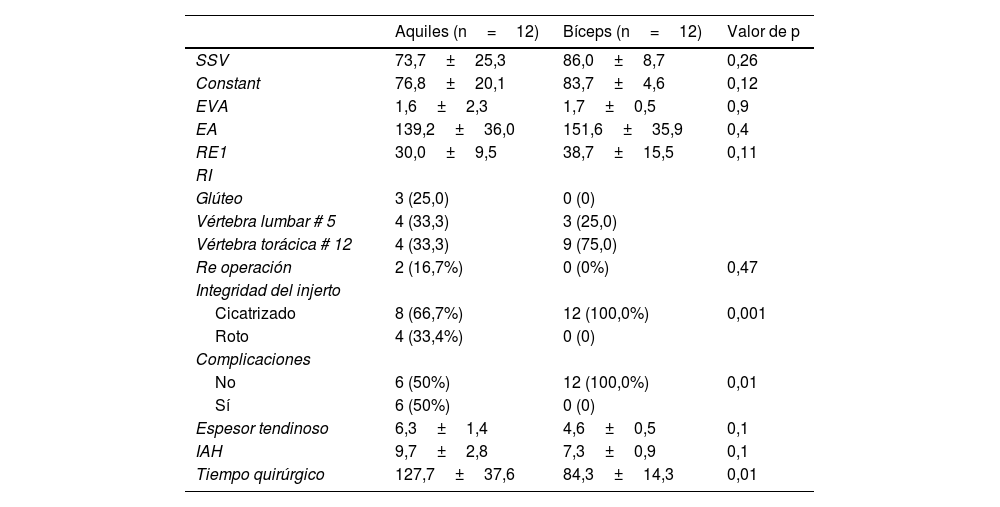
En los resultados por pruebas de imágenes (tabla 4), el grupo AA logró mayor ocupación en el espacio subacromial, con un IAH de 9,7±2,8 vs. 7,3±0,9 para el grupo PLB, sin llegar a ser estadísticamente significativo (p=0,1). Asimismo, el espesor del injerto evaluado por RM mostró en el grupo AA ser de 6,3mm±1,4 con AA vs. 4,6mm±0,5 en el grupo PLB (p=0,1). La tasa de cicatrización tendinosa evidenció una marcada diferencia entre los grupos, siendo del 66,7% para el grupo AA vs. 100% para el grupo PLB (p=0,001). En cuanto a las complicaciones, 2 pacientes tratados con AA (16,7%) requirieron intervención adicional debido a infección, incluyendo la retirada del aloinjerto y el tratamiento con antibióticos específicos. En 4 casos (33,4%) se documentó fracaso en la cicatrización del injerto en el grupo AA. No se registraron complicaciones en el grupo PLB. En el análisis comparativo entre ambas técnicas se observó una reducción significativa en el tiempo quirúrgico en el grupo PLB de 84,3minutos±14,3 vs. 127,7±37,6minutos, para el grupo AA (p=0,01) (tabla 5).
Comparativa postoperatoria
| Aquiles (n=12) | Bíceps (n=12) | Valor de p | |
|---|---|---|---|
| SSV | 73,7±25,3 | 86,0±8,7 | 0,26 |
| Constant | 76,8±20,1 | 83,7±4,6 | 0,12 |
| EVA | 1,6±2,3 | 1,7±0,5 | 0,9 |
| EA | 139,2±36,0 | 151,6±35,9 | 0,4 |
| RE1 | 30,0±9,5 | 38,7±15,5 | 0,11 |
| RI | |||
| Glúteo | 3 (25,0) | 0 (0) | |
| Vértebra lumbar # 5 | 4 (33,3) | 3 (25,0) | |
| Vértebra torácica # 12 | 4 (33,3) | 9 (75,0) | |
| Re operación | 2 (16,7%) | 0 (0%) | 0,47 |
| Integridad del injerto | |||
| Cicatrizado | 8 (66,7%) | 12 (100,0%) | 0,001 |
| Roto | 4 (33,4%) | 0 (0) | |
| Complicaciones | |||
| No | 6 (50%) | 12 (100,0%) | 0,01 |
| Sí | 6 (50%) | 0 (0) | |
| Espesor tendinoso | 6,3±1,4 | 4,6±0,5 | 0,1 |
| IAH | 9,7±2,8 | 7,3±0,9 | 0,1 |
| Tiempo quirúrgico | 127,7±37,6 | 84,3±14,3 | 0,01 |
La RCS con el uso de la PLB resulta superior en términos de cicatrización tendinosa, con una menor incidencia de complicaciones y un menor tiempo quirúrgico en comparación con la RCS con AA. En nuestro estudio la cicatrización tendinosa alcanzó un 100% en el grupo de PLB y un 66,7% en el grupo AA, lo cual fue estadísticamente significativo (p=0,001). Estos excelentes resultados concuerdan con los reportados por Gao et al.22, quienes documentaron una tasa de cicatrización tendinosa de 87,7% con el uso de PLB. La mejora en la cicatrización podría explicarse, según Kim et al.23, por el mantenimiento de la unión intacta de la PLB en el tubérculo supraglenoideo, lo que minimiza los fracasos mediales y permite que el autoinjerto conserve suficiente irrigación, además de ofrecer una mejor propiocepción teórica.
Conocer las ventajas y desventajas de cada injerto es fundamental a la hora de seleccionar la técnica a utilizar. Además, se deben considerar los costos adicionales asociados al procedimiento como parte integral de la toma de decisiones. En nuestro trabajo las complicaciones fueron significativamente menores en el grupo de PLB, sin presentar complicaciones durante el seguimiento, mientras que el grupo AA tuvo una tasa de complicaciones del 50%, destacándose el fracaso de cicatrización tendinosa (33,4%) y la infección (16,7%). Los casos de infección requirieron de lavado quirúrgico, retirada del aloinjerto y antibioterapia dirigida. Estos hallazgos son consistentes con los resultados de Lädermann et al.24, quienes reportaron una tasa de complicaciones del 35% asociadas al uso de aloinjertos, y con la revisión sistemática de Sommer et al.25, que documentaron tasas de complicaciones que varían entre el 5% y el 70% para aloinjertos, comparado con un 14% a 32% para autoinjertos. Gao et al.22, en un estudio retrospectivo con 89 pacientes sometidos a RCS con el uso de PLB, documentaron una tasa de fracaso de cicatrización tendinosa del 12,4%, a la vez que no observaron otras complicaciones. En función de los hallazgos en la literatura y de nuestros resultados podemos afirmar que el uso de autoinjerto de PLB para la RCS proporciona menores complicaciones en comparación con el uso de AA.
La función principal de la RCS es el centrado de la cabeza humeral. Han et al.26, en un estudio biomecánico en el que utilizaron la porción larga del bíceps, evidenciaron una disminución en la traslación superior de la cabeza humeral y una reducción en las presiones de contacto subacromial a 0° y 60° de abducción glenohumeral. En nuestros resultados el PLB mostró un menor espesor en comparación con AA (4,6±0,5 vs. 6,3±1,4; p=01), lo cual es de esperar, dado que el AA tiene un grosor promedio de 8mm y, por tanto, no requiere ser plegado. Sin embargo, a pesar de esta diferencia en espesor, no se observaron diferencias significativas en IAH postoperatorio durante el seguimiento. Zhao et al.27 señalan que la RCS con PLB, al tener un grosor insuficiente, desempeñaría un menor efecto espaciador. Esto sugiere que el efecto del «trampolín invertido» de la RCS28, al recentrar la cabeza humeral, influye directamente en los valores del IAH y no se atribuye únicamente a un efecto de ocupación del espacio subacromial al posicionar el injerto.
El éxito de la RCS con PLB se puede atribuir tanto a factores biológicos como mecánicos. Desde el punto de vista biológico, el PLB ya tiene su propia vascularización, lo que puede promover una mejor cicatrización y regeneración en comparación con un aloinjerto29. Mecánicamente el PLB agrega resistencia y estructura a la cápsula articular, lo que contribuye a la estabilidad de la reconstrucción, como se reporta en el estudio de Han et al.21. Recientemente, se ha descrito la RCS con PLB sin tenotomía, mostrando resultados favorables. McClatchy et al.30 postularon que mantener el PLB intacto después de la transposición podría proporcionar un efecto depresor dinámico y estabilizador de la cabeza humeral, mejorando potencialmente la función del hombro, al preservar la tensión natural del tendón en su nueva posición. Además, un estudio biomecánico en un modelo de conejo mostró que el tendón del bíceps se remodela progresivamente y cicatriza adecuadamente en la nueva posición transpuesta, con una resistencia biomecánica de la cápsula superior que supera la de la cápsula nativa31. En nuestro estudio, que abarca un periodo anterior a la publicación de los hallazgos de McClatchy, se optó por realizar la tenotomía del PLB. Los resultados de la serie de McClatchy son promisorios y sugieren que esta técnica puede ser una alternativa terapéutica viable.
La simplicidad técnica del uso de PLB, que elimina la necesidad de aloinjerto, contribuye a una reducción del tiempo quirúrgico, con un promedio de 84,3±14,3minutos para el grupo PLB, frente a 127,7±37,6minutos para el grupo AA (p=0,01). Esto mejora el rendimiento de la técnica, como también se ha corroborado en revisiones bibliográficas que destacan las ventajas del autoinjerto de bíceps en términos de tiempo quirúrgico y riesgo de infección32. Adicionalmente, el tiempo quirúrgico reducido conlleva beneficios económicos y una menor morbilidad asociada al procedimiento. Además, es importante señalar que las técnicas con aloinjertos implican un costo adicional, no solo debido al aloinjerto en sí, sino también a la utilización de una mayor cantidad de anclajes óseos.
Tanto el grupo AA como el PLB mostraron mejoras en las escalas funcionales (SSV y Constant) y en el rango de movilidad. Aunque no hay estudios comparativos directos entre AA y PLB, revisiones sistemáticas de diversos injertos, incluyendo aloinjerto dérmico acelular, tendón de fascia lata y PLB, han reportado resultados clínicos y funcionales similares a corto plazo, con mejoras en el rango de movilidad y una reducción significativa del dolor. Demostrando puntuaciones postoperatorias de SSV con la utilización de AIDA, FL y PLB de 85,3 (77,5-89), 88,6 (73,7-94,3) y 82,7 (80-85,4) respectivamente. Asimismo, se observó una mejora en el VAS de 0,8, 2,5 y 1,4 y predominantemente una mejora en la elevación anterior de 159,0°, 147,0°, 163,8° respectivamente33.
LimitacionesEste estudio presenta varias limitaciones. En primer lugar, su naturaleza retrospectiva y el tamaño reducido de la muestra limitan la solidez de las conclusiones estadísticas. Además, el seguimiento a corto plazo no permite evaluar la durabilidad de los resultados clínicos a largo plazo.
Otro posible sesgo de selección se debe a la forma en que se aplicaron las técnicas en diferentes periodos de tiempo. Inicialmente, se utilizó el AA como injerto en un grupo de 12 pacientes. Posteriormente, y tras la experiencia obtenida con estos casos, se decidió utilizar el tendón de la cabeza larga del bíceps PLB en los pacientes siguientes. Esta secuencia en la adopción de técnicas podría haber influido en los resultados debido a la evolución de las habilidades del cirujano, introduciendo un sesgo de aprendizaje.
Además, en ambos grupos se realizaron procedimientos adicionales como tenotomía de bíceps, desbridamiento y reparaciones parciales. Aunque estos procedimientos fueron consistentes entre los grupos, impiden conclusiones específicas sobre la efectividad de la RCS frente a técnicas menos invasivas, como la tenotomía de bíceps o el desbridamiento aislado.
Es relevante mencionar que todas las cirugías y el seguimiento fueron realizados por el mismo cirujano, lo que podría introducir un sesgo en la evaluación de los resultados. Para obtener conclusiones más robustas y guiar mejor la elección del tipo de injerto en la RCS, se necesitan estudios adicionales con un mayor número de pacientes y un seguimiento más prolongado. A pesar de estas limitaciones, este es el único estudio que compara directamente estas 2 técnicas hasta la fecha.
ConclusiónLa RCS con el uso de PLB demostró mejores resultados en términos de cicatrización tendinosa y menores complicaciones en comparación con la técnica AA, lo que sugiere que el PLB podría representar una opción más segura de tratamiento. Además, la RCS con PLB presenta ventajas adicionales, como un tiempo quirúrgico reducido, respaldando su utilidad como una opción más simple.
Nivel de evidenciaNivel de evidencia iv.
FinanciaciónNinguno de los autores ha recibido financiación o beneficios de ninguna entidad comercial que pueda tener interés en los resultados presentados en este artículo. Todos los procedimientos y análisis fueron realizados de manera independiente y transparente, asegurando la objetividad e integridad del estudio.
Consideraciones éticasEste estudio fue realizado siguiendo los principios éticos establecidos en la Declaración de Helsinki. Debido a las características retrospectivas del trabajo, y a que todos los pacientes culminaron su tratamiento, no se cuenta con consentimiento informado. Se solicitará la exención del consentimiento informado para este estudio. El protocolo del estudio fue revisado y aprobado por el Comité de Ética del Hospital Británico de Buenos Aires.
Se han tomado todas las medidas para asegurar la confidencialidad de los datos. Asimismo, se ha respetado la Ley de Protección de Datos Personales, garantizando que se ha mantenido el anonimato de los participantes en todas las etapas del estudio.
Conflicto de interesesLos autores declaran que no tienen ningún conflicto de intereses relacionado con este estudio.