La demencia condiciona la nutrición del paciente desde su inicio, produciendo anorexia, pérdida ponderal, apraxias para la ingesta y disfagia. Cada fase evolutiva exige estrategias diferentes que deben comenzar por la sensibilización, el conocimiento del problema y su detección temprana. En la demencia, la disfagia se presenta habitualmente en fases avanzadas y con frecuencia el paciente está institucionalizado. Tras su sospecha, hay que evaluar la tolerancia del paciente mediante el test de volumen/viscosidad, introducir estrategias ambientales y posturales en la alimentación y modificar las texturas de la dieta. Ésta es una labor compleja que exige la participación de un equipo interdisciplinario bien formado que pueda ofrecer información y alternativas, integrando al entorno familiar en el plan de cuidados. La dieta adaptada debe basarse en la alimentación tradicional, que puede combinarse con preparados comerciales y suplementos nutricionales para conseguir una dieta variada que aumente la satisfacción de pacientes, cuidadores y familia. Las sondas de alimentación no han demostrado beneficios en la alimentación de los pacientes con demencia avanzada. Por todo ello, proponemos la alimentación oral asistida como la forma más natural y adecuada en este tipo de pacientes, respetando su voluntad previamente expresada.
From the onset, dementia affects the patient's nutritional status, producing anorexia, weight loss, feeding apraxia and dysphagia. Distinct strategies are required in each of the stages of this disease, starting with awareness and knowledge of the problem and its prompt detection. In dementia, dysphagia usually appears in advanced phases, when the patient is often institutionalized. When dysphagia is suspected, the patient's tolerance must be evaluated by the volume/viscosity test, environmental and postural strategies should be introduced, and the texture of the diet should be modified. This is a complex task requiring the involvement of a properly trained interdisciplinary team, able to provide information and alternatives and integrate the family environment in the patient's care. The adapted diet should be based on the traditional diet that can also be combined with artificial supplements to provide a varied diet that increases patients’, caregivers’ and relatives’ satisfaction. Tube feeding has shown no nutritional benefits in patients with advanced dementia. Therefore, we propose assisted oral feeding as the most natural and appropriate form of feeding in these patients, always respecting their previously expressed wishes.
La deglución es una de las funciones básicas del organismo. Es un proceso neuromuscular complejo, en el que intervienen más de 50 pares de músculos y que requiere de una coordinación muy precisa. La disfagia, o dificultad en la deglución, se suele clasificar según el lugar (orofaríngea, esofágica, paraesofágica) o el mecanismo de producción (mecánico o neurogénico)1. Los cambios musculares (menor masa y fuerza muscular) y del sistema nervioso pueden provocar un empobrecimiento global de la respuesta motora con aumento de la disfagia orofaríngea2, que es la más frecuente en el anciano, por encima de las causas mecánicas y esofágicas3,4. La proporción de >65 años con disfagia se estima entre el 7–22%5, afectando al 15% los mayores en domicilio y al 40% de los mayores institucionalizados1–3. Enfermedades neurológicas degenerativas y vasculares tan ligadas al envejecimiento como el Parkinson, el accidente vascular cerebral (ACV) o las demencias se acompañan de disfagia en ente un 25–50% de los casos en algún momento de su fase evolutiva. Otras circunstancias favorecedoras de la disfagia y la aspiración, como el uso de medicación sedante (disminución del reflejo deglutorio), la disminución de saliva, la pérdida de piezas dentarias y/o la mala higiene oral, son tan frecuentes en el mayor que la disfagia se ha postulado como un gran síndrome geriátrico, infradiagnosticado en la actualidad.
La enfermedad de Alzheimer (EA) es el prototipo de la demencia cortical. La disfagia asociada a esta enfermedad se ha denominado disfagia psudobulbar y es consecuencia de la afectación del neocórtex y del sistema límbico que deteriora las conductas alimenticias voluntarias y estereotipadas de la persona afecta6.
La desestructuración de la conducta alimentaria va pareja a la severidad de la demencia, a la pérdida funcional y cognitiva, afectando clínicamente al 45–50% de demencias severas de diferentes etiologías. Sus consecuencias más importantes son la deshidratación, la pérdida ponderal, la desnutrición y la broncoaspiración, siendo la neumonía aspirativa la principal causa de muerte de estos pacientes6,7.
Lo habitual es que los pacientes con demencia en sus últimos estadios estén institucionalizados. Enfrentarse a la disfagia significa enfrentarse al problema deglutorio y sus causas, al estado cognitivo, al estado nutricional y a sus complicaciones, entre ellas el final de la vida. Ello implica sensibilización y conocimiento del problema, la formación del personal, la relación con las familias y la toma de decisiones con variables tan dispares como la evidencia científica o las creencias personales de familiares y cuidadores.
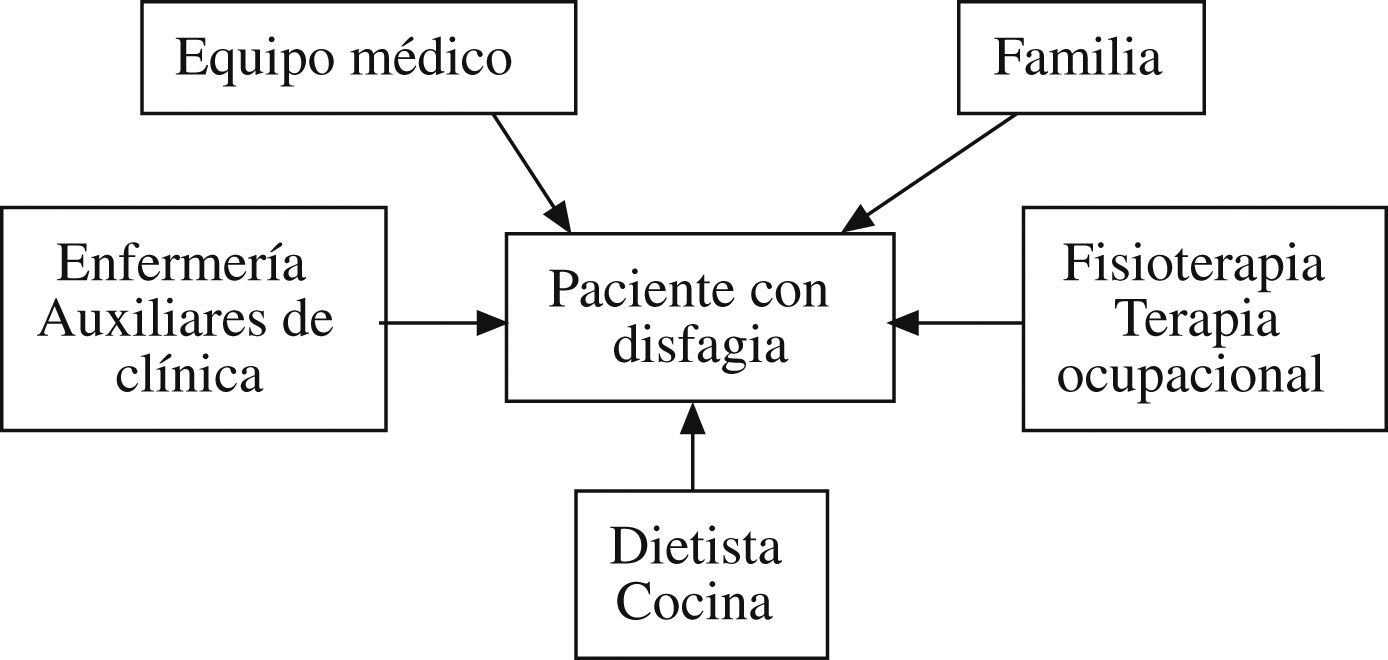
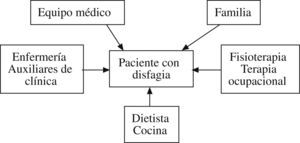
Abordaje de la disfagiaEl abordaje de la disfagia implica a familiares y a cuidadores en una actuación conjunta y multidisciplinaria, como se recoge en la figura 1.
El objetivo general es mejorar el estado nutricional y disminuir la morbimortalidad basándonos en la identificación temprana y en su diagnóstico causal, en el conocimiento de las características de la disfagia y en el desarrollo de estrategias para una deglución segura y eficaz, fundamentalmente la modificación del volumen/viscosidad del bolo alimenticio y el tratamiento postural3. En la demencia, sin embargo, hay que situar la disfagia como un síndrome frecuente de una enfermedad de curso largo y progresivo, en la que las alteraciones de la conducta alimentaria son múltiples, afectando en sus últimos estadios a más del 70% de los pacientes8, habitualmente mayores con múltiples síndromes geriátricos, en un contexto de baja inmunidad, pluripatología y polifarmacia. Intentaremos, por tanto, analizar el contexto general de la disfagia en la demencia avanzada antes de abordar las estrategias posturales, el tipo de alimentación y la vía de administración.
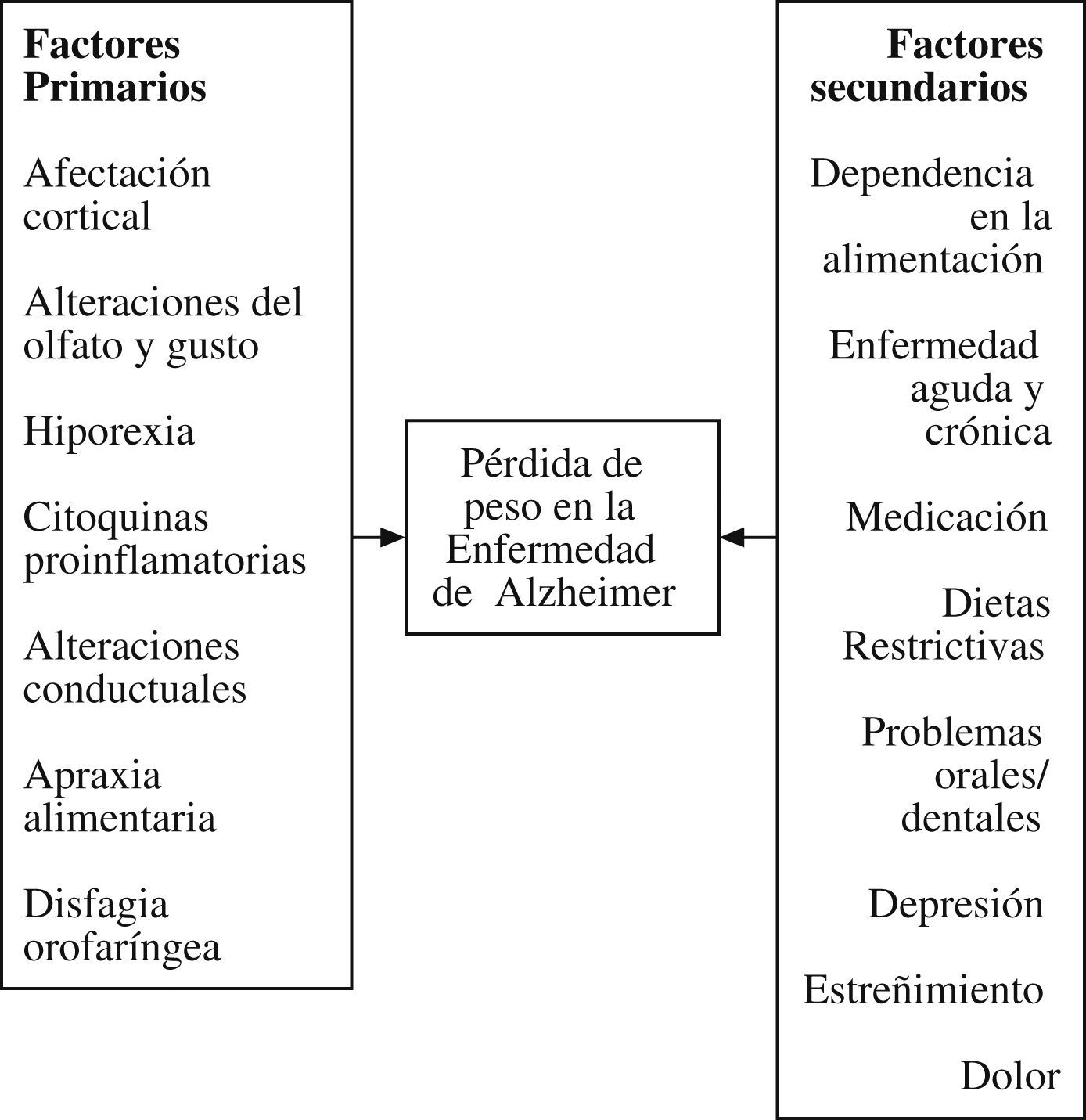
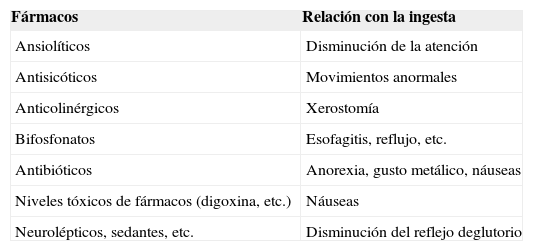
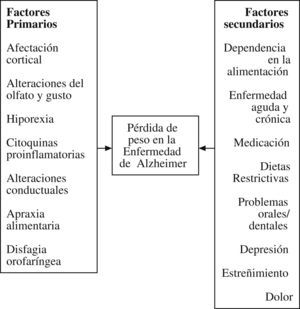
Pérdida ponderal y demenciaEn la EA, la pérdida ponderal está habitualmente presente desde los primeros estadios9, interviniendo factores tan dispares como la atrofia del córtex temporal mesial, los mayores requerimientos energéticos, el hiperinsulinismo con resistencia insulínica o la disminución de neurotrasmisores orexígenos como el neuropéptido Y o la norepinefrina10. Los factores primarios y secundarios más importantes se recogen en la figura 2. La medicación debe ser revisada sistemáticamente, pues son muchos los fármacos y las interacciones que pueden condicionar la ingesta. Algunos de los más representativos se detallan en la tabla 1. Especial relevancia tiene la medicación sedante por su frecuente utilización en estos pacientes y por los efectos depresores del reflejo deglutorio. Es necesario descartar, a su vez, la presencia de síntomas asociados, como depresión, estreñimiento o dolor y valorar el uso de medicación específica, incluidos agentes orexígenos a pesar de su discutida eficacia11,12.
Fármacos que pueden interferir con la ingesta
| Fármacos | Relación con la ingesta |
| Ansiolíticos | Disminución de la atención |
| Antisicóticos | Movimientos anormales |
| Anticolinérgicos | Xerostomía |
| Bifosfonatos | Esofagitis, reflujo, etc. |
| Antibióticos | Anorexia, gusto metálico, náuseas |
| Niveles tóxicos de fármacos (digoxina, etc.) | Náuseas |
| Neurolépticos, sedantes, etc. | Disminución del reflejo deglutorio |
Muchos pacientes con demencia son atendidos en el entorno familiar. En los primeros estadios, a la preocupación de la pérdida de peso y apetito, se suma la de las alteraciones conductuales, como la seguridad, el rechazo a la comida o el olvido de comer. En estadios más avanzados aparecen la apraxia y la disfagia. En un estudio sobre 241 pacientes en domicilio, la mitad con demencias en estadio Global Deterioration Scale (GDS) 6 o superior, Botella y Ferrero13 observaron que el 98% tenía alimentación oral, el 66% precisaba ayuda para comer, y el 40% tomaba dieta triturada con una disfagia a sólidos del 26% y a líquidos del 19%. La pérdida ponderal era del 31% y se correlacionaba con la evolución de la demencia. Al igual que otros autores14, destacan la falta de conocimiento sobre la disfagia y su manejo.
En otras muchas ocasiones, estos pacientes deben ser atendidos en centros geriátricos, donde la prevalencia de la demencia alcanza el 60%, especialmente entre los usuarios de plazas asistidas15. Utilizando la escala GDS complementada con la Functional Assessment Staging (FAST) y la Eating Behaviour Scale (EBS)16 para evaluar la conducta alimentaria, estudiamos las alteraciones de conducta en un colectivo de 143 pacientes institucionalizados con demencia de etiología diversa, encontrando alteraciones del apetito y de la alimentación en 26 casos (18,2%). A medida que progresaba la demencia con empeoramiento cognitivo y funcional, la conducta alimentaria se encontraba más deteriorada y afectaba al 77% de los residentes en estadios GDS-FAST 6 y 7. El 40% de los pacientes en estadio GDS-FAST 6 tenían atragantamientos al igual que el 66% de pacientes con GDS-FAST 717. Estos datos son similares a los hallados en la literatura1,6,8 y remarcan la desestructuración progresiva de la alimentación en la demencia.
Sensibilización con el problemaComer es la actividad más frecuente de cualquier centro geriátrico, siendo muy tranquilizador para cuidadores y familiares que el paciente realice una ingesta adecuada. La alimentación debe siempre pretender ser placentera a la vez que nutritiva y en las personas con demencia también, intentando que mantengan el gusto por la comida y el reflejo deglutorio, aunque precisen ayuda o suplencias. La rutina puede hacer olvidar las premisas básicas de una correcta alimentación para estos pacientes. Un ambiente adecuado en el comedor18, disponer de personal suficiente, invertir tiempo en dar la comida19 y la interrelación cuidador-paciente mejoran el balance energético de la ingesta. La atención individual y la formación de personal se han demostrado determinantes para un correcto registro de las ingestas, mejorando el aporte calórico y la hidratación de los mayores residenciados, tanto en la toma de dietas basales como de suplementos orales20–22. Estos objetivos exigen sensibilización en la dirección del centro y concienciación de trabajadores y familiares, para que, con una correcta formación, ayuden a mejorar el estado nutricional del paciente y podamos identificar las alteraciones en la conducta alimentaria de forma temprana.
Identificación precozEscalas de conducta alimentaria como la EBS o la escala de Blandford23 son útiles como seguimiento del problema, pero para la identificación temprana lo más importante es la observación directa. Los signos más sugestivos de disfagia son aumento del tiempo necesario para la ingesta, dificultad en el manejo de las secreciones, tiempo de masticación o preparación oral prolongado, retención de alimento en la cavidad oral, tos (antes, entre o después de la deglución), voz húmeda y atragantamientos. Estas observaciones deben llevarnos a iniciar, de forma práctica, el estudio de disfagia y el análisis de las modificaciones que se puedan emplear en la mejora de la deglución. Junto con el examen físico y la evaluación del estado nutricional, la prueba de referencia es el test de volumen-viscosidad.
Test de volumen-viscosidadEs un test sencillo, que puede realizarse en cualquier recurso asistencial, basado en la administración de bolos de volúmenes (de 5 a 20ml) y consistencia variables (viscosidad líquida, néctar y pudding)2,24. Así podemos observar si quedan restos del alimento en la cavidad oral y/o con qué volumen y viscosidad del bolo se producen reacciones como cambios en la voz, tos o atragantamientos. La prueba se completa con el control de la saturación de oxígeno en sangre periférica y, en centros especializados, con la monitorización del paciente. Con personal entrenado, el test tiene una sensibilidad diagnóstica para las alteraciones de la seguridad y la eficacia de la deglución del 88,1 y el 89,8%, respectivamente. Además, desde un punto de vista práctico, identifica adecuadamente a los pacientes con alteraciones de la seguridad de la deglución a los que es necesario restringir la viscosidad líquida y ofrece datos acerca del tipo de bolo (volumen y viscosidad) más adecuado para cada paciente.
En la atención de la demencia avanzada es muy útil consensuar entre familiares y equipo asistencial los niveles de intensidad terapéutica que aplicaremos en cada paciente25. Los pacientes con demencia avanzada que presentan disfagia están mayoritariamente en los estadios GDS-FAST 6 y 7, en los que los niveles de intensidad terapéutica serán el nivel 4 (tratamiento conservador en centro sanitario) o nivel 5 (cuidados de confort). A pesar de que en el estudio reglado de la alteración en la seguridad de la deglución se recomienda una prueba de videofluoroscopia3,26,27, a nuestro juicio, la mayoría de estos pacientes no serían candidatos a esta prueba.
Estrategias para mejorar la alimentación en demencias avanzadas con disfagiaSiguiendo los objetivos generales de mejorar el estado nutricional con una deglución más segura y eficiente, las estrategias generales se basan en 5 puntos: tratamiento postural, variaciones en el volumen/viscosidad de la dieta, estrategias de incremento sensorial oral, tratamiento de las praxias neuromusculares y maniobras deglutorias específicas3. Las estrategias más sencillas de aplicar en cualquier recurso asistencial son las primeras, quedando las 2 últimas más reducidas al tratamiento rehabilitador específico.
Modificaciones ambientales y posturalesEl ambiente del comedor, la interacción del personal y el tiempo dedicado a la alimentación condicionan la ingesta de los residentes19,28. De forma general, habrá que cuidar con esmero la higiene oral, cuidando dientes y prótesis, preservando la integridad de mucosas, labios y comisuras. Para minimizar los riesgos, el ambiente del comedor debe ser relajado, con el cuidador sentado a la misma altura que el paciente, utilizando un lenguaje verbal y corporal adecuado para iniciar con paciencia la alimentación. Las normas básicas para recordar son las siguientes:
PosturaEs conveniente colocar al paciente en sedestación, 30min antes de la ingesta, en posición cómoda, con ligera flexión de la cabeza hacia delante. En las demencias con inestabilidad postural cefálica, hay que impedir hiperextensión del cuello con un soporte adecuado para la cabeza. En caso de encamamiento, hay que elevar el cabezal de la cama 90° y mantener las mismas recomendaciones para la cabeza1,29. En caso de hemiplejia, inclinar la cabeza hacia el lado parético. Al finalizar la ingesta, mantener al paciente 30’ en sedestación.
Cómo dar la alimentaciónEs preferible utilizar cucharas que jeringas, pues permiten observar la deglución y la presión en la lengua estimula el reflejo deglutorio. La cuchara debe acercarse desde abajo y colocarse en medio de la boca empujando la lengua hacia abajo para evitar que retroceda hacia el interior. Se deben administrar cantidades pequeñas cada vez, evitando que se acumulen alimentos en la boca y procurando que no hable mientras esté comiendo. Dejaremos tiempo suficiente para la deglución, masajeando la mandíbula o haciéndole imitar nuestros gestos si no abre la boca o no mastica. Después de cada deglución, conviene animarle a que tosa y asegurarnos de que la boca está vacía antes de administrar de nuevo el alimento. Si aparece tos con la deglución, hay que detener la alimentación. Es preferible evitar las pajitas y utilizar vasos bajos de boca ancha. Hay que prestar especial atención a la presencia de grumos, pieles, etc, que pueden quedar en los purés. Recordar también que los sabores ácidos y los alimentos fríos estimulan el mecanismo de la deglución3,30,31.
Modificaciones en la dietaLos cambios en la dieta, siguiendo las referencias anteriores, van encaminados a mejorar la hidratación y nutrición con una deglución más segura y a evitar complicaciones como la broncoaspiración. En la medida de lo posible, debemos esforzarnos en preparar unas dietas que sean variadas y atractivas, asegurando a la vez el aporte adecuado de todos los grupos de alimentos, que combinen las necesidades de seguridad del paciente con el mantenimiento del tradicional gusto por la comida. La degeneración del córtex sensitivo y la alteración mnésica, entre otras alteraciones, impiden que estos pacientes puedan disfrutar plenamente de una comida tradicional. Sin embargo, cuando potenciamos los sabores, variamos la composición y la presentación de los platos, no sólo intentamos actuar sobre el disminuido apetito del paciente, sino también establecer un compromiso con el equipo asistencial y la familia, quienes, al ver la variación y esmero en los menús, comprueban nuestra sensibilidad con el problema, resultando una mayor motivación por la alimentación e implicación en el cuidado. Como norma general, se deben evitar alimentos con consistencias diferentes (sopas de pasta, leche con cereales), alimentos pegajosos (miel, chocolate), fibrosos (piña, espárragos, jamón), frutas o verduras con piel o pepitas (uvas, fresas, kiwis, tomate, etc.), alimentos que producen sialorrea (caramelos) o que desprendan agua o zumo al morderse o aplastarse30,31. Las raciones deben ser más pequeñas y, teniendo en cuenta que el tiempo de deglución está aumentado en 2–4 veces, hay que programar más tomas que no excedan de los 45min repartidas a lo largo de las 24h. Las principales alternativas para la modificación de la textura de los alimentos son:
- •
Triturado de alimentos sólidos (dieta triturada)/productos liofilizados
- •
Empleo de modificadores de textura: espesantes, gelatinas, etc.
- •
Enriquecedores de la dieta: alimentos, módulos, suplementación, etc.
Es frecuente que se convierta en una dieta monótona, hipocalórica, cuya trituración no es óptima y que no motiva a quien la prepara, la sirve ni a quien debe comerla. Lo habitual en estas fases de la demencia es que sean de consistencia miel (como el yogur batido; viscosidad: 351–1.750cP) o consistencia pudding (sólo pueden tomarse con cuchara; viscosidad: >1.751cP). Debe incluir alimentos que aporten agua y fibra (frutas y verduras), que cubran las necesidades proteicas (carnes, pescado, huevos) junto con ingredientes que ayuden a que la mezcla sea homogénea y de textura adecuada (féculas, legumbres, etc.). El aporte calórico puede enriquecerse añadiendo diversos ingredientes, como aceite de oliva, mantequilla, nata, queso o leche32. Los ingredientes diferentes pueden tener tiempos de cocción distintos y en este caso conviene cocer los alimentos de forma separada. El triturado debe ser homogéneo, evitando especialmente la presencia de grumos y espinas. Puede ser necesario triturar de forma separada y/o utilizar un pasapurés después de la batidora. Debemos cuidar las características organolépticas, variando los ingredientes que influirán no sólo en la textura y la consistencia, sino que serán los responsables también del color, el aroma y el sabor final del plato.
Organización de la dieta trituradaEl aporte energético propuesto es de 1.800–2.000Kcal/24h, con la siguiente distribución: desayuno (30%), comida (25%), merienda (10%), cena (hasta el 35%). Esta variación sobre la distribución energética habitual viene motivada por el prolongado ayuno nocturno y el aumento de apetito de estos pacientes por la mañana33,34. Las cantidades han de ser pequeñas, por lo que debemos intentar aumentar el aporte energético en cada toma.
DesayunoEs la toma que rompe el ayuno nocturno. Para conseguir aportar el 30% de la energía diaria, las papillas de cereales comerciales facilitan este objetivo. En su elaboración hay que ser cuidadosos con la temperatura de la leche, las proporciones y el tiempo de espera entre elaboración e ingesta, trabajando la disolución del cereal para evitar la formación de grumos. Se puede completar la toma con zumos espesados o gelatinas enriquecidas con lácteos.
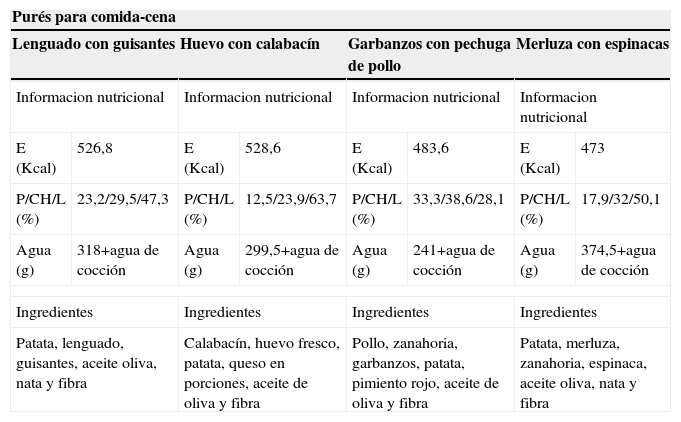
Comida-cenaLos alimentos deben ser variados, de forma que sus características organolépticas queden realzadas y se note. El plato principal puede ser un puré de elaboración propia o un puré comercial. En nuestra opinión, la base deben ser los alimentos naturales siempre que sea posible. Se puede completar la toma con gelatinas y frutas o lácteos, bien de elaboración propia o en preparaciones comerciales. En la tabla 2 se recogen distintos ejemplos de purés, postres, gelatinas enriquecidas y batidos de fruta con su valoración nutricional.
Platos de dieta triturada con su valoración nutricional
| Purés para comida-cena | |||||||
| Lenguado con guisantes | Huevo con calabacín | Garbanzos con pechuga de pollo | Merluza con espinacas | ||||
| Informacion nutricional | Informacion nutricional | Informacion nutricional | Informacion nutricional | ||||
| E (Kcal) | 526,8 | E (Kcal) | 528,6 | E (Kcal) | 483,6 | E (Kcal) | 473 |
| P/CH/L (%) | 23,2/29,5/47,3 | P/CH/L (%) | 12,5/23,9/63,7 | P/CH/L (%) | 33,3/38,6/28,1 | P/CH/L (%) | 17,9/32/50,1 |
| Agua (g) | 318+agua de cocción | Agua (g) | 299,5+agua de cocción | Agua (g) | 241+agua de cocción | Agua (g) | 374,5+agua de cocción |
| Ingredientes | Ingredientes | Ingredientes | Ingredientes | ||||
| Patata, lenguado, guisantes, aceite oliva, nata y fibra | Calabacín, huevo fresco, patata, queso en porciones, aceite de oliva y fibra | Pollo, zanahoria, garbanzos, patata, pimiento rojo, aceite de oliva y fibra | Patata, merluza, zanahoria, espinaca, aceite oliva, nata y fibra | ||||
| Hidratación y postres | |||||||
| Gelatina | Postre cremoso | Batido frutas tipo 2 | Natillas caseras tipo 1 | ||||
| Informacion nutricional | Informacion nutricional | Informacion nutricional | Informacion nutricional | ||||
| E (Kcal) | 85 | E (Kcal) | 104,6 | E (Kcal) | 159,9 | E (Kcal) | 300,8 |
| P/CH/L (%) | 23/42/31 | P/CH/L (%) | 15/36/48 | P/CH/L (%) | 13,3/61,7/24,9 | P/CH/L (%) | 9,3/66/24,4 |
| Agua (g) | 90 | Agua (g) | 88,9 | Agua (g) | 275,77 | Agua (g) | 88,9 |
| Ingredientes | Ingredientes | Ingredientes | Ingredientes | ||||
| Yogur sabor, agua, fibra y gelatina | Preparado comercial en polvo y leche entera | Pera natura, leche entera, pan tostado integral, pera deshidratada y agua | Leche entera, polvo para flanes y azúcar | ||||
| Platos para celebraciones | |||||||
| Alubia blanca con paté | Hongos con carrilleras de ternera | Copa “Noche y día” | Gelatina de “Naranja dulce” | ||||
| Informacion nutricional | Informacion nutricional | Informacion nutricional | Informacion nutricional | ||||
| E (Kcal) | 334,9 | E (Kcal) | 352,9 | E (Kcal) | 278,04 | E (Kcal) | 232,13 |
| P/CH/L (%) | 19,3/44,7/35,7 | P/CH/L (%) | 34,1/22,1/43,9/ | P/CH/L (%) | 18,53/55,2/28,32 | P/CH/L (%) | 17,23/69,96/14,34 |
| Agua (g) | 163,3+agua de cocción | Agua (g) | 318,7+agua de cocción | Agua (g) | 175,75 | Agua (g) | 146 |
| Ingredientes | Ingredientes | Ingredientes | Ingredientes | ||||
| Zanahoria, alubia blanca, calabaza, paté, cebolla, aceite de oliva, fibra y ajo | Carrillera de ternera, hongos, patata, calabacín, aceite de oliva y fibra | Yogur de coco, suplemento nutricional sabor chocolate y gelatina | Postre lácteo sabor chocolate, suplemento nutricional sabor naranja y gelatina | ||||
El tiempo que transcurre entre las tomas principales es corto por lo que el aporte no ha de ser elevado. Es una buena ocasión para la hidratación y la introducción de frutas, bien sea con zumos espesados, gelatinas enriquecidas, compotas o batidos de fruta. Lo ideal sería utilizar frutas naturales, pero la dedicación que requiere el pelado, troceado y triturado es alta. Una alternativa es el uso de fruta deshidratada que, aunque aporta una variedad de frutas menor, permite elaborar batidos con grandes cantidades de líquidos y conseguir la textura deseada.
HidrataciónLo habitual es utilizar líquidos espesados o aguas gelificadas. Debemos aportar hidratación tanto en las tomas principales como a media mañana y merienda. Hay que procurar que la hidratación sirva también para proporcionar aporte energético, utilizando, por ejemplo, gelatinas enriquecidas con lácteos o postres cremosos, como se señala en la tabla 2.
FestividadesLa disfagia no tiene necesariamente que impedir una comida especial en una celebración. Gracias a la motivación y la creatividad de los profesionales de la cocina, hemos podido realizar algunos platos diferentes que han permitido elevar la calidad de nuestra oferta y aumentar la satisfacción de cuidadores y familiares (tabla 2). En la elaboración de estos postres hemos empleado productos tradicionales y suplementos comerciales. Hay multitud de combinaciones atractivas y nutritivas que se pueden utilizar de forma sencilla, como las que se pueden consultar en portales específicos35.
SuplementaciónEn la demencia avanzada concurren la gran mayoría de las características del perfil de riesgo de malnutrición para usuarios de centros geriátricos36 (mayor edad, pérdida de autonomía en las actividades de la vida diaria (AVD), alteraciones cognitivas, dejar más del 25% en la mayoría de las comidas, polifarmacia, etc.). Cuando comprobamos la cantidad de alimento ingerido por estos usuarios, a pesar de todas las modificaciones e implicación del personal, con relativa frecuencia observamos que dista mucho de la ingesta calórica deseada porque el verdadero problema al que tenemos que hacer frente es que estos pacientes se tomen lo que les ponemos en el plato. Esta situación obliga a utilizar dietas enteras como suplementos nutricionales para tratar de alcanzar el aporte energético planteado.
¿Y la disfagia? Las dietas enterales se comercializan en presentaciones líquidas, como batidos, para que sean financiables por los Servicios de Salud. En el caso de las demencias avanzadas con disfagia orofaríngea, la textura indicada sería la consistencia pudding, pero la inclusión de estos suplementos supondría un problema de financiación para la familia o para el centro geriátrico. En nuestro centro hemos visto la posibilidad de utilizar la gelatina comercial de cola de pescado, como vehículo espesante de las dietas enteras comerciales, ya que el uso de otros sistemas espesantes que pudieran ser útiles para uso individual, pierden su viabilidad, a nuestro entender, para un uso colectivo. Las pruebas realizadas aseguran una textura correcta, utilizando suplementos de 2Kcal/ml, con una amplia variedad de sabores y con seguridad bacteriológica durante 5 días si se conserva en frigorífico (4°C)37.
Los suplementos permiten completar una oferta de dieta triturada que combina lo tradicional y lo comercial, mejorando la variedad y la riqueza nutritiva, lo que es muy bien valorado por el personal cuidador y los familiares.
Uso de sondas de alimentaciónA medida que la alimentación se desestructure, el equipo asistencial que atienda a pacientes con demencia tendrá que abordar en cada estadio evolutivo las modificaciones de la dieta y la vía de alimentación. El razonamiento básico para utilizar una sonda es salvar el “obstáculo” orofaríngeo con una deglución más segura, que mejore la situación nutricional del paciente, evite las úlceras por presión, las neumonías aspirativas, ofreciendo más confort y supervivencia al paciente. La implantación de una sonda nasogástrica o de una gastrostomía percutánea endoscópica (PEG), aun siendo una técnica relativamente sencilla, no está exenta de complicaciones, incomodidades y servidumbres38,39. El perfil de la indicación de sonda de alimentación ha cambiado40, habiendo aumentado progresivamente el número de pacientes con demencia avanzada38,40,41, unas veces siguiendo el algoritmo de estudio de la disfagia3 y otras como la alternativa que el avance científico puede ofrecer para mejorar la calidad de vida y las complicaciones de la disfagia en estos pacientes42.
Diversos autores cuestionaron la efectividad de esta medida en los pacientes con demencia, pero fue el trabajo de Finucane, publicado en 1999 en JAMA43, el que más difusión alcanzó, demostrando que esas expectativas no se cumplían con el uso de sondas de alimentación, produciendo además efectos indeseados derivados de la técnica de colocación, manejo y evolución. A los riesgos de la técnica había que sumar la incomodidad para el paciente y sus familiares, la presencia de alteraciones conductuales, como agitación, y el mayor uso de restricciones físicas.
Desde entonces, son legión los trabajos que señalan la falta de evidencia científica en la mejora de la supervivencia, el estado nutricional, la prevención o la cura de úlceras por presión y la prevención de neumonías por aspiración1,6,8,39,44–51 en pacientes con demencia avanzada alimentados por sonda.
Estado nutricionalLa pérdida ponderal está presente desde estadios tempranos en la demencia, aun cuando los pacientes mantienen su capacidad deglutoria intacta9. A pesar de la progresión de la enfermedad, muchos pacientes mantienen una capacidad de deglución suficiente para no perder peso. Incluso con bajo peso corporal y demencia avanzada pueden sobrevivir por largos períodos de tiempo43,52. La alimentación oral con las modificaciones oportunas es un alternativa viable en la demencia avanzada y aconsejada por distintos autores, tanto en el domicilio como en los pacientes institucionalizados1,47,49,52. A modo de ejemplo, en nuestro centro, entre 24 pacientes con demencia avanzada (estadios 6d y 7) con alimentación oral, no encontramos valores de índice de masa corporal (IMC) indicativos de desnutrición y 5 casos (20,9%) presentaban un IMC entre 18,5 y 22 correspondiente a peso insuficiente.
La preocupación por el estado nutricional del paciente con demencia no debe plantearse cuando aparece la disfagia, sino que hay que prestarle atención durante toda la evolución de la enfermedad, tomando en cada fase las acciones oportunas.
Con las sondas de alimentación no se consiguió mejorar el estado nutricional o sus consecuencias. Por eso, la guía ESPEN de nutrición enteral en pacientes geriátricos53 considera “no indicado” el uso de sondas de alimentación la fase final de la demencia. En la aparición o curación de úlceras por presión, que podríamos deducir como secundarias al mal estado nutricional, tampoco se encontraron evidencias de mejoría46.
SuperivenciaRimon et al ponen de manifiesto que la demencia avanzada es un grupo heterogéneo54. En estadios GDS-FAST 6 y 7 encontraron una supervivencia de 161 días, con peor pronóstico si eran varones, con edad superior a 80 años, con comorbilidad, diabetes o demencia vascular. Skelly40 señala la escasa supervivencia o la deteriorada situación funcional del paciente muy anciano y frágil, muchos de ellos con demencias avanzadas, tras la implantación de una PEG. Meier55, estudiando un grupo de demencias en estadios comprendidos entre 6d y 7F, no encontró diferencias de supervivencia entre los alimentados por sonda o de forma oral. En el estudio realizado en pacientes en estadios 7A o superiores por Alvarez-Fernández et al56, no sólo no encuentran más supervivencia en los pacientes con sonda de alimentación, sino que la alimentación por sonda era un factor pronóstico independiente de mortalidad al igual que la hipoalbunemia o la neumonía en el último año. Revisiones posteriores45,48,51 confirman que en este tipo de pacientes, la alimentación por sonda no mejora la supervivencia.
Broncoaspiración y disfagiaSon muchos los factores generales asociados con la penetración de material digestivo a la vía aérea. Entre ellos se citan la medicación sedante o el nivel de conciencia, patologías como la insuficiencia cardíaca, la enfermedad pulmonar obstructiva crónica (EPOC) el mal estado de las piezas dentales, el deterioro funcional severo y la pérdida ponderal mayor al 8%57.
Los trastornos de deglución, expresados clínicamente como imposibilidad de toma oral de la medicación, alimentación oral con necesidad de modificación de texturas y alimentación por sonda, son por sí mismos factores independientes asociados a la neumonía en pacientes con demencia1,6,57. La gravedad de la disfagia se ha clasificado clínicamente en función de la frecuencia y el volumen de la aspiración y el reflejo tusígeno31. Sin embargo, no existe una correlación entre la severidad de la aspiración clínica ni en la observada en la videofluoroscopia, ya que además del volumen aspirado influyen otros factores, como el grado funcional, la resistencia del huésped y la patogenicidad de los microorganismos aspirados6,57. La especificidad del test de volumen/viscosidad disminuye para identificar la penetración del bolo en la laringe y para la aspiración. Sin embargo, su alta sensibilidad y especificidad para identificar pacientes con disfagia que mejorarán con el aumento de la viscosidad del bolo lo convierten en una herramienta de gran ayuda.
El uso de sondas nasogástricas o PEG no disminuyó la presencia de neumonías en pacientes con demencia y propició un aumento de la flora patógena bucal1,6,57,58. La aspiración pulmonar, a pesar de las sondas de alimentación, ha llamado la atención también de la medicina intensiva. En pacientes intubados se encontraron restos de pepsina en las secreciones traqueales. Se postula que el reflujo gastroesofágico y la penetración de secreciones orofaríngeas serían las causas más probables1,45.
¿Por qué colocamos una sonda de alimentación?A pesar de la falta de evidencia sobre su beneficio, el número en la demencia avanzada es elevado1,38,41. Se han invocado factores económicos, ya que la preparación de las comidas para estos pacientes ha de ser cuidadosa, el tiempo de administración es más largo y se precisa más personal, lo que encarece un cuidado residencial si lo comparamos con una alimentación enteral por sonda, lo que determinados sistemas sanitarios por distintas vías favorecen48,54,59.
Pero hay causas más de fondo que pueden estar basadas en factores sociales, creencias personales, religión etc.60,61. Cualquier persona asume el cáncer como una enfermedad terminal, lo que no ocurre con la demencia, que se ha contemplado como una enfermedad banal (cosas de la edad) o como una enfermedad de curso muy largo que hace difícil asumir que ha llegado a un estadio final. El lenguaje que utilizamos no siempre ayuda cuando usamos términos como “life-sustaining” (soporte vital) para referirnos a medidas de prolongar la vida (life-prolonging), que no siempre se adecuan a la intensidad terapéutica de una enfermedad en fase final. Aun en estos casos, la ambivalencia es común entre familiares y cuidadores, de tal forma que retirar una sonda se convierte en una decisión más difícil que la de su implantación61,62. En la implantación de sondas influyen poderosamente tanto las propias creencias y convicciones de los cuidadores como la comprensión y la actitud médica y el modelo de final que planteemos a la familia. Podemos hacer una lectura puramente tecnológica de la enfermedad, viendo sólo la necesidad de salvar un obstáculo (disfagia) o hacer llegar los nutrientes a un determinado órgano, sin contemplar el conjunto de la persona y de su enfermedad60,63. En este mismo número de la revista, Duaso et al hacen un acertado análisis de la aplicación de los principios de la bioética en la demencia avanzada.
Nuestra formación en cuidados paliativos sigue siendo escasa, lo que favorece que no reconozcamos una enfermedad final y nos desenvolvamos con soltura en la demencia avanzada64–66. Así, es fácil que informemos de que la “alternativa tecnológica” que podemos ofrecer es una sonda de alimentación y dejemos en manos de la familia una decisión que, además de técnicamente correcta, debería contemplar la situación global, la dignidad y el confort del paciente, las dudas de los familiares y, además, debería respetar las voluntades del paciente, lo que no siempre ocurre40,67,68.
Monteloni y Clark69 comprobaron que la formación y apoyo al personal sanitario (médicos incluidos) en la alimentación y cuidados paliativos del paciente con demencia avanzada propició un cambio en la cultura del hospital, reduciendo el n.o de sondas en 1 año a la tercera parte y en los pacientes con demencia avanzada a la quinta parte. La mitad de las sondas colocadas en demencias avanzadas lo fueron contra la voluntad de los pacientes previamente expresada. Recientemente, un equipo de enfermeras de nutrición clínica revisaron 88 pacientes con indicación médica de sonda nasogástrica por disfagia orofaríngea. Tras la adaptación de la dieta según el test de volumen-viscosidad, sólo 6 precisaron sonda de alimentación70. Estos datos indican que puede haber un planteamiento rutinario en ciertos casos que no se corresponde con el estudio de las alternativas posibles antes de la toma de decisión y resaltan la gran importancia de la enfermería en el cuidado integral de estos pacientes71. En nuestra opinión, la alimentación oral es una alternativa válida y viable en estos pacientes, que aporta una mayor gratificación, sociabilidad y confort al usuario, estrechando la relación con cuidadores y familia. Negar la alimentación oral en un paciente con demencia avanzada y disfagia debería ser extraordinario y siempre sustentado en una valoración integral de la situación, en los deseos previamente expresados y en la información veraz sobre las evidencias científicas de las alternativas47–49. Por eso, la Asociación Americana de Alzheimer72 no recomienda el uso de sondas en estos pacientes, aunque lo contempla como una opción que se debe tomar conscientes de la falta de beneficios. Algunos autores, aun primando siempre la alimentación oral cuidadosamente adaptada, han recomendado un uso restringido y puntual de las sondas. Por ejemplo, cuando la causa de la disfagia no está relacionada con la evolución de la demencia y no es abordable por otros medios (p. ej.: cirugía en una estenosis esofágica) y el paciente no esté en fase final de la enfermedad. También podría ser útil en situaciones puntuales, como una fractura de cadera, retomando la vía oral lo antes posible6,39.
Como actitud general, creemos que hay que abordar el estado nutricional del paciente con demencia desde las fases iniciales y no cuando la disfagia está presente. La familia precisa una correcta información basada en las evidencias científicas con alternativas para cada situación y no un planteamiento rutinario de alimentación artificial. Una alimentación oral cuidadosamente adaptada y administrada nos parece una alternativa viable y la más adecuada para la disfagia de los pacientes con demencia en fase avanzada.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.