REVISION
Rev Esp Geriatr Gerontol 1998;33(4):236-245
Actualización sobre la eficacia, indicaciones, formas de administración y control de la oxigenoterapia crónica domiciliaria
Ana Vena Martínez*, Jesús Pérez del Molino* y Jorge Castelao Naval**.
* Sección de Geriatría. ** Sección de Neumología. Hospital General Universitario de Guadalajara.
RESUMEN
La oxigenoterapia crónica domiciliaria es un tratamiento con importantes implicaciones clínicas y sociales para el paciente y económicas para el Sistema Nacional de Salud. Presenta importantes variaciones en su prevalencia tanto a nivel internacional como en nuestro país, por lo que es necesario un adecuado conocimiento por parte del médico de sus criterios de indicación y control, así como por parte del paciente de la necesidad de un correcto cumplimiento. Las indicaciones son una PaO2 <55 mm Hg o una PaO2 entre 55 y 59 mm Hg cuando coexiste hipertensión pulmonar, poliglobulia, cor pulmonale o alteraciones de ritmo cardiaco. La prescripción se debe realizar en situación clínica y funcional estable y es necesario un seguimiento periódico del paciente. El principal beneficio de la oxigenoterapia crónica domiciliaria es un aumento de la supervivencia a largo plazo. Existen diversas fuentes de suministro y liberación de oxígeno al paciente, siendo en la actualidad de elección el concentrador de oxígeno y las gafas nasales.
Palabras clave
Oxigenoterapia domiciliaria. EPOC. Insuficiencia respiratoria crónica. Gasometría arterial.
Update of the effectiveness, indications, forms of administration, and control of long-term oxygen therapy
SUMMARY
Regular at-home oxygen therapy has important clinical and social implications for patient and economic implications for public health systems. Its use varies widely internationally and in Spain, so physicians should be aware of the criteria for use and control and patients should be aware of the need for correct compliance. The indications are PaO2 <55 mm Hg, or PaO2 55-59 mm Hg when pulmonary hypertension, polyglobulia, cor pulmonale, and cardiac rhytm abnormalities exist. The prescription should be made with the patient in a stable clinical and functional situation and periodic follow-up is required. The main benefit of regular at-home oxygen therapy is increased long-term survival. Various sources of oxygen supply and release exist, but the oxygen concentrator and nasal tubes currently are of choice.
Key words
At-home oxygen therapy. OCPD. Chronic respiratory failure. Arterial gasometry.
INTRODUCCIÓN
La oxigenoterapia crónica domiciliaria (OCD) constituye un tratamiento sustitutivo de la insuficiencia respiratoria crónica (IRC) en pacientes con enfermedad pulmonar obstructiva crónica (EPOC). Por extensión, aunque no existen estudios que demuestren su eficacia, se aplica también a pacientes en situación de IRC secundaria a otras etiologías.
A pesar de existir criterios de indicación bien establecidos y ampliamente aceptados (1-3), la prevalencia de OCD varía significativamente tanto en el ámbito internacional (tabla I) como en nuestro propio país (tabla II). Esto traduce, más allá de la distinta prevalencia de EPOC, una escasa uniformidad en el tratamiento y control de este tipo de pacientes.
| Tabla I. Prevalencia internacional de oxigenoterapia crónica domiciliaria* | |
| País | Prevalencia** |
| Taiwan | 1,5 |
| Corea | 1,7 |
| Suecia | 15 |
| Japón | 19 |
| Reino Unido | 20 |
| Finlandia | 21 |
| Francia | 26 |
| Australia | 43 |
| Canadá | 60 |
| Estados Unidos | 241 |
| * Modificado de O''Donohue y Plummer (4). ** Por 100.000 habitantes. | |
| Tabla II. Prevalencia de oxigenoterapia crónica domiciliaria en España* | |
| Ámbito | Prevalencia** |
| Navarra | 28 |
| Barcelona | 38 |
| Valencia | 67 |
| País Vasco | 70 |
| Madrid | 109 |
| Castilla-León | 116 |
| * Modificado de Escarrabill (5). ** Por 100.000 habitantes. | |
La OCD genera un importante gasto sanitario. En 1994, y sólo en el territorio del INSALUD (40% de la población española), el gasto generado por la OCD fue de aproximadamente 5.000 millones de pesetas (6). En España el coste es asumido por el Sistema Nacional de Salud y desembolsado directamente por el Hospital de referencia donde se realiza la indicación. El precio de la OCD varía según la Comunidad Autónoma y la empresa suministradora. En la Comunidad de Castilla-La Mancha el precio por paciente y día, en 1996, era de 529 pesetas para el cilindro de presión, 556 pesetas para el concentrador y 1.322 pesetas para el oxígeno líquido.
El índice de prescripciones correctas presenta también amplias variaciones (50-90%) (3, 7). En general los neumólogos prescriben correctamente la OCD con mayor frecuencia que el resto de especialistas o los médicos generales (8).
Por otra parte, diversos estudios han puesto de manifiesto que sólo el 40-60% de los pacientes cumplen correctamente las horas prescritas de oxigenoterapia (9, 10), lo que impide alcanzar los objetivos perseguidos pese al gasto generado.
De lo anterior se deduce la necesidad de un adecuado conocimiento de los criterios de indicación y de las normas de seguimiento y control de los pacientes con OCD, la conveniencia de informar al paciente sobre los objetivos perseguidos y la importancia de un correcto cumplimiento, así como la necesaria existencia de mecanismos que identifiquen a los pacientes no cumplidores.
MECANISMOS COMPENSADORES DE LA HIPOXIA
La respuesta fisiológica a la hipoxia implica la puesta en marcha de una serie de mecanismos que se pueden resumir en los siguientes:
a) Hiperventilación.
b) Vasodilatación del lecho vascular en los tejidos hipoxémicos y aumento del gasto cardíaco.
c) Vasoconstricción de las arteriolas precapilares pulmonares en respuesta a la hipoxia alveolar, con el objetivo de mejorar la relación ventilación/perfusión en las zonas pulmonares afectadas.
d) Si la hipoxemia es crónica, aumento de la producción renal de eritropoyetina, con el fin de aumentar la masa eritrocitaria y consecuentemente la capacidad de transporte de oxígeno por la sangre.
e) Aumento del 2-3-difosfoglicerato eritrocitario, lo que desplaza a la derecha la curva de disociación de la hemoglobina y disminuye la afinidad de ésta por el O2, favoreciendo su liberación a los tejidos.
Los mecanismos anteriores intentan mantener un adecuado aporte de oxígeno a los tejidos, pero en situación de hipoxemia crónica el aumento del gasto cardíaco y, sobre todo, la vasoconstricción pulmonar mantenida pueden producir cambios estructurales en la pared vascular pulmonar con aumento del espesor del músculo liso en la capa media. Estos trastornos se manifiestan clínicamente como hipertensión arterial pulmonar y cor pulmonale. También la poliglobulia puede tener efectos hemodinámicos negativos al aumentar la viscosidad sanguínea e incrementar el trabajo miocárdico.
La hipoxemia produce un efecto deletéreo sobre las funciones neuropsíquicas, caracterizado por irritabilidad, ansiedad, pérdida de memoria reciente y alteraciones en la capacidad de juicio (11, 12).
EFECTOS DE LA OXIGENOTERAPIA CRÓNICA DOMICILIARIA
Supervivencia
En 1970, Neff y Petty (13) sugieren por primera vez que la OCD puede mejorar la supervivencia de los pacientes con EPOC e IRC. Posteriormente dos estudios multicéntricos, el Nocturnal Oxygen Therapy Trial Group (NOTT) (14) y el Medical Research Council (MRC) (15) confirman definitivamente el impacto beneficioso de la OCD y establecen los criterios de su utilización.
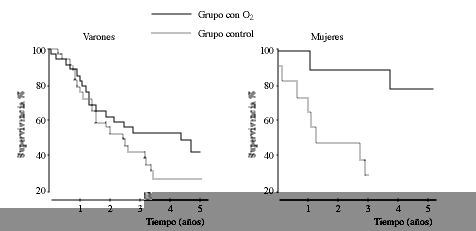
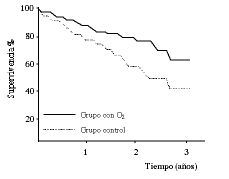
En el estudio MRC la mortalidad a los cinco años fue del 45% en pacientes que recibieron oxigenoterapia a 2 litros/minuto durante al menos 15 horas al día frente al 67% en pacientes sin oxigenoterapia (figura 1). El estudio NOTT demostró también una mejoría significativa de la supervivencia en pacientes que recibieron oxigenoterapia durante una media de 17,7 horas al día frente a aquéllos que la recibieron sólo durante la noche (12 horas al día) (figura 2). La supervivencia mejoró desde el comienzo de la OCD en los pacientes del NOTT y en las 9 mujeres del MRC, mientras que no lo hizo hasta pasados 500 días en los varones del MRC. Si se compara con la mortalidad de pacientes con igual grado de obstrucción de la vía aérea pero sin hipoxemia se observa que la OCD elimina el exceso de mortalidad causado por la hipoxemia (16).
Figura 1.Curvas de supervivencia en el estudio del MRC.
Figura 2.Curvas de supervivencia en el estudio del NOTT.
Los mecanismos a través de los cuales la OCD aumenta la supervivencia son controvertidos. El factor más importante parece ser la mejoría en la hemodinámica pulmonar manifestada como una disminución de la presión en la arteria pulmonar (17), las resistencias vasculares periféricas y el volumen minuto (18). Tampoco se conocen los factores que predicen la supervivencia en estos enfermos (16, 18-23) ni el subgrupo de pacientes que puede beneficiarse más de la OCD o en los que ésta tendrá escaso o nulo impacto.
Tolerancia al esfuerzo
En los pacientes con EPOC el esfuerzo físico puede causar una hipoxemia transitoria con niveles de PaO2 en reposo cercanos a la normalidad. Se ha demostrado que, en esta situación, la oxigenoterapia durante el ejercicio aumenta la tolerancia al esfuerzo y mejora la sensación de disnea tanto en el test de marcha estándar de seis minutos como en test de resistencia (24, 25). Sin embargo, todavía no están claramente definidos los criterios de indicación y se desconoce el impacto real de la oxigenoterapia sobre la actividad física diaria del paciente (26). Parece justificada la oxigenoterapia durante el ejercicio en pacientes en los que se demuestre una mejoría mayor del 50% en la capacidad de esfuerzo con O2 a flujos altos (4-6 litros/min.) (25).
Sueño
Un cierto número de pacientes con EPOC presenta episodios de hipoxemia durante el sueño (fundamentalmente durante las fases REM) generalmente asociados a retención de CO2 y alteraciones en la estructura del sueño, manteniendo en vigilia valores de PaO2 cercanos a la normalidad (27, 28). Estos episodios parecen relacionarse con la existencia de respiraciones rápidas y superficiales, episodios de hipoventilación o hipopnea, reducción de la capacidad residual funcional y alteraciones en la relación ventilación/perfusión. Esta situación puede conducir al desarrollo de hipertensión arterial pulmonar y cor pulmonale (29).
Los estudios sobre oxigenoterapia nocturna han mostrado resultados variables (30, 31). Actualmente la ventilación mecánica no invasiva se perfila como el tratamiento de elección (32). Debe descartarse previamente la coexistencia de un síndrome de apneas obstructivas durante el sueño (SAOS), cuyo tratamiento de elección es la presión positiva continua en la vía aérea (CPAP).
Efectos neuropsíquicos
En pacientes con hipoxemia crónica la administración de OCD produce mejoría en los test de memoria (33), así como en el estado de alerta, velocidad motora y habilidad manual (34).
Calidad de vida
La calidad de vida relacionada con la salud es uno de los conceptos en los que más se ha insistido en los últimos años (35), especialmente en lo referente al impacto que sobre el paciente y su actividad diaria presenta la existencia de una enfermedad o la instauración de una medida terapéutica.
El efecto de la OCD sobre la calidad de vida no ha sido claramente demostrado. Así, en un estudio en el que se aplicó un instrumento genérico de medida (Sickness Impact Profile) no se observó mejoría en la calidad de vida en los seis primeros meses del tratamientos (34). En otro estudio reciente en el que se utilizó un instrumento específico para patología respiratoria (St. George''s Respiratory Questionnaire) tampoco se detectó un impacto positivo sobre la calidad de vida con OCD utilizando fuentes de oxígeno no portátiles (36).
ESTABLECIMIENTO Y CONTROL DE LA OXIGENOTERAPIA CRÓNICA DOMICILIARIA
Indicaciones
La indicación de OCD se realiza tomando como referencia el valor de la PaO2 obtenida mediante gasometría arterial respirando aire ambiente y con el paciente en reposo (tabla III). Está indicada con valores de PaO2 inferiores a 55 mmHg, o con valores de PaO2 entre 55 y 59 mmHg si además existen indicios de repercusión orgánica de la hipoxemia, tales como hipertensión pulmonar, cor pulmonale, insuficiencia cardíaca congestiva, alteraciones del ritmo cardíaco, policitemia (hematocrito > 55%) o alteraciones en las funciones intelectuales (2).
Los estudios que han evaluado la eficacia de la OCD han sido realizados en pacientes con EPOC, por lo que en sentido estricto tan sólo en éstos estaría indicada. No obstante es probable que en otras patologías la corrección de la hipoxemia crónica aporte los mismos beneficios que en la EPOC.
Premisas
Antes de sentar la indicación de OCD deben cumplirse una serie de condiciones (tabla III y figura 3):
| Tabla III. Indicaciones de oxigenoterapia crnica domiciliaria | |
| 1. PaO2 <55 mmHg. | |
| 2. PaO2 55-59 mmHg con evidencia de: | |
| Hipertensin arterial pulmonar. | |
| Cor pulmonale. | |
| Insuficiencia cardaca congestiva. | |
| Arritmias. | |
| Hematocrito > 55%. | |
| Alteraciones de la funcin intelectual. | |
| Premisas | |
| ÐÊTratamiento asociado completo. | |
| ÐÊAbandono del hbito tabquico. | |
| ÐÊSituacin clnica y funcional estable. | |
Figura 3. Establecimiento de la oxigenoterapia crnica domiciliaria.
Tratamiento asociado completo y correcto
La OCD se debe utilizar tan sólo cuando la hipoxemia no se ha conseguido corregir por otros medios. Deben eliminarse todas las alteraciones potencialmente reversibles con un tratamiento completo y a dosis correctas. Aunque no existe consenso sobre el tratamiento óptimo de la EPOC, debe hacerse especial hincapié en el tratamiento broncodilatador, ejercicio diario y control de peso (37, 38). En el anciano debe prestarse una especial atención a la prevención de la broncoaspiración y asegurar una vía aérea permeable favoreciendo la eliminación de secreciones respiratorias mediante la expectoración estimulada, adecuada hidratación y fisioterapia respiratoria.
Abandono del hábito tabáquico
El tabaquismo es el principal factor etiológico en la EPOC, por lo que el abandono del mismo debe ser la primera medida terapéutica. Un fumador activo no es candidato a OCD, por ello debe comprobarse siempre que el paciente no fuma antes de su indicación.
Situación clínica estable
La indicación de OCD se debe realizar con el paciente en situación clínica y funcional estable. Debe comprobarse la ausencia de signos y síntomas de infección respiratoria e insuficiencia cardíaca descompensada, así como de variaciones significativas del FEV1, PaO2 y PaCO2 en dos controles separados como mínimo por un mes de diferencia.
Hasta en un 20-40% de los pacientes en los que se inicia OCD debe suspenderse el tratamiento al cabo de un mes por aumento de la PaO2, generalmente porque la indicación se realizó durante una agudización (14, 39) . Resulta aconsejable, por lo tanto, posponer la indicación definitiva durante un período de tres meses para comprobar de forma fehaciente la estabilidad clínica y funcional del paciente. En este sentido, el alta hospitalaria después de una agudización no puede ser considerada una situación clínica estable.
Dosis
La dosis de oxígeno debe ser la suficiente para mantener la PaO2 por encima de 60 mmHg (o la saturación de la oxihemoglobina SaO2 por encima del 90%). El flujo de O2 se debe ajustar individualizadamente. Para ello el paciente deberá respirar de forma ininterrumpida durante un tiempo no inferior a 30 minutos aire enriquecido con oxígeno, obteniendo a continuación una gasometría arterial. En pacientes sin hipercapnia es suficiente comprobar la SaO2 mediante oximetría para valorar la respuesta. La dosis más común oscila entre 1 y 2 l/min. administrados mediante gafas nasales.
La hipercapnia con pH compensado no es una contraindicación para la OCD. En esta situación es aconsejable realizar una gasometría arterial para valorar la respuesta de la PaCO2. En ocasiones puede producirse un aumento de ésta que suele compensarse con el aumento del bicarbonato sérico, causando escasa o nula acidosis. Valores de pH < 7,33 deben alertarnos sobre la posibilidad de una agudización.
Los resultados del NOTT y MRC apoyan la idea de que la mejoría en la supervivencia es proporcional a la cantidad de horas diarias realizadas de oxigenoterapia (14, 15). En la actualidad se recomienda para que la OCD sea eficaz la administración de O2 durante el mayor número de horas posible, nunca menos de 15 al día e incluyendo siempre los períodos de sueño.
Revisiones
Una vez planteada la indicación de OCD, y previo al comienzo de la misma, se deben realizar revisiones mensuales los tres primeros meses. Su finalidad es confirmar o rechazar la indicación en función de que se mantengan o no los criterios y premisas iniciales. En este período se debe informar al paciente sobre los objetivos que se pretenden alcanzar con la OCD, así como hacer un especial énfasis en la necesidad de una correcta cumplimentación del tratamiento (ver anexo). Es conveniente facilitar una vía de contacto rápida para solucionar las dudas e interrogantes que puedan surgir en el transcurso del programa de OCD, especialmente durante las primeras semanas.
Una vez iniciada la OCD se deben realizar revisiones trimestrales durante el primer año y semestrales en adelante (9, 40). En cada revisión han de hacerse los siguientes estudios:
a) Valoración clínica y funcional. Nos permitirá tener una visión global de la evolución de la enfermedad de base. Comprobaremos que el paciente realiza correctamente el tratamiento asociado prescrito (broncodilatadores, diuréticos, etc.) y que éste es el adecuado. Se debe interrogar específicamente sobre la existencia de signos o síntomas que nos alerten sobre episodios de hipoxemia nocturna (sensación de mala calidad de sueño, hipersomnolencia diurna, cefalea matutina, etc.). En este sentido es útil la determinación del hematocrito, ya que si está elevado debe descartarse un mal cumplimiento de la OCD, la existencia de hipoxemias nocturnas o un SAOS asociado.
Deberemos aseguramos que el paciente cumple correctamente las horas prescritas. La forma más directa es la entrevista personal (preguntar al paciente), pero este método no es fiable (41), por lo que es conveniente disponer de mediciones directas del consumo real de oxígeno, aportadas generalmente por la empresa suministradora del servicio. Debe descartarse la recaída en el hábito tabáquico. Para ello es útil, en casos dudosos, la determinación de carboxihemoglobina o la medición de CO2 en el aire espirado.
b) Comprobar la corrección de la hipoxemia. Con el tiempo puede variar la dosis de oxígeno necesaria para corregir la hipoxemia, por lo que en cada revisión se debe comprobar que la dosis prescrita sigue siendo la correcta. Para ello realizaremos una pulsioximetría (o gasometría arterial si queremos evaluar la PaCO2) mientras el paciente respira, como mínimo durante 30 minutos, aire enriquecido con oxígeno en las mismas condiciones en las que lo realiza en su domicilio. En función del resultado realizaremos los siguientes cambios:
1. Si la SaO2 se encuentra entre el 90-94% (o la PaO2 entre 60 y 80 mmHg), la dosis de oxígeno prescrita sigue siendo la adecuada.
2. Si la SaO2 es menor del 90% (PaO2 < 60 mmHg) debe descartarse la existencia de una agudización. En caso negativo se ajustará la dosis de oxígeno para mantener los niveles adecuados.
3. Si la SaO2 es mayor del 94% (PaO2 > 80 mmHg), se debe comprobar si los criterios de indicación de la OCD se mantienen. La retirada de la OCD requiere comprobar que el paciente se mantiene en una situación clínica estable y presenta una PaO2 respirando aire ambiente mayor de 60 mmHg o una SaO2 > 90% durante un período de tres meses.
INTERPRETACIÓN DE LOS RESULTADOS GASOMÉTRICOS
La indicación de la OCD se basa en el resultado de la gasometría arterial. Antes de instaurar un tratamiento con tan importantes implicaciones clínicas, sociales y económicas, debemos asegurar que la técnica de extracción, transporte y procesamiento de la gasometría ha sido la correcta, descartando los errores que con mayor frecuencia alteran el resultado (tabla IV).
| Tabla IV. Fuentes de error ms frecuentes en la gasometra arterial |
| Ð Puncin arterial dolorosa (sin anestesia). |
| Ð Puncin venosa. |
| Ð Burbujas en la muestra. |
| Ð Muestra en contacto con el aire (sin tapn). |
| Ð Demora > 15 min. en el procesamiento de la muestra. |
| Ð Desconocimiento de la temperatura del paciente. |
| Ð Leucocitosis > 50.000 leucocitos/mm3. |
La gasometría arterial debe realizarse con el paciente alerta y en reposo al menos desde los 10 minutos previos a la extracción, y antes de cualquier otra maniobra de exploración de la función pulmonar. Salvo que la persona encargada de la extracción tenga una gran experiencia, la punción arterial se debe realizar bajo anestesia local inyectando subcutáneamente una pequeña cantidad (0,3 ml) de anestésico sin adrenalina (42). La punción arterial puede causar ansiedad y dolor, y producir hiperventilación con el consiguiente aumento de la PaO2 y disminución de la PaCO2.
Se deben eliminar cuidadosamente las burbujas de la muestra y transportar ésta en condiciones herméticas. Si permanece aire en el interior de la jeringuilla o se transporta sin tapón se produce una tendencia al equilibrio entre la PaO2 de la muestra y la PO2 del aire ambiente (a nivel del mar, aproximadamente 160 mmHg), con la consiguiente variación de la PaO2.
El tiempo desde la extracción de la muestra hasta su procesamiento no debe ser superior a 15 minutos. Por un lado las células sanguíneas continúan produciendo CO2 y consumiendo O2 dentro de la jeringuilla, proceso que se enlentece notablemente si se conserva ésta en hielo. Además los gases difunden a través de las paredes de las jeringuillas de plástico (que son las más ampliamente utilizadas por su comodidad y bajo costo). Si se prevé que la muestra no va a poder ser procesada de forma inmediata (por ejemplo en la realización de gasometrías domiciliarias) la muestra debe ser extraída con jeringuilla de cristal y conservada en hielo hasta su procesamiento, ya que en estas condiciones se asegura la fiabilidad de los resultados durante 90-120 minutos (43-45).
La PaO2 varía de forma importante con la temperatura (46, 47). La práctica totalidad de los gasómetros actuales pueden realizar la corrección, por lo que se debe informar al laboratorio de la temperatura corporal del paciente en el momento de la extracción.
Una leucocitosis importante (mayor de 50.000 leucocitos/mm3) produce un consumo acelerado de O2 generando valores de PaO2 falsamente bajos. En estas condiciones es preferible medir la SaO2 mediante oximetría.
A pesar de la correcta extracción, transporte y procesamiento de la muestra y del control de las fuentes de error, es un hecho bien conocido que se producen variaciones espontáneas en la PaO2 en pacientes clínicamente estables. Estas variaciones pueden ser superiores a 5 mmHg en el plazo de pocos minutos (48), especialmente en pacientes con patología respiratoria crónica. Este hecho enfatiza la necesidad de no realizar la indicación de OCD utilizando como referencia una gasometría aislada.
FUENTES DE SUMINISTRO DE OXÍGENO
Cilindro de presión
Es la fuente más utilizada en nuestro medio. Son recipientes metálicos que almacenan oxígeno a alta presión. En función de su tamaño la autonomía varía, siendo para los más grandes (capacidad para 10.000 litros de oxígeno) de 2-4 días en función del flujo prescrito. Son muy pesados, por lo que no confieren movilidad al paciente.
Concentrador
El concentrador o extractor de oxígeno es el sistema que garantiza una mayor autonomía al depender sólo de una fuente de energía eléctrica. Su funcionamiento consiste en hacer pasar el aire a través de un filtro molecular que absorbe el nitrógeno y el vapor de agua, quedando un gas rico en oxígeno que se acumula en un depósito a partir del cual se libera al paciente. Cuanto mayor es el flujo menor es la cantidad de oxígeno que se alcanza en el gas liberado.
Los requisitos que debe cumplir un concentrador son (49):
a) Contenido de oxígeno del gas liberado superior al 90% a un flujo de 2 l/min.
b) Seguridad en la instalación eléctrica, con alarmas indicadoras de mal funcionamiento.
c) Sencillez en su empleo.
d) Economía, con un bajo consumo de electricidad;
e) Manejabilidad, con un peso inferior a 40 kg.
f) Bajo nivel de ruido.
Los aparatos más modernos garantizan contenido de oxígeno superior al 95% a un flujo de hasta 3 l/min.
La ventaja principal de los concentradores es su bajo costo y su sencillez de uso. Aunque no se pueden considerar aparatos portátiles, garantizan la movilidad dentro del domicilio al disponer de ruedas y permiten solucionar problemas de desplazamiento del paciente (por ejemplo, vacaciones). Requieren un mantenimiento y control regular de su funcionamiento por parte de la empresa suministradora. Incorporan un reloj que mide las horas de utilización, lo que puede ser de utilidad a la hora de valorar el cumplimiento del paciente. El concentrador debe ser la forma inicial de suministro de oxígeno (26).
Oxígeno líquido
El oxígeno pasa del estado gaseoso al líquido cuando se almacena a temperaturas inferiores a 183 °C. El volumen de una determinada cantidad de oxígeno en estado líquido es menor que el 1% del volumen de esa misma cantidad en estado gaseoso.
En nuestro país se comercializan recipientes para almacenamiento y liberación de oxígeno líquido, con capacidad para unos 30 litros y un peso de unos 100 kg. A un flujo medio de 2 l/min presentan una autonomía de 8-10 días. A partir de estos recipientes se pueden recargar unas pequeñas mochilas de 2-3 kg de peso que permiten una autonomía de 6-8 horas.
El oxígeno líquido es la forma más cara de suministro de oxígeno. Su utilización se debe reservar para pacientes buenos cumplidores de la OCD que manifiestan explícitamente el deseo de realizar actividades fuera de su domicilio y en los que la oxigenoterapia demuestra corregir las desaturaciones.
SISTEMAS DE LIBERACIÓN DE OXÍGENO AL PACIENTE
Existen numerosos dispositivos para administrar oxígeno al paciente. En la OCD se emplean fundamentalmente las gafas nasales y el catéter transtraqueal. Se deben evitar las mascarillas con efecto Venturi, ya que su principal ventaja, la estabilidad en la concentración del oxígeno liberado, no resulta imprescindible en la OCD y presentan los inconvenientes del mayor consumo de oxígeno, impedir comer o expectorar sin retirarlas y descolocarse fácilmente durante el sueño.
Gafas nasales
Es la forma más simple y barata de suministro de oxígeno. Consiste en dos pequeños tubos colocados a la entrada de las fosas nasales que se mantienen en su posición sobre el labio superior por diferentes diseños de apoyo alrededor de los pabellones auriculares. Permiten comer, dormir y expectorar sin interrumpir el aporte de oxígeno.
La fracción de oxígeno en el aire inspirado (FiO2) que consiguen puede variar en función del patrón ventilatorio del paciente, pero en general se sitúa en el 24% con un flujo de 1 l/min y 28% para un flujo de 2 l/min (47). Flujos inferiores a 3 l/min suelen ser bien tolerados y no requieren humidificación, mientras que flujos superiores a 4 l/min pueden producir sequedad de mucosas e irritación local.
La ventilación alveolar sólo se produce durante la fase temprana de la inspiración, por lo que el oxígeno administrado durante el final de la inspiración y en toda la espiración se pierde sin participar en el intercambio gaseoso (50, 51). En un paciente con EPOC la espiración ocupa aproximadamente el 65% del ciclo respiratorio, lo que hace que las 2/3 partes del oxígeno aportado sean ineficaces. Con estas premisas se han desarrollado métodos de ahorro de oxígeno para aumentar la autonomía de las fuentes portátiles y disminuir los costes de la OCD.
Reservorios. Son unos colectores de aproximadamente 20 ml de capacidad que se colocan entre la fuente de suministro y las gafas nasales, generalmente en forma de bigoteras. Almacenan el oxígeno durante la espiración y lo liberan en forma de bolo durante la inspiración temprana, continuando luego con el flujo prefijado (52). Con estos reservorios el ahorro de oxígeno puede llegar hasta al 50%.
Sistemas de liberación de oxígeno a demanda. Son dispositivos que se colocan, al igual que los anteriores, entre la fuente de suministro y las gafas nasales. Incorporan sensores electrónicos que detectan cambios de presión o temperatura al inicio de la inspiración, permitiendo la liberación de oxígeno solamente durante la fase precoz de la misma. Al depender de un mecanismo electrónico complejo su principal limitación es el potencial fallo del aparato. No existen estudios que garanticen su eficacia a largo plazo.
Catéter transtraqueal
El catéter transtraqueal es un dispositivo para liberar oxígeno directamente en la tráquea. Se introduce, bajo anestesia local, a través de una vía percutánea o tunelizada entre el segundo y tercer anillo traqueal (53-55). En un 3-5% de los casos se producen complicaciones durante su implantación, siendo las más frecuentes el enfisema subcutáneo, el broncoespasmo y la tos paroxística.
Las principales ventajas del catéter transtraqueal son:
a) Elimina el espacio muerto anatómico que supone la nariz y la faringe.
b) Utiliza la tráquea como reservorio de oxígeno.
c) Se necesitan flujos más bajos para conseguir una buena oxigenación (0,25-1,5 l/min).
d) Permite utilizar flujos mayores de 3 l/min sin molestias para el paciente en los casos de hipoxemia refractaria a los sistemas tradicionales.
e) Supone un importante ahorro en el consumo de oxígeno, lo que aumenta la autonomía de las fuentes portátiles.
f) Evita los problemas estéticos que suponen las gafas nasales.
Las complicaciones potenciales incluyen el desplazamiento del catéter, infecciones en el estoma, hemoptisis, aumento en la frecuencia de infecciones respiratorias y formación de tapones de moco.
Los pacientes subsidiarios de su utilización son aquellos que presentan marcadas desaturaciones con el esfuerzo y precisan una vida más activa (unido al oxígeno líquido), los que requieren flujos elevados por mala oxigenación con los métodos convencionales, y los sujetos con problemas estéticos.
CONCLUSIÓN
La oxigenoterapia crónica domiciliaria es un método terapéutico con importantes implicaciones clínicas, sociales y económicas. Es necesario, por parte del médico prescriptor, un adecuado conocimiento de sus indicaciones, eficacia y formas de administración y control, así como informar al paciente de los objetivos perseguidos y de la necesidad de un correcto cumplimiento.
BIBLIOGRAFÍA
1. Anthonisen NR, Wright EC, Hodgkin JE, and the IPPB Trial Group. Prognosis in chronic obstructive pulmonary disease. Am Rev Respir Dis 1986;133:14-20.
2. Recomendaciones SEPAR. Normativa para la indicación y empleo de la oxigenoterapia crónica domiciliaria (OCD). Arch Bronconeumol 1989;25:306-13.
3. Report of the European Society of Pneumology Task Group. Recommendations for long term oxygen therapy. Eur Respir J 1989;2:160-4.
4. O''Donohue WJ, Plummer AL. Magnitude of usage and cost of home oxygen therapy in the United States. Chest 1995;107:302.
5. Escarrabill J. Situación de la oxigenoterapia domiciliaria en nuestro medio. Arch Bronconeumol 1990;26:151-2.
6. Ministerio de Sanidad y Consumo. Agencia de Evaluación de Tecnologías Sanitarias (AETS). Oxigenoterapia crónica a domicilio, aerosolterapia y ventilación mecánica a domicilio. Indicaciones, requisitos y criterios de supervisión. Madrid: AETS Instituto de Salud «Carlos III»; 1995.
7. Tamayo J, Esteban R, Pérez-Rodríguez E, Flores J, Ortiz de Saracho J. ¿Es correcto el análisis de la prevalencia, sin el índice de correcta prescripción, en la oxigenoterapia crónica domiciliaria? Arch Bronconeumol 1994;30(Supl 1):39.
8. Sánchez I, Echave-Sustaeta J, Ussetti P, Magro R, Bezos A, Robledillo R, et al. Oxigenoterapia domiciliaria en la provincia de Guadalajara. Prevalencia, idoneidad y cumplimiento. Arch Bronconeumol 1994;30(Supl 1):37-38.
9. Restrick LJ, Paul EA, Braid GM. Assessment and follow-up of patients prescribed long-term oxygen therapy. Thorax 1993;48:708-13.
10. Pépin JL, Barjhoux CE, Deschaux C, Brambilla C. The ANTADIR Working Group on Oxygen Therapy. Long-term oxygen therapy at home. Compliance with medical prescription and effective use of therapy. Chest 1996;109:1144-50.
11. Grant I, Heaton RK, McSweeny AJ, Adams KM, Timms RM. Neuropsychologic findings in hypoxemic chronic obstructive pulmonary disease. Arch Intern Med 1982;142:1470-6.
12. Prigatano GP, Parsons OA, Wright E, Levin DC, Hawryluk G. Neuropsychological test performance in middly hypoxemic patients with chronic obstructive pulmonary disease. J Consult Clin Psychol 1983;51: 108-16.
13. Neff TA, Petty TL. Long term continuous oxygen treatment in chronic airway obstruction. Ann Intern Med 1970;72:621-6.
14. Nocturnal Oxygen Therapy Trial Group. Continuous or nocturnal oxygen therapy in hypoxemic chronic obstructive lung diseases. Ann Intern Med 1980;93:391-8.
15. Report of the Medical Research Council Working Party. Long-term domiciliary oxygen therapy in chronic cor pulmonale complicating chronic bronchitis and emphysema. Lancet 1981;1:681-6.
16. ACCP-NHLBI National Conference on Oxygen Therapy. Chest 1984;86: 234-47.
17. Weitzemblum E, Sautegeau A, Ehrhart M, Mammosser M, Pelletier A. Long-term oxygen therapy can reverse the progression of pulmonary hypertension in patients with chronic obstructive pulmonary disease. Am Rev Respir Dis 1985;131:493-8.
18. Timms RM, Khaja FU, Williams GW. The Nocturnal Oxygen Therapy Trial Group. Haemodinamic response to oxygen therapy in chronic obstructive pulmonary disease. Ann Intern Med 1985;102:29-36.
19. France AT, Prescott RJ, Biernacki W. Does right ventricular function predict survival in patients with chronic obstructive lung diseases? Thorax 1988;43:621-6.
20. Oswald-Mammosser M, Weitzemblum E, Quoix E, Moser G, Chaouat A, Charpentier C, et al. Prognostic factors in COPD patients receiving long-term oxygen therapy. Importance of pulmonary artery pressure. Chest 1995;107:1193-8.
21. Sliwinski P, Hawrylkiewicz I, Gorecka D, Zielinski J. Acute effect of oxygen on pulmonary arterial pressure does not predict survival on long-term oxygen therapy in patients with chronic obstructive pulmonary disease. Am Rey Respir Dis 1992;146:665-9.
22. Macnee W, Wathen CG, Flenley DC, Muir AD. The effects of controlled oxygen therapy on ventricular function in patients with stable and decompensated cor pulmonale. Am Rev Respir Dis 1988;137:1289-95.
23. Wright JL, Petty T, Thurlbeck WM. Analysis of the structure of the muscular pulmonary arteries in patients with pulmonary hypertension and COPD: National Institutes of Health Nocturnal Oxygen Therapy Trial. Lung 1992;170:109-24.
24. Dean NC, Brown JK, Mimelman RD, Doherty JJ, Gold WM, Stulbarg MS. Oxygen may improve dyspnea and endurance in patients with chronic obstructive pulmonary disease and only mild hypoxemia. Am Rev Respir Dis 1992;146:941-5.
25. Leach RM, Davidson AC, Chinn S, Twort CHC, Cameron IR, Bateman NT. Portable liquid oxygen and exercise in severe respiratory disability. Thorax 1992;47:781-9.
26. Escarrabill J. Oxigenoterapia domiciliaria: ¿a quién, cómo, cuándo, dónde y quién la controla? Arch Bronconeumol 1996;32:1-2.
27. Koo KW, Sax DS, Snider GL. Arterial blood gases and pH during sleep in chronic obstructive pulmonary disease. Am J Med 1975;58:663-70.
28. Douglas NJ, Flenley DC. Breathing during sleep in patients with obstructive lung diseases. Am Rev Respir Dis 1990;141:1055-70.
29. Levi-Valensi P, Weitzenblum E, Rida Z. Sleep-related oxygen desaturation and daytime pulmonary haemodynamics in COPD patients. Eur Respir J 1992;5:301-7.
30. Calverley PMA, Brezinova V, Douglas NJ, Catterall JR, Flenley DC. The effect of oxygenation on sleep quality in chronic bronchitis and emphysema. Am Rev Respir Dis 1982;126:206-210.
31. Goldstein RS, Ramcharam V, Bowes G, McNicholas WT, Bradley D, Phillipson EA. Effect of supplemental nocturnal oxygen on gas exchange in patients with severe obstructive lung disease. N Engl J Med 1984;310: 425-9.
32. Wedzicha JA, Meecharn-Jones DJ. Domiciliary ventilation in chronic obstructive pulmonary disease: where are we? [editorial]. Thorax 1996; 51:455-7.
33. Krop HD, Block JA, Cohen E. Neuropsychologic effects of continuous oxygen therapy in the aged. Chest 1977;72:737-43.
34. Heaton RK, Grant I, McSweeny AJ, Adams KM, Petty TL. Psychological effects of continuous and nocturnal oxygen therapy in hypoxemic chronic obstructive pulmonary disease. Arch Intern Med 1983;143:1941-7.
35. Guyatt GH, Feeny DH, Patrick DL. Measuring health-related quality of life. Ann Intern Med 1993;118:622-9.
36. Okubadejo AA, Paul EA, Jones PW, Wedzicha JA. Does long-term oxygen therapy affect quality of life in patients with chronic obstructive pulmonary disease and severe hypoxemia? Eur Respir J 1996;9:2335-9.
37. American Thoracic Society. Standards for the diagnosis and care of patients with chronic obstructive pulmonary disease. Am J Respir Crit Care Med 1995;152:S77S-120.
38. ERS Consensus Statement. Optimal assessment and management of chronic obstructive pulmonary diseases (COPD). Eur Respir J 1995;8: 1398-420.
39. Levi-Valensi P, Duwoos H, Racineaux JL. Multicenter study of oxygen therapy: GEMOS Preliminar results. Med Thorac 1983;5 Suppl 4:502-6.
40. Recomendaciones SEPAR. Normativa sobre gasometría arterial. Barcelona: Doyma; 1987.
41. Cottrell JJ, Openbrier D, Lave JR, Paul C, Garland JL. Home oxygen therapy. A comparison of 2-vs 6-month patient reevaluation. Chest 1995;107:358-61.
42. Castelao J, Sánchez I, Izquierdo JL, Carrillo F, Gallardo J. Utilidad de la entrevista personal para evaluar el grado de cumplimiento de la oxigenoterapia crónica domiciliaria. I Congreso de la Sociedad Madrileña de Neumología y Cirugía Torácica. Madrid; 1996.
43. Vaida AM. Contrôle de qualité de la measure des pressions partielles d''oxygène et de gaz carbonique dans le sang. Bull Europ Physiopathol Resp 1980;16:67-78.
44. Izquierdo JL, Ribas MS, Izquierdo M, Rodríguez JM, Viejo JL. Variaciones de la gasometría arterial en relación con la manipulación de la muestra y material empleado. Arch Bronconeumol 1990;26:181-5.
45. Liss HP, Payne CP. Stability of blood gases in ice and at room temperatura. Chest 1993;103:1120-2.
46. Severinghaus JW. Blood gas calculator. J Appl Physiol 1966;21: 1108-16.
47. Ashwood ER, Kost G, Kenny M. Temperature control of blood-gas and pH measurementes. Clin Chem 1983;29:1877-85.
48. Rodríguez-Froján G, Casan P, Miralda R, Sanchis J. Variabilidad de la PO2, la PCO2 y del pH en pacientes con patología respiratoria crónica. Arch Bronconeumol 1992;28:267-9.
49. Pépin JL, Dautzenberg B, Levy P, Brambilia C. What should we expect from an oxygen concentrator in 1995? Eur Respir Buyers 1995;1:21-6.
50. Tiep BL. Long-term oxygen therapy. Clin Chest Med 1990;11:505-21.
51. Barker AF, Burgher LW, Plummer AL. Oxygen conserving methods for adults. Chest 1994;105:248-52.
52. Claibome RA, Paynter DE, Dutt AK, Rowlands JW. Evaluation of the use of an oxygen conservation device in long term oxygen therapy. Am Rev Respir Dis 1987;136:1095-8.
53. Domingo C, Léger P, Morera J. Catéter transtraqueal: una puerta abierta a la oxigenoterapia continua domiciliaria moderna. Med Clin (Barc) 1990;94:103-6.
54. Walsh DA, Govan JR. Long term continuous domiciliary oxygen therapy by transtracheal catheter. Thorax 1990;45:478-81.
55. Díaz Lobato S, Villasante C, Villamor J. Beneficios que aporta la oxigenoterapia por catéter transtraqueal. Med Clin (Barc) 1993;100:264-5.
ANEXO. RECOMENDACIONES PARA EL PACIENTE EN PROGRAMA DE OXIGENOTERAPIA CRîNICA DOMICILIARIA
Apellidos:
Nombre:
Compañía suministradora:
Teléfono de contacto:
La administración de oxígeno en su domicilio tiene por objetivo aliviar algunas de las consecuencias de su enfermedad y mejorar su situación.
Debe tener en cuenta las siguientes recomendaciones:
1. La cantidad de oxígeno necesaria y la forma de administración es la que le ha indicado su médico (generalmente entre 1 y 2 litros por minuto). No haga cambios sin consultárselo. Un aumento del flujo por su cuenta puede tener consecuencias perjudiciales para usted.
2. Debe estar con oxígeno el mayor tiempo posible. Nunca menos de 15 horas al día y siempre durante el sueño, después de las comidas, al realizar esfuerzos físicos y en situaciones de ansiedad o estrés psíquico.
3. Si interrumpe la administración de oxígeno en algún momento, no deberá ser durante más de dos horas. Tenga en cuenta que estos períodos de interrupción no son necesarios, son sólo para su comodidad.
4. Recuerde que el oxígeno no es el único tratamiento de su enfermedad. Es muy importante que no abandone el resto del tratamiento pautado por su médico.
5. Los beneficios de la oxigenoterapia se consiguen a largo plazo. No espere una mejoría espectacular en poco tiempo.
6. Si utiliza cilindros de presión (bombonas) avise con suficiente antelación a la compañía suministradora para sustituirlos. Evite quedarse sin oxígeno.
7. Es importante que realice las revisiones periódicas que le indique su médico con el fin de asegurar la eficacia del tratamiento y atender a posibles problemas que puedan presentarse durante su aplicación.
Cuidados del sistema de administración
Gafas nasales: debe limpiarlas y esterilizarlas como mínimo una vez al día.
Tubos de conducción: la longitud de los tubos no debe sobrepasar los 20 metros. Si es posible deben ser de una pieza, sin uniones. Si existen éstas, vigile que no haya fugas, así como en los enlaces del tubo con el manómetro y con las gafas nasales. Lávelos con jabón al menos una vez a la semana.
Manómetro: si utiliza un vaso con agua, debe cambiar ésta al menos una vez al día y esterilizar el vaso. Evite la entrada de agua en la unidad de medida.
Precauciones
El oxígeno no es un gas inflamable pero favorece que ardan otras materias. No permita que nadie fume en sus proximidades, ni por supuesto fume usted.
En caso de incendio, cierre inmediatamente la fuente de oxígeno y aléjese de ella.
Mantenga la fuente de oxígeno y el tubo de conducción alejado del fuego, braseros, estufas, etc.
Limpieza y esterilización de las gafas nasales y vaso
Desenrosque el vaso humidificador y friéguelo, así como las gafas nasales, con agua caliente y jabón detergente. A continuación introdúzcalos en una solución de clorhexidina al 3% (Deratin solución: 30 cc. en 970 cc. de agua). Déjelos sumergidos durante 15 minutos. Aclárelos después con abundante agua caliente y séquelos con un paño limpio.
Correspondencia: A. Vena Martínez. Sección de Geriatría. Hospital General Universitario. Donantes de Sangre, s/n. 19002 Guadalajara.
Recibido el 17-6-97; aceptado el 10-12-97.