Los angiosarcomas son neoplasias malignas agresivas con diferenciación de células endoteliales. La hemorragia espontánea debida a una coagulación intravascular diseminada con coagulopatía de consumo es una forma poco común de presentación de estos tumores denominada síndrome de Kasabach-Merritt. En el presente estudio describimos 2 casos con estudio necrópsico de angiosarcomas complicado con síndrome de Kasabach-Merritt. El primer caso con diagnóstico de angiosarcoma mediastínico asociado a un tumor de células germinales y el segundo caso con angiosarcoma primario hepático y múltiples metástasis.
Angiosarcomas are aggressive vascular malignancies of endothelial cell differentiation. An uncommon clinical presentation of angiosarcoma is spontaneous bleeding due to disseminated intravascular coagulation by consumption coagulopathy, known as the Kasabach-Merritt syndrome. We report two autopsy cases of angiosarcomas associated with Kasabach-Merritt syndrome; one was a mediastinal angiosarcoma associated with a germ cell tumour and the other a primary liver angiosarcoma and multiple metastases.
El angiosarcoma (AS) es una neoplasia maligna agresiva originada en las células endoteliales que bordean los canales vasculares1–4. Estos tumores muestran una diferenciación endotelial que puede detectarse con el análisis histopatológico, inmunohistoquímico (IHQ) o ultraestructural1–14. Los AS representan menos del 1% de todos los sarcomas de partes blandas y pueden aparecer en cualquier parte del cuerpo, predominantemente en tejido celular subcutáneo y partes blandas profundas1,3,4. Estas neoplasias pueden originarse espontáneamente (AS primarios) o ser secundarias a la radiación ionizante o el linfedema crónico1–17.
Esporádicamente los AS pueden asociarse o aparecer en el curso de otros tumores como los sarcomas neurales17–19 o neoplasias no mesenquimales como los tumores germinales20. En algunos casos se describe una franca transformación de tumores neurales en AS con una evolución más agresiva17–19.
Los AS son neoplasias generalmente con mal pronóstico, y la asociación con el síndrome de Kasabach-Merritt (SKM) se observa usualmente en neoplasias avanzadas de gran tamaño que generan un secuestro de elementos sanguíneos, sobre todo plaquetas, induciendo hemorragias y evolución clínica aguda generalmente mortal21–28.
En el presente estudio describimos 2 casos con estudio necrópsico de AS asociados a SKM con una evolución clínica aguda y mortal. Uno de los casos fue diagnosticado como AS mediastínico asociado a tumor de células germinales (TCG) y el otro caso como AS hepático con metástasis múltiples.
Historia clínicaCaso 1Varón de 23 años de edad, que acudió al hospital por dificultad respiratoria, tos y pérdida de peso. El estudio radiológico por tomografía axial computarizada mostró una lesión sólida bien circunscrita en el mediastino anterosuperior. No se encontraron lesiones metastásicas en otras localizaciones. Los análisis de laboratorio clínico mostraron anemia y trombocitopenia severa. El paciente evolucionó desfavorablemente con hemorragias múltiples, falleciendo por shock hipovolémico y fallo cardíaco.
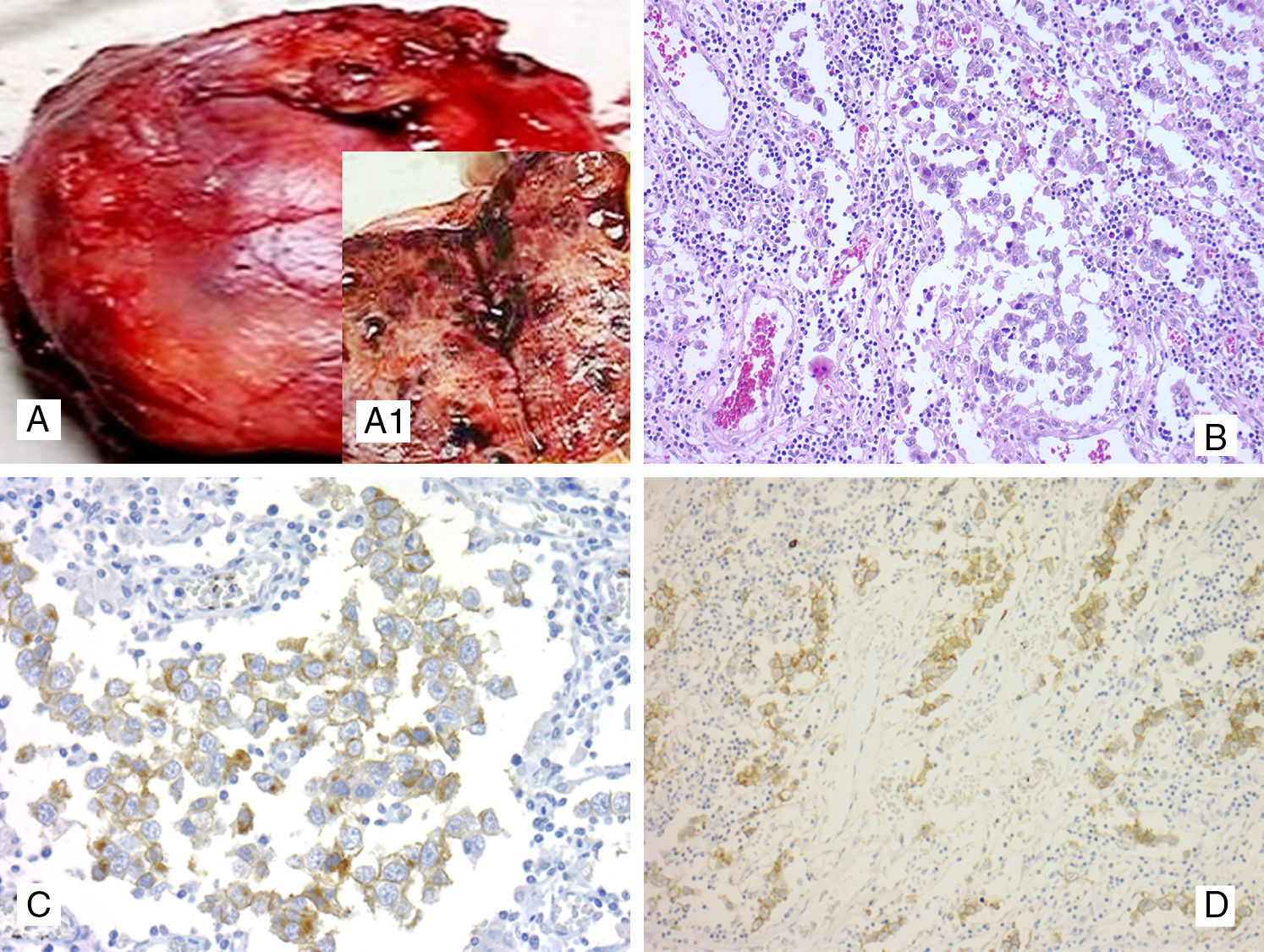
El estudio de la autopsia demostró una gran masa mediastínica hemorrágica de (130×100×20mm), consistencia sólida y que al corte mostraba un color pardo-rojizo, con abundante hemorragia (fig. 1A) así como quistificación y necrosis focal. El examen de los demás órganos demostró la presencia de hemorragias en hígado, páncreas y ambos pulmones así como esplenomegalia. No se encontraron metástasis a distancia.
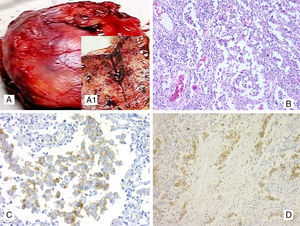
(Caso 1). A. Masa mediastínica hemorrágica de (130×100×20mm), consistencia sólida y que al corte mostraba un color pardo-rojizo, con abundante hemorragia (A1). B. Nidos de células tumorales que formaban ocasionalmente estructuras alveolares, donde predominaban células tumorales redondas con citoplasma abundante claro y anfofílico con un núcleo central y vesicular con nucléolo eosinofílico prominente correspondiente con el componente de TCG entremezclado con linfocitos maduros, hematoxilina y eosina (H&E) 400x. C. Positividad intensa de membrana y citoplasmática en las células neoplásicas para PLAP, 400x. D. Positividad intensa de membrana en las células neoplásicas para CD117, 400x.
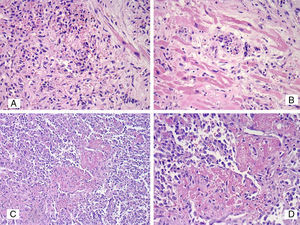
La histopatología del tumor mediastínico mostró la existencia de 2 componentes limitados por zonas de tejido tímico residual. El componente del tumor localizado en la región subcapsular morfológicamente estaba constituido por nidos de células tumorales que formaban ocasionalmente estructuras alveolares y donde predominaban células tumorales redondas con citoplasma abundante claro y anfofílico con un núcleo central y vesicular con nucléolo eosinofílico prominente (fig. 1B) Las células neoplásicas estaban entremezcladas y rodeadas por células linfoides de pequeño tamaño sin atipia, correspondientes con linfocitos maduros. La actividad mitótica era escasa y se observaron zonas de necrosis y hemorragia. El aspecto morfológico fue sugestivo de TCG tipo seminoma y el estudio IHQ confirmó la sospecha histopatológica, demostrando positividad intensa de membrana y citoplasmática para PLAP (fig. 1C), CD117 (fig. 1D) y vimentina. La tinción para OCT4 mostró positividad nuclear moderada y la CK (AE1/AE3) así como CK8/18 mostraron positivad focal con tinción tipo Golgi (dot-like) en las células tumorales.
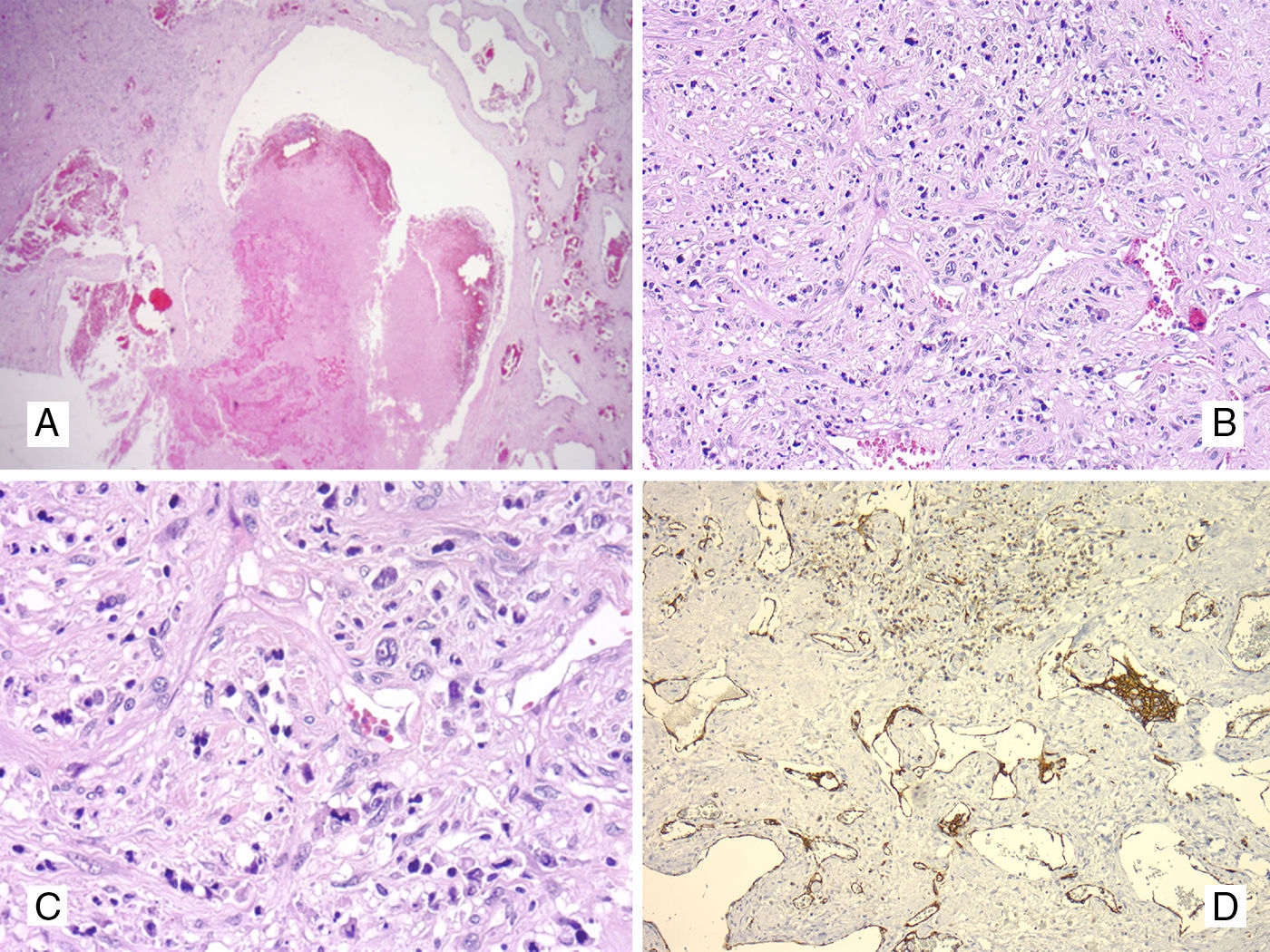
El segundo componente del tumor estaba constituido por una red de vasos dilatados separados por fascículos de células fusiformes que formaban hendiduras con pequeños espacios vasculares. Estos vasos cavernosos tenían paredes gruesas y en muchos de ellos se encontró trombosis intraluminal (fig. 2A, B) organizada, así como proliferaciones digitiformes intraluminales de células endoteliales con un centro fibroso acelular simulando una arquitectura papilar. Las células tumorales fusiformes formaban fascículos y vasos elongados que rodeaban y separaban los grandes canales vasculares (fig. 2C). En algunas de estas células se encontraron vacuolas citoplasmáticas. En otras zonas del tumor se observó extensa esclerosis e hialinización del estroma. El componente vascular neoplásico mostró evidente diferenciación endotelial con positividad intensa para CD31 (fig. 2D), CD34, ERG y D2-40 en los grandes canales vasculares así como en las células tumorales fusocelulares. El índice de proliferación Ki-67 fue del 30%. CK (AE1/AE3), CK8/18, PLAP, CD117, S100, HMB-45, melan A, CD45, desmina, CD68, ALK, AFP, lisozima, mieloperoxidasa, CD168, CD30, CD3, CD4, CD5 CD8, CD99, EMA y HNK-1 fueron todos negativos en los canales vasculares así como en la proliferación neoplásica de células fusiformes. En resumen, el estudio autópsico demostró un seminoma mediastínico con componente sarcomatoso tipo AS, que en este caso se asoció clínicamente con un SKM. En el bazo e hígado se vieron focos de hematopoyesis extramedular con presencia de megacariocitos probablemente reactivos a la anemia y trombocitopenia severa.
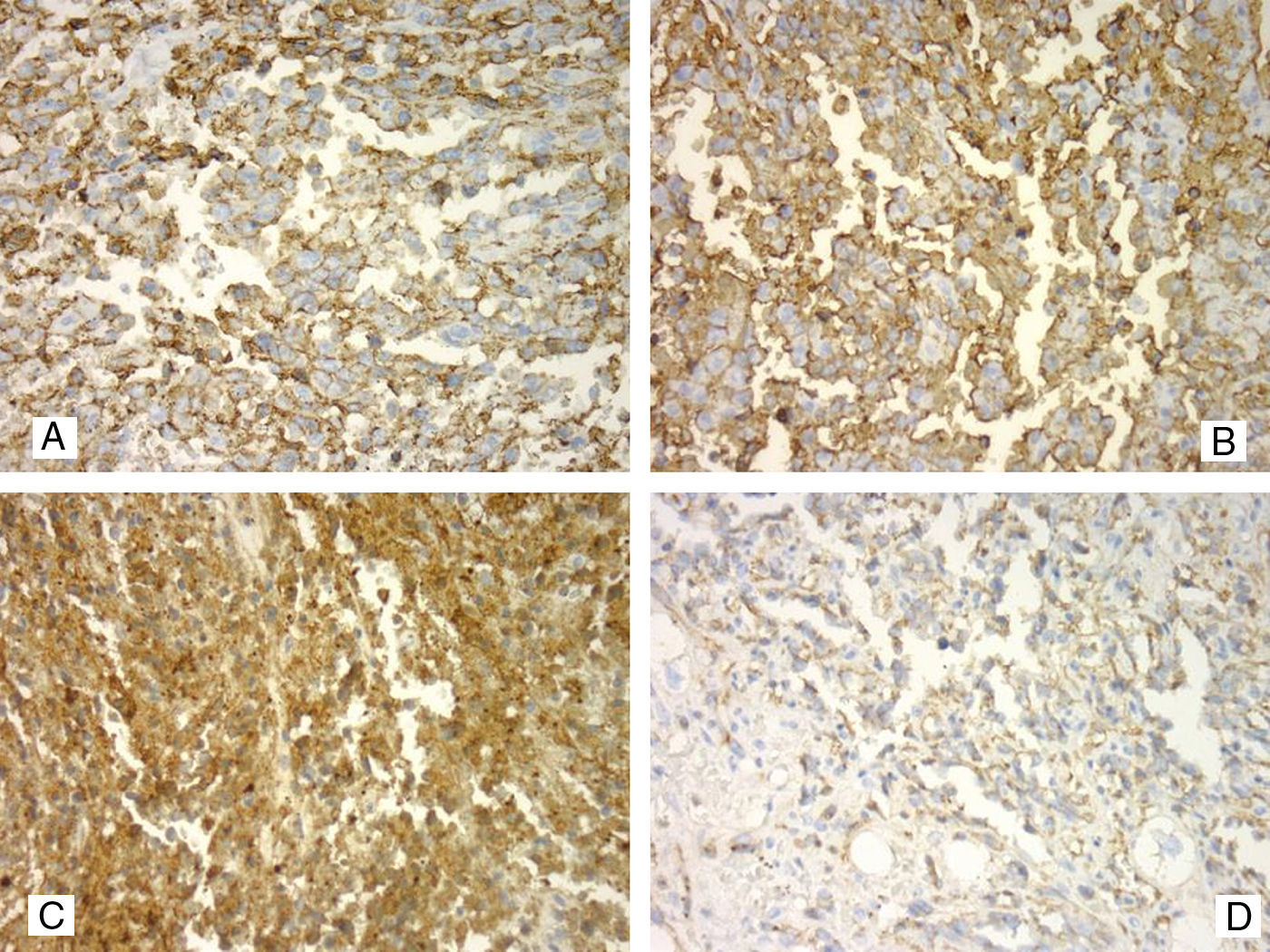
(Caso 1). A. Segundo componente del tumor constituido por una red de vasos dilatados con trombosis intraluminal, H&E 100x. B. Proliferación vascular neoplásica entremezclada con fascículos de células fusiformes que formaban hendiduras con pequeños espacios y canales vasculares, H&E 200x. C. Componente angiosarcomatoso con presencia de células tumorales fusiformes formando fascículos alrededor de los vasos con atipia nuclear y mitosis, H&E 400x. D. CD31 positivo intenso en el componente vascular; se observa positividad en los vasos dilatados así como positividad focal en el componente fusiforme y la proliferación papilar endotelial intraluminal, 200x.
Mujer de 26 años, puérpera de 21 días que ingresó con ictericia, hepatomegalia, poliserositis y un cuadro de taponamiento cardíaco, que requirió la realización de pericardiocentesis, evacuándose 1.000ml de líquido serohemático. El estudio de los parámetros de laboratorio clínico mostró anemia, leucopenia y trombocitopenia severa. La paciente falleció a las 72h posteriores al ingreso con fallo cardíaco y multiorgánico.
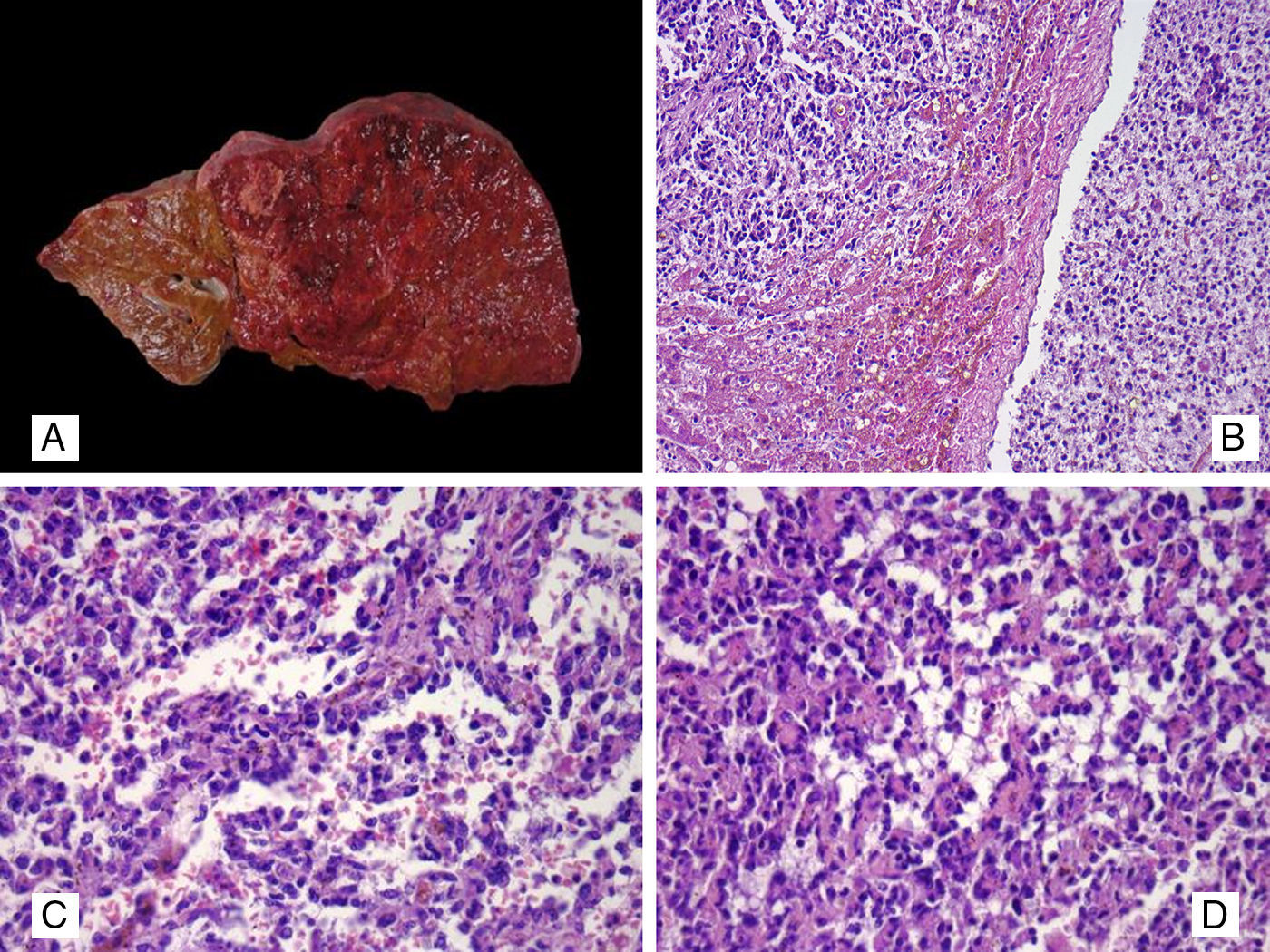
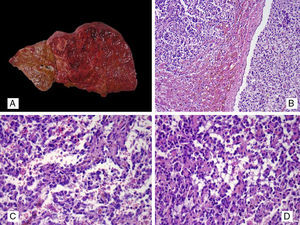
La autopsia reveló una gran tumoración hepática que comprometía más del 80% del órgano (fig. 3A) así como una enfermedad metastásica generalizada. Se observaron siembras tumorales en el diafragma así como en pericardio y pleura. En el corazón se constató una extensa infiltración de la pared de predominio derecho que engrosaba la pared del ventrículo derecho (hasta 25mm) respetando los músculos papilares. La aurícula derecha estaba infiltrada en su totalidad. El tumor se extendía por la pared de la aorta y la cava, estando infiltrados los ganglios del mediastino. Se encontraron metástasis pulmonares así como en las suprarrenales y ovario derecho.
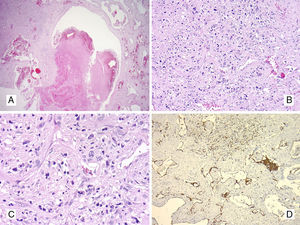
(Caso 2) A. Aspecto macroscópico del hígado mostrando una masa tumoral hemorrágica que prácticamente ocupa gran parte del parénquima hepático. B. Infiltración del parénquima hepático por angiosarcoma asociado a trombosis venosa tumoral, H&E 200x. C. Histopatología del angiosarcoma hepático con presencia de canales vasculares, proliferación endotelial papilar maligna y células tumorales sueltas en las hendiduras vasculares, H&E 400X. D. Infiltración hepática por angiosarcoma con presencia de microtrombos de fibrina, H&E 400x.
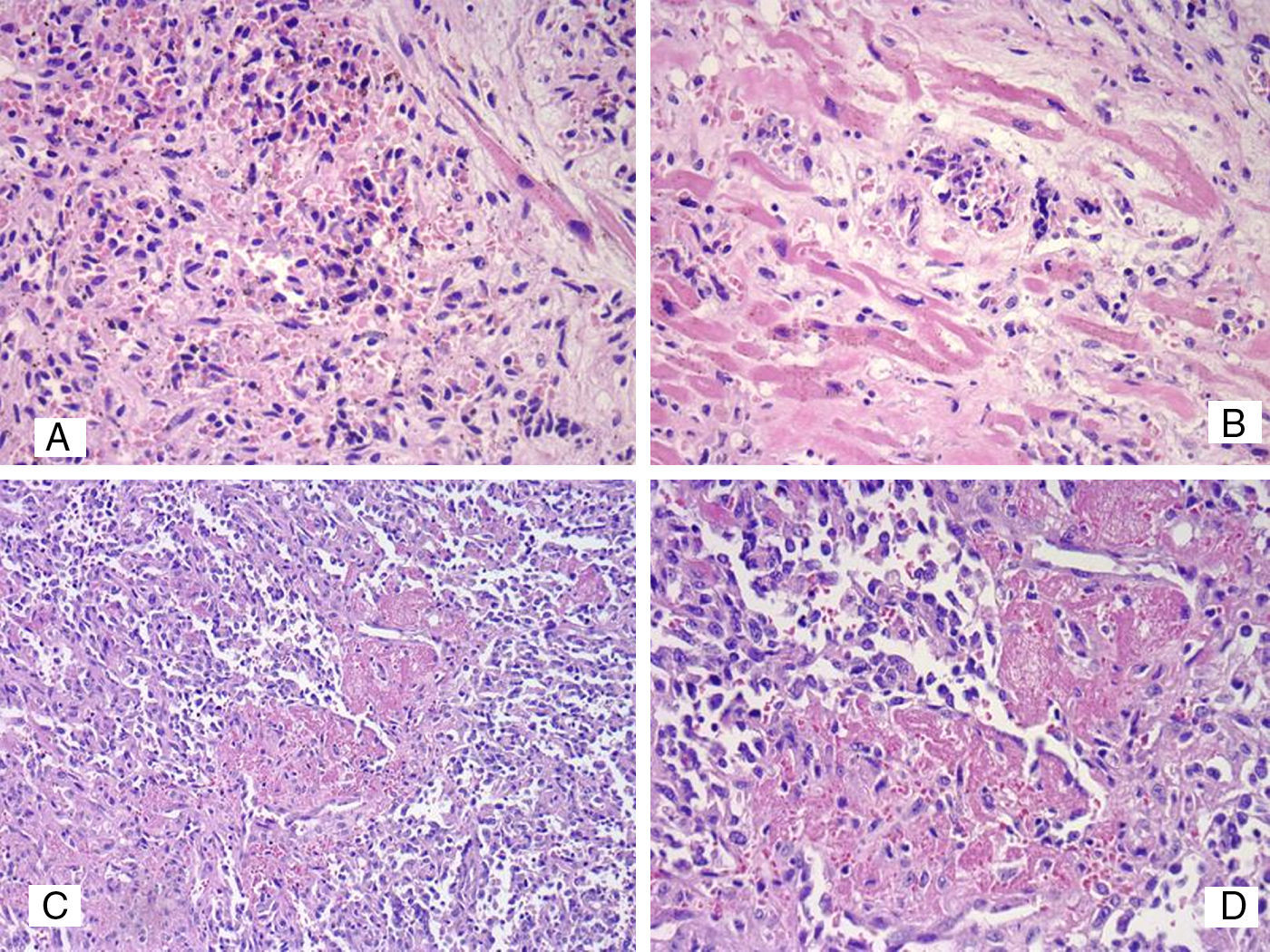
El examen histopatológico del hígado mostró una proliferación de células neoplásicas constituida por fascículos de células fusiformes que formaban hendiduras con pequeños espacios vasculares. Las células tumorales diseñaban fascículos y vasos elongados con evidente atipia endotelial que separaban los grandes canales vasculares (fig. 3B, C, D). Se observaron células neoplásicas con atipia nuclear, nucléolo y aumento de actividad mitótica. El tumor mostró extensas zonas de necrosis y hemorragia. En algunas zonas se evidenció la presencia de vacuolas citoplasmáticas englobando hematíes, así como trombosis tumoral y microtrombos de fibrina (fig. 3D). Los hallazgos morfológicos vistos en las metástasis cardíaca (fig. 4A, B), pleurales e intrabdominales tenían características microscópicas similares a los de la lesión hepática. En los cortes histológicos del corazón se observó trombosis vascular con abundante fibrina y signos histológicos correspondientes a una coagulación intravascular (fig. 4C, D). El estudio IHQ confirmó la naturaleza endotelial de la neoplasia hepática y las metástasis, mostrando intensa positividad para CD31 (fig. 5A), CD34 (fig. 5B), factor viiiI (fig. 5C) y Fli1. Con D2-40, VE-cadherina (fig. 5D) y ERG la positividad fue moderada y focal. El índice de proliferación celular fue del 30%. El diagnóstico final fue de AS de alto grado primitivo hepático con metástasis múltiples asociado a un SKM.
(Caso 2/corazón) A. Infiltración del músculo cardíaco por angiosarcoma, H&E 200x. B. Infiltración cardíaca por angiosarcoma con presencia de trombosis tumoral de vasos de pequeño y mediano calibre, H&E 400x. C y D. Histopatología del angiosarcoma metastásico en corazón con presencia de canales, hendiduras vasculares y fibrina, H&E 200x y 400x.
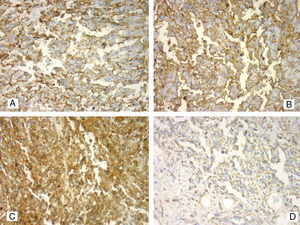
(Caso 2). A. Positividad intensa para CD31 en las células neoplásicas del angiosarcoma infiltrando el corazón, 400x. B. CD34 con positividad intensa de membrana en angiosarcoma hepático, 400x. C. Factor viii+++ en células tumorales del angiosarcoma hepático, 400x. D. Positividad moderada para VE-cadherina en infiltración cardíaca por angiosarcoma, 200x.
Los AS son neoplasias generalmente con mal pronóstico, y la asociación con SKM se observa usualmente en neoplasias avanzadas de gran tamaño que generan un secuestro de elementos formes de la sangre, principalmente plaquetas, induciendo hemorragias y evolución clínica aguda generalmente mortal1,3,16,21–28. El primer caso de SKM fue publicado en 1940; se trataba de un niño con hemangiomas y trastornos de la coagulación23. Este síndrome se ha descrito fundamentalmente en pacientes pediátricos y solo existen casos esporádicos reportados en pacientes adultos con AS22–28. El SKM constituye una forma de hemólisis microangiopática relacionada con un secuestro de plaquetas que puede aparecer en lesiones vasculares tipo malformaciones, tumores benignos (hemangiomas) y lesiones malignas (hemangioendotelioma y AS)23–26. La fisiopatología del SKM está relacionada con la proliferación del endotelio vascular dentro del tumor con activación de plaquetas y factores de coagulación que induce trombosis intratumoral. El exceso de consumo de plaquetas y factores de coagulación genera fibrinólisis que a la vez induce hemorragia intratumoral con el consiguiente incremento del tamaño del tumor vascular y mayor secuestro22–28. Además del serio problema de coagulación que generan estas lesiones, los grandes tumores vasculares con muchos vasos pueden inducir un estrés cardiovascular con insuficiencia cardíaca como ocurrió en los 2 casos descritos en el presente estudio. Los hallazgos de laboratorio más frecuentes son la anemia, trombocitopenia severa e hipofibrinogenemia23–27. La asociación de AS y SKM tiene una tasa de mortalidad aproximada del 20-40% generalmente producida por hemorragias, fallo cardíaco y sepsis22,24–26. Aunque el tratamiento óptimo del AS requiere de una exéresis quirúrgica completa con márgenes libres, no es siempre posible realizar este proceder debido a la tendencia de estas neoplasias a mostrar bordes difusos e irregulares22–28. Otras modalidades de tratamiento incluyen el uso de altas dosis de corticoides para provocar efecto antiangiogénico así como la radioterapia y/o la quimioterapia23. De cualquier manera, el pronóstico es ominoso y la supervivencia generalmente es pobre. Los 2 casos descritos en este estudio presentaban tumores vasculares de gran tamaño con trombocitopenia severa asociada y fallo cardíaco que provocó la muerte en un corto periodo de tiempo desde el diagnóstico.
Las neoplasias vasculares primarias de mediastino son raras y particularmente los AS originados en mediastino son muy infrecuentes1,3,20. Adicionalmente la coexistencia en mediastino de AS y germinoma es inusual20,29–31. El desarrollo de algunas neoplasias somáticas en TCG es un fenómeno raro pero bien conocido que puede ocurrir en neoplasias gonadales, mediastínicas e intracraneales20,30,31. La neoplasia somática puede ser, o bien un carcinoma, o bien un sarcoma. La serie más amplia de TCG asociados a sarcomas ha sido descrita por Malagón et al.20 donde los sarcomas más frecuentemente asociados a TCG fueron los rabdomiosarcomas y los AS El componente sarcomatoso en los TCG puede estar presente en el tumor primario en las recurrencia o en las metástasis, bien en combinación con el componente de tumor germinal, bien como una neoplasia independiente20. Aunque el pronóstico de los TCG depende de la localización del tumor y del estadio clínico, el estudio descrito por Malagón et al.20 muestra que la presencia de un componente sarcomatoso en un TCG augura un peor pronóstico. Particularmente la localización mediastínica de los TCG permite que puedan llegar a alcanzar mayores dimensiones antes de ser sintomáticos, lo que imposibilita muchas veces la cirugía y además incrementa el potencial de desarrollar una transformación maligna sarcomatosa en cualquier sitio del tumor. Adicionalmente, el componente sarcomatoso es usualmente más resistente a la quimioterapia convencional20.
Particularmente el primer caso de la serie actual fue diagnosticado como un AS asociado a un TCG. Varias hipótesis se han propuestos en los casos previamente descritos con esta asociación20,29. La primera sería un TCG con componente sarcomatoso tipo AS, quizá la más probable considerando la cercanía entre ambos componentes del tumor y la extensa proliferación vascular en el componente seminomatoso. Las otras 2 posibilidades incluían un TCG metastásico o un tumor de colisión que se define como la coexistencia de 2 neoplasias malignas histológicamente diferentes que ocurren en el mismo órgano sin mezclarse histológicamente. Un TCG metastásico era poco probable porque durante el estudio de extensión no se encontró neoplasia primaria en otro sitio incluyendo el examen de los testículos. Tampoco se encontró neoplasia testicular durante el estudio en la autopsia. La posibilidad de tumor de colisión o sincrónico no es posible excluirla aunque es muy infrecuente según Biernat et al.29.
En el primer caso la proliferación tumoral de células germinales enmascaró inicialmente el componente vascular maligno, sin embargo el aspecto macroscópico muy sugestivo de tumor vascular con extensa hemorragia nos hizo muestrear otras áreas del tumor donde se observó una evidente proliferación vascular maligna con trombosis.
El segundo caso fue diagnosticado como AS primario hepático con metástasis múltiples incluyendo corazón. La localización hepática no es habitual en los AS y en ocasiones el diagnóstico diferencial con tumores vasculares benignos tipo hemangioma o incluso metástasis con extensa hemorragia o vascularización pronunciada es difícil6,7,9–12. Los métodos diagnósticos citológicos o por biopsia de estos tumores implican un riesgo elevado de hemorragia.
El diagnóstico de los AS requiere una integración de los hallazgos clínicos, morfológicos, IHQ y ultraestructurales1,3,6,17. El estudio IHQ ayuda en los casos con morfología indiferenciada donde la positividad para marcadores vasculares confirma el diagnóstico de AS (CD31, CD34, CD105, ERG, VEGF, VE-cadherina, D2-40, factor viii, caveolina-A y Fli-1)1,3,4. No obstante, en algunos casos particularmente con morfología muy indiferenciada o donde la IHQ no es concluyente se pueden realizar estudios ultraestructurales que generalmente demuestran la presencia de cuerpos de Weibel-Palade, confirmando el diagnóstico de AS1,3,4,17. Aunque no existen anomalías genéticas que definan este tipo de neoplasia, recientemente se han descrito mutaciones somáticas en genes de señalización de angiogénesis como PTPRB y PLCG14. El diagnóstico diferencial se debe realizar con otras neoplasias vasculares como los hemangioendoteliomas, carcinomas sarcomatoides y otros sarcomas primarios de mediastino o hígado con prominente vascularización1-4,6.
En conclusión, la asociación de AS con SKM es de muy mal pronóstico por lo que en aquellos pacientes con diagnóstico de AS en localizaciones donde la neoplasia pueda alcanzar gran tamaño de manera paulatina es necesario una monitorización exhaustiva del recuento de plaquetas y otros elementos formes de la sangre con el objetivo de detectar tempranamente la posibilidad de evolución a un SKM y poder aplicar una conducta terapéutica adecuada.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.