Analizar los cambios histopatológicos en la mucosa gástrica de portadores de Helicobacter pylori, genotipos cagA y vacA, en 2 zonas de riesgo opuesto para cáncer gástrico en Colombia.
Materiales y métodosSe estudiaron 297 pacientes con gastritis asociadas a infección por Helicobacter pylori; 109 de la zona de riesgo alto y 107 de la zona de riesgo bajo para cáncer gástrico con toma de biopsias en antro y cuerpo gástrico; la clasificación y calificación de las gastritis se hizo según el sistema de estadificación OLGA y el sistema actualizado de Sydney. La genotipificación de Helicobacter pylori se realizó mediante PCR, a partir de extracción de ADN de biopsias. El análisis estadístico incluyó la prueba Mann-Whitney, X2, regresión lineal múltiple y regresión logística multivariada.
ResultadosLa severidad de las alteraciones histopatológicas en los pacientes infectados con los genotipos cagA y vacAs1/m1 fue mayor en la zona de riesgo alto (p≤0,05). El grado de inflamación crónica, atrofia y metaplasia es mayor en los pacientes de la zona de riesgo alto. El gen vacA se asoció a una severidad mayor de atrofia y metaplasia. En gen cagA positivo aumenta el riesgo de metaplasia intestinal en la zona de riesgo alto (OR=9,13; IC 95% 1,75-47,75).
ConclusiónLos resultados sugieren que los cambios histopatológicos resultantes de la infección gástrica por los genotipos cagA+ y vacAs1/m1 de Helicobacter pylori muestran un grado de severidad significativamente mayor de los parámetros histopatológicos en zonas de riesgo alto en comparación con las de riesgo bajo de cáncer gástrico.
To analyze histopathological changes in the gastric mucosa of carriers of Helicobacter pylori cagA and vacA in 2 areas of Columbia at risk for gastric cancer.
Materials y methods297 patients with gastritis associated with Helicobacter pylori infection were studied; 109 from a high risk area for gastric cancer and 107 from a low risk area. Biopsies were taken from the antrum and body of the stomach; the OLGA staging for gastritis and the updated Sydney system for classification of gastritis were used for their classification and grading. The Helicobacter pylori genotyping was carried out with PCR on the DNA obtained from the biopsies. Statistical analysis included the Mann-Whitney test, X2, multiple linear regression and multivariate logistic regression.
ResultsThe histopathological changes were more severe in patients infected with cagA and vacA1/m1 in the high risk area (P≤0.05). There was a higher degree of chronic inflammation, atrophy and metaplasia in the patients in the high risk area. The gene vacA was associated with more severe atrophy and metaplasia. There was an increased risk of intestinal metaplasia in patients positive for the gene cagA in the high risk area (OR=9.13; CI95% 1.75-47.75).
ConclusionsThe results suggest that the histopathological changes resulting from gastric infection with the cagA+ and vacAs1/m1 genes of Helicobacter pyloriare significantly more severe in areas of high risk for gastric cancer than in areas of low risk.
El Helicobacter pylori (H. pylori) es el agente etiológico más importante asociado a gastritis e induce una respuesta inflamatoria de tipo crónica activa que puede afectar la mucosa gástrica en toda su extensión, iniciándose en el antro1. La infección por H. pylori se asocia a lesiones secuenciales preneoplásicas en la mucosa gástrica (gastritis multifocal atrófica, metaplasia intestinal y displasia) y carcinoma gástrico, principalmente en zonas de alto riesgo para cáncer gástrico2. Los linfomas primarios de MALT también están asociados a la infección por H. pylori y pueden presentar lesiones preneoplásicas similares en la mucosa gástrica circundante3. Sin embargo, la mayor proporción del cáncer gástrico está dado por el carcinoma gástrico (95%) mientras que los linfomas y otros cánceres gástricos primarios como sarcomas y tumores neuroendocrinos son muy raros.
La severidad y la topografía de la gastritis se ha observado asociada al tipo de cepa del H. pylori4. La severidad de la respuesta inflamatoria inducida por el H. pylori es determinada por la acción de proteínas citotóxicas que sintetiza; las más reconocidas son la citotoxina asociada con el gen A (cagA) y la citotoxina vacuolizante del gen A (vacA), citoxinas que se asocian con la atrofia y la metaplasia intestinal4–6. El gen cagA, considerado el marcador de islote de patogenicidad, codifica la síntesis de la proteína citotóxica CagA, se le atribuye actividad oncogénica7 y se asocia a gastritis más severas y carcinoma gástrico6,8,9. El gen vacA está presente en todas las cepas de H. pylori, codifica la proteína citotóxica vacuolizante VacA, con mayor proporción en las cepas vacAs1/m18 que se asocia a diferentes lesiones preneoplásicas y carcinoma gástrico6,10,11. La relación entre estos genes es estrecha12,13 y la identificación del predictor de severidad en las diferentes formas de gastritis varía de acuerdo con la población estudiada13,14.
La mayor severidad de los cambios histológicos en la gastritis asociada a H. pylori se aprecian con los genotipos: cagA positivo (cagA+), vacAs1/m14,13. Las diferencias observadas en la incidencia de carcinoma gástrico podrían ser atribuidas a las expresiones variadas en la topografía de la gastritis asociada con H. pylori, apreciándose un compromiso corporal mayor de la gastritis en regiones con incidencia de carcinoma gástrico alta15 y un compromiso antral de la gastritis en regiones de incidencia baja16.
En Colombia, el cáncer gástrico es la segunda causa de muerte por cáncer en hombres y la tercera en mujeres, con una TAE de 23,4×100.000 y 12,5×100.000 respectivamente17. La heterogeneidad geográfica en el riesgo de muerte por cáncer gástrico en el país con zonas de riesgo bajo en las regiones costeras y zonas de riesgo alto en las regiones montañosas18, con TAE de mortalidad 2,8-6,0×100.000 en la Costa Atlántica y 8,1-19,6×100.000 en la zona montañosa central del país19, con diferencias culturales y étnicas propias de estas zonas, pero con prevalencia de infección por H. pylori semejante20 son circunstancias que han llevado a la búsqueda de factores de la bacteria, del huésped y del ambiente que contribuyan a explicar esta heterogeneidad. Este estudio tiene como objetivo analizar los cambios histopatológicos en la mucosa gástrica de portadores de genotipos H. pylori cagA y vacA en 2 zonas de riesgo opuesto para cáncer gástrico en Colombia.
Materiales y métodosPoblaciónLos pacientes de este estudio forman parte del proyecto «Genotipos de Helicobacter pylori, polimorfismos del huésped y factores ambientales asociados al proceso de carcinogénesis gástrica en Colombia». La metodología de ingreso de los pacientes se publicó previamente9. Brevemente, se incluyeron pacientes con dispepsia a quienes se les realizó una endoscopia digestiva alta para un diagnóstico inicial de enfermedad gastroduodenal, que asistieron a hospitales estatales e instituciones particulares en las ciudades de Bogotá y Tunja (zona de riesgo alto), y Barranquilla, Cartagena y Santa Marta (zona de riesgo bajo) entre febrero de 2000 y julio de 2008; todos los pacientes firmaron el consentimiento informado. Se incluyeron 297 pacientes, 190 de la zona de riesgo alto y 107 de la zona de riesgo bajo para cáncer gástrico, con diagnósticos de gastritis asociada a H. pylori, y con infección por H. pylori positivo por histopatología y genotipificación. Se excluyeron los pacientes con infección mixta por H. pylori (vacAs1s2 o vacAm1m2). El estudio fue aprobado por el Comité de Ética e Investigaciones del Instituto Nacional de Cancerología E.S.E.
Diagnóstico histopatológicoEn cada paciente se tomaron 6 biopsias: 3 en antro, 2 en cuerpo y una en la incisura angularis, que se fijaron en formalina neutra al 10%; se incluyeron en parafina, se realizaron cortes histológicos a 5 micras y se colorearon con hematoxilina y eosina (HE) y Giemsa, y en los casos con metaplasia intestinal con PAS Azul Alcian. La gastritis se clasificó en: gastritis no atrófica (GNA) (gastritis crónica superficial y gastritis antral difusa), gastritis multifocal atrófica sin metaplasia (GMA) y gastritis multifocal atrófica con metaplasia (MI)21. El diagnóstico histológico se estableció con base al estado más avanzado demostrado en las biopsias de cada paciente. Para la definición de parámetros histopatológicos de densidad de H. pylori, actividad, cronicidad, atrofia y metaplasia intestinal se estableció una escala nominal considerándose: 0, ausente; 1, leve; 2, moderado; y 3, severo22. Se analizaron las biopsias de antro y cuerpo de cada paciente, y el puntaje mayor fue el criterio final de análisis en cada localización.
El diagnóstico inicial fue realizado por el patólogo de cada una de las instituciones participantes, y posteriormente revisado por patólogos nacionales acreditados internacionalmente como expertos en lesiones gástricas.
Extracción de ADN y genotipificación de Helicobacter pyloriDe las biopsias de antro se extrajo el ADN, siguiendo el método de extracción con proteinasa K a 56°C durante 2h y luego se centrifugó a 10.000rpm durante 5min y se recuperó el sobrenadante que se almacenó a −20°C. La genotipificación de los genes vacA y cagA se realizó a partir del ADN extraído de las biopsias mediante PCR. Para la PCR se emplearon los iniciadores reportados en estudios previos23,24. La amplificación del gen cagA siguió las condiciones de PCR indicadas en el estudio de van Door et al. empleando la solución de ADN original y una dilución 1/1023. La amplificación del gen vacA se realizó empleando la solución de ADN inicial diluida en 1/10 para la región s, y el análisis de la región media con diluciones de 1/10 y 1/5 de la solución original de ADN, siguiendo la metodología descrita previamente25. Los productos de amplificación se verificaron en geles de agarosa al 2,5% teñidos con bromuro de etidio (0,5ug/ml) y se visualizaron bajo luz ultravioleta en un analizador de imágenes Gel Doc EQ (Biorad); posteriormente la imagen del gel se analizó con el programa QuantityOne 1-D versión 4,4 (BIo Rad).
De los 297 pacientes, se detectó la presencia del gen cagA en 297 (100%) casos; del gen vacA, el alelo s1 y s2, en 266 (89,6%) casos y el alelo m1 y m2 en 233 (78,5%) casos.
Análisis estadísticoSe utilizó la prueba Mann-Whitney para evaluar el grado de severidad de los parámetros histológicos. Las diferencias en la distribución porcentual de los parámetros histológicos se analizaron con la prueba de X2 de diferencia. El análisis de regresión lineal múltiple, con el método hacia atrás, se realizó para determinar qué factores de la bacteria estaban asociados a la severidad de los parámetros histológicos. A través de la regresión logística multivariada se obtuvo el riesgo de presentar los diferentes grados de severidad de GMA y MI en relación con la infección por los genotipos cagA y vacA de H. pylori, y con la regresión múltiple se evaluó el riesgo de presentar GMA y MI según los genotipos de H. pylori (odds ratios [OR] y su IC 95%); los diferentes modelos se ajustaron por sexo, edad, zona de riesgo y los polimorfismos IL-1B511 e IL-1RN (según resultados previos)9. Se consideró un valor significativo aquel con una p≤0,05. Se utilizó el programa estadístico SPSS versión 19.0.
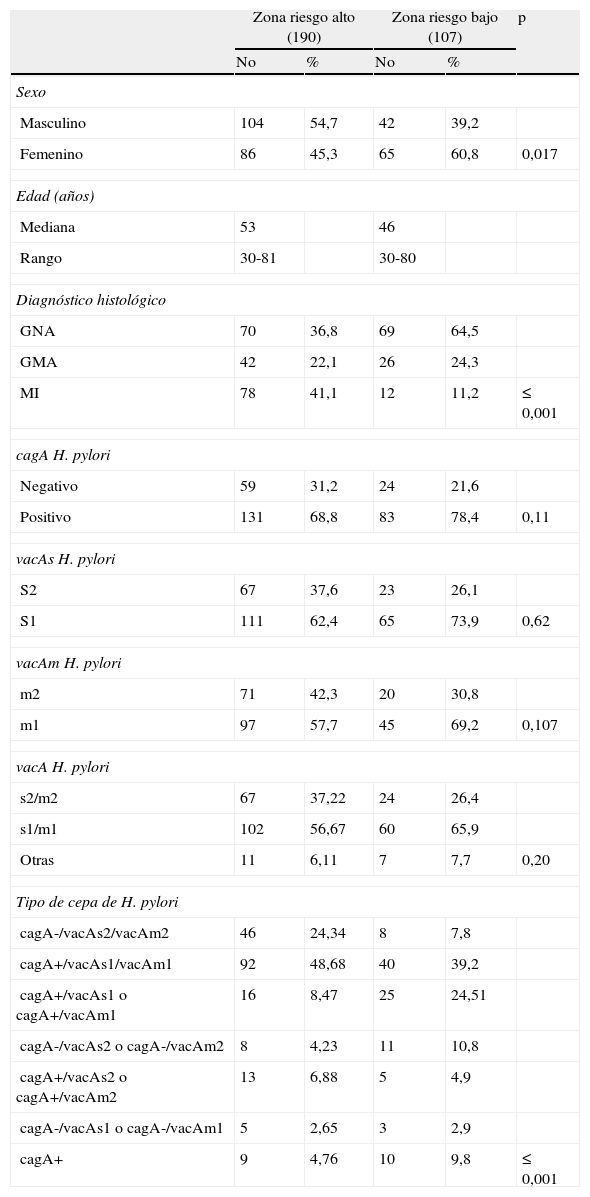
ResultadosCaracterísticas clinicopatológicas de pacientes y genotipos de Helicobacter pyloriSe analizaron 139 pacientes con GNA, 68 con GMA y 90 con MI. La frecuencia de infección por H. pylori fue similar en ambas zonas de riesgo (77,7% zona riesgo alto y 78,1% zona de riesgo bajo). La caracterización de los pacientes, genotipos y cepas de H. pylori de las zonas de riesgo alto y bajo se muestra en la tabla 1. Se halló una frecuencia mayor de cepas cagA-/vacAs2/vacAm2 y cagA+/vacAs1/vacAm1 en la zona de riego alto en comparación con la zona de riesgo bajo (p≤0,001) (tabla 1).
Características clínicas y genotipos de Helicobacter pylori en los pacientes estudiados
| Zona riesgo alto (190) | Zona riesgo bajo (107) | p | |||
| No | % | No | % | ||
| Sexo | |||||
| Masculino | 104 | 54,7 | 42 | 39,2 | |
| Femenino | 86 | 45,3 | 65 | 60,8 | 0,017 |
| Edad (años) | |||||
| Mediana | 53 | 46 | |||
| Rango | 30-81 | 30-80 | |||
| Diagnóstico histológico | |||||
| GNA | 70 | 36,8 | 69 | 64,5 | |
| GMA | 42 | 22,1 | 26 | 24,3 | |
| MI | 78 | 41,1 | 12 | 11,2 | ≤0,001 |
| cagA H. pylori | |||||
| Negativo | 59 | 31,2 | 24 | 21,6 | |
| Positivo | 131 | 68,8 | 83 | 78,4 | 0,11 |
| vacAs H. pylori | |||||
| S2 | 67 | 37,6 | 23 | 26,1 | |
| S1 | 111 | 62,4 | 65 | 73,9 | 0,62 |
| vacAm H. pylori | |||||
| m2 | 71 | 42,3 | 20 | 30,8 | |
| m1 | 97 | 57,7 | 45 | 69,2 | 0,107 |
| vacA H. pylori | |||||
| s2/m2 | 67 | 37,22 | 24 | 26,4 | |
| s1/m1 | 102 | 56,67 | 60 | 65,9 | |
| Otras | 11 | 6,11 | 7 | 7,7 | 0,20 |
| Tipo de cepa de H. pylori | |||||
| cagA-/vacAs2/vacAm2 | 46 | 24,34 | 8 | 7,8 | |
| cagA+/vacAs1/vacAm1 | 92 | 48,68 | 40 | 39,2 | |
| cagA+/vacAs1 o cagA+/vacAm1 | 16 | 8,47 | 25 | 24,51 | |
| cagA-/vacAs2 o cagA-/vacAm2 | 8 | 4,23 | 11 | 10,8 | |
| cagA+/vacAs2 o cagA+/vacAm2 | 13 | 6,88 | 5 | 4,9 | |
| cagA-/vacAs1 o cagA-/vacAm1 | 5 | 2,65 | 3 | 2,9 | |
| cagA+ | 9 | 4,76 | 10 | 9,8 | ≤0,001 |
p: X2 de diferencia.
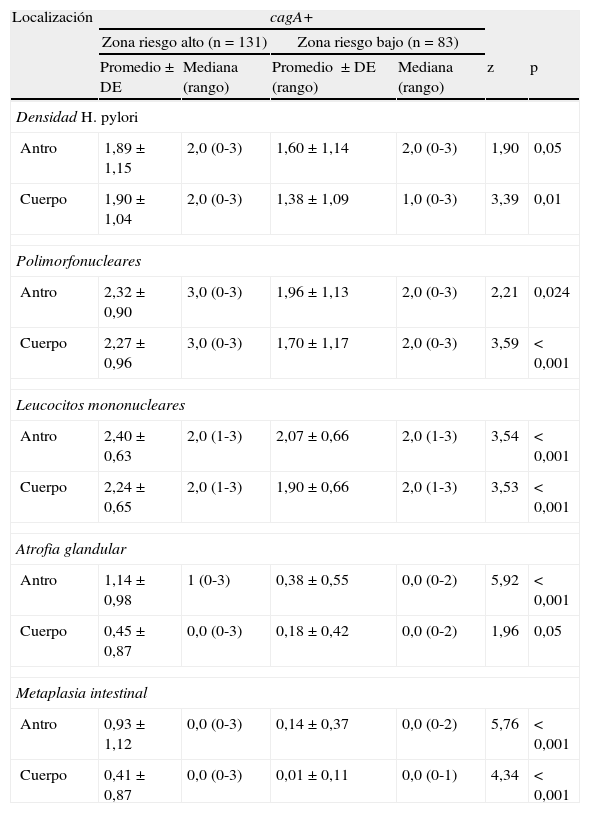
La mayor actividad, cronicidad, atrofia y metaplasia intestinal en antro y cuerpo se encontró asociada a la infección por genotipos cagA+, vacAs1 y vacAm1 (p≤0,001); y en relación con la densidad de H. pylori, esta fue mayor en pacientes infectados con el genotipo cagA+ al ser comparados con el cagA-, no así con los otros genotipos del gen vacA.
La expresión de los diferentes parámetros histológicos en pacientes infectados con el genotipo cagA+, en antro y cuerpo, fue mayor en la zona de riesgo alto. La respuesta de polimorfonucleares (en cuerpo) y de mononucleares (en antro y cuerpo), la atrofia (en antro) y la metaplasia intestinal (en antro y cuerpo) asociadas con los genotipos vacAs1 y vacAm1 fue mayor en pacientes de la zona de riesgo alto en relación con los pacientes de la zona de riesgo bajo (tabla 2).
Parámetros histopatológicos y su relación con los genotipos de Helicobacter pylori según localización gástrica y zona de riesgo en pacientes con gastritis
| Localización | cagA+ | |||||
| Zona riesgo alto (n=131) | Zona riesgo bajo (n=83) | |||||
| Promedio±DE | Mediana (rango) | Promedio ±DE (rango) | Mediana (rango) | z | p | |
| Densidad H. pylori | ||||||
| Antro | 1,89±1,15 | 2,0 (0-3) | 1,60±1,14 | 2,0 (0-3) | 1,90 | 0,05 |
| Cuerpo | 1,90±1,04 | 2,0 (0-3) | 1,38±1,09 | 1,0 (0-3) | 3,39 | 0,01 |
| Polimorfonucleares | ||||||
| Antro | 2,32±0,90 | 3,0 (0-3) | 1,96±1,13 | 2,0 (0-3) | 2,21 | 0,024 |
| Cuerpo | 2,27±0,96 | 3,0 (0-3) | 1,70±1,17 | 2,0 (0-3) | 3,59 | <0,001 |
| Leucocitos mononucleares | ||||||
| Antro | 2,40±0,63 | 2,0 (1-3) | 2,07±0,66 | 2,0 (1-3) | 3,54 | <0,001 |
| Cuerpo | 2,24±0,65 | 2,0 (1-3) | 1,90±0,66 | 2,0 (1-3) | 3,53 | <0,001 |
| Atrofia glandular | ||||||
| Antro | 1,14±0,98 | 1 (0-3) | 0,38±0,55 | 0,0 (0-2) | 5,92 | <0,001 |
| Cuerpo | 0,45±0,87 | 0,0 (0-3) | 0,18±0,42 | 0,0 (0-2) | 1,96 | 0,05 |
| Metaplasia intestinal | ||||||
| Antro | 0,93±1,12 | 0,0 (0-3) | 0,14±0,37 | 0,0 (0-2) | 5,76 | <0,001 |
| Cuerpo | 0,41±0,87 | 0,0 (0-3) | 0,01±0,11 | 0,0 (0-1) | 4,34 | <0,001 |
| Localización | vacAs1 | |||||
| Zona riesgo alto (n=111) | Zona riesgo bajo (n=67) | |||||
| Promedio±DE | Mediana (rango) | Promedio ±DE (rango) | Mediana (rango) | z | P | |
| Densidad H. pylori | ||||||
| Antro | 1,98±1,12 | 2,0 (0-3) | 1,75±1,12 | 2,0 (0-3) | 1,47 | 0,143 |
| Cuerpo | 1,97±1,03 | 2,0 (0-3) | 1,53±1,08 | 1,0 (0-3) | 2,59 | 0,01 |
| Polimorfonucleares | ||||||
| Antro | 2,41±0,82 | 3,0 (0-3) | 2,17±1,06 | 3,0 (0-3) | 1,10 | 0,27 |
| Cuerpo | 2,37±0,89 | 3,0 (0-3) | 1,95±1,03 | 2,0 (0-3) | 2,68 | 0,007 |
| Leucocitos mononucleares | ||||||
| Antro | 2,46±0,58 | 3,0 (1-3) | 2,13±0,65 | 2,0 (1-3) | 3,29 | 0,001 |
| Cuerpo | 2,31±0,61 | 2,0 (1-3) | 2,02±0,64 | 2,0 (1-3) | 2,84 | 0,005 |
| Atrofia glandular | ||||||
| Antro | 1,12±1,00 | 1,0 (0-3) | 0,48±0,66 | 0,0 (0-3) | 4,29 | <0,001 |
| Cuerpo | 0,47±0,89 | 0,0 (0-2) | 0,23±0,50 | 0,0 (0-2) | 1,41 | 0,157 |
| Metaplasia intestinal | ||||||
| Antro | 0,91±1,14 | 0,0 (0-3) | 0,14±0,39 | 0,0 (0-2) | 4,88 | <0,001 |
| Cuerpo | 0,41±0,87 | 0,0 (0-3) | 0,03±0,17 | 0,0 (0-1) | 3,39 | 0,001 |
| Localización | vacAm1 | |||||
| Zona riesgo alto (n=97) | Zona riesgo bajo (n=46) | |||||
| Promedio±DE | Mediana (rango) | Promedio ±DE (rango) | Mediana (rango) | z | P | |
| Densidad H. Pylori | ||||||
| Antro | 1,93±1,12 | 2,0 (0-3) | 1,94±1,21 | 2,0 (0-3) | 0,39 | 0,69 |
| Cuerpo | 1,89±1,01 | 2,0 (0-3) | 1,53±1,16 | 2,0 (0-3) | 1,70 | 0,08 |
| Polimorfonucleares | ||||||
| Antro | 2,39±0,84 | 3,0 (0-3) | 2,09±1,19 | 3,0 (0-3) | 0,87 | 0,38 |
| Cuerpo | 2,39±0,87 | 3,0 (0-3) | 1,84±1,20 | 2,0 (0-3) | 2,62 | 0,01 |
| Leucocitos mononucleares | ||||||
| Antro | 2,4±0,59 | 3,0 (1-3) | 2,00±0,65 | 2,0 (1-3) | 3,74 | <0,001 |
| Cuerpo | 2,32±0,63 | 2,0 (1-3) | 1,98±0,70 | 2,0 (1-3) | 2,70 | 0,01 |
| Atrofia glandular | ||||||
| Antro | 1,10±1,00 | 1,0 (0-3) | 0,48±0,69 | 0,0 (0-3) | 3,68 | <0,001 |
| Cuerpo | 0,54±0,96 | 0,0 (0-3) | 0,26±0,54 | 0,0 (0-2) | 1,36 | 0,17 |
| Metaplasia intestinal | ||||||
| Antro | 0,93±1,13 | 0,0 (0-3) | 0,16±0,43 | 0,0 (0-2) | 4,08 | <0,001 |
| Cuerpo | 0,50±0,98 | 0,0 (0-3) | 0,05±0,21 | 0,0 (0-1) | 3,00 | 0,003 |
p de la prueba de Mann-Whitney.
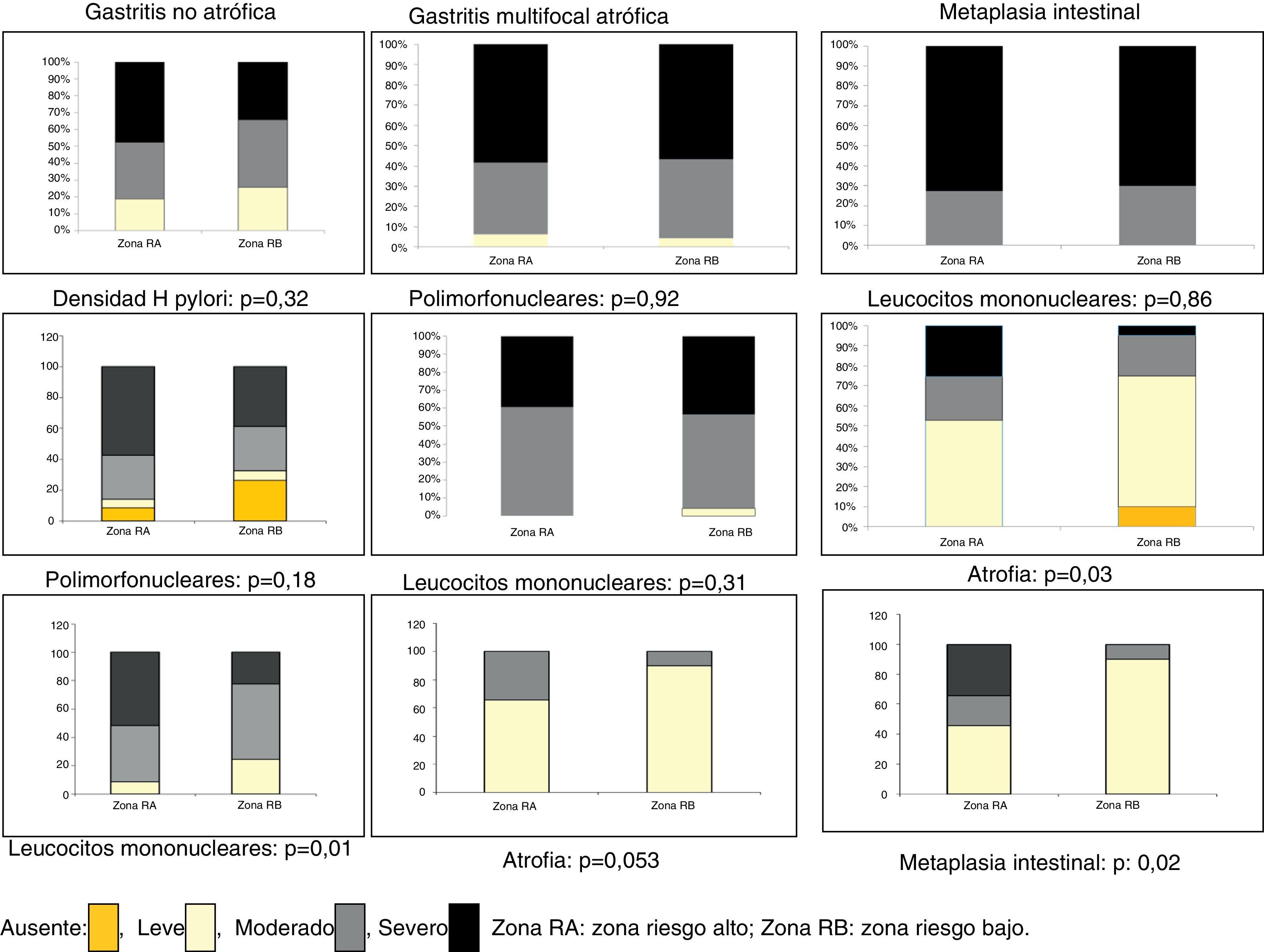
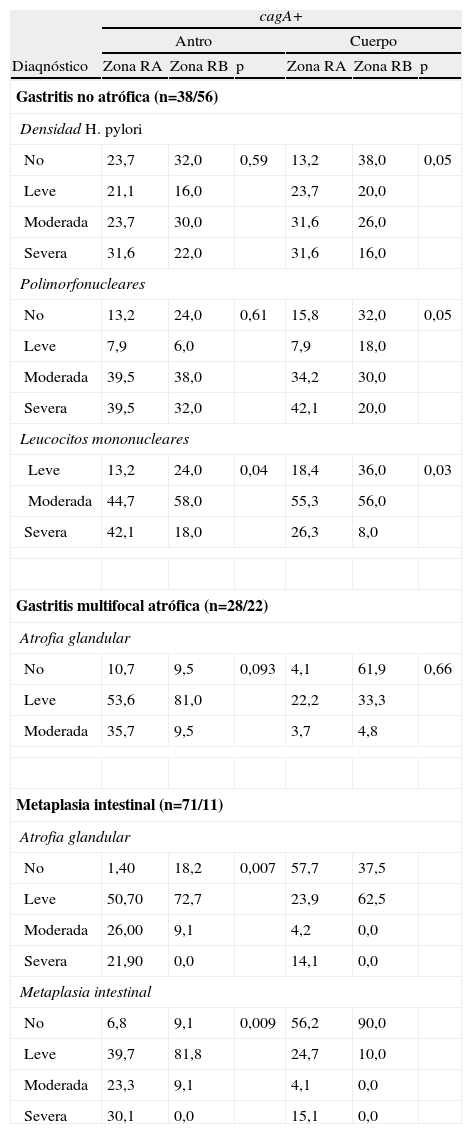
La distribución de la densidad de H. pylori en los pacientes con GNA fue similar en las 2 zonas de riesgo (fig. 1); se observó igual resultado para la GMA y la MI (resultados no mostrados). El análisis por genotipo mostró que los pacientes de la zona de riesgo alto con GNA e infectados con el genotipo cagA+ presentaron una frecuencia mayor de grado severo de densidad de H. pylori en el cuerpo en comparación con los pacientes de la zona de riesgo bajo (31,6-16,0% respectivamente) (tabla 3); ninguna diferencia se observó con los genotipos vacAs1 y vacAm1. En los pacientes con GMA y MI no se observó diferencias entre los genotipos de H. pylori con la densidad de H. pylori.
Severidad de los parámetros histopatológicos y su relación con los genotipos de Helicobacter pylori según diagnóstico histológico y zona de riesgo
| cagA+ | ||||||
| Antro | Cuerpo | |||||
| Diaqnóstico | Zona RA | Zona RB | p | Zona RA | Zona RB | p |
| Gastritis no atrófica (n=38/56) | ||||||
| Densidad H. pylori | ||||||
| No | 23,7 | 32,0 | 0,59 | 13,2 | 38,0 | 0,05 |
| Leve | 21,1 | 16,0 | 23,7 | 20,0 | ||
| Moderada | 23,7 | 30,0 | 31,6 | 26,0 | ||
| Severa | 31,6 | 22,0 | 31,6 | 16,0 | ||
| Polimorfonucleares | ||||||
| No | 13,2 | 24,0 | 0,61 | 15,8 | 32,0 | 0,05 |
| Leve | 7,9 | 6,0 | 7,9 | 18,0 | ||
| Moderada | 39,5 | 38,0 | 34,2 | 30,0 | ||
| Severa | 39,5 | 32,0 | 42,1 | 20,0 | ||
| Leucocitos mononucleares | ||||||
| Leve | 13,2 | 24,0 | 0,04 | 18,4 | 36,0 | 0,03 |
| Moderada | 44,7 | 58,0 | 55,3 | 56,0 | ||
| Severa | 42,1 | 18,0 | 26,3 | 8,0 | ||
| Gastritis multifocal atrófica (n=28/22) | ||||||
| Atrofia glandular | ||||||
| No | 10,7 | 9,5 | 0,093 | 4,1 | 61,9 | 0,66 |
| Leve | 53,6 | 81,0 | 22,2 | 33,3 | ||
| Moderada | 35,7 | 9,5 | 3,7 | 4,8 | ||
| Metaplasia intestinal (n=71/11) | ||||||
| Atrofia glandular | ||||||
| No | 1,40 | 18,2 | 0,007 | 57,7 | 37,5 | |
| Leve | 50,70 | 72,7 | 23,9 | 62,5 | ||
| Moderada | 26,00 | 9,1 | 4,2 | 0,0 | ||
| Severa | 21,90 | 0,0 | 14,1 | 0,0 | ||
| Metaplasia intestinal | ||||||
| No | 6,8 | 9,1 | 0,009 | 56,2 | 90,0 | |
| Leve | 39,7 | 81,8 | 24,7 | 10,0 | ||
| Moderada | 23,3 | 9,1 | 4,1 | 0,0 | ||
| Severa | 30,1 | 0,0 | 15,1 | 0,0 | ||
| vacAs1 | ||||||
| Antro | Cuerpo | |||||
| Diaqnóstico | Zona RA | Zona RB | P | Zona RA | Zona RB | p |
| Gastritis no atrófica (n=32/39) | ||||||
| Densidad H. Pylori | ||||||
| No | 25,0 | 27,0 | 0,53 | 15,6 | 28,6 | 0,64 |
| Leve | 25,0 | 16,2 | 28,1 | 22,9 | ||
| Moderada | 18,8 | 32,4 | 28,1 | 25,7 | ||
| Severa | 31,3 | 24,3 | 28,1 | 22,9 | ||
| Polimorfonucleares | ||||||
| No | 12,5 | 16,2 | 0,97 | 15,6 | 17,1 | 0,2 |
| Leve | 9,4 | 8,1 | 12,5 | 22,9 | ||
| Moderada | 37,5 | 35,1 | 25 | 37,1 | ||
| Severa | 40,6 | 40,5 | 46,9 | 22,9 | ||
| Leucocitos mononucleares | ||||||
| Leve | 9,4 | 18,9 | 0,11 | 15,6 | 25,7 | 0,12 |
| Moderada | 50,0 | 62,2 | 53,1 | 62,9 | ||
| Severa | 40,6 | 18,9 | 31,33 | 11,4 | ||
| Gastritis multifocal atrófica (n=23/20) | ||||||
| Atrofia glandular | ||||||
| No | 13,0 | 5,3 | 0,08 | 72,7 | 68,4 | 0,95 |
| Leve | 52,2 | 84,2 | 22,7 | 26,3 | ||
| Moderada | 34,8 | 10,5 | 4,5 | 5,3 | ||
| Metaplasia intestinal (N=56/9) | ||||||
| Atrofia glandular | ||||||
| No | 1,8 | 11,1 | 0,28 | 54,5 | 25,0 | 0,05 |
| Leve | 50,0 | 66,7 | 27,3 | 62,5 | ||
| Moderada | 23,2 | 11,1 | 1,8 | 12,5 | ||
| Severa | 25,0 | 11,1 | 16,4 | 0,0 | ||
| Metaplasia intestinal | ||||||
| No | 7,1 | 11,1 | 0,09 | 55,4 | 77,8 | |
| Leve | 37,5 | 77,8 | 25,0 | 22,2 | ||
| Moderada | 23,2 | 11,1 | 3,6 | 0,0 | ||
| Severa | 32,1 | 0,0 | 16,1 | 0,0 | ||
| vacAm1 | ||||||
| Antro | Cuerpo | |||||
| Diaqnóstico | Zona RA | Zona RB | p | Zona RA | Zona RB | P |
| Gastritis no atrófica (n=28/27) | ||||||
| Densidad H. Pylori | ||||||
| No | 21,4 | 32,0 | 0,38 | 14,3 | 36,0 | 0,19 |
| Leve | 25 | 8,0 | 28,6 | 12,0 | ||
| Moderada | 21,4 | 28,0 | 28,6 | 20,0 | ||
| Severa | 32,1 | 32,0 | 28,6 | 32,0 | ||
| Polimorfonucleares | ||||||
| No | 14,3 | 28,0 | 0,53 | 14,3 | 32,0 | 0,29 |
| Leve | 3,6 | 4,0 | 10,7 | 16,0 | ||
| Moderada | 39,2 | 24,0 | 25,0 | 24,0 | ||
| Severa | 42,9 | 44,0 | 50,0 | 28,0 | ||
| Leucocitos polimorfonucleares | ||||||
| Leve | 10,7 | 32,0 | 0,009 | 17,9 | 40,0 | 0,03 |
| Moderada | 46,4 | 60,0 | 46,4 | 52,0 | ||
| Severa | 42,9 | 8,0 | 35,7 | 8,0 | ||
| Gastritis multifocal atrófica (n=20/13) | ||||||
| Atrofia glandular | ||||||
| No | 15,0 | 8,3 | 0,24 | 68,4 | 66,7 | 0,94 |
| Leve | 55,0 | 83,3 | 26,3 | 25,0 | ||
| Moderada | 30,0 | 8,3 | 5,3 | 8,3 | ||
| Metaplasia intestinal (n=52/7) | ||||||
| Atrofia glandular | ||||||
| No | 1,9 | 14,3 | 0,36 | 56,0 | 16,7 | 0,03 |
| Leve | 53,8 | 57,1 | 26,0 | 66,7 | ||
| Moderada | 19,2 | 14,3 | 2,0 | 16,7 | ||
| Severa | 25,0 | 14,3 | 20,0 | 0,0 | ||
| Metaplasia intestinal (n=28/27) | ||||||
| No | 7,7 | 14,3 | 0,2 | 50 | 71,4 | |
| Leve | 36,5 | 71,4 | 25,0 | 28,6 | ||
| Moderada | 25,0 | 14,3 | 3,8 | 0,0 | ||
| Severa | 30,8 | 0,0 | 21,2 | 0,0 | ||
p: X2 de diferencia.
La actividad inflamatoria no presentó diferencias en los pacientes con GNA, GMA (fig. 1), ni MI entre las 2 zonas. Tener una infección por H. pylori cagA+ aumenta la actividad inflamatoria crónica en el cuerpo gástrico de los pacientes con GNA de la zona de riesgo alto (42,1%, 20,0% respectivamente) en comparación con los de la zona de riesgo bajo; no se hallaron otras diferencias entre los polimorfonucleares en pacientes infectados con los genotipos del gen vacA (tabla 3), ni en los pacientes con GMA o MI.
Infiltrado por mononuclearesEl grado severo de inflamación crónica fue mayor en los pacientes con GNA de la zona de riesgo alto (51,4%) en comparación con los de la zona de riesgo bajo (22,4%), y no se observó diferencias en los pacientes con GMA ni MI (fig. 1). El análisis por los genotipos de H. pylori mostró que los pacientes con GNA infectados con los genotipos cagA+ y vacAm1 en antro y cuerpo de la zona de riesgo alto tuvieron un puntaje severo mayor en comparación con los pacientes de la zona de riesgo bajo (p<0,05) (tabla 3), ninguna otra diferencia se halló en los pacientes con GMA y MI.
Atrofia glandularLa atrofia se localizó en: un 77,6% (52) en antro; un 9,0% (6) en cuerpo y un 13,4% (10) en antro y cuerpo; no hubo diferencias en la localización según zona de riesgo (p=0,47).
La atrofia se encontró en grados leve y moderado en los pacientes con GMA en las 2 zonas, con una proporción mayor de la atrofia de grado moderado en la zona de riesgo alto (fig. 1). La atrofia de grado severo se presentó en los pacientes con MI, con una proporción mayor en los pacientes de la zona de riesgo alto; la atrofia de grado severo se halló en un paciente de la zona de riesgo bajo (fig. 1). No se observaron diferencias en la severidad de la atrofia en relación con los genotipos de H. pylori en los pacientes con GMA (tabla 3).
Metaplasia intestinalLa metaplasia intestinal se localizó en: un 61,1% (55) en antro, un 7,8% (7) en cuerpo y un 31,1% (28) en antro y cuerpo. La localización de la MI en antro y cuerpo simultáneamente fue mayor (34,6%) en la zona de riesgo alto en comparación con la zona de riesgo bajo (8,3%) (p≤0,001).
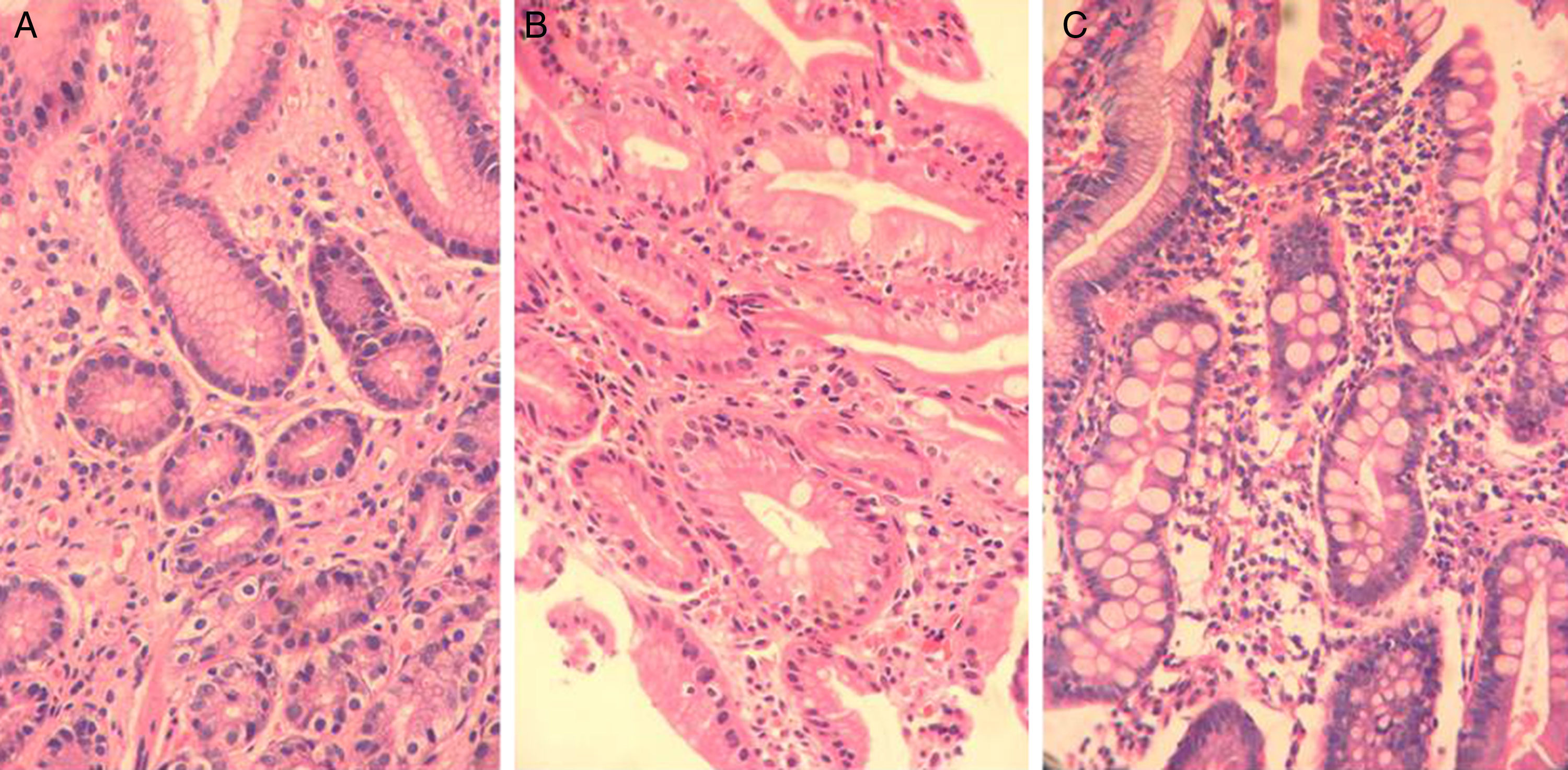
En los pacientes con MI de la zona de riesgo bajo no se halló el grado severo en antro ni en cuerpo, ni el grado moderado en el cuerpo. El grado de severidad de la MI fue mayor en los pacientes de la zona de riesgo alto (fig. 1) (fig. 2), al igual que lo observado por cada genotipo de H. pylori (tabla 3).
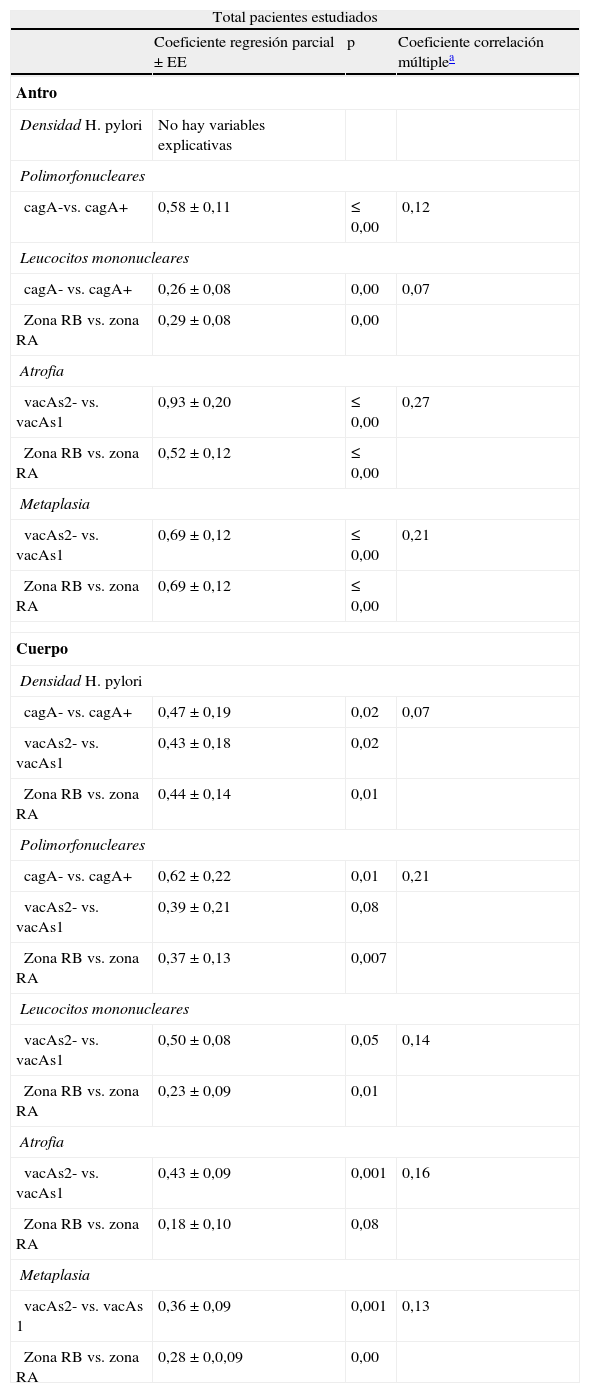
Factores asociados a la severidad histológica según topografía de la gastritisLos coeficientes de regresión del genotipo cagA+ indican puntajes más altos significativos en comparación con el genotipo cagA- en: la densidad de H. pylori en cuerpo, la infiltración de polimorfonucleares en antro y cuerpo, y los leucocitos mononucleares en antro. Los coeficientes de regresión del genotipo vacAs1 mostraron puntajes más altos en comparación con el genotipo vacAs2 en: los polimorfonucleares y los leucocitos mononucleares en cuerpo, y la atrofia y la metaplasia intestinal en antro y cuerpo. Se observó que los coeficientes de regresión del genotipo vacAm1 en relación con el genotipo vacAm2 presentaron un puntaje mayor en la densidad de H. pylori en cuerpo y la atrofia en el antro (tabla 4).
Genotipos de Helicobacter pylori asociados a la severidad de los parámetros histológicos según topografía gástrica
| Total pacientes estudiados | |||
| Coeficiente regresión parcial±EE | p | Coeficiente correlación múltiplea | |
| Antro | |||
| Densidad H. pylori | No hay variables explicativas | ||
| Polimorfonucleares | |||
| cagA-vs. cagA+ | 0,58±0,11 | ≤0,00 | 0,12 |
| Leucocitos mononucleares | |||
| cagA- vs. cagA+ | 0,26±0,08 | 0,00 | 0,07 |
| Zona RB vs. zona RA | 0,29±0,08 | 0,00 | |
| Atrofia | |||
| vacAs2- vs. vacAs1 | 0,93±0,20 | ≤0,00 | 0,27 |
| Zona RB vs. zona RA | 0,52±0,12 | ≤0,00 | |
| Metaplasia | |||
| vacAs2- vs. vacAs1 | 0,69±0,12 | ≤0,00 | 0,21 |
| Zona RB vs. zona RA | 0,69±0,12 | ≤0,00 | |
| Cuerpo | |||
| Densidad H. pylori | |||
| cagA- vs. cagA+ | 0,47±0,19 | 0,02 | 0,07 |
| vacAs2- vs. vacAs1 | 0,43±0,18 | 0,02 | |
| Zona RB vs. zona RA | 0,44±0,14 | 0,01 | |
| Polimorfonucleares | |||
| cagA- vs. cagA+ | 0,62±0,22 | 0,01 | 0,21 |
| vacAs2- vs. vacAs1 | 0,39±0,21 | 0,08 | |
| Zona RB vs. zona RA | 0,37±0,13 | 0,007 | |
| Leucocitos mononucleares | |||
| vacAs2- vs. vacAs1 | 0,50±0,08 | 0,05 | 0,14 |
| Zona RB vs. zona RA | 0,23±0,09 | 0,01 | |
| Atrofia | |||
| vacAs2- vs. vacAs1 | 0,43±0,09 | 0,001 | 0,16 |
| Zona RB vs. zona RA | 0,18±0,10 | 0,08 | |
| Metaplasia | |||
| vacAs2- vs. vacAs 1 | 0,36±0,09 | 0,001 | 0,13 |
| Zona RB vs. zona RA | 0,28±0,0,09 | 0,00 | |
| Zona de riesgo alto | |||
| Coeficiente regresión parcial±EE | p | Coeficiente correlación múltiplea | |
| Antro | |||
| Densidad H. pylori | No hay variables explicativas | ||
| Polimorfonucleares | |||
| cagA- vs. cagA+ | 0,54±0,13 | ≤0,00 | 0,10 |
| Leucocitos mononucleares | |||
| cagA- vs. cagA+ | 0,27±0,09 | ≤0,02 | 0,05 |
| Atrofia | |||
| vacAs2- vs. vacAs1 | 0,75±0,33 | ≤0,02 | 0,25 |
| Metaplasia | |||
| vacAs2- vs. vacAs1 | 0,87±0,15 | ≤0,00 | 0,22 |
| Cuerpo | |||
| Densidad H. pylori | No hay variables explicativas significativas | ||
| Polimorfonucleares | |||
| cagA- vs. cagA+ | 0,61±0,24 | 0,01 | 0,23 |
| vacAs2- vs. vacAs1 | 0,39±0,23 | 0,09 | |
| Leucocitos mononucleares | |||
| vacAs2- vs. vacAs1 | 0,53±0,09 | ≤0,001 | 0,16 |
| Atrofia | |||
| vacAm2- vs. vacAm1 | 0,48±0,11 | ≤0,001 | 0,18 |
| Metaplasia | |||
| vacAm2- vs. vacAm1 | 0,44±0,10 | 0,001 | 0,17 |
| Zona de riesgo bajo | |||
| Coeficiente regresión parcial±EE | p | Coeficiente correlación múltiplea | |
| Antro | |||
| Densidad H. pylori | No hay variables explicativas | ||
| Polimorfonucleares | |||
| cagA- vs. cagA+ | 0,78±0,29 | 0,009 | 0,25 |
| Leucocitos mononucleares | |||
| cagA- vs. cagA+ | 0,50±0,22 | 0,02 | 0,10 |
| vacAs2- vs. vacAs1 | 0,37±0,18 | 0,04 | |
| Atrofia | |||
| cagA- vs. cagA+ | 0,68±0,31 | 0,030 | 0,15 |
| vacAs2- vs. vacAs1 | 0,70±0,30 | 0,02 | |
| Metaplasia | No hay variables explicativas | ||
| Cuerpo | |||
| Densidad H. pylori | No hay variables explicativas significativas | ||
| Polimorfonucleares | |||
| vacAs2- vs. vacAs1 | 0,91±0,31 | 0,006 | 0,26 |
| Leucocitos mononucleares | No hay variables explicativas significativas | ||
| Atrofia | |||
| vacAs2- vs. vacAs 1 | 0,82±0,24 | ≤0,002 | 0,23 |
| cagA- vs. cagA+ | 0,73±0,27 | ≤0,007 | |
| Metaplasia | |||
| cagA- vs. cagA+ | 0,37±0,10 | 0,001 | 0,19 |
| vacAs2- vs. vacAs1 | 0,33±0,10 | 0,002 | |
Los diferentes genotipos de H. pylori explican entre un 7 hasta un 23% la respuesta inflamatoria, la atrofia y la metaplasia en las 2 zonas (tabla 4).
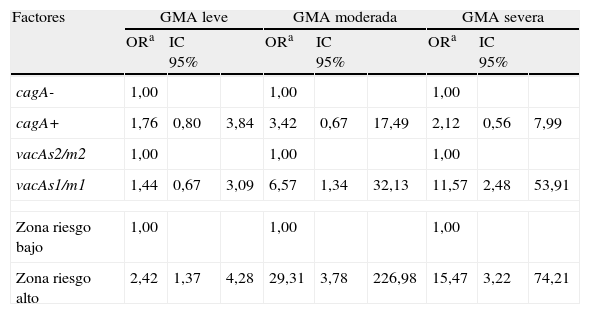
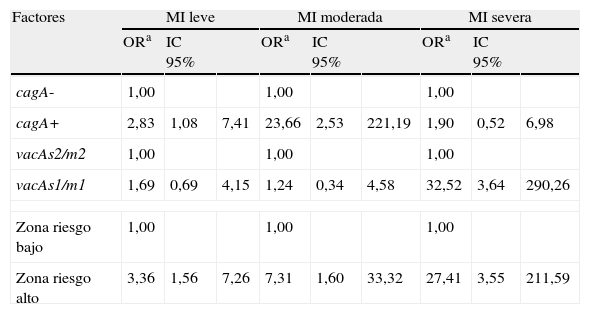
Genotipos de Helicobacter pylori y su asociación con atrofia y metaplasia intestinalEl genotipo cagA+ se identificó como un factor independiente asociado a la MI en la zona de riesgo alto (OR ajustado=9,13; IC 95% 1,75-47,75). El genotipo vacAs1 se asoció a la MI en la zona de riesgo alto y a las lesiones preneoplásicas en la zona de riesgo bajo, aunque no en forma significativa (OR=8,34; IC 95% 0,65-107,24 y OR=32,03; IC 9%% 0,93-115,49 respectivamente); se asumió conjuntamente los pacientes con GMA y MI de la zona de riesgo bajo como lesiones preneoplásicas por el número escaso de casos de cada entidad diagnóstica. Los genotipos vacAs1/m1 se asociaron a un mayor riesgo de presentar atrofia de grado moderado y severo (tabla 5a) y MI de grado severo (tabla 5b). El genotipo cagA+ se asoció a un riesgo mayor de presentar MI de grado leve y moderado (tabla 5b).
Asociación de los genotipos de Helicobacter pylori y zona de riesgo al grado de severidad de la gastritis multifocal atrófica
| Factores | GMA leve | GMA moderada | GMA severa | ||||||
| ORa | IC 95% | ORa | IC 95% | ORa | IC 95% | ||||
| cagA- | 1,00 | 1,00 | 1,00 | ||||||
| cagA+ | 1,76 | 0,80 | 3,84 | 3,42 | 0,67 | 17,49 | 2,12 | 0,56 | 7,99 |
| vacAs2/m2 | 1,00 | 1,00 | 1,00 | ||||||
| vacAs1/m1 | 1,44 | 0,67 | 3,09 | 6,57 | 1,34 | 32,13 | 11,57 | 2,48 | 53,91 |
| Zona riesgo bajo | 1,00 | 1,00 | 1,00 | ||||||
| Zona riesgo alto | 2,42 | 1,37 | 4,28 | 29,31 | 3,78 | 226,98 | 15,47 | 3,22 | 74,21 |
ORa: ajustado por sexo, edad, zona de riesgo y polimorfismos IL-1B-511 e IL-1RN.
Asociación de los genotipos de Helicobacter pylori y zona de riesgo al grado de severidad de la metaplasia intestinal
| Factores | MI leve | MI moderada | MI severa | ||||||
| ORa | IC 95% | ORa | IC 95% | ORa | IC 95% | ||||
| cagA- | 1,00 | 1,00 | 1,00 | ||||||
| cagA+ | 2,83 | 1,08 | 7,41 | 23,66 | 2,53 | 221,19 | 1,90 | 0,52 | 6,98 |
| vacAs2/m2 | 1,00 | 1,00 | 1,00 | ||||||
| vacAs1/m1 | 1,69 | 0,69 | 4,15 | 1,24 | 0,34 | 4,58 | 32,52 | 3,64 | 290,26 |
| Zona riesgo bajo | 1,00 | 1,00 | 1,00 | ||||||
| Zona riesgo alto | 3,36 | 1,56 | 7,26 | 7,31 | 1,60 | 33,32 | 27,41 | 3,55 | 211,59 |
ORa: ajustado por sexo, edad, zona de riesgo y polimorfismos IL-1B-511 e IL-1RN.
En este estudio se halló que el grado de severidad de la histopatología gástrica, por la infección de los mismos genotipos de H. pylori, es mayor en los pacientes de la zona de riesgo alto. El grado de severidad de la histopatología gástrica y el riesgo asociado, especialmente en la atrofia y la MI, según los genotipos de H. pylori difieren entre las 2 zonas de riesgo. Estos resultados muestran la importancia de una evaluación detallada de los parámetros histopatológicos de pacientes infectados por H. pylori y su correlación con la procedencia de los mismos.
Concordante con las publicaciones previas de Bravo et al. y de Sablet et al.20,26 este estudio muestra una prevalencia mayor de cepas cagA+, vacAs1/m1 de H. pylori en la zona de riesgo alto en relación con la zona de riesgo bajo. Igualmente, el grado mayor de densidad de H. pylori, de infiltrado inflamatorio, de atrofia y metaplasia intestinal se observaron con los genotipos cagA+, vacAs1/m1 en comparación con los genotipos cagA-, vacAs2/Am2, cambios histopatológicos que se documentan en varios estudios4,12,13,27 mostrando su importancia diferencial en el desarrollo de la patología gástrica.
Uno de los hallazgos interesantes es la diferencia en la severidad de todos los parámetros histopatológicos entre las 2 zonas, la cual fue significativamente mayor en los pacientes infectados con los genotipos cagA+, vacAs1 y vacAm1 de la zona de riesgo alto en comparación con los pacientes infectados con los mismos genotipos de la zona de riesgo bajo. Estos resultados se explicarían por los niveles altos de CagA que contienen modificaciones mayores de AATAAGATA en las cepas de H. pylori provenientes de una zona de riesgo alto en comparación con las de una zona de riesgo bajo para cáncer gástrico, como lo reportó el estudio de Loh et al. en población colombiana28. También, de Sablet et al.26 demostraron que todas las cepas de H. pylori procedentes de la zona andina de riesgo alto tienen un ancestro filogeográfico europeo y las de la zona pacífica de riesgo bajo un ancestro predominantemente africano; las cepas de ancestro europeo se asociaron fuertemente con lesiones histológicas más avanzadas y con un daño mayor de ADN de las células epiteliales gástricas; y las cepas cagA+, vacAs1/m1 se correlacionaron altamente con el ancestro europeo.
La densidad mayor de H. pylori se relaciona con la presencia de los genotipos cagA+, vacAs1/m1; sin embargo hay diferencias según las poblaciones. Reportes en población colombiana de riesgo alto no son concluyentes; en población de Túquerres y Pasto la relación significativa es con los genotipos vacAs1 y vacAm1 en antro4; en población de Bogotá, ningún genotipo se relacionó con la densidad del H. pylori en antro ni cuerpo13; en otras poblaciones de riesgo alto, la densidad de H. pylori fue significativa con los genotipos vacAs1 y cagA+ en el cuerpo4, el genotipo cagA+27, o con ningún genotipo29,30. Nuestros resultados son disímiles a los estudios colombianos referenciados, pero similares a los pacientes portugueses4. La divergencia de resultados posiblemente se debe a las diferencias en la prevalencia específica de los genotipos de H. pylori en cada una de las poblaciones estudiadas.
Se encontró una asociación significativa entre los genotipos cagA+ y vacAs1 con el aumento en la actividad inflamatoria y la inflamación crónica, con variaciones topográficas; estos resultados también han sido documentados en diferentes poblaciones4,29–31, con variaciones en la topografía gástrica27,30, asociaciones solo con el genotipo vacAs131, y en otras poblaciones no se ha evidenciado esta respuesta en antro ni cuerpo32. Las variaciones en los genotipos asociados a la respuesta inflamatoria según la zona de riesgo podrían responder a las diferencias en la prevalencia de los tipos de cepa de la bacteria; Schneider et al. publicaron que la respuesta inflamatoria difiere de acuerdo con el tipo de cepa de H. pylori, respuesta que ejerce una influencia fuerte en el desarrollo de la atrofia y la metaplasia intestinal en las personas de riesgo bajo en comparación con las de riesgo alto33. El grado de severidad de la inflamación crónica mayor en la zona de riesgo alto se explicaría por lo planteado en el estudio de Piazuelo et al.34. Los autores encontraron en sujetos de la zona de riesgo bajo elevada eosinofilia, revelando una fuerte y prolongada actividad antiinflamatoria que aminora la inflamación crónica y sesga la respuesta de la mucosa por la infección de H. pylori hacia una respuesta Th2, factor que limita el daño del tejido.
La GMA y la MI presentaron una localización mayor en el antro, resultado opuesto a lo reportado por otros autores15,16; y llama la atención la ausencia del grado severo de la atrofia y la metaplasia intestinal en los pacientes con MI de la zona de riesgo bajo, resultado que puede ser atribuido a los pocos casos en esta zona; sin embargo, el grado de severidad de la atrofia y la metaplasia intestinal fueron significativamente mayores en la zona de riesgo alto, resultados consistentes con los de Recavarren-Arce et al. en zonas de los Andes y de la Costa en el Perú35.
De otra parte, la asociación entre el genotipo vacAs1 al aumento de puntaje de la atrofia y la metaplasia intestinal en antro y cuerpo son hallazgos parcialmente consistentes con varios estudios que incluyeron población colombiana4,13 y difieren de otros, tanto por los genotipos como por la localización13,23,27. De acuerdo con la zona de riesgo, la diferencia en los genotipos asociados al aumento de puntaje de atrofia y MI responderían a la diferencia en las cepas de H. pylori presentes en cada zona, como lo plantearon Schneider et al.33, hallazgo no documentado en otros estudios indexados. Los genotipos presentes según topografía gástrica muestran concordancia con lo expresado por Yamaoka et al., hay menos del 1% de diferencia en los genotipos localizados en antro y cuerpo36.
El aumento de riesgo de la GMA y la MI asociado a los genotipos cagA+ y vacAs1 es conocido5,6,10,32. No se encontró asociación de estos genotipos con la GMA; posiblemente este resultado se explique por el grado de la severidad de la atrofia encontrado; sin embargo, el gen vacAs1/m1 muestra un papel clave en el grado de severidad de la atrofia en las 2 zonas de riesgo. En los pacientes con MI se corrobora el aumento de riesgo asociado al genotipo cagA+, solo en la zona de riesgo alto, y el gen vacAs1/m1 desempeña un papel diferencial con el grado severo de la MI. Estos resultados revelan una divergencia importante en el riesgo de las lesiones preneoplásicas asociado a los diferentes genotipos de H. pylori y el valor del gen vacAs1/m1 entre las 2 zonas de riesgo, al igual que el grado de severidad. Es posible que en estos resultados las relaciones entre la frecuencia de los tipos de cepas de H. pylori, factores ambientales y del huésped, al igual que la persistencia en la infección en los pacientes con metaplasia intestinal desempeñen un papel complejo que incide en las variaciones del riesgo de los genotipos en la 2 zonas, al igual que la asociación de los genotipos de la bacteria con la parámetros histopatológicos.
En conclusión, los cambios histopatológicos resultantes de la infección gástrica por los genotipos cagA+ y vacAs1/m1 de H. pylori muestran que el grado de severidad de los parámetros histopatológicos es significativamente mayor en zonas de riesgo alto de cáncer gástrico. La detección de diferentes genotipos de H. pylori asociados a la GMA y la MI en las 2 zonas de riesgo opuesto podría contribuir a explicar la diferencia en la incidencia del cáncer gástrico en el país.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
FinanciaciónInternational Agency Research in Cancer (IARC), y el Instituto Nacional de Cancerología: Inversión Nación, C401 C41030310-108.
Conflicto de interesesLos autores declaramos que no tenemos ningún conflicto de interés.
Los autores expresamos nuestro agradecimiento al grupo de médicos y paramédicos que captaron los pacientes: Carlos Rizo, Andrés Vecino, Carlos Pinzón y Rosaura Galvis, y Adrey González (citohistotecnóloga) en el Instituto Nacional de Cancerología ESE. Juan Carlos Espinel, Cristina Millán y Gloria Páez en el Hospital San Rafael Tunja. Nuestro agradecimiento asimismo a todos los gastroenterólogos involucrados en el proyecto: Ricardo Oliveros y Rosario Albis (Grupo de Gastroenterología del Instituto Nacional de Cancerología ESE), Fernando Peñalosa (Hospital Universitario de Kenedy, Bogotá, D.C.), Jorge Salek (Hospital Militar), Albis Jani (Hospital Universitario San Ignacio, Bogotá, D.C.), César Redondo (Cartagena), César Suárez (Santa Marta), Óscar Páez Rodríguez (Barranquilla) y José Jaramillo (Santa Martha). También, nuestro agradecimiento a los patólogos Juan Carlos Bravo (Fundación Valle de Lili, Cali) y Germán Barbosa (Instituto Nacional de Cancerología). Finalmente, agradecemos de manera especial a la Dra. Nubia Muñoz, exdirectora de Unit of Field and Intervention Studies, IARC, Lyon, France, su empeño para que fuera posible la realización del estudio HELICOBACTER PYLORI: INTERNATIONAL PREVALENCE, PEPTIC ULCER DISEASE AND GASTRIC NEOPLASIA en nuestro país.