Introducción
El alendronato (ALN) es un poderoso inhibidor de la resorción ósea que produce sensibles incrementos de la densidad mineral ósea (DMO) y un considerable descenso del riesgo de fractura1-5. A pesar de la contrastada eficacia del ALN para la prevención de la osteoporosis posmenopáusica, el sitio que éste ocupa en la práctica clínica está aún por definir. Su tolerancia digestiva y su coste económico son dos razones de peso que desequilibran negativamente su perfil coste-beneficio y limitan su uso en la prevención de la osteoporosis cotidiana6. El empleo del ALN en poblaciones osteoporóticas de mal pronóstico contribuye a corregir positivamente su relación coste-beneficio7. El ALN ha demostrado ser un fármaco altamente eficaz en la prevención de osteoporosis de alto riesgo como la inducida por corticoides8. Sin embargo, existe muy contada información acerca de su comportamiento en otro tipo de pacientes de mal pronóstico. Las osteoporosis posmenopáusicas con fractura previa o con muy baja DMO son las osteoporosis de mal pronóstico más frecuentes en la práctica clínica. El objetivo de este estudio es describir el comportamiento a largo plazo del ALN en un grupo homogéneo de pacientes con osteoporosis posmenopáusica de alto riesgo de fractura.
Pacientes y métodos
Pacientes
Durante el período de un año se incluyeron en el estudio de forma sistemática todas las pacientes visitadas en nuestro servicio que cumplían los criterios de osteoporosis posmenopáusica grave. El número total de pacientes incluidos fue de 34, con edades comprendidas entre 42 y 72 años (media: 60,6 años). El tiempo medio de menopausia fue de 16,6 años. Se consideró que los pacientes tenían una osteoporosis posmenopáusica grave con alto riesgo de fractura, si cumplían alguno de los siguientes criterios:
1. DMO en cuello de fémur (CF) o en columna lumbar (CL) con una escala T < 3,5.
2. DMO con una escala T < 2,5 y fractura osteoporótica previa.
La DMO media basal (± EE) en CL fue de 0,63 ± 0,011 g/cm2 y en CF de 0,64 ± 0,014 g/cm2.
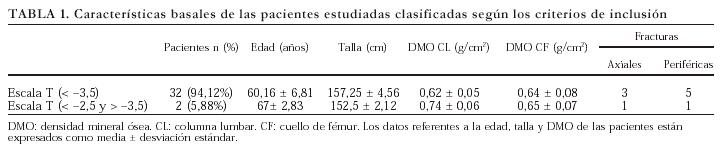
Diez pacientes presentaban fracturas antes de empezar el tratamiento (29,41%), siendo el 60% periféricas (Colles, pelvis, cadera) y el resto vertebrales (tabla 1).
Se excluyó a las mujeres con osteoporosis secundaria, alteración significativa de la función renal o con enfermedades incapacitantes graves o crónicas. También se excluyó a las que habían recibido algún fármaco que pudiera alterar el metabolismo óseo en los 6 meses previos. Por último, se excluyó a todas las pacientes con antecedentes de úlcera péptica y/o reflujo gastroesofágico sintomático. No hubo exclusiones por posibles artefactos de la DMO lumbar (alteraciones degenerativas graves, ateromatosis, etc.) al considerarse éstas muy poco significativas en el estudio radiológico previo, ni tampoco se excluyó a las pacientes con fractura vertebral previa, al afectar dichas fracturas a columna dorsal.
Método
Se observó el efecto de 36 meses de tratamiento con 10 mg diarios de ALN sobre la DMO y la aparición de nuevas fracturas. Todas las pacientes recibieron suplementos cálcicos hasta completar una ingesta diaria > 1 g de calcio elemento.
El seguimiento de la DMO se realizó mediante absorciometría dual de rayos X con un densitómetro Hologic QDR en columna lumbar y en cuello femoral. Se realizó una densitometría basal y tres sucesivas a los 12, 24 y 36 meses de iniciado el tratamiento. La altura de las pacientes se evaluó anualmente mediante mediciones en cada visita médica. La aparición de nuevas fracturas periféricas se controló mediante cuidadoso seguimiento clínico semestral. En el caso de fracturas vertebrales, se realizaron radiografías de perfil de la columna lumbar y dorsal a todas las pacientes, antes y después de finalizar los 36 meses de tratamiento. Se comparó la altura vertebral al principio y al final del tratamiento, entendiéndose como nueva fractura toda aquella pérdida de altura vertebral (anterior, media o posterior) mayor del 15%.
Los efectos adversos se registraron semestralmente en cada visita con una anamnesis detallada y una exploración física completa.
El análisis estadístico de los cambios en la DMO, en la altura y en el tamaño vertebral, se realizó mediante análisis de la variancia y posterior test de Tukey. Se consideraron como significativas todas las p < 0,05.
Resultados
De las 34 pacientes que iniciaron el estudio, 32 completaron el seguimiento (94,11%) y 2 abandonaron por mala tolerancia al fármaco antes de completar el primer año de seguimiento. Todas las pacientes con fractura previa acabaron los 36 meses de tratamiento con ALN.
Efecto del alendronato sobre la densidad mineral ósea
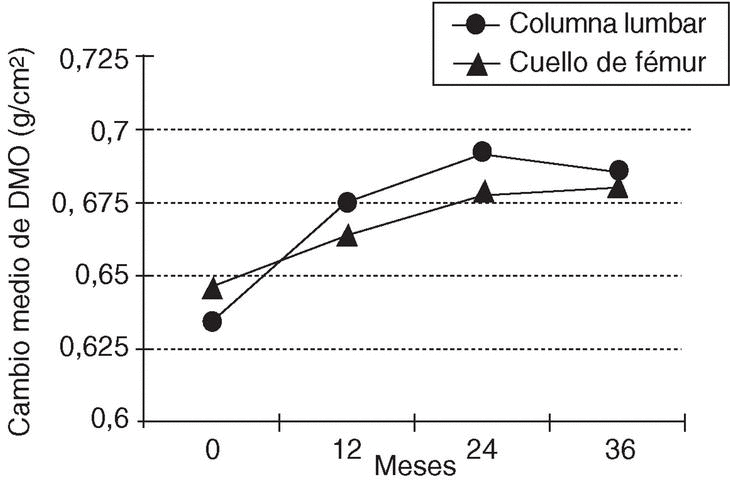
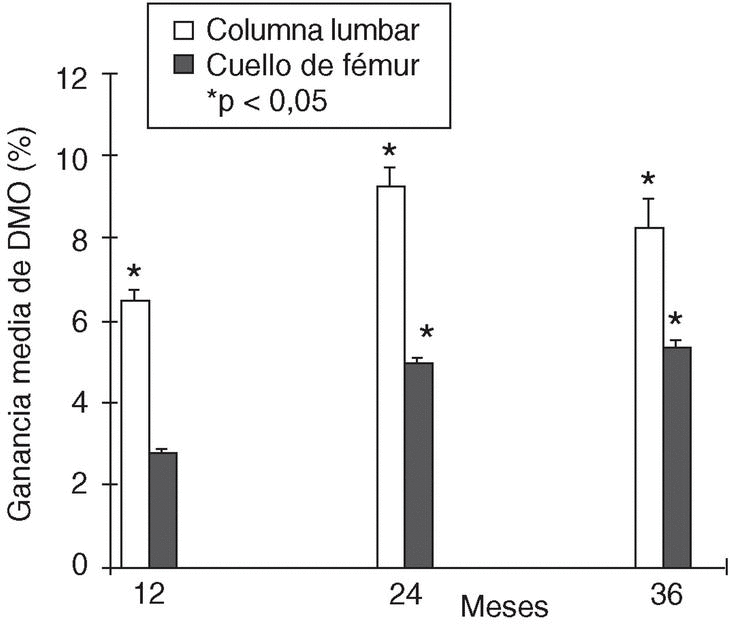
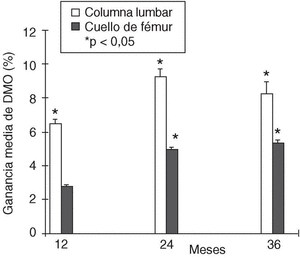
El tratamiento durante 36 meses con 10 mg diarios de ALN produjo un aumento significativo de la DMO lumbar en todas las pacientes desde el primer al tercer año de tratamiento (fig. 1). También se observó un incremento progresivo de la DMO en CF, que resultó significativo a partir del segundo año (fig. 1). La ganancia máxima de DMO en CL se observó a los 24 meses de tratamiento (9,24 ± 5,11%), mientras que en CF se observó a los 36 meses (5,27 ± 4,46%) (fig. 2). Cumplido el segundo año, la DMO en columna lumbar se estabiliza o disminuye y en cuello femoral sigue aumentando (figs. 1 y 2). La evolución de la DMO no presentó diferencias estadísticamente significativas entre las pacientes con y sin fractura previa, aunque llama la atención una mayor ganancia de DMO en CF en el segundo y en el tercer año en las pacientes sin fractura previa (datos no expuestos).
Figura 1. Evolución del cambio de la densidad mineral ósea (DMO) en columna lumbar y cuello de fémur tras 36 meses de tratamiento con 10 mg diarios de alendronato.
Figura 2. Ganancia porcentual media de densidad mineral ósea (DMO) de columna lumbar y cuello de fémur a los 12, 24 y 36 meses de tratamiento con 10 mg diarios de alendronato.
Efecto del alendronato sobre la aparición de nuevas fracturas
Se detectaron nuevas fracturas en dos pacientes (6,25%). Dichas fracturas fueron periféricas (Colles y costal) y ocurrieron en 2 de las 10 pacientes que tenían fracturas antes de empezar el estudio. En consecuencia, ninguna de las pacientes con osteoporosis grave, sin fractura previa, tuvo fracturas en los 36 meses de tratamiento. Frente a éstas, tan sólo el 20% de las mujeres, con fractura previa, presentó alguna fractura adicional. En el 11,11% de las pacientes se objetivó una discreta disminución de altura que no superó en ningún caso 1 cm y que no se acompañó de una disminución significativa de la altura vertebral.
Efectos secundarios
Dos pacientes abandonaron el seguimiento por intolerancia gastrointestinal en el primer año de tratamiento. En uno de los casos, se pudo comprobar endoscópicamente una esofagitis por reflujo que no precisó hospitalización y evolucionó favorablemente con tratamiento médico adecuado. En el otro no se consideró oportuna la prescripción de endoscopia digestiva al presentar la paciente una clínica inespecífica de náuseas y dolor abdominal que desapareció a las 48 h de la suspensión del ALN.
Discusión
Existen múltiples ensayos clínicos que han analizado la eficacia del ALN en la osteoporosis posmenopáusica, que demuestran que no sólo existen aumentos significativos de la DMO, sino también reducciones marcadas en la incidencia de fracturas1-3. El ALN también ha demostrado ser eficaz en la prevención de osteoporosis de alto riesgo de fractura, como es la osteoporosis inducida por corticoides8. La eficacia del ALN en otro tipo de osteoporosis de mal pronóstico se deduce en diferentes metaanálisis, pero no puede ser extraída de los diferentes ensayos clínicos publicados. Dichos estudios están forzosamente restringidos a centrar sus conclusiones sobre poblaciones con osteoporosis leves o moderadas en las que sea ético tratar un elevado número de pacientes con placebo durante 2-3 años. Por contra, los estudios no controlados pueden ayudar a estudiar este tipo de pacientes de mal pronóstico. Paradójicamente, este último tipo de pacientes, mejora la relación coste-beneficio de un fármaco con un perfil de eficacia como el ALN y es el que más puede contribuir a realzar su potencial antifractura. Sin embargo, dicha eficacia no es suficiente para obviar una serie de inconvenientes que claramente restringen el uso cotidiano del fármaco. Por un lado, las limitaciones que suponen su forma de administración y su tolerancia digestiva. Por otro, las reticencias del médico prescriptor a utilizar un fármaco gravoso para hacer frente a una enfermedad crónica, incurable y que además tiene otras alternativas terapéuticas más baratas.
Con este estudio hemos pretendido constatar la información intuida de los ensayos clínicos y necesaria para la práctica clínica diaria. En definitiva, averiguar el comportamiento a largo plazo del ALN en pacientes con osteoporosis posmenopáusica de mal pronóstico. Hemos podido comprobar como, al igual que en los ensayos clínicos, se produce un aumento significativo de la DMO en CL y CF, y se alcanza el máximo incremento al segundo y al tercer año respectivamente. Bien es cierto que, probablemente por la escasez de la muestra, los resultados en CF durante el primer año de tratamiento no han resultado estadísticamente significativos a pesar de obtener resultados similares a los ensayos clínicos. Las conclusiones sobre la incidencia de fracturas no son valorables en este estudio debido al tamaño de la muestra y al diseño del mismo. Sin embargo, sí puede afirmarse que el 80% de las pacientes con osteoporosis grave y fractura previa no volvió a fracturarse durante los 3 años de tratamiento con ALN, lo que no deja de tener un notable interés clínico. El hecho de tratarse de una muestra seleccionada por su mal pronóstico, mejora notablemente el perfil coste-beneficio del ALN, ya que la intervención terapéutica con este fármaco sobre este tipo de pacientes posiblemente es, desde el punto de vista económico, todavía más rentable que sobre pacientes con osteoporosis de bajo riesgo. La incidencia de abandonos por efectos adversos igualmente se aproxima a la publicada previamente6,9,10.
En resumen, el comportamiento del ALN en este estudio es superponible cuantitativa y cualitativamente al publicado previamente en ensayos clínicos con osteoporosis menos graves1-3. En consecuencia, el ALN es un fármaco de notable utilidad para el tratamiento de cualquier tipo de osteoporosis, siendo una opción especialmente interesante en aquellos casos de mal pronóstico.