Introducción
Las modalidades terapéuticas en el tratamiento de la artrosis son muy numerosas, como queda de manifiesto tanto en la última revisión de las guías EULAR para el tratamiento de la artrosis de rodilla recientemente publicadas1 (tabla 1), como en las guías previas del ACR2. Los SYSADOA, cuyas siglas proceden del término inglés symptomatic slow action drug osteoarthritis, son los fármacos capaces de modificar lentamente los síntomas de la artrosis de manera independiente a los antiinflamatorios no esteroideos (AINE), analgésicos u otras opciones terapéuticas. Desde la introducción de este concepto, siempre se han manifestado entusiastas detractores y defensores de él, en ambos casos con poderosas razones, que lo único que han conseguido es que permanezca el desacuerdo acerca del uso de estos fármacos en la práctica clínica habitual. Sigue estando en entredicho cuándo utilizarlos y cuál es el mecanismo de acción real de cada uno de ellos. Ninguna de las guías publicadas recomienda abiertamente su utilización, pero tampoco la desestima.
Después de muchos años de experiencia en este campo, todavía aparecen ensayos clínicos con notables lagunas metodológicas que hacen cuestionables sus resultados. Además, también están apareciendo recientemente estudios independientes con resultados negativos que también cuestionan aquellos buenos resultados previamente publicados por estudios patrocinados por la industria farmacéutica interesada, de manera lícita, en difundirlos.
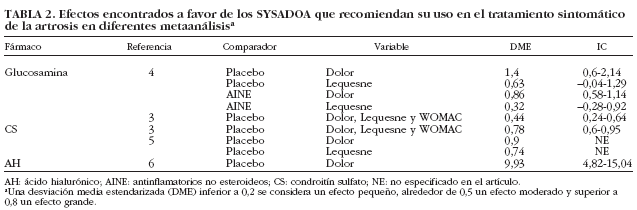
Por lo tanto, es hora ya de intentar elevar un escalón en el nivel de evidencia del que disponemos hasta ahora, y por este motivo aquí se intentará enfocar el tema desde la máxima evidencia científica posible, el metaanálisis, acerca del uso en la artrosis de los fármacos con un efecto potencial como SYSADOA de que disponemos actualmente en la práctica clínica habitual: la glucosamina, el condroitín sulfato (CS), el ácido hialurónico (AH) y la diacereína (tabla 2).
Glucosamina
Después de múltiples experiencias y ensayos clínicos, de diferente metodología y calidad, el primer metaanálisis que intentó subir el grado de evidencia clínica acerca del uso de la glucosamina en el tratamiento de la artrosis fue publicado en JAMA en el año 20003. Su objetivo fue evaluar la eficacia de la glucosamina en el tratamiento de la artrosis mediante un metaanálisis de ensayos clínicos aleatorios (ECA). El primer problema de este estudio fue encontrar ECA que cumplieran los criterios de inclusión del metaanálisis. De hecho, en la búsqueda sistemática de la bibliografía, tan sólo 6 ensayos con glucosamina cumplieron los criterios preestablecidos de inclusión, todos ellos en artrosis de rodilla. En las variables analizadas en este metaanálisis, la desviación media estandarizada (DME) fue de 0,44 (intervalo de confianza [IC] del 95%, 0,24-0,64) a favor del tratamiento con glucosamina con respecto al placebo. Es conocido que el valor de la DME por encima de 0 a favor del grupo de tratamiento nos inclina a recomendar su uso. Sin embargo, este valor es relativo y se puede matizar. Así, de una manera arbitraria, se ha propuesto que la DME con valor inferior a 0,2 correspondería a un efecto favorable «pequeño», un valor alrededor de 0,5 se consideraría un efecto favorable «moderado» y por encima de 0,8 el efecto sería «grande»4. Por lo tanto, la conclusión de este metaanálisis sería que la glucosamina tendría un efecto beneficioso «moderado» para el tratamiento sintomático de la artrosis.
Existe otro metaanálisis más reciente y de mayor calidad, publicado en la librería Cochrane4. Su objetivo fue evaluar la eficacia y seguridad de la glucosamina en el tratamiento de la artrosis mediante el análisis de ECA. Se establecieron como principales criterios de selección de estudios los ECA simple o doble ciego controlados con placebo u otro comparador. En este estudio se contactó de manera personal con grupos de investigación relevantes, y se encontraron estudios no publicados con lo cual se intentó eliminar el sesgo de publicación (tendencia a publicar resultados positivos), lo que da mayor valor al metaanálisis. Con la estrategia de búsqueda de citas bibliográficas aparecieron centenares de artículos de los que tan sólo 16 cumplieron los criterios de inclusión con un total de 992 pacientes tratados con glucosamina y 1.037 con placebo o AINE. De los 16 ECA, 9 se encontraban incluidos en Medline, 2 en otras bases de datos bibliográficas y 5 estudios no se habían publicado.
Doce de los 16 se realizaron en artrosis de rodilla, 13 se compararon con placebo, resultando en 12 de éstos que la glucosamina fue superior. En 4 se comparó la glucosamina con un AINE, encontrándose mejores resultados con la primera en 2 de ellos. No se encontraron diferencias entre los grupos en los otros 2 ensayos.
Comparado con placebo, el resultado global de la DME del metaanálisis fue de 1,4 (IC del 95%, 0,65-2,14) para la variable «dolor» y 0,64 (IC del 95%, 0,04 a 1,29) para el índice de Lequesne. Por lo tanto, respecto al placebo, la glucosamina parece tener un efecto favorable y grande en cuanto al dolor y moderado en cuanto al índice de Lequesne. Respecto a éste, hay que recordar que el IC incluía el resultado negativo, por lo que este efecto «moderado» podría incluso considerarse cuestionable.
En la comparación que se hizo con los AINE en este metaanálisis, el resultado de la DME fue de nuevo grande y favorable a la glucosamina en lo que respecta al dolor (DME, 0,86; IC del 95%, 0,58-1,14) y moderado aunque favorable a la glucosamina respecto al índice de Lequesne (DME, 0,28; IC del 0,28 a 0,92). Nuevamente, el IC de la DME en este caso incluye el resultado negativo por lo que este efecto «moderado» es también cuestionable.
Un hecho destacable de todos los estudios incluidos en este metaanálisis fue la escasa aparición de acontecimientos adversos (0,6% del total de pacientes tratados y sin diferencia respecto al placebo).
Condroitín sulfato
En el año 2000 aparecieron 2 metaanálisis publicados de ECA con la intención de valorar la eficacia del CS en el tratamiento de la artrosis. En el primero de ellos3, 9 estudios cumplieron los criterios preestablecidos de inclusión, 8 en artrosis de rodilla y uno en rodilla y cadera. Se encontró un efecto grande y favorable al CS con una DME de 0,96 (IC del 95%, 0,63-1,3) con respecto al placebo. No obstante, de los 9 estudios, uno presentaba un efecto excesivamente favorable para el CS no concordante con los demás estudios analizados. Excluyendo a éste, la DME bajó a 0,78.
En el otro metaanálisis publicado5, se identificaron 16 estudios de los cuales 7 cumplieron los criterios de inclusión para su análisis, todos ellos controlados con placebo, en los que se trataron a 703 pacientes (372 con CS y 331 controles). En este estudio se encontró una DME de 0,9 y de 0,74 favorable al CS en cuanto a la mejoría del dolor y del índice de Lequesne, respectivamente.
Se encontró un porcentaje bajo de acontecimientos adversos con el CS (alrededor del 5%) que fue incluso inferior al placebo, aunque sin diferencias significativas.
En conclusión, ambos estudios muestran un efecto favorable del CS respecto al placebo de moderado a grande.
Ácido hialurónico
Muy recientemente se ha publicado un metaanálisis con el objetivo de evaluar la eficacia y seguridad del AH con respecto al placebo, en el tratamiento de la artrosis de rodilla mediante el análisis de ECA6. De 665 estudios encontrados y revisados con la búsqueda sistemática de bibliografía, 20 cumplieron los criterios de inclusión con un total de 1.647 rodillas tratadas (818 con AH y 829 con placebo). Aunque algún ensayo de los incluidos no encontró diferencias significativas con respecto al placebo, el resultado global de la DME en la variable «dolor» fue claramente favorable al AH, con un valor muy notable y claro de 9,93 (IC del 95%, 4,82-15,04). En este análisis se encontró un riesgo relativo de acontecimientos adversos con AH muy bajo, de 1,19 (IC del 95%, 1,01-1,41). En todas las rodillas tratadas sólo se encontraron 4 acontecimientos adversos mayores (una reacción local dolorosa a la inyección, una inflamación articular severa, una vasculitis y una reacción de hipersensibilidad).
No se han encontrado metaanálisis que estudien el AH respecto a otro comparador, por ejemplo un AINE oral o corticoides intraarticulares. No obstante, existe otra publicación en la que no se hace un metaanálisis pero en la que se realiza una revisión sistemática de la bibliografía, con el objetivo de evaluar la eficacia y seguridad del AH en el tratamiento de la artrosis de rodilla7. De las referencias encontradas se seleccionaron 13 ECA y 5 series abiertas de casos clínicos, y se llegó a la conclusión de que el AH mejora significativamente tanto el dolor como la función en los estudios en los que se usó AH de alto peso molecular. Los resultados con AH de bajo peso molecular no fueron consistentes.
Diacereína
Aunque el desarrollo de este producto en el tratamiento de la artrosis se ha estudiado desde hace más de 10 años, hasta hace poco no hemos podido disponer de él en nuestro mercado. Existen pocos estudios clínicos que evalúen su eficacia en el campo de la artrosis, ninguno de ellos es un metaanálisis. Los principales ECA son 2, y el primero de ellos, publicado en 19948, demostró que la diace-reína mejoró en el límite de la significación estadística (p = 0,05) el dolor respecto al placebo, con una eficacia similar al tenoxicam en artrosis de cadera y a corto plazo (8 semanas). En otro estudio publicado más reciente9, no se encontraron diferencias respecto al placebo en el efecto sobre los síntomas de la artrosis de cadera a largo plazo (3 años), por lo que su posible efecto como SYSADOA es cuestionable. No obstante, en este mismo trabajo se pudo objetivar que la evolución radiológica de los pacientes tratados con diacereína era significativamente menor respecto al placebo, por lo que este fármaco podría tener un efecto modificador de la enfermedad a pesar de que su efecto como SYSADOA no quede claro.
Conclusiones
La principal conclusión de esta revisión es que los metaanálisis de ECA existentes hasta la fecha han demostrado que la glucosamina y el CS se pueden considerar SYSADOA, con un efecto entre moderado y grande respecto al placebo, con un grado de evidencia 1A. Asimismo, el AH se puede considerar un SYSADOA con un efecto grande sobre los síntomas de la artrosis con respecto al placebo, con un grado de evidencia 1A. Por lo tanto, el grado de recomendación de su uso para el tratamiento sintomático de la artrosis es A.
La glucosamina se ha podido comparar en un metaanálisis con AINE, y se encontró un efecto favorable y moderado de aquella para el dolor y el índice de Lequesne, aunque cuestionable en este último ya que el IC del efecto incluyó el valor 0. Los metaanálisis de otros SYSADOA no incluyen comparación con AINE o infiltraciones intraarticulares de esteroides.
No está claro que la diacereína se pueda considerar un SYSADOA, aunque ha demostrado un efecto sobre los síntomas de la artrosis de cadera similar al tenoxicam. Los posibles efectos sobre la modificación de la enfermedad de éste y otros SYSADOA serán tratados en otro artículo.