Los métodos tradicionales para el cierre de heridas y fijación de mallas en las hernioplastias, tanto abiertas como laparoscópicas, se asocian a problemas como dolor, hemorragia, hematoma o infección. La introducción de nuevos adhesivos tisulares sintéticos como los cianoacrilatos puede suponer una alternativa con ciertas ventajas, tales como la rapidez de aplicación, su sencillez de uso, la posibilidad de evitar añadir un traumatismo, la disminución del tiempo quirúrgico y del dolor, un mejor resultado estético, etc. Sin embargo, estos productos todavía son muy poco conocidos, y plantean algunos interrogantes: ¿tienen toxicidad?, ¿cómo actúan?, ¿cómo se utilizan?, ¿cuáles son sus inconvenientes?, etc. El propósito de esta revisión sistemática es analizar los conocimientos sobre los adhesivos sintéticos centrados en una mejor comprensión sobre su posible uso en el campo de la cirugía de pared abdominal.
MétodoSe realiza una revisión de la literatura según las palabras clave «cianoacrilatos», «adhesivos tisulares» y «pegamentos» en los registros Medline, Embase y Cochrane. Se verifican las referencias de los artículos para obtener otros estudios accesorios y se establece contacto con los fabricantes y casas comerciales para completar información técnica.
ConclusiónLos cianoacrilatos pueden ser usados para fijar la malla en la reparación de las hernias con seguridad y ventajas clínicas. Se precisan estudios de mayor calidad sobre estos productos.
Traditional methods of wound closure and mesh fixation in hernia repair, both open and laparoscopic, are associated with problems such as pain, bleeding, hematoma or infection. The introduction of new synthetic tissue adhesives such as cyanoacrylates, can be an alternative to certain advantages such as speed of implementation, ease of use, possibility of avoiding a trauma, reduced surgical time and decreased pain, better cosmetic result, and so on. However, these products still raise a number of questions about their potential toxicity, mechanism of action, application forms, disadvantages, etc. The purpose of this systematic review is to analyze the knowledge of synthetic adhesives focused on a better understanding for potential use in the field of surgery of the abdominal wall.
MethodA review of all literature by keywords «cyanoacrylate», «tissue adhesives» and «glue» records in Medline, Embase and Cochrane. We checked the bibliographies of the articles for additional studies and contacted accessories manufacturers and trading houses for complete information.
ConclusionCyanoacrylates can be used to secure the mesh in the repair of hernias and safely certain advantages. Higher quality studies on these products are required.
A lo largo de la historia se ha buscado la solución más adecuada para cerrar una herida (traumática o quirúrgica) de forma que cause la menor reacción inflamatoria y consiga una cicatriz lo más estética posible. Durante décadas se ha forjado la imagen del cirujano como la de un «profesional o artesano que cose», que usa suturas para cerrar las heridas. Pero todas las suturas, ya sean absorbibles o no, añaden un nuevo microtrauma, y con él, una variable reacción tisular; no obstante, en la actualidad las heridas también pueden ser tratadas mediante adhesivos tisulares sintéticos o pegamentos. El desarrollo de este nuevo método de tratamiento es importante en la medida en que puede ofrecer ventajas a los pacientes, aumentando su calidad de vida. La introducción de los adhesivos en cirugía ha sido recibida con un gran entusiasmo inicial, ya que parece que pueden conseguir una resistencia de tensión equivalente a la de cualquier sutura, con mejor aspecto estético de la cicatriz final y una tasa de infección menor. Si estos hechos se terminan confirmando, si los adhesivos demuestran ser una mejor solución (con mayor eficacia y menor daño), la imagen tradicional del cirujano unido a una sutura podría modificarse en un futuro no muy lejano, o incluso desaparecer.
MetodologíaEsta revisión sistemática está basada en una detallada búsqueda electrónica que incluye los repertorios de las bases de datos Cochrane, Google, Embase y Medline, usando PubMed. No se han utilizado restricciones ni de año de publicación, ni de idioma, ni de diseño (experimental o clínico, animales o personas, niños o adultos) ni por tipo de pegamento utilizado. Las palabras clave usadas en la investigación han sido «adhesivo tisular» (tissue glue or adhesive), cyanoacrylate («cianoacrilato») y hernia. Tras la búsqueda inicial en PubMed, se identificaron otros estudios adicionales referenciados en estos. Se analizan todos aquellos que incluyen el uso de los adhesivos en cualquier cirugía de la pared abdominal.
HistoriaEn el año 1942, Harry Coover descubre de forma casual el cianoacrilato de metilo (CA) mientras trabajaba en los laboratorios de Kodak buscando un material transparente para ser usado en las miras telescópicas plásticas de los fusiles de asalto; sin embargo, el producto obtenido es abandonado por su imposibilidad de empleo, debido a su rápida adhesión. En 1951, cuando trabajaba con polímeros resistentes al calor para los toldos de los aviones, Coover se da cuenta por fin del interés de esta sustancia como pegamento de gran resistencia que no precisa calor o presión para ejercer su función. El producto fue patentado en 1958 como Eastman 910 (Superglue: alcohol-catalyzed cyanoacrylate adhesive compositions), y adquirió una rápida difusión y aceptación en múltiples aplicaciones comerciales y domésticas (fig. 1).
En la guerra de Vietnam los CA fueron usados para tratar las heridas de los soldados, con lo que se consiguió disminuir el sangrado y facilitar su traslado a centros médicos mejor dotados. Los buenos resultados obtenidos hicieron posible su aprobación para usos médicos, aunque pronto se demostró la existencia de una posible toxicidad y fueron retirados del uso civil. Estudios experimentales posteriores demostraron que el efecto tóxico era debido al formaldehído que se producía durante la degradación del metil-2-cianoacrilato. Sir H. Coover fue galardonado con la medalla nacional de la tecnología y la innovación en 2010. Murió en 2011, a la edad de 94 años1–3.
Desarrollo de los cianoacrilatosEl primer producto desarrollado tras el metil-CA fue el etil-CA (C6H7NO2), que se caracteriza por tener una densidad específica de 1.05g/ml, un punto de ebullición de 65°C, un punto de ignición de 83°C, una presión de vapor de <0.27kPa a 25°C. Además, es soluble en metil-etil-cetona y tolueno, y se define ya como un adhesivo tisular sintético (AT) –es decir, no biológico– que al contacto con una superficie y mediante reacción exotérmica se pega formando una cubierta de gran resistencia. Los AT son sintetizados por condensación a partir del cianoacetato y para-formaldehído en presencia de un catalizador. Son líquidos incoloros de baja viscosidad y altamente reactivos. La aplicación de una fina lámina del producto desarrolla una rápida polimerización, usualmente entre 5 y 60s, desencadenada por los grupos hidroxilo en la superficie en la que se está pegando. El agua puede actuar fácilmente como este catalizador y activar la polimerización aniónica. Dado que los tejidos biológicos contienen muchos residuos de bases proteicas, los CA son extremadamente adhesivos para ellos, dado su buen potencial de humedad. Como extensión a esta propiedad principal, los CA en aplicaciones biológicas suman también los beneficios de un efecto hemostático y bacteriostático para los gérmenes grampositivos, al formar una capa oclusiva impermeable.
Los CA son capaces de mantener los tejidos en su lugar durante el tiempo necesario para que se lleve a cabo una correcta cicatrización. Un exceso de humedad (sangre, suero, etc.) puede alterar esta unión. A temperatura ambiente polimerizan por 3 mecanismos básicos: radicalia, aniónica y zwitteriónica. Iniciadores de esta polimerización pueden ser los aniones CH3COO-, OH-, I-, las bases débiles como los alcoholes, el agua, y los aminoácidos presentes en los tejidos vivos. Al degradarse forman cianoacetato y formaldehído, causante este último de una reacción inflamatoria local tóxica e irritante (figs. 2 y 3).
Como adhesivos tisulares poseen 3 características elementales: a) gran resistencia en la adhesión; b) son biocompatibles, y c) son biodegradables, además de tener una gran facilidad de aplicación y estabilidad. Su desventaja fundamental es la rapidez de su efecto, que hace prácticamente imposible poder rectificar las superficies a unir (tablas 1 y 2)4–7.
Clasificación de los adhesivos tisulares en función de su origen
| Biológicos | Fibrina homólogaFibrina autóloga | Tissucol® (Baxter, Westlake Village, California, EE. UU.)Vivostat® (Vivolution A/S, Birkeroed, Dinamarca)Cryoseal® (Thermogenesis, Rancho Cordova, California, EE. UU.) |
| Trombina bovinaGelatina porcina | Floseal® (Baxter, Westlake Village, CA, EE. UU.)Surgiflo® (Ethicon, Nueva Jersey, EE. UU.) | |
| Semisintéticos | FormaldehídoGlutaraldehídoGelatina porcinaResorcinol | Bioglue® (Cryolife, Kennesaw, Georgia, EE. UU.)GFR |
| Sintéticos | Cianoacrilatos | Glubran II® (GEM Srl, Viareggio, Italia)Ifabond® (Fimed, Les treilles, Quincie-en-Beaujolais, Francia)Omnex® (Ethicon, Nueva Jersey, EE. UU.)Histoacryl® (Braun, Aesculap AG, Tuttinggen, Alemania)Dermabond® (J&J, Somerville, Nueva Jersey, EE. UU.)Indermil® (Covidien, Norwalk, Connecticut, EE. UU.) |
Ejemplos de aplicaciones médicas y quirúrgicas de los compuestos de cianoacrilato publicados en la literatura
| Especialidad | Aplicaciones |
| Cirugía general | Reparación de heridasControl de la hemorragiaRefuerzo de anastomosis |
| Cirugía torácica | Cierre de fuga pulmonar |
| Neurocirugía | Reparación de nervios periféricos |
| Cirugía plástica | Tratamiento del labio leporinoLaceraciones facialesBarrera de piel humana |
| Otorrinolaringología | Reconstrucción de la cadena óseaEstabilización de cartílagos |
| Urgencias | Reparación heridas traumáticas |
| Digestivo | Control del sangrado de varices esofagogástricas y úlceras gastroduodenalesCierre de fístulas biliares refractarias a drenajeCierre de fístulas pancreáticas |
| Oftalmología | Reparación temporal de perforaciones cornealesCirugía de cataratas |
| Radiología | Embolización de malformaciones vasculares y aneurismas o fístulas arteriovenosas |
| Pediatría | Cierre de heridas y hemostasia |
| Ginecología | Cierre de episiotomía |
| Traumatología | Fijación de fracturasTratamiento de colgajos óseos |
| Urología | Anastomosis de vía urinaria |
| Odontología | Cierre de heridas de mucosa oralApósito periodontalEstomatitis aftosaFracturas dentales |
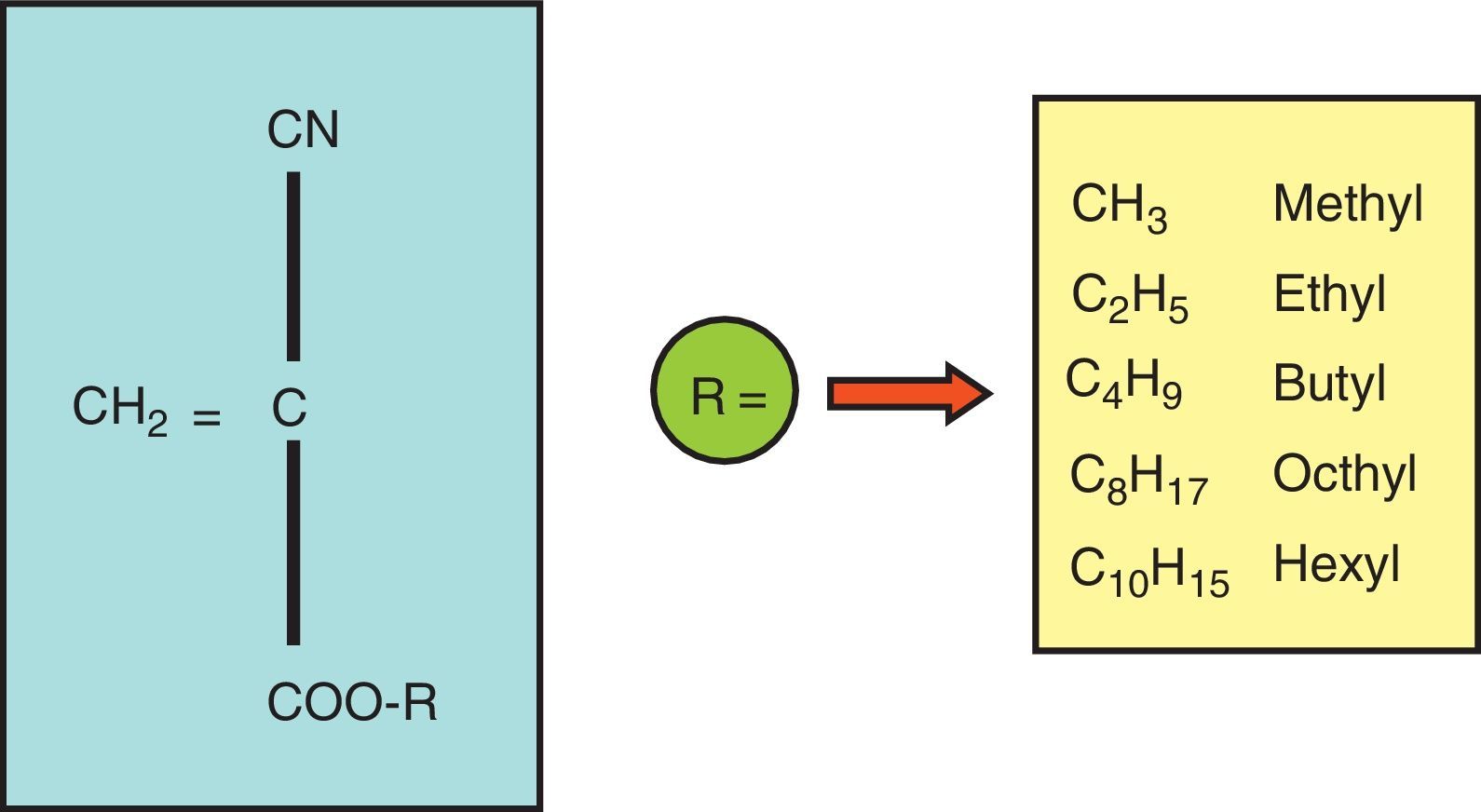
Podemos distinguir 2 grupos de CA basándonos en la longitud del radical en el grupo carboxilo del polímero, ya que esta variación estructural influye significativamente en sus propiedades clínicas:
- 1)
Los de cadena corta (metil- o etil-). Se degradan muy rápidamente in vivo, y el formaldehído producido causa una rápida toxicidad tisular. Estos derivados han sido retirados del uso médico.
- 2)
Los de cadena larga (butil-, hexil- y octil-). Son menos citotóxicos, ya que presentan una degradación mucho más lenta, sin alcanzar una concentración de formaldehído superior a la que se presenta en la sangre de forma habitual y, por ello, pueden ser utilizados de forma segura en múltiples aplicaciones médicas, tanto a nivel externo como interno6–10.
El metil-2-CA ya fue utilizado como adhesivo quirúrgico. Este derivado de cadena corta contiene un grupo metil- como subunidad (R=CH3). Aunque fue considerado un gran avance, su uso fue rápidamente limitado, al demostrarse su citotoxicidad. Más tarde se sintetizó el etil-2-CA, que aunque contenía un grupo carboxilo más largo, también causaba una considerable reacción inflamatoria con una mayor formación de seromas, necrosis tisular y reacción a cuerpo extraño. En ambos casos la degradación de la cadena corta iniciaba una respuesta inflamatoria aguda, seguida de una reacción crónica tipo células gigantes a cuerpo extraño. Investigaciones posteriores demostraron que la citotoxicidad era proporcional a la longitud de la cadena del monómero, lo que llevó a sintetizar productos de cadena más larga como el butil- o hexil-. El butil-2-CA presenta una biodegradación mucho más lenta, de lo que resulta una mínima toxicidad al permitir una aclaración más eficiente de los subproductos de degradación. A pesar de las buenas publicaciones iniciales, también aparecieron estudios que advertían de que su uso bajo la piel en tejidos bien vascularizados causaba una marcada inflamación subcutánea con el consiguiente eritema o infección. El octil-2-CA fue el primer monómero en pasar todos los requisitos internacionales obligados para el uso de un medicamento en 1998. Su resistencia a la rotura es 4 veces mayor que la de sus predecesores, es muy superior a la de los adhesivos de fibrina y equivale a la de una sutura de nailon de 4-0, pero solo se aconsejaba para uso externo, sobre la piel. Nuevos derivados, como el hexil-2-CA, presentan actualmente los mismos resultados, pero libres de toxicidad (ya que la cantidad producida de formaldehído es muy débil, por debajo de los índices sanguíneos normales) y con posibilidad de aplicación tanto externa como interna, con lo que se consigue una mejor resistencia adicional y plasticidad, lo que aumenta la flexibilidad de los tejidos11–13.
Aplicaciones quirúrgicasAlgunas de las aplicaciones médicas y quirúrgicas en las que han sido empleados los CA se muestran en la tabla 2. El uso más aceptado es como adhesivo para reparar heridas traumáticas o quirúrgicas, y del que existe una amplia documentación acumulada de más de 30 años. En la actualidad disponemos de algunas revisiones y metaanálisis que demuestran que no hay diferencias estadísticamente significativas entre la proporción de heridas con dehiscencia, la tasa de infecciones, el resultado estético o la satisfacción del paciente o del cirujano al tratar una herida de forma mecánica (con sutura) o química (con CA), pero sí que presentan ventajas en cuanto al tiempo de tratamiento (entre un 30-60% menos que con las suturas, relacionado sobre todo con el tiempo del cirujano, la disminución en la necesidad de equipos, servicios y visitas en el seguimiento), la posible formación de queloides o el riesgo de incidentes por exposición a instrumentos (agujas y pinzas) estimado por Makary entre el 1.4% y 15% de todos los procedimientos quirúrgicos, posiblemente infravalorado y asociado a un alto coste económico y social2,13–16.
Ventajas y desventajas de los cianoacrilatosVentajas de los cianoacrilatos de metiloEl uso de un CA se asocia con las siguientes ventajas: 1) rapidez de aplicación (15 veces más rápido que una sutura estándar); 2) es indoloro, y puede evitar la necesidad de un anestésico local; 3) función de barrera antimicrobiana (especialmente contra gérmenes grampositivos), con lo que crea unas mejores condiciones para la cicatrización de las heridas y evita la necesidad de aplicar antibióticos tópicos; 4) elimina el riesgo de lesión vascular y disminuye la formación de hematomas; 5) evita la necesidad de retirar la sutura y, por lo tanto, el dolor que ello supone y su ansiedad; 6) aumenta la satisfacción de los pacientes; 7) elimina el riesgo de punciones accidentales con agujas, y 8) aunque su coste directo puede ser 4 veces mayor, tiene una mejor coste-efectividad que la sutura o grapas, atribuido a la reducción en la necesidad de un seguimiento, tiempo de los profesionales y curas de enfermería2,7,17.
Desventajas de los cianoacrilatos de metiloLas desventajas principales al usar un CA son consecuencia de la falta de estudios en ciertas situaciones específicas como son: 1) en zonas de tensión elevada, donde se aconseja dar algunas suturas profundas de aproximación para reducir la tensión y facilitar el contacto de las superficies a unir; 2) sobre incisiones mayores de 5cm, en las que todavía no ha sido documentado su efecto; 3) en zonas contaminadas o infectadas; 4) en pacientes con problemas para una cicatrización normal, como en diabéticos, pacientes con enfermedades vasculares, pacientes inmunodeprimidos, etc.; 5) en el interior de las mucosas (p. ej., en la cavidad nasal u oral), y 6) tampoco se aconseja utilizarlos en mujeres embarazadas4.
Toxicidad clínicaInicialmente se demostró que los CA causaban toxicidad tisular. Este efecto es inapreciable en los preparados para uso médico, debido a la pequeña proporción de impurezas del producto. A pesar de ello, es cierto que cuando se usa un AT se produce una reacción inflamatoria que puede conllevar necrosis tisular e incluso fenómenos de trombosis arterial. Los CA se degradan espontáneamente en polímeros, y el formaldehído parece ser el principio que al acumularse en las zonas tratadas causa el efecto citotóxico, tanto in vitro como in vivo. Actualmente, se sabe que esta degradación del CA y la aparición del formaldehído pueden ser evitadas al modificarse la longitud del radical alkil- (del metil- o etil- al radical butil- o hexil-CA). Este aumento de la cadena produce un enlentecimiento del proceso de degradación y disminuye el efecto tóxico del producto por unidad de tiempo, lo que evita el problema de los derivados de cadena corta. Este fenómeno ha sido clínicamente documentado por Maw et al.18. A pesar de todo, no disponemos todavía de estudios metabólicos in vivo, por lo que lo más recomendable sería aconsejar siempre el uso de la menor cantidad de CA necesaria para obtener la función que buscamos, lo que aumentará nuestra seguridad en la aplicación del producto.
CitotoxicidadExisten referencias en la literatura que muestran un efecto citotóxico de los CA al entrar en contacto directo con células in vitro. La polimerización se produce mediante reacción exotérmica, lo que genera calor y explica el potencial daño celular. Se ha sugerido que los CA pueden actuar mediante 2 mecanismos: 1) generar hidroperóxidos lipídicos, que activarían la biosíntesis de prostaglandinas y tromboxanos, y 2) oxidar y lisar membranas celulares. Estos 2 mecanismos explican algunos de los fenómenos trombóticos y de necrosis que aparecían con los derivados de cadena corta. Algunos estudios han observado también que el uso de inhibidores de la prostaglandina H sintetasa, como el ácido acetilsalicílico y la indometacina, reducen dicha citotoxicidad.
GenotoxicidadNo existe ninguna publicación clínica que relacione los CA con toxicidad a largo plazo o que evidencie que tengan efecto carcinogénico. Los de cadena corta sí se han relacionado con la posibilidad de genotoxicidad, como es el caso del methyl-2-CA, con el que se ha demostrado un efecto mutagénico in vitro en un microsoma de Salmonella. A nivel molecular, el incremento de la cadena alkil- reduce esta posibilidad de toxicidad. La pureza del compuesto y su longitud de radical son, por tanto, 2 parámetros a conocer para evitar posibles efectos adversos. A pesar de todo, necesitamos de mayor documentación sobre el metabolismo de estos productos dada la gran difusión que podrían alcanzar en el campo médico y quirúrgico5.
Productos comercialesEs necesario recordar primero la diferencia entre los AT sintéticos y los biológicos, ya que se confunden con frecuencia, incluso algunos cirujanos los utilizan indistintamente (p. ej., Tissucol® frente a CA). Hay que tener claro que los adhesivos biológicos son concentrados de fibrinógeno y factor xiii, preparados a partir de plasma humano y que son clasificados como «drogas» por la agencia mundial del medicamento, lo cual es una gran diferencia, ya que los AT son clasificados como «productos médicos». Además, los adhesivos biológicos pueden tener contaminación (riesgo de transmisión de enfermedades), requieren de una preparación previa (mientras los AT pueden ser aplicados inmediatamente después de su apertura) y son mucho más caros.
Glubran II®Es el adhesivo tisular derivado de comonómero n-butil-CA, con elevadas propiedades adhesivas y hemostáticas, y que presenta la marcación de la Unión Europea clase iii para uso interno. Es un producto transparente que forma una delgada capa que una vez se solidifica puede ser fácilmente atravesada con una aguja de sutura, ya que la polimerización no forma agregados cristalinos. El tiempo de polimerización puede variar en función del tipo de tejido con el que la cola entra en contacto, de la cantidad y naturaleza de los líquidos presentes y de la cantidad de producto aplicado, y alcanza una temperatura de 45°C (tabla 3). En condiciones de correcta aplicación la cola empieza a solidificarse después de 1 o 2s, y completa su reacción de solidificación en torno a los 60-90s. Al final de esta reacción la cola alcanza su máxima resistencia mecánica. Una vez sólida ya no tiene ningún poder adhesivo, por lo que se podrán yuxtaponer tejidos o gasas quirúrgicas sin correr el riesgo de adherencias no deseadas. La película de cola se elimina a través de un proceso de degradación hidrolítica cuya duración depende del tipo de tejido y de la cantidad utilizada. Su principal desventaja es su moderada pureza y la presencia de otros compuestos agregados a la formulación. Dispone de introductor para dosificación endoscópica y forma de aplicación en espray, aunque esta es algo engorrosa y necesita de las 2 manos para poder sujetar el dispositivo por su longitud (la cola se une al gas en una varilla larga).
Propiedades de los cianoacrilatos utilizados en cirugía (marcación de la comunidad europea
| Adhesivos tisulares sintéticos derivados del cianoacrilato | ||||
| Ifabond® | Glubran II® | Histoacryl® | Dermabond® | |
| Compuesto | α-hexil | n-butil | n-butil | n-octilo |
| Empresa | Fimed (Francia) | GEM Srl (Italia) | B Braun (Alemania) | J&J (EE. UU.) |
| Marcación | III | III | IIb | IIa |
| Pureza | 98 | 64 | 96 | 80 |
| Temp. (grados) | +2 | 45 | 45 | 40-45 |
| T. (s) | 1-30 | 1-90 | 5-7 | 95-180 |
| Degradación (meses) | 3-9 | >12 | 12 | 5-14d |
III: uso interno y externo; IIb: uso externo; pureza en % de cianoacrilato; Temp.: temperatura de polimerización; T.: tiempo de polimerización.
Los datos no incluidos no han sido facilitados por la empresa consultada.
El histoacryl® es un adhesivo tisular líquido y estéril, compuesto por n-butil-2-CA (sinónimo: enbucrilato), que polimeriza en contacto con el calor y la humedad y se convierte en un material sólido y resistente que presenta una absorción completa al cabo de un año –aproximadamente– por mecanismos celulares, fagocitosis por macrófagos y células gigantes. Se presenta teñido con un tono azul en ampollas de plástico de 0.5ml, con una caducidad de 24 meses, y totalmente histocompatible. Para la fijación de mallas en la hernia inguinal se aconseja dejar caer una gota cada 2cm aproximadamente, para facilitar la integración de la malla o en el lugar donde habitualmente su usan los puntos de sutura o tackers. El color azul facilita la visión de la gota. La polimerización tarda unos 10s, y la máxima unión se crea en 1min; por encima de los 10s ya no se puede recolocar la malla. Se precisa solo una ampolla (0.5ml) para fijar una malla de 10×15cm. Esta dosis no altera el proceso de integración normal de la malla, ni modifica sus propiedades ni funcionalidad. Aunque es un preparado de mayor pureza, también tiene una temperatura de polimerización cercana a los 50°C.
Dermabond®Dermabond® es un derivado del 2-octil-CA que contiene una traza variable de estabilizador radical en su formulación y que en 1998 se convirtió en el primer pegamento aprobado por la FDA para el cierre tópico de heridas cutáneas. A pesar de tener su indicación para uso externo, también se ha utilizado para fijar mallas en la reparación de las hernias. Para conseguir su efecto adhesivo necesita unos 30s manteniendo las superficies unidas, que es el tiempo que tarda en cristalizar formando una capa sólida pero flexible. Este proceso no se acelera soplando o ventilando la zona. Posteriormente se aconseja esperar un mínimo de 3min a que el pegamento se seque completamente, ya que este alcanza su estructura y fuerza definitiva en 3-5min, proporcionando una firmeza de unión similar a la obtenida a los 7 días cuando se fija mediante sutura. Se presenta en viales líquidos y transparentes de 0.5 y 0.7ml.
Ifabond®Es el adhesivo tisular líquido derivado del monómero de n-hexil-CA que solo contiene mínimas trazas de estabilizantes (radical y aniónico). Fue sintetizado por el Dr. Valérie Vidal-Sailham en 2004, y se denominó pegamento EG 2000. Reformularizado en 2006 para conseguir una mejor duración de su vida, pasó a llamarse Microbond, y obtuvo en 2007 su marca CE para empleo como sustituto de tacker y suturas para fijar mallas en las hernioplastias. Finalmente, en 2009, pasó a llamarse Ifabond®. Obtuvo una nueva licencia para ser usado sin limitaciones en todos los procedimientos quirúrgicos, tanto de nivel externo como interno.
Las ventajas fundamentales de este preparado son su gran pureza y la baja temperatura de polimerización que presenta, lo que contribuye a evitar su toxicidad como adhesivo, a la vez que, al no existir casi impurezas en su formulación, no se ve afectada su eficacia como adhesivo. Esta pureza del Ifabond® permite no tener que recurrir al uso de estabilizantes (generalmente tóxicos) utilizados de manera frecuente en otros CA. Se presenta en viales de 0.5 y 1ml. Dispone de introductor para cirugía endoscópica y de un sencillo aplicador para dosificar en espray fácil de usar y controlar con una sola mano (tabla 3).
Hernias y cirugía de pared abdominalHernia inguinalLa primera referencia sobre el uso de un CA se remonta a 1984 por Shapkina y Kravtsov, en el tratamiento de la hernia inguinal en niños19,20. Canonico et al., en 1995, compararon el uso de un adhesivo biológico con una sutura en la operación de Lichtenstein; no encontraron diferencias en el número de seromas, pero sí una menor tasa de hematomas21. Farouk et al., en 1996, sugirieron que la hernioplastia inguinal abierta puede ser reparada con seguridad y rapidez, sin recurrencias tempranas, usando un AT22. Otros estudios posteriores con dicha técnica en el abordaje abierto han sido realizados por Helbling y Schlumpf23 (2003), Nowobilski et al.24 (2004), Paajanen et al.25 (2011) y Shen et al. (2012), en los que se obtuvieron excelentes resultados con CA y se registraron menor tiempo quirúrgico, hematomas, dolor, consumo de analgésicos y retorno temprano a las actividades diarias con igual tasa de recurrencias a 5 años26. Kim-Fuchs et al., en el mismo año, obtuvieron resultados similares, pero advirtieron de una posible mayor tasa de recidivas (que explican por problemas técnicos durante los meses iniciales), por lo que aconsejan seleccionar su uso para pacientes propensos al dolor27. Para Paajanen et al. el método de fijación de la malla no afecta la aparición posterior de dolor crónico, y las variables que se demuestran como predictores independientes son: 1) la edad más joven; 2) la existencia de dolor preoperatorio, y 3) la duración de la operación. Sobre este último factor sí podría influir notablemente el uso de un AT por cirujanos experimentados25.
Con la operación de Rutkow-Robbins, Testini et al. (2010) obtienen mejores resultados globales en morbilidad a corto y largo plazo, y Eldabe et al. (2012) aconsejan su uso en pacientes con alto riesgo de presentar hematomas, con enfermedades de transmisión sanguínea como el VIH y con dolor preoperatorio a nivel inguinal28,29.
La primera aplicación de un AT en la hernioplastia laparoscópica fue publicada por Jourdan y Bailey en 199830. El principal interés que centra el uso de un adhesivo en la cirugía endoscópica de la hernia es el hecho de poder sustituir el empleo de tackers que se asocia con problemas graves como neuralgias por atrapamiento nervioso, lesión ósea sobre el pubis, hemorragias de la corona mortis y hematomas del espacio de Retzius, dolor crónico, y que encarecen en gran medida el coste del proceso. Estos problemas son erradicados al cambiar las grapas por un adhesivo. Esposito et al. utilizaron en el año 2004 el AT para obliterar el proceso vaginal en el caso de hernias congénitas, evitando su cierre con sutura o grapas sin ninguna incidencia. En 2 casos pudieron verificar el resultado por la necesidad de un segundo procedimiento endoscópico (a 20 y 25 meses), y encontraron una anatomía inguinal perfecta y sin residuos31. En el mismo año y a nivel experimental, Miyano et al., confirmaron la eficacia de la técnica del cierre del saco inguinal en el anillo interno para tratar las hernias indirectas mediante inyección de adhesivo sin riesgo de lesión sobre el conducto deferente y vasos espermáticos (sin que afectara a la fertilidad)32.
Kukleta et al., en 2012, no encuentran efectos adversos ni complicaciones en una larga serie de 1300 reparaciones transabdominales, y obtienen ventajas claras respecto al uso de tackers o fibrina en la variable coste/beneficio. Las mallas fijadas con adhesivo se integran más rápidamente que con suturas: a los 30 días, el 80% de la malla fijada con AT está cubierta por tejido, por un 45% cuando se usa sutura; a los 90 días, la malla con AT está integrada al 100% y con sutura necesita 60 días más. Los autores concluyen que el uso de CA en la fijación de una malla es más rápido, fuerte y rentable que con fibrina, y menos doloroso que con suturas o tackers33. Brügger et al., en el mismo año, demuestran que también mejora de forma significativa la hipoestesia posoperatoria, tanto abdominal como inguinal o genitofemoral, y que es más frecuente y severa cuando se usan tackers (tabla 4)34.
Análisis bibliográfico. Estudios clínicos donde se han utilizado cianoacrilatos en la cirugía de las hernias
| Documentación clínica | ||||||
| Autor, año | Tipo de estudio | Tipo de cianoacrilato utilizado | Número de casos | Seguimiento | Variables | Resultadosa |
| Helbling, 2003 | R | B | 46 | 21,3meses | D | + D |
| Nowobilski, 2004 | R | B | 46 | 1, 3meses | TQ, D, Ca, Ra, Re | + D Ra= TQ Ca Re |
| Testini, 2010 | R | B | 156 | 1, 3, 6, 12meses | D, H, CcRe | + D H Cc= Re |
| Paajanen, 2011 | R | B | 302 | 1, 12meses | TQ, Ca, If | = TQ Ca If= D Cc Re |
| Shen, 2012 | R | B | 110 | 1, 3, 6, 9, 12meses | TQ, D, H, Re | + TQ H D |
| Kim-Fuchs, 2012 | R | B | 264 | 3, 12meses, 5años | TQ, He, D, Re | + TQ= He D Re |
| Eldabe, 2012 | C | B | 198 | 6, 12meses | D, Eh | + He D Eh |
| Kukleta, 2012 | S | B | 1 300 | 1, 6, 12meses, 5años | D, Eh, If, Re | + D Eh If Ce |
| Brügger, 2012 | R | B | 80 | 1, 6, 12meses | He, D, Ra | + He |
| Moreno-Egea, 2012 | C | H | 70 | 12meses | TQ, Ca, D, CeRe | + TQ Ca, D Ce= Re |
Tipo de estudio (C: comparativo; R: randomizado; S: serie personal caso control).
Tipo de cianoacrilato utilizado (B: butil-; H: hexil-).
Variables: variables cuantificadas clínicas (Ca: consumo de analgésicos; Cc: sensación de cuerpo extraño; Ce: coste económico del proceso; D: dolor; Eh: estancia hospitalaria; H: hematoma; He: hipoestesia; If: infecciones; Mo: morbilidad global; Ra: retorno a las actividades diarias; Re: recurrencia; TQ: tiempo quirúrgico) o biomecánicas (resistencia tensil, elasticidad) o histológicas (residuos, inflamación, integración).
No disponemos todavía de ensayos clínicos en el campo de las eventraciones: todas las referencias bibliográficas son de tipo experimental (en ratas). Palmieri et al., en 1999, confirman la ausencia de toxicidad del etil-CA en pared abdominal35. En el año 2001, Birch y Park36 muestran que una malla fijada con octil-CA no afecta al proceso de reperitonización y que induce similares adherencias intraabdominales que los tackers y menos que las suturas, aunque con menor resistencia a la rotura. A nivel de la interfase malla/tejido, en el caso de utilizar suturas se encuentra una migración celular a los intersticios de la prótesis, mientras que en el caso de emplear el AT se aprecia un infiltrado inflamatorio sobre la superficie muscular, aunque las mallas son integradas sin problemas. Los autores concluyen que el CA puede permitir el desarrollo de una nueva técnica para fijar la malla en la reparación de eventraciones. Si pudiéramos eliminar el uso de tackers, podríamos reducir las complicaciones, el dolor posoperatorio y el coste total del procedimiento.
Fortelny et al.37, en 2007, publican resultados desfavorables a nivel biomecánico (existencia de residuos, menor resistencia y mayor rigidez), explicables por el uso de demasiado pegamento y una valoración temprana de los resultados. El trabajo posterior de Losi et al.38 en 2010, sin embargo, muestra una reacción inflamatoria e integración comparable a la causada por la sutura, con un tejido bien vascularizado alrededor de los residuos de adhesivo sin presencia de polimorfonucleares, necrosis o células apoptosicas, y aconseja evitar el uso de grandes cantidades de adhesivo (30μl por cm2).
Dilege et al., en 2010, no encuentran diferencias en la tasa de infecciones, recurrencias, formación de adherencias o resistencia tensil entre el butil-CA y el uso de suturas, y a nivel histológico obtienen iguales resultados en términos de incorporación tisular, fibrosis, infiltración inflamatoria, formación de abscesos y necrosis, y el CA es mejor que la sutura al causar menor reacción a cuerpo extraño39. Ladurner et al., en 2011, sin embargo, muestran que a igual integración de la malla, retracción y formación de adherencias, el pegamento tiene de forma estadísticamente significativa una menor resistencia tensil (9.6±0.8N) que los tackers (14.8±0.7N). Los autores concluyen que el AT todavía no puede sustituir a los tackers en la fijación de la malla, solo reducir su número (tabla 5)40,41. Desde el año 2007, el autor ha venido sustituyendo el tratamiento mecánico de las heridas (suturas o tackers) por el físico (n-hexil-CA) en múltiples procesos de pared abdominal (hernias umbilicales, epigástricas, incisionales, de colostomía y urostomía, de diafragma, etc.,) con excelentes resultados clínicos y sin presentar toxicidad alguna. Dicha experiencia le ha llevado a la reparación de las hernias sin ninguna sutura, experiencia que fue presentada en el Congreso Nacional de Cirugía y publicada en el año 201242,43.
Análisis bibliográfico. Estudios experimentales en animales donde se han utilizado cianoacrilatos en modelos de hernias
| Documentación experimental | |||||
| Autor, año | Tipo de cianoacrilato utilizado | Número de casos | Seguimiento | Variables | Resultadosa |
| Birch, 2001 | O | 22 | 42 (días) | In, Ad, Rt | − RT + Ad |
| Fortelny, 2007 | B | 20 | 17,28 (días)-3 (meses) | Re, Rt, El, In | − RT El In |
| Losi, 2010 | B | 25 | 17,28 (días)-3, 4, 5 (meses) | Re, Rt, In | + RT In |
| Dilege, 2010 | B | 32 | 21,42 (días) | Ad, Rt, If, In, Re | = Ad RT In It |
| Ladurner, 2011 | B | 40 | 1-3 meses | Ad, Rt, In | − RT In = Ad |
Tipo de cianoacrilato utilizado (B: butil; O: octil).
Variables: variables cuantificadas biomecánicas (Ad: adherencias; El: elasticidad; Rt: resistencia tensil) o histológicas (In: inflamación; It: integración Re: residuos).
El análisis de la bibliografía actual nos permite obtener las siguientes afirmaciones respecto al uso de los AT en la cirugía de la pared abdominal: 1) facilidad de aplicación; 2) no precisan de antibióticos; 3) disminuyen la necesidad de anestesia; 4) sellado hermético de las zonas aplicadas; 5) disminuyen el tiempo quirúrgico; 6) eliminan la necesidad de suturas en más del 50% (en heridas superiores a 5cm); 7) mayor bienestar durante el tratamiento y durante el periodo posoperatorio; 8) no presentan efectos adversos (salvo en pacientes alérgicos); 9) abaratan el coste global del proceso quirúrgico por el ahorro en la anestesia, en el tiempo de quirófano, en las suturas, necesidad de analgésicos y visitas o curas durante el seguimiento; 10) dejan una cicatriz de resistencia adecuada (aunque algo menor que con suturas o tackers) pero más estética y con menor dolor crónico, y 11) no modifican la tasa de dehiscencias o recidivas respecto al uso de una sutura tradicional.
Sin embargo, estas conclusiones deben ser tomadas con la adecuada reserva, pues aunque están apoyadas en estudios, algunos de ellos presentan problemas metodológicos como los siguientes: a) calidad general deficiente; b) inclusión de diferentes patologías y técnicas; c) diferentes grupos de pacientes en edad y patologías asociadas; d) pequeño tamaño muestral; e) falta de definiciones precisas (dehiscencia, infección, hematoma, dolor, etc.); f) diferentes métodos de medida, de escalas y de puntuación; g) inclusión de varios adhesivos diferentes; h) exclusión de las incisiones en áreas de tensión; i) heridas de longitud superior a 5cm, y j) pacientes con deterioro de la cicatrización de la herida. En estos 2 últimos casos, nada podemos concluir sobre la posible utilidad de los adhesivos tisulares.
Puntos técnicosLas posibilidades del AT en el campo de la cirugía de las hernias se muestran en la tabla 6. La selección de los pacientes para usar un adhesivo sintético debe comenzarse con la exclusión de aquellos que presenten evidencia de infección activa o riesgo potencial de infección. El cirujano ha de ser cauto cuando se quieran usar en regiones expuestas a tensión o presión directa, tomando las medidas necesarias para reducir previamente esta condición. De la misma manera, debe evitarse su uso en aquellas heridas anfractuosas y en mordeduras de animales que precisen de un desbridamiento. Se debe aconsejar restringir el uso de los CA en pacientes con patologías que puedan alterar el proceso normal de la cicatrización, de la coagulación, posible atopia o reacción de idiosincrasia, alergias dérmicas o dermatitis, y en aquellas mucosas con una secreción constante o hipersecreción.
Usos del adhesivo tisular (cianoacrilato) en la cirugía de la pared abdominal y hernias, propuestos por el autor
| Cirugía | Aplicación | Manejo |
| Heridas | Cerrar la incisión quirúrgica | En capa fina |
| Cerrar planos (aponeurosis y fascias) | En capa fina | |
| Hernias | Fijar la malla | 6-8 gotas |
| Obliterar el proceso vaginal | 1-2 gotas | |
| Cerrar aperturas del saco | 1-2 gotas | |
| Pared abdominal | Estabilizar nudos (evita el deslizamiento) | Una gota sobre los nudos |
| Fijar suturas continuas largas | Una gota repartida 3 veces | |
| Reducir puntos viscerales (evita microtraumatismos y hemorragia) | Fina capa entre 2 puntos de sutura | |
| Reducir el uso de drenajesa | En espray sobre el lecho | |
| Control de sangrado | 1-2 gotas sobre el punto | |
| Laparoscopia | Fijar la malla | 2-3 gotas (Cooper y músculo recto anterior) |
| Cerrar puertos de acceso | 1-2 gotas |
Cuando se quieran utilizar para cerrar una incisión debe asegurarse que existe un bien rasurado, que la piel no esté cubierta de vello. No existe evidencia firme sobre el beneficio de usar antibióticos profilácticos en la hernioplastia; por ello, en el caso de elegir un CA como técnica, no debe usarse tampoco de forma rutinaria, pues aporta un efecto bacteriostático. El cirujano debe ser meticuloso al realizar la hemostasia para asegurar que las superficies a pegar estén limpias y secas para garantizar un óptimo contacto con el adhesivo. La aplicación debe hacerse de forma controlada y bajo visión, para evitar un derrame de pegamento cerca de estructuras nerviosas o del cordón espermático. Los nervios ilioinguinal y genitofemoral deben ser siempre controlados y retirados hasta que el adhesivo esté bien seco, para evitar dejarlo cerca de ellos y que puedan dañarse durante la polimerización y causar una neuralgia. No se debe tocar el tejido con la cánula, para evitar que se obstruya dando una falsa sensación de efectividad; este problema es especialmente difícil de advertir en la cirugía laparoscópica, donde el adhesivo es aplicado a través de una larga cánula.
Los mejores resultados estéticos se obtienen cuando se aplican varias capas finas de adhesivo sobre la superficie, más que cuando se usa una sola aplicación en capa gruesa. Unas 6-8 gotas pequeñas sobre los bordes son suficientes para fijar una malla de 10×15cm. Una cantidad excesiva solo aumenta el calor de la polimerización y no aporta nada a la resistencia final. Tras la primera capa se aconseja esperar unos 30s, pero en las sucesivas capas solo es preciso esperar unos 5-10. Los puntos de fijación deben ser los mismos que para el empleo de suturas, en especial a nivel del pubis y ligamento inguinal. Cuando se utilice una malla de poro pequeño, el adhesivo se debe poner directo sobre el tejido, y después se deja caer la malla rápidamente para asegurar un contacto óptimo. Cuando la malla es macroporosa, se coloca primero la malla bien extendida, y después se aplica el pegamento sobre ambas estructuras. También las aponeurosis (del oblicuo mayor) y fascias (Scarpa y Camper) pueden aproximarse mediante pinzas, y cerradas mediante la aplicación de una ligera capa sobre estos planos, evitando el tejido graso y manteniendo la zona lo más seca posible en el momento de la unión. Este cierre de los planos de la pared evita añadir traumatismos a los tejidos y hemorragias por lesión de pequeños vasos, disminuye los espacios muertos y la tasa final de hematomas o seromas. Podemos aprovechar así el pegamento sobrante haciendo la cirugía más eficiente desde un punto de vista económico. Finalmente, sobre la piel ya tratada no debería aplicarse ningún apósito bajo excesiva presión2,5,12,42,43.
ConclusiónEn la cirugía de las hernias, el empleo de los CA en muchos pasos de la intervención (fijación de la malla, cierre de planos, hemostasia o cierre de la herida, etc.) es una alternativa técnica muy sugerente y de gran relevancia, al ser una de las operaciones que con mayor frecuencia se realiza. En los hospitales aún existe mucha resistencia a su uso en los quirófanos, incluso para tratar heridas quirúrgicas y/o traumáticas, a pesar de ser una práctica con más de 30 años de experiencia. Resulta difícil para el cirujano sustituir la sutura tradicional, realizada de forma manual por la aplicación «poco glamurosa de un pegamento». Este trabajo de revisión no pretende defender la sustitución de todas las suturas quirúrgicas, pero sí parece evidente que en pacientes seleccionados esta nueva técnica podría ofrecerles una mejor calidad de vida. Actualmente, los cirujanos de pared abdominal deben conocer esta nueva forma de tratar una herida y fijar una malla, y a la hora de elegir un método tradicional (suturas o grapas) o un adhesivo tisular deben valorar adecuadamente las características del paciente (edad, comorbilidad, etc.) y las necesidades concretas de la cirugía a realizar (tamaño y tensión de la incisión, estado de los tejidos, hemostasia, lugar donde se sitúa la malla, tamaño y poro de esta riesgo de infección, posibilidad de recidiva, etc.) para poder tomar una decisión bien razonada y que ofrezca el máximo beneficio posible al paciente y a la institución.
Conflicto de interesesEl autor declara no tener ningún conflicto de intereses.