Introducció
Entre les malalties freqüents en l'edat pediàtrica, la patologia al·lèrgica és sense cap mena de dubte la que preval, amb un predomini evident de la patologia respiratòria (rinitis, rinosinusitis, asma, bronquitis eosinofílica), a més de l'afectament d'altres òrgans, com la conjuntiva (conjuntivitis/rinoconjuntivitis), la pell (èczema, urticària, angioedema), l'aparell digestiu (esofagitis eosinofílica, gastroenteritis), i tot com a conseqüència de la sensibilització a diverses substàncies, normalment ben tolerades, que es comporten com al·lergògens (pneumoal·lergògens, aliments, medicaments). A més, diversos estudis posen de manifest l'augment progressiu observat en els darrers anys, amb l'afectament especial de la patologia respiratòria. L'estudi internacional d'asma i al·lèrgies en nens ISAAC (International Study of Asthma and Allergies in Childhood), el més ampli, comprèn una gran extensió geogràfica (66 centres en 37 països) i s'ha dut a terme en dos grups d'edat (6-7 i 13-14 anys). Fins ara s'ha repetit tres cops amb un interval de 7 anys entre la fase I i la III, i ha demostrat l'augment d'aquesta afecció en tots els països1. Els darrers anys a Espanya l'asma ha augmentat del 6,2 al 9,6% de la població, amb diferències en ambdós grups d'edat, mentre que la rinoconjuntivitis i l'èczema es mantenen en xifres semblants1,2. En altres països trobem resultats similars, tot i que les diferències en els percentatges són molt variades1,3.
Les causes de l'increment de la patologia al·lèrgica, sobretot l'afectament de l'aparell respiratori, són discutibles i hi poden influir des de la conscienciació de professionals de diversos països amb nivells de desenvolupament diferents, fins al concepte o definició variable de l'asma, de vegades propiciat per les diferents guies terapèutiques, cosa que pot donar lloc a la inclusió de més pacients amb aquest diagnòstic. Malgrat tot, allò que sembla més demostrat és la influència d'un canvi en l'activitat dels limfòcits T col·laboradors (en anglès, T helper [Th]), que s'activen com a conseqüència de l'estímul d'agents patògens o d'allergògens. Els limfòcits Th1 activats per bacteris o virus donen lloc a la producció d'anticossos específics contra aquests per mitjà de diverses citocines (interleucina [IL] 2, interferó gamma [IFN-γ], factor de necrosi tumoral beta [TNF-β], etc.) que actuen sobre els limfòcits B corresponents. D'altra banda, els Th2 són la causa de la producció d'anticossos contra paràsits i al·lergògens per la intervenció d'altres citocines (IL-4, IL-13, etc.). Hi ha un equilibri en la resposta Th1/Th2, de manera que la producció d'anticossos contra patògens està garantida pel predomini de l'acció de Th1. La producció d'IgE específica contra al·lergògens per l'acció dels Th2 és conseqüència fonamentalment de la predisposició atòpica del pacient, determinada per l'herència o per la disminució de l'activitat dels Th1 pel fet d'haver-hi menys risc davant de patògens4.
Pel que fa a la predisposició atòpica, acceptem que un 12% dels fills de pares no atòpics poden tenir al·lèrgia, mentre que si un dels pares és al·lèrgic, el 19% de la descendència té probabilitats de ser al·lèrgic, xifra que augmenta fins al 42% si els dos progenitors són atòpics i fins al 72% si els dos pateixen la mateixa malaltia al·lèrgica (generalment asma). Per tant, la predisposició atòpica es deu a determinades alteracions de gens encarregats de la resposta immunitària relacionada amb la producció d'IgE específica, la inflamació al·lèrgica i la labilitat bronquial.
Pel que fa al desequilibri Th1/Th2 a favor de les Th2, s'ha establert el criteri d'allò que es coneix com a hipòtesi higiènica5. La millora del nivell de vida i de les condicions higièniques, la influència de les vacunacions i, en definitiva, la reducció del risc d'infeccions en els països desenvolupats sembla tenir una influència important en l'augment de la prevalença de l'al·lèrgia a mesura que disminueix la necessitat de l'acció dels Th1. Així, quan la predisposició atòpica és poc important i hi predomina el risc d'infeccions, els Th1 dominen la situació, que es redueix al màxim quan es minimitza aquest risc (acció de Th2). Malgrat això, el predomini de l'activitat de Th2 també pot succeir a causa de la sobreexposició a contaminants ambientals o a al·lergògens, per un mecanisme epigenètic, pel fet que els mecanismes de regulació genètica no impliquen canvis seqüencials d'ADN6,7. De tota manera, no es descarten altres possibles coadjuvants en l'aparició de malalties respiratòries, com ara l'obesitat o l'activitat física, més habituals en països desenvolupats8.
Incidència en la síndrome de Down
Hi ha pocs estudis referents a la incidència de patologies allèrgiques en aquests nens, cosa que probablement indica l'escassa probabilitat que experimentin aquestes malalties. En una publicació recent, Mannan et al9 presenten un estudi interessant que pot servir de base a altres treballs més amplis amb la mateixa finalitat: el cribratge de la població amb síndrome de Down per tal d'esbrinar l'existència o risc de patologia al·lèrgica. Es tracta d'un estudi retrospectiu en què es van incloure 39 nens amb síndrome de Down (amb edats compreses entre els 0,75 i els 17 anys) que es van remetre als serveis d'al·lèrgia de diferents hospitals nord-americans amb símptomes indicatius d'al·lèrgia: rinitis crònica, sinusitis crònica o recurrent, tos o dispnea i d'altres no determinats. Els resultats es van comparar amb els d'un grup de control que tenia el mateix nombre de nens d'edats similars, estudiats en els mateixos centres i per motius clínics semblants. En tots els casos es van fer proves cutànies (prick-test) amb pneumoal·lergògens comuns (àcars, pòl·lens, fongs) que van donar resultats positius (no s'especifica a quants al·lergògens en cada cas) en 7 dels nens (18%) i en 21 (54%) dels controls. Com es pot apreciar, hi ha una diferència notable entre els dos grups, amb la singularitat que en 30 dels 39 pacients amb síndrome de Down hi havia familiars de primer grau afectats per processos al·lèrgics (asma, rinitis, dermatitis atòpica), cosa que contrasta amb les xifres esmentades anteriorment sobre el risc de tenir al·lèrgia els fills de les persones afectades per aquesta patologia.
En un altre treball, Forni et al10 van investigar la presència d'asma en nens amb síndrome de Down de 545 famílies en què hi havia altres 294 germans que també es van sotmetre a l'estudi. La prevalença d'asma en els nens amb síndrome de Down va ser significativament més baixa (p < 0,001) que en els germans, en els quals la incidència d'asma era semblant a la de la població general en el moment de la publicació. A més, en 30 de les 545 famílies, almenys un dels pares tenia antecedents d'asma i la mateixa malaltia es va detectar en 12 fills d'aquestes famílies. Només un dels pacients estudiats amb síndrome de Down, de 10 anys, havia tingut símptomes lleus d'asma a l'edat de 2-5 anys, amb proves cutànies d'IgE positives a àcars, mentre que un germà de 12 anys tenia asma greu.
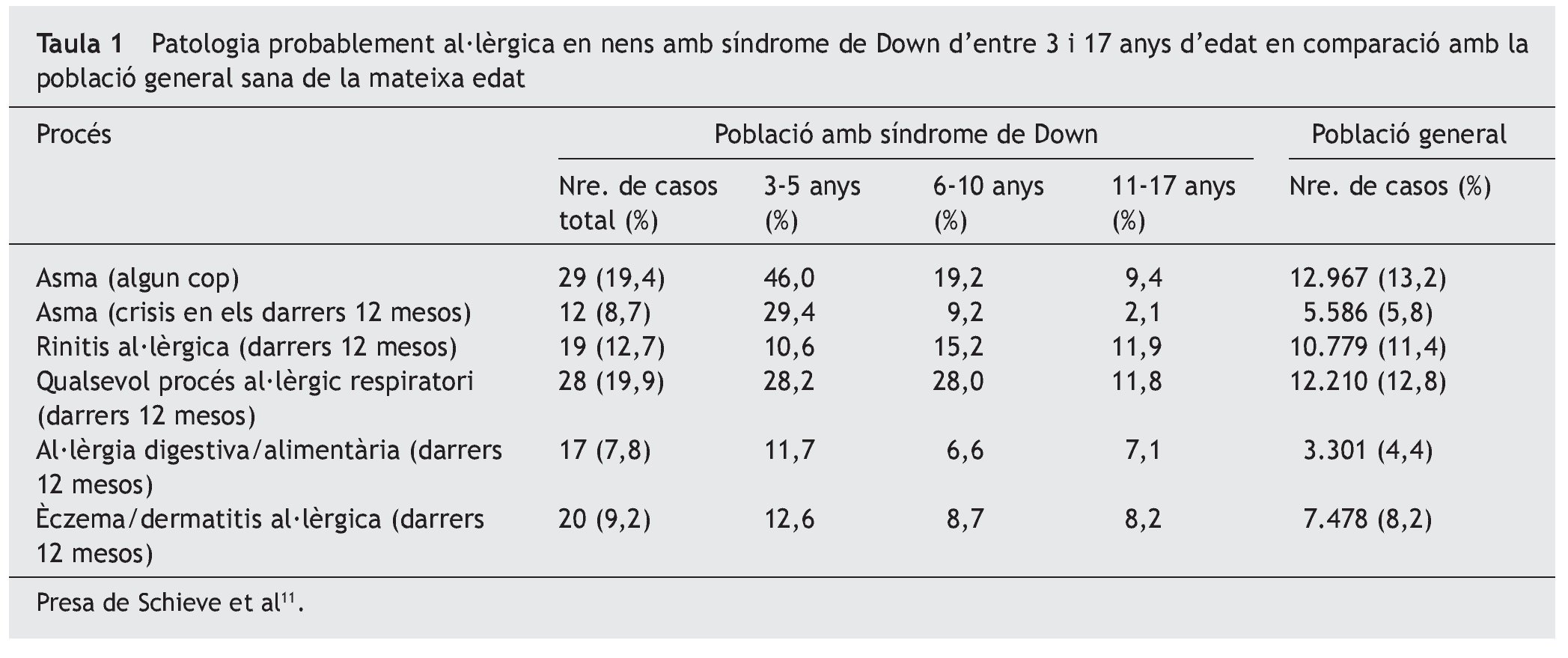
Aquests resultats contrasten amb els que van obtenir Schieve et al11 en un estudi realitzat entre 1997 i 2005 en 146 nens amb síndrome de Down amb edats compreses entre els 3 i els 17 anys, i un grup de control de 95.454 nens de les mateixes edats. A més, hi van incloure 604 pacients amb diferents processos mentals no especificats, els resultats dels quals no especifiquem. Van estudiar processos respiratoris (asma, rinitis), digestius/alimentaris i èczema, a més d'altres no relacionats amb atòpia. Van trobar més del doble de la població general, afectats d'al·lèrgia digestiva/ alimentària i un augment moderat de processos respiratoris (taula 1). Per grups d'edat, la freqüència de tots aquests processos es va reduint, cosa que d'altra banda és habitual en la població al·lèrgica general, pels possibles motius que es comenten més endavant.
Condicionants genètics
Trisomia 21
Actualment sabem que en el cromosoma 21 hi ha més de 400 gens, 139 més que en la primera seqüenciació, publicada per Hattori et al12 l'any 2000. D'aquests, almenys 83 són exclusius de l'espècie humana, mentre que 140 són compartits amb el ratolí, animal que ha servit de model per al coneixement de l'activitat d'aquests13. La relació d'aquests gens amb la patologia immunoal·lergològica és molt incerta, tret que la triplicació impliqui alguna mutació o modificació de l'ARN, els nivells del qual augmenten fins al 50%14,15. Els gens amb més possibilitats de estar-hi implicats són els que participen en la resposta immunitària per interferó i els que regulen algun aspecte de les molècules d'adhesió.
En un estudi sobre les bases genètiques de la dermatitis atòpica, Bu et al16 han vist implicats una sèrie de gens en diversos cromosomes, un d'ells el 21q21, que podria estar involucrat en la gravetat del procés, sobretot en persones que a més presenten asma. Aquest descobriment indica una possible relació entre la trisomia 21 i la incidència de processos al·lèrgics.
Immunitat
En la defensa enfront de patògens intervé un intricat complex immunològic, des dels elements que constitueixen la "immunitat innata", com les barreres cutaneomucoses i el sistema complement, i les diferents cèl·lules implicades en la "immunitat adquirida", que assoleixen el seu objectiu per mitjà dels mediadors (citocines), els receptors de diverses cèl·lules, la producció d'anticossos i altres elements que participen en la dinàmica cel·lular (molècules d'adhesió) i la inflamació (quimiocines). El procés passa per la captació dels patògens per part de les cèl·lules que presenten antígens (dendrítiques, macròfags), el seu processament intracel·lular (fragmentació), la presentació als diferents limfòcits, l'estímul dels limfòcits B i el seu pas a plasmòcits productors dels anticossos (immunoglobulines M, G i A i les seves subclasses). En el funcionament de tot aquest sistema tan complex intervenen molts gens, que es troben en la major part dels cromosomes; fins i tot els diferents fragments que componen les immunoglobulines (dues cadenes pesants i dues lleugeres) estan codificats per gens distints17. L'agressivitat del patogen o les circumstàncies del pacient (socials, ambientals, patològiques) fan que aquests mecanismes defensius fallin, però sobretot l'existència de mutacions o d'altres alteracions genètiques donen lloc a les diferents immunodeficiències conegudes, per a les quals s'han identificat una centena d'alteracions genètiques responsables d'aquestes18.
La freqüència més gran de malalties infeccioses amb possibilitat de ser greus en les persones amb síndrome de Down s'ha associat en part amb el desenvolupament diferent del tim, que és més petit i té una estructura anormal, per la qual cosa observem una disminució marcada de diverses subclasses de limfòcits i un possible augment dels NK (de l'anglès, natural killer), així com la deficiència o l'alteració en la producció d'immunoglobulines, que pot relacionar-se amb la producció marcadament més petita de limfòcits B. Alguns d'aquests fets, juntament amb la incidència més gran de processos autoimmunitaris i tumorals, més freqüents en edats molt posteriors, han fet que s'hagi titllat d'envelliment precoç del sistema immunitari en la síndrome de Down19.
Atòpia
La reacció al·lèrgica es produeix pel predomini de l'activitat dels limfòcits Th2 i el consegüent augment d'IgE específica, així com, en el cas de l'asma, per la hiperreactivitat bronquial (HRB)20,21. El cromosoma 11 (11q13) va ser el primer en el qual van provar d'identificar gens implicats en la producció d'IgE; en aquest cromosoma radica la síntesi de la cadena β del receptor d'alta afinitat d'IgE (FcεRI-β), l'interès del qual en la resposta al·lèrgica no està ben establert.
Fins avui s'han identificat una vintena de locus en diversos cromosomes i encara queda per confirmar la relació d'alguns d'aquests amb el desenvolupament de l'atòpia (taula 2). L'interès més gran es centra en el cromosoma 5 (5q31-q33), que conté els gens que modulen la producció d'interleucines secretades pels limfòcits Th2, com la IL-4 i la IL-13, encarregades de la resposta atòpica pel fet d'estar implicades en la secreció d'IgE pels limfòcits B (plasmòcits), així com d'altres interleucines (IL-3, IL-5, IL-9) que també participen en la patogènia de l'asma (eosinofília, inflamació). El receptor de la IL-4 en les Th2 sembla que depèn d'un gen situat al cromosoma 16 (16p12.1), on també hi ha gens que podrien controlar altres elements implicats en la patogènia de l'atòpia. Sembla que la producció d'IgE també podria dependre d'altres gens situats als cromosomes 7 i 14 i també al 6, que controla el complex d'histocompatibilitat principal (HLA II), que s'ha relacionat amb una possible susceptibilitat individual més gran a alguns allergògens.
La coincidència de la predisposició atòpica i l'existència d'HRB és la condició per patir asma al·lèrgica. La precocitat en l'aparició de la malaltia apunta a l'existència d'HRB congènita, que podria estar causada per polimorfismes o possibles mutacions. La freqüent coexistència d'aquests dos condicionants va fer pensar que els gens responsables podrien trobar-se en el mateix cromosoma 5 en què ja s'havien observat locus que codifiquen la producció de les interleucines implicades en la producció d'IgE, tal com es va confirmar més tard.
A més, també s'han demostrat fins a 9 mutacions en el receptor adrenèrgic β2 del múscul llis bronquial, de les quals la substitució de glicina por arginina en posició 16 de la cadena proteica del receptor s'ha relacionat amb la gravetat de l'asma, en el sentit d'una resposta menor a l'administració d'agonistes β2. La substitució de glutamat per glutamina en la posició 27 agreuja la situació, mentre que també s'hi concedeix alguna participació a la substitució de la treonina per isoleucina.
En els fibroblasts del pulmó i en el múscul llis bronquial, però no en les cèl·lules epitelials, s'ha demostrat l'existència del gen ADAM33, situat al braç curt del cromosoma 20 (20p13), que codifica la metal·loproteasa, un grup d'enzims que s'han relacionat amb la HRB i amb el procés de remodelació bronquial.
Comentaris
Sense cap mena de dubte, la menor incidència de malalties al·lèrgiques en aquests nens està relacionada amb aquest entramat genètic i, sobretot, amb la incidència més alta d'infeccions pels defectes que hi ha hagut en els responsables genètics de la defensa antiinfecciosa. Aquest risc més alt de patir infeccions concordaria amb la "hipòtesi higiènica", perquè, tot i que amb dificultats, el sistema immunitari en aquests casos ha de ser predominant davant dels patògens en un esforç per superar les deficiències.
En el treball esmentat de Schieve et al11, en què hi ha un predomini clar de "patologia al·lèrgica" en aquests nens en comparació amb la població general, el diagnòstic es basa en la referència dels pares i no hi consta la confirmació per un professional, cosa que pot haver generat diagnòstics incorrectes o insegurs. En el cas de l'asma en la població pediàtrica general, el més habitual és que les xifres d'incidència disminueixin de manera semblant a les que presentem aquí, d'acord amb els diferents fenotips descrits22. Gairebé sempre, la causa en són les infeccions víriques (VRS, rinovirus, parainfluença i altres) que es repeteixen com a conseqüència de la immaduresa immunitària en els més petits, cosa que sovint dóna lloc a etiquetar-les erròniament d'asma, en lloc de bronquiolitis o bronquitis amb dispnea. Amb els casos inclosos en l'estudi pot haver succeït el mateix, pel fet de tenir més possibilitats de patir virasis respiratòries23,24.
En conclusió, vistes les poques publicacions sobre la incidència de processos al·lèrgics de qualsevol tipus en els nens amb síndrome de Down, malgrat que per contra hi predominen els que s'ocupen de la prevalença d'infeccions o d'altres processos relacionats amb la fallida de la defensa immunitària (autoimmunitàries, leucèmies, neoplàsies), és evident l'escassa presència de patologies al·lèrgiques en aquestes persones.
Correu electrònic: 5314fml@comb.cat (F. Muñoz).
Rebut el 19 de juliol de 2010;
acceptat el 20 d'octubre de 2010