Las técnicas en cirugía de catarata han evolucionado hasta la actualidad con el láser de femtosegundo, empleado para realizar precisas incisiones corneales, capsulotomía anterior, fragmentación del núcleo y corrección de astigmatismo corneal de bajo grado mediante incisiones arqueadas. Se han observado mejores resultados con el láser en relación con la reproducibilidad y la exactitud de cada procedimiento, logrando cada vez más aceptación en todo el mundo. Por eso es necesario establecer los puntos principales de esta técnica para hacerla más reproducible, resaltar las diferencias que existen con relación a la técnica de facoemulsificación convencional y acortar la curva de aprendizaje que esta puede representar.
The techniques in cataract surgery have evolved to the present with the femtosecond laser, used to make precise corneal incisions, anterior capsulotomy, fragmentation of the nucleus, and correction of low grade corneal astigmatism by arcuate incisions. Best results have been observed with the laser with respect to reproducibility, and accuracy of each procedure; achieving growing acceptance worldwide. So it is necessary to establish the main points of this technique to make it more reproducible, highlight the differences in relation to conventional phacoemulsification technique and shorten the learning curve that this may represent.
Las técnicas en cirugía de catarata han evolucionado desde sus comienzos con la extracción intracapsular a la extracapsular, y hacia la facoemulsificación, llevando a un decremento progresivo en el tamaño de la incisión quirúrgica, incrementando la seguridad y mejorando los resultados visuales; siendo la facoemulsificación, la cirugía de elección en las últimas 2 décadas1. El láser ha sido utilizado en cirugía de catarata desde los 70, cuando en 1975 Krasnov reportó el uso en una modalidad de láser rubí (694nm) para crear microincisiones en la cápsula anterior, nombrándola facopuntura2. Posteriormente, en 1987 Peyman y Katoh enfocaron el láser Nd:YAG en el núcleo cristaliniano, induciendo una fotoablación3; y Kanellopoulos et al.4 reportan en 1999 el uso del láser de nanosegundos (Dodick Photolysis, Q-switched Nd:YAG laser) para fragmentar y emulsificar el cristalino, con baja liberación de energía y calor intraocular, de forma segura y eficaz. Estos esfuerzos ayudaron a la investigación y el desarrollo de la cirugía de catarata asistida con láser de femtosegundo, que es una de las principales innovaciones en la cirugía oftálmica moderna. El láser de femtosegundo es útil en la cirugía ocular debido a los pulsos ultrarrápidos en el rango de 10−15segundos, capaz de crear incisiones precisas, mediante fotodisrupción por ionización de átomos y formación de ondas de choque con el fenómeno llamado Laser-Induced Optical Breakdown (LIOB), creando un plasma el cual al enfriarse genera una burbuja de cavitación que a su vez crea disrupción de los enlaces químicos liberando CO2 y agua, formando una línea continua para separar el tejido, disminuyendo así los requerimientos de energía para la disrupción tisular y limitando los cambios de los tejidos adyacentes al sitio de aplicación. Este tipo de láser actúa con longitudes de onda cercanas al infrarrojo (1,030nm), y es capaz de penetrar la córnea transparente, en algunos casos con opacidad leve, con la limitación en casos vascularizados y/o presencia de placas densamente calcificadas5. Con el advenimiento de estas nuevas tecnologías, y de lentes intraoculares tóricos, multifocales y trifocales, denominados Premium, los pacientes solicitan cirugía de forma más temprana, con menor tolerancia a las alteraciones visuales posteriores, aumentado así las expectativas de resultados refractivos satisfactorios6. En 2009, Nagy et al. publicaron el primer estudio con el sistema láser de femtosegundo LenSx para cirugía de catarata, comparando la creación de capsulorrexis manual versus asistida por láser en ojos porcinos, y observaron mejores resultados con el láser con relación a reproducibilidad, resistencia, uniformidad y exactitud7. En agosto de ese mismo año, el LenSx fue aprobado por la FDA para la realización de capsulotomía anterior, y en diciembre para la realización de las incisiones corneales. En abril del 2010 se aprueba para la fragmentación del núcleo cristaliniano, marcando el inicio de una nueva era. Sin embargo, la introducción de un nuevo procedimiento en la práctica clínica siempre involucra una curva de aprendizaje. Actualmente el láser de femtosegundo es empleado para crear incisiones corneales, capsulotomía anterior, fragmentación del núcleo, y corrección de astigmatismo corneal de bajo grado mediante incisiones arqueadas, mejorando los resultados8. En junio del 2012 se introduce en el Hospital Central Militar el primer láser de femtosegundo para cirugía de catarata en México, siendo pioneros en esta tecnología, la cual exitosamente se ha extendido en las diversas regiones de nuestro país por lo que se cree necesario establecer los puntos principales de esta técnica para hacerla más reproducible, resaltar las diferencias que existen con relación a la técnica de la facoemulsificación convencional, así como para acortar la curva de aprendizaje que esta puede representar.
Descripción de la técnicaSe divide el procedimiento en 3 fases:
- 1.
Programación de los parámetros
- 2.
Procedimiento femto
- 3.
Facoemulsificación asistida con láser de femtosegundo (femtofaco).
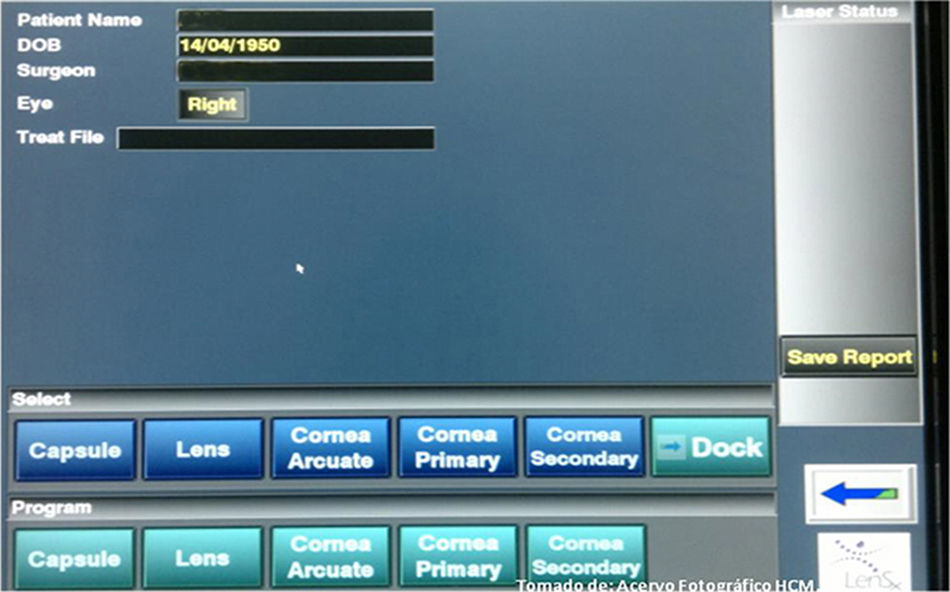
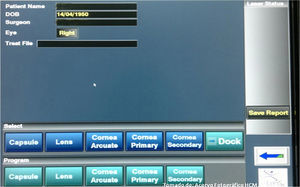
Se puede realizar dentro de un quirófano estándar cubriendo los requerimientos indicados por la casa comercial para el equipo láser (temperatura ambiente de 18-24° y porcentaje de humedad≤65%), utilizando la plataforma LenSx V2.23 (longitud de onda 1,030nm de 50kHz, pulsado de 600-800femtosegundos, con un pulso máximo de energía de15μJ; ALCON Laboratorios, Fort Worth, TX, EE. UU.) para la programación de las incisiones corneales, capsulotomía anterior, fractura del cristalino, y en algunos casos, incisiones arqueadas. Se programa el software introduciendo los datos del paciente seleccionado: nombre (iniciales), fecha de nacimiento, nombre del cirujano y ojo a operar. Posteriormente se seleccionan los procedimientos que se realizarán guiados por monitor con control táctil (fragmentación de cristalino, capsulotomía anterior, incisión corneal primaria, incisión corneal secundaria e incisión arqueada) (fig. 1). Cada parámetro se puede realizar de forma personalizada de acuerdo a las características del ojo a operar, o preferencia del cirujano.
- •
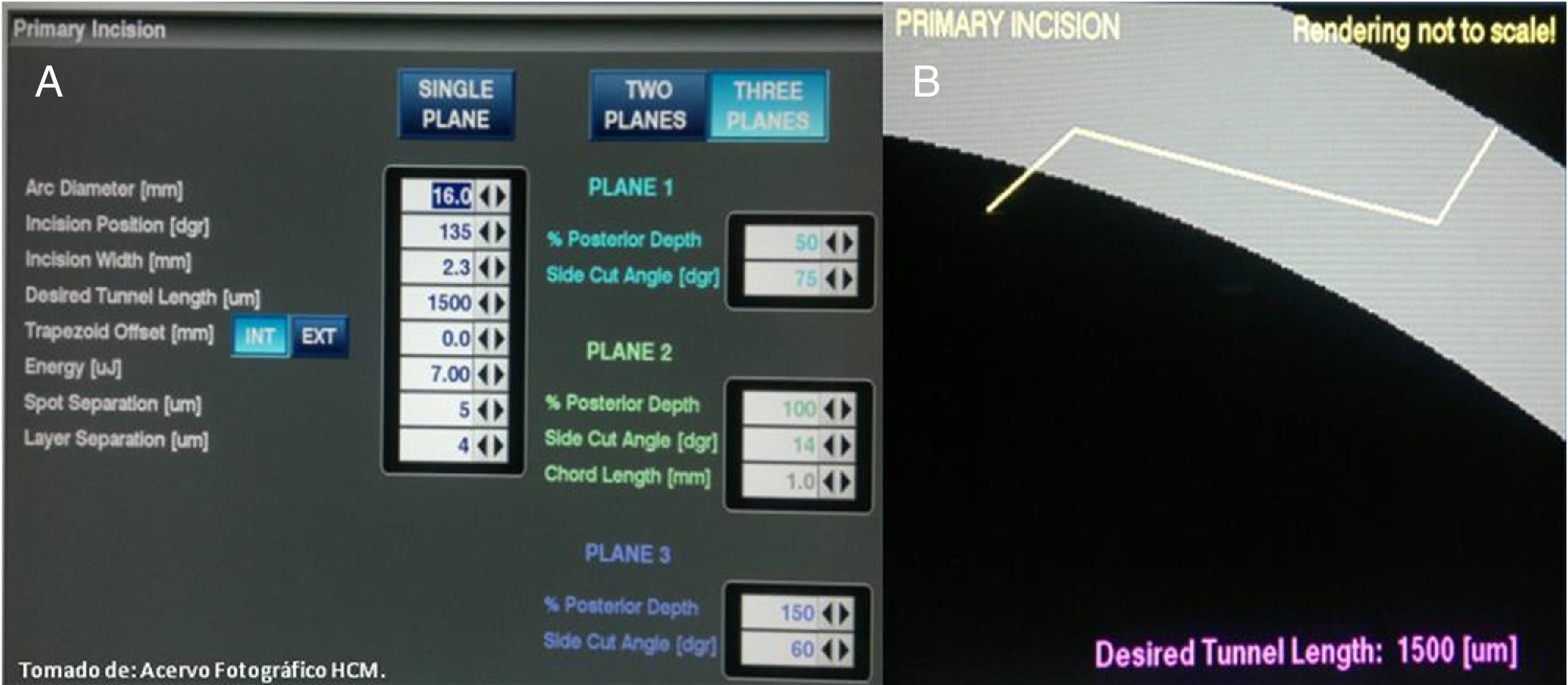
Incisión corneal primaria: se puede realizar de acuerdo al tipo de punta/manga de facoemulsificación a utilizar, así como del cartucho y lente seleccionados siendo los estándar de 1.8-3mm, con una longitud de 1,500μm, recomendando realizarla en 3 planos, con una energía de 7μJ (fig. 2).
- •
Incisión corneal secundaria: diámetro externo a 1.1mm, con longitud de 1,500μm, con la posibilidad de realizar hasta 2 incisiones, con una energía de 6μJ. (fig. 3).
Se recomienda realizar las incisiones en forma trapezoide, siendo 0.1mm mayor el diámetro externo que el interno, con objetivo de lograr una incisión hermética y de fácil acceso. Posteriormente, se selecciona el eje de cada incisión, siendo factible realizar una rotación del mismo in vivo ya con el acoplamiento (docking) en el ojo (como en los casos donde se desea alinear con marcas previas para lentes tóricos, o tratando de evitar alguna cicatriz o incisión corneal previa, como en la queratotomía radiada), recomendando colocar la incisión primaria a 120-135¿, y la secundaria a 90¿ de la primaria. Se utiliza separación del spot de 5μm, separación entre capas de 4μm, y energía de 6-7μJ.
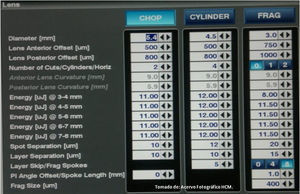
Capsulotomía anteriorEl diámetro que se recomienda es de 0.5mm menor al diámetro de la óptica del lente a utilizar; siendo lo más frecuente de 5-5.5mm; con separación del spot de 5μm, separación entre capas de 5μm, energía de 11μJ (variando de acuerdo a las características de la cápsula, siendo mayores en jóvenes, con presencia de pigmento capsular o calcificaciones) (fig. 4).
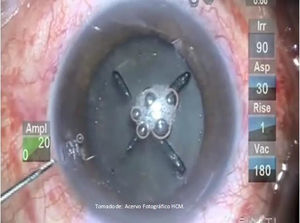
Fractura del cristalinoVaría de acuerdo al caso, dureza y elección del cirujano; recomendando no exceder 1mm del diámetro de la capsulotomía (de forma convencional se realiza con longitud de 6mm, con buen resultado). Habitualmente se utilizan parámetros con un diámetro de 5-6.5mm, separación del spot de 10μm, separación entre capas de 10μm, energía de 10μJ (este parámetro puede variar de acuerdo a la densidad del cristalino, siendo proporcional a esta, con límite superior de 15μJ). En el software actual se pueden utilizar chops (hasta 3), cilindros (hasta 8), o con un patrón de fragmentación en cubo (tipo Waffle); cada caso es diferente, tomando en cuenta que en cataratas densas es más útil un mayor número de chops y/o cilindros; y dentro de la curva de aprendizaje se sugiere iniciar con 2-3 chops, combinados o no con 1-2 cilindros (fig. 5).
Preparación del pacienteSe inicia 45min antes de la cirugía, con administración de tropicamida y fenilefrina (TP Ofteno, 50mg/8mg/ml, Sophia, Zapopan, Jalisco, México) en gotas en fondo de saco del ojo a operar cada 15min en 3 ocasiones, para lograr una adecuada dilatación pupilar; se lleva a cabo una monitorización de signos vitales bajo supervisión de médico anestesista, sin realizar sedación (para permitir una adecuada cooperación del paciente y que pueda seguir instrucciones durante el procedimiento). Posterior a esto, se desplaza la camilla (debe ser capaz de levantar a un paciente en decúbito supino de 84-105cm, medida desde el suelo hasta el plano de la córnea, y un ancho de camilla<84cm para permitir un adecuado alineamiento del ojo bajo el objetivo láser) hacia la plataforma láser, dentro del mismo quirófano, verificando que se encuentre a la altura y distancia adecuada del mismo. Se instila anestesia tópica tipo tetracaína al 0.5% (Ponti Ofteno, 5mg/ml, Sophia, Zapopan, Jalisco, México), administrándola sobre la superficie ocular 5min antes de la cirugía, y otra gota inmediatamente antes del acoplamiento ocular.
Preparación de interfase estéril SoftFitEste dispositivo está conformada por una interfase curva y un lente de contacto (hidrogel-silicona, contenido en una solución estéril, con rango queratométrico recomendado de 35-48D), los cuales al acoplarse son montados en la terminación del objetivo láser (girándola hacia el lado derecho o izquierdo de acuerdo al ojo seleccionado, hasta escuchar un «click», el cual indica que se realizó de forma correcta, sirviendo como barrera estéril entre el láser y el paciente) (fig. 6).
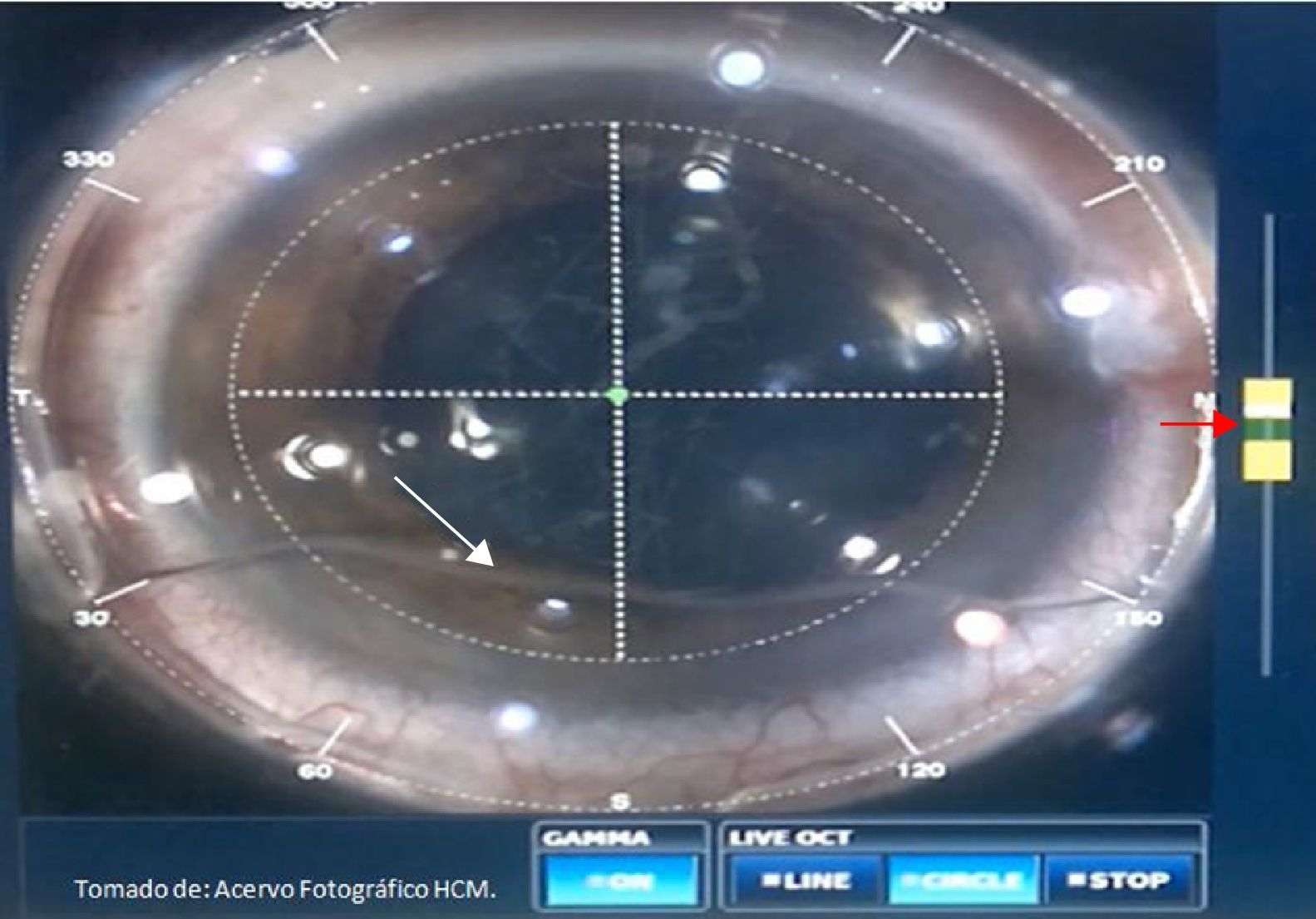
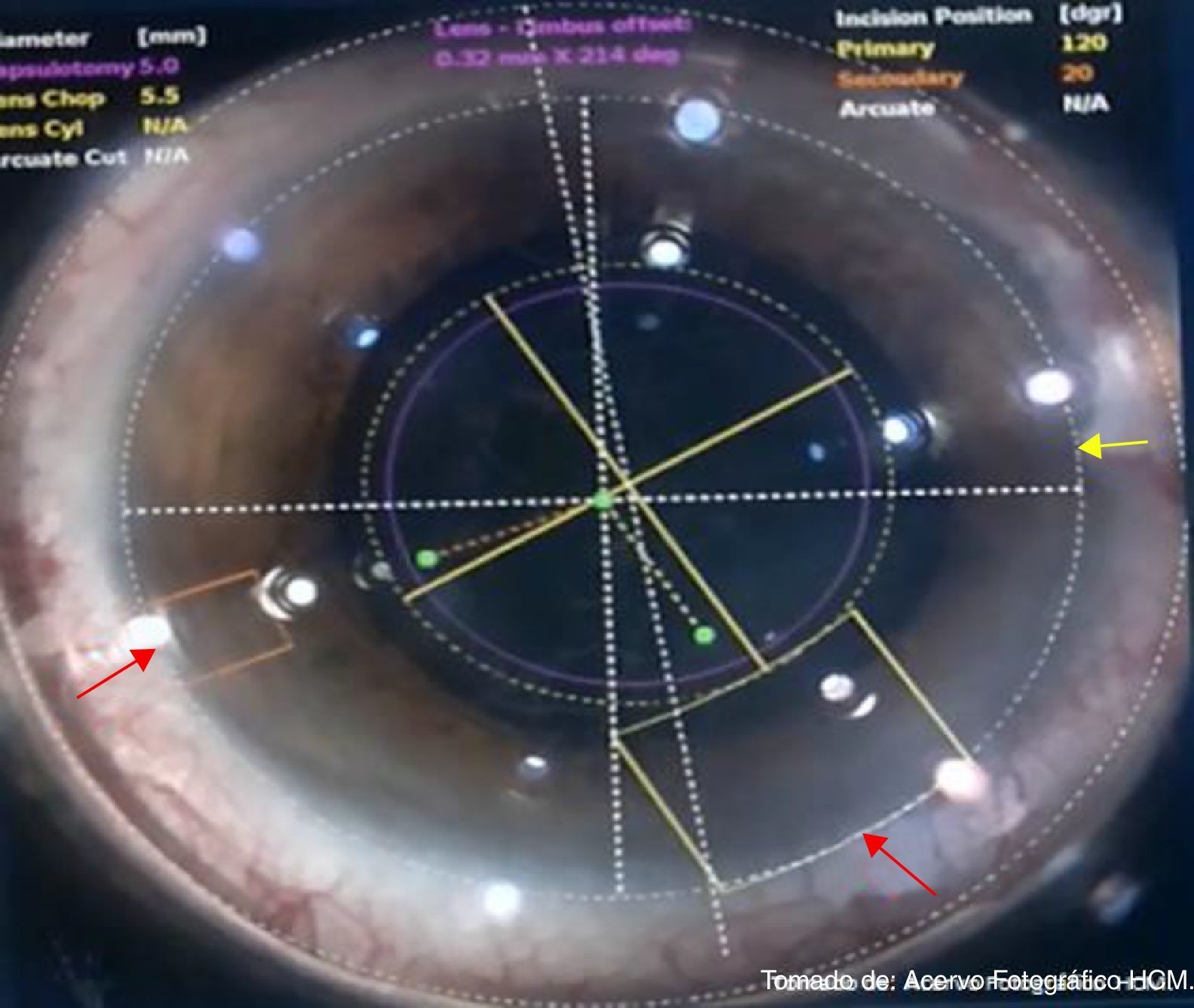
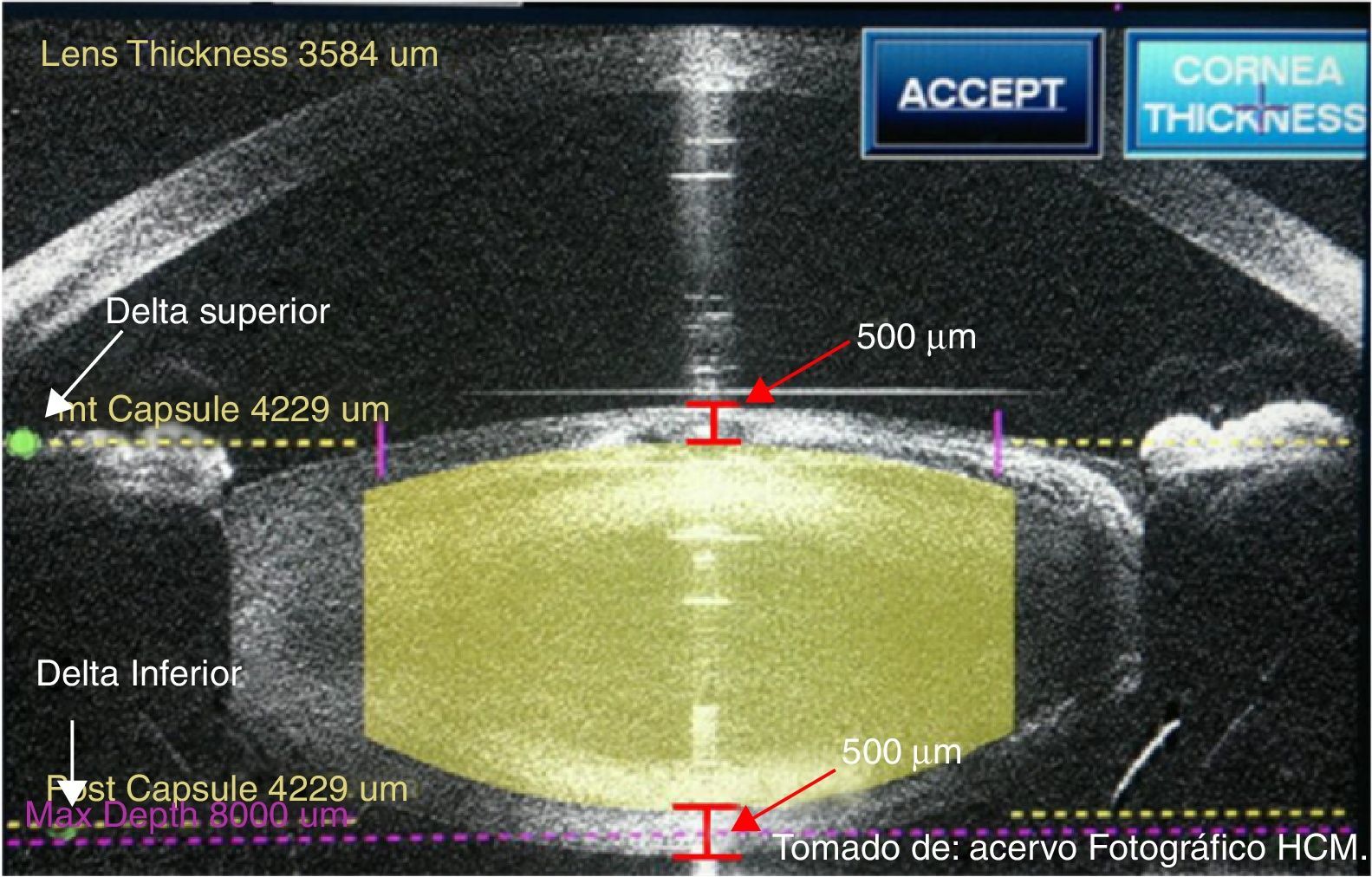
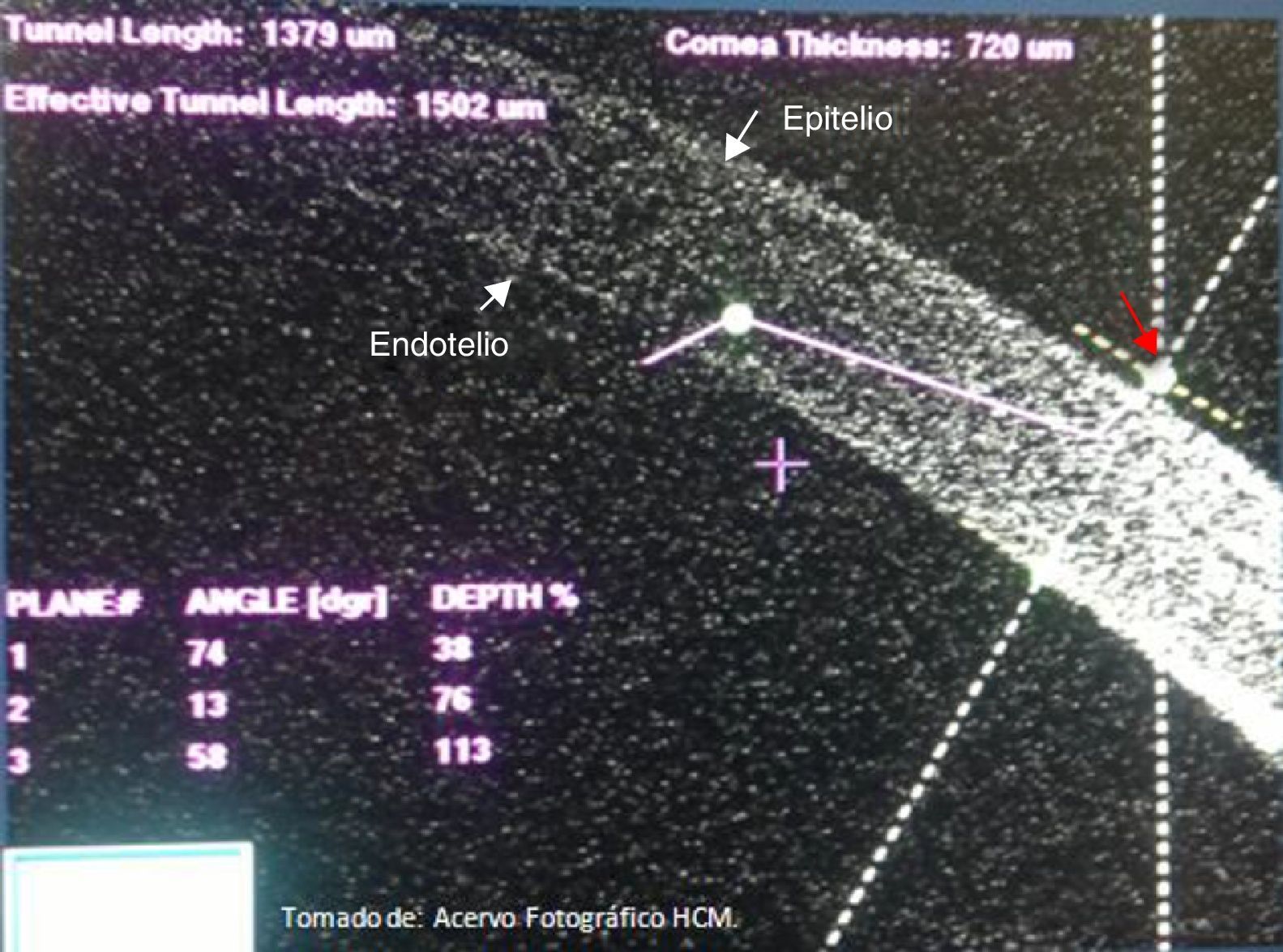
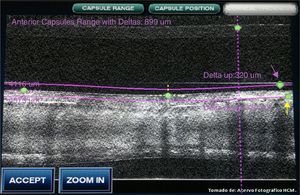
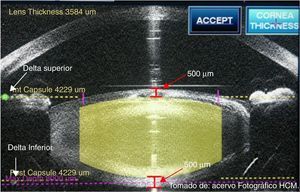
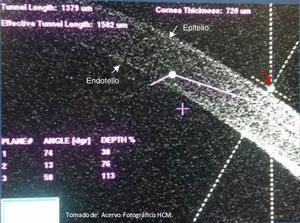
Procedimiento femtoAcoplamiento cornealDespués de seleccionar todos los parámetros y preparar al paciente, se coloca blefaróstato tipo Slade-Murdoch (AE-1033 Asico, Westmont, IL, EE. UU.) y se procede a realizar contacto corneal mediante acoplamiento utilizando una interfase estéril SoftFit; el sistema desciende hasta realizar contacto con el ojo, se detecta mediante sensores la posición del objetivo y la fuerza de aplanamiento, el cirujano observa el aplanamiento de la córnea usando un dispositivo de videomicroscopio, aplicando succión cuando se consiguió un acoplamiento corneal adecuado (fig. 7). El primer paso es lograr un adecuado centrado del limbo esclerocorneal, posteriormente el centrado de la capsulotomía en relación con la pupila y la posición de las incisiones corneales (principal y secundaria) (fig. 8). Al realizar estos pasos, se inicia la lectura mediante tomografía de coherencia óptica del segmento anterior; es necesario un correcto alineamiento del globo ocular (fig. 9), procediendo a verificar que la profundidad de la capsulotomía sea la adecuada mediante una imagen en tiempo real en forma lineal, la cual debe ajustarse entre los 2 deltas de referencia (fig. 10), y el correcto ajuste de profundidad y longitud de la fragmentación del cristalino (respetando 500μm por debajo de la capsula anterior y 500μm por arriba de la posterior) (fig. 11). Se verifican las características de la incisión corneal primaria, ajustando la longitud (se recomienda empezar con 1,500-1,800μm, ajustando el parámetro en cada caso y la arquitectura de la incisión), procurando que el corte epitelial sobrepase el plano corneal para realizar una adecuada apertura epitelial transquirúrgica, y a nivel endotelial mantener el plano de corte por encima del mismo (fig. 12). Una vez verificado y aceptado este proceso, se da inicio al tratamiento con láser en una secuencia de: capsulotomía, fragmentación del cristalino e incisiones corneales. El procedimiento varía 30-60seg en promedio, dependiendo de la programación establecida; con un tiempo total desde el inicio del acoplamiento corneal hasta la liberación de la interfase del mismo de 2.5-3min.
Visualización del acoplamiento corneal. Flecha blanca: interfase de acoplamiento que indica un adecuado contacto con la superficie ocular. Flecha roja: durante el descenso del objetivo láser, el indicador de acoplamiento debe encontrarse dentro del límite marcado entre las 2 barras amarillas (barra verde), para realizar una exitosa succión ocular.
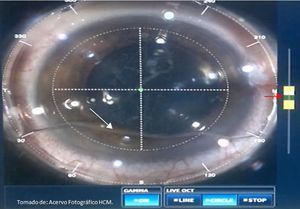
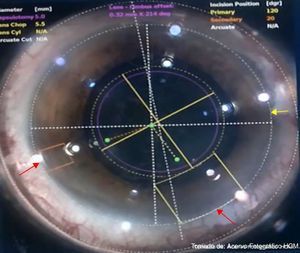
Centrado del limbo esclerocorneal e incisiones corneales. El centrado del limbo se realiza ajustando la línea punteada (flecha amarilla) sobre el limbo esclerocorneal mediante movilización del cursor central. Las incisiones corneales se ajustan en su borde periférico al limbo esclerocorneal (flecha roja), en una secuencia de incisión primaria y posterior la secundaria.
Tomografía de coherencia óptica para ajuste de la fragmentación del cristalino: Ajuste de profundidad y longitud de la fragmentación del cristalino (flechas blancas: deltas de referencia para ajuste. Flechas rojas: margen de seguridad de 500μm por debajo de la capsula anterior y 500μm por arriba de la posterior).
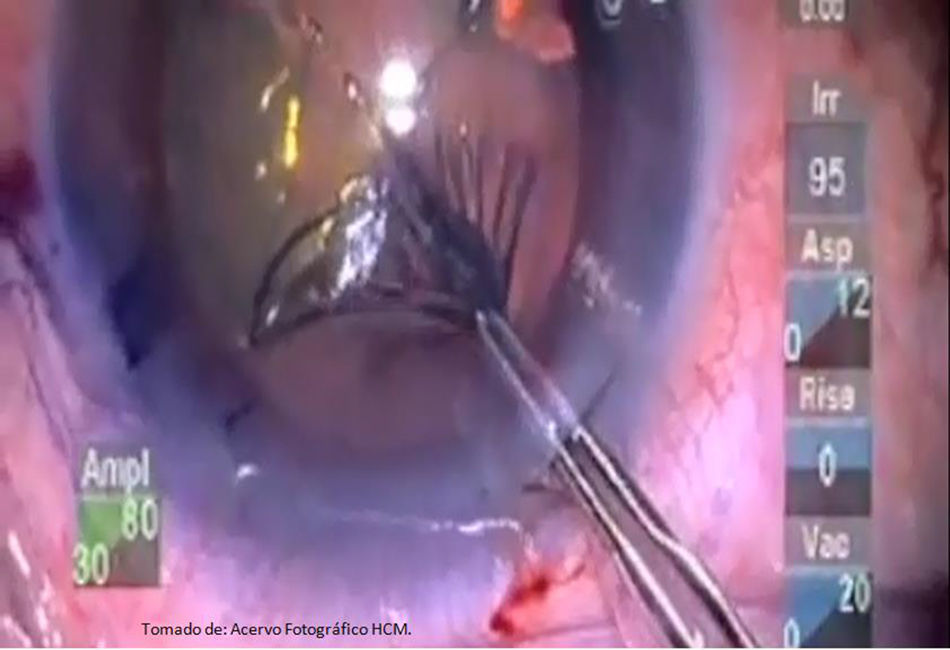
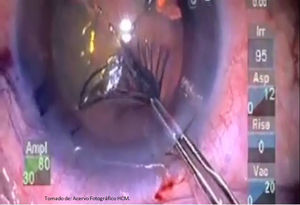
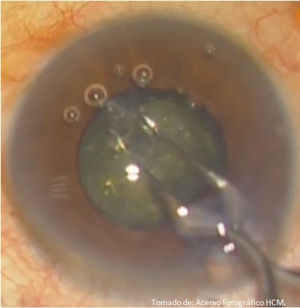
Después de realizar el procedimiento femto, se desplaza en el mismo quirófano y camilla al paciente bajo el microscopio quirúrgico, continuando con la monitorización sistémica, asistido bajo una sedación con un ansiolítico y opioide a dosis respuesta, sin causar hipnosis; continuando con la administración de anestesia tópica sobre la superficie ocular y posterior a criterio del cirujano. Se continúa la preparación quirúrgica estéril de la región periocular con isodine solución al 10%, incluyendo fondos de saco con dilución al 5%, exposición de 3min; colocación de campos estériles; blefaróstato (Lieberman, Asico, Westmont, IL, EE. UU.); irrigación de fondos de saco conjuntival (solución salina balanceada, SSB; Laboratorio PISA, S.A de C.V., Zapopan, Jalisco, México); en este paso es posible visualizar burbujas de aire dentro de cámara anterior (fig. 13), procediendo a hacer una apertura epitelial mediante disección roma de la incisión corneal secundaria con una espátula tipo Slade (AE-2326, Asico, Westmont, IL, EE. UU.) siguiendo el plano de la incisión, inyectando azul tripán (Vision Blue, 0.06% D.O.R.C, Zuidland, Holanda) seguido por viscoelástico (Discovisc, condroitín sulfato 4%, hialuronato de sodio 1.65%, Alcon; Arlington, Texas, EE. UU.) hasta presurizar cámara anterior; se procede a realizar la apertura de la incisión corneal primaria con la misma técnica, y posteriormente se verifica que haya logrado una separación completa de los 360°, continuando con el retiro de la cápsula anterior asistido con utrata con técnica en servilleta9 (capsulotomía flotante) (fig. 14); en caso de no lograr una capsulotomía completa, se termina con una técnica capsulorrexis convencional10.
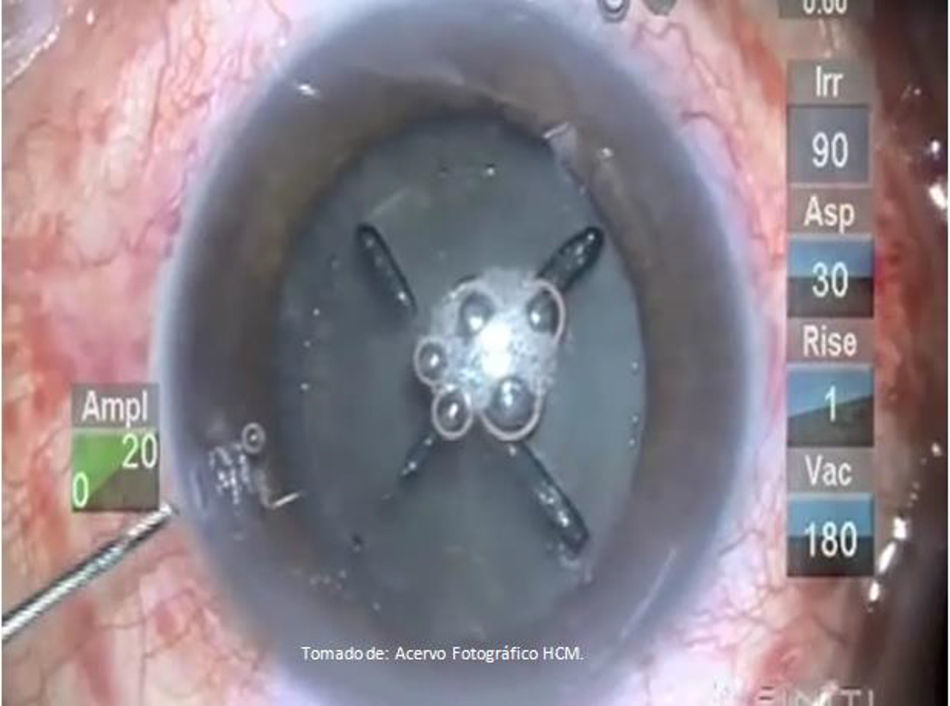
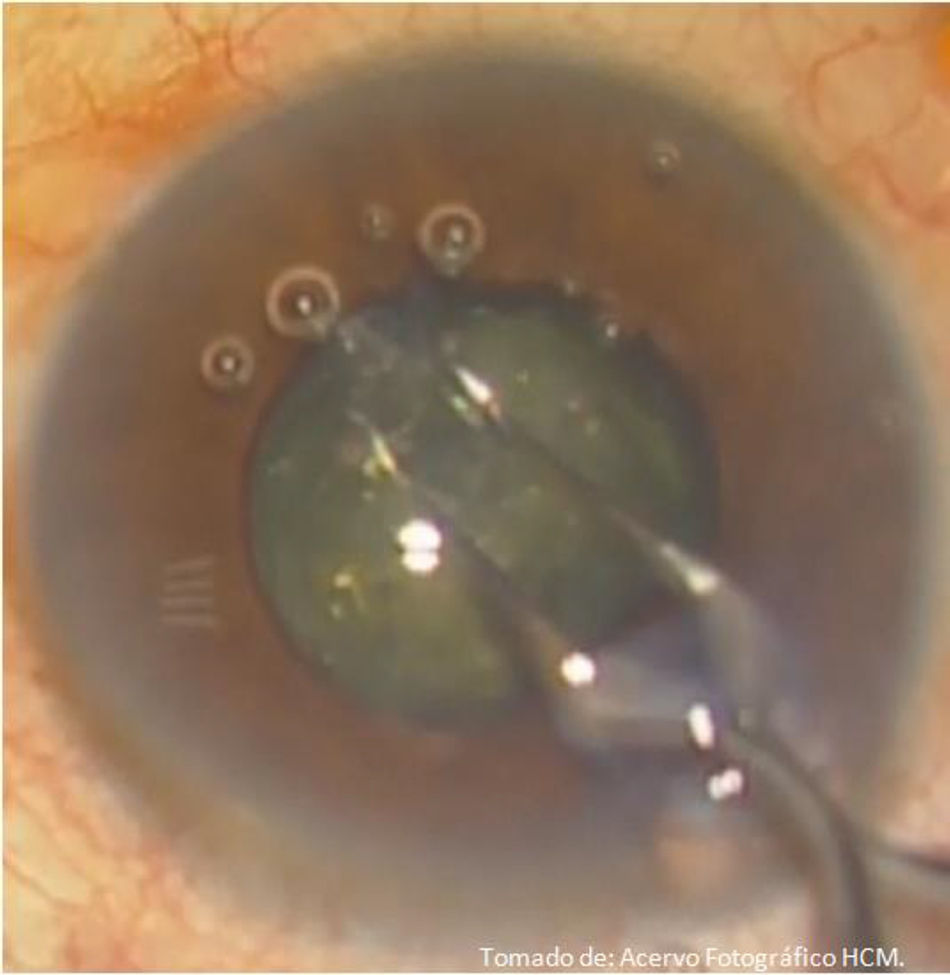
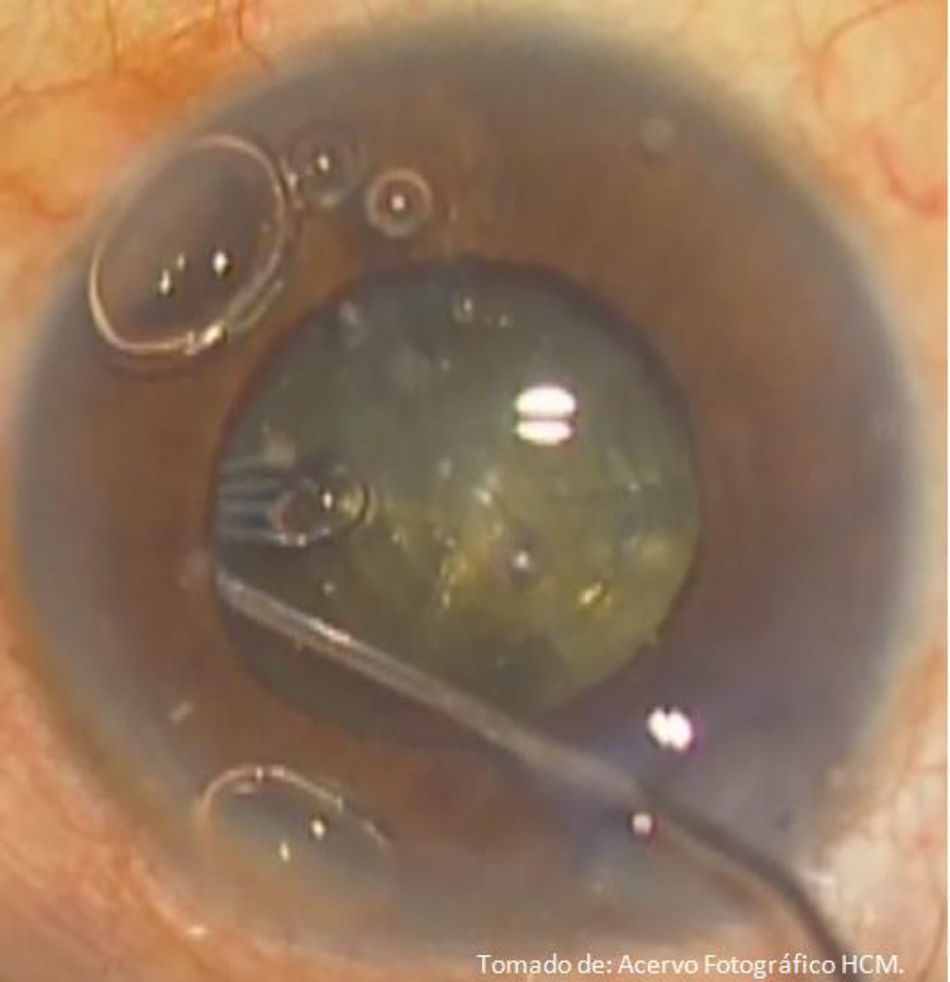
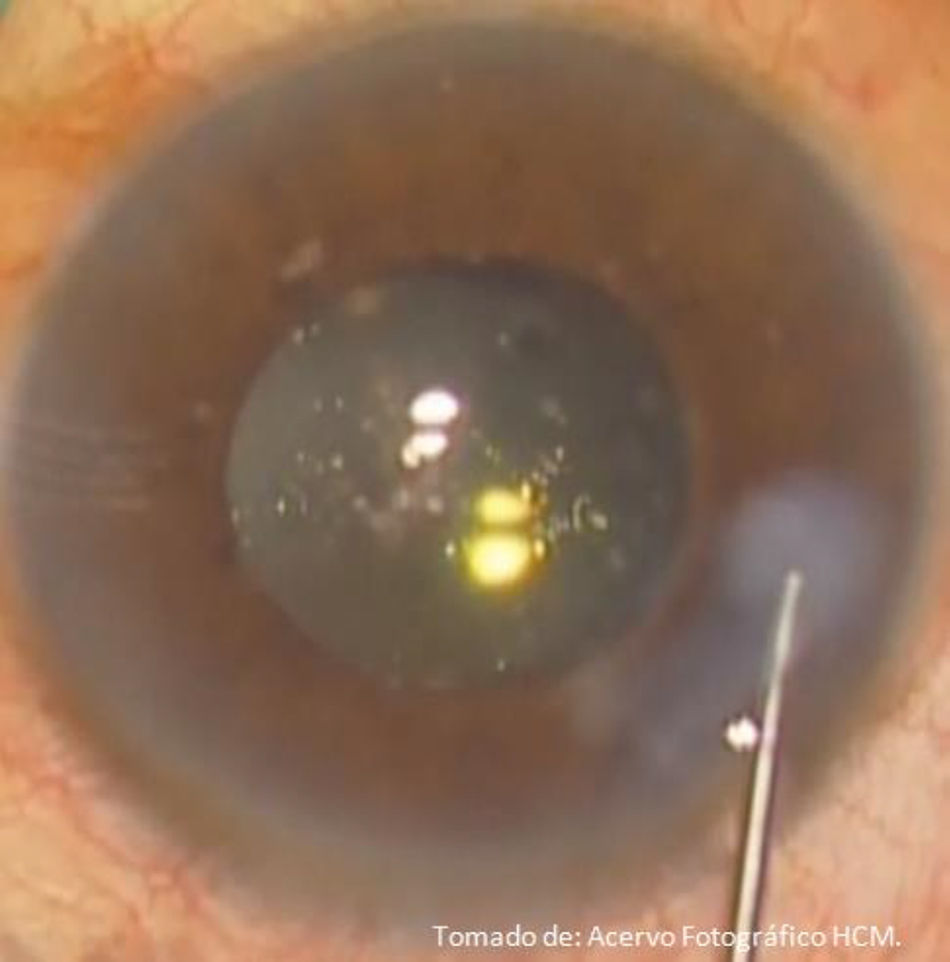
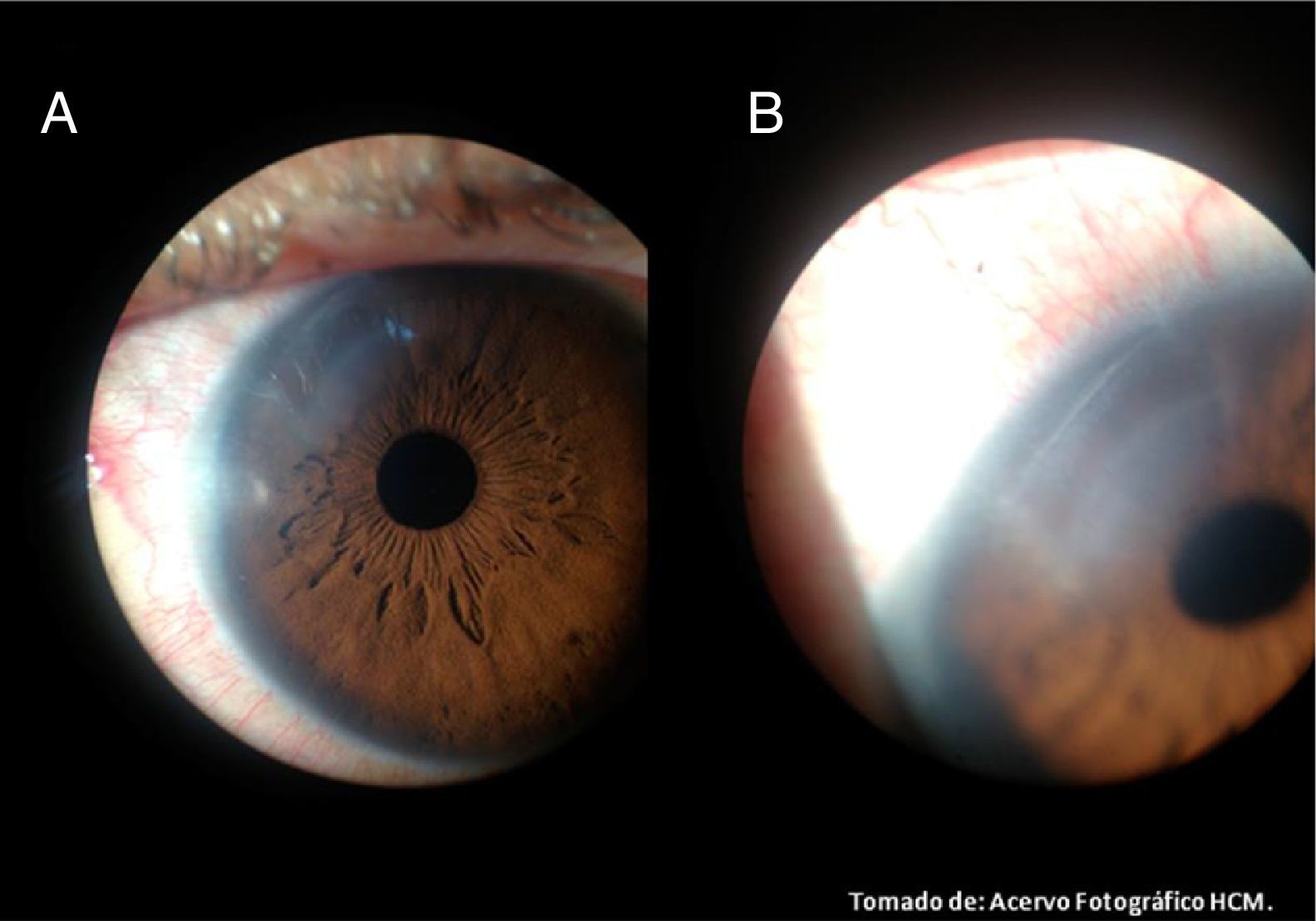
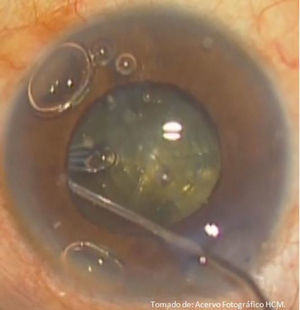
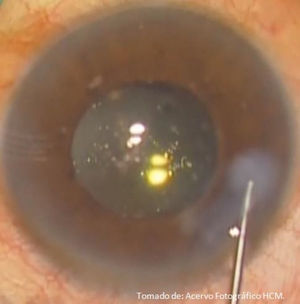
A diferencia de la facoemulsificación convencional, en la femtofaco se recomienda realizar separación de los fragmentos cristalinianos previa a la hidrodisección, con el objetivo de liberar la tensión generada por la presencia de burbujas de CO2 a nivel de cápsula posterior, evitando así un bloqueo capsular y rotura capsular. Se realiza la segmentación del cristalino, completándose según preferencia del cirujano, guiados a través de las marcas generadas por los chops (ya que siempre existen adherencias residuales del tejido cristaliniano), recomendando hacerla con prechopper (Akahoshi Nucleus Splitter AE-4289 femtosecond chopper, Asico, Westmont, IL, EE. UU.)11; se liberan las burbujas por cavitación formadas por el láser, aspirándolas mediante cánula de 27Ga (fig. 15), continuando con la hidrodisección de forma convencional con SSB y cánula 27Ga conectada a una jeringa de 1ml (fig. 16); se continúa con la extracción de los fragmentos cristalinianos mediante facoemulsificación (Centurion® Vision System, ALCON, Arlington, Texas, EE. UU.), utilizando una técnica de «cuchareo» (descrita por la Dra. Martha Verónica Nieto Aguilar; Hospital Central Militar, datos no publicados), por la cual con la punta de la pieza de mano de facoemulsificación se deprime uno de los cuadrantes, y con el segundo instrumento se levanta el cuadrante cristaliniano adyacente para ser emulsificado; se sigue con la aspiración de restos corticales, y pulido de cápsula posterior en caso necesario; se realiza implante de lente intraocular plegable indicado para el paciente por técnica de inyección, continuando con la aspiración de viscoelástico y centrado de lente intraocular, se procede a hidratar las incisiones corneales con SSB, verificando que estén herméticamente selladas (fig. 17); se instila colirio de antibiótico/esteroide (Sophixin Dx Ofteno, fosfato de dexametasona/clorhidrato de ciprofloxacino, Laboratorios Sophia S.A. de C.V.), y parche oclusor al terminar procedimiento. El manejo estándar postoperatorio utilizado es colirio de antibiótico/esteroide cada 4horas la primera semana, reduciendo la dosis en los días subsecuentes (fig. 18).
La cirugía de catarata asistida con láser de femtosegundo ha demostrado ser una técnica eficaz, reproducible y segura, si se realiza una adecuada selección del paciente; sin aumentar el riesgo de complicaciones ni la dificultad técnica para el cirujano. Dentro de la experiencia en el Hospital Central Militar a lo largo de 2 años, se han establecido diferencias en la técnica estándar de femtofaco, como son los límites para la fractura del cristalino (profundidad y longitud de chops), corte epitelial por arriba del plano corneal para lograr mayor porcentaje de apertura de incisión principal, la modificación en la secuencia de fractura e hidrodisección para evitar un bloqueo capsular por las burbujas de aire almacenadas en cápsula posterior, y el abordaje del núcleo mediante técnica de «cuchareo», considerando estas variables como fundamentales para optimizar los resultados de la técnica y acortar la curva de aprendizaje que esta puede representar. Si bien esta técnica permite personalizar las características de cada paso, se pretende aportar los parámetros iniciales y pautas, para que cualquier oftalmólogo que empiece con esta técnica pueda realizarla con mayor seguridad, obteniendo resultados reproducibles. Una de las limitantes de este trabajo es la característica subjetiva de los parámetros empleados, los cuales si bien no pueden ser completamente generalizados, sirven como base para la mayoría de los casos.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
FinanciamientoLos autores no recibieron patrocinio para llevar a cabo este artículo.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Ing. Ricardo Rodríguez González.