La terapia de bloqueo androgénico (BA) ha sido considerada el tratamiento de elección para cáncer de próstata. Por razones desconocidas, con un promedio 24 meses, el tumor se caracteriza por el crecimiento independiente de andrógenos. Por lo anterior, se ha propuesto que el BA intermitente podría impedir la progresión del tumor hacia la insensibilidad a los andrógenos.
ObjetivoBuscar la asociación del BA intermitente con la disminución de resistencia a la castración.
Material y métodosEstudio analítico, retrospectivo, de casos y controles. Se analizaron 91 pacientes con diagnóstico de cáncer de próstata tratados sólo con BA desde un inicio, se dividieron en 2 grupos: uno conformado por 39 pacientes, el cual se manejó con BA intermitente; y el otro, conformado por 52 pacientes bajo manejo con BA continuo. Se determinó razón de Momios (RM), con valor significativo establecido a p<0.05.
ResultadosSe evidenció una disminución del riesgo de desarrollar resistencia a la castración en el grupo con BA intermitente (RM=0.31; intervalo de confianza, IC 95 %=0.038-2.5) pero con p=0.25, lo cual no es estadísticamente significativo.
DiscusiónEl análisis de asociación de riesgos sugiere una tendencia, aunque no significativa, a una menor probabilidad de desarrollar resistencia a la castración, así como de un desenlace fatal, cuando se utiliza BA intermitente.
ConclusiónEl BA intermitente no mostró disminuir significativamente el riesgo de resistencia a la castración.
Androgen deprivation therapy (ADT) has been considered the treatment of choice for prostate cancer. For reasons still unknown, on an average of 24 months, this tumor is characterized by androgen-independent growth. It has therefore been proposed that intermittent androgen deprivation (IAD) could stop the tumor from progressing to androgen insensitivity.
AimsThe aim of the present study was to look for the association between IAD and a decrease in castration-resistant disease.
Material and methodsA retrospective, analytic, case-control study was conducted. Ninety-one patients diagnosed with prostate cancer and treated exclusively with ADT from the onset were analyzed. They were divided into 2 groups. Group 1 was made up of 39 patients managed with IAD. Group 2 consisted of 52 patients managed with continuous androgen deprivation (CAD). Odds ratio (OR) was determined and statistical significance was set at a p<0.05.
ResultsThere was a reduced risk for developing castration-resistant disease in the IAD group (OR=0.31, 95 %CI=.038-2.5), but with a p=0.25, which was not statistically significant.
DiscussionWhen IAD was used, the risk association analysis suggested a tendency, although not statistically significant, toward a lower probability of both developing castration-resistant disease and having a fatal outcome.
ConclusionsIAD did not significantly reduce the risk for castration-resistant disease.
Históricamente, la terapia de bloqueo androgénico (BA) ha sido considerada el tratamiento de elección para cáncer de próstata avanzado o metastásico, sin embargo existen otros numerosos escenarios en los cuales el BA es utilizado1.
Actualmente, el BA como terapia única para cáncer de próstata localizado ha ganado popularidad2,3. Smith resalta en una reciente publicación, que de 2 millones de hombres diagnosticados con cáncer de próstata en Estados Unidos, aproximadamente 600,000 (30 %) reciben BA4.
Más allá de los efectos en la calidad de vida, la supresión de producción de testosterona ha sido asociada con varios y severos efectos adversos, tales como el síndrome de derivación androgénica5, con manifestaciones como pérdida del libido, disfunción eréctil, fatiga, osteoporosis, bochornos, resistencia a la insulina, eventos cerebrovasculares, dislipidemia y síndrome metabólico6-12.
Más importante, por razones desconocidas, el proceso de la muerte celular inducida por la ablación de andrógenos falla para eliminar toda la población de células malignas, y después de un periodo variable, con un promedio de 24 meses, el tumor inevitablemente se repite, caracterizándose por el crecimiento independiente de andrógenos13. Por lo anterior, se ha propuesto que el BA intermitente (BAI) podría impedir la progresión del tumor hacia la insensibilidad a los andrógenos14.
El BAI no conlleva a un mayor riesgo de muerte que el BA continuo (BAC), éste debe ser considerado como la terapia estándar para el cáncer de próstata. Sin embargo, los pacientes con enfermedad avanzada, Gleason alto, antígeno prostático específico (APE) pretratamiento aumentado, no muestran adecuada respuesta bioquímica del APE a la terapia de deprivación de andrógenos, y no deberían ser candidatos para el BAI15.
La literatura médica más reciente refiere que el uso temprano de BA, reduce en 30 % el riesgo de metástasis a 10 años, pero no la resistencia a la castración ni la muerte por cáncer, en comparación con la deprivación androgénica diferida16. El objetivo del presente estudio es asociar el BAI con la disminución de la resistencia a la castración, en pacientes con cáncer de próstata.
Material y métodosSe realizó un estudio trasversal, analítico. El estudio se llevó a cabo en el Hospital Regional “Lic. Adolfo Lopez Mateos” del ISSSTE. Se revisaron los expedientes de 134 pacientes desde los años 2005 a 2012, diagnosticados con cáncer de próstata localizado o localmente avanzado, que hayan recibido BA por cualquier motivo. Se obtuvieron 91 pacientes con expediente clínico completo. Los criterios de inclusión fueron pacientes con diagnóstico de adenocarcinoma de próstata detectado mediante biopsia transrectal de próstata (BTRP), cualquier Gleason, estadio clínico T1-4 N0-1 M 0, indistinto valor de APE. Se excluyeron aquellos con expediente incompleto o radioterapia previa.
Todos los pacientes fueron tratados con BA desde un inicio con análogo de la hormona liberadora de la hormona luteinizante (LHRH) trimestral y bicalutamida 50 mg al día los primeros 15 días, una vez que el APE llegó al nadir en cada sujeto. Para su análisis, se dividieron en 2 grupos aquellos con adecuada respuesta al tratamiento inicial. El grupo 1 se conformó por 39 (42.8 %) pacientes manejados con BAI, suspensión transitoria de éste cuando se llegó al nadir del APE y se reinició nuevamente BA cuando se elevó el APE hasta 4ng/mL. El grupo 2 se conformó por 52 (57.1 %) pa - cientes manejados con BAC.
Los pacientes se siguieron cada 12 semanas, los criterios utilizados para definir resistencia a la castración son las recomendaciones de las Guías Europeas de Urología 2013. Los pacientes que presentaron resistencia a la castración fueron enviados a quimioterapia. Se utilizó t de Student para las variables paramétricas, el nivel de significancia se fijó en p<0.05, se utilizó razón de Momios (RM) y se usó el programa estadístico SPSS® versión 19.
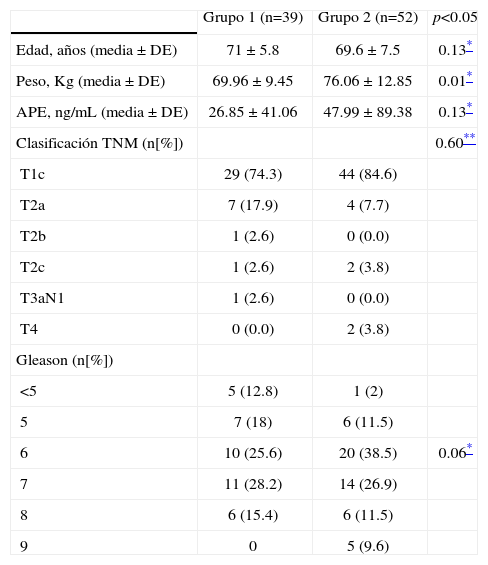
ResultadosSe incluyeron a 91 pacientes los cuales se dividieron en 2 grupos, cuyas características basales se muestran en la tabla 1.
Características demográficas de los grupos.
| Grupo 1 (n=39) | Grupo 2 (n=52) | p<0.05 | |
| Edad, años (media±DE) | 71±5.8 | 69.6±7.5 | 0.13* |
| Peso, Kg (media±DE) | 69.96±9.45 | 76.06±12.85 | 0.01* |
| APE, ng/mL (media±DE) | 26.85±41.06 | 47.99±89.38 | 0.13* |
| Clasificación TNM (n[%]) | 0.60** | ||
| T1c | 29 (74.3) | 44 (84.6) | |
| T2a | 7 (17.9) | 4 (7.7) | |
| T2b | 1 (2.6) | 0 (0.0) | |
| T2c | 1 (2.6) | 2 (3.8) | |
| T3aN1 | 1 (2.6) | 0 (0.0) | |
| T4 | 0 (0.0) | 2 (3.8) | |
| Gleason (n[%]) | |||
| <5 | 5 (12.8) | 1 (2) | |
| 5 | 7 (18) | 6 (11.5) | |
| 6 | 10 (25.6) | 20 (38.5) | 0.06* |
| 7 | 11 (28.2) | 14 (26.9) | |
| 8 | 6 (15.4) | 6 (11.5) | |
| 9 | 0 | 5 (9.6) |
DE: desviación estándar; APE: antígeno prostático específico.
Se utilizaron distintas pruebas de acuerdo a las características de la variable:
La media de seguimiento para el grupo BAI y BAC fue de 49.6 meses (rango 8-156) y 45.29 meses (6-192), respectivamente, con una p=0.60.
La resistencia a la castración se documentó en un caso del grupo de BAI a los 18 meses, mientras que en 4 pacientes del grupo de BAC se presentó en promedio a los 10.5 meses. La RM de resistencia a la castración fue de 0.31, el intervalo de confianza (IC) 95 %=0.038-2.5, con una p=0.25. Se registraron 3 muertes en el estudio, un paciente del grupo de BAI y 2 pacientes del grupo de BAC, estos 2 últimos fueron por causa directa del cáncer (RM=0.67; IC 95 %=0.05- 7.67; p=0.61).
DiscusiónEl análisis de asociación de riesgos sugiere una tendencia, aunque no significativa, a una menor probabilidad de desarrollar resistencia a la castración, así como de un desenlace fatal cuando se utiliza BAI.
La falta de significancia estadística muy probablemente se debe a que la muestra es pequeña y dado que es un estudio descriptivo, los resultados deben tomarse con precaución.
No proponemos que el BAI sea superior al BAC, sino que ambos tratamientos son iguales de seguros y eficaces en el tratamiento del cáncer de próstata localizado y localmente avanzado; con la reducción de costos y efectos secundarios ocasionados por el BAC.
Es interesante que en nuestra población el periodo de inicio de tratamiento con BA hasta que se presenta resistencia a la castración es superior a lo que marca la literatura médica, la cual refiere, es en promedio de 24 meses, ya que la mayoría de los pacientes en nuestro estudio llevan una media de 46.28 meses de tratamiento y no han presentado resistencia a la castración.
ConclusiónEl BAI no mostró disminuir significativamente el riesgo de resistencia a la castración.
Conflicto de interesesLos autores declaran no tener ningún confl icto de intereses.
Financiamiento