La nefrectomía parcial es recomendada por la Sociedad Europea de Urología y la Asociación Americana de Urología, para el manejo de masas renales sólidas, estadificadas como T1a y casos seleccionados T1b.
El objetivo es demostrar la reproducibilidad de la técnica laparoscópica en la nefrectomía parcial.
Presentamos el caso clínico de una paciente femenina de 50 años, sin antecedentes de importancia, se le diagnosticó tumoración de 3 x 3 cm dependiente del riñón izquierdo. Se le realizó gamagrama renal, con una TFG global de 112 mL/min, riñón izquierdo 44%.
Tiempo quirúrgico 130 minutos, tiempo de isquemia caliente 24 minutos, sangrado 140 cc, tiempo de estancia hospitalaria 3 días, reporte histopatológico final, tumor de 3.8 cm, bordes quirúrgicos negativos, carcinoma de células renales (CCR) claras Fuhrman 2. Creatinina sérica preoperatorio 0.8, creatinina postoperatoria 1.1. Gamagrama renal a las 12 semanas con TFG 95 mL/min, riñón izquierdo 40%.
La nefrectomía parcial es actualmente el tratamiento de elección para masas renales órganoconfinadas.
La nefrectomía parcial vía laparoscópica es un procedimiento reproducible, seguro y efectivo.
Partial nephrectomy is recommended by the European Association of Urology and the American Urological Association for managing solid renal masses staged as T1a and for selected T1b cases.
The aim of this article was to demonstrate the reproducibility of the laparoscopic technique in partial nephrectomy.
We present the clinical case of a 50-year-old woman, with an unremarkable past medical history that was diagnosed with a 3 x 3 cm tumor dependent on the left kidney. A kidney scintigram was done that showed an overall glomerular filtration rate (GFR) of 112 mL /min, left kidney 44%. Surgery duration was 130 minutes, warm ischemia time was 24 minutes, there was blood loss of 140 cc, and hospital stay was 3 days. The final histopathologic study reported a 3.8 cm tumor with negative surgical margins, identifying Fuhrman 2 clear cell renal cell carcinoma (CCRCC). Preoperative creatinine was 0.8 and postoperative creatinine was 1.1. At 12 weeks, a kidney scintigram showed a GFR of 95 mL/min, left kidney 40%.
Partial nephrectomy is currently the treatment of choice for organ-confined renal masses. Laparoscopic partial nephrectomy is a safe, effective, and reproducible procedure.
Introducción
La nefrectomía parcial es recomendada por la Sociedad Europea de Urología para el manejo de las masas renales sólidas T1a y T1b. Las indicaciones absolutas incluyen casos de pacientes monorrenos o con tumores renales bilaterales. Indicaciones relativas incluyen función disminuida secundaria a alguna enfermedad o bien, que en el futuro pudiera disminuir la función renal, ejemplo de estas enfermedades son: enfermedad renovascular, diabetes, hipertensión, así como tipos hereditarios de carcinoma de células renales (CCR)1,2. La nefrectomía parcial laparoscópica (NPL) permanece como un método bajo evaluación, el cual puede ser establecido como una alternativa a la nefrectomía parcial abierta3,4. Apropiada escisión tumoral requiere un claro margen quirúrgico de 1 cm, aproximadamente. La NPL es un procedimiento cambiante dependiente de adelantos en tecnología en sistemas de visión, métodos de imagenología y agentes hemostáticos4-10. Contraindicaciones relativas son: intolerancia al pneumoperitoneo, tumores hiliares. La NPL incluye una adecuada hemostasia renal posterior a la escisión del tumor y a la reconstrucción pielocalicial, todo esto limitado en tiempo por la isquemia caliente1-3,11-15. Actualmente, se acepta que este no debe ser mayor a 30 minutos, aunque en estudios recientes se han propuesto 20 minutos como tiempo máximo de isquemia caliente5,16.
Presentación del caso
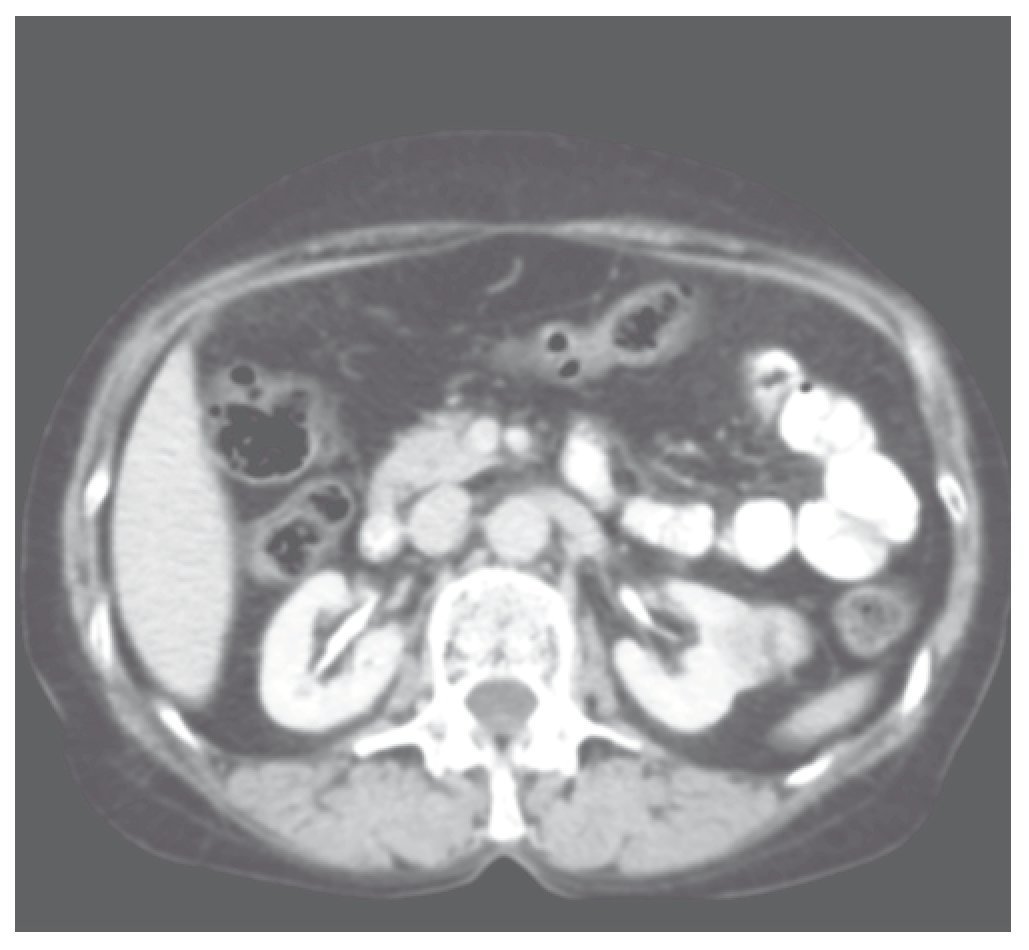
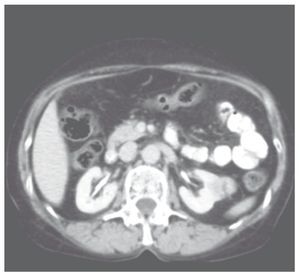
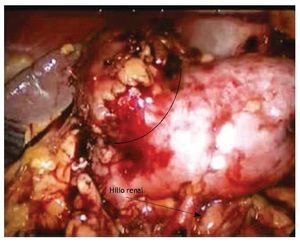
Paciente femenino de 50 años de edad, sin antecedentes de importancia, sometida a protocolo de estudio por hematuria microscópica diagnosticándose en ecografía de abdomen superior, tumoración hiperecoica de 3 x 3 cm dependiente de parénquima renal izquierdo, por lo que se solicitó urotomografía (UroTAC) donde se confirmó el diagnóstico de tumor sólido de 3.4 cm, dependiente de riñón izquierdo (fig. 1). Se realizó gamagrama renal, con una TFG global de 112 mL/ min, riñón izquierdo 44%. Previa anestesia general y colocación de sonda Foley, se situó a la paciente en decúbito lateral izquierdo, con aguja de Veress se realizó pneumoinsuflación a 15 mmHg y flujo de 5 L/min. Se colocó un trocar de 10 mm para la visión paraumbilical, uno más para rectal cefálico al primero de 10 mm y, 2 más en línea axilar media y posterior de 5 mm. Posterior a laparoscopía exploratoria, se realizó movilización medial del colon hasta exponer la fascia de Gerota, misma que se abrió, localizándose el tumor (fig. 2); se procedió a identificar los vasos del hilio renal así como el uréter. Se localizaron 2 arterias y una vena renal, se le administraron líquidos intravenosos a la paciente, así como manitol previo al camplaje de las arterias renales.
Figura 1 Tomografía abdomino-pélvica contrastada, donde se muestra lesión sólida heterogénea mesofítica dependiente de riñón izquierdo, de aproximadamente 3.4 cm.
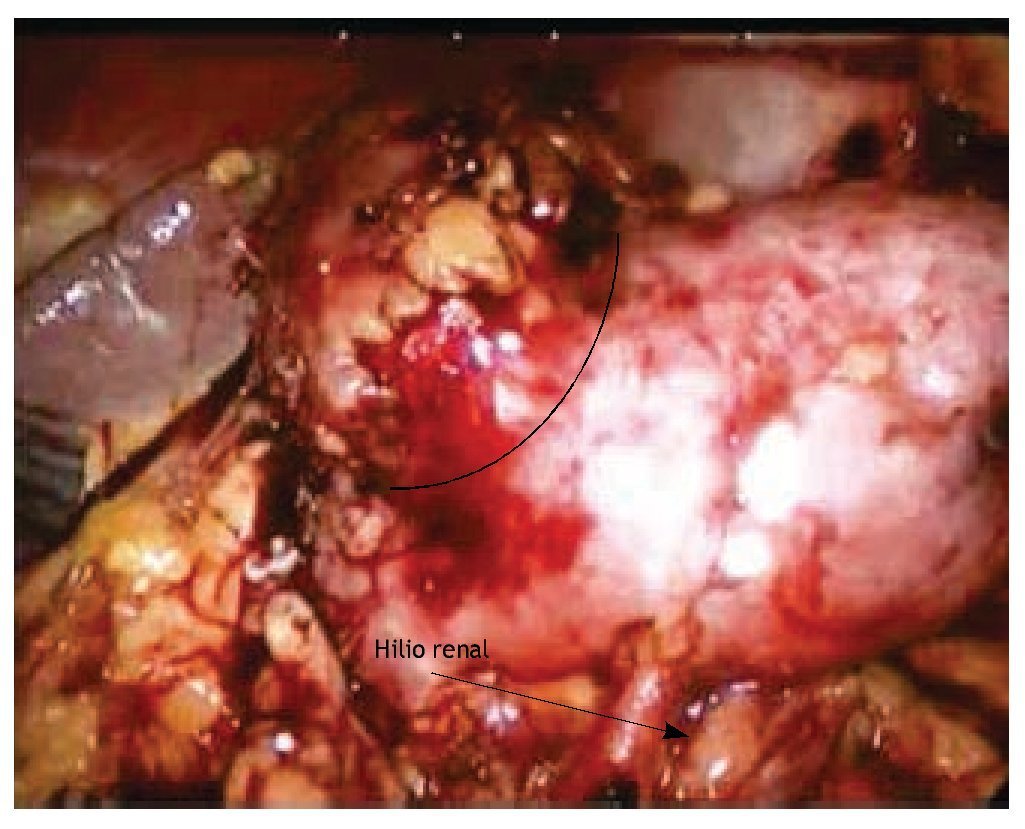
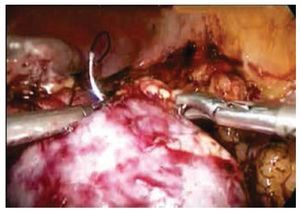
Figura 2 Visión laparoscópica de tumoración renal dependiente de polo superior izquierdo.
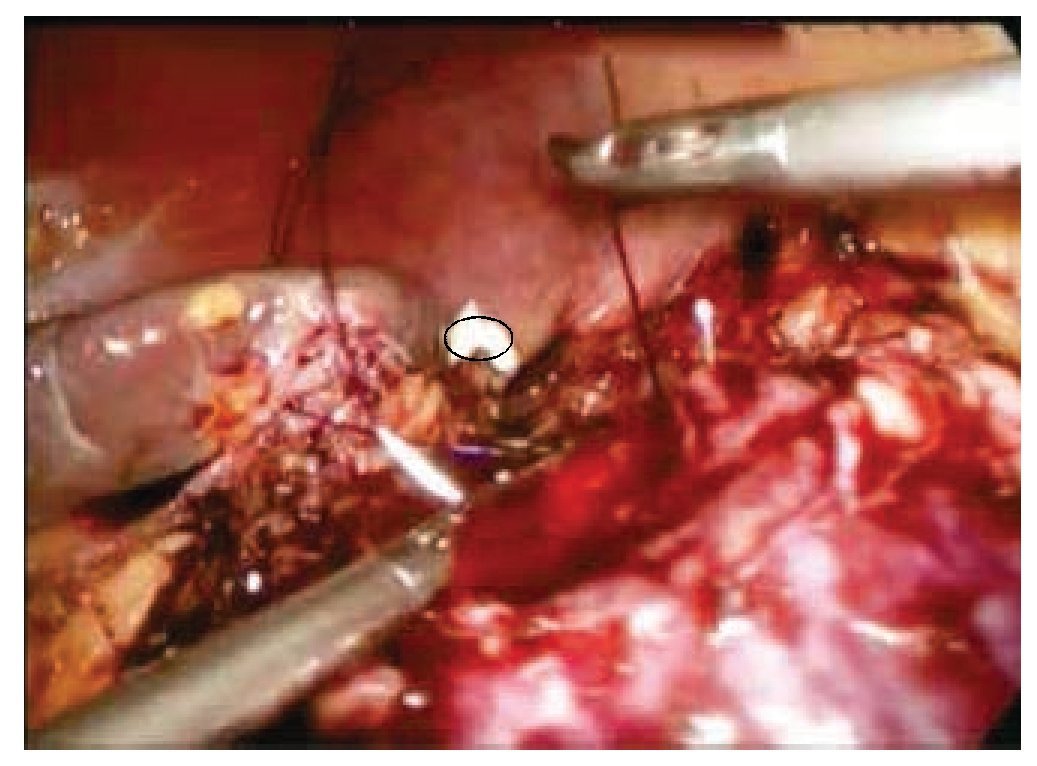
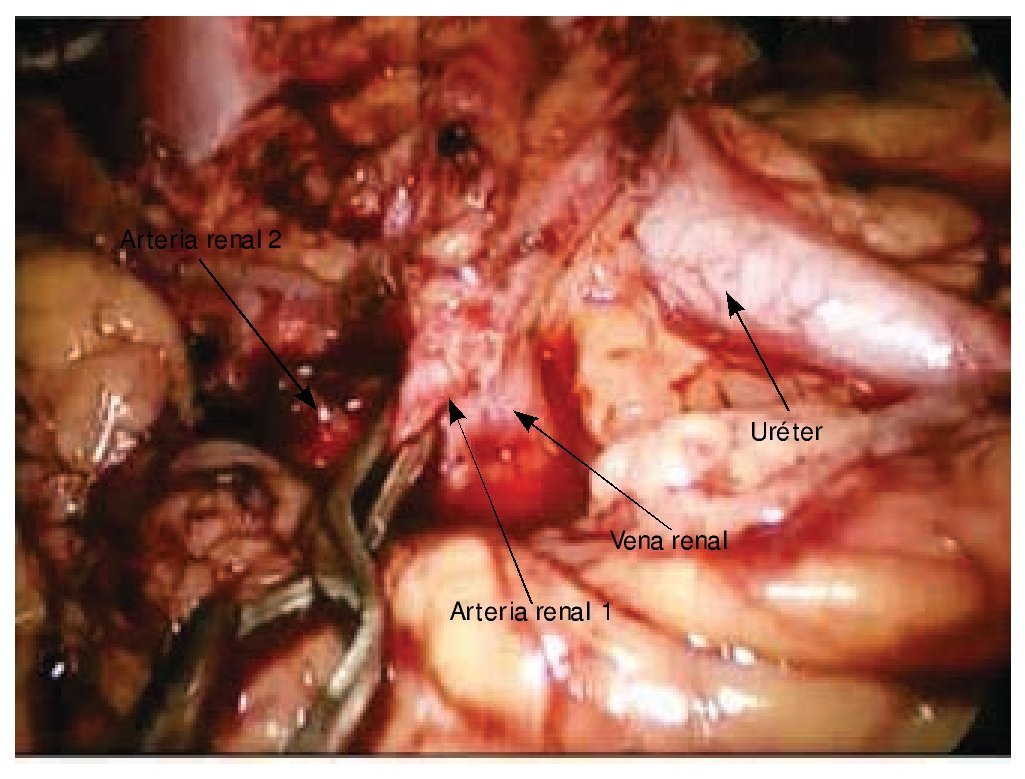
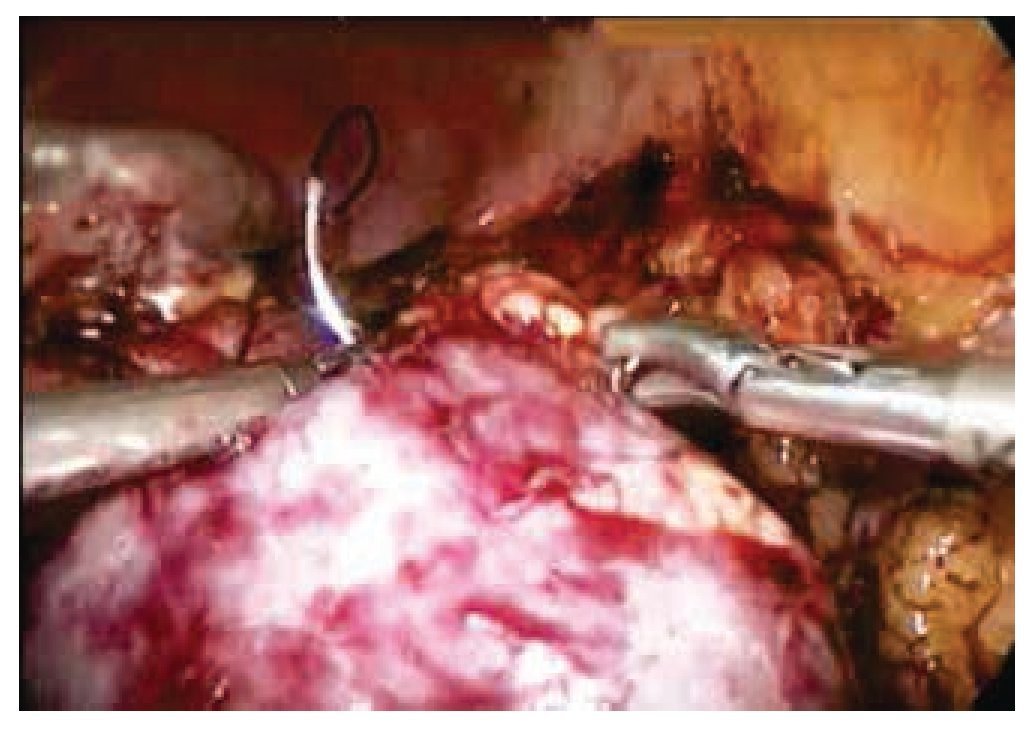
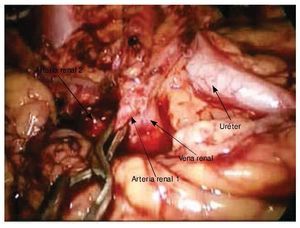
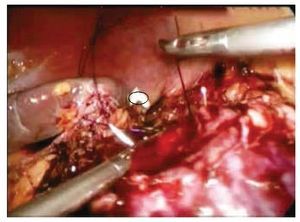
Se procedió a colocar bulldog2 a las arterias, iniciando el tiempo de isquemia caliente (fig. 3). Se realizó tumorectomía, seguida de reparación pielocalicial con MonocrylTM 2/0 (fig. 4); puntos totales separados con misma sutura (fig. 5), se deja Gelfoam®, se retiraron clamps sin observar sangrado, se colocó drenaje tipo Penrose. Se extrajo la pieza quirúrgica.
Figura 3 Visión laparoscópica de hilio renal, presencia de estructuras, vasculares y uréter, momento de camplaje de una de las arterias renales.
Figura 4 Posterior a la tumorectomía, se realiza calicorrafía y hemostasia del lecho quirúrgico con MonocrylTM 2-0 sutura continua. Obsérvese en el círculo la presencia de rollo de Gelfoam®, para la nefrorrafia; éste así como las suturas son introducidas en la cavidad abdominal previo al camplaje arterial.
Figura 5 Nefrorrafia con MonocrylTM 2-0 puntos separados anclados con Hem-o-lockTM.
El tiempo quirúrgico fue de 130 minutos, tiempo de isquemia caliente 24 minutos, sangrado 140 cc, tiempo de estancia hospitalaria 3 días, reporte histopatológico final, tumor de 3.8 cm, CCR claras Fuhrman 2, bordes quirúrgicos negativos, creatinina preoperatoria 0.8 mg/dL, creatinina sérica postoperatoria 1.1 mg/dL. Gamagrama renal a las 12 semanas con TFG 97 mL/min, riñón izquierdo 40%.
La paciente fue dada de alta al tercer día de postoperatorio. En la vigilancia de 3, 6 y 9 meses, el control oncológico y funcional fue satisfactorio.
Discusión
El control hiliar es un paso importante en la NPL, este no debe ser mayor a 30 minutos; nosotros no contamos con angiotomografía (angioTAC) en nuestra Institución, pero es importante conocer la disposición de la o las arterias renales. Para la enucleación del tumor, nosotros preferimos la escisión con un margen de 1 cm de seguridad, lo anterior en la primicia de no tener márgenes positivos1. La nefrorrafia la realizamos con MonocrylTM 2-0 sutura continua. Posteriormente, 2 o 3 puntos separados del mismo MonocrylTM 2-0 anclado con Hem-o-lock®. Para tratar de disminuir el tiempo de isquemia caliente, preparamos todo el material para el clampaje y nefrorrafia dentro de la cavidad abdominal. Posterior a la nefrorrafia desclampamos, disminuimos la pneumoinsuflación y observamos si existe algún sangrado, colocando satín o Gelfoam® hemostático sobre el lecho quirúrgico. Entre los avances recientes, Gill et al.16 presentó una técnica de "isquemia zero" para NPL y asistida con robot. Esta técnica permite la disección del tumor sin control hiliar a través de la reducción farmacológica de la presión arterial, siendo estrechamente monitorizada. Eisenberg et al. reportó 15 pacientes con comorbilidades y tumores complejos. El tiempo quirúrgico promedio fue de 3 horas (rango 1-6) y una media de sangrado transoperatorio de 150 mL (rango 20 a 400 mL). Complicaciones transoperatorias no hubo; complicación postoperatoria fueron fístula urinaria, corregida conservadoramente. La inducción de la hipotermia ha sido propuesta como un método para reducir las consecuencias de la isquemia renal, se han ideado métodos desde la aplicación laparoscópica de hielo frappé, hasta la infusión de soluciones frías a través del uréter o incluso la arteria renal10-15. El campo quirúrgico exangüe es imprescindible para una adecuada exéresis tumoral. El uso de una coagulación por radiofrecuencia, resulta en una coagulación esférica que incluye un margen alrededor de la lesión de 1 cm. Esta área posteriormente puede ser resecada con corte en frío, aunque este procedimiento se ha relacionado a daño al sistema colector y/o vascular. De los agentes hemostáticos, el Floseal® ha sido asociado con un decremento significativo en las complicaciones hemorrágicas. Por lo que, el uso de este agente ha sido adoptado por la mayoría de los centros que realizan nefrectomía parcial1-6.
Conclusiones
La nefrectomía parcial es actualmente el tratamiento de elección para masas renales órgano-confinadas, que anatómicamente pueden ser sometidas a tratamientos órganospreservadores. En la última década, los beneficios de la nefrectomía parcial comparada a la nefrectomía radical, y la correlación entre la enfermedad renal crónica y el riesgo de eventos cardiovasculares y muerte, han sido bien establecidos.
Conflicto de intereses
Los autores declaran no tener ningún conflicto de intereses.
Financiamiento
No se recibió patrocinio para llevar a cabo este artículo.
* Autor para correspondencia:
Arístides N° 640, Colonia Cumbres Tercer Sector,
Monterrey, N.L., México.
Teléfono: (81) 8300 3922.
Correo electrónico: contacto@drantoniozapata.com (J. A. Zapata-González).