El manejo del cáncer de próstata metastásico resistente a la castración ha variado notablemente en la última década con grandes cambios en el paradigma de tratamiento, aunque, en última instancia, la enfermedad seguirá progresando a pesar de los tratamientos disponibles en la actualidad.
Caso clínicoMasculino de 72 años con diagnóstico de cáncer de próstata resistente a castración, con gammagrama óseo que evidencia lesiones óseas metastásicas, tratado con abiraterona, con respuesta clínica y bioquímica, el cual en su seguimiento muestra regresión de metástasis óseas documentadas en la gammagrafía ósea.
ConclusionesEl presente caso clínico muestra la particularidad de regresión aparente de lesiones óseas en el contexto de cáncer de próstata metastásico en resistencia a castración, tras el inicio del fármaco acetato de abiraterona, mostrando asimismo respuesta bioquímica y clínica sostenida tras el mantenimiento del fármaco.
There have been significant modifications in metastatic castration-resistant prostate cancer management in the last decade, with great changes in the treatment paradigm, even though the disease will ultimately continue to progress despite the currently available treatments.
Case reportA 72-year-old man diagnosed with castration-resistant prostate cancer underwent a bone scintigram that identified metastatic bone lesions. He was treated with abiraterone, with clinical and biochemical response. Follow-up revealed regression of bone metastasis documented in the bone scintigram.
ConclusionsThis clinical case shows the particularity of apparent bone lesion regression in the context of metastatic castration-resistant prostate cancer after treatment with abiraterone acetate that also showed sustained clinical and biochemical response.
El cáncer de próstata (CaP) es la segunda causa de muerte por cáncer en los hombres en el mundo occidental después del cáncer de pulmón1,2. De acuerdo con las estimaciones de la Sociedad Americana del Cáncer en 2013, más de 230,000 hombres estadounidenses serán diagnosticados con CaP y casi 29,720 morirán de la enfermedad2. El CaP progresa desde su diagnóstico hasta la muerte a través de una serie de estados clínicos caracterizados por la extensión de la enfermedad y la presencia o ausencia de metástasis. El manejo del CaP metastásico resistente a la castración ha variado notablemente en la última década con grandes cambios en el paradigma de tratamiento, aunque, en última instancia, la enfermedad seguirá progresando a pesar de los tratamientos disponibles en la actualidad.
El uso de acetato de abiraterona ha demostrado asociarse a un incremento en la supervivencia global y libre de progresión bioquímica en el contexto de enfermedad resistente a castración previo a tratamiento con quimioterapia sistémica.
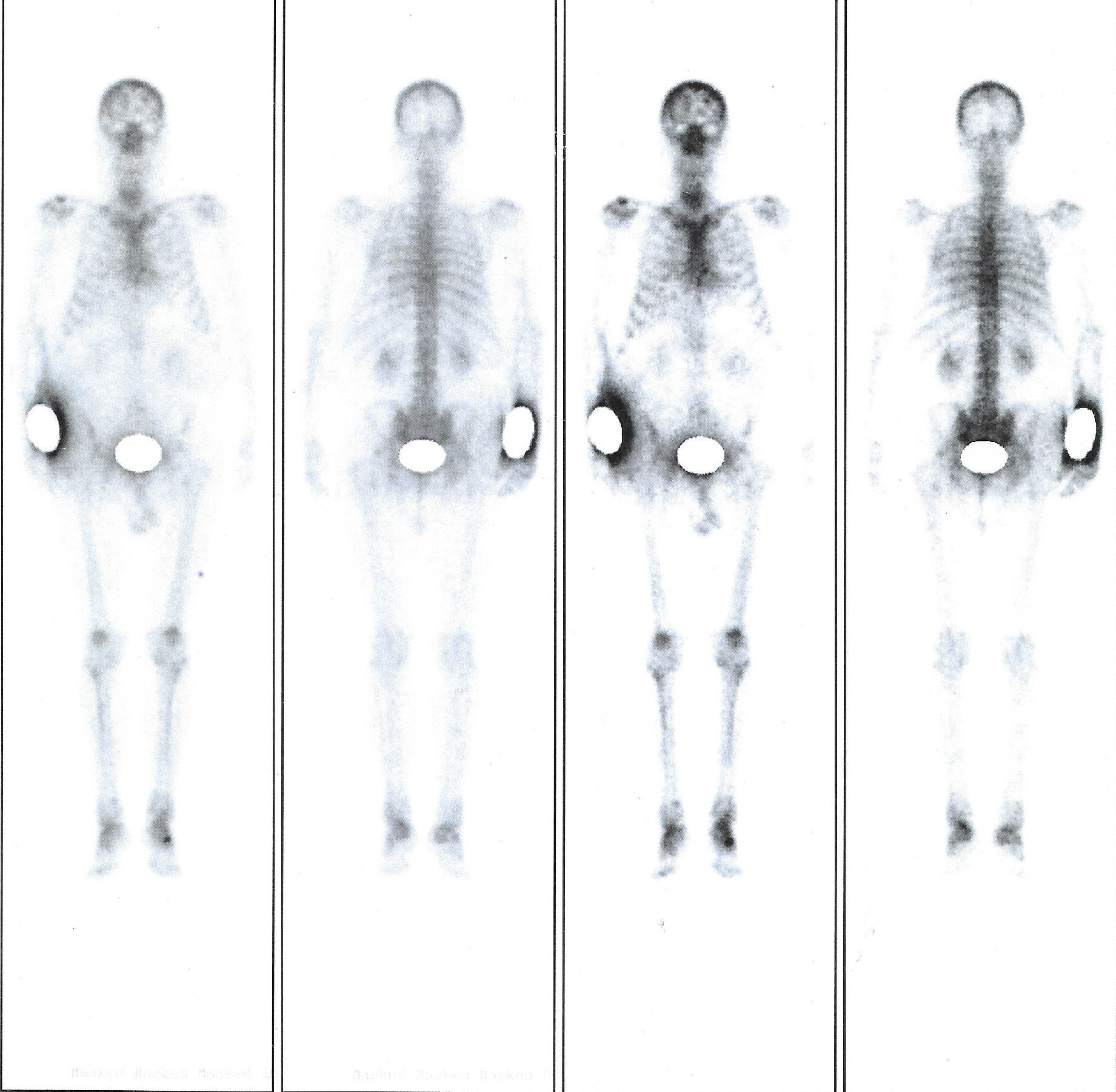
Presentación de casoMasculino de 72 años, sin antecedentes heredofamiliares de CaP, presenta elevación de antígeno prostático (28.5ng/ml) y tacto rectal sospechoso. Se realiza biopsia transrectal de próstata con reporte histopatológico de adenocarcinoma de próstata Gleason 9 (5+4). En estudios de extensión se detecta enfermedad ganglionar metastásica a nivel pélvico además con gammagrama óseo (Metil-difosfonatos, Tecnecio 99 Metaestable), en el cual se observa adecuada captación del radiotrazador por el tejido óseo con zona de incremento del recambio iónico en región frontoparietal izquierda y cabeza de fémur izquierda. (fig. 1). Clínicamente con ECOG (Eastern Cooperative Oncology Group) 0. Se inició manejo con bloqueo androgénico completo. Tras control bioquímico por lapso de 5 años presenta incremento paulatino de antígeno prostático hasta alcanzar determinación de 13.15ng/ml y confirmación con valor de 14.2ng/ml, corroborando asimismo testosterona en rango de castración. Se documenta ausencia de progresión ósea tras nuevo rastreo, no obstante, aparece de dolor óseo (escala visual análoga 3/10).
Se inicia tratamiento con acetato de abiraterona (1,000mg/24h). Presenta respuesta clínica sostenida, con disminución franca en dolor óseo, así como respuesta bioquímica, con nadir de 0.34ng/ml durante el seguimiento. Seis meses después, en el rastreo óseo de control con metil-difosfonato-tecnecio 99 metaestable se observa adecuada concentración del radiofármaco por tejido óseo sin datos francos de enfermedad ósea metástasica (fig. 2). Tomografía axial computarizada sin evidencia de lesiones metastásicas viscerales. El paciente continúa en vigilancia oncológica, clínicamente con ECOG 0.
DiscusiónLa mayoría de los pacientes responden inicialmente a la privación de andrógenos. Desafortunadamente, CaP en última instancia, deja de responder y se repite dentro de 1-3 años después de la privación de andrógenos como cáncer de próstata resistente a la castración3. El estudio COU-AA 302, que agrupó a pacientes con cáncer de próstata resistente a la castración, evaluó como uno de los objetivos primarios de eficacia terapéutica la supervivencia libre de progresión radiológica, definida, en la evaluación del rastreo óseo, como enfermedad progresiva de acuerdo al Prostate Cancer Working Group 2. El beneficio en términos de enfermedad ósea se evidenció de manera consistente, con reducción significativa en el riesgo de progresión radiológica a nivel óseo (16.5 vs. 8.3 meses en el grupo tratado con placebo tras seguimiento a 2 años). La presente revisión muestra un caso con remisión de sintomatología en paciente sometido a régimen con acetato de abiraterona en el contexto previo a recibir quimioterapia citotóxica, además de mostrar aparente remisión de datos imagenológicos compatibles con enfermedad metastásica.
ConclusionesEl diagnóstico oportuno de CaP resistente a castración en enfermedad metástasica con mínimos síntomas y el tratamiento ante este escenario plantean la posibilidad de mejoría de la calidad de vida y supervivencia. El presente caso clínico muestra la particularidad de regresión aparente de lesiones óseas en el contexto de cáncer de próstata metastásico en resistencia a castración, tras el inicio del fármaco acetato de abiraterona, mostrando asimismo respuesta bioquímica y clínica sostenida tras el mantenimiento del fármaco.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
FinanciaciónNo se recibió patrocinio de ningún tipo para llevar a cabo este artículo.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.