La leucemia se encuentra entre los trastornos oncológicos más comunes en la primera década de vida. Ésta se caracteriza por la producción excesiva de células inmaduras linfocíticas no funcionales denominadas blastos que invaden el torrente sanguíneo produciendo consecuencias fatales. Se trata de un padecimiento grave y mortal si no es tratado oportunamente. Entre sus manifestaciones más comunes se encuentran: la palidez generalizada, las linfadenopatías, hemorragias espontáneas, lesiones vasculares como moretones o petequias, malestar general, pérdida de peso y manifestaciones estomatológicas específicas como palidez de mucosa oral, los infiltrados leucocitarios, gingivorragias o aparición de petequias en algunos sitios de la boca. En el presente artículo se informa el caso de una niña de cinco años de edad diagnosticada con leucemia aguda linfoblástica precursora de células B, quien fue sometida a rehabilitación bucal bajo anestesia general, pues presentaba múltiples focos infecciosos en sus dientes que contraindicaban el inicio de su tratamiento de quimioterapia.
Leukemia is one of the most common oncological disorders found in the first decade of life. It is characterized by the excessive production of non-functional immature lymphocytic cells, called blasts, which invade the bloodstream causing fatal consequences. Unless timely treated, it is a deadly, severe condition. Its more common manifestations are the following: generalized paleness, spontaneous hemorrhaging, vascular lesions such as bruises and petechiae, general malaise, weight loss, and specific stomatological manifestations such as oral mucosa paleness, leukocyte infiltrate gingivorrhageor apparition of petechiae in some locations of the mouth. The present article documents the case of a five year old girl, diagnosed with B-cell precursor acute lymphoblastic leukemia. The child was subjected to oral rehabilitation under general anesthesia due to the fact that she exhibited multiple infectious foci in her teeth which contraindicated initiation of chemotherapy treatment.
La leucemia es el trastorno oncológico más común de la infancia caracterizado por una afección de la médula ósea que origina una producción excesiva de células inmaduras denominadas blastos. Las leucemias cuentan con una gran pluralidad de características para poder ser clasificadas con base en el tipo celular que las produce o el grado de maduración de éstas.
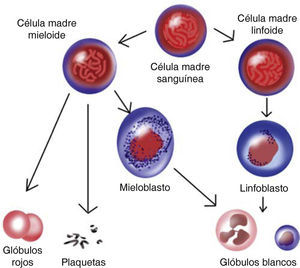
De acuerdo con los estirpes celulares que las producen, las leucemias pueden ser linfoblásticas o mieloblásticas.1
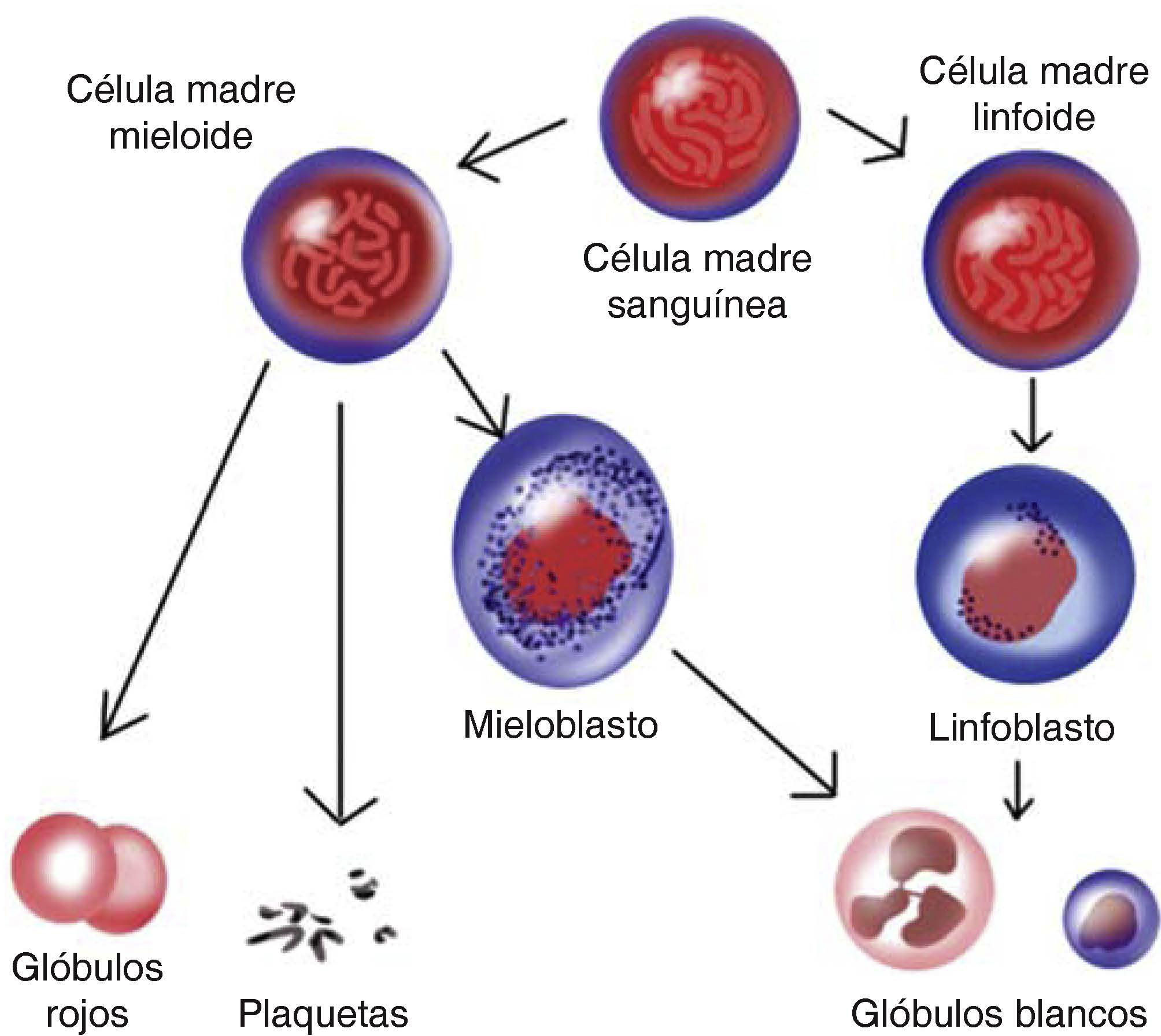
Las leucemias linfoblásticas son aquéllas cuya celularidad deriva del estirpe linfoide, es decir, linfocitos B y T respectivamente. Mientras que las leucemias mieloblásticas derivan de las células del estirpe mieloide como los glóbulos rojos, neutrófilos, basófilos, eosinófilos y plaquetas (Figura 1). Así se diferencian entre agudas y crónicas de acuerdo con la funcionalidad de las células. Las leucemias agudas se caracterizan por tener una población celular no funcional al estar absolutamente inmaduras a diferencia de las leucemias crónicas en donde las células tienen un mayor grado de maduración. A partir de esta premisa podemos inferir que las leucemias agudas generalmente son más agresivas que las crónicas. El origen de este padecimiento se asocia fuertemente a factores genéticos como el síndrome de Down,2 síndrome de Li-fraumeni, síndrome de Klinefelter, enfermedad de Wiskott Aldrich, anemia de Fanconi, la exposición a radiaciones ionizantes, a agentes químicos en edades tempranas y a una predisposición citogenética específica como la presencia del cromosoma Filadelfia.1,2
En la población pediátrica mexicana la leucemia más común es la leucemia aguda linfoblástica precursora de células B.
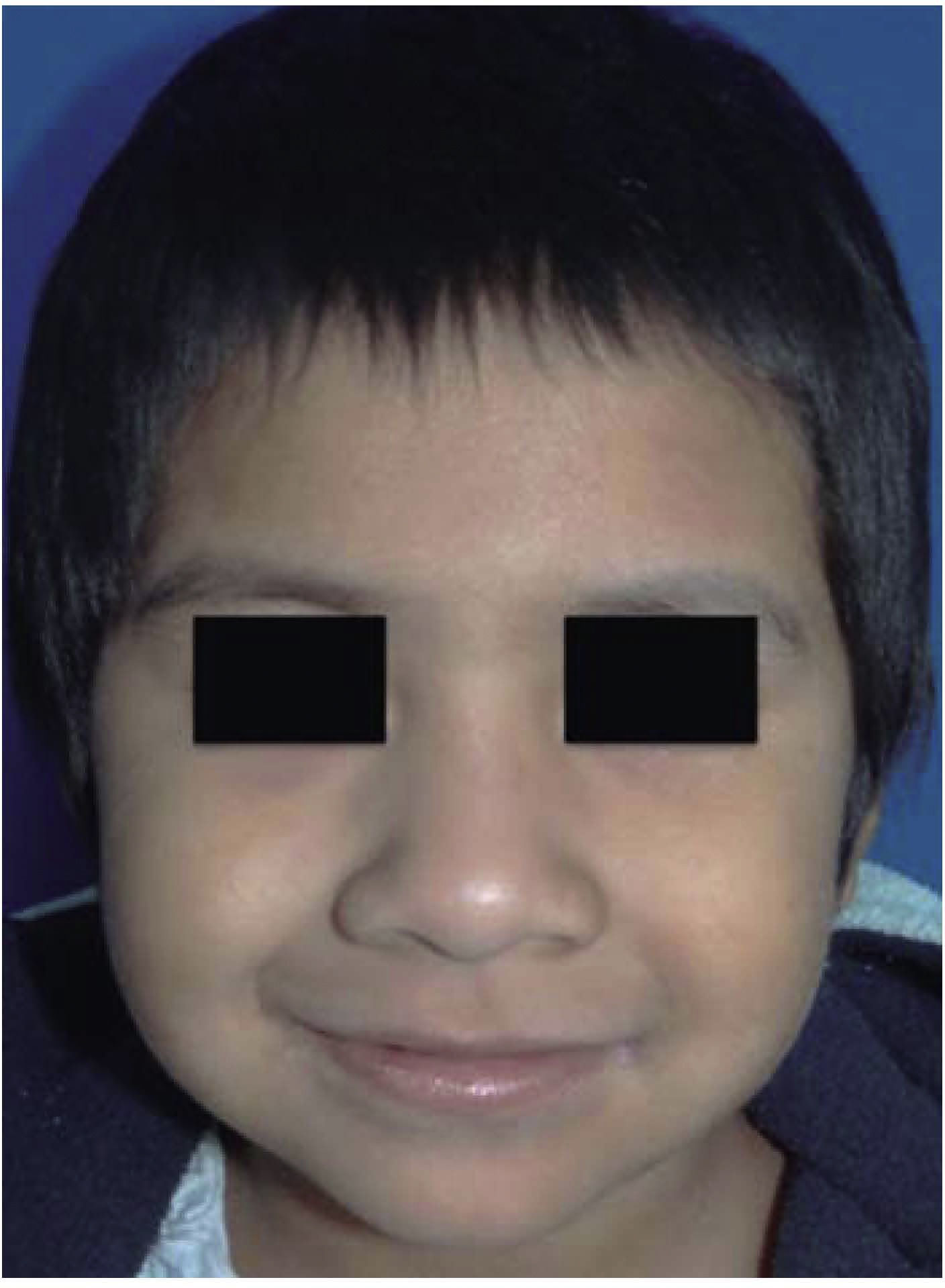
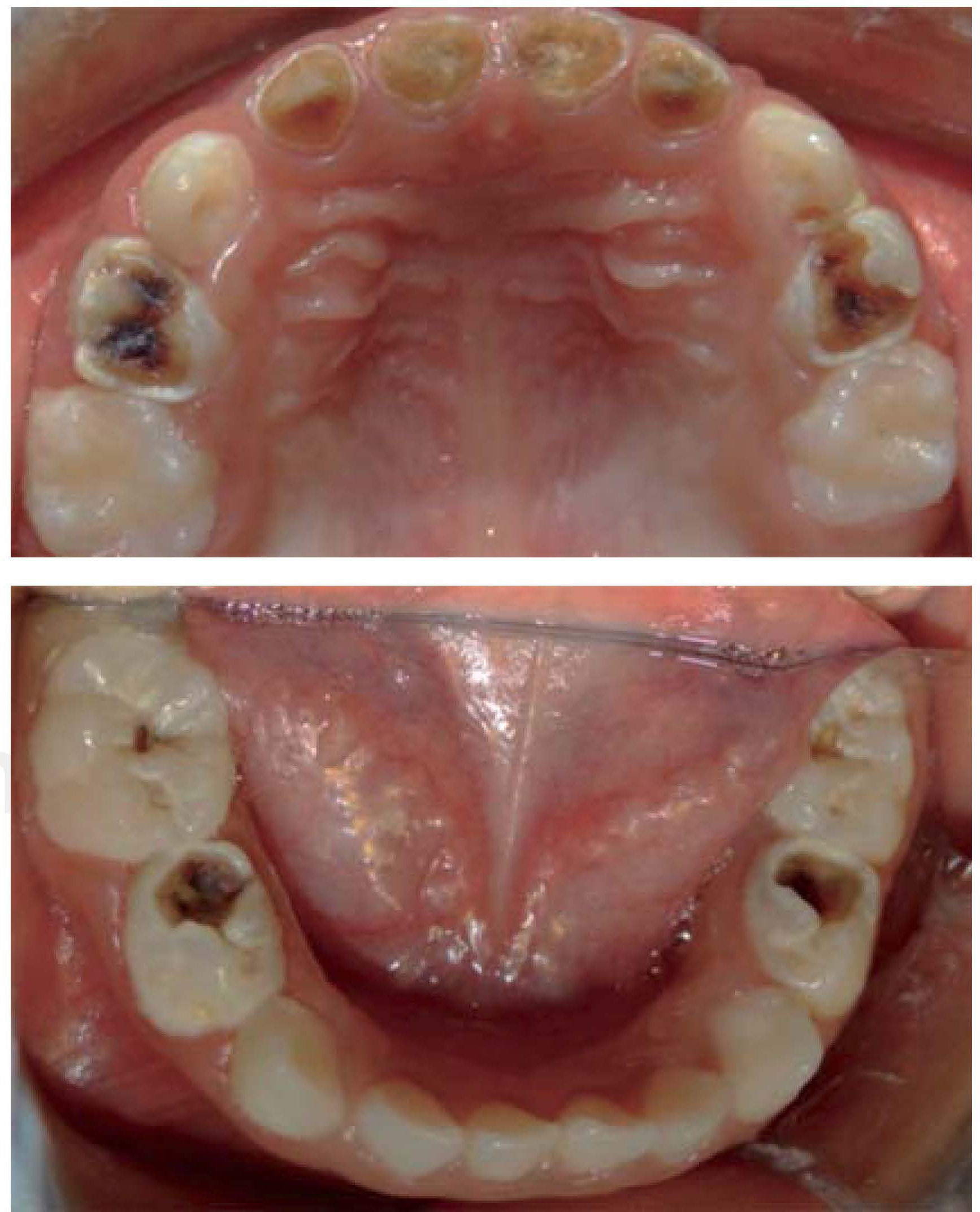
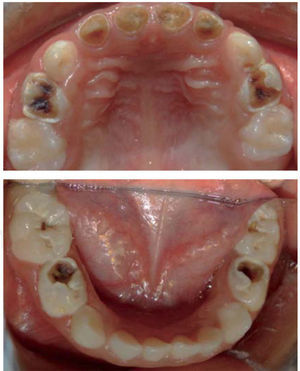
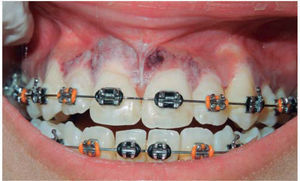
CASO CLÍNICOSe trata de paciente femenino de cinco años de edad proveniente de León, Guanajuato con diagnóstico de leucemia aguda linfoblástica precursora de células B, quien es referida a consulta odontológica por indicación del médico oncólogo tratante para rehabilitación dental urgente para poder comenzar el tratamiento con quimioterapia (Figura 2). Al revisar su historial médico se encuentra que la paciente debutó con palidez generalizada, debilidad, dolor óseo, petequias generalizas en la espalda, tórax y en las extremidades, al ser valorada por el médico pediatra es referida de inmediato al oncólogo por sospecha de leucemia. Debido a la nula cooperación de la paciente, a la complejidad de su padecimiento y a la urgencia del mismo se decide rehabilitar a la paciente bajo anestesia general (Figura 3).
Previo al tratamiento odontológico bajo anestesia general se realizan los estudios correspondientes para preparar preoperatoriamente a la paciente. Se le solicita estudios de laboratorio de biometría hemática y tiempos de coagulación. En la biometría hemática se observa que la paciente se encuentra anémica con una hemoglobina de 9g/dL, neutropénica con un conteo de neutrófilos de 500/mm3 y trombocitopénica con un conteo de plaquetas de 50,000/mm3.
Antes de comenzar el procedimiento se le administra una aféresis plaquetaria para regular al máximo los niveles de plaquetas, logrando elevarlos hasta 90,000/ mm3. Ya en quirófano se administra profilaxis antibiótica dosificada a 20mg/kg/dosis con clindamicina intravenosa, y la paciente es intubada vía nasotraqueal.
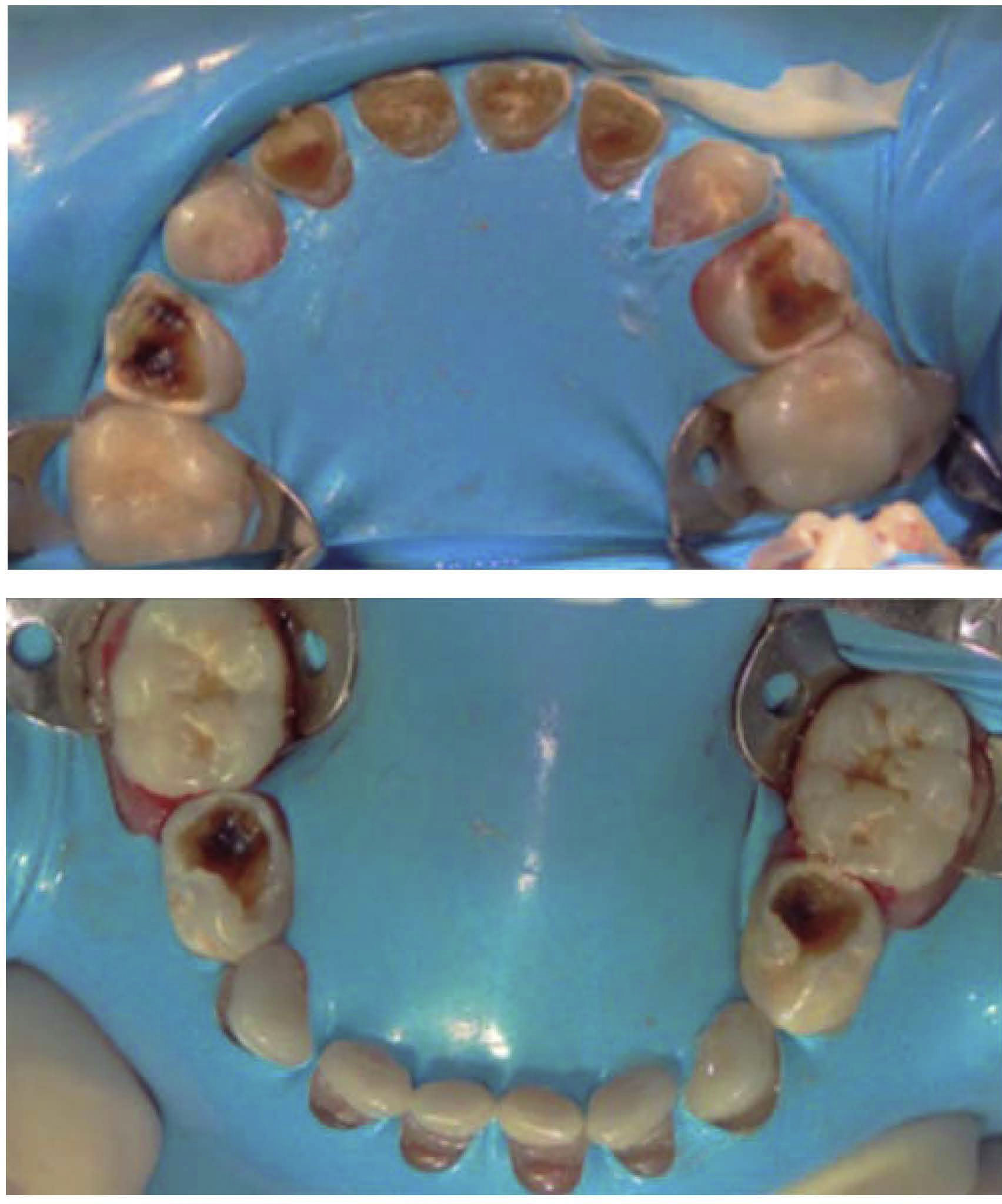
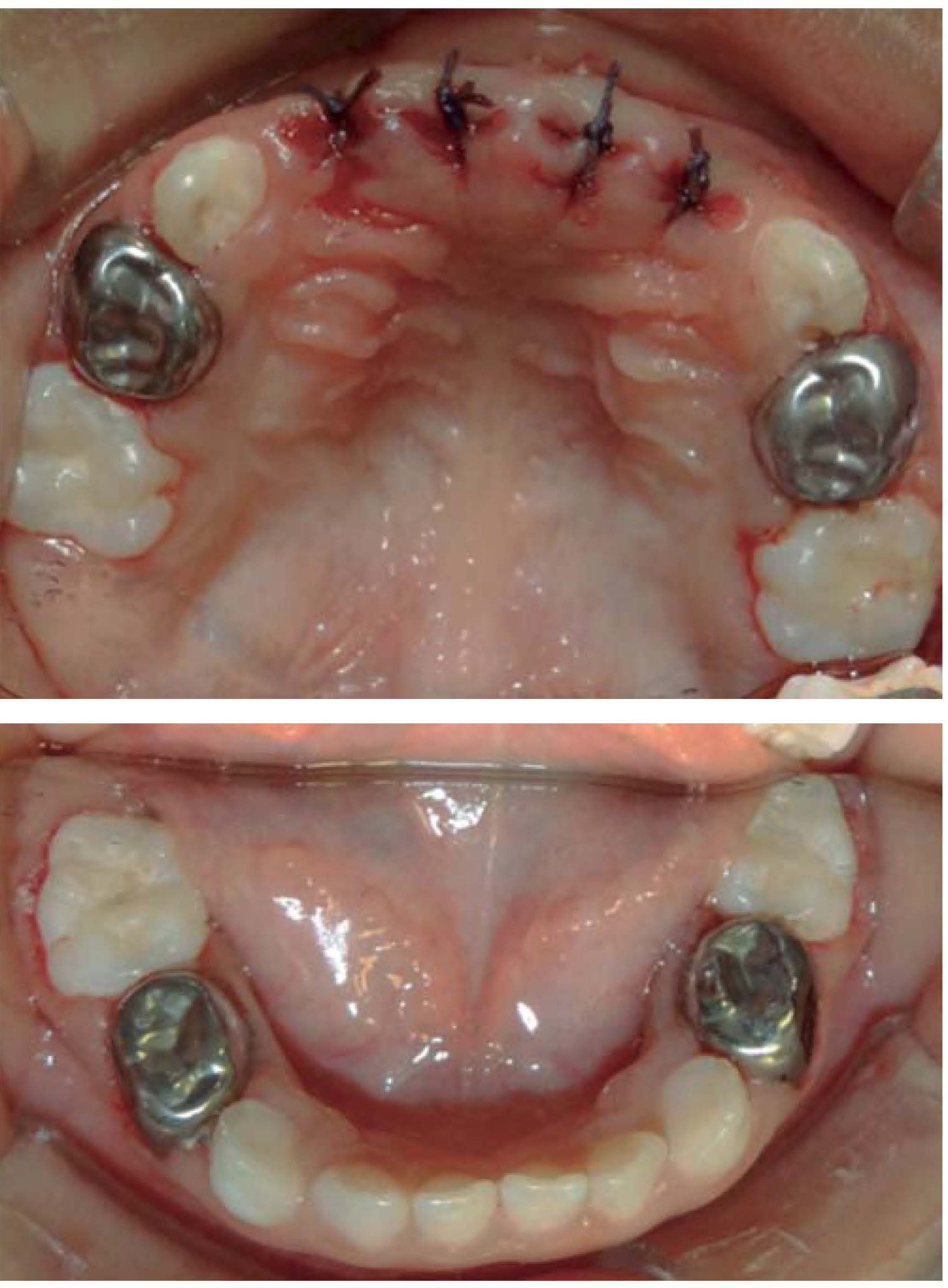
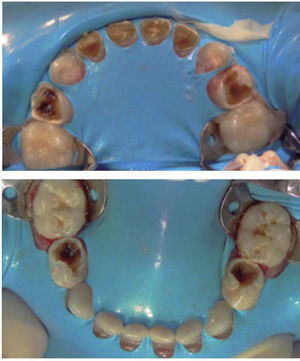
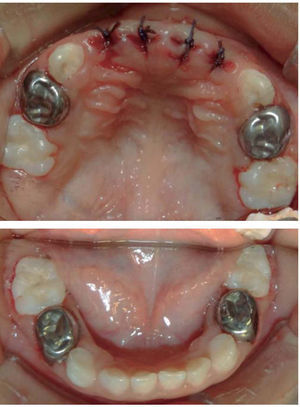
Se colocan los campos estériles de forma convencional y se aísla la totalidad de las arcadas con dique de hule (Figura 4), se realizan los siguientes tratamientos dentales: pulpotomías de primeros molares superiores, coronas de acero inoxidable en primeros molares superiores e inferiores, resinas en segundos molares inferiores, y selladores de fosetas y fisuras en segundos molares superiores.
Debido a que la paciente cursaría con un tratamiento de quimioterapia que la inmunosuprimiría, importantemente se decide realizar las extracciones de los incisivos centrales y laterales superiores preventivamente para evitar el riesgo latente de infección odontogénica que pueda agravar su estado de salud y no se indica en este momento la colocación de ninguna aparatología estética que reemplace los órganos dentarios extraídos pues dicha aparatología puede actuar como reservorio de bacterias que en un momento determinado podrían complicar su evolución clínica (Figura 5).
La paciente evoluciona adecuadamente sin presentar ninguna complicación gracias a los cuidados preventivos que se tuvieron previo a iniciar el tratamiento y es trasladada a sala de recuperación para monitorear signos vitales.
Una vez concluido el procedimiento la paciente se encuentra lista para poder comenzar el tratamiento de quimioterapia a la brevedad posible una vez que las heridas producidas por las extracciones de los dientes se encuentren cicatrizadas.
DISCUSIÓNLas leucemias pertenecen al grupo de enfermedades proliferativas malignas. Éstas son de los trastornos oncológicos más comunes en la infancia, además del retinoblastoma, el osteosarcoma y el neuroblastoma.3 Como ya se mencionó con anterioridad las leucemias pueden clasificarse de acuerdo al estirpe celular que las produce y al grado de diferenciación y funcionalidad de las células.1–3
De acuerdo con estudios estadísticos realizados en el 2001 por la Secretaría de Salud en México se registraron alrededor de 13,558 pacientes que fueron ingresados a los hospitales con el diagnóstico de leucemia, de los cuales murieron 232 en un grupo de edad de 1 a 4 años y 558 en el grupo de edad de 5 a 14 años.4,5 La leucemia linfoblástica aguda se caracteriza por aparecer en la primera década de vida; sin embargo, es posible que su frecuencia pueda incrementarse también en pacientes de la tercera edad. Las células inmaduras que en condiciones normales se diferenciarían a cualquier célula del estirpe linfoide o mieloide se le denomina blasto,6 estas células al ser no funcionales no deberían encontrarse en la circulación sanguínea; sin embargo, cuando el paciente debuta con leucemia aparece una producción excesiva de blastos que invaden la médula ósea y por ende, la circulación general. Al producirse una gran cantidad de células inmaduras, éstas ocupan un espacio amplio dentro de la médula ósea de los huesos largos, impidiendo así que las otras células bien diferenciadas puedan reproducirse de forma normal y ocupar su espacio dentro de la médula ósea, generando entonces en el paciente una disminución de todos los conteos celulares (pancitopenia) y además dolor en las extremidades superiores e inferiores. Al tener un descenso importante en el conteo de la hemoglobina y de las plaquetas el paciente cursa con anemia y trombocitopenia que se traduce clínicamente en palidez generalizada, astenia, adinamia y lesiones vasculares en la piel y en la mucosa bucal.5–7 Todo paciente que debuta con leucemia cursa por determinados síndromes asociados, a saber: febril, infiltrativo, hemorrágico, anémico, tumoral y consuntivo (Cuadro I).
Signos y síntomas tempranos del paciente con leucemia
| Síndrome | Signos y síntomas |
|---|---|
| Febril | Fiebre continua de hasta 40°C que no cede a la administración de fármacos antipiréticos. Asociado a susceptibilidad, a infecciones y a úlceras orales |
| Infiltrativo | Invasión de células leucémicas a diferentes tejidos y órganos como los huesos, el riñón o el hígado |
| Hemorrágico | Debido a la trombocitopenia tan severa que el paciente presenta es común que curse con epistaxis, equimosis, petequias en mucosa bucal y en las conjuntivas y gingivorragias |
| Tumoral | Hepatoesplenomegalia por infiltración blástica al hígado, bazo, ganglios y gónadas. Presencia de adenomegalias en más de dos sitios |
| Consuntivo o de desgaste | Pérdida de peso corporal excesivo, debilidad y fiebre |
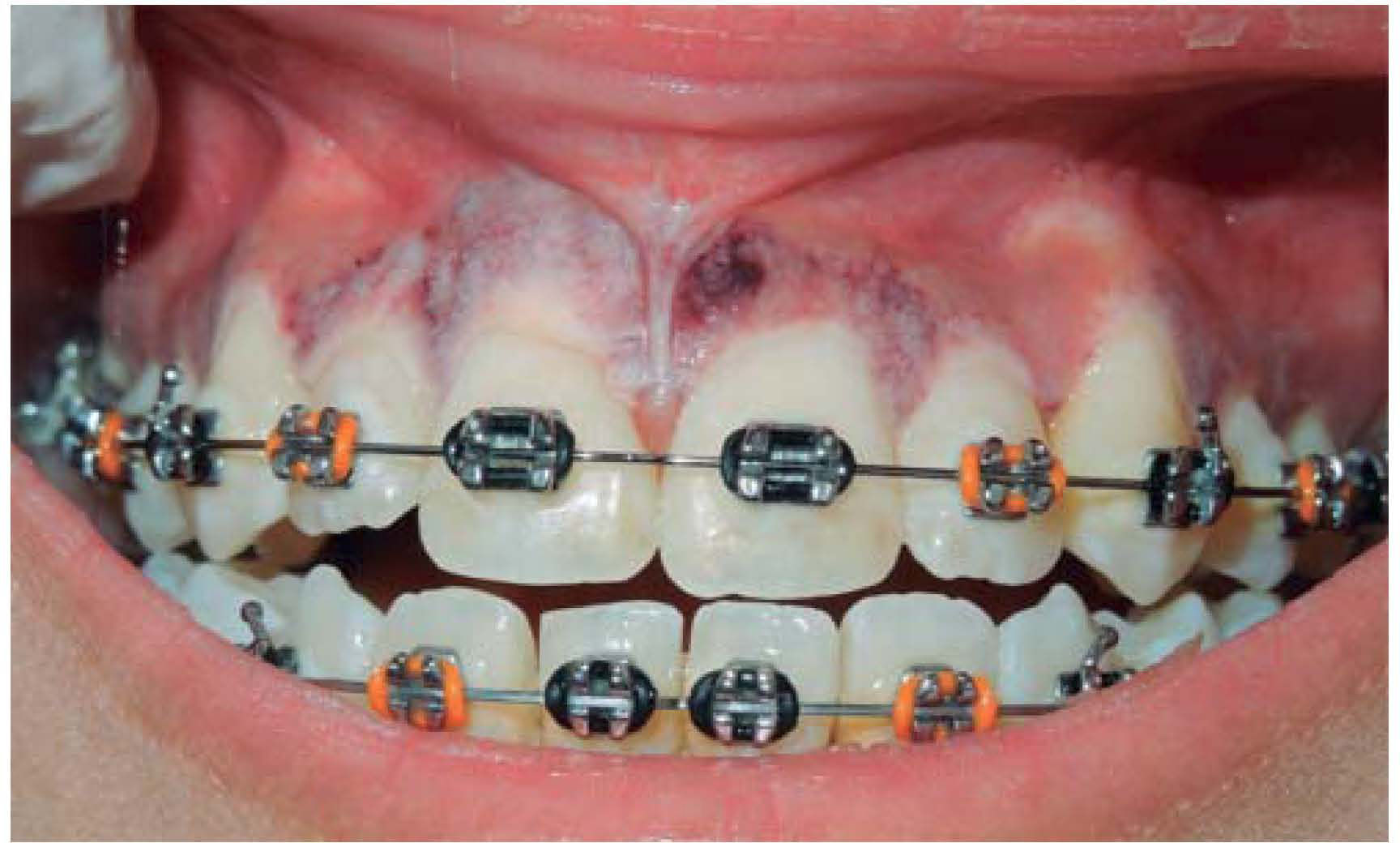
Al tratarse de un padecimiento derivado de los glóbulos blancos es común encontrar infiltrados leucocitarios en la mucosa bucal, esto último es una invasión de células neoplásicas leucocitarias que penetran en la mucosa bucal destruyéndola. Clínicamente se observan como lesiones blanquecinas que no desprenden al raspado. El infiltrado leucocitario puede ser una manifestación subclínica indicativa de que un paciente se encuentra cursando con leucemia (Figura 6).
El diagnóstico médico de la leucemia se basa en la sintomatología característica y en los estudios de laboratorio que se le indiquen al paciente (Cuadro II). Generalmente para corroborar el diagnóstico se indica un aspirado de médula ósea para valorar si existe o no invasión de blastos, si existe una blastosis medular que supere el 30% de la totalidad celular se podrá emitir dicho diagnóstico. Además de los conteos celulares de la biometría hemática que se caracterizan por tener un conteo elevado de leucocitos (mayor de 50,000 mm3) y la presencia de blastos reportados en la misma, y en consecuencia una disminución importante en el conteo de las plaquetas, neutrófilos, hemoglobina, eritrocitos.
Estudios diagnósticos realizados a un paciente con leucemia
| Estudio diagnóstico | Justificación del estudio |
|---|---|
| Recuento de células sanguíneas | Valoración de los diferentes tipos de células y su aspecto microscópico |
| Biopsia y aspirado de médula ósea | Obtenido del hueso iliaco para observar o descartar la presencia de blastos en la médula ósea |
| Otras pruebas de sangre | Pruebas de función renal y hepática para descartar invasión de células leucémicas a estos órganos |
| Punción lumbar | Descartar la presencia de células leucémicas en el líquido cefalorraquídeo |
| Citometría de flujo | Determinar con alta especificidad el tipo de leucemia que tiene el paciente mediante el uso de anticuerpos que se adhieren exclusivamente a ciertos tipos de células leucémicas |
| Citogenética | Detección de anormalidades cromosómicas como la translocación, ayuda a estimar el pronóstico de la enfermedad, observando si las células citogenéticamente son sensibles o resistentes a la quimioterapia |
La citogenética es muy importante para determinar el pronóstico de la leucemia. Cuando en el estudio citogenético se observan células con un mayor número de cromosomas (denominadas hiperdiploides) los pacientes tienen mayores posibilidades de cura, a diferencia de los pacientes que tienen menor cantidad de cromosomas (hipodiploides) que generalmente tienen peor pronóstico. La presencia del llamado cromosoma Filadelfia es un factor que determina mal pronóstico para la enfermedad también.4,5,7
Sin embargo, además de la citogenética existen otros factores que condicionan el pronóstico de la leucemia (Cuadro III).
Factores que afectan al pronóstico del paciente con leucemia
| Factor pronóstico | Justificación |
|---|---|
| Edad | Los niños de menos de 1 año y mayores de 10 años tienen peor pronóstico que los niños de 1 a 9 años |
| Sexo | Los varones tienen peor pronóstico a diferencia de las niñas, debido al riesgo de recaída por los testículos |
| Etnia | Los niños de raza negra e hispana tienen peor pronóstico que los de raza caucásica |
| Conteo de glóbulos blancos | Si presenta un conteo de 50,000mm3 o mayor es indicativo de mal pronóstico |
| Enfermedad extramedular | Si hay invasión de células leucémicas a Sistema Nervioso Central o a testículos |
| Respuesta al tratamiento | Si el niño responde adecuadamente a las primeras fases del tratamiento es indicativo de buen pronóstico. Por lo contrario los niños que no responden al tratamiento inicial es un criterio de mal pronóstico |
Una vez que el paciente ha sido diagnosticado debe iniciarse a la brevedad el tratamiento de quimioterapia; sin embargo, éste no puede llevarse a cabo si el niño presenta focos infecciosos en su boca, es por ello que el odontólogo juega un papel crucial en el tratamiento de estos pacientes.8
Todo odontólogo debe conocer las fases de la quimioterapia a las cuales será sometido un paciente con esta condición patológica, pues en cada fase en particular existen medicamentos y secuelas específicas que pueden contraindicar o exigir una modificación en la ruta del tratamiento dental de este paciente. Cuando el niño no ha sido sometido a tratamiento quimioterápico, el odontólogo deberá valorar la biometría hemática y los tiempos de coagulación para valorar si el paciente requiere aféresis plaquetaria o administración de profilaxis antibiótica previo a la realización de los tratamientos odontológicos invasivos debido al descenso tan importante en sus células de defensa. También es necesaria en esta etapa la remoción total de aparatología ortodóntica u ortopédica que el paciente porte pues puede convertirse en un reservorio de placa que puede afectar la evolución del paciente una vez que comience la inmunosupresión por la quimioterapia.
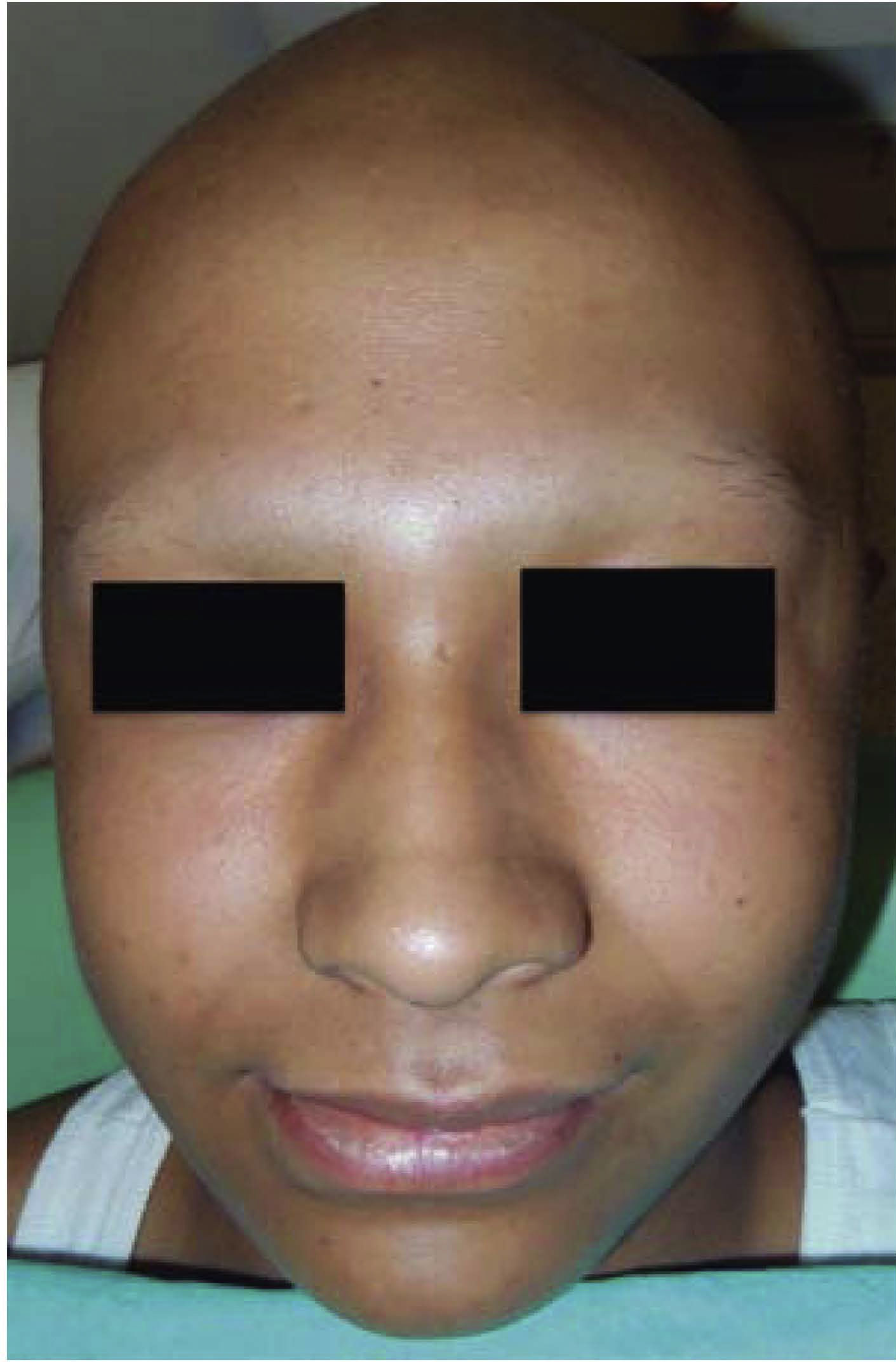
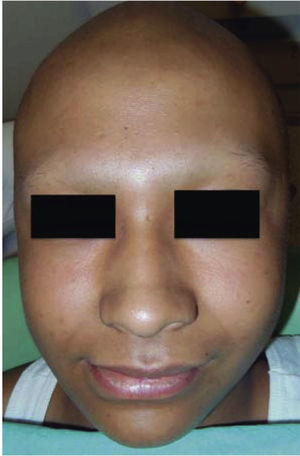
A la primera fase de la quimioterapia se le denomina inducción a la remisión.2,3,8 En esta fase al paciente se le administran dosis altas de corticosteroides como la metilprednisolona, con el único objetivo de inmunosuprimirlo y detener inicialmente la evolución de la enfermedad, si el paciente evoluciona adecuadamente, se pasará a la siguiente fase que recibe el nombre de consolidación o intensificación,2,8 en la cual además de administrar corticosteroides, se administrarán también medicamentos quimioterápicos como la vincristina, citarabina, daunorubicina, L-asparginasa, etopósidos, ciclofosfamida, metotrexato, entre otros. Tras haber administrado estos medicamentos el paciente cursará con secuelas específicas como el efluvio anágeno, pérdida de peso, náusea, vómito y palidez generalizada (Figura 7). Tras una semana de haber administrado estos medicamentos al paciente comenzará un padecimiento llamado neutropenia del séptimo día o fase nadir, la cual se caracteriza por tener conteos de neutrófilos por debajo de 200, pudiendo llegar incluso a un conteo de 0 neutrófilos por milímetro cúbico.
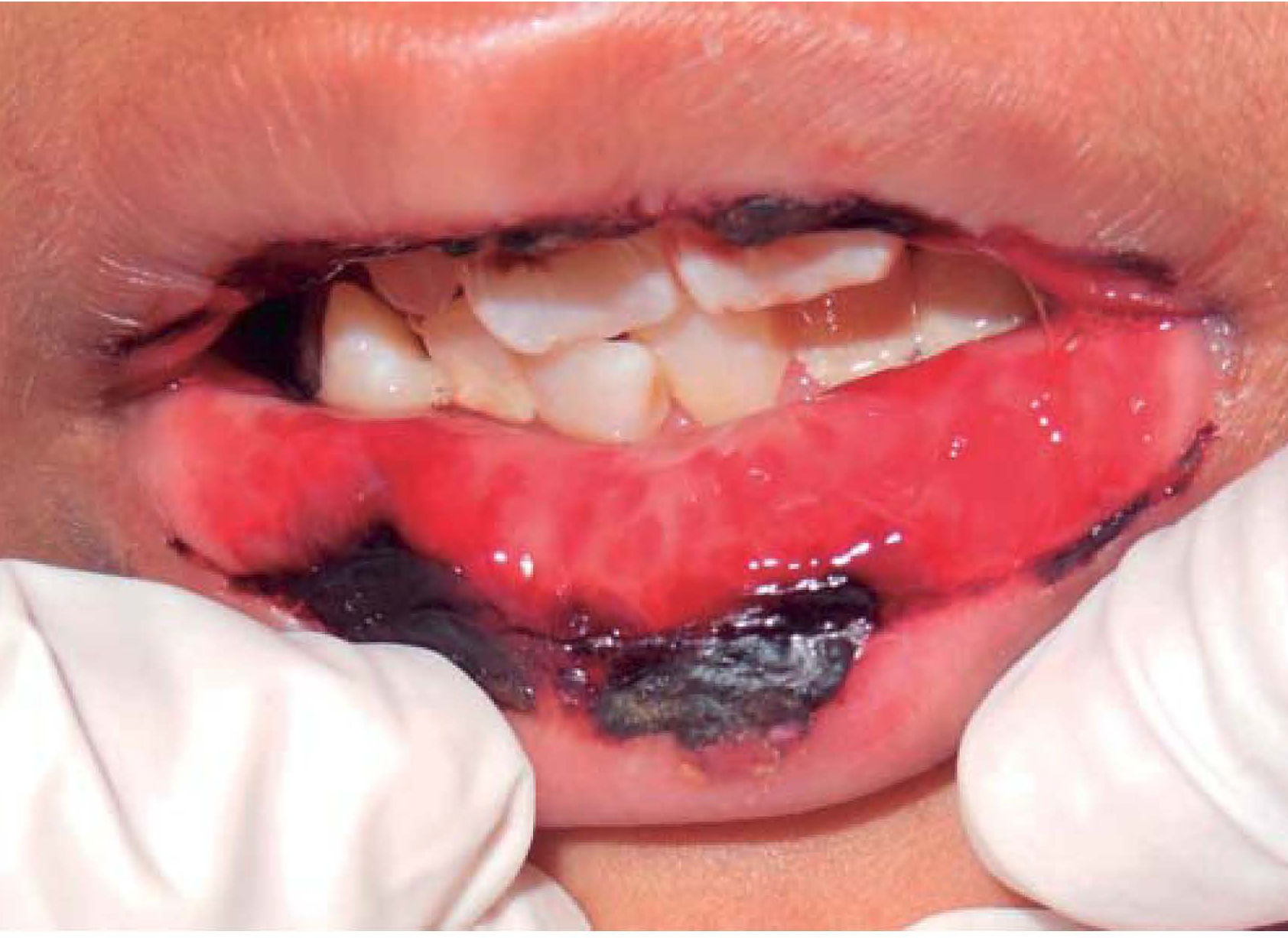
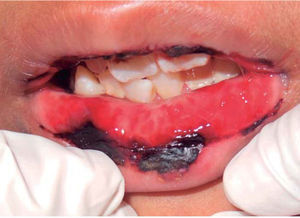
Es en esta fase cuando el paciente puede presentar la secuela más dolorosa de la quimioterapia en la cavidad bucal, denominada mucositis. La mucositis tiende a aparecer a consecuencia de la administración del metotrexato y se caracteriza por la descamación y ulceración de toda la mucosa del tracto digestivo, desde la boca hasta el ano, disminuyendo en el paciente la tolerancia a la vía oral en un cien por ciento, el odontólogo deberá indicar tratamientos paliativos que ayuden al paciente a tolerar la ingesta vía oral, como recubridores de mucosa o antihistamínicos tópicos que disminuyan la inflamación local de la mucosa bucal ulcerada (Figura 8).9–12
Es en este momento cuando el odontólogo debe omitir la totalidad de sus tratamientos por las condiciones tan delicadas del niño y cualquier padecimiento deberá tratarse de forma paliativa únicamente (analgésicos, antibióticos o antimicóticos en caso necesario), en espera de que los conteos celulares se normalicen en los próximos días.10,13
Una vez superada esta fase, el paciente es sometido a un nuevo aspirado de médula ósea y a otra biometría hemática en donde se espera ver un descenso importante de las células blásticas, lo cual es indicativo de una adecuada respuesta al tratamiento.
Posterior a esto, el paciente pasa a la siguiente y penúltima fase que recibe el nombre de mantenimiento, en la cual se le administran quimioterápicos y corticosteroides periódicamente con el fin de controlar su padecimiento. Un paciente puede durar varios años en esta fase, al someterse, desde luego, a estudios de laboratorio esporádicos de control (BH, aspirados de médula ósea y punciones lumbares). Este paciente puede ser tratado en el consultorio dental tomando en cuenta las posibles secuelas de los medicamentos que le son administrados, y puede ser necesario que requiera la administración de profilaxis antibiótica antes de ser tratado.
Cuando el paciente ha superado la enfermedad tras haber pasado mínimo dos años con dosis bajas de medicamento y ausencia total de blastos en los estudios realizados periódicamente, pasa a la última fase del tratamiento oncológico denominado vigilancia. Todo individuo que se encuentra en la fase de vigilancia deberá estar en revisiones periódicas anuales toda su vida; sin embargo, se debe resaltar que un paciente que se encuentra en vigilancia puede ser tratado odontológicamente como un paciente sano.
La leucemia tiene un riesgo importante de recaída una vez superada la enfermedad, esto debido a situaciones específicas que deben preverse antes de comenzar el tratamiento de quimioterapia. Las células leucémicas tienden a introducirse dentro de los llamados «órganos santuario», siendo éstos el sistema nervioso central y los testículos de los varones, éstas son zonas donde los medicamentos quimioterápicos no surten efecto y son entonces las zonas anatómicas con mayor riesgo a producir recaída.2,3,14 Es por eso que la terapia intratecal es obligatoria en el tratamiento de un paciente con leucemia y la realización de varias punciones lumbares durante el tratamiento para descartar la invasión de blastos dentro del sistema nervioso central.14,15
CONCLUSIÓNEl odontólogo juega un papel fundamental en el diagnóstico y el tratamiento de un paciente con leucemia. Dentro de la cavidad oral pueden aparecer muchas lesiones tempranas indicativas de leucemia, es por ello que el personal odontológico está obligado a conocerlas. La intervención odontológica es crucial debido a la necesidad de erradicar focos infecciosos, previo al comienzo de la terapia oncológica y tratar los padecimientos bucodentales que pudieran presentarse a consecuencia de la quimioterapia. El conocimiento de las fases de la quimioterapia a las cuales un paciente será sometido determina importantemente la conducta odontoestomatológica a seguir.
Este artículo puede ser consultado en versión completa en http://www.medigraphic.com/facultadodontologiaunam