El caso clínico que se muestra ejemplifica la conjunción de múltiples técnicas quirúrgicas con el objetivo de rehabilitar protésicamente a un paciente desdentado, para el tratamiento del maxilar superior atrófico con injerto autólogo de cresta iliaca anterior tipo onlay. Se trata de paciente del sexo femenino de 60 años de edad, la cual presenta un proceso alveolar atrófico tipo IV de Cawood y Howell, por lo que se realiza la conservación y reconstrucción de proceso alveolar con injerto autólogo de cresta iliaca.
The clinical case presented in this article illustrates the combination of multiple surgical techniques geared to the prosthetic rehabilitation of an edentulous patient for the treatment of an atrophic upper jaw with an onlay type iliac crest autologous graft. Treated patient was a 60 year old female presenting a type IV Cawood and Howell atrophic alveolar process. Therefore, treatment conducted was reconstruction of the alveolar process with an iliac crest autologous graft.
El paciente que ha sufrido la amputación total de los órganos dentarios está condenado a ser un inválido por el resto de su vida, hasta no recibir el benefi cio de una rehabilitación protésica adecuada, lo que implica un reto al momento de restituir el hueso basal y alveolar del maxilar o mandíbula, para lograr su grosor así como altura a largo plazo.
La fisiopatología de la reabsorción alveolar se da por factores metabólicos (nutrición, endocrinos, osteopenias asociadas, etc.) y locales; ambos son de un impacto significativo en lo que a la cirugía reconstructiva se refiere.1
Dentro de los factores locales el más común es la ausencia de los órganos dentales, lo que provoca en el hueso maxilar una reabsorción ósea por falta de estímulo intraóseo, modificándose la proporción de hueso medular en comparación con el hueso cortical, teniendo menos pérdida en el hueso cortical.
Por lo anterior, es importante tener en consideración el proceso fisiológico de reabsorción del hueso maxilar y mandibular para poder realizar una adecuada reconstrucción. En el caso del hueso maxilar la reabsorción es de tipo centrípeta dando como resultado un colapso; sin embargo, en la mandíbula la reabsorción es de tipo centrífuga.
Este proceso se inicia en el reborde alveolar tras la pérdida de los órganos dentales, lo cual ocasiona colapso gingival y una disminución del volumen óseo, entre los primeros seis meses y dos años postextracción. 1,2
Esto puede incrementarse por el resto de la vida, por la compresión producida por el uso de prótesis removibles mal ajustadas, ya que el paciente se tiene que acoplar a la utilización de éstas, modificando hábitos alimenticios y procesos funcionales del sistema estomatognático.1,3
La alteración en la forma o función del hueso es seguida por ciertos cambios en su arquitectura interna y externa; por lo tanto, si un hueso es cargado en una nueva dirección, su estructura y forma pueden cambiar de acuerdo a su nueva función; si un hueso deforme es rectificado y su función es restaurada toda la estructura del hueso retorna a su forma original.4,5
Esta alteración en la forma y función se puede explicar por el principio de Wolf, donde la formación ósea alveolar se produce mediante el esfuerzo mínimo indispensable para mantenerse a sí mismo teniendo un proceso fisiológico óseo estable. Por el contrario, si este esfuerzo es insuficiente o si existe una carga excesiva esto puede conducir a una remodelación regresiva del hueso,4,5 ya que existe un equilibrio entre el colapso y la reparación por medio de la osteona, unidad funcional del hueso, dando como consecuencia la viabilidad de la forma del hueso.
Esta forma de reabsorción ósea alveolar se ha descrito y clasificado por Cadwood y Howell, la cual es la siguiente:6,7
- a)
Clase I: dentados.
- b)
Clase II: postextracción.
- c)
Clase III: proceso de forma convexa, con anchura y altura adecuadas.
- d)
Clase IV: filo de navaja con la adecuada altura, anchura insuficiente de proceso alveolar.
- e)
Clase V: forma plana con la pérdida de proceso alveolar.
- f)
Clase VI: la pérdida de hueso basal.
Con el objetivo de rehabilitar los diferentes tipos de atrofias alveolares en maxilar y mandíbula, se han diseñado diferentes técnicas de cirugía preprotésica, algunas de ellas encaminadas al aumento de la profundidad vestibular por la disección de tejidos blandos, como: vestibuloplastias de Wassmund, Kazanjian, Obwgeser, etc., las cuales no cumplieron las expectativas en casos de atrofia severa y a largo plazo.7
Los procedimientos en la actualidad están encaminados al aumento del hueso remanente por medio de: autoinjertos, aloinjertos, xenoinjertos; derivando de ello técnicas híbridas como injertos de tipo onlay, de interposición con osteotomía tipo Lefort I, de seno maxilar, piso nasal, proteína morfogenética, injertos microvasculares, implantes dentales, implantes cigomáticos y distracción osteogénica. Todos son métodos exitosos en la reconstrucción del proceso maxilar atrófico.2,7,8
En sitios de pérdida dentaria unitaria o múltiple limitada a 3 o 4 dientes es posible realizar las técnicas de injertos con sitios donantes intraorales como son; mentón, rama mandibular, y tuberosidad del maxilar. 7,8
No obstante, en casos de procesos maxilares atróficos desdentados totales, el volumen óseo ofrecido por estos sitios es insuficiente para la reconstrucción. En este ámbito, el clínico tiene la opción de escoger un sitio donante extrabucal, que ofrezca la opción de reconstrucciones completas de los maxilares, con hueso suficiente para obtener el volumen deseado.9
Los procedimientos para la toma de estos injertos pueden presentar diversas complicaciones, como dolor postoperatorio, lesiones nerviosas y de la cicatrización. Estas complicaciones, en caso de tener la experiencia y el conocimiento anatómico quirúrgico, son mínimas.9,10
El injerto autólogo de cresta iliaca anterior proporciona hueso con un alto contenido de componentes óseos celulares, por lo que se considera el estándar de oro en el tratamiento de la reconstrucción de los diferentes grados de atrofia maxilar, ya que permite un volumen suficiente de hueso corticoesponjoso, el cual es un requisito para el éxito en la cirugía preprotésica.10–12
Existe un consenso en la literatura internacional en la indicación de reconstrucción de rebordes atróficos con el objetivo de la colocación de implantes, para esto se requiere la elaboración de un plan de tratamiento, donde es importante considerar la cantidad y el origen de la pérdida ósea, siendo esto fundamental para obtener el resultado exitoso en la reconstrucción, recordando que el objetivo es el aumento del proceso alveolar, tanto en espesor como en altura a largo plazo.7,10–12
En procesos alveolares atróficos, clasificación Cawood y Howell IV-VI, está indicado un injerto tipo onlay de cresta iliaca para restablecer las dimensiones maxilares fijado con tornillos de 1.5 a 2mm como fuentes de retención y estabilización.7,10–12
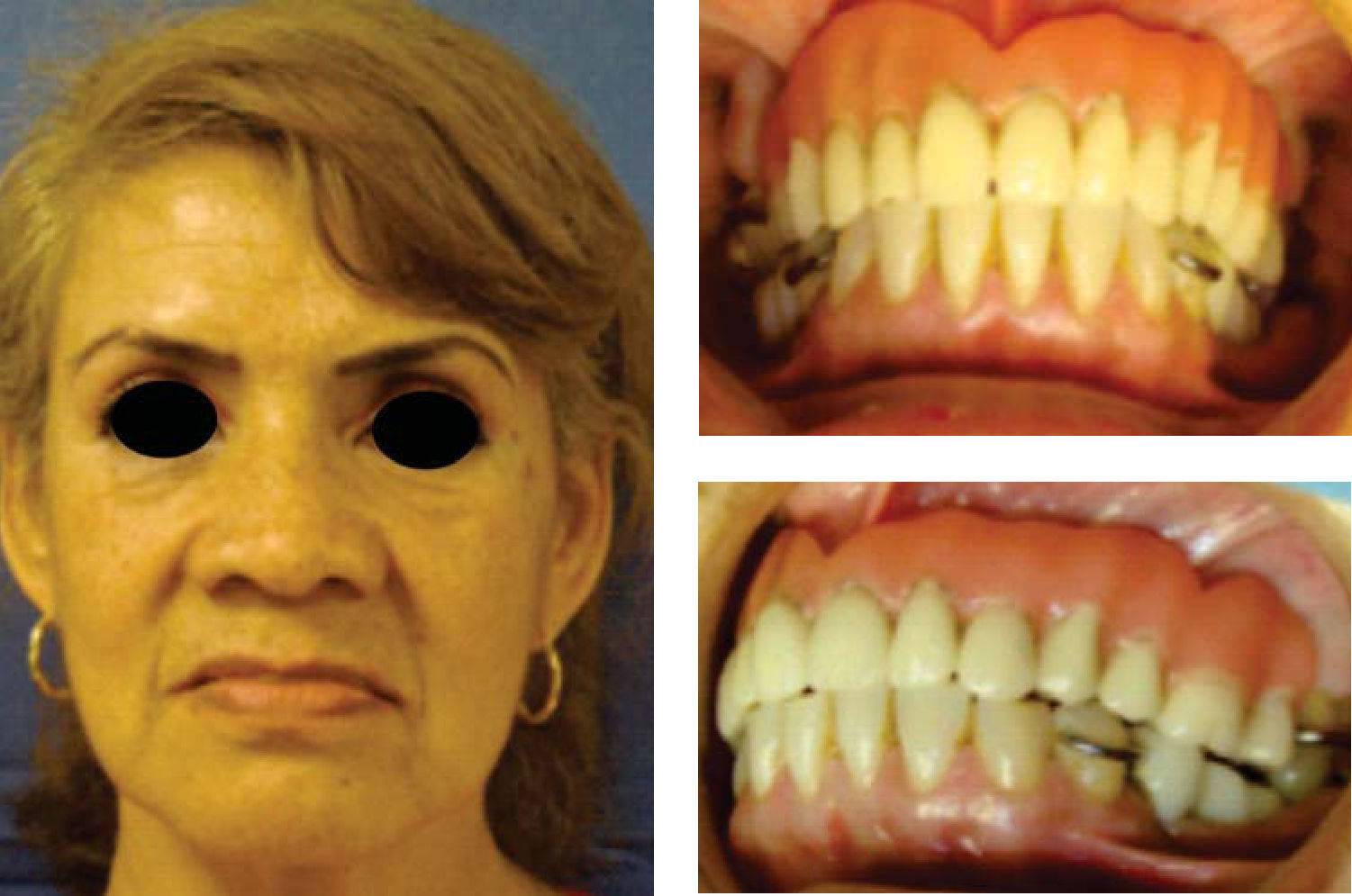
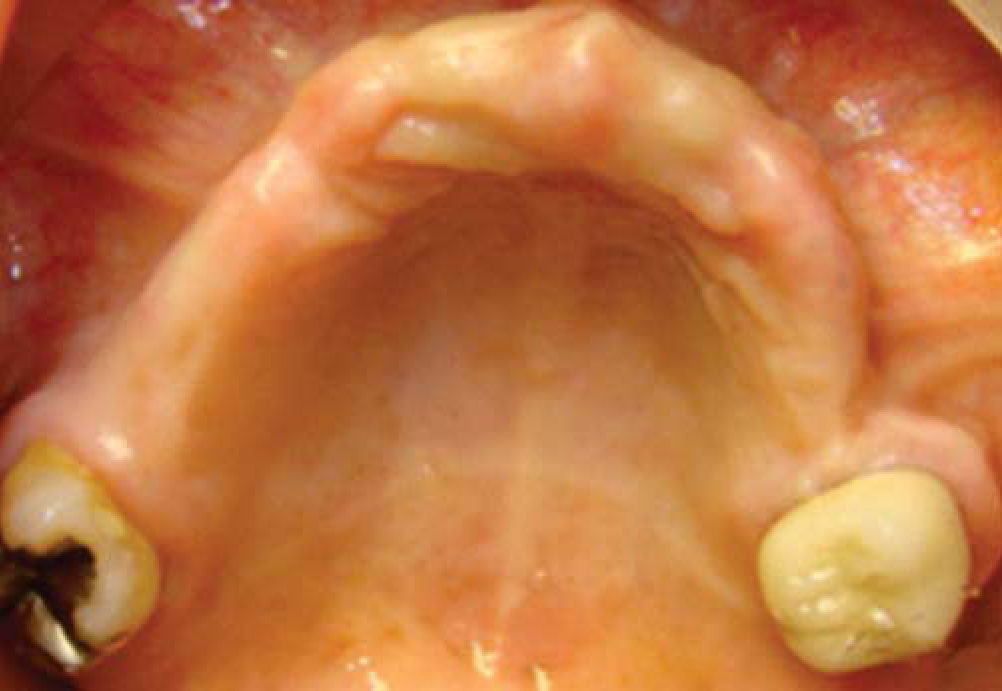
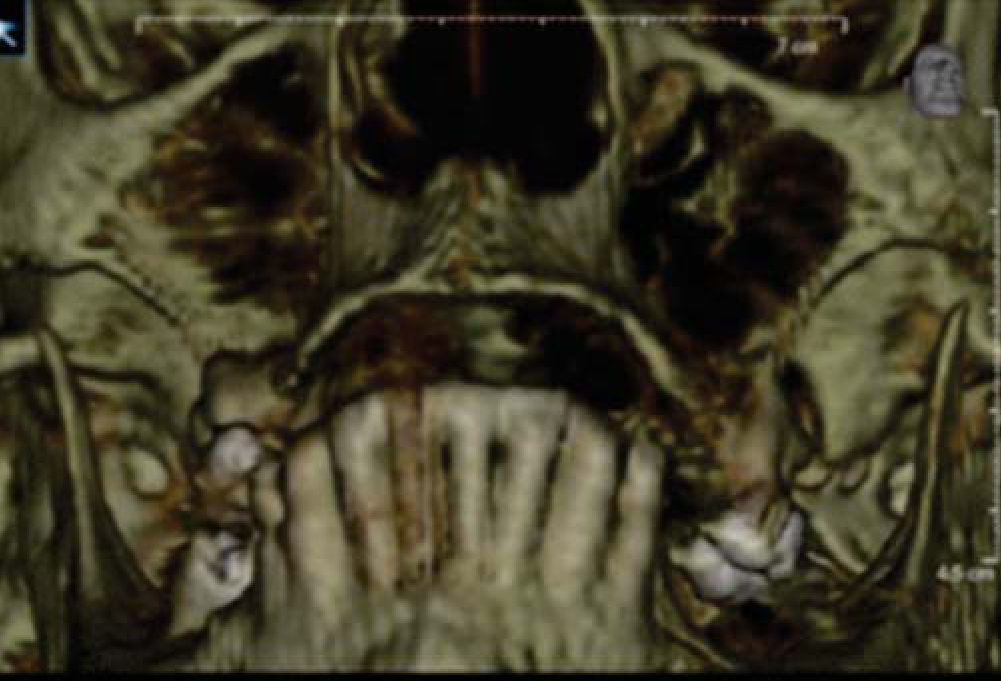
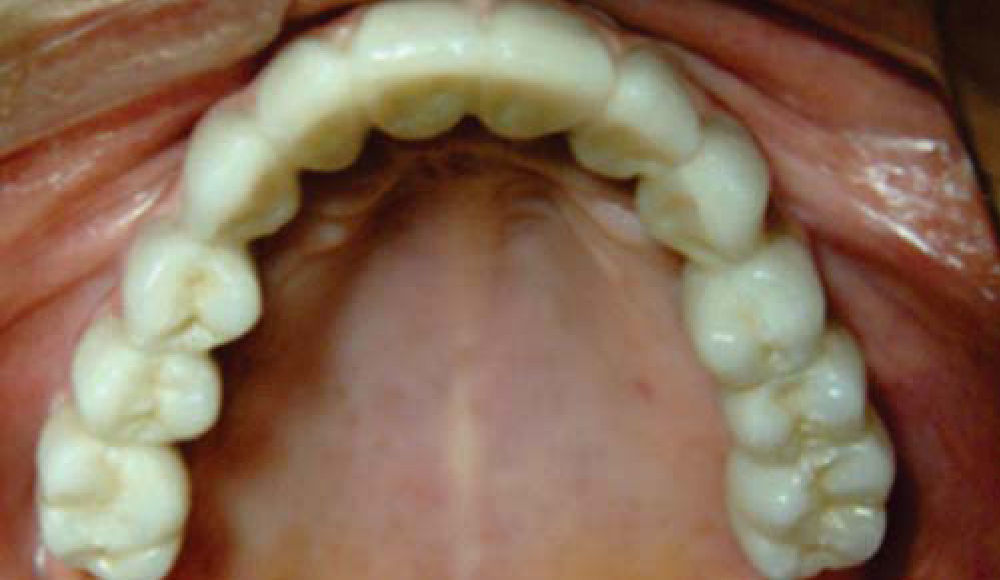
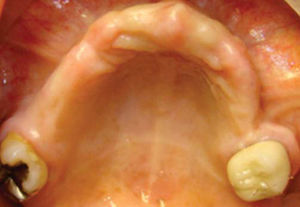
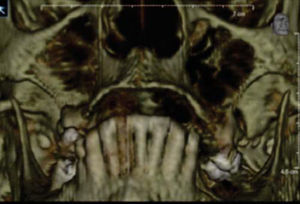
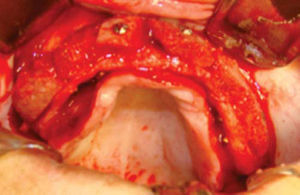
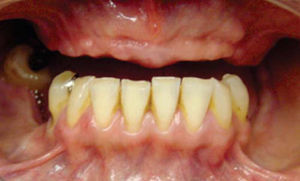
Paciente y métodoSe trata de una paciente del sexo femenino de 60 años de edad sin antecedentes crónico-patológicos, la cual refiere como queja principal inestabilidad de prótesis superior, siendo ésta el resultado de múltiples especialistas. A la exploración física intraoral presenta dentición secundaria incompleta, maxilar con presencia de dos órganos dentales con movilidad grado III, proceso alveolar atrófico clasificación IV de Cadwood y Howell, que a su calibración clínica medía 3mm de espesor, lo cual se confirma con estudio tomográfico (Figuras 1 a 3).
Se decide realizar odontectomías de órganos dentales residuales maxilares conservando su alvéolo y la reconstrucción del proceso alveolar con injerto de cresta iliaca anterior tipo onlay con el fin de colocar implantes en un segundo tiempo quirúrgico.
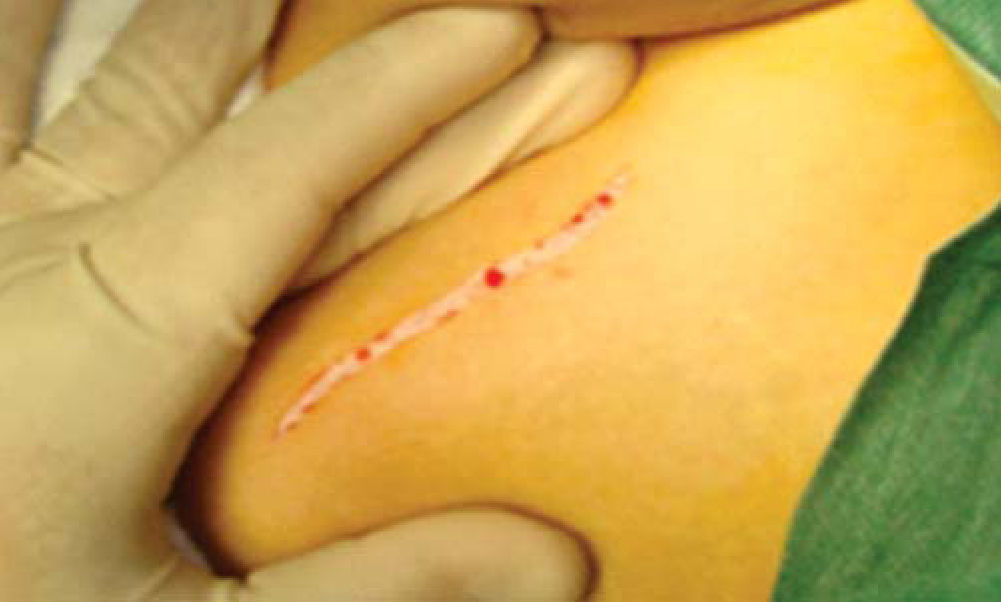
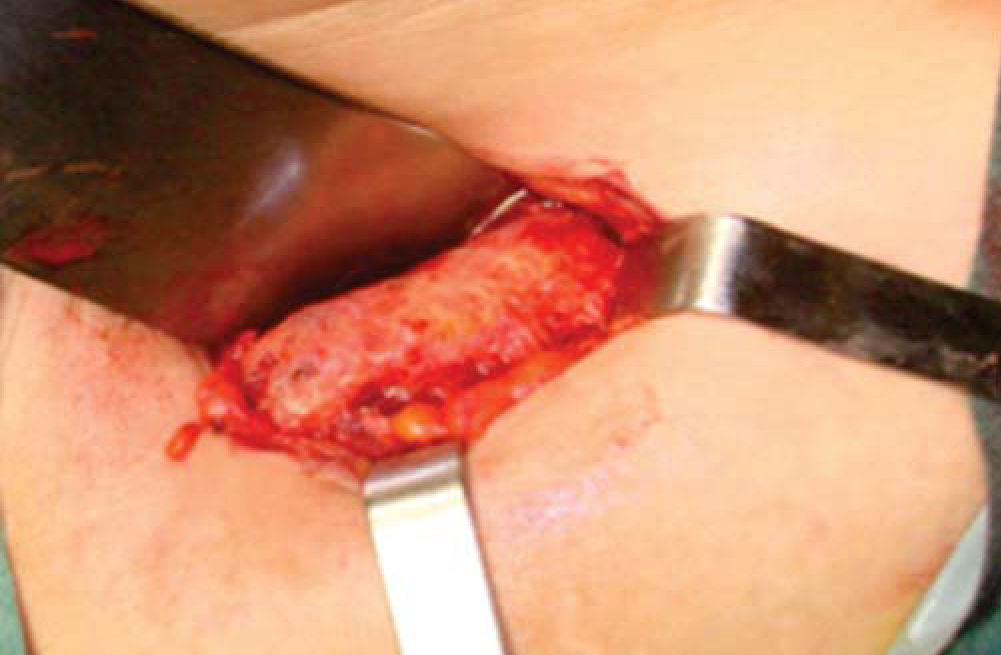
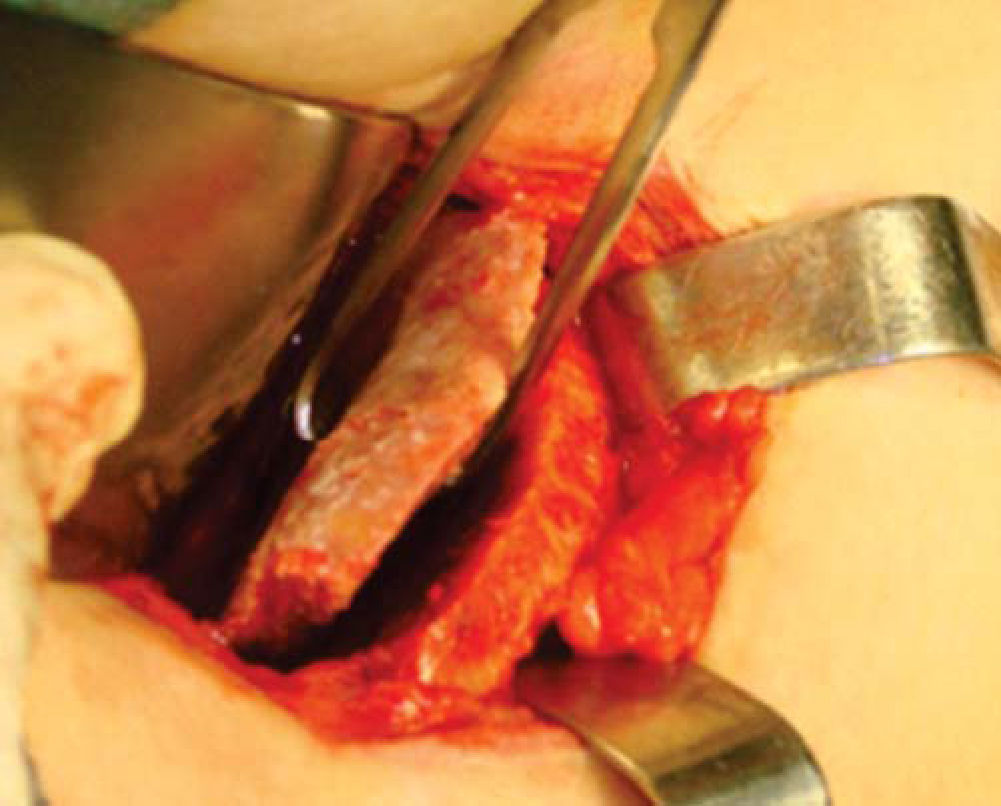
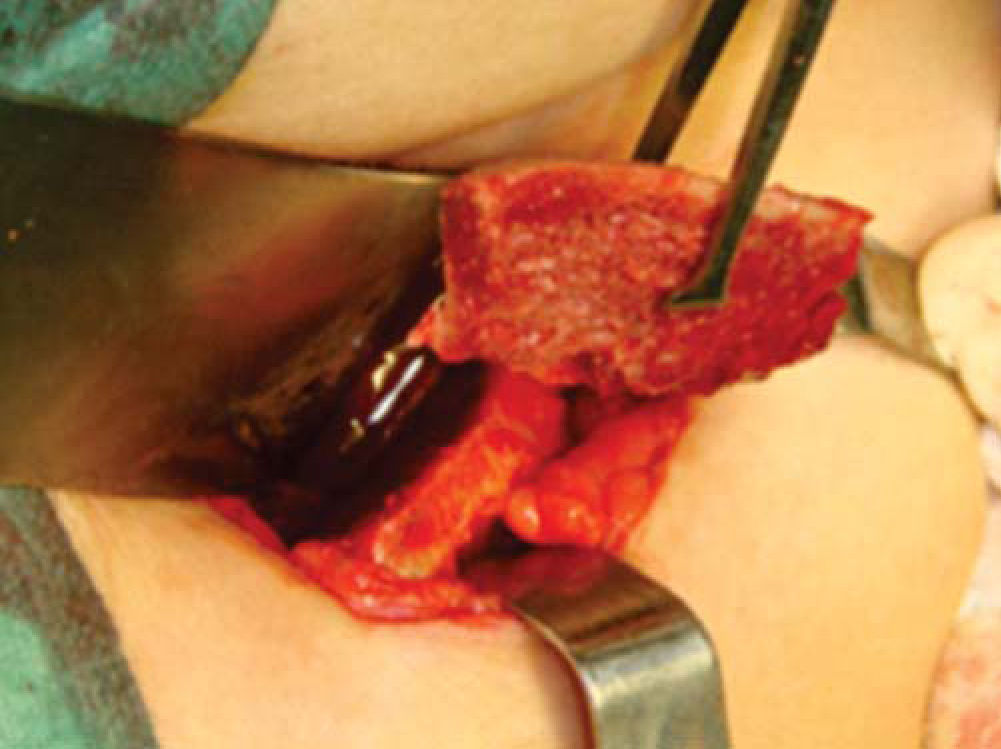
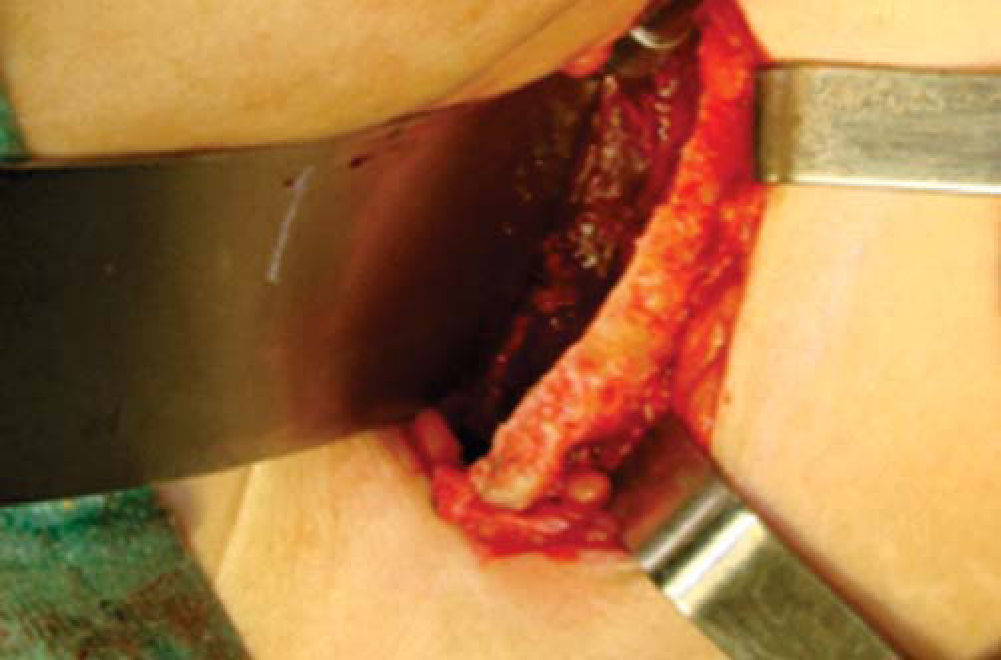
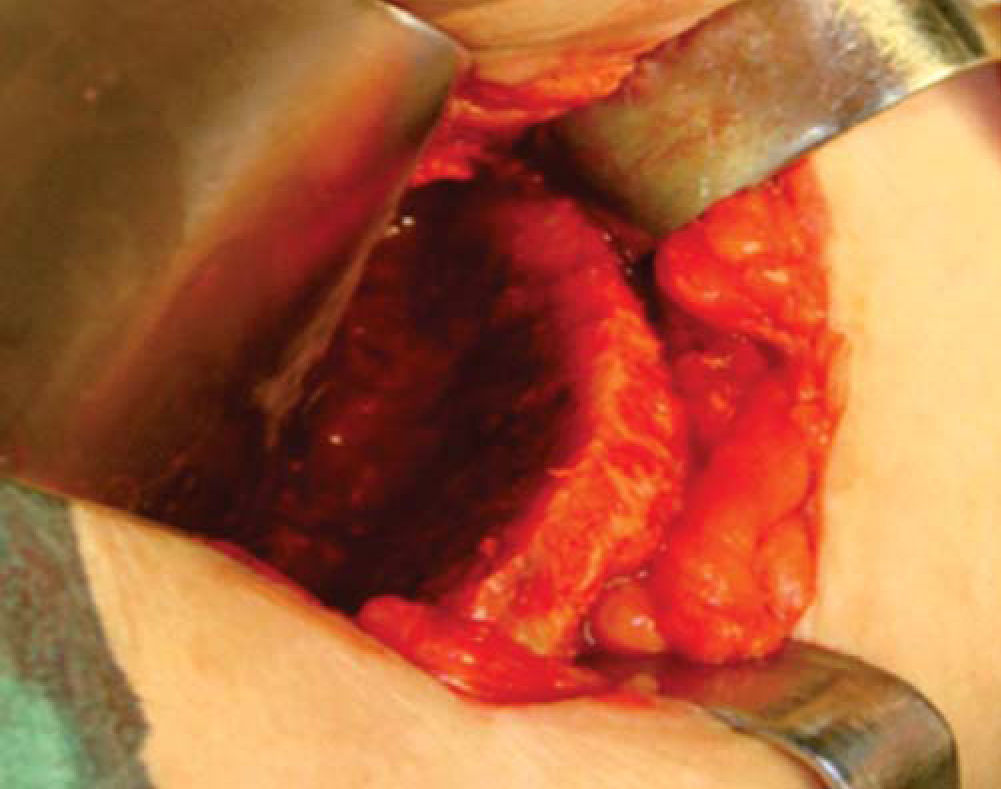
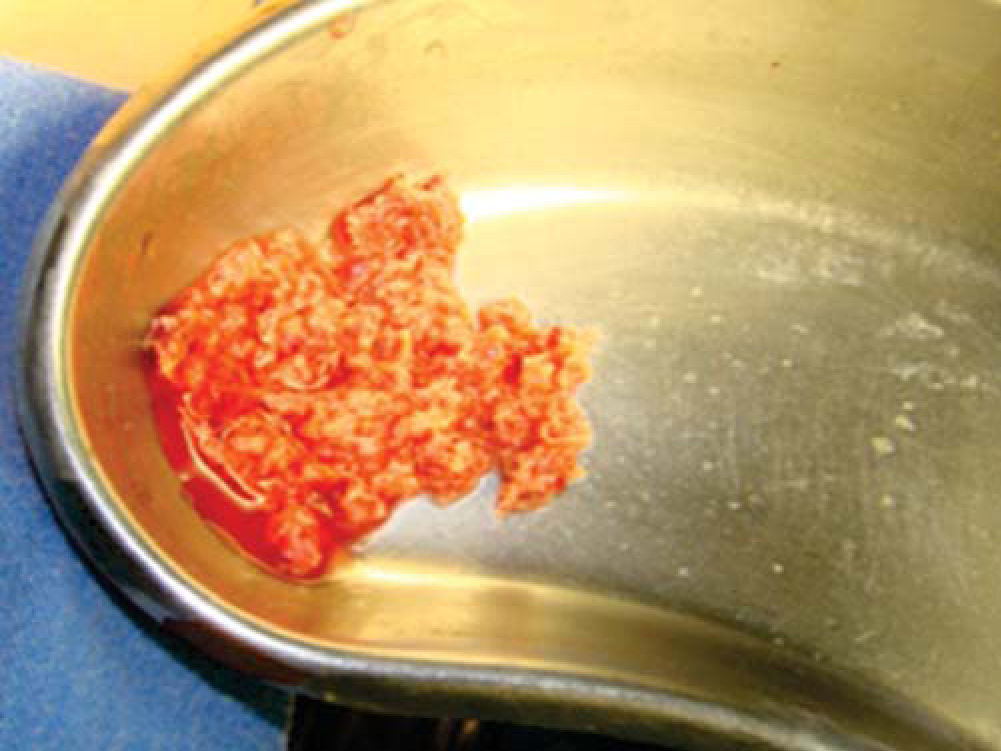
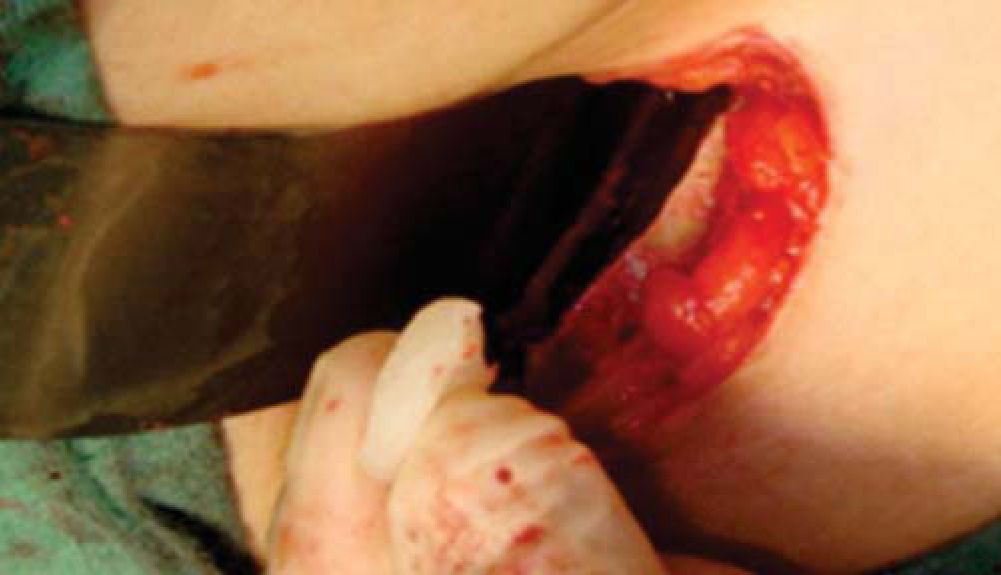
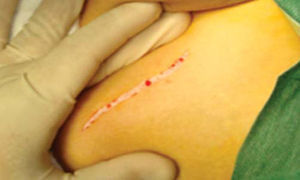
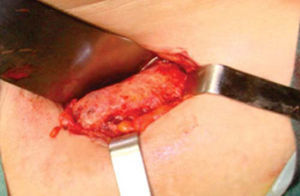
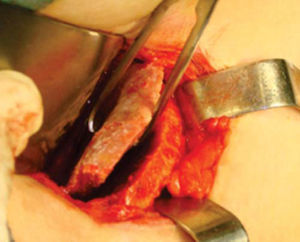
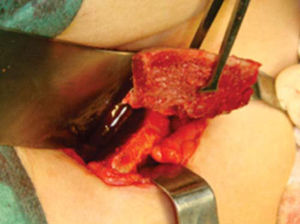
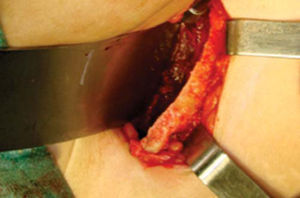
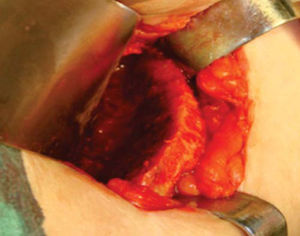
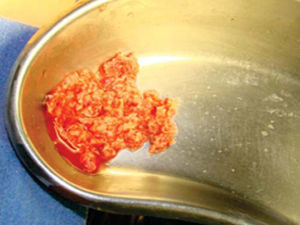
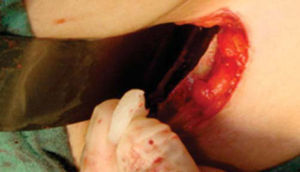
Técnica quirúrgicaEl procedimiento se realiza bajo anestesia general balanceada, iniciando con la toma de injerto de cresta iliaca anterior siguiendo la técnica de Kalk, tomando bloque corticoesponjoso con cierre reciprocante, cincel recto y curvo; el hueso esponjoso adicional se toma con curetas. Teniendo el injerto se realiza hemostasia mediante la colocación de cera para hueso9,13 (Figuras 4 a 11).
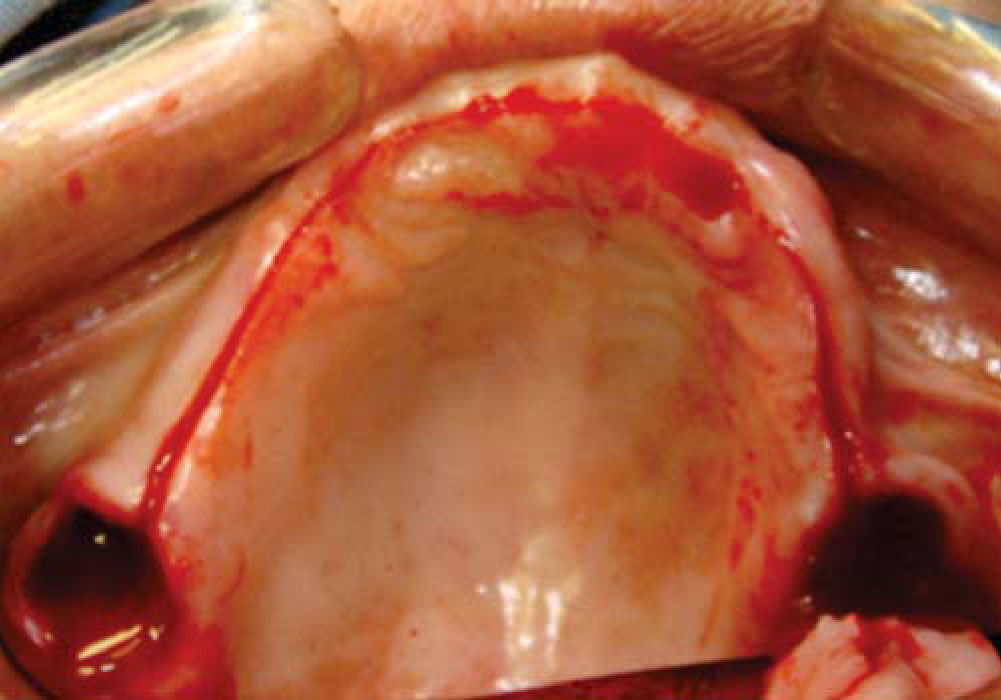
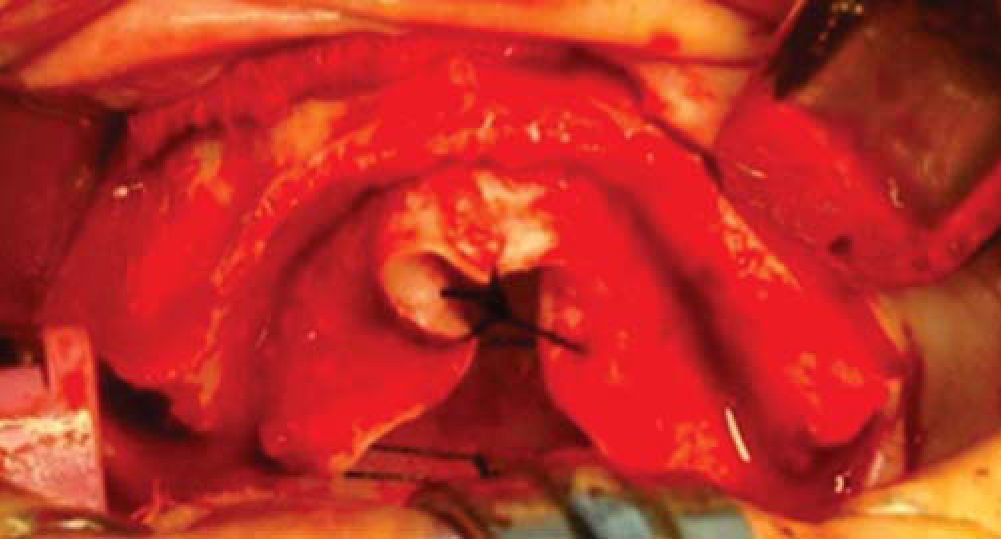
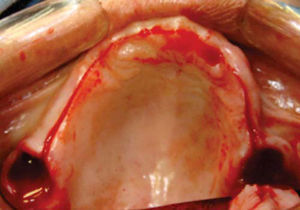
Inmediatamente se realizan odontectomías de órganos dentales residuales conservando el alvéolo, así como una incisión lineal mucoperióstica a la cual se le colocan puntos de suspensión con sutura seda 3-0 en la mucosa platina (Figuras 12y13).
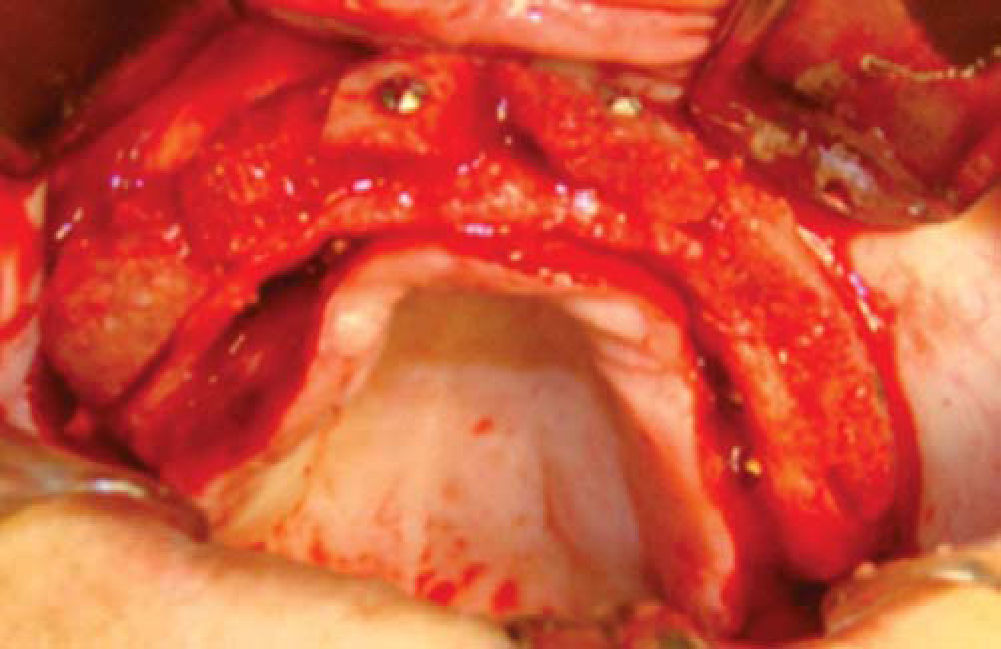
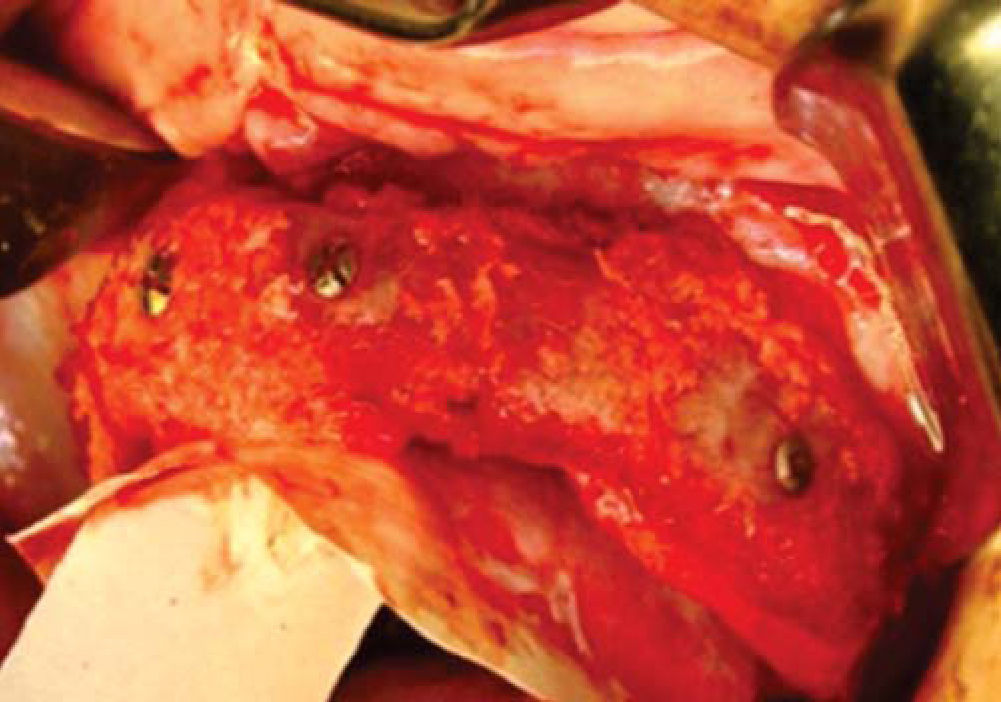
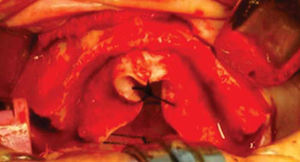
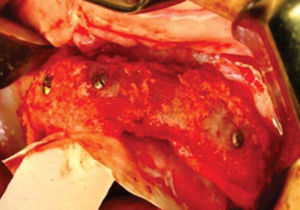
Una vez expuesto el proceso alveolar se realiza decorticación de cortical vestibular, así como de una pared del injerto, colocando los bloques de injerto tipo onlay, sujetándolo con tornillos de 1.5mm de diámetro y 10mm de largo para fijación; el material de osteosíntesis fue colocado en dirección vestibular del injerto a proceso alveolar; al realizar este procedimiento a nivel de la región canina donde está la parte más curva del proceso maxilar algunos bloques del injerto comenzaron a fracturarse por lo que se cambió la dirección de éstos, iniciando por la cara palatina, evitando con esto la pérdida de algunos bloques (Figura 14).
Teniendo la fijación de los bloques se coloca injerto esponjoso para realizar la conformación anatómica del proceso alveolar, se coloca una membrana de colágeno de 0.3mm como conformador y mantenedor de hueso esponjoso (Figura 15).
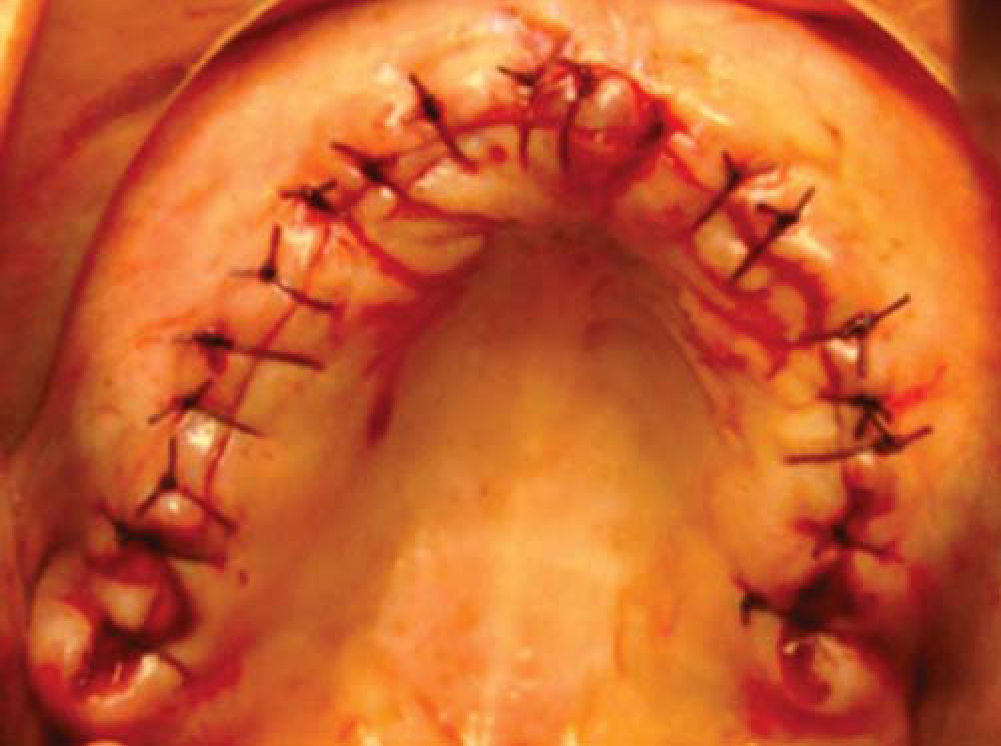
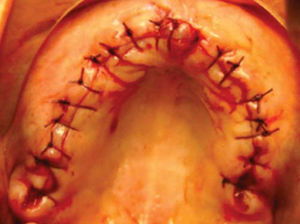
Una vez fijado el injerto en bloque así como el esponjoso y la membrana de colágeno, se realiza elevación de mucosa vestibular quitando tensión en el periostio para tener un cerrado mucoso sin tensión ni exposición del injerto suturando con puntos simples (Figura 16).
La paciente cursa postoperatorio sin complicaciones en herida de cresta iliaca e intraoral, por lo que se coloca prótesis temporal con acondicionador de tejidos (Figura 17).
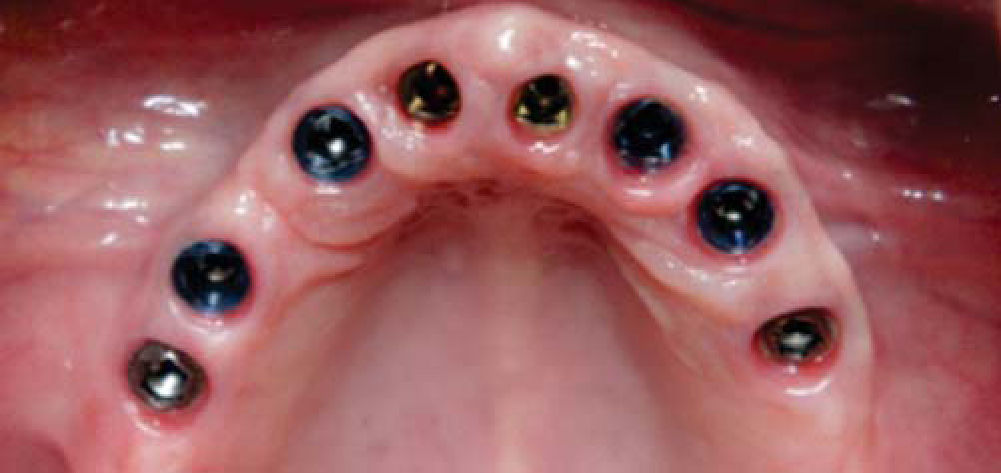
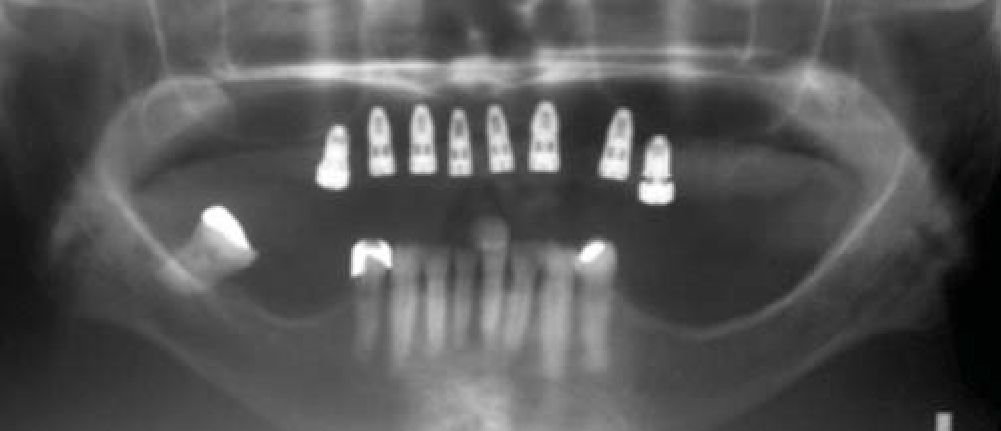
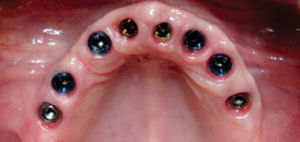
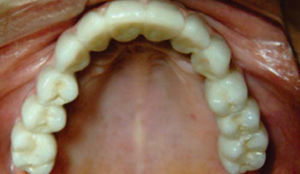
Con los anteriores procedimientos, se obtiene a los seis meses un proceso alveolar lo suficientemente amplio en longitud y en espesor (Figura 18), permitiendo la colocación de ocho implantes intraóseos (Figuras 19y20).
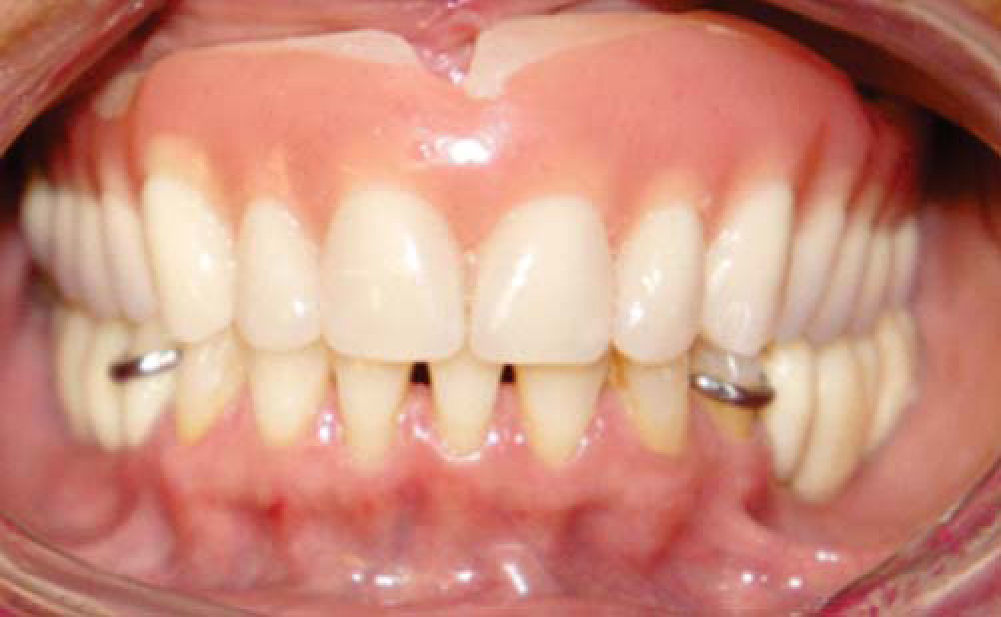
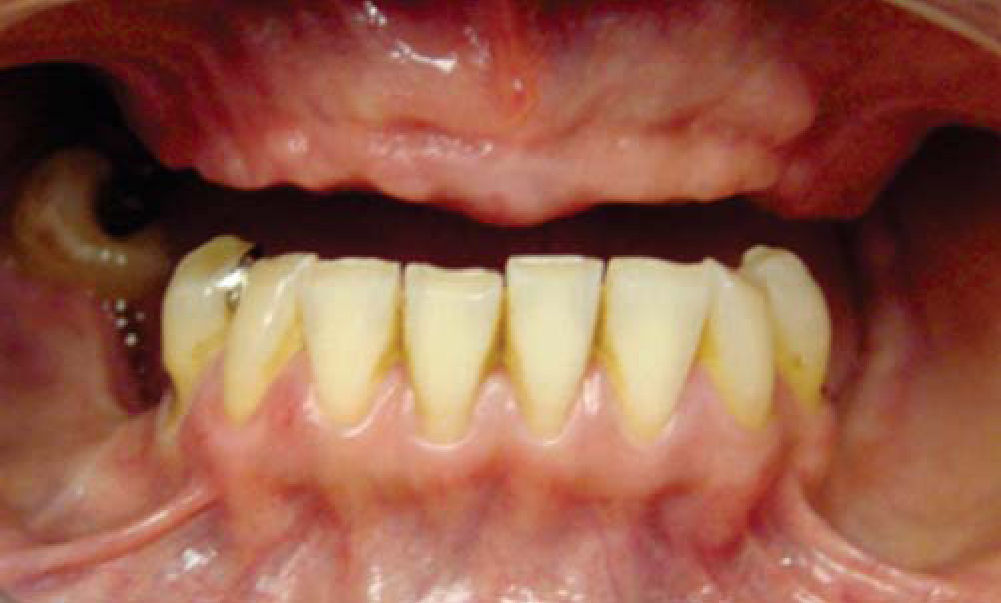
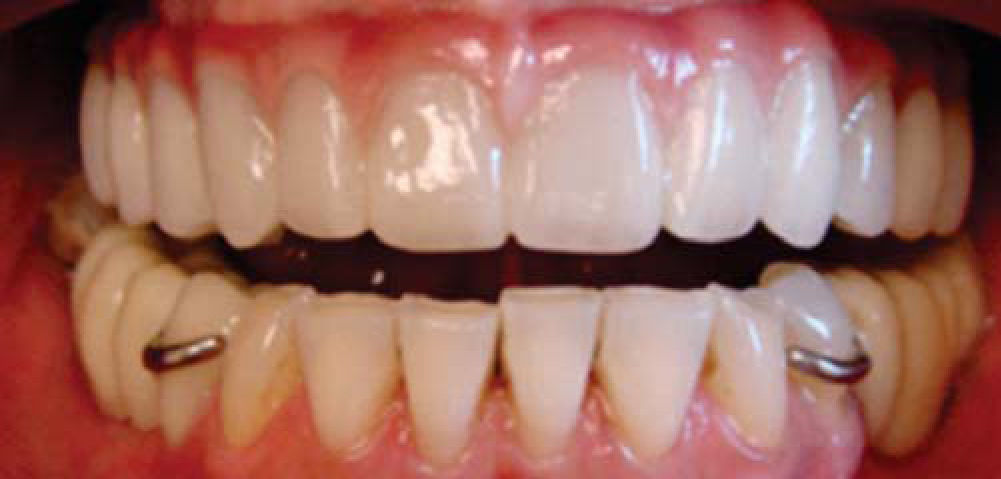
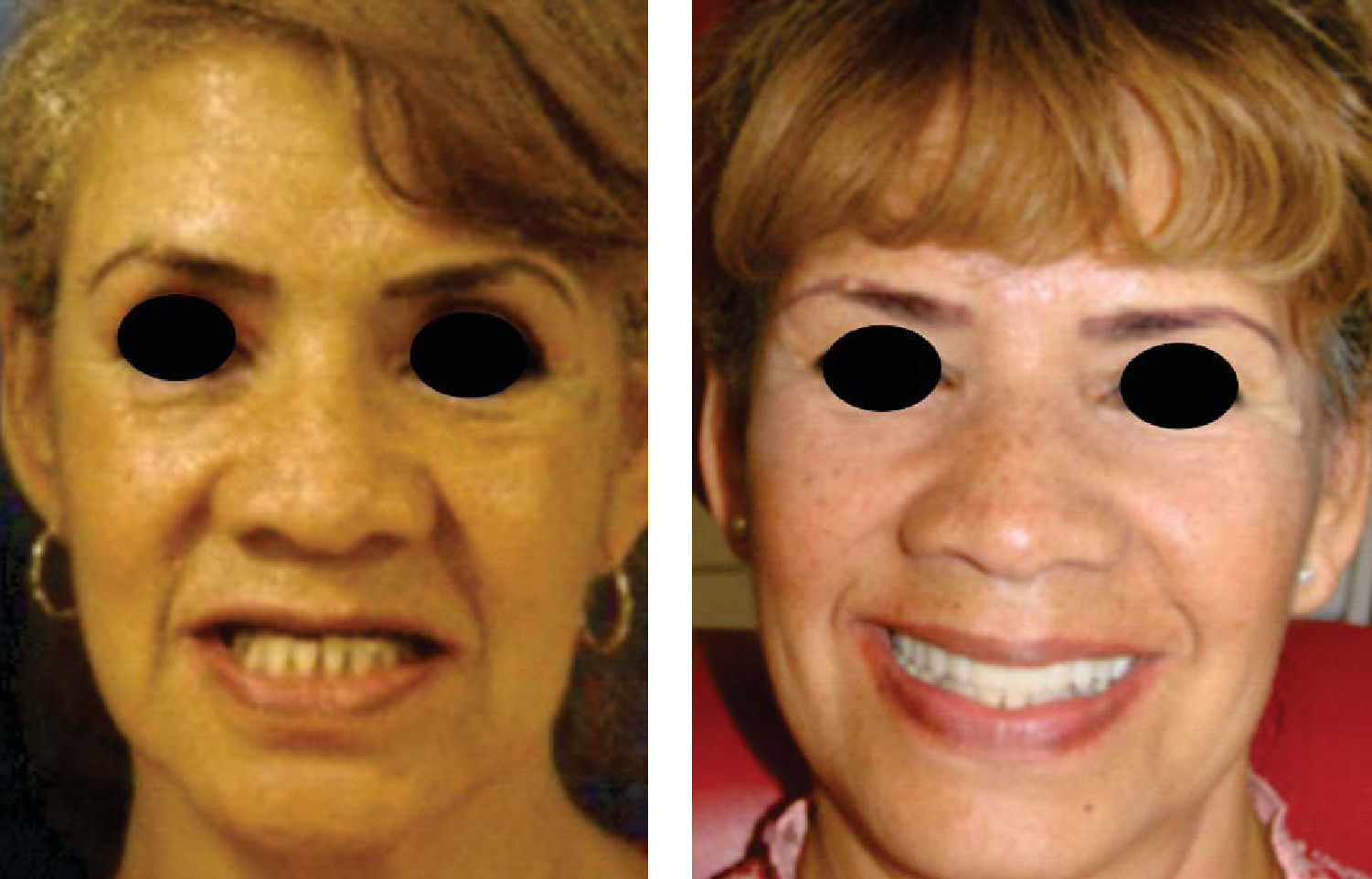
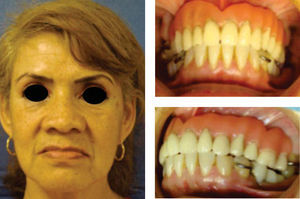
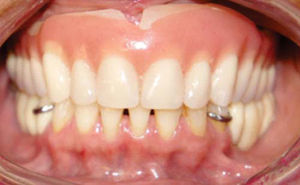
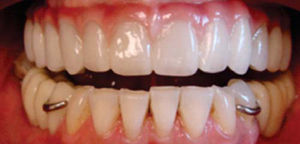
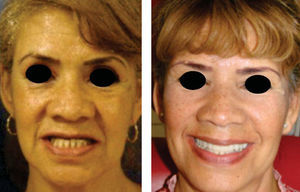
Después se coloca una prótesis fija total implanto soportada de zirconio-cerámica con una evolución de cuatro años, reconstruyendo el proceso alveolar en altura como en espesor a largo plazo, cumpliendo el objetivo quirúrgico así como las expectativas estéticas de la paciente (Figuras 21 a 23).
DiscusiónLa reconstrucción del proceso maxilar atrófico desdentado con injerto de hueso autólogo y colocación de implantes endoóseos, es hoy en día un tratamiento bien establecido con un buen pronóstico.14–16
Este procedimiento está ampliamente reportado en la literatura; Sjöström y colaboradores17 reportan que el injerto de cresta iliaca anterior tipo onlay es el más utilizado, ya que nos permite tomar una gran cantidad de hueso cortical y esponjoso requerido para la reconstrucción del maxilar desdentado atróficamente, siendo un sitio donante casi sin complicaciones para su obtención.14–17 Estos factores hacen que la cresta iliaca anterior sea la primera opción para la toma de injerto en la reconstrucción maxilar.16–19
Cuando es trasplantado el hueso de una zona donadora a otra en un mismo individuo se inician varios procesos durante la integración del injerto que para que se lleve a cabo depende del contacto entre ambos.13,14,17,19
Para que la integración sea adecuada, deberán ocurrir ciertas condiciones como: actividad proliferativa de células osteoprogenitoras, diferenciación celular, osteoconducción, osteoinducción y las propiedades bioquímicas del injerto y el lecho receptor. El mecanismo de integración en el hueso cortical y medular es similar; no obstante, existen algunas diferencias.19,20
El injerto medular contiene un gran número de células hematopoyéticas, elementos vasculares, grasa medular, y un número significativo de células en la superficie trabecular o cerca de ella que puede sobrevivir en el injerto contribuyendo directamente a la respuesta osteogénica del injerto óseo sobre el lecho receptor; sin embargo, una gran cantidad de componentes se necrosan.17–19
La revascularización del trasplante medular puede ocurrir en horas dando como resultado anastomosis de los vasos del huésped al trasplante. En el tejido medular trasplantado las células osteogénicas se diferencian primero en osteoblastos, que se alinean en las trabéculas, depositando tejido osteoide.18–20
Las diferencias básicas entre la reparación del injerto cortical y medular son; a) la velocidad de revascularización es mayor en el injerto medular, b) la iniciación de actividad osteoclástica y osteoblástica es mayor en el injerto medular y c) el injerto medular tiende a ser reparado con el tiempo y el cortical permanece como una mezcla de sustancias necróticas y hueso variable.19
Múltiples estudios describen tres técnicas principales para la reconstrucción ósea: onlay, de interposición maxilar con Lefort I y elevaciones de seno maxilar, con un éxito de tratamiento bastante alto.2,3,13,14
Un punto de controversia en diferente literatura es la técnica de colocación de implantes con el injerto en una sola fase, o en un segundo tiempo quirúrgico. Existen mejores resultados reportados cuando el procedimiento es realizado en dos etapas, teniendo una tasa más alta de supervivencia (88%).16,18–20
Una de las razones de esta diferencia es probablemente que en la técnica de dos fases la revascularización del injerto es mejor que con el trauma quirúrgico generado en la colocación de implantes. También tiene la ventaja de mejor planeación para la rehabilitación posterior.1,3,4,7
Estos resultados cambian gradualmente en la literatura, teniendo cada vez más éxito en la terapia de reconstrucción y colocación de implantes mediante técnicas híbridas.14–16,18