Introducción
El síndrome de apneas-hipopneas del sueño (SAHS), es una enfermedad bien definida, con una prevalencia conocida, y unos factores clínicos y fisiopatológicos bien caracterizados, con un tratamiento eficaz, y cuyas consecuencias e historia natural están siendo cada vez más clarificados. Forma parte de un amplio espectro de trastornos respiratorios del sueño, entre los cuales existiría un solapamiento de los factores implicados.
Existen pacientes en los que en los estudios respiratorios del sueño se objetiva un predominio de eventos centrales. Estos pueden ser consecuencia de una respiración de Cheyne-Stokes, secundaria a insuficiencia cardíaca, o también descritos en enfermos con patologías cerebrovasculares. En ocasiones no se evidencia ninguna alteración subyacente que justifique su presencia, y se catalogan como de origen idiopático. La aparición de eventos centrales y respiración periódica, no solo durante el sueño, sino también en vigilia, están documentados en la respiración a gran altitud y también con relación a tratamientos con opiáceos.
Se describe asimismo la aparición de eventos centrales durante el ajuste de la presión positiva continua en las vías aéreas (CPAP) para el tratamiento del síndrome de apneas del sueño, denominándose a dicha situación complex sleep apnea syndrome (CompSAS), o «síndrome complejo de apneas del sueño».
El síndrome de apneas-hipopneas del sueño es la entidad mejor conocida del espectro de trastornos respiratorios del sueño, considerado como un problema de salud pública, dada la importante prevalencia en la población general, su contribución en la comorbilidad y mortalidad, sobre todo con relación a enfermedades cardiovasculares y cerebrovasculares. La aplicación de CPAP es un tratamiento eficaz, a presiones óptimas, para evitar el colapso de la vía aérea, al conseguir una mejoría sintomática, de la calidad de vida y del pronóstico de los pacientes1.
El objetivo de realizar ajuste de presión de la CPAP es encontrar la presión mínima eficaz para revertir y evitar el colapso de la vía aérea superior durante toda la noche, en diferentes estadios de sueño y posiciones corporales, y conseguir la normalización de la arquitectura del sueño. Existen varias alternativas para conseguir la presión más adecuada. Hasta hace poco, se recomendaba únicamente el ajuste de la presión mediante una polisomnografía (PSG) convencional, pero dados los problemas de listas de espera y su complejidad, se ha validado el ajuste mediante polisomnografía en noche partida (split-night). Actualmente se posibilita el ajuste de presión mediante dispositivos de autoCPAP, con lo que se simplifica y facilita enormemente este proceso.
El ajuste de presión realizado mediante poligrafía, en el que se tienen en cuenta características clínicas y antropométricas del paciente2, es más controvertido, así como la indicación de una presión de forma empírica. Existen varios estudios que comparan las diversas alternativas, en los que no se encuentran diferencias significativas3,4. El ajuste de presión mediante PSG estaría fundamentalmente indicado en los pacientes que no responden al tratamiento.
Los pacientes con apnea-hipopneas de sueño se caracterizan por presentar de forma predominante o exclusiva eventos obstructivos. En muchos pacientes, lo habitual es encontrar todo el espectro de los diversos eventos respiratorios, obstructivos, mixtos y centrales.
Durante el ajuste de presión, la presencia de eventos centrales o respiración periódica de Cheyne-Stokes supone una dificultad para optimizar presiones. Es más, en algunos pacientes con SAHS obstructivo, la aplicación de presión positiva continua durante la realización del ajuste de presión es la que provoca los trastornos de tipo central. Muchos autores, conscientes de esta «complejidad», han definido este trastorno como complex sleep apnea, o apneas complejas durante el sueño5,6. Su reconocimiento abre un debate acerca de su naturaleza: enfermedad propiamente definida7, frente a un epifenómeno del SAHS, sin implicaciones más allá de su mera identificación8.
Clasificación y fisiopatología de apneas centrales
El síndrome de apneas centrales se caracteriza por la presencia de pausas respiratorias, de más de 10 segundos de duración, identificadas por ausencia de flujo, en las que no existe actividad o esfuerzo de la musculatura respiratoria. Las apneas centrales se pueden clasificar en alguno de los siguientes grupos9,10:
1. Síndrome de apneas centrales hipercápnicas: respuesta atenuada del control respiratorio frente al CO2. Fallo o insuficiencia de la bomba ventilatoria, o depresión del impulso respiratorio central. Se encuadra dentro de un espectro de patologías con hipoventilación alveolar11.
- síndrome de hipoventilación central,
- enfermedad pulmonar obstructiva crónica (EPOC). Enfermedades neuromusculares. Alteraciones restrictivas toracógenas, etc.
2. Formas no hipercápnicas: existe una inestabilidad intermitente del control respiratorio con una respuesta excesiva frente al estímulo del CO2. Respiración periódica y respiración de Cheyne-Stokes, esta última entendida como un tipo de respiración periódica con apneas centrales.
- síndrome de apneas centrales idiopático,
- insuficiencia cardíaca,
- respiración periódica por altitud,
- acromegalia,
- insuficiencia renal,
- secundarias a enfermedad cerebrovascular y tratamiento con derivados opiáceos,
- en este grupo se pueden incluir las apneas relacionadas con el CompSAS y las formas de eventos centrales que aparecen en pacientes con SAHS predominantemente obstructivo, que podrían ser consecuencia de una disfunción de los quimiorreceptores respiratorios.
Los mecanismos implicados en la génesis de eventos centrales es más complejo que en las apneas obstructivas. De una manera muy simplista, la ausencia de contracción de los músculos respiratorios puede ser consecuencia de una reducción o déficit en el estímulo central por alteración de los centros respiratorios, o una alteración de los músculos respiratorios en sí, que es la base del origen de las formas hipercápnicas. Por el contrario, en las no hipercápnicas, existe una inestabilidad del control respiratorio, en el que aparece un incremento del estímulo respiratorio que provoca episodios de hiperventilación, con hipocapnia secundaria, que es lo que originaría la apnea central en el caso de sobrepasar un valor de PaCO2 umbral (umbral de apnea)12-14.
Durante el sueño, tras la ausencia del estímulo respiratorio tónico y estabilizador que ejerce la vigilia, los mecanismos de la regulación respiratoria están sujetos principalmente al sistema de control metabólico o automático, dependiente de quimiorreceptores periféricos y centrales, que es más patente sobre todo en el sueño no REM, al comienzo del sueño, y en los períodos de transición. Existe por tanto, durante estos períodos, una desestabilización de la regulación respiratoria hasta que se alcanza un nuevo punto de equilibrio. Se produce finalmente una tendencia fisiológica a una discreta elevación de la PaCO2.
Para mantener los valores de PaCO2 en unos márgenes estrechos, el sistema de control respiratorio se regula mediante un sistema de reflejos de retroalimentación (feed back loops), a través de los quimiorreceptores y mecanorreceptores. Este mecanismo de retroalimentación tiene el potencial de volverse inestable, lo que se explica en términos mecanicistas como ganancia de un sistema (loop gain). Si la ganancia es alta, el sistema responde de forma rápida e intensa a una pequeña perturbación; por el contrario, si la ganancia es baja, el sistema responde de forma más lenta y débil. Las variables que definen la ganancia de este sistema de control-retroalimentación, son por una parte la quimiosensibilidad (quimioreponsiveness) es decir, la repuesta al estímulo hipóxico/hipercápnico (controller gain) y, por otra, la efectividad de un nivel dado de ventilación (funcionamiento de la bomba ventilatoria) para eliminar CO2 (plant gain)15,16.
En la generación de las apneas centrales y la respiración periódica durante el sueño, se deben dar una serie de circunstancias. El factor básico es la inestabilidad transitoria del control respiratorio, asociada a una fluctuación en el sistema nervioso central que impide una rápida estabilización del sueño. Estos dos elementos interactúan entre sí, condicionados por factores que perpetuarían la inestabilidad17. Dependiendo del tipo básico de apneas centrales predominan unos factores u otros de los siguientes:
1. Hipocapnia. Se ha objetivado en los sujetos con apneas centrales una PaCO2 más reducida que en los controles. Esta hipocapnia mantenida acercaría los niveles de la PaCO2 al umbral de apnea.
2. Arousals. Los despertares o microdespertares producen una hiperventilación que desestabiliza la respiración, reduciendo la PaCO2. Además, la misma hiperventilación con la consiguiente fluctuación de los gases, produciría un arousal. Existiría, asimismo, un umbral para la generación de arousal que condicionaría una mayor o menor susceptibilidad para su aparición.
3. Incremento de la respuesta de los centros respiratorios a los estímulos reflejos de los quimiorreceptores/mecanorreceptores, o un aumento de su sensibilidad. Es decir, como se comentó previamente, una elevada ganancia del sistema.
4. Hipoxia. Al estimular la ventilación, reduciría la PaCO2 de forma suficiente como para sobrepasar el umbral de apnea.
5. Retardo en la señal de retroalimentación: tiempo de respuesta aumentado (long circulation time). Se supone que está más directamente relacionado con la duración de los ciclos de apnea-hiperpnea, y contribuye al patrón respiratorio crescendo-decrescendo.
La patogénesis de las apneas centrales en pacientes con insuficiencia cardíaca es mejor conocida18. La congestión pulmonar produce un estímulo de los mecanorreceptores, incrementando el estímulo respiratorio, que junto con la hipoxia (en caso de presentarse), favorecería la hipocapnia. Además existe un incremento del tono simpático, y un tiempo circulatorio alargado19,20.
Sin embargo, la frontera entre las apneas centrales y las obstructivas no es tan nítida, dado que en ambas formas existe una inestabilidad del control respiratorio. Asimismo el cese de estímulo respiratorio que caracteriza las apneas centrales afecta también la actividad de los músculos faríngeos, observándose un estrechamiento de la vía aérea21. Las apneas mixtas pueden ser la consecuencia de este fenómeno, en pacientes con unos factores anatómicos con tendencia a una mayor colapsabilidad. Un ejemplo más de la interacción entre los factores que favorecen la aparición del colapso de la vía aérea y la inestabilidad de los centros respiratorios es el hecho de que en algunos sujetos se ha observado una tendencia a lo largo de la noche del cambio de predominio de apneas obstructivas hacia formas centrales22.
Fletcher describió un paciente que, tras la realización de traqueostomía para el tratamiento de apneas obstructivas, desarrolló apneas centrales. Se puso en evidencia por primera vez la complejidad que subyace en el espectro de los eventos respiratorios del sueño23.
Thomas et al reconocen la aparición de un patrón de inestabilidad respiratoria asociada a obstrucción de la vía aérea, que se manifiesta durante el ajuste de presión de la CPAP, y que aparece típicamente en fases no REM, asociándose a dificultades en el ajuste de una presión óptima y por tanto, a la persistencia de sintomatología a pesar del tratamiento con CPAP24. Existiría un patrón cíclico alternante en el sueño no REM, consistente en un patrón bifásico de arousal transitorio (fase A), que de forma periódica interrumpe una actividad tónica delta/theta del sueño no REM (fase B). Este patrón (CAP o cyclic alternating pattern) estaría asociado a una mayor probabilidad de arousal. Los sujetos con un patrón CAP dominante tendrían más tendencia a desarrollar apneas centrales, en contraste con los pacientes con un patrón REM dominante, que tendrían una mayor estabilidad.
La patogénesis de las apneas centrales emergentes con CPAP no se conoce, pero se considera que estaría basada en la inestabilidad del control ventilatorio, condicionado por una elevada sobrerrespuesta correctora en los mecanismos de compensación (loop gain). Existe un diferente comportamiento según los estadios de sueño, predominando en no REM. Se postulan varias hipótesis8,25:
1. Cambios en la eliminación de CO2 tras resolución de las apneas obstructivas. La resistencia aumentada de la vía aérea superior podría haber producido una desensibilización del sistema de control ventilatorio, dificultando la eficiencia en la eliminación de CO2. Con la aplicación inicial de CPAP, mejoraría la ventilación tras reducir la resistencia, facilitando una caída de la PaCO2 por debajo del umbral de apnea, que ocasiona la aparición de eventos centrales. Tras el transcurso de varias semanas con CPAP, se produciría una estabilización de los centros respiratorios con la normalización de la respuesta al CO2 y, por tanto, la desaparición de eventos centrales. Un fenómeno similar se ha descrito en la respiración a gran altitud así como tras traqueotomía.
Sin embargo, recientemente se ha demostrado que los pacientes con SAHS presentan una menor reserva de CO2 y una mayor sensibilidad frente a cambios del CO2 (controller gain), que en sujetos normales. El tratamiento con CPAP durante un mes resultó en una normalización de ambas alteraciones, lo que sugiere que las apneas centrales emergentes con CPAP podrían estar causadas por un incremento reversible de la quimiosensibilidad a la hipocapnia26.
2. Sobreajuste de presión de CPAP. Por estimulación de receptores de estiramiento que inhibirían el estímulo ventilatorio (reflejo de Hering-Breuer). Por otra parte, existiría un lavado del CO2 del espacio muerto anatómico si se produjeran fugas orales por presión de CPAP excesiva. El ajuste de presión mediante la aplicación de presión a dos niveles (BIPAP) aumenta la ventilación, reduciendo más si cabe la PaCO227,28.
3. El inicio de la aplicación de CPAP puede empeorar la calidad de sueño, de forma que una mayor inestabilidad y fragmentación del mismo, con períodos de transición más frecuentes de vigilia-sueño, facilitarían también la aparición de apneas centrales. En este caso la hiperventilación que se produce como respuesta al arousal, reduciría la PaCO2 por debajo del umbral de apnea29. Por otra parte, la aplicación de la CPAP suprime la elevada resistencia de la vía aérea superior, por lo que la respuesta ventilatoria al arousal estaría aumentada.
Epidemiología y diagnósticoAunque el concepto del CompSAS es simple (la CPAP elimina los eventos obstructivos, pero persiste un índice de eventos centrales residual elevado) su determinación en la práctica reviste cierta dificultad, debido a que no existe una definición exhaustiva y consensuada, tampoco un método diagnóstico completamente validado. La confirmación del origen central de los eventos respiratorios requiere determinar las presiones esofágicas, lo que resultaría inviable en la práctica clínica rutinaria, utilizándose solo en el ámbito de la investigación. Se han propuesto otras técnicas diagnósticas, como la determinación del tiempo de tránsito de pulso (pulse transit time), o métodos basados en diferentes fenotipos detectados por espectrografía electrocardiográfica, que parecen diferenciar los eventos obstructivos, centrales y complejos30,31.
Generalmente se establece en la mayoría de los estudios un punto de corte de 5 apneas centrales residuales por hora (índice de apneas centrales por hora [IAC > 5]), o la aparición de un patrón de respiración periódica de Cheyne-Stokes persistente, que sea claramente patológico. Se han diferenciado varios tipos de CompSAS: aquellos que aparecen durante el ajuste de presión antes de iniciar CPAP pero que persisten tras la aplicación de esta, y las que aparecen tras el inicio de CPAP (apneas centrales emergentes). Además hay que tener en cuenta que en muchos casos las apneas centrales mejoran tras varias semanas de tratamiento con CPAP, es decir, que podría ser un fenómeno transitorio, mientras que en otros casos persistirían de forma indefinida32.
Otra de las limitaciones en el diagnóstico del síndrome de apneas complejas es la dificultad en la caracterización de las hipopneas centrales. Aunque la naturaleza obstructiva, central o mixta de las apneas se determina con más claridad, no ocurre lo mismo con las hipopneas, lo que limita la detección de formas más leves de CompSAS.
Los métodos diagnósticos y de ajuste de presión podrían condicionar el diagnóstico de CompSAS. Los estudios de noche partida no ofrecen una visión completa de lo que ocurre durante toda la noche, como la posibilidad de un viraje de eventos obstructivos a centrales, y además podrían inducir de forma iatrogénica apneas centrales al producir una mayor disrupción del sueño, con la aparición de arousal, y por lo tanto mayor fluctuación de la PaCO2. Puede condicionar un infra ajuste de presión o por el contrario un sobre ajuste, con aparición de fugas orales, perpetuándose así un círculo vicioso con más arousals, lo que impediría finalmente la consecución de una presión óptima que resolviera todos los eventos respiratorios. En los estudios de ajuste de presión en noche completa un incremento más progresivo de la presión a lo largo de la noche podría alterar menos el sueño, sobre todo si es diferido tras un tiempo de adaptación a una presión empírica.
La prevalencia de las apneas complejas, por tanto, varía en diferentes trabajos, como consecuencia de los distintos criterios y métodos diagnósticos (ajuste de presión en noche partida o completa, protocolo de ajuste de presión, utilización de la señal de cánula nasal, etc.), diseños de los estudios y poblaciones de estudio.
Uno de los primeros trabajos que analizan los patrones respiratorios durante la aplicación de CPAP objetivó en 25 de 40 pacientes alteraciones consistentes en apneas centrales, hipopneas, respiración periódica y desaturaciones prolongadas33.
Morgenthaler et al en un estudio retrospectivo de 233 pacientes, utilizando PSG y ajuste de presión en noche partida, encontró una prevalencia de CompSAS del 15%, frente al 84% de apneas obstructivas y 0,4% de apneas centrales idiopáticas34. Lehman et al, en 99 sujetos diagnosticados de SHAS, detectaron en los estudios de ajuste de presión un 13% de sujetos con CompSAS35. En otro estudio retrospectivo, Pusalavidyasagar et al, utilizando también ajuste de presión en noche partida, detectan una prevalencia del 20,4%36.
Dermaika et al, empleando la titulación en noche partida, encontraron una prevalencia del 19,8%29. Johnson et al revisaron PSG en pacientes en tratamiento con BIPAP por apneas centrales y objetivaron un empeoramiento de estas en el 34% de los pacientes28.
El trabajo más importante hasta la fecha que intenta determinar la prevalencia de las apneas complejas fue realizado por Javaheri et al recientemente37. Se trata de un estudio retrospectivo de 1.288 pacientes con SAHS. En el estudio de ajuste de presión mediante PSG en noche completa, se detectaron 84 pacientes con apneas centrales (6,5%). Tras un segundo estudio de ajuste de presión en 42 pacientes, el índice de apneas centrales por hora continuaba elevado (IAC > 5/hora) en 9 sujetos, por lo que estimaron que la prevalencia de las apneas centrales persistentes estaría en torno al 1,5%.
En una población japonesa de 1.312 sujetos con SAHS a los que se realizó estudio de ajuste de presión, se encontró una prevalencia del 5%38. En otro estudio japonés posterior, se objetivaron apneas centrales persistentes o emergentes en el 5,7%, tras estudio de ajuste de presión mediante PSG en 297 sujetos39.
En todos los trabajos se objetiva un claro predominio en varones, hasta el 81%34. Este predominio podría explicarse por una respuesta ventilatoria más elevada en los arousal transitorios en sueño no REM40 y una mayor respuesta ventilatoria a la hipercapnia en vigilia. La combinación de esta respuesta incrementada, combinada con un bajo umbral de apnea al CO2, así como un sueño más fragmentado y superficial que en las mujeres, justificaría la mayor susceptibilidad en varones.
Implicaciones clínicas
Existe controversia sobre la repercusión de las apneas complejas. Mientras algunos autores consideran que se trata de un fenómeno inocuo, infrecuente y transitorio, y que no precisa de un manejo terapéutico específico, otros mantienen que se trata de una enfermedad con unas implicaciones clínicas importantes. En las apneas centrales que se manifiestan como consecuencia de la insuficiencia cardíaca, se ha demostrado claramente su papel deletéreo en el pronóstico de estos pacientes, y el beneficio del tratamiento específico. Por ello, al objetivarse eventos centrales en pacientes en tratamiento con CPAP, lo primero que se debe considerar es si existe alguna cardiopatía subyacente. Por otra parte es necesario tener en cuenta la medicación del paciente, sobre todo si toma opiáceos, y la presencia de otras enferme dades, especialmente del sistema nervioso central, y hepá ticas.
Se han identificado posibles factores predictores. Los pacientes con CompSAS presentan un índice de apneahipopnea (IAH) más elevado con mayor número de eventos centrales en el estudio basal (IAC > 5), y una historia de cardiopatía más frecuente35,37. También se ha objetivado una peor tolerancia y cumplimiento de la CPAP41. Aunque otros estudios no encuentran diferencias en el cumplimiento42, sí hallan una somnolencia inicial mayor, una tendencia a un menor índice de masa corporal (IMC), y más problemas referidos con la CPAP.
Pusalavidyasagar et al no pudieron confirmar que los pacientes con CompSAS tuvieran una peor tolerancia a la CPAP y consecuentemente un peor cumplimiento, no encontraron diferencias en el seguimiento respecto a la mejoría clínica o el cumplimiento, aunque presentaron con más frecuencia problemas de mascarillas, sensación de hambre de aire o disnea, y requirieron precozmente atención durante el seguimiento, lo que sugiere mayor dificultad en la adaptación a la CPAP. Sin embargo, este estudio está limitado por el reducido porcentaje de pacientes que finalizaron el seguimiento, tan solo el 35% con SAHS y el 50% con Comp-SAS36.
En varios estudios, los eventos centrales serían en su mayoría transitorios, y se resolverían tras unos 2 meses de tratamiento con CPAP29,37. Si tenemos en cuenta el estudio
CANPAP, aunque se trata de pacientes con insuficiencia cardíaca, tras un seguimiento prolongado, se pudo comprobar la persistencia de eventos centrales a pesar de la CPAP, así como una peor tolerancia a esta43.
Otro problema asociado es que ante la sospecha clínica o la presencia de apneas centrales significativas en el estudio diagnóstico, se desaconseja el empleo de autoCPAP para ajuste de presión44.
Se podría concluir, a la luz de estos estudios, que el síndrome de apneas complejas es infrecuente, que en su aparición influyen la gravedad del SAHS, un elevado número de eventos centrales, tratamiento con opioides y posiblemente, en algunos casos, una cardiopatía subyacente. Son por tanto necesarios más estudios, con un diseño prospectivo y una descripción más rigurosa de las apneas complejas, para definir claramente la historia natural y sus repercusiones clínicas.
Tratamiento
La CPAP es el tratamiento de elección en la apnea-hipopnea obstructiva durante el sueño (SAHS), y es una de las alternativas más estudiadas en los trastornos respiratorios de tipo central, esencialmente en pacientes con insuficiencia cardíaca. Ha demostrado reducir las apneas centrales45, mejorar los síntomas46, la función cardíaca47 y reducir la actividad simpática. Y en algunos trabajos iniciales, como el estudio de Sin et al48, aleatorizado y controlado de 29 pacientes con central sleep apnea (CSA), parece reducir la mortalidad y la necesidad de trasplante.
El estudio CANCAP es el más importante, controlado y aleatorizado realizado hasta la fecha para evaluar los efectos de la CPAP en las apneas centrales del sueño e insuficiencia cardíaca. Concluyó que no existían diferencias con el grupo control en el número de hospitalizaciones, calidad de vida, niveles de péptido natriurético atrial (ANP) ni mostró mejorar la supervivencia, a pesar de que por otra parte mejoraba los eventos centrales, la función cardíaca, la oxigenación nocturna, incrementaba la fracción de eyección (FE), la distancia caminada en 6 minutos y reducía los niveles de norepinefrina. En general, la CPAP reducía el IAH al menos un 50%42. Como resultado de este estudio, la CPAP no se consideraría en la actualidad como un tratamiento estándar de la apneas centrales del sueño, aunque podría ser beneficioso en pacientes con altas presiones de llenado ventricular izquierdo sin fibrilación auricular.
Un análisis posterior de dicho estudio49 sugiere que en el grupo que presentaba una mayor reducción del IAH (por debajo de 15/hora) experimentó un mayor incremento de la FE a los 3 meses y una mejoría significativa de la supervivencia libre de trasplante.
La utilidad de la administración de soporte ventilatorio mediante BIPAP en las formas de apneas centrales hipercápnicas está demostrada; sin embargo, en las formas no hipercápnicas no se considera una alternativa eficaz.
El aporte de concentraciones elevadas de CO2 se ha utilizado para tratar los eventos respiratorios centrales durante el sueño mediante inhalación directa o incrementando el espacio muerto. Ha demostrado que reduce el IAH, aunque se ha observado también la ausencia de mejoría en la calidad del sueño y que podría incrementar la actividad simpática. Recientemente se ha utilizado en combinación con la CPAP, mediante un nuevo método (positive airway pressure gas modulator), que resulta eficaz en controlar eventos respiratorios mixtos y centrales. No obstante, dados los riesgos potenciales de la utilización del CO2, son necesarios más estudios para establecer su indicación50.
En los pacientes con insuficiencia cardíaca y apneas centrales, se está considerando la hipótesis de que los tratamientos que consigan una reducción más efectiva de los trastornos centrales podrían tener un efecto concluyente sobre la supervivencia, lo que permitiría utilizarlos con una mayor evidencia científica en el arsenal terapéutico de la insuficiencia cardíaca. Por otra parte, se demostraría la importancia de realizar estudios diagnósticos dirigidos a detectar estos trastornos respiratorios del sueño de tipo central.
Los pacientes con CompSAS requieren de un tratamiento que combine la estabilización de la vía aérea superior y la disfunción ventilatoria central51. Una de las terapias más prometedoras es la servoventilación (ASV). Esta modalidad de ventilación consiste básicamente en ajustar la respiración del paciente: estabiliza la vía aérea corrigiendo las apneas e hipopneas, y controla la respiración evitando la hiperventilación característica de los trastornos centrales en la respiración periódica. Ha demostrado ser eficaz según estudios iniciales, para mantener un ritmo respiratorio normal durante el sueño, anulando los efectos negativos de los eventos respiratorios. Su particular mecanismo de adaptación a la respiración del paciente hace que sea muy cómodo, lo que implica una mejor adaptación, tolerancia y, por tanto cumplimiento, en comparación con la CPAP, e incluso la BIPAP. En el mercado existen tres dispositivos, el Auto-SetCs (ResMed®), BiPAP Auto SV (Respironics®) y SOMNOvent (Weinmann®). Existe un ensayo clínico en marcha, específicamente diseñado para determinar si la servoventilación mediante VPAP Adapt SV es superior a una presión fija de CPAP en pacientes con CompSAS, cuyos resultados aclararán más el papel de este tipo de dispositivos en estos pacientes52.
La primera descripción de este tipo de terapia ventilatoria fue publicada por Teschler et al53 en 2001, quienes realizaron un estudio cruzado de una única noche, para determinar los efectos agudos en 14 pacientes, comparando el O2, CPAP y VPAP II (ResMed). Este último reducía las apneas centrales un 85% más que la CPAP.
Morgenthaler et al,54 en un estudio aleatorizado y cruzado, comparan la servoventilación frente a BIPAP, en 21 pacientes con SAHS, apneas centrales, mixtas y CompSAS, concluyendo que aunque ambos son eficaces, la servoventilación es más efectiva para controlar los eventos respiratorios y los arousals relacionados con los mismos. El IAH residual fue de 0,8 ± 2,4 con ASV frente a 6,2 ± 7,6 con BIPAP. Randerath et al55 en otro trabajo observacional y prospectivo, en 10 pacientes con coexistencia de SAHS y trastornos respiratorios del sueño de tipo central con o sin insuficiencia cardíaca, demuestran que la ASV reduce el IAH de forma significativa, así como los parámetros de sueño, tras 6 semanas de tratamiento. La ASV suprime de forma efectiva todos los tipos de eventos respiratorios tanto en pacientes con patología cardíaca como sin ella.
En otro trabajo retrospectivo, Allam et al56 presentan los datos de 100 pacientes tratados con servoventilación (VPAP Adpapt, ResMed), un 63% diagnosticados de CompSAS en los que la indicación para ASV fue una respuesta subóptima a CPAP. Entre los hallazgos del estudio, destaca que la BIPAP en modo T incrementa el IAH total, por empeoramiento de eventos centrales. Por el contrario, en modo ST mejora el IAH. La máxima mejoría ocurría con ASV. Mientras la ASV parece igual que BIPAP-ST en CSA, y funciona igual de eficazmente que CPAP en CSA/CSR, en CompSAS la ASV es superior a las otras modalidades. Comparado con CPAP y BIPAP-ST, ASV mejora el porcentaje de REM en todos los grupos, y reduce de forma significativa el índice de arousal; además se objetivó una mejor tolerancia.
Menor evidencia existe en el tratamiento de las apneas centrales idiopáticas y las secundarias al tratamiento con opiáceos. Banno et al57, en un estudio descriptivo de una serie de 3 pacientes con Cheyne-Stokes de carácter idiopático, utilizaron CPAP y O2, sin respuesta, por lo que iniciaron tratamiento con ASV (AutoSet CS, ResMed). Se objetivó una mejoría clínica, con mejor tolerancia, y una reducción de los eventos respiratorios (IAH de 35 a 3,5), tras 6-12 m eses los pacientes mantienen una mejoría significativa de la somnolencia.
Kuzniar et al58, en un estudio retrospectivo de 115 pacientes, 44% con insuficiencia cardíaca, proponen un protocolo de ajuste de presión específico en aquellos sujetos en los que en el estudio PSG aparecen eventos centrales, consistente en probar en la misma noche diferentes modalidades terapéuticas que evitan la necesidad de realizar nuevos estudios, con el consiguiente ahorro. La servoventilación fue la terapia que mostró un mayor éxito (78%). Consideran que una respuesta inicial insuficiente a la CPAP es predictiva de un inadecuado control a largo plazo.
Otras alternativas que se han empleado en el tratamiento de diferentes formas de apneas centrales son las teofilinas, azetazolamidas, progestágenos y, recientemente, el zolpidem.
Conclusión
La aparición de eventos centrales que persisten o aparecen tras iniciar tratamiento con CPAP por el diagnóstico de un SAHS es un fenómeno evidente, y existen múltiples hipótesis que explican su fisiopatogenia. No parece tener una importante prevalencia, ni puede determinarse qué pacientes en concreto lo presentarán, aunque posiblemente serían varones con más gravedad del IAH. Su importancia viene dada por las posibles consecuencias negativas de los eventos residuales, de forma análoga a los eventos obstructivos residuales en el SAHS, o los centrales y la respiración de Cheyne-Stokes de la insuficiencia cardíaca. Por otra parte, pueden condicionar la persistencia de síntomas y una mala tolerancia y adaptación a la CPAP. La realización de estudios de ajuste de presión mediante PSG en noche completa son la mejor forma de detectar los pacientes con CompSAS, mientras la utilización de dispositivos de autoCPAP, dejaría pacientes sin diagnosticar. La opción terapéutica que ha demostrado una mayor eficacia es la servoventilación, tanto en la reducción de los eventos centrales como en los parámetros de sueño, la sintomatología y la tolerancia, aunque se necesita, no obstante, una mayor evidencia para su recomendación generalizada, por lo que debe pautarse de forma individualizada. Son necesarios más estudios que analicen las repercusiones del CompSAS y la utilidad de la servoventilación, dado que la mayoría de los trabajos son retrospectivos, con escaso número de pacientes, y resultados a veces contradictorios.
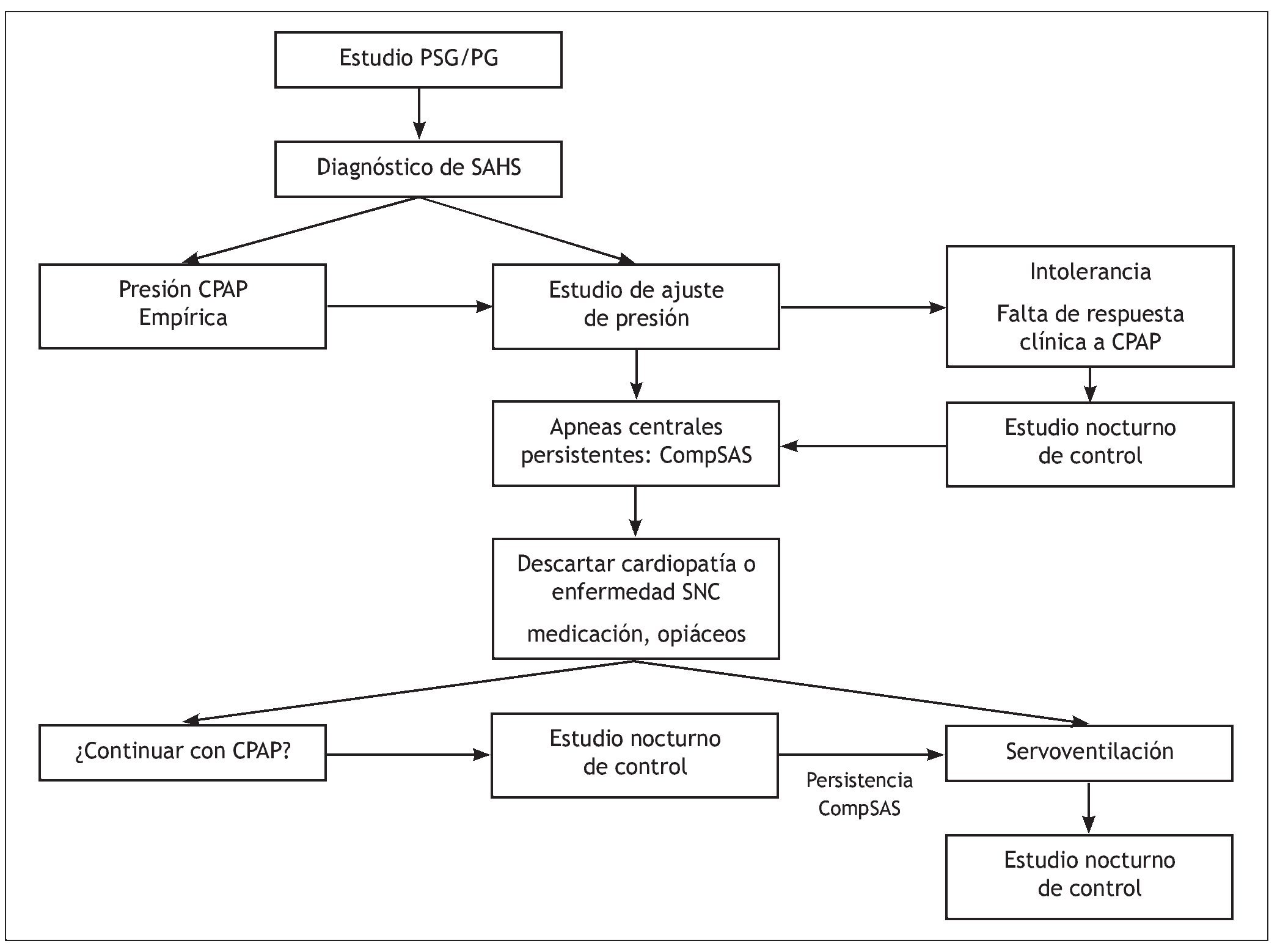
Se propone un algoritmo diagnóstico-terapéutico para el abordaje del CompSAS, partiendo fundamentalmente de la base de un estudio de ajuste de presión riguroso, y sobre todo del control clínico y nocturno de los pacientes tratados con CPAP (fig. 1).
Figura 1 Algoritmo diagnóstico-terapéutico para el síndrome complejo de apneas del sueño. CPAP: presión positiva continua sobre la vía aérea; PG: poligrafía; PSG: polisomnografía; SAHS: síndrome de apneas-hipopneas del sueño; SNC: sistema nervioso central.
*Autor para correspondencia.
Correo electrónico:rhcarvajal@hotmail.com (R. Hidalgo Carvajal).
Recibido el 26 de febrero de 2010;
aceptado el 2 de julio de 2010