Traqueotomía en las Unidades de Cuidados Intensivos
La indicación del momento en el que debe realizarse la traqueotomía en el paciente sometido a intubación prolongada sigue siendo motivo de controversia1-3. Esta decisión era clara hace unos 35 años: en los pacientes que requerían intubación durante más de tres semanas, se aconsejaba practicar la traqueotomía debido a lo lesivo de los tubos de la época4.
A partir de finales de los 70, se produce una mejora de la calidad y diseño de los materiales utilizados en la intubación. Ello ha supuesto una significativa reducción de las complicaciones tardías sobre la vía aérea superior5. A pesar de estas mejoras y de la gran cantidad de estudios sobre la cuestión, queda aún por responder cuál es el mejor protocolo de utilización de la intubación y la traqueotomía en los enfermos de la Unidad de Cuidados Intensivos (UCI). No existen estudios que definan de forma clara cuál es el momento ideal de paso a la traqueotomía. La complejidad del problema, la gran variedad de causas que provocan la necesidad de ventilación mecánica, las diferentes técnicas de traqueotomía, con tasas de complicaciones diferentes, y la dificultad de detectar complicaciones de la vía aérea en pacientes críticos hacen que no haya una respuesta taxativa y que, muchas veces, esta decisión tome un carácter de individualización según el centro y según el tipo de paciente5.
Cuando se habla de definir unos tiempos, lo más frecuente, sobre todo después de la Conferencia de Consenso sobre la vía aérea de 1989, es aportar pautas muy flexibles. Si se prevé una intubación inferior a los 10 días, se aconseja mantener el tubo. Si se prevé que ésta supere las tres semanas, se aboga por pasar a la traqueotomía. En caso de no poder hacer esta previsión, se aconseja realizar evaluaciones periódicas frecuentes, pero eso sí, en el momento en que se decida el paso hay que hacerlo cuanto antes6,7.
Los motivos que se esgrimen para pasar precozmente de intubación a traqueotomía son, fundamentalmente, los de mejorar la confortabilidad del paciente8, el facilitar los cuidados por parte de enfermería9, y el evitar o reducir las lesiones tardías sobre el eje laringotraqueal10.
Traqueotomías en unidades de cuidados intermedios
Sea cual sea la causa que motivó la intubación inicial del enfermo, una vez estabilizado hemodinámicamente y resuelta la situación que propició dicha intubación, por lo general tras una ventilación prolongada existe el problema de la desconexión definitiva de ventilación mecánica y decanulación.
Existen varios factores que inciden sobre ciertos pacientes que precisan de tiempos prolongados para liberarlos del todo de la ventilación artificial y vías accesorias como la traqueotomía:
1. La edad: cada vez en los países industrializados la esperanza de vida aumenta más y pacientes por encima de la década de los 70 años son operados y reanimados. El pulmón de estos pacientes y sus mecanismos de defensa se deterioran con la edad y en muchas ocasiones el destete es difícil.
2. La ventilación mecánica prolongada y las numerosas infecciones respiratorias a las que da lugar deterioran tanto la distensibilidad como la resistencia de los tejidos, apareciendo fenómenos de malacia traqueo bronquial y atelectasias de repetición en los intentos de desconexión que abocan al fracaso del destete.
3. Tras periodos prolongados de ventilación el equilibrio de las presiones intratorácicas se pierde al pasar de la presión positiva a la negativa. El corazón dañado por los factores anteriormente mencionados en una nueva situación de presión externa nula falla, y los intentos de desconexión tienen como resultado fracasos cardiacos francos.
4. La miopatía y neuropatía de las UCI asociadas en ocasiones a una pobre matriz nutricional empeoran la situación.
5. La ansiedad del paciente, que por lo general con una traqueotomía no puede comunicarse, o la persistencia de fármacos depresores en su circulación pueden condicionar los intentos de desconexión de la ventilación mecánica.
6. La traqueo bronquitis o la broncorrea persistente iniciada casi siempre por una infección y perpetuada por ésta, junto con la presencia de un cuerpo extraño en la tráquea dificultan el proceso de desconexión/decanulación.
Todos estos factores hacen que un paciente traqueostomizado tras una estancia prolongada en la UCI precise de unos tiempos prolongados de cuidados hasta su destete total y decanulación. Este proceso va derivándose hacia unidades especializadas en el control y manejo de la vía aérea, lideradas por especialistas neumólogos en las ya conocidas como unidades de cuidados intermedios respiratorios. Estos especialistas y las enfermeras que atienden a estos pacientes deben tener una formación en cuidados críticos y un enfoque multidisciplinar, dado que no son siempre pacientes de origen respiratorio.
Equipo de profesionales en la unidad de cuidados intermedios
Las unidades de cuidados intermedios respiratorios deben ser lideradas por neumólogos especializados en reanimación respiratoria, cuidados críticos y atención integral y multidisciplinar de este tipo de enfermos. Sin embargo, para garantizar el éxito de sus intervenciones deben rodearse de especialistas del eje laringo-faringo-traqueal como un nutricionista y un otorrinolaringólogo. Además, deben dominar las técnicas endoscópicas y disponer en todo momento de un equipo de broncoscopia flexible con un canal amplio para aspirar sangre o secreciones. Las enfermeras de estas unidades deben ser especialistas en ventilación mecánica invasiva por traqueotomía y no invasiva mediante mascarilla, deben conocer los procedimientos endoscópicos y los cuidados de traqueotomías, además del manejo de tubos torácicos, líneas arteriales, venosas, etc. Todo el equipo debe saber coordinar una situación de parada cardiorrespiratoria. El equipo de fisioterapia respiratoria y rehabilitación general es imprescindible para lograr nuestros objetivos.
Protocolo de actuación ante un traqueotomizado temporal procedente de una Unidad de Cuidados Intensivos por destete difícil
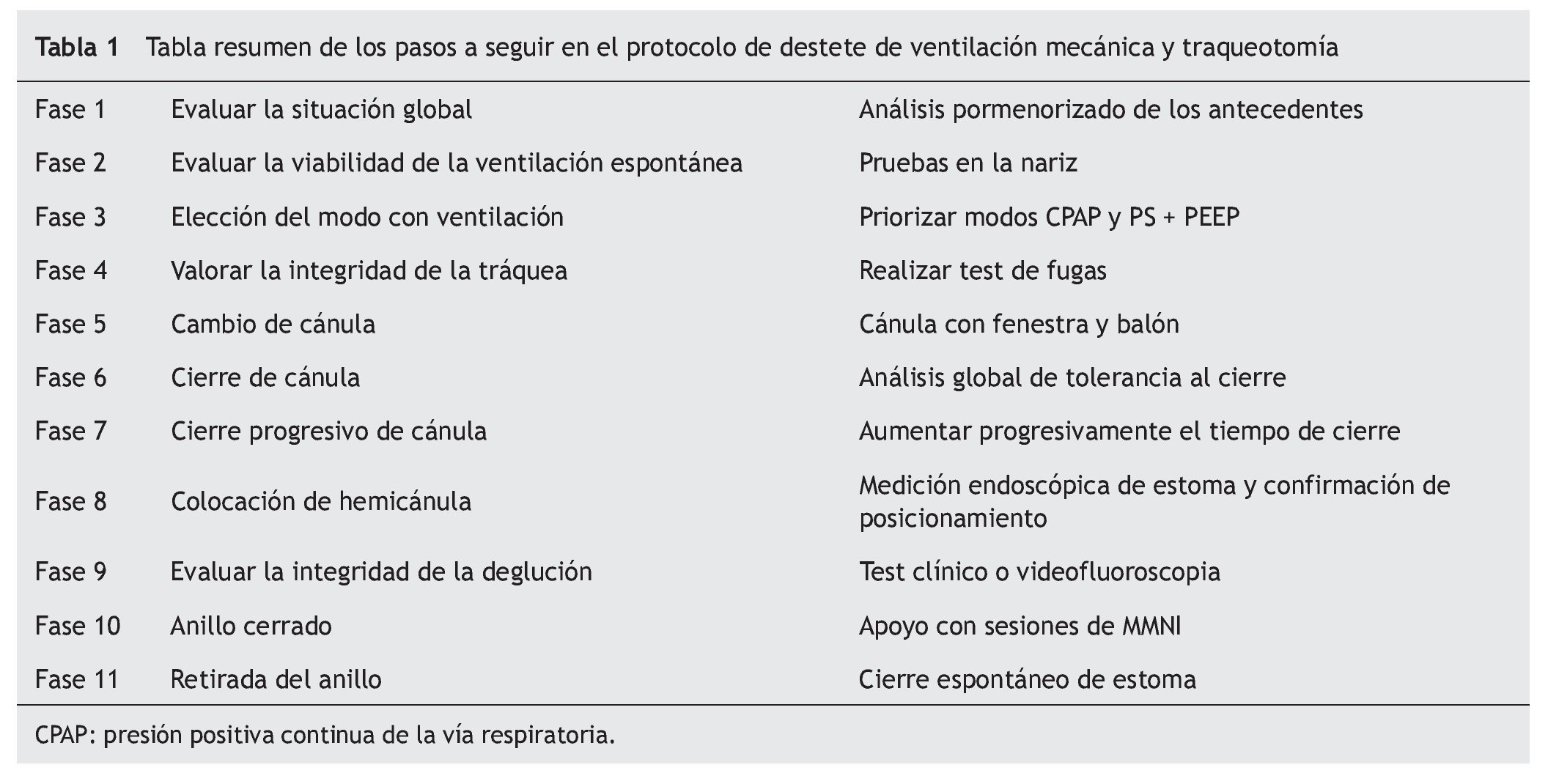
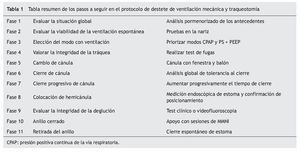
La tabla 1 muestra el protocolo global de decanulación y destete de ventilación mecánica de nuestra unidad que pasamos a analizar en detalle a continuación.
Evaluar la situación global
Es imprescindible conocer al detalle qué motivó la intubación, todos los antecedentes del enfermo y conocer qué ha acontecido durante su estancia en la UCI por órganos y aparatos. Un buen servicio de intensivos refleja por apartados lo acontecido con cada órgano, los problemas que se encontraron y las soluciones que dieron. Hay que prestar especial atención a los pasos que se siguieron hasta llegar a la traqueotomía, cómo se ventiló al enfermo, qué parámetros se utilizaron, qué estrategias ventilatorias se utilizaron, qué complicaciones infecciosas hubo y cuáles fueron los gérmenes responsables, qué tratamientos antibióticos recibió el enfermo, anotar los cultivos y los antibiogramas de estos gérmenes, saber si se utilizaron curares, si hubo drenajes torácicos por qué y cuándo se retiraron, si hubo reintubaciones urgentes tras los intentos de extubación y cuáles fueron las causas potenciales. Si se hicieron broncoscopias en la UCI acceder a los informes o a los broncoscopistas para conocer los detalles de la anatomía laringo traqueal.
A nivel cardiológico es preciso conocer qué medicación ha precisado y si se usaron fármacos vasoactivos y durante cuánto tiempo, la necesidad de anticuagulación, analizar una ecografía cardiaca reciente si la hay (tiene especial valor aquella realizada en periodos de desconexión de ventilación mecánica) y si existe esa ecografía anotar el diámetro del ventrículo derecho, la presión en la arteria pulmonar si la tiene y la compresibilidad de la vena cava inferior a demás de la fracción de eyección del ventrículo izquierdo (FEVI). Es imperativo disponer de un electrocardiograma (ECG) de 12 derivaciones a su llegada a la unidad, conocer las necesidades transfusionales y disponer de un hemograma basal.
A nivel digestivo es imprescindible conocer el tipo de alimentación, si es parenteral desde cuándo, el catéter con la fecha de inserción, evaluar detenidamente el punto de inserción de ese catéter (a diario), valorar la composición de la nutrición y disponer a la llegada del enfermo de iones y parámetros nutricionales básicos como albúmina, pre albúmina y proteína fijadora del retinol. Si la nutrición es renteral disponer de una radiografía que confirme el buen posicionamiento de la sonda y su adecuada fijación a la nariz, confirmar que existen ruidos abdominales idóneos y en todos los casos anotar las 2 últimas deposiciones y su consistencia. Una exploración abdominal de entrada es obligada, pero cuando la nutrición es artificial es imprescindible y muy importante.
A nivel renal es imprescindible conocer si el paciente requirió depuración extrarrenal y por cuánto tiempo, disponer de los niveles de creatinina de las ultimas 2 semanas y un aclaramiento e iones en orina a su llegada. También es preciso conocer el balance acumulado de las últimas 2 semanas y tener una idea de los balances según la medicación diaria y el grado de respuesta a esa medicación
Todas las infecciones documentadas de origen respiratorio o no deben ser conocidas, fecha de detección, antibióticos y antibiogramas. En presencia de traqueotomía en nuestra unidad se solicita de entrada secreción bronquial y orina. Un hemograma basal de llegada es imperativo, así como disponer de curvas de temperatura y leucocitos de la última semana.
A nivel neurológico, según llega el enfermo, hay que disponer de una escala de Glasgow y realizar una exploración neurológica básica pero completa. Conocer los problemas neurológicos en la UCI, los requerimientos de sedoanalgesia, los eventos de depresión o agitación y la necesidad de medicación psiquiátrica si la hubo.
Para pacientes quirúrgicos una entrevista con el cirujano responsable servirá para conocer con detalle el motivo de la intervención, la técnica quirúrgica, los cuidados y las potenciales complicaciones de la cirugía. La enfermera deberá estar presente en esta reunión y el cirujano la orientará en los cuidados. En nuestra unidad para pacientes quirúrgicos un médico del equipo de la especialidad visita al enfermo diariamente para evaluar la herida quirúrgica y orientar en los cuidados de enfermería de la misma.
Una excelente colaboración entre servicios médicos y quirúrgicos es fundamental y no debe prescindirse de ella en caso de necesidad.
Evaluación de la viabilidad de la ventilación espontánea
Uno de los primeros análisis que se deben realizar es la viabilidad de un tiempo no inferior a 2 horas de ventilación espontánea con nariz. Durante este periodo hay que valorar:
1. La tos eficaz; ver si el enfermo es capaz de subir secreciones hasta la traqueotomía y aprovechar este momento para recogerlas, observar su color y consistencia y enviarla a microbiología.
2. Es recomendable obtener una gasometría tras estas 2 horas para observar si se producen ascensos en el nivel de CO2 respecto del basal, lo que indicaría las pautas a seguir en relación tanto con el número de sesiones diarias de ventilación como con el modo en que debería utilizarse.
3. La taquicardia, taquipnea, ansiedad, sudoración, utilización de musculatura accesoria o la aparición en la auscultación de roncus gruesos o crepitantes y regiones de hipoventilación nuevas deben alertar sobre un posible fracaso de destete y orientar a su causa (malacia, secreciones, insuficiencia cardiaca, atelectasias, etc.).
Elección del modo de ventilación
En primer lugar, diremos que son necesarios equipos con doble tubuladura que ofrezcan los valores en tiempo real de volumen tidal inspirado (VTI) y espirado (VTE), y que permitan visualizar curvas de flujo y de presión, si es posible, es muy útil le presencia de curvas de espirometría y distensibilidad. En el sistema no debe faltar un humidificador de agua o un filtro humidificador, este último genera un espacio muerto no desdeñable, pero la traqueotomía per se elimina un espacio muerto fisiológico mayor al del filtro, por lo que puede ser utilizado en este contexto. Además, al evitar condensaciones es menos peligroso que el humidificador.
El enfermo debe estar monitorizado mientras esté ventilado.
Si se confirma la necesidad de sesiones de ventilación, en el contexto de destete de ventilación mecánica hay que priorizar aquellos modos donde hay poco o nulo control sobre la ventilación. Son así preferibles el modo de CPAP si no hay hipercapnia o datos de mala mecánica o los modos de presión de soporte más PEEP (PS + PEEP) garantizando en todo momento una ventilación espontánea. El trigger inspiratorio debe ser fijado sensible (± 2 lpm), aunque en ocasiones para recuperar la actividad normal diafragmática conviene mantener ciclos temporales con un trigger inspiratorio menos sensible, en torno a 5 lpm. El trigger espiratorio debe estar inicialmente fijado poco sensible (30-40% de la caída de flujo inspiratorio), si en este contexto se observan en la curva de flujo espirada pequeñas depresiones que reflejan esfuerzos espiratorios tardíos es conveniente disminuir el trigger espiratorio para mejorar la sincronía del paciente con el respirador, de igual manera, esfuerzos inspiratorios en fase espiratoria indican que hay que aumentar el valor del trigger espiratorio. En estos modos sin frecuencia de rescate si se observan frecuencias respiratorias < 11 rpm es preferible aumentar el control de la ventilación, bien ajustando una frecuencia de rescate o pasando a un modo mandatario controlado por presión, fijando así un número de ciclos controlados obligados. En caso de observarse apneas prolongadas de carácter central (sin esfuerzos respiratorios asociados observados a pie de cama) deberá reducirse el nivel de soporte o pasar a un modo de presión continua (por ejemplo, la presión positiva continua de la vía respiratoria [CPAP]), si esto no corrige el cuadro, hay que fijar frecuencias de rescate que eliminen estas apneas. Las presiones pico nos orientarán a la hora de conocer problemas obstructivos en la vía aérea (por ejemplo, secreciones) o distensibilidades bajas pulmonares (por ejemplo, atelectasia aguda), en este sentido, la espirometría invertida y la curva de distensibilidad nos proporcionarán una ayuda valiosa para orientar o solucionar el problema, por ello deben ser monitorizadas intentado siempre establecer una curva tipo basal en situación estable. Durante estas sesiones el volumen tidal espirado debe ser igual al inspirado, si no es así, debemos revisar nuestro circuito en Y, la adecuada compensación de volúmenes y la calibración del respirador, e inflar más el balón de la traqueotomía. Si esto no soluciona el problema debemos plantearnos que el balón esté roto (en este caso hay que cambiar de cánula de traqueotomía) o chequear que no tenemos una cánula fenestrada con macho fenestrado. Si todo esto es negativo, una broncoscopia es obligada para descartar una fístula traqueal o bronquial.
Valorar la integridad de la tráquea: el test de fugas
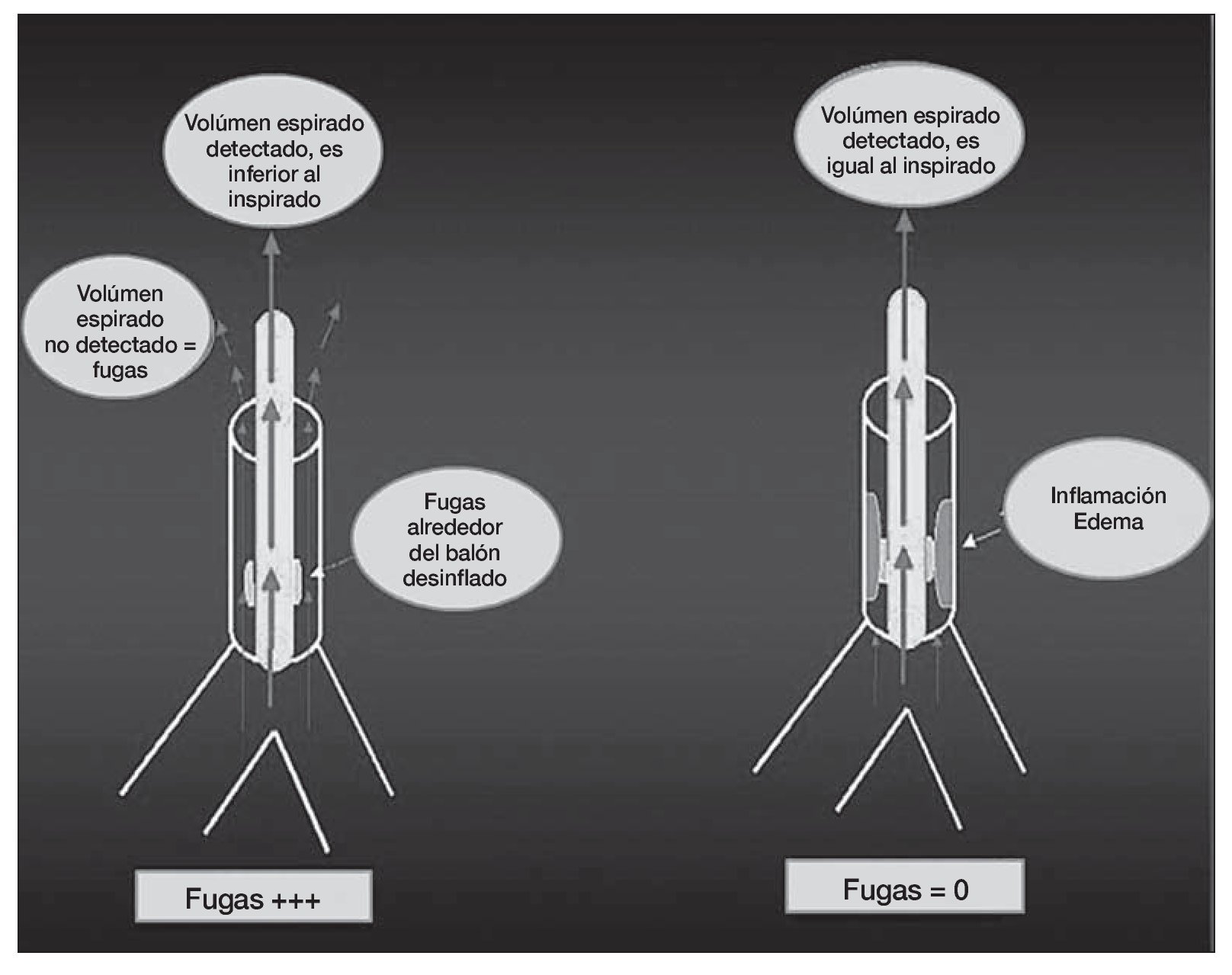
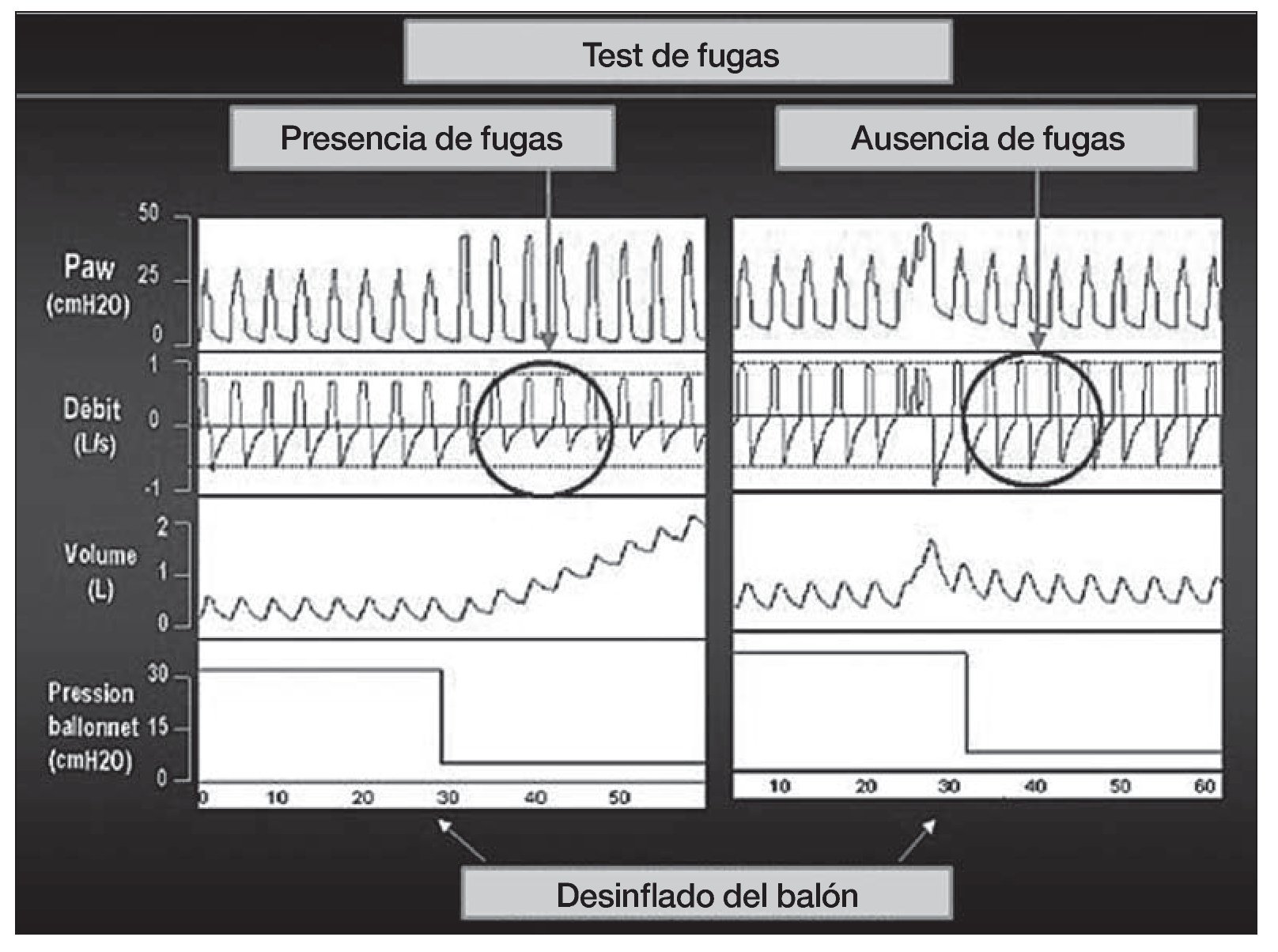
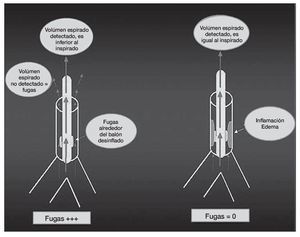
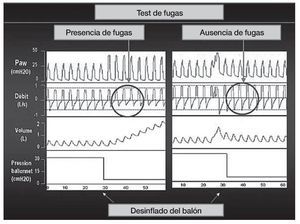
Recientemente se han publicado en la misma revista dos trabajos11,12 sobre la predicción de edema laríngeo post-extubación o decanulación mediante el test de la fuga del balón de neumotaponamiento. El test se lleva a cabo de la siguiente manera (fig. 1), antes de la extubación o decanulación, se ventila al paciente en modo asistido-controlado con un volumen tidal (Vt) de 10-12 ml/kg. Se realizan varias mediciones del Vt espirado calculando una media. Posteriormente se desinfla el balón y tras la estabilización (evitando la tos) se vuelve a calcular el Vt espirado tomando la media entre varios ciclos. La lógica nos dice que cuanto menor diferencia haya entre uno y otro Vt (pre y post desinflado del balón) mayor edema laríngeo debe haber y, por tanto, mayor riesgo de fracaso de la extubación. En el trabajo belga1 8 de 76 pacientes (11%) necesitaron reintubación por edema laríngeo. El punto de corte más adecuado que permite predecir la presencia de edema laríngeo es menos del 15,5 % de diferencia porcentual entre Vt pre y post test. La sensibilidad de la prueba fue del 75%, especificidad 72%, valor predictivo positivo 25% y valor predictivo negativo 96,1% con un porcentaje de clasificación correcta del 72,4%.En el trabajo francés2 con 112 pacientes, el punto de corte es del 12% (o menor de 130 ml), con sensibilidad y especificidad de 85 y 95%, respectivamente, valor predictivo positivo 69% y negativo 98%. En estos trabajos identifican pacientes con mayor riesgo de edema laríngeo como aquellos con SAPS II más elevados, ingresados por razones médicas, con intubación traumática o difícil, historia de autoextubación, sobre-inflación del balón y periodo prolongado de ventilación mecánica. Ambos trabajos concluyen adecuadamente con el diseño de los estudios y la posible utilidad de la prueba con puntos de corte relativamente similares. La principal limitación es que el test debe estandarizarse convenientemente y buscar aquellos pacientes que presentan mayor riesgo de edema laríngeo para su aplicación en ellos. Los esteroides no han demostrado utilidad para reducir el edema, aunque es una medida que se aplica frecuentemente13. Por tanto, quizá sea un paso adecuado para identificar pacientes que puedan beneficiarse de medidas terapéuticas o preventivas. En el contexto de la decanulación, este test lo realizamos diariamente y sólo deca nulamos o pasamos a una cánula fenestrada con balón en caso de test de fuga positivo, es decir, con diferencias del vte > 130 ml (fig. 2).
Figura 1 Efecto de desinflado del balón de neumotaponamiento sobre el volumen tidal espirado.
Figura 2 Visualización en la curva de flujo de una notoria reducción (promedio 130 ml) en el volumen tidal espirado.
Valorar la integridad de la deglución
Una vez evaluada la integridad de la vía aérea y antes de cambiar a cánulas de fonación solicitamos la valoración por un otorrinolaringólogo para conocer si una alimentación por vía oral será factible14 para las diferentes texturas de alimentos.
Test clínico de deglución
Se puede comprobar la capacidad de deglución del paciente en una exploración a pie de cama como primera aproximación diagnóstica15. Esto se realiza administrando una pequeña cantidad de alimento, coloreado con azul de metileno, en distintas consistencias (pudding, néctar, líquido), aumentando progresivamente el volumen (5, 10 y 20 ml) y observando la seguridad y eficacia de la deglución en las distintas condiciones. Los signos que indican una alteración de la seguridad en la deglución son la tos, la desaturación o a través del traqueostoma donde se puede observar si se emiten restos a través de la cánula después de la deglución. Los signos de alteración de la eficacia de la deglución son el sello labial alterado con emisión de alimento fuera de la cavidad oral, deglución oral fraccionada requiriendo deglutir el bolo en fragmentos y presencia de residuo faríngeo tras la deglución. Hay que tener en cuenta que esta prueba tiene como limitación que puede existir una aspiración silente que pase desapercibida al explorador.
Videoendoscopia de deglución
La vídeo endoscopia16 de deglución consiste en valorar de forma directa, mediante un nasofibroscopio, la capacidad de deglución del paciente. Además nos permite conocer si la alimentación oral es segura, las medidas necesarias para facilitarla o si es preciso contraindicarla. Esta técnica consta de 2 partes: valoración anatómica y valoración de la deglución.
Valoración anatómica
Antes de comenzar la exploración se aplica pomada anestésica en la fosa nasal, no se debe utilizar líquido anestésico para que no difunda al resto de estructuras. Se valorará si existen alteraciones anatómicas o funcionales.
Test sensitivo
Se comprueba la sensibilidad acercando el fibroscopio al repliegue aritenoepiglótico, lo que produce un reflejo de medialización de la cuerda vocal de ese lado en condiciones normales. También se debe valorar la sensibilidad de la base de la lengua, epiglotis y paredes faríngeas. La manera ideal de valorar la sensibilidad es utilizando una bomba de pulsos de aire, que además sirve para identificar la severidad del déficit sensitivo según el incremento de presión que es necesario aplicar para inducir el reflejo.
Valoración de la deglución
Se administrarán al paciente alimentos de distintas consistencias y volúmenes, coloreados con azul de metileno, para observar si se produce aspiración o retención del alimento y en qué fase de la deglución. Se debe comenzar con las texturas más sencillas e ir aumentando la dificultad progresivamente.
Videofluoroscopia de deglución
La vídeo fluoroscopia17 de deglución consiste en la administración por vía oral de un contraste radioopaco y la visualización dinámica mediante radioscopia de la capacidad de deglución del paciente, tanto en proyección lateral como ántero-posterior. Las imágenes obtenidas se registran mediante un vídeo de alta resolución. Se puede modificar la consistencia y volumen de los bolos administrados de manera similar a la vídeo-endoscopia de deglución. Esta técnica tiene la ventaja de ser muy sensible en la valoración de la fase oral y faríngea de la deglución, pero tiene el inconveniente de someter al paciente a radiaciones ionizantes.
Si el test de deglución es normal, se retira la sonda nasogástrica que puede ser problemática en caso de tener que decanular en ventilación no invasiva mediante mascarilla.
Cambio a cánula fenestrada con balón
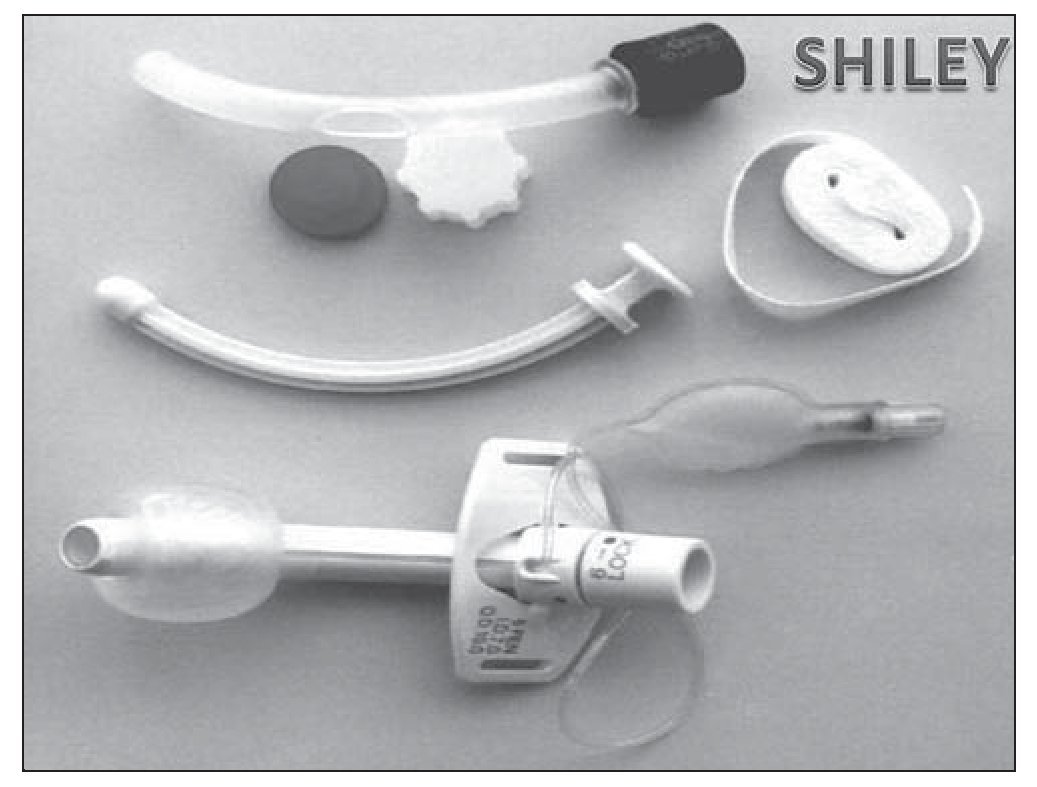
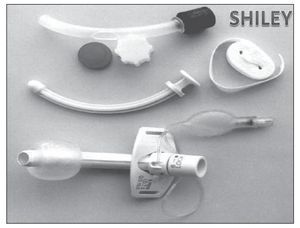
En cuanto se ha comprobado la viabilidad de la vía aérea y de la deglución oral, aunque el paciente siga precisando alguna sesión de ventilación mecánica se cambia la cánula de ventilación con balón por una cánula de menor calibre fenestrada y con balón que nos ayudará a avanzar en la fonación, mientras valoramos el momento adecuado de la decanulación completa. Se inician sesiones de cierre de cánula con fenestra con O2 por mascarilla o gafas nasales en periodos de 1 a 2 horas. Aquí si el test de fugas se realizó adecuadamente no debe de haber compromiso de la vía aérea superior. Sin embargo, como este test se hace en ventilación mecánica existe la posibilidad de pasar por alto problemas de malacia o broncoespasmo que se detectarán ante signos de estridor, sibilancias, etc. en el momento del cierre. En estos casos se inician sesiones más o menos prolongadas de ventilación y se administran nebulizaciones por vía oral hasta que la sintomatología desaparece. Estas cánulas (fig. 3) disponen de 2 machos, uno fenestrado para el cierre de la cánula desinflando el balón, con lo que el paciente respira a través de la fenestra y peri cánula, y otro de ventilación que anula la fenestra. Con él se debe inflar el balón para ventilar al enfermo sin fugas. Estas cánulas son muy valiosas en el procedimiento de decanulación.
Figura 3 Cánula de Shiley fenestrada con balón.
El momento de la decanulación
Cuando un enfermo es capaz de mantener una cánula fenestrada cerrada durante 24-48 horas y la deglución es eficaz se puede decanular sin dudas y con seguridad.
En ocasiones ocurre que este momento no llega, y los intentos de cierre de más de 6 horas son un fracaso por elevaciones de la pCO2 o mala mecánica y muy frecuentemente por broncorrea estéril, la mayoría de las veces perpetuada por la propia cánula. En estos casos decanulamos en ventilación no invasiva. Este concepto nace de la necesidad de decanular al paciente para así recuperar los mecanismos de defensa de su vía aérea superior. Para lograr esto lo ideal sería retirar la cánula y comenzar con sesiones de ventilación no invasiva facial o nasal por mascarilla, pero el estoma tarda en cerrarse entre 48 y 72 horas, lo que impide la ventilación no invasiva, pues el estoma genera serias fugas y la fuga perpetúa el estoma.
En nuestra unidad realizamos una decanulación precoz en ventilación no invasiva gracias a artilugios diseñados para mantener el estoma abierto pero que no van más allá de este, es decir, no penetran en la tráquea, se trata de las hemicánulas BMD con tapón (figs. 3 y 4).
Figura 4 Hemicánulas BMD de silicona, existen en distintos diámetros y longitudes. Su colocación precisa de una broncoscopia para medir la longitud del estoma, el diámetro viene dado por la cánula que se retira. Disponen de un orificio que permite aspirar secreciones y por el que pasa un broncoscopio que puede taparse con el tapón adecuado.
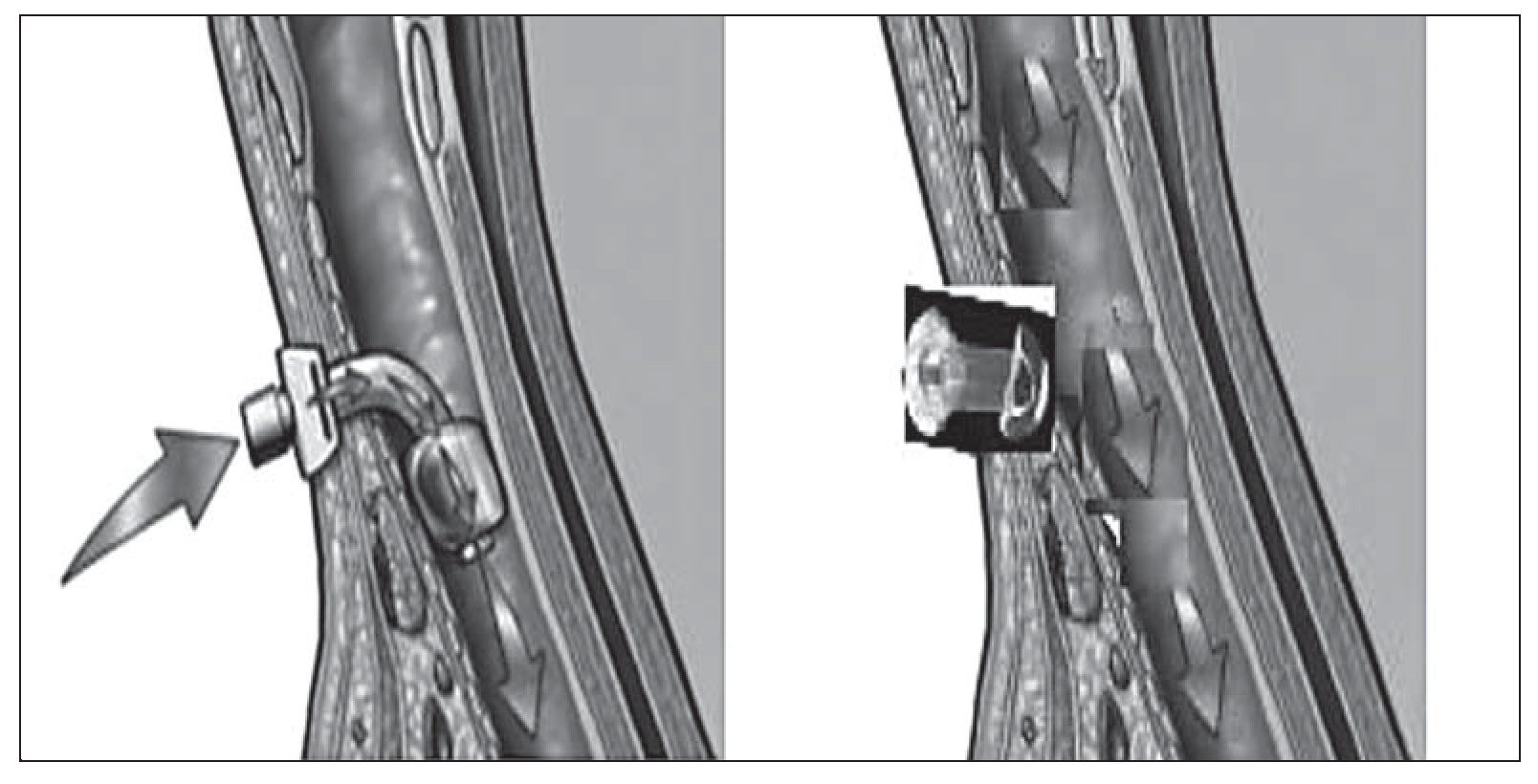
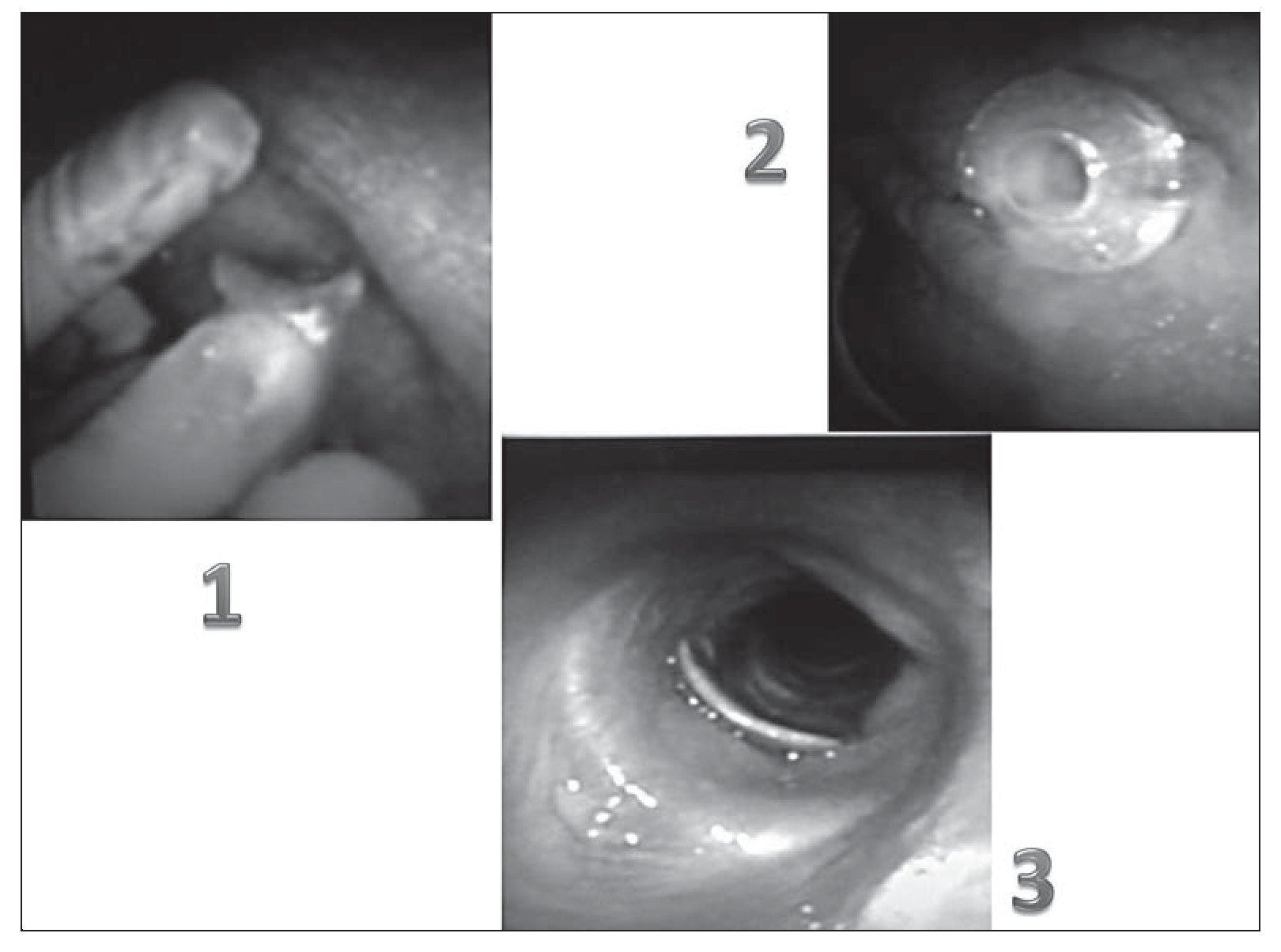
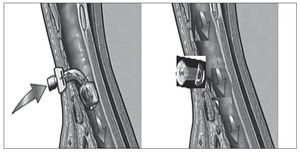
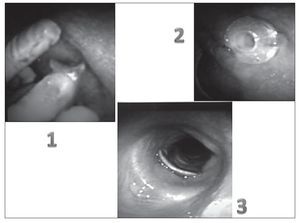
Como se puede observar en la figura 5, el dispositivo de silicona ocupa el lugar de la traqueotomía manteniendo el estoma abierto pero su trayectoria termina donde termina el estoma en su cara traqueal. Su posicionamiento como se observa en la secuencia de la figura 6 requiere el uso de un broncoscopio para establecer la longitud del dispositivo que debe ser idéntica a la profundidad del estoma, puesto que el diámetro del mismo viene marcado por el diámetro de la traqueotomía. Su colocación es manual (fig. 6-1) y se debe revisar la correcta colocación con el broncoscopio entrando a través del orificio del dispositivo en la tráquea (fig. 6-2) y finalmente entrando por la nariz o la boca y atravesando las cuerdas (fig. 6-3) debe confirmarse que las lenguetas distales quedan adheridas a la pared interna traqueal.
Figura 5 Disposición del anillo traqueal.
Figura 6 Colocación manual de hemicánula (1). Hemicánula colocada en el estoma traqueal (2). Visión endoscópica de la parte traqueal de la hemocánula y sus lenguetas (3).
Estos artilugios nos permiten decanular al enfermo y empezar con sesiones de ventilación no invasiva, en caso de fracaso no es preciso reintubar al enfermo o abrir quirúrgicamente una traqueotomía previa, y bastará con retirar la hemicánula y colocar una cánula de traqueotomía convencional. Durante este periodo el equipo de fisioterapeutas respiratorios es crucial para poder enseñar al enfermo a manejar de manera óptima sus secreciones y prepararlo para cuando se retire el dispositivo y no sea posible una ventilación no invasiva de apoyo. Cuando estemos seguros de que el paciente no necesitará soporte durante 48 horas se retira la estructura y se cierra el estoma mandando previamente a microbiología un exudado de estoma, en estos días, no se podrá aplicar ventilación no invasiva y adquirirán un extraordinario valor los fisioterapeutas y rehabilitadores que deberán hacer de nuestro paciente un individuo autónomo tanto respiratoria como motoramente.
Conclusiones
En los enfermos críticos que han evolucionado a una traqueotomía tras largas estancias en la UCI y con problemas respiratorios de destete francos es previsible una decanulación lenta en la que va a jugar un papel importante la ventilación invasiva, la no invasiva, y el manejo de la encrucijada faringotraqueal por un equipo de nutricionistas, otorrinolaringólogos, fisioterapeutas, rehabilitadores y neumólogos. Para llevar a cabo una decanulación segura y definitiva es recomendable seguir unos pasos precisos que se han pormenorizado en este artículo y con los que en nuestra unidad hemos tenido buenos resultados.
Conflicto de intereses
Los autores declaran que no tienen ningún conflicto de intereses.
*Autor para correspondencia.
Correo electrónico:sheili@fjd.es
Recibido el 7 de marzo de 2011;
aceptado el 11 de abril de 2011