Descrever e analisar a ocorrência de internações por pneumonia adquirida na comunidade em crianças antes e após a implantação, no Programa Nacional de Imunização, da vacina pneumocócica 10‐valente (conjugada).
MétodosTrata‐se de um estudo ecológico que incluiu registros de crianças menores de um ano, vacinadas e não vacinadas com a vacina antipneumocócica 10‐valente conjugada, no período pré e pós‐inclusão da vacina no Programa Nacional de Imunização na área de abrangência da Superintendência Regional de Saúde de Alfenas, MG, Brasil. A vacinação foi considerada como fator de exposição e a hospitalização por pneumonia adquirida na comunidade como desfecho, com o uso de dados anuais secundários por município. Para verificar a associação entre as variáveis foi empregada a razão de prevalência e seu intervalo de confiança 95% (IC95%). Para o cálculo de diferença entre proporções empregou‐se o teste Z.
ResultadosConsiderando os 26 municípios da Superintendência Regional de Saúde de Alfenas, houve redução significativa do número de hospitalização por pneumonia adquirida na comunidade em crianças abaixo de um ano, com razão de prevalência (RP)=0,81 (IC95% 0,74‐0,89; p<0,05), o que indica uma prevalência de internação por pneumonia adquirida na comunidade 19% menor no período pós‐vacinal.
ConclusõesOs resultados sugerem a efetividade da vacina pneumocócica 10‐valente (conjugada) na prevenção de casos graves da pneumonia adquirida na comunidade em crianças menores de um ano.
To describe and analyze the occurrence of hospitalizations for community‐acquired pneumonia in children before and after the pneumococcal 10‐valent conjugate vaccine implementation into the National Immunization Program.
MethodsThis is an ecological study that includes records of children younger than one year old, vaccinated and not vaccinated with the pneumococcal 10‐valent conjugate vaccine in the periods pre‐ and post‐inclusion of the vaccine in the National Immunization Program in the area covered by the Regional Health Superintendence of Alfenas, state of Minas Gerais, Brazil. Vaccination was considered as the exposure factor and hospitalization for community‐acquired pneumonia as the endpoint, using secondary annual data by municipality. The prevalence ratio and its 95% confidence interval (95%CI) were used to verify the association between variables. The Z test was used to calculate the difference between proportions.
ResultsConsidering the 26 municipalities of the Regional Health Superintendence of Alfenas, there was a significant reduction in hospitalizations for community‐acquired pneumonia in children younger than one year of age, with prevalence ratio (PR)=0.81 (95%CI: 0.74 to 0.89; p<0.05), indicating a 19% lower prevalence of hospitalization for community‐acquired pneumonia in the post‐vaccination period.
ConclusionsThe results suggest the effectiveness of the pneumococcal 10‐valent conjugate vaccine in preventing severe cases of community‐acquired pneumonia in children younger than one year of age.
Entre os vários agentes etiológicos bacterianos envolvidos na gênese da pneumonia adquirida na comunidade (PAC), o Streptococcus pneumoniae é o principal causador da doença em crianças e adultos. Atualmente são relatados 91 sorotipos1,2 associados a essa e outras doenças. No entanto, as PAC são as que provocam maior morbidade, estima‐se a ocorrência de 13,8 milhões de novos casos em todo o mundo a cada ano.3,4
Entre 6‐16% dos casos de PAC necessitam de hospitalização e em crianças abaixo dos cinco anos, a doença, sobretudo de etiologia bacteriana, é responsável por 20‐40% das internações apenas no continente americano.4 No Brasil, entre 2004 e 2006, as doenças pneumocócicas foram responsáveis por cerca de 34.000 internações.
A estimativa mundial da incidência de PAC nos países em desenvolvimento entre crianças de 1‐5 anos é de 0,29 episódios/criança/ano. Isso equivale a uma incidência de anual de cerca de 150 milhões de casos da doença; 11‐20% desses precisam de internação hospitalar.4 No Brasil, segundo o Sistema de Informação Hospitalar (SIH‐SUS), de janeiro de 2005 a março de 2006 a PAC foi a causa de internação de cerca de 20% nos menores de cinco anos.5–7
Medidas preventivas são consensualmente a melhor maneira de reduzir a ocorrência das doenças pneumocócicas e de suas consequências, como a hospitalização e a morte prematura.5 Dentre tais medidas, a imunização ativa contra os principais agentes causadores, em especial alguns sorotipos do Streptococcus pneumoniae, se mostra, ao longo dos anos, altamente eficiente na redução do aparecimento de formas graves da doença.5,6
No Brasil, com a incorporação de vacinas pneumocócicas, especialmente a 10‐valente, a partir de 2010,6,7 observa‐se a redução de doenças pneumocócicas, como as meningites e as PAC,8–10 em crianças abaixo dos dois anos, com queda do número de internações, de desnutrição, de mortes e absenteísmo no trabalho dos pais, além de diminuição de custos, entre outras.11,12
O presente estudo teve como objetivo avaliar o impacto da vacina conjugada pneumocócica 10‐valente (PCV‐10), antes da dose de reforço vacinal, em crianças menores de um ano hospitalizadas com PAC antes e após a sua introdução no Programa Nacional de Imunização (PNI) em municípios pertencentes à Superintendência Regional de Saúde de Alfenas (SRS/Alfenas, MG, Brasil).
MétodoTrata‐se de um estudo ecológico que incluiu registros de crianças vacinadas e não vacinadas com a PCV‐10, no período pré e pós‐inclusão no PNI, e considerou‐se a vacinação o fator de exposição e a hospitalização por PAC o desfecho. O estudo usou dados anuais secundários por município para cálculo da cobertura vacinal e das taxas de morbidade por pneumonia em menores de um ano de 2007 a 2013. Procedeu‐se à comparação dos números brutos, ou seja, números não proporcionais, de hospitalização por PAC de 2007 a 2013 nos municípios pertencentes à SRS/Alfenas.
Foram investigados registros de crianças com até um ano, residentes nos 26 municípios sob a jurisdição da SRS/Alfenas – Secretaria Estadual de Saúde de Minas Gerais, Brasil. Os dados foram coletados por meio de busca no sistema de informação do SI‐PNI (Sistema de Informação do Programa Nacional de Imunização)13 e do banco de dados do Tabwin disponível no Núcleo de Regulação da SRS/Alfenas, MG. Os municípios pertencentes à SRS/Alfenas são: Alfenas, Alterosa, Arceburgo, Areado, Bandeira do Sul, Botelhos, Cabo Verde, Campestre, Campo do Meio, Campos Gerais, Carmo do Rio Claro, Carvalhópolis, Conceição da Aparecida, Divisa Nova, Fama, Guaranésia, Guaxupé, Juruaia, Machado, Monte Belo, Muzambinho, Nova Resende, Paraguaçu, Poço Fundo, São Pedro da União e Serrania.
Foi incluída toda a população infantil no período já definido. Para verificar a associação entre variáveis (independentes e resposta), foram usadas análises univariadas e empregaram‐se a razão de prevalência relativa (RP) e seu respectivo intervalo de confiança a 95% (IC95%) como estimadores de associação. Posteriormente, foi feita análise multivariada por regressão logística, inseriram‐se todas as variáveis explicativas no modelo (número de hospitalizações por PAC, idade ajustada, sexo, município de residência, estado vacinal, cobertura vacinal). Para análise de diferenças entre proporções foi usado o teste qui‐quadrado e para diferenças entre médias o teste t de Student para amostras independentes. Em todas as análises considerou‐se um nível de significância de 5%. No armazenamento e na análise dos dados foi empregado o software estatístico SPSS 20.0® (IBM SPSS Statistics for Windows, Version 20.0, Armonk, NY, USA).
O projeto de pesquisa foi submetido ao Comitê de Ética e Pesquisa do Hospital das Clínicas da Faculdade de Medicina de Ribeirão Preto da USP e foi aprovado em 19 de março de 2013 (n° CAAE: 12487113.5.0000.5440).
ResultadosO estudo pretendeu avaliar o número de internações por PAC em menores de um ano, portanto antes do reforço vacinal, que deve ocorrer entre 12 e 15 meses, e a cobertura vacinal, que ocorreram no período que compreendeu a fase pré (2007, 2008 e 2009) e pós (2011, 2012 e 2013) introdução da PCV‐10 no calendário vacinal do PNI preconizado pelo Ministério da Saúde. A tabela 1 mostra o número de crianças em cada um dos anos nos períodos pré e pós‐vacinal, bem como o número de crianças incluídas no estudo. Nota‐se que, no período anterior à introdução da PCV‐10, as perdas foram de 11,3%, enquanto, no período pós‐vacinal, foram de 8,3%. Todas as perdas se deveram a registros inconsistentes.
Distribuição de crianças menores de um ano de idade cadastradas nos 26 municípios da SRS/Alfenas, MG; nos períodos pé e pós‐vacinal, bem como, número bruto e média de crianças incluídas no estudo com respectivas perdas por período
| Períodos | ||||||
|---|---|---|---|---|---|---|
| Pré‐vacinal | Introdução da PCV‐10 | Pós‐vacinal | ||||
| 2007 | 2008 | 2009 | 2010 | 2011 | 2012 | 2013 |
| 5969 | 5622 | 5628 | 5765 | 5669 | 5723 | 5667 |
| Média (A) | – | Média (B) | ||||
| 5740 | 5765 | 5686 | ||||
| Registros (PNI) – SRS/Alfenas, MG | ||||||
|---|---|---|---|---|---|---|
| 2007 | 2008 | 2009 | 2010 | 2011 | 2012 | 2013 |
| 5107 | 5088 | 5080 | 5765 | 5215 | 5212 | 5213 |
| Média (C) | – | Média (D) | ||||
| 5091 | – | 5213 | ||||
| Perdas A‐C (%) | Perdas B‐D (%) | |||||
| 11,3 | – | 8,3 | ||||
O número bruto de registros de crianças do sexo masculino e do feminino entre 2007 e 2009, foi, respectivamente de 2.632 e 2.459 (p<0,05), com média de nove meses (±1) para o sexo feminino e de 10 meses (±1) para o masculino (p<0,05). Considerando‐se o período de 2011 a 2013, foram 2.737 registros de crianças do sexo masculino e 2.476 do feminino (p<0,05), com respectivas médias de 9,5±1 meses e 10±1,2 meses. Houve diferença significativa (p<0,05).
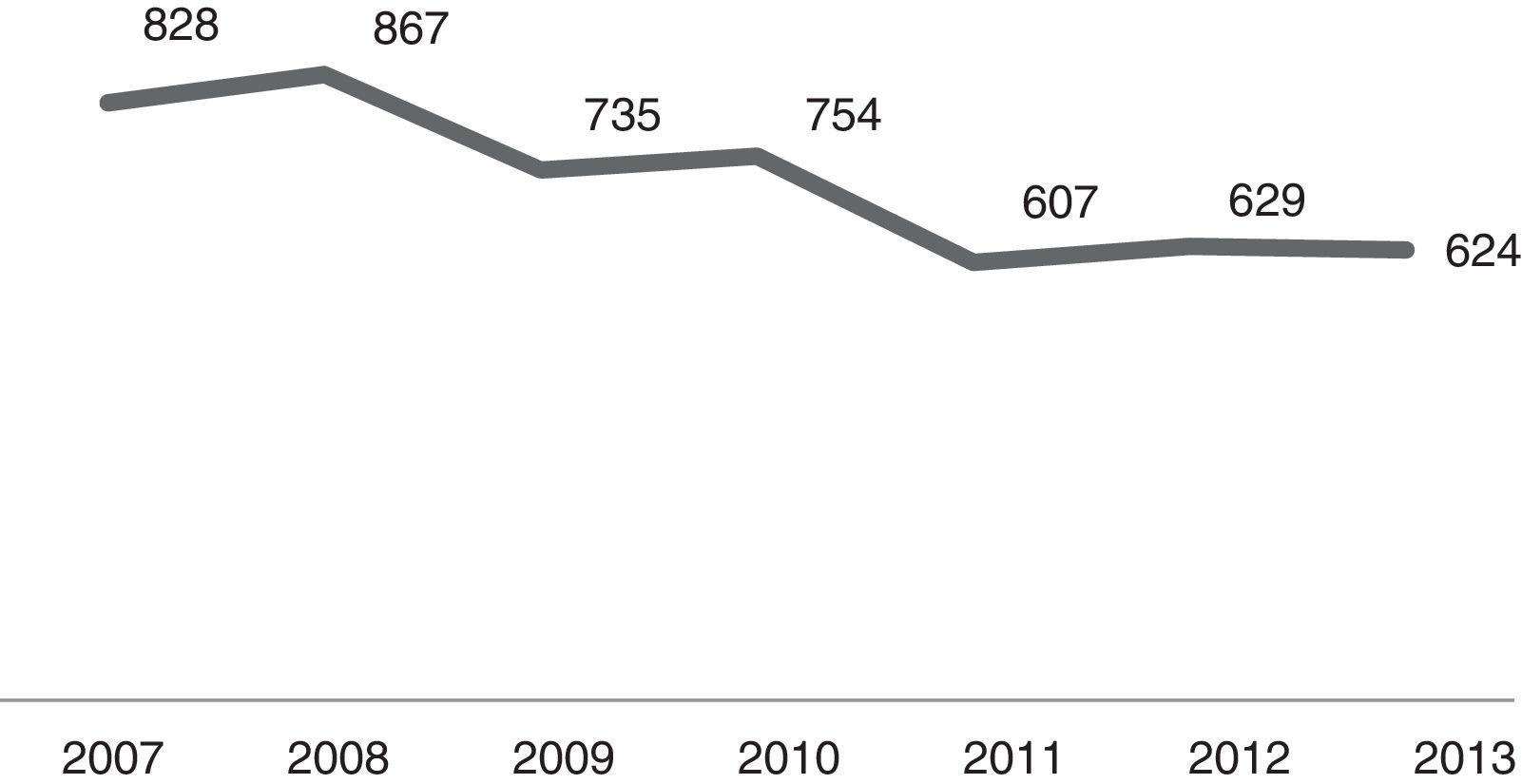
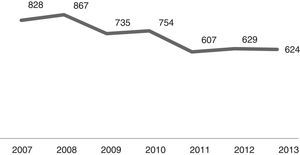
O número de internações durante o período analisado pode ser verificado na figura 1. Como pode ser observado, o número de internações por PAC na faixa etária menor de um ano passou de 828 em 2007 para 624 em 2013. Foram 5.044 casos de internações por PAC durante o período de análise.
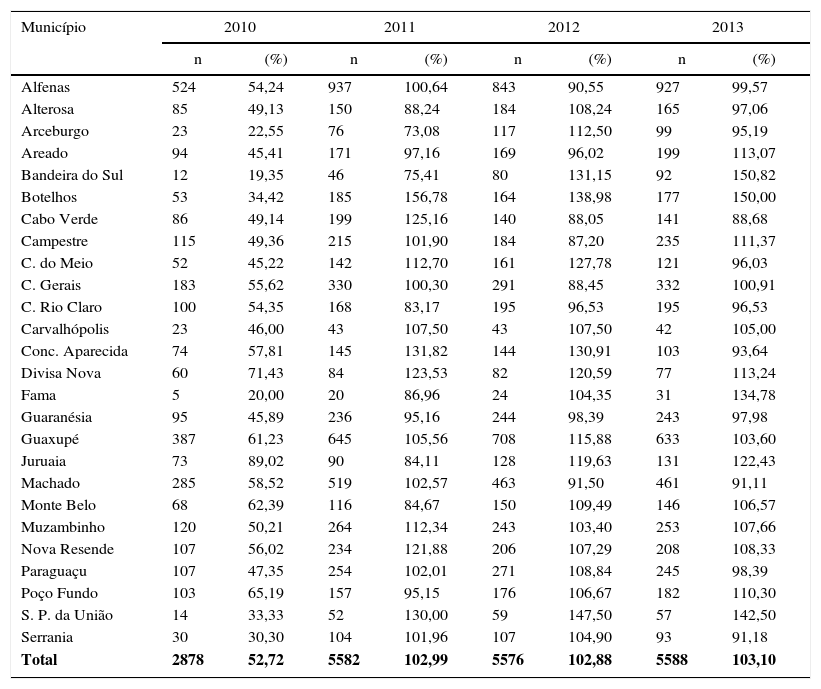
Em março de 2010 ocorreu a implantação da vacina pneumocócica 10‐valente (conjugada) no calendário de vacinação da criança no PNI. Assim, a cobertura vacinal desse ano não alcançou os 95% de cobertura preconizada (tabela 2). Não foi avaliado 2010 em relação à cobertura vacinal, pois poderia introduzir viés na análise, tanto pela baixa cobertura quanto pela possibilidade de retardo na soroconversão vacinal.
Distribuição da cobertura vacinal da vacina pneumocócica 10‐valente (conjugada) em crianças em 2010, 2011, 2012 e 2013, na SRS/Alfenas, MG, Brasil
| Município | 2010 | 2011 | 2012 | 2013 | ||||
|---|---|---|---|---|---|---|---|---|
| n | (%) | n | (%) | n | (%) | n | (%) | |
| Alfenas | 524 | 54,24 | 937 | 100,64 | 843 | 90,55 | 927 | 99,57 |
| Alterosa | 85 | 49,13 | 150 | 88,24 | 184 | 108,24 | 165 | 97,06 |
| Arceburgo | 23 | 22,55 | 76 | 73,08 | 117 | 112,50 | 99 | 95,19 |
| Areado | 94 | 45,41 | 171 | 97,16 | 169 | 96,02 | 199 | 113,07 |
| Bandeira do Sul | 12 | 19,35 | 46 | 75,41 | 80 | 131,15 | 92 | 150,82 |
| Botelhos | 53 | 34,42 | 185 | 156,78 | 164 | 138,98 | 177 | 150,00 |
| Cabo Verde | 86 | 49,14 | 199 | 125,16 | 140 | 88,05 | 141 | 88,68 |
| Campestre | 115 | 49,36 | 215 | 101,90 | 184 | 87,20 | 235 | 111,37 |
| C. do Meio | 52 | 45,22 | 142 | 112,70 | 161 | 127,78 | 121 | 96,03 |
| C. Gerais | 183 | 55,62 | 330 | 100,30 | 291 | 88,45 | 332 | 100,91 |
| C. Rio Claro | 100 | 54,35 | 168 | 83,17 | 195 | 96,53 | 195 | 96,53 |
| Carvalhópolis | 23 | 46,00 | 43 | 107,50 | 43 | 107,50 | 42 | 105,00 |
| Conc. Aparecida | 74 | 57,81 | 145 | 131,82 | 144 | 130,91 | 103 | 93,64 |
| Divisa Nova | 60 | 71,43 | 84 | 123,53 | 82 | 120,59 | 77 | 113,24 |
| Fama | 5 | 20,00 | 20 | 86,96 | 24 | 104,35 | 31 | 134,78 |
| Guaranésia | 95 | 45,89 | 236 | 95,16 | 244 | 98,39 | 243 | 97,98 |
| Guaxupé | 387 | 61,23 | 645 | 105,56 | 708 | 115,88 | 633 | 103,60 |
| Juruaia | 73 | 89,02 | 90 | 84,11 | 128 | 119,63 | 131 | 122,43 |
| Machado | 285 | 58,52 | 519 | 102,57 | 463 | 91,50 | 461 | 91,11 |
| Monte Belo | 68 | 62,39 | 116 | 84,67 | 150 | 109,49 | 146 | 106,57 |
| Muzambinho | 120 | 50,21 | 264 | 112,34 | 243 | 103,40 | 253 | 107,66 |
| Nova Resende | 107 | 56,02 | 234 | 121,88 | 206 | 107,29 | 208 | 108,33 |
| Paraguaçu | 107 | 47,35 | 254 | 102,01 | 271 | 108,84 | 245 | 98,39 |
| Poço Fundo | 103 | 65,19 | 157 | 95,15 | 176 | 106,67 | 182 | 110,30 |
| S. P. da União | 14 | 33,33 | 52 | 130,00 | 59 | 147,50 | 57 | 142,50 |
| Serrania | 30 | 30,30 | 104 | 101,96 | 107 | 104,90 | 93 | 91,18 |
| Total | 2878 | 52,72 | 5582 | 102,99 | 5576 | 102,88 | 5588 | 103,10 |
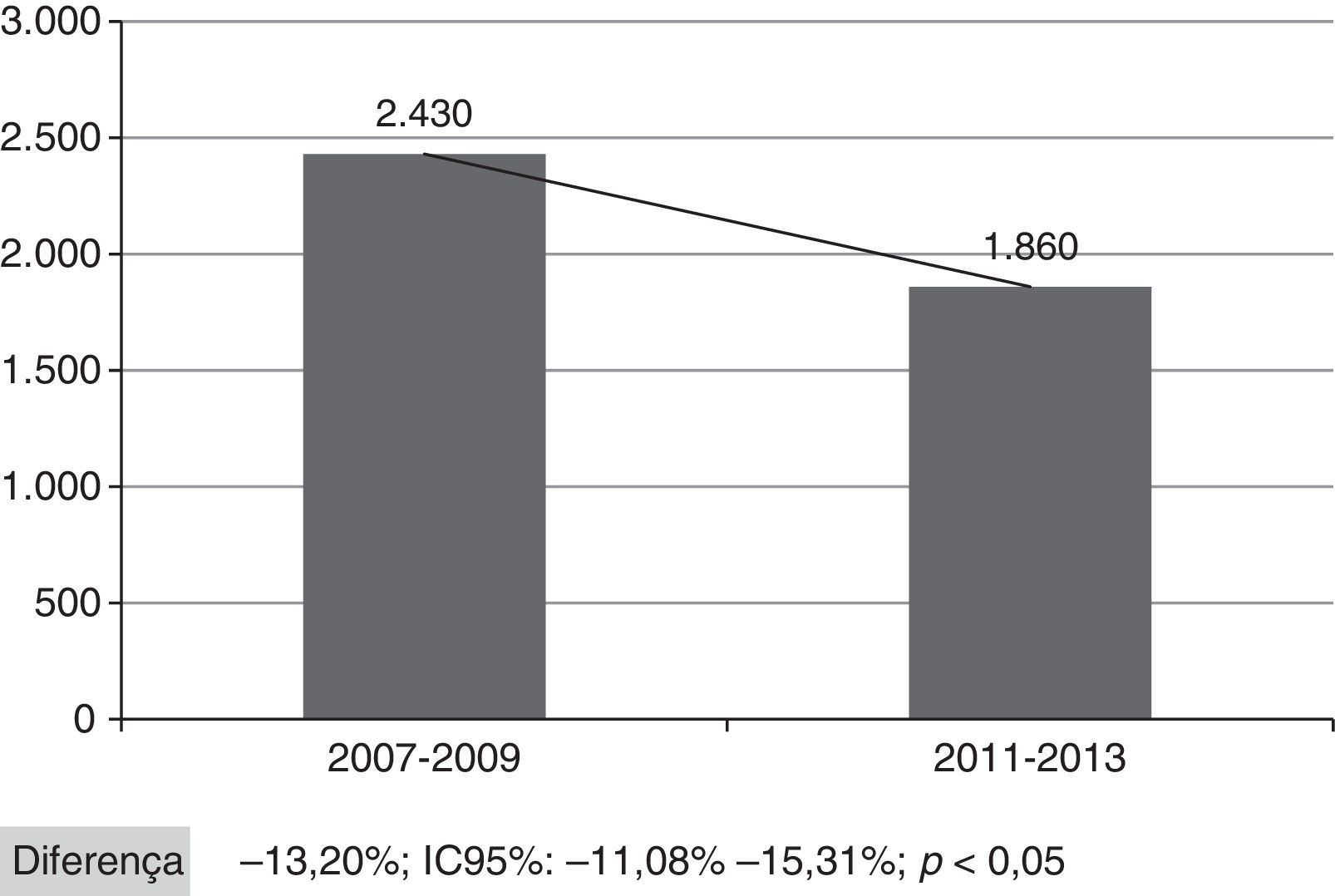
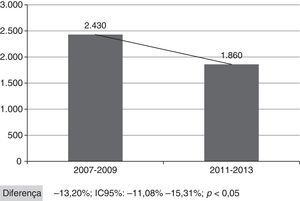
Na figura 2 é apresentada a quantidade global de internações por PAC nos períodos pré e pós‐incorporação da vacina no PNI, considerando‐se todos os municípios da SRS/Alfenas. Ao se considerar o conjunto de municípios que compõe a SRS/Alfenas, houve uma diferença significativa de ‐13,20% (IC95%: ‐44,08% a ‐15,31%; p<0,05) na ocorrência de casos de internação por PAC em crianças entre os períodos estudados.
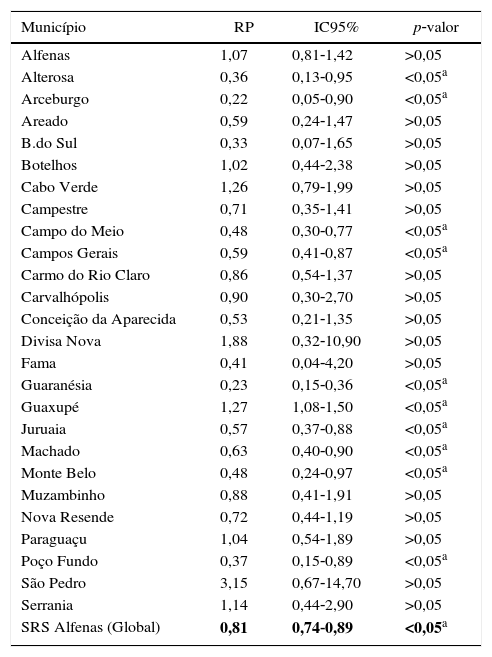
A análise multivariada entre o estado vacinal e a ocorrência de internação por PAC em cada um dos 26 municípios, ajustada para variáveis de confusão, bem como da SRS como um todo, pode ser observada na tabela 3.
Análise de associação entre vacinação e ocorrência de PAC em crianças dos 26 municípios da SRS/Alfenas, MG, Brasil, comparando 2007‐2009 (antes da imunização antipneumocócica) com 2011‐2013 (após introdução da vacina pneumocócica)
| Município | RP | IC95% | p‐valor |
|---|---|---|---|
| Alfenas | 1,07 | 0,81‐1,42 | >0,05 |
| Alterosa | 0,36 | 0,13‐0,95 | <0,05a |
| Arceburgo | 0,22 | 0,05‐0,90 | <0,05a |
| Areado | 0,59 | 0,24‐1,47 | >0,05 |
| B.do Sul | 0,33 | 0,07‐1,65 | >0,05 |
| Botelhos | 1,02 | 0,44‐2,38 | >0,05 |
| Cabo Verde | 1,26 | 0,79‐1,99 | >0,05 |
| Campestre | 0,71 | 0,35‐1,41 | >0,05 |
| Campo do Meio | 0,48 | 0,30‐0,77 | <0,05a |
| Campos Gerais | 0,59 | 0,41‐0,87 | <0,05a |
| Carmo do Rio Claro | 0,86 | 0,54‐1,37 | >0,05 |
| Carvalhópolis | 0,90 | 0,30‐2,70 | >0,05 |
| Conceição da Aparecida | 0,53 | 0,21‐1,35 | >0,05 |
| Divisa Nova | 1,88 | 0,32‐10,90 | >0,05 |
| Fama | 0,41 | 0,04‐4,20 | >0,05 |
| Guaranésia | 0,23 | 0,15‐0,36 | <0,05a |
| Guaxupé | 1,27 | 1,08‐1,50 | <0,05a |
| Juruaia | 0,57 | 0,37‐0,88 | <0,05a |
| Machado | 0,63 | 0,40‐0,90 | <0,05a |
| Monte Belo | 0,48 | 0,24‐0,97 | <0,05a |
| Muzambinho | 0,88 | 0,41‐1,91 | >0,05 |
| Nova Resende | 0,72 | 0,44‐1,19 | >0,05 |
| Paraguaçu | 1,04 | 0,54‐1,89 | >0,05 |
| Poço Fundo | 0,37 | 0,15‐0,89 | <0,05a |
| São Pedro | 3,15 | 0,67‐14,70 | >0,05 |
| Serrania | 1,14 | 0,44‐2,90 | >0,05 |
| SRS Alfenas (Global) | 0,81 | 0,74‐0,89 | <0,05a |
RP, razão de prevalência; IC95%, intervalo de confiança 95%.
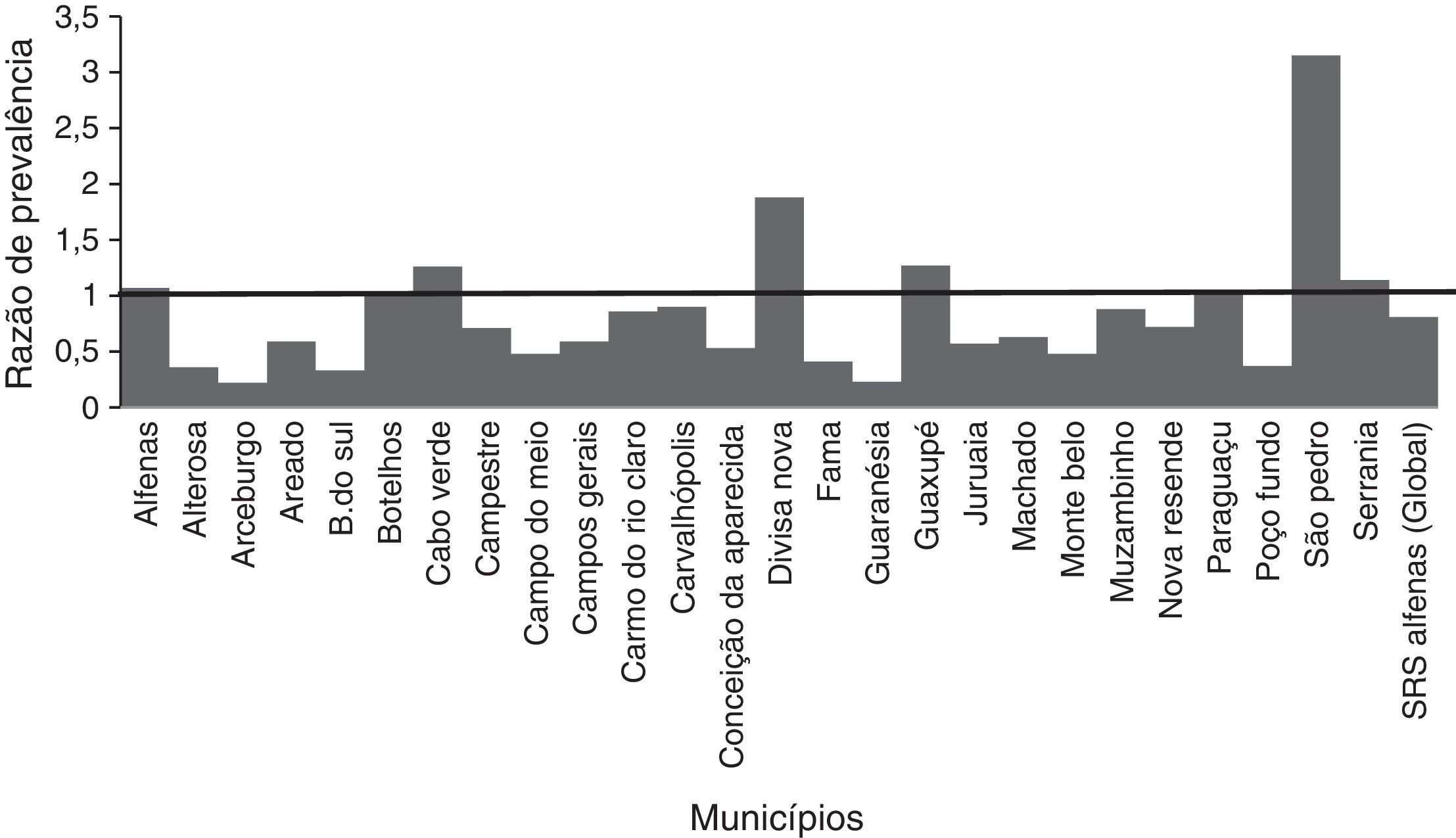
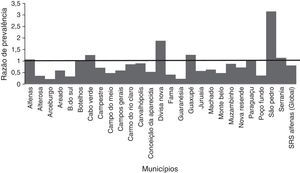
Nos municípios de Alfenas, Areado, Bandeira do Sul, Botelhos, Cabo Verde, Campestre, Carmo do Rio Claro, Carvalhópolis, Conceição da Aparecida, Divisa Nova, Fama, Muzambinho, Nova Resende, Paraguaçu, São Pedro da União e Serrania não foram observadas diferenças de prevalência de PAC, entre crianças vacinadas e não vacinadas. Nos municípios de Alterosa, Arceburgo, Campo do Meio, Campos Gerais, Guaranésia, Juruaia, Machado, Monte Belo e Poço Fundo houve diminuição nas internações por PAC em crianças vacinadas, quando comparadas com as não vacinadas, conforme pode ser visto na figura 3. Já no município de Guaxupé, houve um aumento significativo de 27% no registro de hospitalização por PAC entre os dois períodos estudados (pré e pós‐vacinal). Tal fenômeno necessita de melhor esclarecimento. No conjunto dos 26 municípios, a vacinação pode ter sido responsável por uma redução de 19% nas hospitalizações decorrentes de casos PAC em crianças menores de um ano. Durante esse período não houve mortalidade causada por PAC em menores de um ano no conjunto dos municípios da SRS/Alfenas.
Representação dos valores pontuais da razão de prevalência (RP) relativos às internações por PAC em crianças com até um ano, em cada um dos 26 municípios e considerando‐se o valor total da SRS‐Alfenas, MG, Brasil, após a introdução da vacina PCV‐10. As colunas representam os valores da razão de prevalência de hospitalização por PAC, após a introdução da vacina PCV‐10. A linha horizontal representa a razão de prevalência=1, ou seja, a linha de não alteração na prevalência de PAC após introdução da vacina PCV‐10.
Este estudo mostrou uma redução de 19% em PAC, em crianças menores que do um ano, entre 2007‐2009 e 2011‐2013, correspondente aos períodos antes e após a implantação do Calendário Vacinal da PCV‐10 em 2010 no PNI, em 26 municípios sob a jurisdição da SRS/Alfenas.
O Ministério da Saúde preconiza como 95% a taxa ideal de cobertura vacinal capaz de dar eficiência à vacina pneumocócica 10‐valente na redução de casos de PAC e outras doenças pneumocócicas invasivas.11,12,14 No presente estudo, a taxa média de cobertura no ano da incorporação da vacina foi de apenas 52,7%; no entanto, em 2011, 2012 e 2013 as taxas foram respectivamente 104,0%, 102,9% e 103,1%, ou seja, acima do preconizado. Espera‐se, portanto, uma redução no número de casos de PAC e de suas consequências como a hospitalização e a mortalidade, a qual realmente foi observada. Esse achado é semelhante ao estudo publicado por Afonso et al.,15 no qual se notou que, em cidades onde a cobertura vacinal foi superior a 95%, houve redução dos casos de pneumonia, ao contrário das cidades com menor cobertura, como São Paulo, com 75%, e Porto Alegre, com 85%, onde tal redução não foi observada No presente estudo, conforme demonstrado nos dados da tabela 2, muitos municípios apresentaram cobertura vacinal superior a 100%. Isso aconteceu provavelmente devido a dois fatos importantes. O primeiro se refere à intensa migração sazonal nos municípios no período de colheita do café. Os trabalhadores rurais e suas famílias que procuram os postos de vacinação são vacinados em suas respectivas faixas etárias. O outro fato seria a extensa zona rural que muitos municípios possuem. Assim, para muitas famílias fica mais perto ir ao posto de vacinação de outra cidade do que em sua própria cidade de residência.
Além dos aspectos diretamente ligados à morbidade e mortalidade das PAC, com impacto na qualidade de vida das crianças e seus parentes, há ainda a questão econômica associada à doença, por exemplo, o custo atrelado ao seu manejo, como gastos com antibióticos, internação, feitura de exames, falta ao trabalho por parte dos pais, entre outros. Diante disso, alguns estudos têm mostrado que a vacinação para o pneumococo em crianças é custo‐efetiva sob a perspectiva da sociedade, reduz os encargos totais decorrentes das doenças pneumocócicas, incluindo as PAC. Martí et al.,11 em análise da custo‐efetividade que tomou por base os anos de vida ganhos com qualidade (QALY) da PCV‐10 em seis países latino‐americanos, incluindo o Brasil, mostraram que a incorporação dessa imunização é uma estratégia custo‐efetiva na melhoria dos padrões de saúde da população infantil.
Ao se analisarem os períodos anteriores e posteriores à introdução PCV‐10 no PNI, conforme pode ser visto na figura 1, o número de internações por PAC nos 26 municípios selecionados já havia apresentado um declínio a partir de 2009 (período pré‐vacinal), fato que certamente pode ser explicado pelas melhores condições sanitárias, aumento da renda das famílias, bem como aos ganhos na assistência à saúde das crianças observados nos últimos anos em todo Brasil. Assim, a vacinação contra o pneumococo trouxe um incremento à queda observada no período pós‐introdução da mesma, a partir de 2010.16–19
Uma das limitações deste estudo é o fato de se tratar de um estudo ecológico, em que a unidade observada não é o indivíduo, mas um conjunto de pessoas que representa uma parcela da população que está sob a jurisdição da SRS/Alfenas (crianças menores de um ano), porém foram usadas fontes oficiais que têm controle de qualidade – Datasus, SI‐PNI e Tabwin – disponíveis no Núcleo de Regulação da SRS/Alfenas, mas ainda assim podem apresentar falhas, fato que foi observado nas perdas de registros em pelo menos 8,3% dos casos no período pós‐vacinal. Outros aspectos limitantes no presente estudo relacionam‐se a possíveis fatores de confundimento, como, por exemplo, a melhoria nos padrões nutricionais das crianças, observados na última década, que contribui para a queda de ocorrência de casos graves de PAC, além da vacinação, bem como a presença de algumas comorbidades e as diferenças na prevalência de PAC entre os gêneros masculino e feminino.18,20 Finalmente, outra limitação reside no fato de se ter estudado apenas crianças antes do reforço vacinal preconizado entre 12 e 15 meses.
No período pós‐advento da PCV‐10 houve diminuição do número de PAC em crianças menores de 12 meses nas crianças da região da SRS/Alfenas, MG, Brasil. Em países em que foram implantadas vacinas antipneumocócicas conjugadas e mesmo polissacarídicas e que se mantêm com altas coberturas vacinais, a redução das doenças pneumocócicas invasivas é significativa; o mesmo resultado foi encontrado neste estudo, que mostrou redução do número de crianças internadas por PAC, no período estudado.
FinanciamentoO estudo não recebeu financiamento.
Conflitos de interesseOs autores declaram não haver conflitos de interesse.