La asenapina, recientemente comercializada en Estados Unidos y pronto en Europa, es un antipsicótico de segunda generación con acción multireceptorial, derivada de su afinidad por múltiples receptores dopaminérgicos (D2, D3 y D4), serotoninérgicos (5HT2A, 5HT2B, 5HT2C, 5HT6 y 5HT7) y adrenérgicos (αa1A, α2A, α2B y α2C). Su administración se realiza por vía sublingual. Tras culminar las fases iniciales de desarrollo, se han realizado diversos ensayos clínicos en dos indicaciones principalmente: esquizofrenia y manía. Este artículo sintetiza la evidencia científica de su eficacia y seguridad en manía aguda y adelanta algunas de sus posibilidades clínicas inmediatas y futuras.
ConclusionesLa asenapina es eficaz y generalmente bien tolerada en el tratamiento de la manía aguda moderada o grave asociada al trastorno bipolar tipo I. Su administración sublingual plantea el reto de evitar su coadministración con comida u otros fármacos, pero puede suponer una ventaja para la adherencia terapéutica. Por su perfil receptorial, puede asociarse a diversos efectos adversos, pero destaca por la baja intensidad de todos ellos, sin ninguno que destaque por encima de los demás. En Europa está indicada solamente para la manía aguda, pero se están realizando también numerosos ensayos en esquizofrenia y en depresión bipolar.
Asenapine, recently marketed in United States and ready to be so in Europe, is a multimodal action second-generation antipsychotic, with high affinity for multiple dopaminergic (D2, D3 y D4), serotonergic (5HT2A, 5HT2B, 5HT2C, 5HT6 and 5HT7) and adrenergic (α1A, α2A, α2B and α2C) receptors. Asenapine has to be administered sublingually. After going through succesfully the preliminary phases of development, several clinical trials have been completed in two main indications: schizophrenia and mania. This article summarizes the available evidence on its safety and efficacy in acute mania and provides some prospect on its clinical immediate and future applications.
ConclusionsAsenapine is effective and generally well tolerated in the treatment of moderate-to-severe acute mania associated to bipolar I disorder. The sublingual administration may be a challenge (coadministration with food or other drugs needs to be avoided) but also an opportunity (improved treatment adherence). Due to its multimodal receptor profile, it may cause several side-effects, but most of those are relatively mild, with none being particularly outstanding. In Europe, asenapine is indicated for the treatment of acute mania only, but several trials are being conducted in schizophrenia and bipolar depression.
Asenapina, antipsicótico atípico de segunda generación, ha sido aprobado por la Food and Drug Administration (FDA) estadounidense en agosto de 2009 para el tratamiento agudo de la esquizofrenia y de la manía pura o mixta en el trastorno bipolar de tipo I1,2, y el 24 de junio de 2010 el Comité para productos farmacéuticos de uso humano (CHMP) ha emitido una opinión favorable para su autorización en Europa en la indicación de «tratamiento de los episodios de manía aguda moderada o grave asociada al trastorno bipolar tipo I (EMA/CHMP/397789/2010)». Esta indicación se fundamenta básicamente en 3 ensayos clínicos positivos que apoyan su eficacia y seguridad en dicha indicación3.
El desarrollo en humanos de asenapina sublingual comenzó en 1996 para el tratamiento de la esquizofrenia, y no fue hasta 2004 que se estudió para la manía aguda en el trastorno bipolar4,5.
ORG 5222 (primera denominación de la molécula de asenapina), tras su primer estudio preclínico en 19906, se investigó inicialmente en Europa y Japón con formulación oral e intravenosa; sin embargo, debido a la baja biodisponibilidad oral y al elevado metabolismo de primer paso hepatogastrointestinal asociados a la formulación oral, se procedió al desarrollo de la presentación sublingual7.
MétodoSe ha realizado una revisión bibliográfica y de las fuentes primarias de ensayos clínicos, desde agosto de 2009 hasta la actualidad en las páginas de http://www.pubmed.gov; http://www.fda.gov; www.clinicaltrials.gov, http://www.clinicaltrials.results.gov/con la búsqueda de los términos «asenapina» o bien «ORG 5222». Nuestra revisión sistemática se ha centrado en la obtención de datos de los ensayos clínicos conducidos con fin de registro de la molécula. Con los datos obtenidos hemos pretendido sintetizar las características farmacocinéticas y farmacodinámicas, así como la eficacia y la seguridad de asenapina y su aplicación práctica en el tratamiento de la manía aguda.
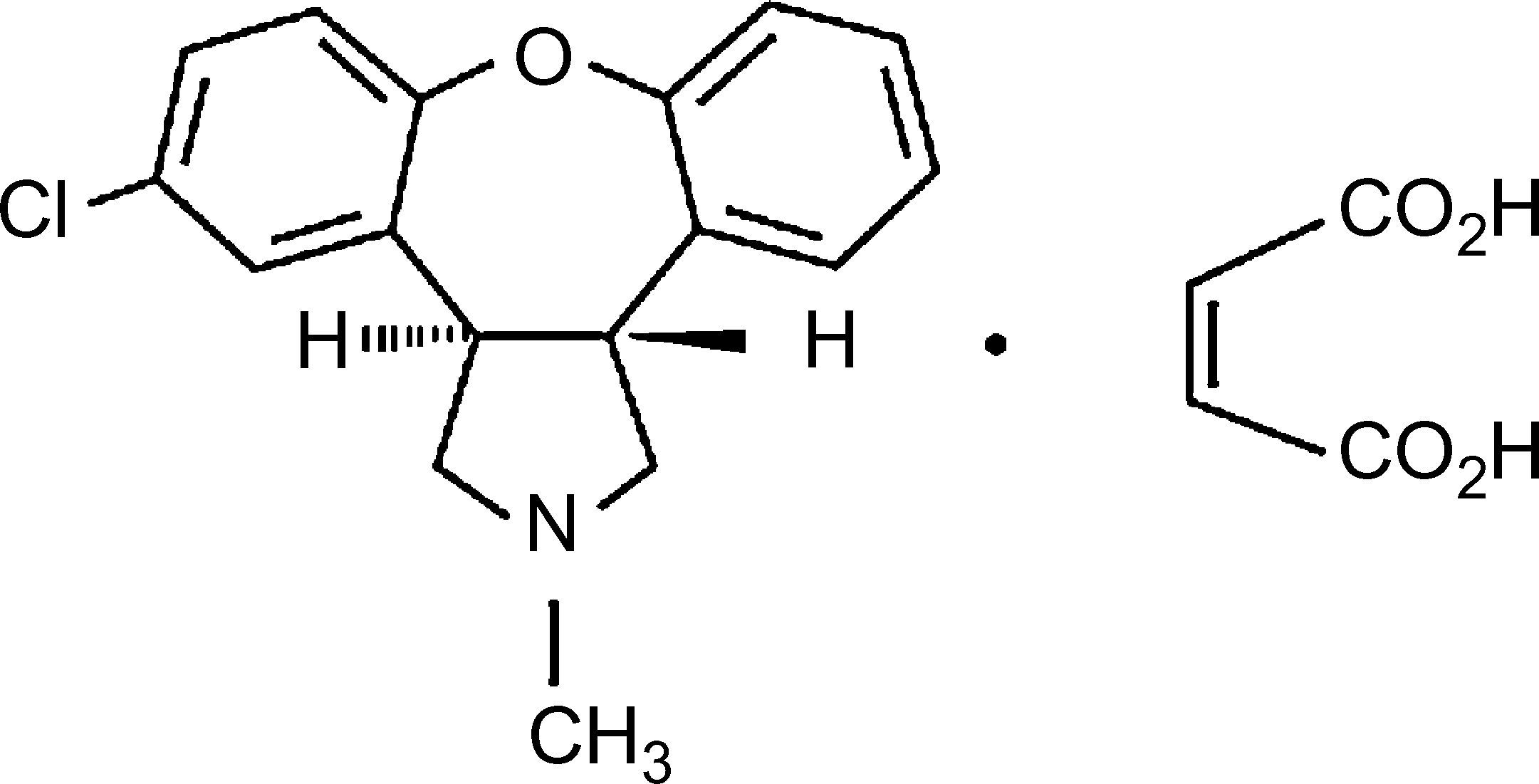
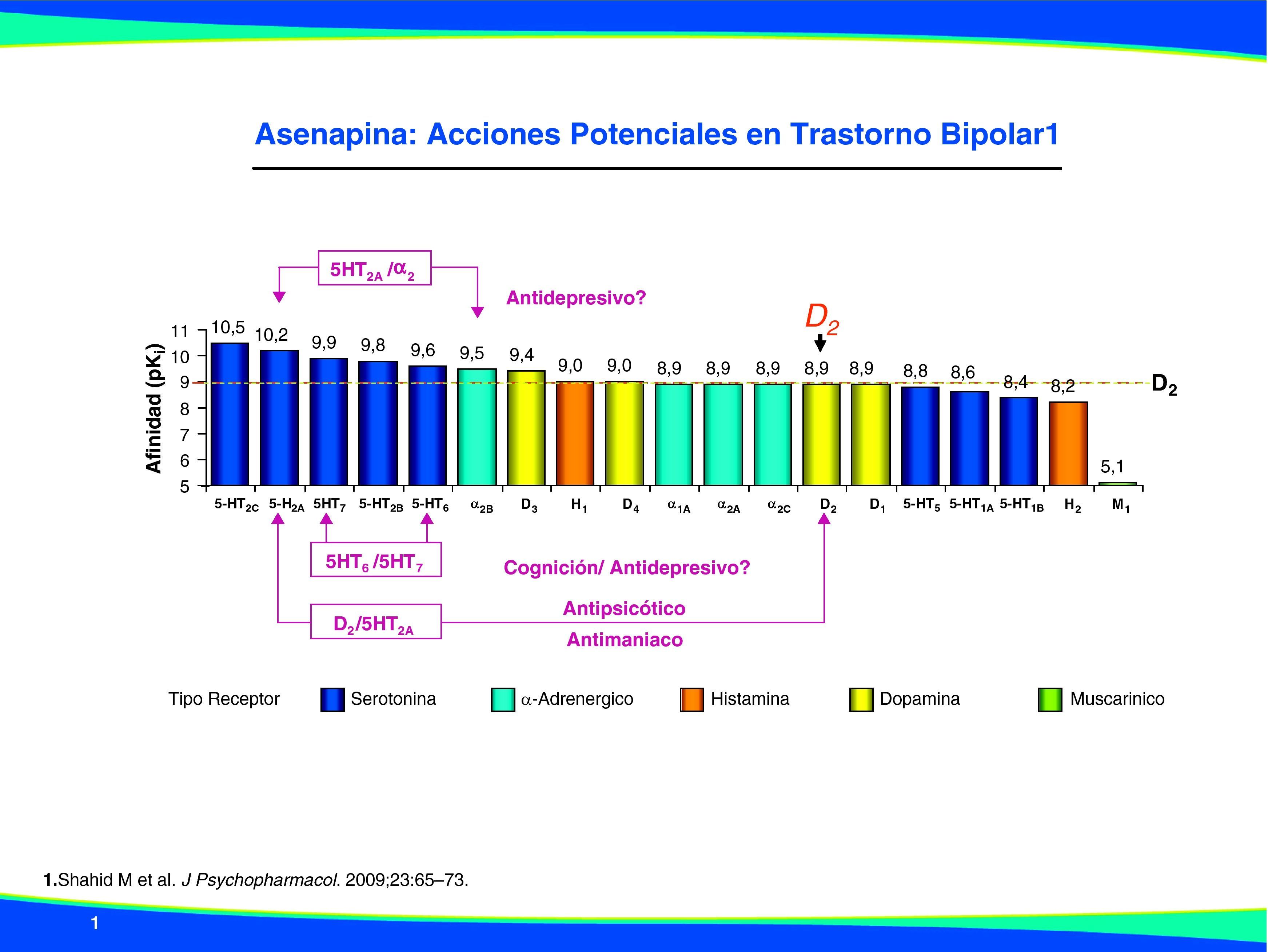
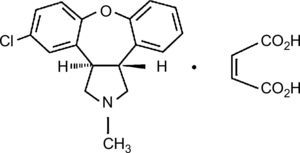
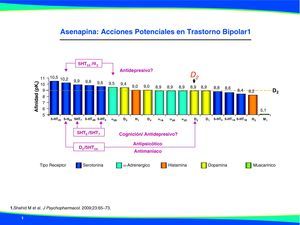
FarmacodinamiaAsenapina es un agente farmacológico novedoso en el desarrollo clínico del tratamiento de la manía. En la figura 1 se muestra la estructura química de asenapina. Este nuevo antipsicótico presenta una alta afinidad por diversos receptores, que incluye el antagonismo serotoninérgico 5HT2A, 5HT2B, 5HT2C, 5HT6 y 5HT7; adrenérgico α1A, α2A, α2B y α2C, y dopaminérgico D3 y D4. En la figura 2 se esquematiza su perfil farmacodinámico. Al igual que con los antipsicóticos atípicos, asenapina también exhibe una afinidad por los receptores D2 con una destacable afinidad serotoninérgica en la relación 5HT2A/D2. Aunque es similar a clozapina en su alta afinidad para una variedad de receptores diferentes, no tiene afinidad apreciable por los receptores muscarínicos, con la proporción más alta en la relación de afinidad entre receptores D2 y los M1, M2, M3 y M48.
La naturaleza multipotencial de este nuevo antipsicótico atípico ha dado lugar a ciertas expectativas, tanto por su eficacia como por su tolerabilidad. La mayor afinidad de asenapina para receptores 5HT2A en relación con los receptores D2 le da su «atipicidad», mecanismo encargado de la mayor selectividad de los antipsicóticos atípicos que representa un menor potencial de EPS9,10. Además, el antagonismo de los receptores 5HT2A, que conduce a un aumento de la actividad de la dopamina en la corteza prefrontal cerebral, también se ha indicado como un posible mecanismo para la mejora de la cognición11. Los resultados de estudios preclínicos reflejan un aumento dependiente de la dosis de dopamina cortical12 y del hipocampo12, además de un incremento de noradrenalina y acetilcolina13, comparables a los efectos descritos previamente para clozapina y quetiapina. Estos efectos podrían asociarse también a una cierta acción antidepresiva14,15. La evidencia emergente indica que el antagonismo del receptor 5HT6 puede ofrecer beneficios para cognición16 y que el antagonismo 5HT7 puede conferir beneficios para el control de la ansiedad y del estado de ánimo, así como también en cognición17, a pesar de que se requieren estudios más exhaustivos de confirmación8. Del mismo modo, el antagonismo de asenapina de receptores α-adrenérgicos también se ha indicado para mejorar los síntomas negativos y cognitivos por el antagonismo de los receptores α2, mientras que la mejora en los síntomas positivos es a través de los receptores α118. Los datos de estudios preclínicos también indican que el antagonismo de los receptores D3 pueden ayudar a mejorar los síntomas negativos y cognitivos19, aunque de nuevo la evidencia clínica con asenapina para estas variables aún requiere un número mayor de estudios. De hecho, en los modelos animales, asenapina a dosis superiores a las necesarias para la actividad antipsicótica disminuyó el rendimiento cognitivo debido a la perturbación de la función motora20. Sin embargo, este efecto también se ha observado con olanzapina y risperidona. Por el contrario, en estudios preclínicos con monos, asenapina ha producido una mejora sustancial en las funciones ejecutivas, que se han mantenido tras un período de dosificación a largo plazo21. Por otro lado, otros estudios en ratas han mostrado que el tratamiento crónico con asenapina ejerce, de forma dependiente de la dosis, efectos cerebrales de tipo glutamato inotrópico22.
La escasa afinidad de unión de la asenapina por el antagonismo M38 reduce la potencialidad de los efectos adversos anticolinérgicos y del síndrome metabólico asociados a olanzapina y clozapina23. Otro efecto de la asenapina, compartido con el resto de antipsicóticos atípicos, es la inducción del aumento de la dopamina en el núcleo accumbens, en comparación con la región central. El perfil farmacológico de asenapina descrito se podría traducir en beneficios clínicos específicos para el tratamiento de la manía y otras indicaciones, pero su confirmación requiere todavía de la realización de estudios pragmáticos de continuación a los estudios realizados hasta la fecha, caracterizados por un perfil más exploratorio y regulatorio.
FarmacocinéticaAsenapina se ha estudiado en humanos en presentación sublingual, y muestra una biodisponibilidad ideal del 35%, siempre que su absorción no interaccione con líquidos ni alimentos, principalmente grasos, en un rango variable de tiempo (de 10 minutos a 4 horas) respecto a su administración. Asenapina presenta una farmacocinética de tipo no lineal en relación con la dosis. Administrando el rango recomendado de 5-10mg en dos tomas diarias, la exposición al fármaco aumenta 1,7 veces en caso de doblar la dosis24,25. La vida media oscila entre 13,4 y 39,2 horas24. El metabolismo de asenapina es fundamentalmente hepático a través de los citocromos CYP1A2, principalmente, CYP 3A4 y CYP2D6, en menor grado, a pesar de que este último puede adquirir relevancia clínica en caso de combinación de asenapina con otros antipsicóticos atípicos CYP2D6 dependientes, principalmente clorpromazina, olanzapina, clozapina, perfenacina, quetiapina, risperidona, sertindol y tioridazina. No se encontraron correlaciones significativas entre el aclaramiento de creatinina y la exposición a asenapina en la insuficiencia renal. Por otro lado, a pesar de que en casos de insuficiencia hepática leve o moderada no se vio afectada la exposición a asenapina, la insuficiencia hepática grave produjo un aumento de la exposición de 7 veces. El tabaquismo no se ha asociado a cambios en la exposición de asenapina26.
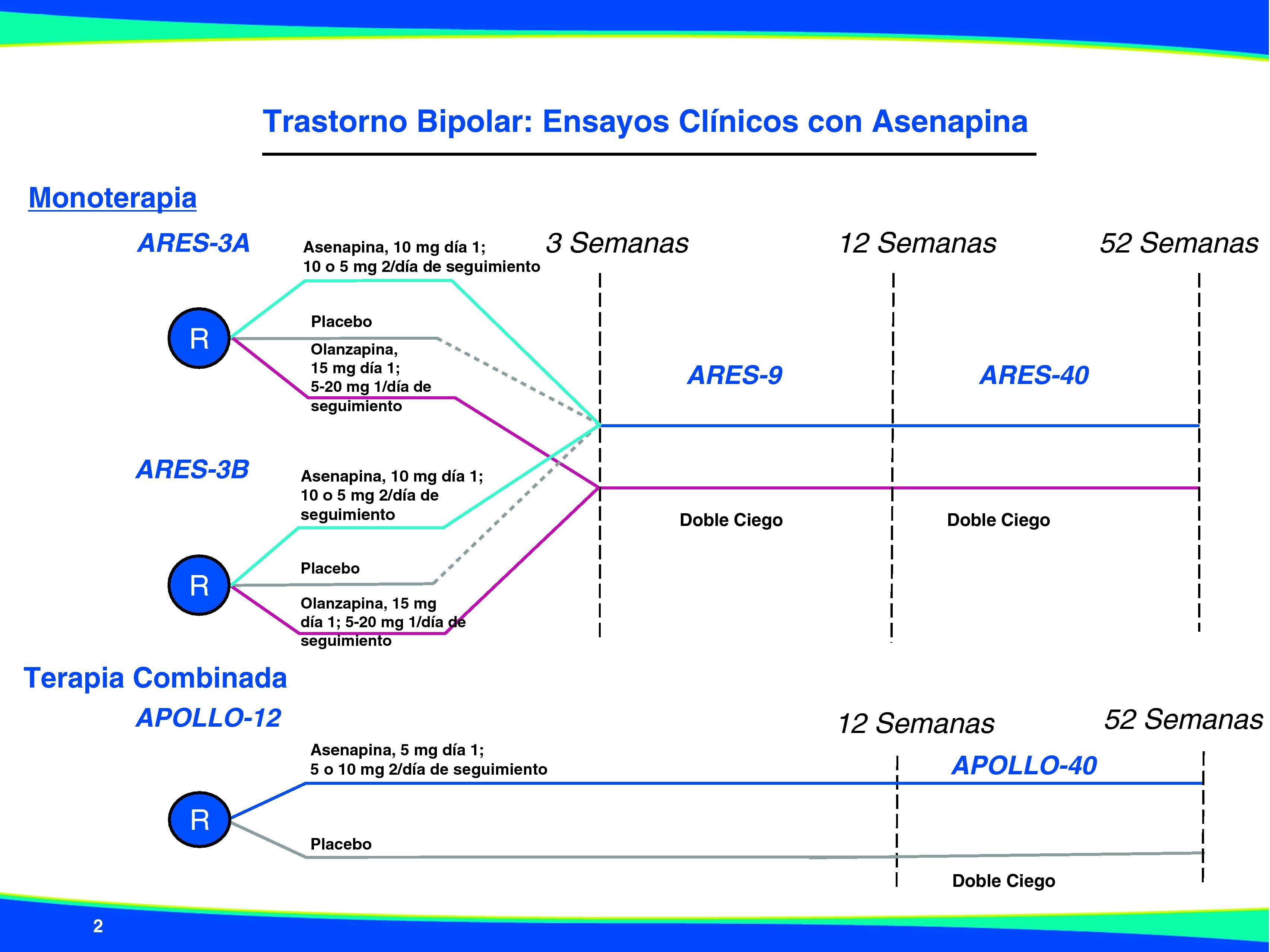
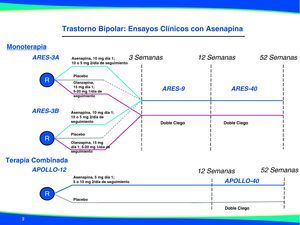
Eficacia de asenapina en ensayos clínicos en manía agudaEn la figura 3 se resumen los estudios de asenapina sublingual en manía aguda o mixta a corto y largo plazo y sus diseños. A continuación se describen los datos de eficacia y seguridad publicados hasta la fecha y que han dado lugar a la autorización de asenapina en Estados Unidos y en Europa. Básicamente se trata de 3 ensayos, dos en monoterapia y otro en terapia combinada a litio o valproato, con sus respectivas fases de extensión27–30.
Eficacia a corto plazo en monoterapiaSe han realizado un total de dos estudios de fase aguda con asenapina en fase III, aleatorizados de tres ramas y controlados con placebo y control activo en un total de 977 pacientes bipolares de tipo I con manía aguda o episodios mixtos (Ares 7501004 y Ares 7501005) durante un período de 3 semanas. Éstos se diseñaron de manera idéntica, controlados con placebo y con olanzapina en monoterapia a dosis flexible.
Se administró una dosis de asenapina sublingual de 5-10mg, en dos tomas diarias en pacientes bipolares de tipo I con episodios agudos maníacos o mixtos.
Aproximadamente, el 30% de los participantes tenían un episodio mixto y el 70% tuvo un episodio de manía pura en el episodio actual. Los individuos en ambos estudios fueron asignados aleatoriamente para recibir asenapina, olanzapina o placebo en un tratamiento aleatorizado (2: 2: 1). La dosis inicial de asenapina fue de 10mg y la de olanzapina fue de 15mg/día. Después del primer día, la dosis era flexible, basada en la eficacia, seguridad y tolerabilidad, dentro de un rango de 5-10mg en dos tomas diarias para asenapina y 5-20mg/día para olanzapina. Generalmente, los pacientes permanecieron en su dosis inicial de asenapina y menos de un 10% de los sujetos requirieron la dosis reducida. Todos los participantes tenían que ser hospitalizados por lo menos durante los primeros 7 días, para continuar de forma ambulatoria.
Como medicación concomitante se permitieron benzodiacepinas (lorazepam hasta 4mg/día) en caso de agitación, desde el día de cribado hasta el día 7 del estudio, siempre con un margen de mínimo 4 horas respecto de cualquier evaluación de eficacia, aspirina o antiinflamatorios no esferoidales para el dolor y medicación antiparkinsoniana para los síntomas extrapiramidales. En caso de insomnio, se permitieron hipnóticos (zolpidem 10mg/día, zaleplon 20mg/día o temazepam hasta 30mg/día), hasta un máximo de 3 noches por semana. La variable principal de eficacia fue el descenso en la puntuación de la escala de Young (Young Mania Rating Scale [YMRS]) respecto al estado basal. Los resultados de estos primeros dos estudios se resumen a continuación.
Estudio Ares 7501004 (registrado con el número NCT00159744)La edad promedio de los pacientes participantes fue de aproximadamente 40 años y la media de las puntuaciones basales en la escala de YMRS tuvo un rango de 28-30. Las tasas de abandono fueron del 33% para asenapina, del 20% para olanzapina y del 42% para placebo. La mejoría de la puntuación total de la YMRS fue estadísticamente significativa desde el inicio del estudio hasta el día 21, tanto para asenapina (p<0,007), como para olanzapina (p<0,0001), en comparación con el placebo. El cambio medio al final del estudio en la puntuación de la YMRS fue de 11,5±0,8 puntos para asenapina, 14,6±0,8 para olanzapina y 7,8±1,1 para la rama placebo. La mejoría estadísticamente significativa frente a placebo se observó para asenapina y olanzapina desde el día 2 en adelante. La proporción de respondedores, medido a través de la YMRS (50% de disminución respecto al valor basal) y de remisión (puntuación total de 12 o menor), como variables secundarias del estudio, fue mayor para asenapina (42,6 y 35,5%, respectivamente) que para la rama placebo (34 y 30,9%, respectivamente), aunque no alcanzó significación estadística. El número de pacientes necesario a tratar (NNT) para que uno de ellos se beneficie de la eficacia de asenapina frente a placebo fue de 12, mientras que el NNT de olanzapina frente a placebo fue de 5.
Estudio Ares 7501005 (registrado con el número NCT00159796)Este estudio también apoya la eficacia de asenapina. La edad promedio de los pacientes fue de aproximadamente 40 años y la media de las puntuaciones basales de la escala YMRS variaron de 28-29. Las tasas de abandono fueron del 37% para asenapina, del 20% para olanzapina y del 38% para la rama placebo. La mejoría en la puntuación total de la YMRS fue estadísticamente significativa desde el día 2 del estudio hasta el día 21, tanto para asenapina como para olanzapina, en comparación con la rama placebo. El cambio medio al final del estudio en la puntuación de la YMRS basal fue de 10,8±0,8 para asenapina, 12,6±0,8 para olanzapina y 5,5±1,1 para placebo. El inicio de la mejoría estadísticamente significativa en la YMRS en comparación con el placebo se observó para asenapina y olanzapina desde el día 2 en adelante. La proporción de respondedores medido a través de la YMRS (50% de disminución respecto al valor basal) y de pacientes en remisión (puntuación total de 12 o menor en la YMRS), los días 14 y 21 fue mayor para asenapina (42,3 y 40,2%, respectivamente) en comparación con el placebo (25,2 y 22,3%, respectivamente). El NNT de asenapina frente a placebo fue de 6, mientras que para olanzapina frente a placebo fue de 5.
Eficacia a medio y largo plazo en monoterapia en manía aguda: estudios de extensiónSe han realizado dos estudios de extensión para los pacientes que participaron en los estudios a 3 semanas, uno de 9 semanas (Ares 7501006; registrado con el número NCT00143182) para evaluar no inferioridad frente a olanzapina29,31, cubriendo así datos de eficacia para 12 semanas de tratamiento, seguido de otro de 40 semanas (Ares 7501007; número NCT00159783) focalizado en datos de seguridad a largo plazo30,31.
Un total de 504 individuos recibieron por lo menos una dosis de medicación del estudio doble ciego durante el ensayo de extensión de 9 semanas que representó un total de 181 pacientes tratados con asenapina y 229 pacientes tratados con olanzapina en los ensayos de fase aguda a 3 semanas comentados previamente A7501004 y A7501005 (y que continuaron con el mismo tratamiento en la extensión). Además, 94 pacientes tratados con placebo en los ensayos de fase aguda fueron reasignados a recibir asenapina 5-10mg dos veces al día en el ensayo de extensión. El diseño y las ramas farmacológicas de los estudios de extensión se encuentran también representados gráficamente en la figura 3.
Ares 7501006; número NCT00143182Las tasas de abandono fueron del 47% para el grupo de asenapina que habían recibido el placebo en los ensayos de fase aguda; del 38% para los que continuaron asenapina, y del 36% de los que continuaron con olanzapina31.
El análisis primario de eficacia demostró que asenapina fue estadísticamente no inferior a la olanzapina (p>0,05), medida por la puntuación total YMRS desde el inicio hasta el día 84 en los pacientes que presentaron 3 semanas de exposición previa a asenapina, con una media de –20,1 (± 10,7) frente a –21,3 (± 9,6) para asenapina y olanzapina, respectivamente. Las proporciones de participantes que fueron respondedores y remitentes según la escala de YMRS fueron similares en la rama de asenapina frente a la rama de olanzapina (p>0,05).
Ares 7501007; número NCT00159783La variable principal del estudio fue la seguridad y la tolerabilidad a través de la recogida de episodios adversos (EA), síntomas extrapiramidales, los valores de laboratorio y medidas antropométricas. La eficacia constituyó una variable secundaria, medida como el cambio en la YMRS calculada desde la semana 3 de referencia hasta la semana 52 para comparar asenapina frente a olanzapina. Las ramas placebo/asenapina sólo fueron evaluadas para seguridad. La incidencia de EA fue del 71,9, el 86,1 y el 79,4% con placebo/asenapina, asenapina y olanzapina, respectivamente, donde los EA más frecuentes fueron cefalea y somnolencia con placebo/asenapina; insomnio, sedación y depresión con asenapina, y aumento de peso, somnolencia y sedación con olanzapina. Entre los casos observados, la media±desviación estándar del cambio en la puntuación total YMRS en la semana 52 fueron –28,6±8,1 y –28,2±6,8 para asenapina y olanzapina, respectivamente. La limitación de este estudio representa la ausencia de rama placebo como comparador a largo plazo. En conclusión, los datos obtenidos apoyan el mantenimiento de la eficacia de asenapina posteriormente a la fase aguda; de la semana 12 a la 52, así como la buena tolerabilidad de ella.
Eficacia en combinación con litio o valproatoUn tercer estudio evaluó la eficacia de asenapina a dosis de 5-10mg/día en dos tomas diarias frente a placebo, en manía aguda o episodios mixtos en combinación con litio o valproato (estos últimos sin enmascaramiento) durante 12 semanas (Apollo 12; 7501008) y a continuación se realizó una extensión de seguridad hasta 40 semanas (Apollo 12; 7501009) para los pacientes que completaron el primer estudio a 12 semanas. Los resultados no se han publicado todavía, pero se dispone de los resultados de eficacia a 12 semanas que demuestran la superioridad de asenapina en combinación frente a los eutimizantes en monoterapia en cuanto a la mejoría de los síntomas de manía aguda en bipolares tipo I y que ha motivado la opinión positiva del CHMP para su autorización en Europa.
Seguridad de asenapina en ensayos clínicosAsenapina ha sido globalmente bien tolerada y tiene un efecto mínimo en la prolactina y los parámetros metabólicos. Evaluaciones cardiovasculares no han encontrado ningún motivo de preocupación y los efectos de asenapina en prolongación del intervalo QTc fueron comparables a la quetiapina, en el rango de dosis más alta de asenapina, aunque la incidencia de síntomas extrapiramidales (SEP) fue mayor con asenapina que olanzapina en uno de los estudios.
Los efectos secundarios más frecuentemente asociados a asenapina (observados en más de 1 de cada 10 pacientes) son la ansiedad y la somnolencia. Otros EA frecuentes (observados en entre 1 y 10 de cada 100 pacientes) son el aumento de peso, aumento del apetito, distonía (lenta o sostenida contracciones musculares), acatisia (inquietud), discinesia (contracciones musculares involuntarias), parkinsonismo (movimientos lentos y temblor), sedación, mareos, disgeusia (alteración del gusto), hipoestesia oral (sensación de entumecimiento de la lengua o en la boca), aumento de la alanina aminotransferasa (aumento del nivel de proteínas del hígado), rigidez muscular y la fatiga.
En términos de seguridad, las tasas de incidencia de EA relacionados con el tratamiento fueron del 65,7% para asenapina y del 61,7% para olanzapina. Aunque la elevación de prolactina, aumento de peso y el síndrome metabólico son más frecuentes en el grupo de olanzapina, los SEP fueron más frecuentes con asenapina32.
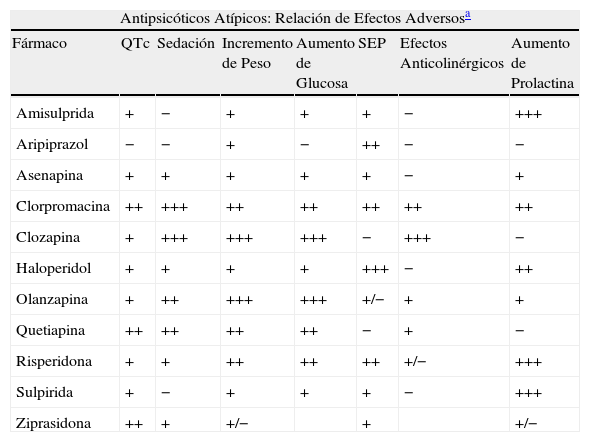
En la tabla 1 se resumen los EA de asenapina en comparación con otros antipsicóticos.
Efectos adversos de asenapina en comparación con otros antipsicóticos
| Antipsicóticos Atípicos: Relación de Efectos Adversosa | |||||||
| Fármaco | QTc | Sedación | Incremento de Peso | Aumento de Glucosa | SEP | Efectos Anticolinérgicos | Aumento de Prolactina |
| Amisulprida | + | − | + | + | + | − | +++ |
| Aripiprazol | − | − | + | − | ++ | − | − |
| Asenapina | + | + | + | + | + | − | + |
| Clorpromacina | ++ | +++ | ++ | ++ | ++ | ++ | ++ |
| Clozapina | + | +++ | +++ | +++ | − | +++ | − |
| Haloperidol | + | + | + | + | +++ | − | ++ |
| Olanzapina | + | ++ | +++ | +++ | +/− | + | + |
| Quetiapina | ++ | ++ | ++ | ++ | − | + | − |
| Risperidona | + | + | ++ | ++ | ++ | +/− | +++ |
| Sulpirida | + | − | + | + | + | − | +++ |
| Ziprasidona | ++ | + | +/− | + | +/− | ||
SEP = síntomas extrapiramidales.
Un plan de farmacovigilancia para asenapina se llevará a cabo en el marco de la autorización de comercialización europea33.
Conclusiones y aplicabilidad terapéuticaA pesar de la amplia variedad de antipsicóticos disponibles en el mercado, todavía hay la necesidad de optimizar el tratamiento del trastorno bipolar, especialmente para abarcar las áreas de la cognición y del deterioro funcional asociado a la cronicidad de la enfermedad. Por otro lado, cualquier mejoría en el perfil de tolerabilidad de los antipsicóticos atípicos, especialmente el síndrome metabólico, puede aportar, no sólo una mejoría del beneficio-riesgo y de la calidad de vida de los pacientes, sino que también aumenta la probabilidad de adherencia terapéutica. La dosificación y la titulación de la asenapina en el tratamiento de la manía, según la evidencia de los ensayos clínicos realizados en fase III, consiste en la administración de una dosis de 10 a 20mg/día dividido en dos tomas diarias que puede ser aumentada o disminuida a un ritmo de 5mg/día semanalmente, en función de la tolerabilidad. Como inconveniente, su presentación sublingual de dos veces al día y la recomendación de que ningún alimento o líquidos se consuman durante 10 minutos tras la administración puede ser un obstáculo hacia su adopción y requiere un esfuerzo psicoeducativo en los pacientes. Es posible que éstos se quejen de sabor amargo o desagradable, aunque la administración sublingual puede favorecer las garantías de que la medicación ha sido tomada y puede presentarse como una ventaja al evitar el tránsito gastrointestinal. Aripiprazol o ziprasidona comparten algunas de las ventajas de tolerabilidad de asenapina; sin embargo, se requieren más alternativas. Asenapina tiene afinidad por un gran número de receptores que incluyen el antagonismo de receptores serotoninérgicos, dopaminérgicos y adrenérgicos, pero, a diferencia de la clozapina, no tiene afinidad por los receptores muscarínicos, lo que le confiere una tolerabilidad mejor. Su mecanismo de acción podría conferirle propiedades antidepresivas34. En síntesis, asenapina presenta un perfil metabólico favorable respecto a olanzapina, y una baja propensión a síntomas extrapiramidales en comparación con haloperidol. Se ha asociado con mayor frecuencia que placebo con somnolencia, mareos, acatisia, SEP y aumento de peso. En el trastorno bipolar, asenapina se ha mostrado comparable en cuanto a eficacia a 12 semanas frente a olanzapina y con eficacia mantenida durante 40 semanas, con buenos datos de seguridad a largo plazo.
Asenapina podría tener ventajas de tolerabilidad y para la función cognitiva, si nos basamos en su farmacodinamia frente a otros antipsicóticos, aunque se requiere un número mayor de estudios para demostrar su relevancia clínica y la capacidad de mejorar la capacidad funcional a largo plazo. En un futuro cercano, se podría disponer de datos concluyentes en esquizofrenia y en depresión bipolar, que en caso de ser favorables podrían complementar la indicación de manía aguda si los estudios se muestran tan positivos como en esta indicación.
Conflicto de interesesEl Dr. Vieta ha recibido apoyo a la investigación y honorarios como consultor o ponente por parte de las siguientes compañías: Almirall, AstraZeneca, Bristol-Myers Squibb, Eli Lilly, Forest Research Institute, Geodon Richter, Glaxo-Smith-Kline, Janssen-Cilag, Jazz, Lundbeck, Merck Sharpe and Dohme, Novartis, Organon, Otsuka, Pfizer, Pierre-Fabre, Qualigen, Sanofi-Aventis, Servier, Shering-Plough, Solvay, Takeda, y Wyeth.
La Dra. Cruz no manifiesta ningún conflicto de interés.
Los autores agradecen al Ministerio de Ciencia e Innovación, Instituto de Salud Carlos III, CIBERSAM y a la Generalitat de Catalunya (2009 SGR 1022) su ayuda en el Programa de Investigación del Trastorno Bipolar de Barcelona.