Introducción
El envejecimiento de la población está provocando nuevas necesidades de atención y esta nueva realidad va a modificar la atención sanitaria, social, política y económica de los países desarrollados. El índice de envejecimiento, según datos del padrón del año 2003, es del 17% (población mayor de 65 años entre el total de la población) estimándose, según proyecciones demográficas, que para el año 2050 alcanzará el 35%; España es, tras Japón, el segundo país más envejecido del mundo. El tramo de edad que más va a crecer es el de los mayores de 80 años, que pasarán del 4 al 11% provocando el fenómeno conocido como "envejecimiento del envejecimiento"1,2.
El dolor debe considerarse como un síndrome geriátrico, al ser fuente de deterioro funcional, de causa multifactorial y cuya identificación depende de una valoración multidisciplinar. Sin embargo, el dolor se encuentra infradiagnosticado e infratatado, por lo que la Asociación Internacional de Estudio del Dolor (IASP) declaró el año 2007 como el año del dolor en las personas mayores.
Hay escasos datos de prevalencia en el ámbito nacional. La prevalencia estimada de dolor es de un 25-40% en la comunidad, aumentando a un 71-88% en medios residenciales. Se estima que la prevalencia de dolor crónico en población geriátrica alcanza el 50-80%, y aumenta especialmente en el último año de vida. En el 40% de los casos no se llega a alcanzar un adecuado control de éste. Por otro lado, es conocido que en dichos segmentos de población el uso de opiáceos es menor3,4.
En la Encuesta Nacional de Salud del año 2006, el porcentaje de personas mayores de 65 años que no tienen una valoración positiva de su salud es del 52% en varones y del 66% en mujeres, aumentando con relación a la edad, por lo que puede considerarse un factor de riesgo de reducción del umbral álgico5. La presencia de comorbilidad en la población geriátrica es muy frecuente, especialmente de procesos osteoarticulares (osteoartritis, osteoporosis y sus consecuencias como fracturas vertebrales y no vertebrales), por lo que va a ser frecuente la aparición de dolor.
La presencia de dolor está relacionada con trastornos del sueño, alteraciones nutricionales, depresión, deterioro funcional y aumento de recursos sanitarios, aspectos todos ellos que alteran en gran medida la calidad de vida de la persona y de su entorno, con la circunstancia de tratarse de personas con expectativa de vida corta6,7.
Con relación a los cambios que se producen con el envejecimiento, el paciente geriátrico presenta problemas para la discriminación y localización del dolor. La respuesta puede ser de menor intensidad y más lenta que en población adulta. La experiencia sensorial y emocional dependerá, en gran medida, de influencias culturales, sociales, tipo de personalidad previa y estado afectivo. Con la edad aumenta la frecuencia de aparición de dolores atípicos como síntoma de diversas enfermedades, retrasando su diagnóstico y, por tanto, dificultando el pronóstico y graduación de la gravedad (p. ej., infarto agudo de miocardio sin dolor, abdomen agudo asintomático)8.
El dolor maligno es más frecuente con el envejecimiento, ya que la presencia de neoplasias aumenta con la edad. Así, el 60% de todas las neoplasias y el 70% de todas las muertes producidas por cáncer se desarrollan en personas mayores de 65 años. Un adecuado control de síntomas y la correcta identificación de necesidades psicológicas y espirituales garantizan un óptimo manejo del paciente geriátrico oncológico. En estudios en pacientes institucionalizados con dolor maligno, hasta el 29% presenta dolor diario, muchas veces no tratado. En ancianos de la comunidad con procesos oncológicos en fase terminal, el 87-90% presenta dolor que en un 13% es de intensidad elevada9,10.
En cuanto a los factores que influyen en una infrautilización de recursos terapéuticos, se encuentran aspectos del propio paciente, que lo asume como cambios inherentes a la edad, miedo a molestar, incomodidad a realizar pruebas complementarias; asimismo, la familia lo ve como cambios propios del envejecimiento y esta percepción la tienen también algunos profesionales sanitarios.
Los problemas de comunicación y sensoriales (visuales y auditivos) dificultan, en gran medida, la valoración adecuada del dolor así como la creencia o el miedo a reacciones adversas a fármacos, limitando la utilización de fármacos adecuados para su control.
Las personas con deterioro cognitivo presentan una doble discriminación: primero por la edad, y segundo por la enfermedad neurodegenerativa que dificulta la comunicación. Así, hay estudios en paciente con demencia y fractura de cadera, donde se administra un 50% menos de opiáceos con relación a controles sin demencia. Es frecuente la presentación de dolor en forma de trastornos conductuales, cuadro confusional, disminución de movilidad y posturas antiálgicas que, en último término, provocan sobrecarga del cuidador principal11,12. Para realizar una adecuada valoración de un aspecto tan subjetivo como el dolor en pacientes con dificultad de comunicación, es fundamental disponer de información adecuada por parte de los cuidadores habituales, formales e informales.
La detección precoz y sistemática del dolor debe constituir una prioridad asistencial en el paciente geriátrico. Con este objetivo, se ha realizado un estudio para determinar la prevalencia de dolor en población institucionalizada, valorando las posibles variables asociadas y estableciendo métodos adecuados de detección del dolor, especialmente en las personas con problemas de comunicación.
Material y método
Se realiza un estudio descriptivo transversal a lo largo del año 2007 en 2 centros residenciales de San Sebastián, gestionados por Fundación Matia: Residencia Alai-Etxe (69 residentes) y Txara 1 (120 residentes).
En los pacientes sin deterioro cognitivo se recoge información acerca de la presencia de dolor en las últimas 2 semanas, recogiendo sus características, localización, intensidad, frecuencia, historia farmacológica, escalas de valoración afectiva (Yesavage), ansiedad (Hamilton), capacidad funcional (índice de Barthel), comorbilidad (índice de Charlson). Para valorar la intensidad del dolor se administra la escala visual analógica (EVA), escala numérica del dolor y escala descriptiva del dolor, con el objetivo de identificar en dicha población la más adecuada.
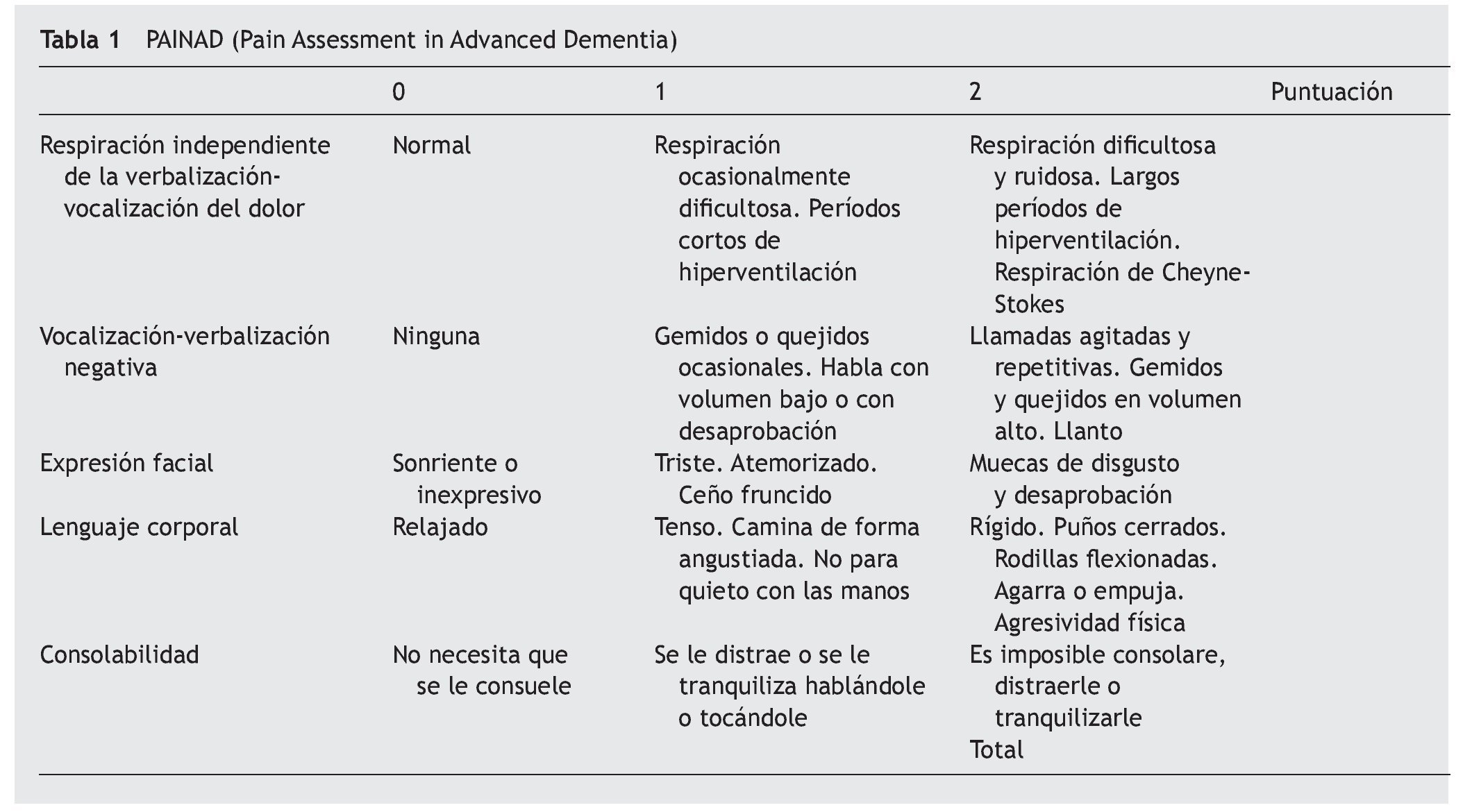
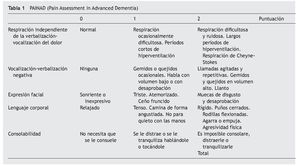
En los residentes con deterioro cognitivo se pasa la escala PAINAD (Pain Assessment in Advanced Dementia)13 que contempla aspectos no verbales y de respuesta vegetativa, como el tipo de respiración, verbalización, expresión facial, lenguaje corporal, consolabilidad, con una puntuación de 0 a 10. El cuestionario se administra a los auxiliares o gerocultores que hayan estado en contacto con la persona que se estudia las últimas 2 semanas (tabla 1). La valoración afectiva se determina a través de la escala de depresión de Cornell, y la valoración conductual mediante la escala NPI-NH (Neuropsichiatric Inventory-Nursing Home). Para el diagnóstico de los diferentes tipos de demencia se siguen los criterios del DSM IV y del NINCDS-ADRA (National Institute of Neurological and Communicative Disorders and Stroke and the Alzheimer's Disease and Related Disorders Association).
A todos los residentes, en el momento del ingreso y periódicamente, se les realiza una valoración geriátrica integral, que incluye una valoración física (antecedentes personales, exploración física, hemograma y bioquímica, electrocardiograma, valoración nutricional), otra valoración psíquica (cognitiva, afectiva y conductual), otra funcional a través de la determinación de actividades básicas de vida diaria (ayuda en higiene, alimentación, vestido, continencia, marcha) con el índice de Barthel, y las actividades instrumentales de vida diaria (uso de teléfono, asuntos económicos, medios de transporte) con el índice de Lawton y, por último, una valoración social.
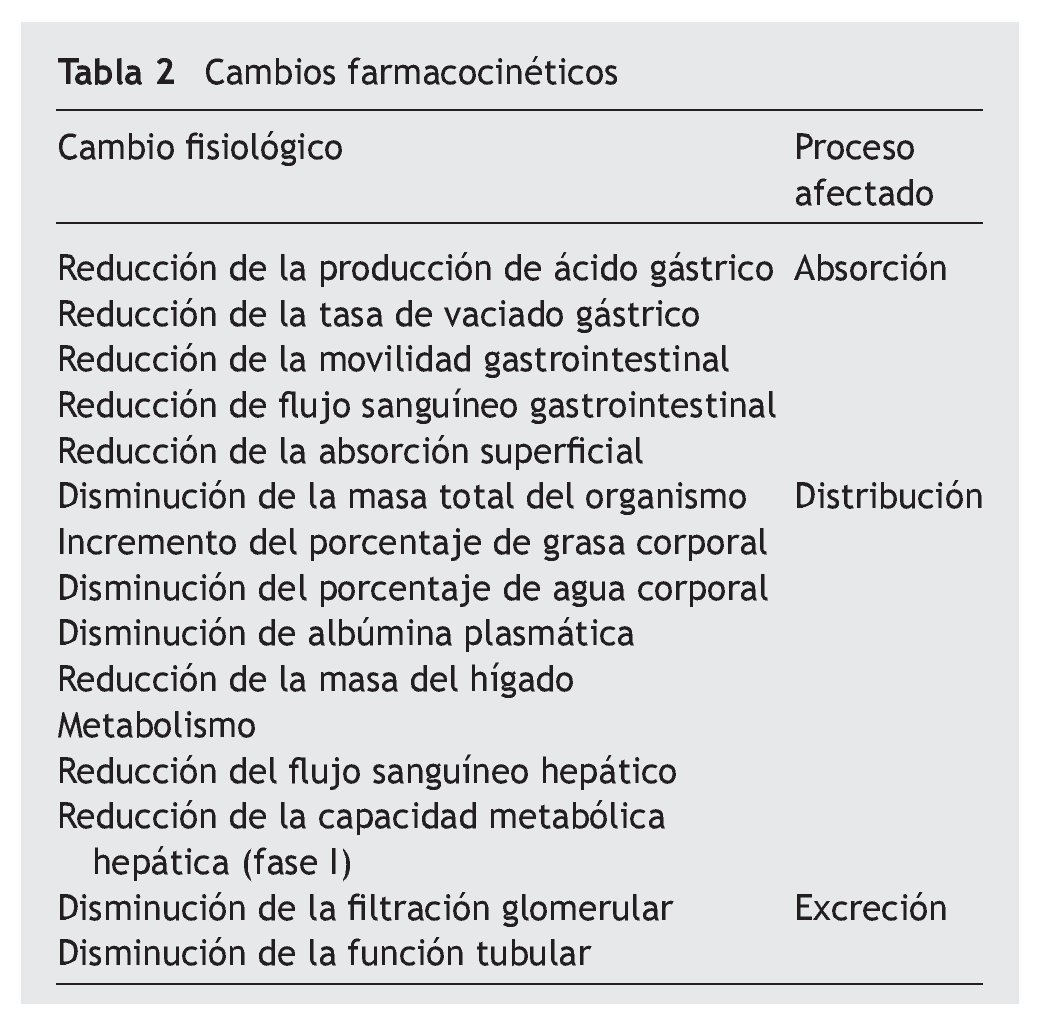
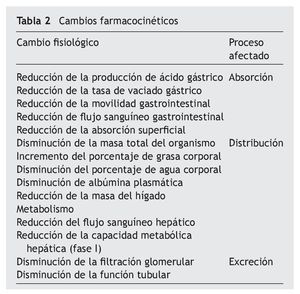
De los cambios farmacocinéticos que se producen en el paciente geriátrico (taba 2), los más relevantes se deben a los cambios en la eliminación urinaria; de esta forma, las cifras de creatinina no son representativas de la función renal en el paciente geriátrico, por lo que se determina el aclaramiento de creatinina según la fórmula de Cockroft y Gault, excepto en los residentes con un índice de masa corporal >35 o < 19 kg/m2, presencia de amputaciones o enfermedades neuromusculares. Según la National Kidney Foundation, se considera enfermedad renal crónica de acuerdo al aclaramiento de creatinina como grado 1 si es > 90 ml/ min, grado 2 de 60 a 90 ml/min, grado 3 de 30 a 60 ml/min, grado 4 de 15 a 30 ml/min y grado 5 si es < 15 ml/min o precisa de terapia sustitutiva renal.
El análisis estadístico se realiza con el sistema informático SPSS11.0, el cálculo de correlaciones entre las diferentes variables se realiza a través de pruebas no paramétricas al ser una población muy seleccionada, no siguiendo las variables una distribución normal.
Resultados
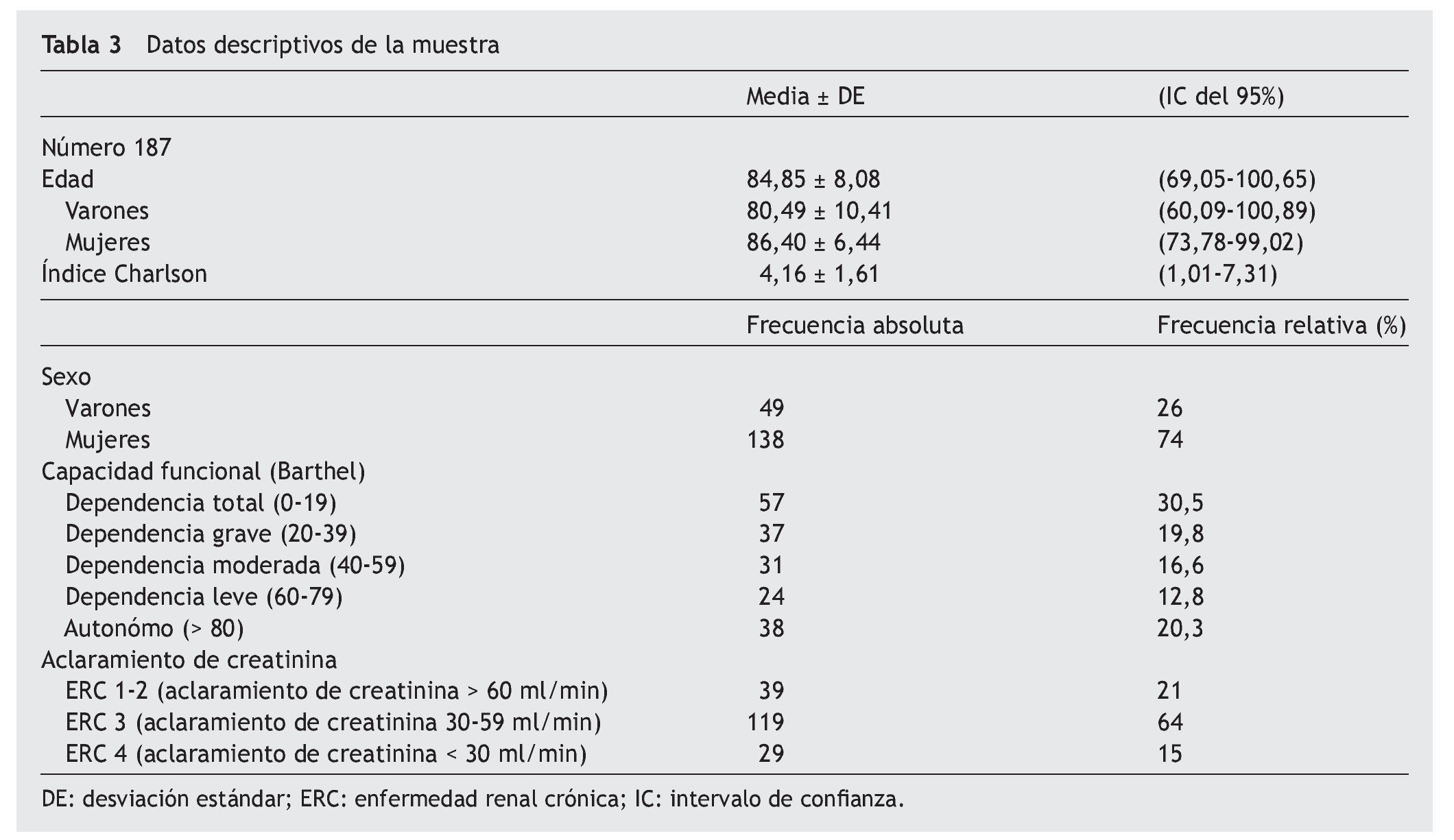
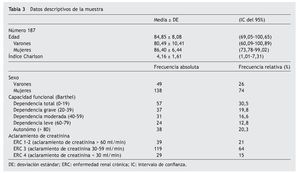
El tamaño muestral es de 187 residentes analizados, con una edad media de 84,8 años (desviación típica, 8,08), donde el 73,8% son mujeres. Siendo superior la edad media de las mujeres que la de los varones, aunque ambas sobrepasan la expectativa de vida, que en los varones es de 78 años y en las mujeres de 84 (tabla 3).
En la valoración funcional se aprecia que un 40% de los residentes presenta dependencia grave o total, con una alta comorbilidad que indica la pluripatología de los residentes y donde un 64% de los residentes cumple criterios clínicos de demencia.
Un 79% de los residentes presenta aclaramientos de creatinina < 60 ml/min, cuyo conocimiento es importante para el manejo farmacológico, garantizando la máxima seguridad de los fármacos prescritos, especialmente en la población geriátrica donde la polifarmacia es frecuente.
Residentes sin deterioro cognitivo
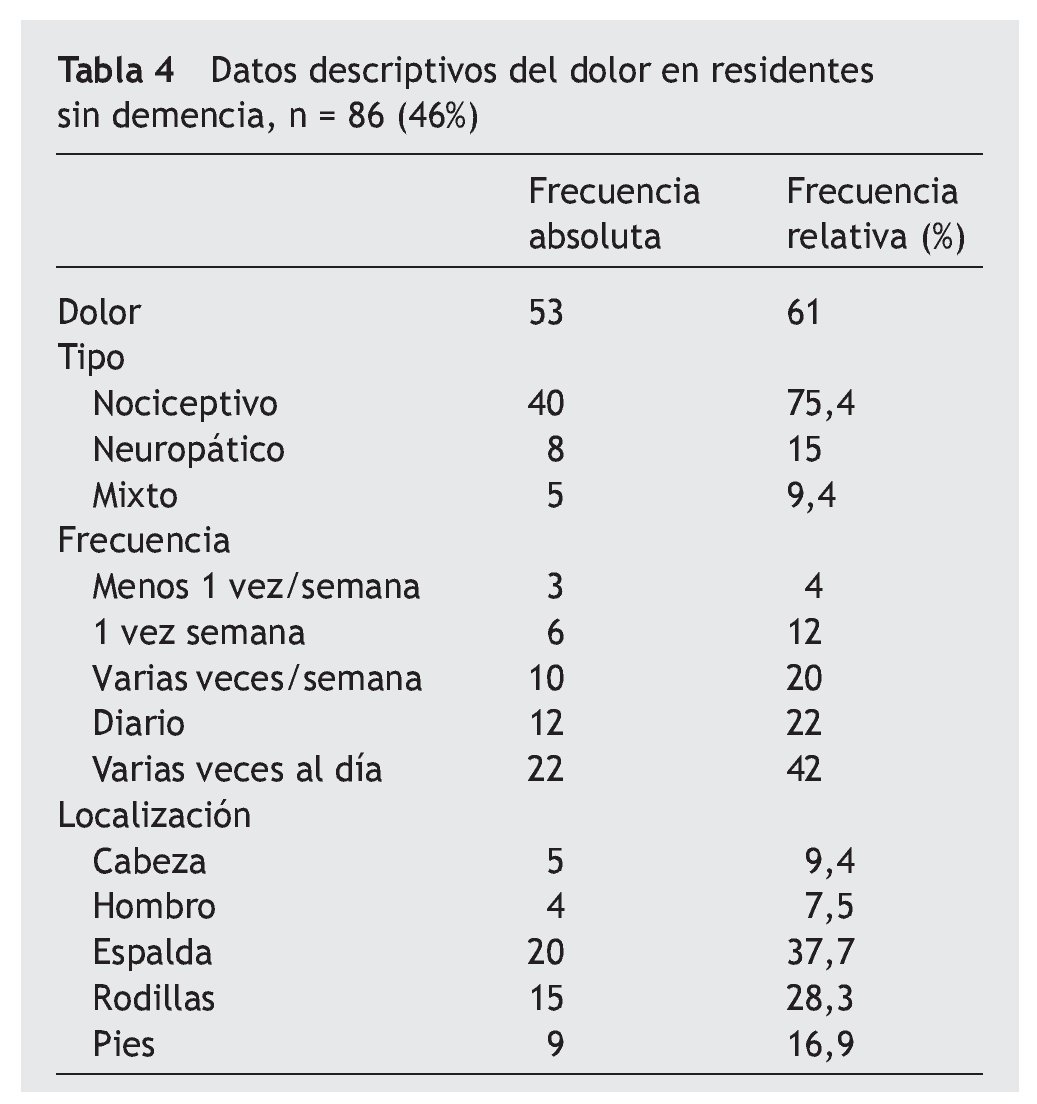
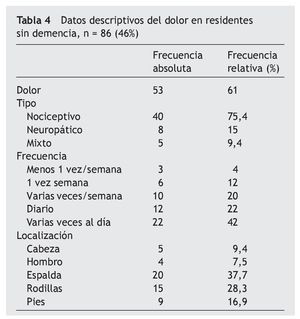
La prevalencia de dolor es del 61%, principalmente de tipo nocicéptivo somático y en menor porcentaje neuropático.
En un 64% de los residentes el dolor es diario o varias veces al día (tabla 4).
Para medir la intensidad del dolor la escala más utilizada ha sido la escala numérica del dolor, que ha sido cumplimentada por el 57% de la muestra; sin embargo, la EVA ha sido cumplimentada por el 5,9% y la escala descriptiva del dolor por un 14%.
Mediante la escala numérica, un 56% refiere intensidad severa ≥ 6 puntos y, con la escala cuantitativa, es > 6 puntos en un 31%. Con las diferentes escalas se aprecia que en un 29% de los residentes el dolor es muy intenso (≥ 6 puntos).
El dolor es generalizado, sin una localización precisa, en un 8% de los residentes. En los varones el dolor predomina en la espalda y en las mujeres en las piernas.
En cuanto a los tratamientos analgésicos, se aprecia que un 35,7%, en el momento del estudio descriptivo, está con fármacos del primer escalón de la escalera analgésica de la Organización Mundial de la Salud, un 4,8% en un segundo escalón y un 4% con fármacos opiáceos mayores. Como coadyuvantes, la prevalencia de uso de anticomiciales es del 18%, inhibidores selectivos de la recaptación de serotonina en un 37%, triciclicos (principalmente amitriptilina) en un 3%.
En el contraste de hipótesis, la presencia de dolor se correlaciona estadísticamente con la capacidad funcional (p < 0,05, test Mann Whitney), y no hay correlación con la comorbilidad, nivel de ansiedad (p = 0,09, test χ2) o de depresión. La intensidad del dolor se correlaciona con la capacidad funcional y nivel de ansiedad (coeficientes de correlación de Spearman).
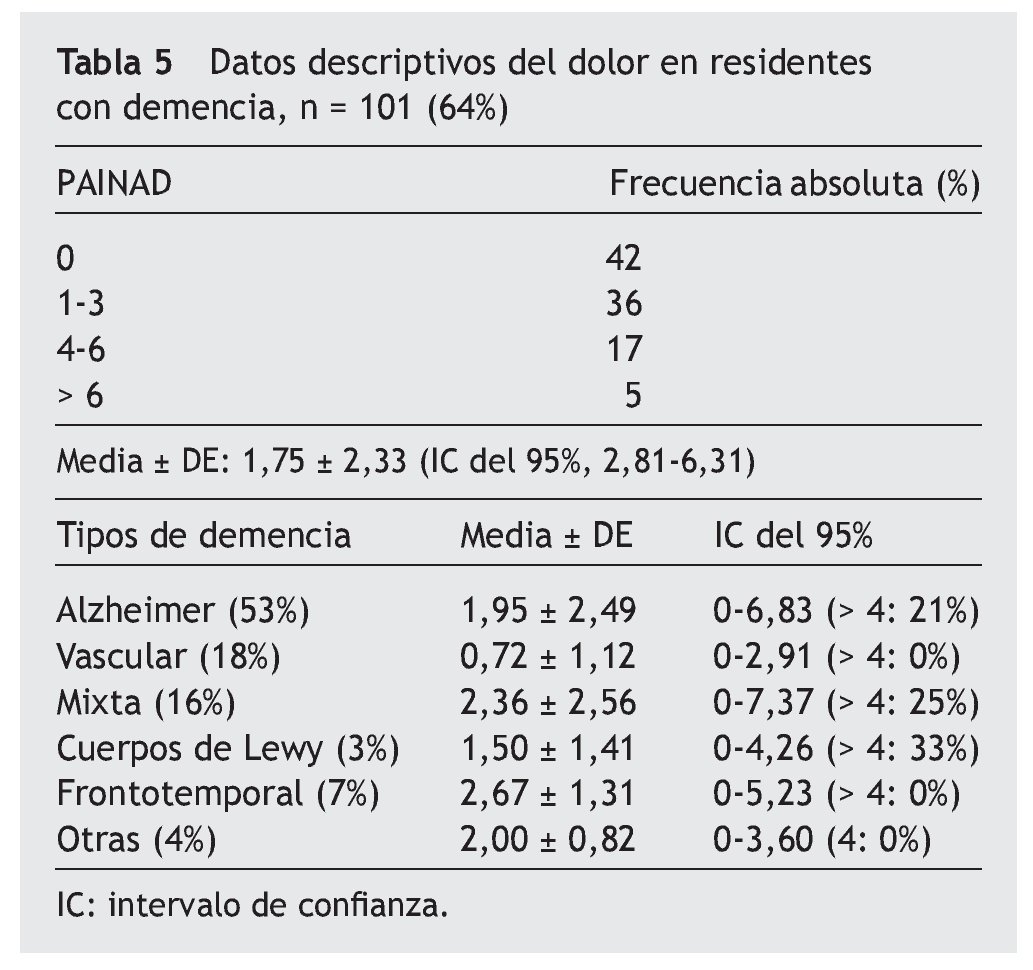
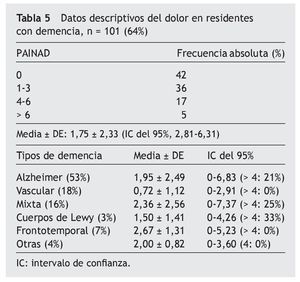
Pacientes con deterioro cognitivo (tabla 5)
La escala de PAINAD es > 4 en un 22%, puntuando 0 puntos en un 42% de los pacientes valorados, y no hay cambios estadísticamente significativos con relación al tipo de demencia (demencia frontotemporal y mixta mayores puntuaciones medias, siendo frecuencias > 4 en Lewy, mixta y Alzheimer). En el análisis multivariable hay correlación estadísticamente significativa según el análisis de Kruskall Wallis entre la comorbilidad y tipo de demencia (mayor en demencia mixta y degenerativa tipo Alzheimer), así como los trastornos conductuales y etiología de demencia (mayor puntuación NPI [Neuropsichiatric Inventory] en demencia frontotemporal y de cuerpos de Lewy). Al realizar análisis de regresión lineal hay correlación entre la puntuación de la escala PAINAD con el índice de Barthel (p = 0,036), escala de depresión de Cornell (p < 0,01), escala de valoración conductual NPI-NH (p = 0,013), y no es estadísticamente significativa con el índice de comorbilidad de Charlson (p = 0,251). La correlación de Spearman entre los datos conductuales mediante el NPI y el PAINAD es de 0,24 (p < 0,014).
Las cifras de creatinina de todos los residentes únicamente son superiores a 1,5 mg/dl en el 4% de toda la muestra, al realizar aclaramiento de creatinina se aprecia que es < 30 ml/min en un 23% de residentes, y entre 30-60 ml/min en el 58%. Ello implica que el 81% del total de la muestra analizada presenta enfermedad renal crónica con estadificación 3 o 4. Este dato es importante por las repercusiones tanto dietéticas como terapéuticas que conlleva.
Discusión
La población geriátrica institucionalizada de la muestra presenta gran dependencia, una edad media cercana a la expectativa de vida de la población general, sexo femenino y deterioro cognitivo, considerándose como el perfil de residente más frecuente en los diferentes centros gerontológicos.
La prevalencia de dolor en pacientes sin deterioro cognitivo del 61% es inferior a la de otros estudios epidemiológicos que alcanza al 70-80% de la población residencial. Sin embargo, en una cuarta parte de los pacientes con dolor, éste es de intensidad severa, lo cual contrasta con una infrautilización de opiáceos, que no llega al 5%.
La escala de medición acerca de la intensidad del dolor más aceptada es la escala numérica del dolor, aunque su medición es compleja en dichos pacientes por la variabilidad en las respuestas de ésta, retraso en la comprensión que, junto a la deprivación sensorial visual y auditiva, afecta en gran medida a la validez y fiabilidad de ésta.
Hay una correlación entre el nivel de discapacidad y el deterioro funcional con la presencia de dolor, por lo que todas las medidas preventivas y rehabilitadoras de ésta incidirán directamente en un mejor control del dolor.
De los pacientes con deterioro cognitivo, el 22% de la muestra analizada presenta dolor de intensidad moderada o severa, con escasa capacidad de comunicarlo, influyendo como factores de riesgo la capacidad funcional, el estado afectivo y el conductual.
La correlación conductual con la presencia de dolor es baja (r: 0,24), aunque estadísticamente significativa.
Hay controversia en cuanto al instrumento más adecuado para la valoración del dolor en pacientes con demencia, existiendo más de 30 escalas de las cuales las más validadas son la PACSLAC (Pain Assessment Checklist for Seniors with Limited Ability to Comunícate) y DOLOPLUS 2. La escala utilizada en este estudio, la PAINAD, en diferentes estudios ha demostrado su validez y fiabilidad, aunque con muestras pequeñas, y es sencilla de realizar14,15.
Hay estudios donde hacen énfasis en la valoración a través de autoescalas en pacientes con demencia leve o moderada, e incluso en pacientes con demencia severa, lo que contrasta en la práctica asistencial con la severa dificultad de comunicación que presentan16.
Por todo ello, actualmente, hay un dilema acerca del uso de escalas observacionales o autoescalas para la identificación del dolor en pacientes con demencia.
Cohen-Mansfield y Lipson17 postulan que puede haber una disminución en la percepción del dolor con relación al grado evolutivo de la enfermedad neurodegenerativa, posiblemente relacionado al daño de circuitos corticosubcorticales; por ello, las cifras de prevalencia de dolor en los pacientes con demencia es inferior (< 25%) que en aquellos sin deterioro cognitivo.
Estos datos hay que analizarlos como medidas de frecuencia transversales, donde las correlaciones que se establecen suponen hipótesis qye hay que desarrollar, pues en un estudio de cohortes hay multicausalidad y multiefectividad.
La fiabilidad de la valoración dependerá, en gran medida, de la capacidad observadora del cuidador, con el sesgo que puede suponer en el ámbito comunitario la sobrecarga de cuidado del cuidador principal, especialmente en los pacientes que a lo largo de su vida hayan presentado episodios previos de dolor intenso (fracturas vertebrales, convalecencias de fracturas pelvianas o femorales).
Dentro de la escasa investigación nacional en este campo, destaca un artículo en una unidad de convalecencia donde es superior la correlación de la información obtenida de la entrevista médico/paciente que la de enfermera/paciente, aunque todas las fuentes de información se deben tener en cuenta18.
Frecuentemente, los pacientes refieren dolor leve-moderado y éste no queda registrado en la historia clínica, especialmente si el paciente padece una demencia. Su registro y valoración provoca una mejora de los cuidados de forma global, permitiendo la comprobación de los cuidados asistenciales a través de auditorías.
Las instituciones y el personal sanitario (médico, enfermería, gerocultores) deben disponer de herramientas de detección del dolor, observando/preguntando sistemáticamente acerca de su presencia en los residentes, especialmente en aquellos con problemas de comunicación (demencia, afasias, aislamiento sensorial severo) a través de escalas que analicen respuestas no verbales al dolor. Una vez detectada la presencia de dolor, la realización de un procedimiento de actuación elaborado multidisciplinarmente (médicos de familia, geriatras, unidades de dolor, rehabilitación), con unos indicadores de seguimiento y monitorización, permitirá una mejora de la calidad asistencial, estableciendo cauces de derivación para técnicas más complejas en caso de necesidad.
Asimismo, la formación del equipo interdisciplinario en aspectos de detección y manejo del dolor, incrementa la sensibilización en un aspecto de gran importancia en la consecución de una adecuada calidad de vida a los residentes.
El uso adecuado de fármacos en los pacientes geriátricos, requiere del conocimiento de los cambios farmacocinéticos con la disminución de agua corporal e incremento de grasa que modifica los volúmenes de distribución y los cambios en la filtración glomerular que se producen con el proceso de envejecimiento.
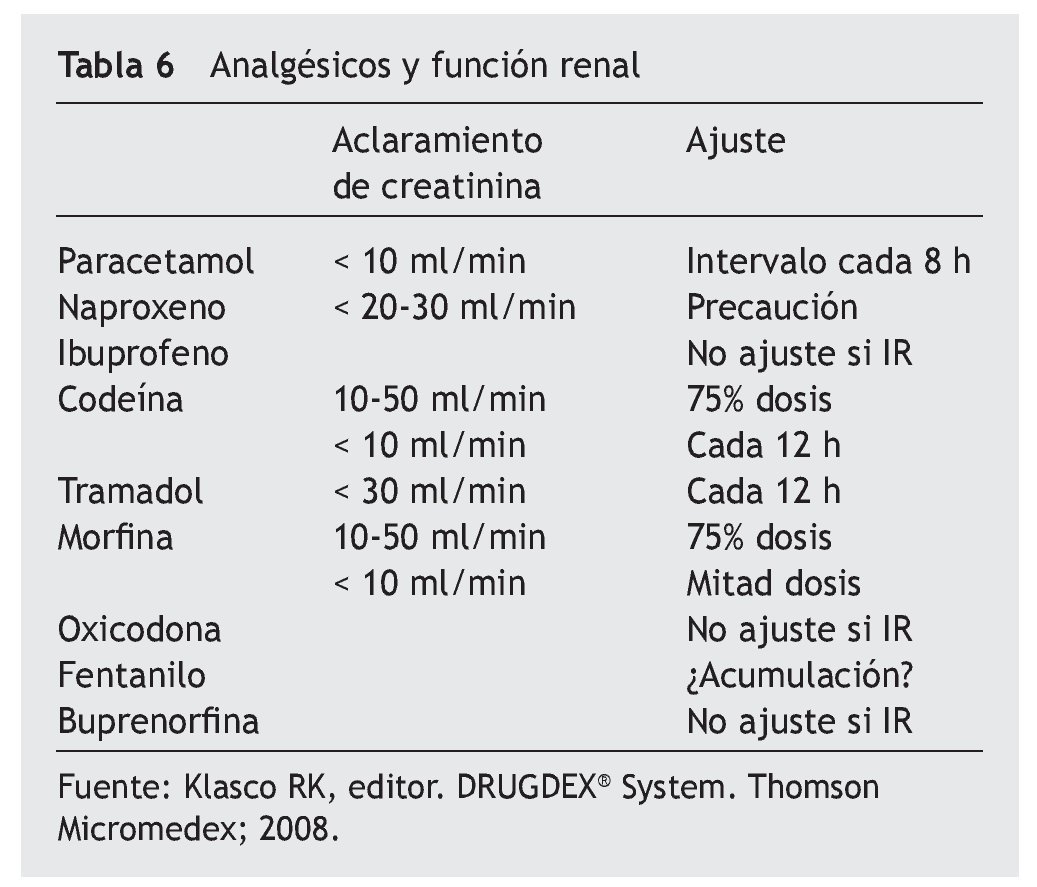
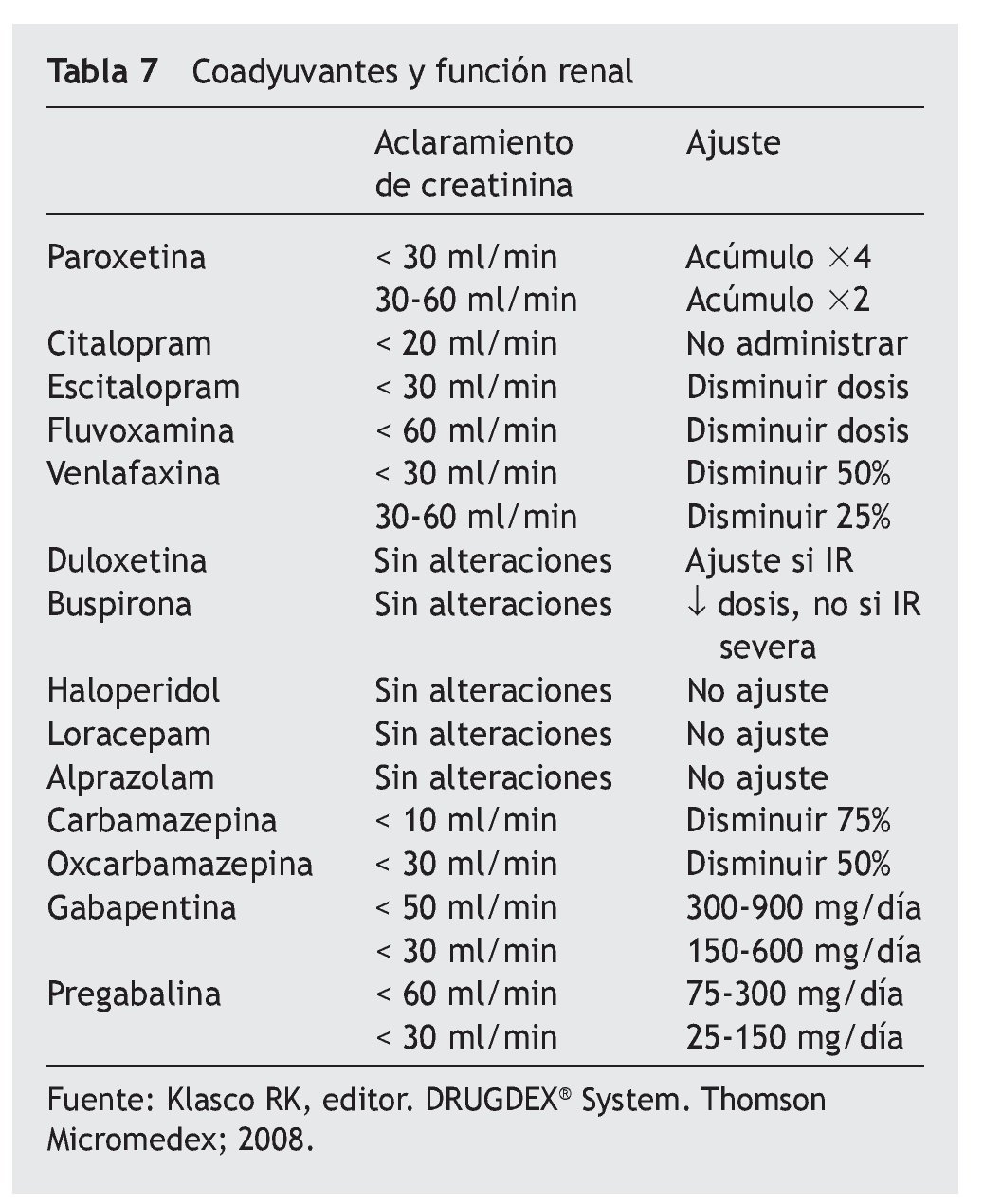
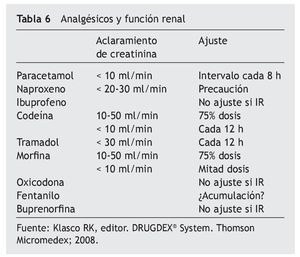
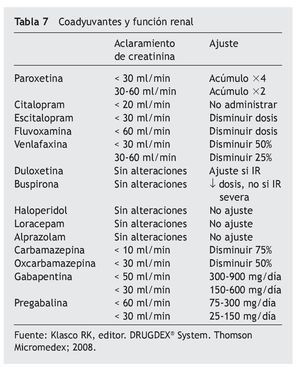
Un 23% de los residentes analizados presenta un aclaramiento de creatinina < 30 ml/min, con los riesgos de toxicidad que conlleva en los analgésicos de eliminación renal como los opiáceos, por lo que un adecuado manejo de éstos requiere una disminución de dosis o aumento del intervalo de administración para una adecuada tolerancia (tablas 6 y 7).
Del mismo modo, los cambios farmacodinámicos, con las modificaciones de los receptores, implican un incremento de las reacciones adversas a medicamentos, especialmente con el uso de psicofármacos, dificultando el control analgésico al haber un balance entre eficacia y seguridad muy estrecho.
Por lo tanto, hay riesgo de sobredosificación sin un ajuste adecuado o de infratratamiento en caso de no realizar un seguimiento continuado.
Estas circunstancias, lejos de caer en un nihilismo diagnóstico y terapéutico, deben ser un acicate de valoración e intervención individualizado, estableciendo objetivos realistas de atención, acompañando al anciano en los tramos finales de la vida con un óptimo control sintomático.
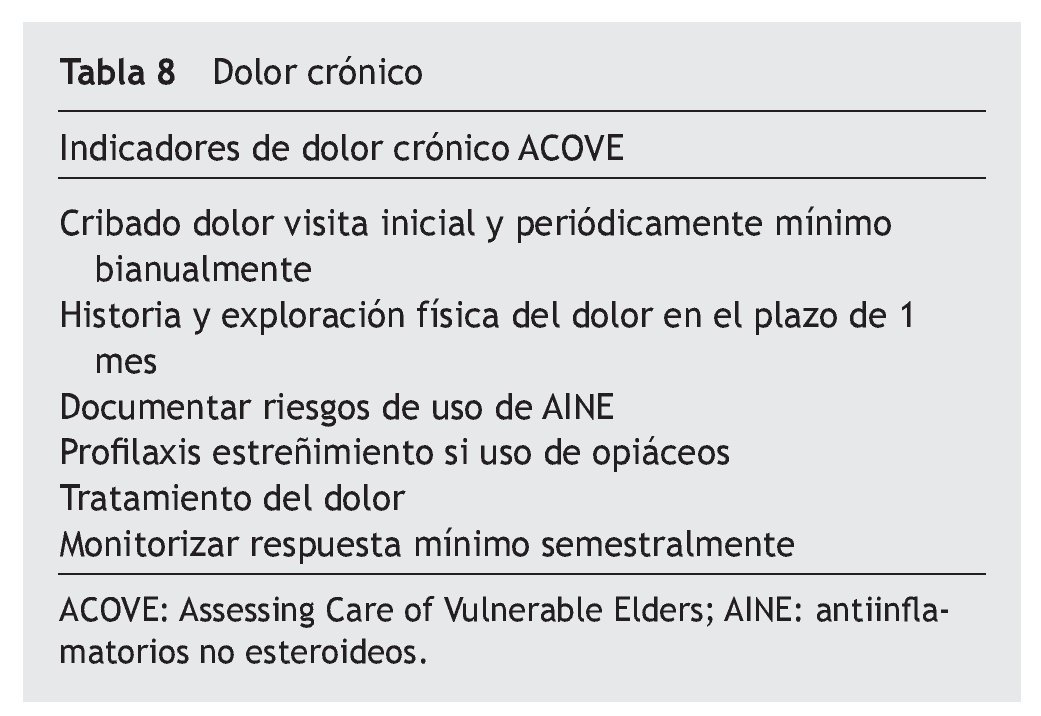
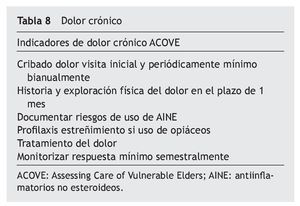
Para lograr una aproximación multidisciplinar, en el año 2001, en Estados Unidos, se consolida el proyecto ACOVE (Assessment Care of Vulnerable Elderly) para establecer unos indicadores de calidad asistencial en los pacientes vulnerables (frágiles), que sirve de marco de referencia para adecuar una atención sanitaria de calidad y que indica unos tiempos predeterminados para el seguimiento. En la tabla 8 se muestran los indicadores de calidad en el manejo del dolor19.
Posteriormente, en el año 2002, la Asociación Americana de Geriatría crea un procedimiento de actuación y manejo en el dolor crónico en pacientes geriátricos (tabla 9)20.
El concepto de dolor total cobra especial relevancia en el paciente geriátrico, donde la detección de necesidades encubiertas latentes depende de una valoración geriátrica integral, continuada, dinámica, de las áreas física, psíquica, social y su repercusión en la funcionalidad del individuo.
Una vez detectadas las necesidades de atención, se puede establecer un plan de atención individual, con unos objetivos determinados y realistas con relación a la clasificación del paciente geriátrico.
Para alcanzar realmente una adecuada calidad de vida, es indispensable realizar un adecuado manejo de la presencia de dolor, trastornos afectivos, así como de diferentes formas de malestar.
— El dolor es un síntoma frecuente en residencias, que está infradiagnosticado e infratratado.
— Los residentes con deterioro cognitivo y con pluripatología son una población creciente en este recurso asistencial.
— Las instituciones y el personal sanitario deben disponer de herramientas de detección del dolor, especialmente para los usuarios con problemas de comunicación: demencia, afasias o aislamiento sensorial severo.
— Para los sanitarios que atienden a esta población, es imprescindible conocer los cambios en la farmacocinética y en la farmacodinamia que provoca el proceso de envejecimiento.
— Los centros gerontológicos pueden constituirse en el futuro en centros gigantescos de cuidados paliativos.
— El control sintomático y el bienestar permiten aportar la máxima calidad de vida y deben constituir un indicador de calidad asistencial para alcanzar la mejor calidad de cuidado.
Agradecimientos
A la Fundación Matia por habernos permitido realizar esta investigación en el Centro Gerontológico Txara 1.
Conflicto de intereses
Los autores declaran no tener ningún conflicto de intereses.
* Autor para correspondencia.
Correo electrónico: jalaba@matiaf.net (J. Álaba).
Recibido el 18 de marzo de 2009;
aceptado el 1 de junio de 2009