El presente artículo realiza una exhaustiva revisión de la artrosis erosiva de las manos, repasando los pequeños cambios observados a lo largo del tiempo, en cuanto a la epidemiología de la enfermedad, la literatura existente sobre datos genéticos y etiopatogénicos, sus características clínicas, las pruebas complementarias más útiles, los puntos clave de su diagnóstico diferencial, para acabar con una actualización de su tratamiento.
Mediante el mejor conocimiento de esta entidad podemos conseguir una identificación más precoz de sus manifestaciones, un abordaje terapéutico más enérgico y un seguimiento más próximo de su evolución, para poder evitar la discapacidad asociada a ella.
This article provides a thorough review of erosive osteoarthritis of the hands, including the small changes observed over time in the epidemiology of the disease and the literature on genetic, etiopathogenic and clinical features. We also review the most useful complementary tests, the key points of the differential diagnosis, and end with an update on the treatment of this entity. Better understanding of this disease will help to achieve en earlier diagnosis of its signs and symptoms, a better therapeutic approach, and closer monitoring of disease progression to avoid future disability.
Desde que en el siglo xviii el destacado médico inglés William Heberden (1710-1801) describiera los nódulos interfalángicos que han inmortalizado su nombre1, y un siglo después Charles-Joseph Bouchard (1837-1915), ilustre patólogo francés, identificara los nódulos que llevan el suyo, ambos como expresión de la artrosis de las manos, y distinguiéndolos de forma definitiva de otros nódulos reumáticos, muchas han sido las publicaciones que han intentado caracterizar esta patología como un proceso degenerativo generalizado, con una fase inicial francamente inflamatoria y que en el curso de su evolución conlleva el desarrollo de una serie de deformidades en las articulaciones de los dedos que confieren a las manos un aspecto muy característico2.
Con un resplandor propio, la artrosis erosiva (AE) de las manos ha sido objeto también de unas cuantas comunicaciones, cuyo propósito ha sido el de aportar una serie de datos que permitan identificarla inequívocamente y que incluyen aspectos etiopatogénicos, clínicos, radiológicos, ecográficos e incluso terapéuticos.
La AE de las manos debe ser considerada, pues, como una variante de la poliartrosis de las manos, con características clínicas y radiológicas propias, y con una evolución más severa que la forma clásica de artrosis.
A pesar de que ya Kellgren y Moore2 hicieron en 1952 referencia a la inflamación episódica de las pequeñas articulaciones de las manos, la primera alusión escrita específica a la artrosis erosiva data del año 1966, fecha en que Peter et al.3 acuñaron el término, publicándolo en una prestigiosa revista médica3. En dicho artículo se utilizaba el nombre de AE debido a las erosiones centrales descubiertas en las radiologías simples de los pacientes, así como a los hallazgos inflamatorios encontrados en las muestras de sinovial obtenidas de articulaciones afectadas. Posteriormente, autores como Ehrlich4 utilizaron un término más clínico, artrosis inflamatoria, para referirse a la misma patología, pero dando mayor protagonismo a sus peculiaridades clínicas que a las radiológicas.
La ausencia de criterios diagnósticos establecidos, o de definición validada para la AE, constituye un obstáculo a la investigación científica en este terreno. Para subsanar este inconveniente, algunos autores han intentado definir la AE como una artrosis de manos, con diagnóstico basado en los criterios del American College of Rheumatology (ACR) de 1990, junto a la presencia de erosiones radiológicas en al menos dos articulaciones interfalángicas distales (IFD), ausencia de factor reumatoide (FR), de anticuerpos antipéptido citrulinado (AAPC) y de elevación de reactantes de fase aguda, e historia personal y familiar negativa para artropatías como la psoriásica y las provocadas por depósito de microcristales (tabla 1)5.
| Propuesta de criterios diagnósticos de artritis erosiva (según Anandarajah)5 |
| - Artrosis de manos según criterios del American College of Rheumatology |
| - Erosiones en al menos 2 articulaciones interfalángicas de las que, al menos una, debe ser una IFD |
| - Factor reumatoide negativo y/o anticuerpo antipéptido citrulinado negativo |
| - Ausencia de historia familiar y personal de artritis psoriásica |
| - Ausencia de historia personal de gota y condrocalcinosis |
| - Presencia de erosiones subcondrales centrales |
| - Velocidad de sedimentación globular normal (o casi normal) |
| - Proteína C reactiva normal (o casi normal) |
Los primeros dos puntos son esenciales para el diagnóstico de artritis erosiva. Los tres últimos sumaran especificidad al diagnóstico.
Se trata de un subtipo infrecuente de artrosis que aparece generalmente en mujeres de raza blanca en edad peri o posmenopáusica (40-50 años)6. Aunque los varones pueden verse afectados también por la AE, lo hacen con mucha menos frecuencia. Durante años se ha estimado que la relación mujer:varón en esta patología es aproximadamente de 12:15,7.
Recientemente, un grupo de autores han comunicado la prevalencia de la AE en la población general, utilizando para ello los datos del estudio Framingham (cohorte de pacientes europeos y norteamericanos)8. Los resultados obtenidos, considerando como AE la artrosis con al menos una articulación interfalángica erosionada, fueron de una prevalencia del 3,3% para varones y del 9,9% para mujeres, discretamente superior a la obtenida con datos del estudio Rotterdam (cohorte holandesa), del cual se desprendieron prevalencias de AE para todas las edades en la población general del 2,8%, sin evidentes diferencias entre sexos9. Con estas cifras, la dominancia de la enfermedad en el sexo femenino parece persistir, si bien lo hace con proporciones francamente inferiores a las antaño consideradas. Así mismo, ambos trabajos observan una elevada prevalencia de AE en varones >80 años, todo lo cual modifica la clásica visión de que la enfermedad afecta casi únicamente a mujeres de edad media.
Al evaluar la prevalencia de AE en una población seleccionada con artrosis de manos, las cifras obtenidas también han sido variables, pero podríamos hablar de un 24% entre mujeres y de un 9,5% entre varones mayores de 60 años8, o de un 15,5% entre personas con artrosis de manos, sin hacer diferenciaciones entre sexos10.
Las articulaciones más afectadas desde un punto de vista erosivo son las IFD, seguidas, aunque con una frecuencia muy inferior, por las interfalángicas proximales (IFP). Las articulaciones metacarpofalángicas (MCF) raramente se ven erosionadas8.
Un dato curioso para comentar es la ausencia de factores de riesgo conocidos para el desarrollo de AE. En este sentido, alguna publicación ha presentado, incluso, una asociación inversa con un clásico factor como es la realización de un trabajo manual. La obesidad, tan claramente relacionada con cualquier tipo de artrosis en la población general, muestra una discreta asociación positiva con la AE9.
Genética y etiopatogeniaLa tendencia familiar observada en la AE ha motivado la realización de diversos estudios dirigidos a evaluar las posibles alteraciones genéticas causantes del desarrollo de la enfermedad. Uno de esos estudios mostró anormalidades en la región del cromosoma que codifica la interleucina (IL)-1 en pacientes con AE; este hecho podría ayudar a explicar la naturaleza destructiva de la AE, al ser ya conocida la participación de la mencionada interleucina en la patogénesis erosiva de la artritis reumatoide6. En otro estudio se evidenció un incremento de un fenotipo de alfa-1 antitripsina (el fenotipo MS), en un grupo de pacientes con AE, al compararlos con otro de artrosis nodular de manos, sin que existieran entre ambos grupos diferencias significativas en la edad de los pacientes6.
Investigadores del norte de Italia, a diferencia de otros predecesores que intentaron sin fortuna hallar antígenos leucocitarios humanos (HLA) específicos en pacientes con AE, han identificado el HLA-DRB1 *07 como un HLA asociado con el desarrollo y la mayor severidad de la AE11. Otros antígenos también encontrados en este mismo estudio y relacionados con AE fueron el HLA-B44, el HLA-A23 y el HLA-B38, si bien el significado de estos datos genéticos resulta incierto por tratarse de antígenos ya vinculados a enfermedades muy diversas. Los autores son conscientes, no obstante, de que la artrosis de manos podría presentar múltiples factores de riesgo, y de que la contribución genética es muy compleja y precisa ser estudiada en mayor profundidad en el futuro.
En los últimos años, cada vez son más los autores que reconocen la inflamación sinovial como fundamental para justificar la aparición de dolor en la artrosis en general. En el caso específico de la AE, la presencia de sinovitis fue aceptada ya desde el principio5.
No es totalmente conocido el papel que desempeñan las citocinas proinflamatorias en la fisiopatología de la AE, pero recientemente se han comunicado ciertas evidencias indirectas relacionadas; unas demuestran elevados niveles séricos de IL-2 en pacientes con AE, en comparación con aquellos con artrosis de manos no erosiva; otras hablan de niveles séricos incrementados de receptores de IL-4 en pacientes con AE entre otros tipos de artrosis, al compararlos con controles sanos. Puesto que la IL-4 media una acción antiinflamatoria a través de la regulación de la IL-1 y del factor de necrosis tumoral alfa (TNF-α), un incremento de sus receptores puede asociarse con una menor disponibilidad de IL-4, contribuyendo así al inicio del daño articular en la AE5.
Por otra parte, la aparición de erosiones podría estar determinada por factores inflamatorios locales. El dolor y el grado de pinzamiento articular, por ejemplo, constituyen dos factores de riesgo independientes para el desarrollo de erosiones en la articulación correspondiente, mientras que la determinación de parámetros indicativos de inflamación sistémica (como la proteína C reactiva [PCR]) no ha mostrado asociación con la evolución erosiva de este tipo de artrosis a lo largo de 6 años10. En estos mismos términos ya se habían pronunciado previamente autores checos, cuyos estudios no mostraron diferencias en los niveles séricos de PCR entre pacientes con formas erosivas y no erosivas de artrosis de manos, a pesar de que técnicas sensibles como la gammagrafía ósea reflejaran marcadas diferencias en el grado de afectación de las pequeñas articulaciones; según ellos, en esta patología los cambios inflamatorios locales no son tan intensos como para inducir una respuesta inflamatoria sistémica12.
Estos mismos autores, conocido el papel crucial que el ácido hialurónico (AH) juega en la integridad estructural y funcional del cartílago articular, por ser el responsable de las propiedades viscoelásticas del líquido sinovial, dedicaron un estudio a determinar los niveles séricos de dicho AH en personas con artrosis de manos, encontrándolos significativamente más elevados en los pacientes con formas erosivas, incluso después de ajustar los resultados en función de la edad y de la duración de la enfermedad, que son dos reconocidos factores de confusión. Se sugiere que modificaciones en la concentración y en el peso molecular del AH podrían estar implicadas en el proceso degenerativo de la artrosis, y que la presencia de niveles séricos elevados de AH puede reflejar inflamación y destrucción articular en la enfermedad erosiva12.
En otro orden de cosas, desde hace varios años, investigadores de varias partes del mundo han sugerido que la adiponectina participa activamente en procesos como la respuesta inmunitaria, y la inflamación y degradación tisular, en las artritis destructivas. Siguiendo en esta línea de estudio, los investigadores checos han demostrado recientemente elevados niveles séricos de adiponectina en mujeres con AE, en comparación con otras afectadas de artrosis no erosiva de las manos, sugiriendo que esta sustancia puede jugar un papel importante en la fisiopatología de este subtipo erosivo de artrosis. No se encontró, en estas pacientes, correlación entre niveles de adiponectina ni de resistina e índice de masa corporal (IMC)13.
Entre posibles patologías asociadas a la AE se ha propuesto la acción de los cristales de hidroxiapatita y de pirofosfato cálcico sobre el cartílago articular, como causa del proceso inflamatorio y erosivo, e incluso mecanismos en relación con la deprivación hormonal propia de la menopausia, justificando la mayor prevalencia de la enfermedad en esta etapa femenina de la vida6.
Finalmente, y como dato curioso, se ha asociado la aparición de AE al uso de ciertos fármacos, como es el caso del bevacizumab y del paclitaxel, empleados en el tratamiento de varios cánceres, que desencadenaron la aparición de una AE en una mujer con cáncer ovárico que ya presentaba con anterioridad una artrosis de manos poco sintomática14, e incluso con enfermedades de base autoinmune, como la morfea, indicando, tal vez, que ambas enfermedades podrían formar parte de una misma familia15.
ClínicaLas manifestaciones clínicas clásicas de la AE tienen un inicio brusco, en edades más tempranas que la artrosis no erosiva de manos. Generalmente incluyen dolor, tumefacción y rubor de las pequeñas articulaciones de ambas manos, con mayor frecuencia IFD y ocasionalmente IFP. La afectación de la primera carpometacarpiana, de MCF o del carpo, aunque también posible, es rara6. También existen descripciones puntuales de AE en los pies, con sintomatología mucho más suave, aunque con considerable pérdida de movilidad. Estas características de la AE en los pies sirven de argumento a ciertos autores para justificar el escaso número de casos comunicados de esta patología que, en su opinión, podría ser tan frecuente en esta localización como en las manos16,17.
Los pacientes pueden presentar rigidez matutina, que suele ser inferior a una hora, así como parestesias, quistes mucoides, nódulos de Heberden y de Buochard, e incluso deformidades más severas como subluxaciones, anquilosis articular o artropatías mutilantes5,6.
A pesar de la mayor severidad de las manifestaciones clínicas de la AE, en comparación con las de la artrosis no erosiva de las manos, las diferencias clínicas entre ambas entidades no siempre resultan obvias. De hecho, un reciente estudio en el que se realizó una amplia revisión de la literatura para identificar dichas diferencias indica que únicamente el daño estético muestra resultados significativamente distintos entre grupos (mayor en pacientes con AE). Aspectos como el dolor, la rigidez y la capacidad funcional obtienen resultados similares en todos los pacientes18.
La evaluación capilaroscópica del lecho periungueal de pacientes con AE y artrosis no erosiva de manos no ha mostrado patrón específico alguno, pero ha revelado la presencia de más capilares tortuosos y cortos y de mayor número de microhemorragias en la población con AE, en comparación con los controles y con el grupo de artrosis no erosiva. Estos hallazgos inespecíficos, similares a los atribuidos a personas con artropatía psoriásica, permiten hipotetizar que estas alteraciones microvasculares periungueales podrían conducir a la afectación inflamatoria de las IFD observada en estos dos diagnósticos19.
El curso de la enfermedad es en forma de brotes, que pueden durar desde varios meses hasta 5 años, antes de la aparición de las deformidades que resultan en la mayor o menor discapacitación de las manos6.
Datos de laboratorioA pesar de la inflamación articular existente, los resultados de laboratorio son poco expresivos y hasta el momento actual no existen parámetros que permitan establecer el diagnóstico o evaluar el seguimiento de la enfermedad. Como ya se ha dicho en apartados anteriores, los reactantes de fase aguda no traducen, por lo general, la actividad erosiva de la enfermedad, si bien algunos autores han detectado moderados incrementos de PCR que podrían corresponder a los casos de AE con mayor número de articulaciones clínicamente activas y con más dolor20, y otros, elevaciones variables de la velocidad de sedimentación globular (VSG) en algo más de la mitad de sus pacientes evaluados con AE, aunque aquellos con los valores más altos desarrollaran finalmente una artritis reumatoide (AR)4. El FR, los AAPC y los anticuerpos antinucleares son negativos, confirmando que no se trata de una entidad autoinmune4,6,7.
Dada la naturaleza erosiva de la enfermedad, se ha postulado la existencia de un metabolismo óseo acelerado. La determinación de C-telopéptido sérico, como marcador de resorción ósea, ha confirmado una significativa liberación de dicha sustancia en pacientes con AE, indicando una mayor agresividad del proceso de remodelado óseo21.
Pruebas de imagenRadiología simpleLa radiología simple ha sido, durante años, la gran arma diagnóstica de la AE, permitiendo la detección de las lesiones erosivas articulares que le dan nombre.
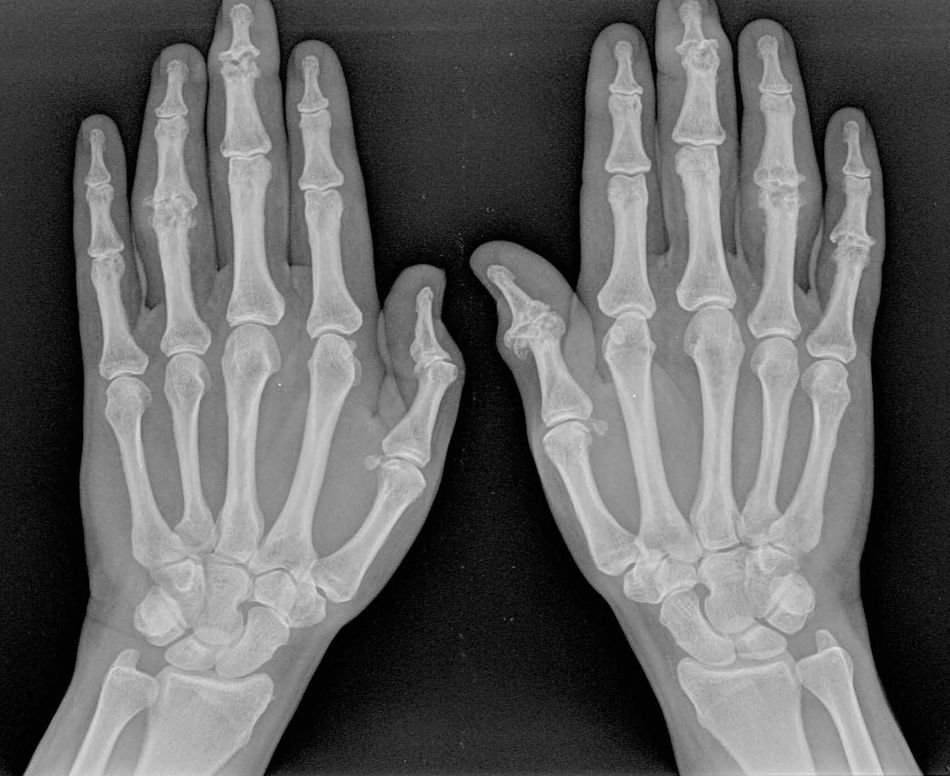
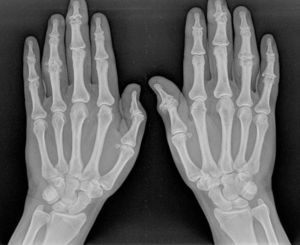
En las fases iniciales de la enfermedad, y coincidiendo con los brotes inflamatorios, es fácil encontrar un aumento de partes blandas periarticulares, como traducción de la sinovitis subyacente. Algún tiempo después, es posible apreciar un pinzamiento articular, generalmente asimétrico. Posteriormente, el desarrollo de erosiones óseas que de forma característica se localizan a nivel central, a menudo combinadas con proliferación ósea marginal de extensión variable, confieren a la articulación su típica imagen en «alas de gaviota» (fig. 1)6.
Las erosiones pueden provocar una cavidad pronunciada en la epífisis de la falange media, concediendo a la articulación IFP una morfología que J. Muñoz Gomez et al.22 consideraron característica de esta entidad y que bautizaron con el nombre de «imagen falciforme». En estos casos la falange distal se desvía de forma lateral. Otras lesiones radiológicas muy típicas de la AE son las de destrucción de la epífisis falángica (más frecuentemente a nivel de IFD)22.
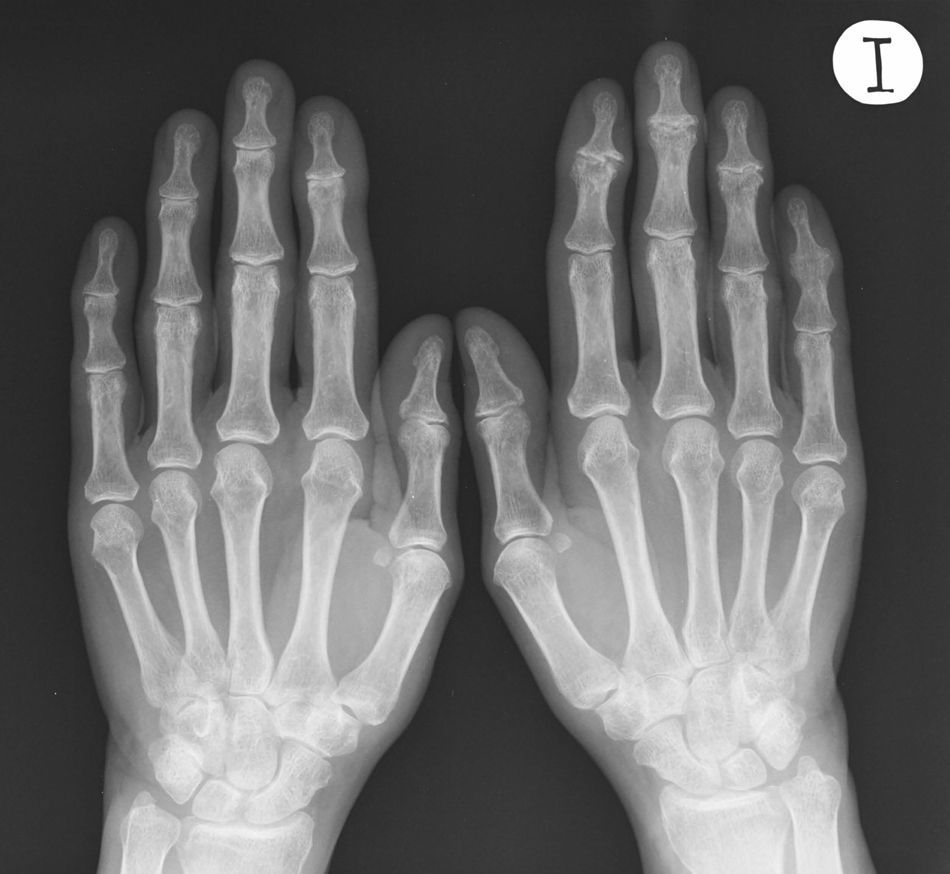
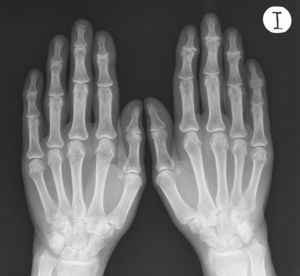
Estos fenómenos erosivos pueden desencadenar una respuesta reparativa, en forma de aparición de osteofitos (más frecuentes en las erosiones falciformes) o de anquilosis (en las articulaciones más destruidas) (fig. 2). Estas fases radiológicas se correlacionan clínicamente con la desaparición de los signos inflamatorios y la aparición de la deformidad articular. No es extraño encontrar en una misma radiografía, articulaciones con alteraciones en diversas fases evolutivas, ni que un mismo paciente muestre, en varios tiempos, estados diferentes de la enfermedad, como reflejo de su curso natural22.
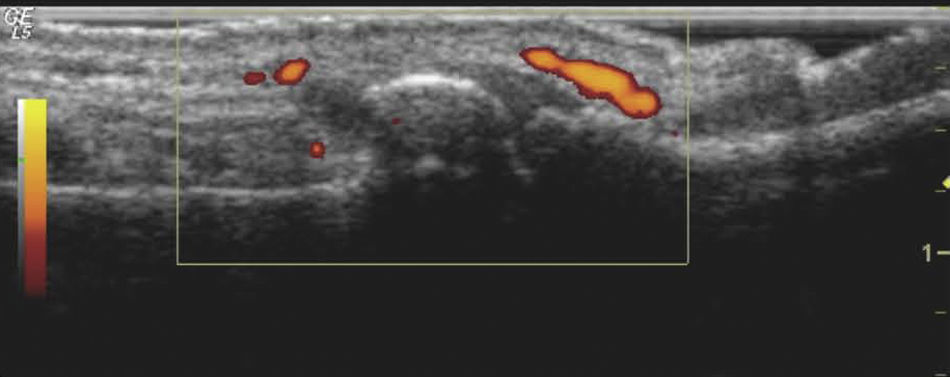
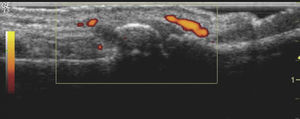
EcografíaDesde que la ecografía iniciara su andadura como prueba de imagen de gran utilidad en el estudio articular, muchos han sido los autores que han hablado de su superioridad sobre la radiología simple, especialmente por su mayor precocidad a la hora de detectar alteraciones. La presencia de derrame articular y de sinovitis con señal power doppler (fig. 3) son indicadores de que la AE es una forma inflamatoria de la artrosis de manos. Estas manifestaciones, halladas en casi la mitad de articulaciones exploradas de pacientes con AE, pueden sugerir que los tratamientos utilizados resultan insuficientes23. En este sentido, la ecografía es considerada, incluso, más sensible que el examen físico, pues permite la detección de inflamación articular en fases subclínicas de la enfermedad. Este hecho, cuyo significado clínico no está del todo claro, podría servir para identificar articulaciones en las que la elevada actividad inflamatoria precediera a los cambios erosivos y al deterioro funcional, y en las que tal vez estaría justificado ser más agresivo en la elección del tratamiento24.
Varios estudios han mostrado también, que la ecografía es más sensible que la radiología convencional en la detección de erosiones y de osteofitos. De este modo, la exploración ecográfica puede contribuir a observar lesiones erosivas de forma más temprana, y a clasificar y tratar al paciente más precozmente23,25. La explicación de esa mayor sensibilidad se basa, por un lado, en la capacidad de la técnica de explorar planos longitudinales y transversales, ampliando así la superficie articular analizada, y por otro, en el hecho de que las erosiones de muy pequeño tamaño son mejor apreciadas ecográfica que radiológicamente23.
Resonancia magnéticaLa resonancia magnética, por último, a juzgar por los resultados de un reciente artículo que compara su sensibilidad en la detección de inflamación, erosiones y osteofitos con la de la radiología convencional y la ecografía, no parece aportar grandes beneficios en la evaluación de pacientes con AE. El trabajo confirma una gran correlación entre ecografía y resonancia magnética en la valoración de los tres tipos de alteraciones, e incluso señala que la resonancia visualiza peor los osteofitos, debido a la presencia de calcio en su interior26.
Radiología convencional y ecografía son, pues, técnicas complementarias que, usadas de forma adecuada, y apoyadas en los datos clínicos, permiten realizar un diagnóstico precoz y un correcto seguimiento de los pacientes con AE.
Diagnóstico diferencialEl diagnóstico diferencial de la AE con otras artropatías es amplio y debe realizarse en base a las manifestaciones clínicas, las alteraciones radiológicas y los parámetros de laboratorio, teniendo siempre en cuenta las enfermedades que puedan cursar con erosiones a nivel de IFD de las manos. Las entidades más comunes a considerar son la artritis psoriásica (AP), la artritis reumatoide (AR), la gota tofácea y la reticulohistiocitosis multicéntrica. Además de los datos clínicos y epidemiológicos de cada una de ellas, serán las características de sus erosiones las que nos ayudarán en el diagnóstico7,27.
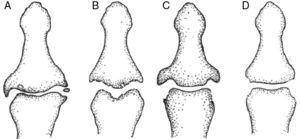
Ya en el año 1980, Martel et al.28 describieron las diferencias entre la AE y AP, haciendo énfasis en la forma y la distribución de las erosiones que ambas generan. Como ya se ha mencionado antes, las erosiones de la AE son subcondrales, centrales y suelen acompañarse de la posterior proliferación ósea marginal que produce un crecimiento osteofítico en las superficies articulares adyacentes, originando la imagen típica en «alas de gaviota» (fig. 4). Casi siempre se ven afectadas las IFD y ocasionalmente las IFP. Además, en la radiología simple de pacientes con AE pueden convivir signos típicos de la artrosis no erosiva como osteofitos, pinzamiento del espacio articular, quistes subcondrales y esclerosis subcondral. De igual modo, la afectación de las IFD es una de las características distintivas de la AP, si bien en ésta suele ser asimétrica y puede afectar en eje longitudinal a un mismo radio, quedando íntegros el resto. Las erosiones son marginales al inicio, van progresando hacia la región central, afectan el hueso subcondral y con el tiempo acaban confluyendo y dando lugar a una imagen de ensanchamiento del espacio articular. Si esta alteración se combina con el afilamiento del extremo distal de la falange y la consiguiente remodelación, finalmente podrá observarse la típica imagen en «lápiz en copa» (fig. 4). La AP, además, puede producir una reabsorción de los penachos de las falanges distales originando acroosteólisis, que no aparece en la AE. Como rasgos distintivos cabe recordar también la posibilidad de que aparezcan en el paciente con AP onicopatía, dactilitis o entesitis asociados a la artritis7,29.
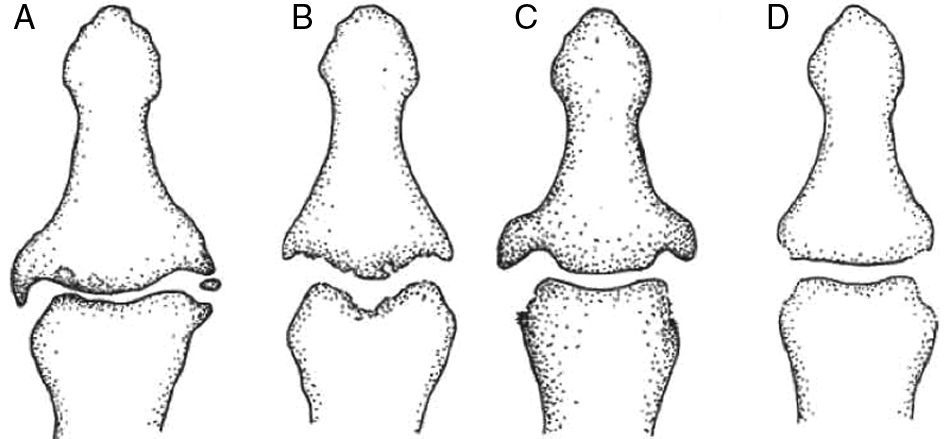
Características radiológicas diferenciales a nivel de las interfalángicas distales. A) Artrosis no erosiva: pinzamiento articular focal, osteofitos marginales, esclerosis. B) Artrosis erosiva: erosiones centrales subcondrales, proliferación ósea marginal. C) Artritis psoriásica: erosiones marginales proliferativas. D) Artritis reumatoide: erosiones marginales no proliferativas, osteopenia yuxtaarticular. (De Zhang et al.1).
La AR se caracteriza por afectar con mayor frecuencia a las MCF y las IFP de las manos, y a las muñecas. La afectación de IFD no es característica de esta entidad y no suele ser una manifestación inicial o aislada, sino que, de presentarse, lo hace de forma episódica y con mayor frecuencia en pacientes con FR positivo. Suele ser una poliartritis simétrica, acompañada o no de tenosinovitis y nódulos. Conforme la enfermedad progresa pueden aparecer deformidades típicas, como la desviación de los dedos en «ráfaga cubital» o el dedo en «cuello de cisne». A nivel radiológico, las características principales de la AR son: osteopenia yuxtaarticular, pinzamiento simétrico del espacio articular y erosiones marginales (fig. 4). El aspecto común que comparten la AR y la AE es que en estadios avanzados pueden aparecer subluxaciones y anquilosis7,29.
La gota tofácea puede, ocasionalmente, cursar como una poliartritis simétrica con nódulos periarticulares o tofos, capaces de dar lugar a erosiones que suelen rodearse de un borde escleroso, dando un aspecto en «sacabocados». Sin embargo, y a pesar de los rasgos comunes entre gota y AE, las erosiones de la primera suelen ser grandes y asimétricas y con insuflación de la cortical, algo que no ocurre en la segunda7.
La reticulohistiocitosis multicéntrica o dermatoartritis lipoidea se caracteriza por cursar con lesiones cutáneas en forma de erupción papulonodular y poliartritis simétrica erosiva, agresiva y progresivamente destructiva, que puede llegar, incluso, a ser mutilante. Radiológicamente, las erosiones que provoca son marginales, bien delimitadas y progresan centralmente con ausencia de osteoporosis yuxtaarticular o resorción perióstica7,29.
Otras entidades más raras, que pueden cursar con afectación clínica y erosiva a nivel de IFD de las manos y que deben tenerse en cuenta a la hora de hacer el diagnóstico diferencial son: la AE rápidamente progresiva de pacientes con insuficiencia renal sometidos a hemodiálisis, la hemocromatosis, la enfermedad de Still del adulto y la enfermedad de Fabry7,27,29.
TratamientoEl tratamiento de la AE fue descrito hace ya varias décadas por Muñoz et al.22 como desalentador por apoyarse únicamente en su manejo sintomático. Desafortunadamente, en la actualidad seguimos sin disponer de guías sobre el abordaje terapéutico óptimo, ni de fármacos que hayan demostrado modificar el curso evolutivo de la enfermedad7,30. De hecho, el tratamiento suele incluir las medidas terapéuticas utilizadas habitualmente en la artrosis no erosiva, las cuales, conocidas las características inflamatorias de la AE, suelen resultar insuficientes6.
Dentro de las medidas no farmacológicas recomendadas se incluyen la educación del paciente, que debe aprender a proteger las articulaciones de agresiones mecánicas; el tratamiento rehabilitador, y la terapia física. Las férulas digitales, especialmente cuando son utilizadas durante la noche, han demostrado en diversos estudios ser eficaces en la disminución del dolor, mejorando la funcionalidad de las manos y reduciendo la necesidad de cirugía6,31. Las guías EULAR del año 200732, así como algunos otros trabajos, recomiendan, además de estas medidas generales, la aplicación local de calor húmedo, los baños de parafina y ejercicios de rango de movimiento y de fortalecimiento de la musculatura intrínseca5,6,33.
En cuanto al tratamiento farmacológico inicial, pueden utilizarse el paracetamol y otros analgésicos, los antiinflamatorios no esteroideos (AINE) y, de forma mucho más ocasional, los glucocorticoides orales a dosis bajas, todos ellos con el objetivo de disminuir el dolor y mejorar la función articular, resultado que no siempre se consigue en su totalidad32,34.
El beneficio, en cuanto a la disminución del dolor y la inflamación, de las infiltraciones intraarticulares de glucocorticoides fue examinado y descrito por primera vez por Utsinger et al.35 en el año 1978. Trabajos posteriores, como el de Anandarajah5 y uno propio34, entre otros, han confirmado su utilidad, si bien destacan que el beneficio suele ser temporal y que en ningún caso han demostrado prevenir la aparición o la progresión de las erosiones7,32.
Durante los últimos años se han incorporado al tratamiento de la AE y de la artrosis no erosiva de manos un grupo de fármacos llamados SYSADOA (symptomatic slow action drug osteoarthritis) en el que están incluidos el sulfato de glucosamina y el condroitín sulfato (CS). Estos fármacos han generado polémica por las dudas sobre su potencial beneficio en la disminución del dolor, que, de existir, aparece de forma retardada y mantenida una vez suspendido el fármaco, y más aún sobre la hipotética disminución de la progresión radiológica en pacientes con artrosis de manos. Algunos ensayos clínicos, como los de Rovetta et al.36,37 y los de Verbruggen et al.38,39 documentaron una disminución del dolor y de la progresión radiológica de las erosiones en pacientes con AE de manos tratados con CS, pero contaron con un escaso número de pacientes y no fueron controlados ni aleatorizados. Por el contrario, trabajos aleatorizados y doble ciego como el de Malaise et al.40 y el de Goemaere et al.41, demostraron únicamente diferencias significativas respecto a la disminución del dolor en el grupo tratado con CS frente al grupo tratado con placebo. Más recientemente, Gabay et al.42 han confirmado que el tratamiento de la artrosis de manos con CS es superior al placebo, con respecto al dolor, a la funcionalidad de las manos y a la rigidez matutina.
Dentro de los fármacos modificadores de enfermedad (FAME), el más utilizado durante años ha sido la hidroxicloroquina (HCQ), probablemente para aprovechar su acción antiinflamatoria a nivel lisosomal, su acción inhibidora de la formación de inmunocomplejos y su acción supresora de la producción de IL-1 por los monocitos5,6. Dos estudios retrospectivos realizados por Robertson et al.43 y Bryant et al.44 documentaron que la HCQ fue efectiva en la disminución del dolor y de la inflamación en pacientes con AE que no habían respondido al tratamiento con AINE. Lamentablemente, estos estudios no permiten extraer conclusiones definitivas en este sentido, debido al escaso número de pacientes incluidos y a sus defectos metodológicos7,45. No existen datos publicados que defiendan la eficacia del metotrexato y de las sales de oro en el tratamiento de la AE5.
En el año 2000, una publicación comunicó una buena respuesta de las crisis de dolor al tratamiento con clodronato intravenoso. Este dato sugería que los bifosfonatos podrían desempeñar un papel importante en el tratamiento del dolor y de la rehabilitación funcional de los pacientes con AE46. Un estudio piloto posterior, abierto y aleatorizado, llevado a cabo por Saviola et al.47 comparó un grupo de pacientes con AE tratado con clodronato intravenoso con otro grupo tratado con HCQ, confirmando la eficacia del clodronato en esta entidad y su superioridad sobre la HCQ47.
En los últimos años, diversos trabajos de investigación han abordado el estudio del tratamiento de la AE con agentes biológicos, atendiendo al conocimiento del posible papel de la IL-1 y del TNF-α en la etiopatogenia de dicha enfermedad. Bacconnier et al.48 mostraron 3 pacientes con AE severa que fueron tratados con anakinra, con una buena tolerancia al fármaco y mejoría del dolor, que permitió, incluso, la retirada del antiinflamatorio. Un estudio piloto reciente que incluyó 10 pacientes con AE comparó el efecto de las infiltraciones intraarticulares con infliximab (IFP e IFD) frente a suero glucosalino, obteniendo, transcurrido un año, una disminución significativa del dolor y la inflamación con infliximab. Se detectó también una disminución de la progresión radiológica que no resultó estadísticamente significativa49. En un estudio también reciente de Magnano et al.50, el tratamiento con adalimumab durante 3 meses no demostró, de manera significativa, mejorar los signos ni los síntomas de la cohorte de pacientes con AE. Únicamente se detectó una disminución significativa del número de articulaciones inflamadas.
Para terminar, es obligado comentar que, en los pacientes con dolor crónico y déficit funcional severo, o en aquellos en los que existan deformidades graves, puede hacerse necesaria la cirugía. La realización de artroplastias, osteotomías o artrodesis puede ofrecer buenas posibilidades en casos seleccionados7,32.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.