La articulación interfalángica proximal tiene un arco de movilidad natural de 0-100º. La flexión y extensión completas del dedo se acompañan de un movimiento espiral, aproximadamente el 30% del rango total de movilidad que tiene lugar a nivel de la articulación interfalángica proximal17. La pérdida de movilidad de esta articulación se pone especialmente de manifiesto en los movimientos de prensión de objetos. En las articulaciones artríticas, la artrodesis ha demostrado ser un procedimiento seguro y estable para el control del dolor. Sin embargo, conduce a la pérdida completa del movimiento. Por ello se han desarrollado varias alternativas para conservar la movilidad de las articulaciones artríticas. La artroplastia de resección e interposición ha producido complicaciones a largo plazo, especialmente con respecto a la estabilidad articular de los dedos índice y medio. Por ello actualmente sólo se utiliza de manera ocasional6,8,28. También se ha logrado una buena disminución del dolor en casos individuales con la denervación y sinovectomía9, pero este procedimiento no ha sido satisfactorio a largo plazo4,25. Los trasplantes vascularizados articulares de los dedos de los pies se reservan sólo para casos excepcionales, debido a sus altos costes y la falta de un resultado predecible28. Así se busca la mejoría de la función mediante una artroplastia porque proporciona estabilidad y un arco móvil no doloroso. Se realizaron intentos precoces de desarrollo de modelos para la prótesis de articulación IFP2,3,7,18. Las prótesis de silicona, utilizadas con frecuencia, y originalmente diseñadas para pacientes con artritis reumatoidea, también han sido utilizadas fuera de esta indicación. Sin embargo, en los casos con artritis primarias y en particular en la postraumática, se han presentado un número creciente de casos de prótesis fracturadas o inestabilidad articular8,13,16,22-25,27. Como consecuencia ya no se recomiendan este tipo de prótesis para estas indicaciones. Por otro lado los sistemas protésicos constreñidos y semiconstreñidos con articulaciones de tipo bisagra se aflojan y se rompen12,14,24. Esto se debe a las propiedades biomecánicas específicas de la articulación IFP. Fisiológicamente no es una articulación bisagra pura, sino que presenta un movimiento de “enrollamiento” y des-lizamiento1,10,11,15,17,19 en el cual el sistema de ligamentos colaterales, con sus mecanismos alternantes de tensión y relajación durante el movimiento, y la forma de las superficies articulares juegan un papel crucial10,20,21,26,29. Basándose en estos conocimientos, se introdujo el primer modelo de prótesis no constreñida en el año 197515. Con el tiempo, los modelos no constreñidos se han ido diseñando de manera que mimetizan la forma anatómica bicondilar, facilitando una técnica de implantación que preserva el hueso y los ligamentos colaterales. Así se restablece el movimiento natural de enrollamiento y deslizamiento alrededor de un eje imaginario con un centro de rotación variable. La elección del material protésico de tipo carbón pirolítico ha proporcionado a los componentes menor fricción, más durabilidad y mejor biocompatibilidad.
Principios quirúrgicos y objetivosSustitución protésica de la articulación IFP con prótesis no constreñidas de carbón pirolítico, para disminuir el dolor y al mismo tiempo conservar movilidad y estabilidad.
Ventajas- Conservación de los tejidos blandos estabilizadores.
- Conservación de la reserva ósea y colocación sin ce-mentación.
- Posibilidad de seleccionar diferentes tallas para loscomponentes protésicos proximal y distal.
- Buena biocompatibilidad y biomecánica. Baja fricción.
- El lecho del implante, los tendones y los ligamentosdeben estar intactos.
- Aflojamiento, luxación y sonido de “roce” potencia-les.
- Coste elevado.
- Experiencia limitada a largo plazo.
- Artritis primaria o postraumática de la articulaciónIFP sintomática con una cobertura de partes blandas intacta.
- Paciente motivado y colaborador.
- Ligamentos inestables.
- Soporte óseo insuficiente.
- Tendones extensores irreconstruibles.
- Infección articular no tratada.
- Falta de colaboración por parte del paciente.
- Duración de la intervención de aproximadamente 90 min.
- Aflojamiento y migración de la prótesis.
- Duración limitada de la prótesis.
- Movimiento limitado o pérdida de fuerza comparadacon la articulación sana.
- Potenciales ruidos de “roce”.
- Seguimiento del tratamiento complejo y prolongado.
- Algodistrofia.
- Riesgos quirúrgicos habituales.
- Historia clínica cuidadosa, exploración física detalla-da, especialmente con respecto a la estabilidad articular IFP y a la función tendinosa.
- Radiografías estándar dorsopalmar y lateral estrictasde los dedos centradas en la articulación IFP. Medición de las tallas correctas de los componentes distal y proximal de la prótesis utilizando una plantilla (los componentes distal y proximal se pueden seleccionar de la misma talla o con tallas diferentes. Hay cuatro tallas disponibles en cada caso: 10, 20, 30, 40).
- Intrumental para cirugía de mano.
- Sierra oscilante.
- Instrumental específico para las prótesis articulares in-terfalángicas proximales de carbón pirolítico (PIP Pyro-Carbon Total Joint, Ascension Orthopaedics, Austin, TX, EE. UU.).
- Intensificador de imágenes de alta resolución.
- Bloqueo del plexo braquial, regional intravenosa, o anestesia general.
- Posición de decúbito supino con el brazo colocado so-bre una mesa de mano y tallado de manera que la movilidad sea libre.
- Exclusión del aporte vascular de la extremidad supe-rior con torniquete en la parte proximal del brazo.
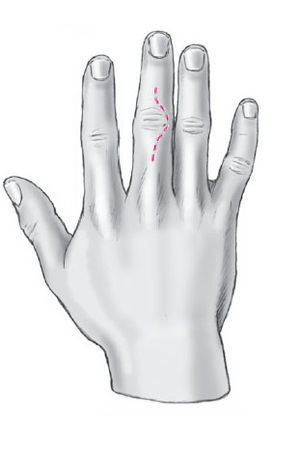
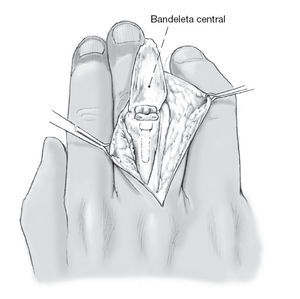
Figura 1 La mano se coloca en posición prono después de desinfectarla y de preparar el campo quirúrgico estéril. Se realiza una incisión curva en la piel en el lado extensor sobre la articulación interfalángica proximal.
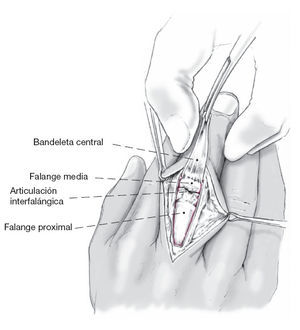
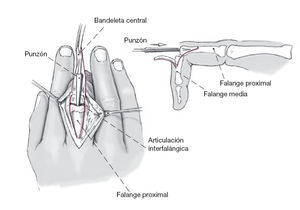
Figura 2 Se separa el colgajo de piel de la aponeurosis dorsal para exponer la aponeurosis dorsal central (bandeleta central, parte medial). Se realiza la técnica de Chamay5, basada en un pedículo con base distal en la inserción, se traza una incisión en forma de V en la aponeurosis dorsal central en dirección proximal, se continúa la disección hasta la inserción en la base de la falange media, y se abre la articulación5. Existe la posibilidad alternativa de incidir el tendón extensor desde la mitad de la falange proximal hasta su inserción en la falange media y de separarlo con un periostiotomo colocando elevadores radial y cubital. Sin embargo, sólo lo recomendamos en situaciones excepcionales tales como las deformidades en ojal, porque este abordaje conlleva un importante riesgo de lesión de la bandeleta central.
Figura 3 Se resecan la membrana sinovial y todos los osteofitos utilizando una pinza de Luer, y se abre la cavidad medular de la falange proximal a través de la superficie troclear con un punzón. Se tiene que flexionar la falange media a 90º para poder hacerlo.
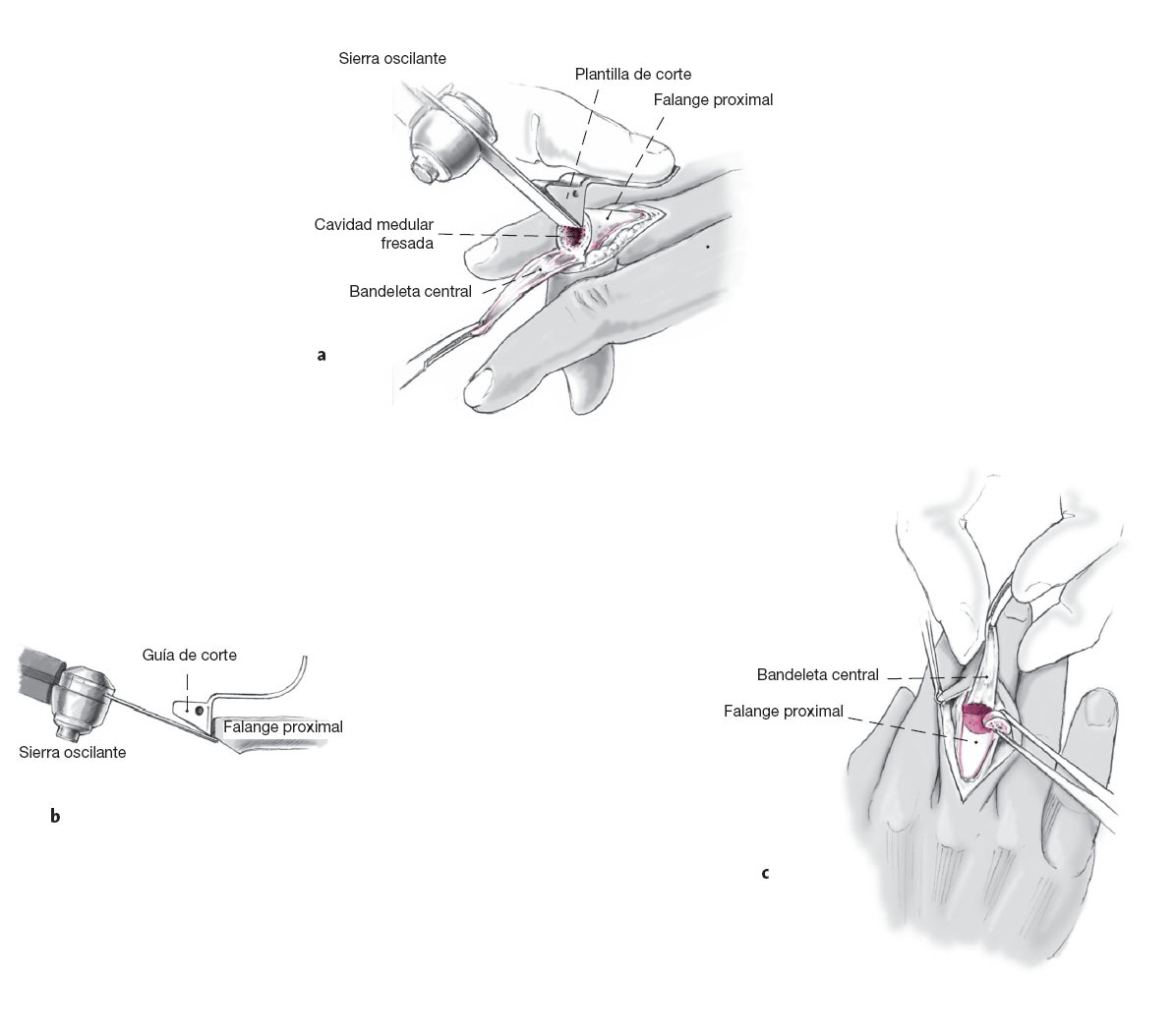
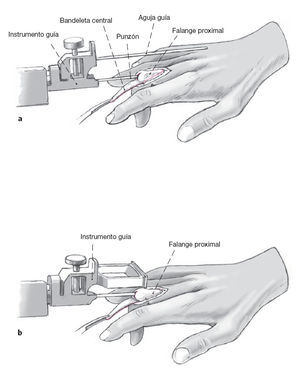
Figuras 4a y 4b Se introduce el instrumento guía paralelo a la superficie extensora de la falange y al eje central longitudinal de la falange proximal. Se introduce una aguja guía paralela al punzón para medir la posición, esto permite evaluar la orientación (a). Si hay alguna duda acerca de que la alineación sea correcta, se utiliza un intensificador de imágenes. Se desliza la guía de osteotomía hasta alcanzar su posición y se utiliza una sierra oscilante para hacer la osteotomía de la superficie troclear distal a los ligamentos colaterales. Se saca el instrumento guía para completar la osteotomía (b).
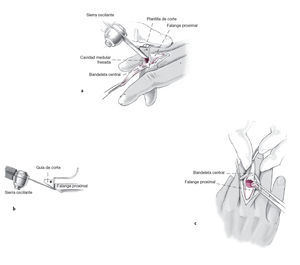
Figuras 5a a 5c a) Mediante un fresado progresivo se ensancha la cavidad medular, tras lo cual se introduce una plantilla de tamaño adecuado para la osteotomía oblicua. b) Se osteotomiza el reborde óseo palmar con la sierra oscilante, y se retira la plantilla. c) Se regulariza el reborde óseo palmar. Es especialmente importante que los bordes de corte sean paralelos, especialmente entre la segunda superficie de osteotomía y la superficie palmar de la cavidad medular, ya que el componente protésico debe quedar bien encajado. De ningún modo el ángulo de osteotomía puede ser superior al de la plantilla con el fin de prevenir que el margen proximal del componente protésico se asiente en la cortical palmar a medida que se impacta en la misma. De ser así el componente podría producir una fractura al ser impactado.
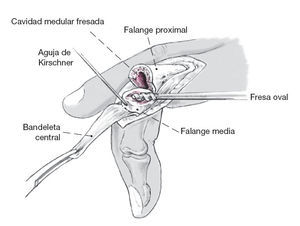
Figura 6 Resección del cartílago y regularización de la base de la falange media mientras se protege la inserción de la bandeleta central y de los ligamentos colaterales, p. e., utilizando fresa de dentista, sierra, gubia o pinza de Luer. Se puede colocar una aguja de Kirschner de 0,6 mm justo delante de la inserción del extensor para protegerlo. Una vez que se han resecado todos los osteofitos y que se ha obtenido un lecho liso y sin cartílago, se puede abrir la cavidad medular con un punzón y se puede agrandar gradualmente con una fresa. El tamaño de la fresa intramedular final debe corresponder a la de la prótesis definitiva. La talla del componente puede ser la misma o puede oscilar una talla arriba o abajo con respecto al componente proximal.
Figura 7 Primero se coloca el componente de prueba distal. El margen debe quedar a plano de manera muy precisa con el margen de la osteotomía y la prótesis debe quedar firmemente asentada. El componente proximal de prueba se introduce a continuación y se comprueba la exactitud de su asentamiento. La posición se considera correcta cuando los componentes quedan bien alineados con el hueso vistos lateralmente con la articulación en extensión. Si se ve una brecha dorsal, se deberá repetir la osteotomía transversa con la plantilla de corte. También se debe repetir la resección en caso de que los componentes no tengan un buen deslizamiento con el movimiento. Se retira la prótesis de prueba, y se colocan los componentes definitivos de carbón pirolítico, colocando primero el distal y luego el proximal. Se deberá imprimir una presión suave en los componentes con un impactador hasta que queden asentados de forma segura. Los márgenes de la prótesis deben quedar a plano con la superficie de osteotomía. Se reduce la articulación, y se comprueba la colocación de la prótesis con el aparato de escopia en los planos estándar.
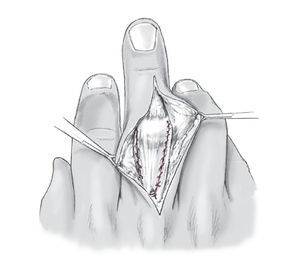
Figura 8 Se cierra proximalmente la aponeurosis central dorsal con dos hilos de PDS de 3.0, y los laterales se cierran con material de sutura reabsorbible de 4.0 (p. e. Vicryl). Se vuelve a comprobar la posición de las prótesis y los dedos. En casos excepcionales se puede haber lesionado la bandeleta central durante la sección longitudinal de la aponeurosis dorsal, en tales casos se debe reinsertar, ya sea al periostio, ya transóseamente a través de dos pequeños orificios de broca según necesidad. Se coloca un vendaje estéril levemente compresivo en la herida después de suturar la piel.
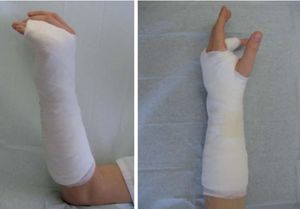
Manejo postoperatorio- Inmovilización con una férula posterior y palmar que“envuelve” los dedos cubitales, dejando los dedos II-V en posición “intrínseco plus” (fig. 9). La muñeca debe estar ligeramente en extensión, aproximadamente a 20-30º, la falange proximal del dedo medio se debe colocar a 70º de flexión y la falange media en extensión. La falange distal debe quedar libre. Entonces se libera la isquemia.
- El yeso colocado al final de la cirugía debe mantener-se durante 2 días.
- Se debe instruir al paciente en la limitación del edemapostoperatorio mediante la elevación de la extremidad y con una movilización amplia de las articulaciones del codo y el hombro.
- Tras retirar el yeso, se colocan férulas termoplásticas,y desde la segunda semana, férulas funcionales (figs. 10a a 10c, tabla 1).
- Se debe realizar ejercicios específicos de mano si-guiendo la tabla 1 con el fin de prevenir el aflojamiento protésico y la formación de adherencias postoperatorias. Estos ejercicios deben basarse en un rango de movilidad de 0-0-75º hasta un máximo de 0-0-90º.
- Se hacen radiografías dorsopalmar y lateral de los de-dos en el postoperatorio y antes de empezar la aplicación de carga cerca del final de la 12.ª semana (fig. 11).
Figura 9 Colocación postoperatoria de un yeso en posición “intrínseco plus” de los dedos con una ligera extensión de la muñeca, dejando las falanges distales libres.
Figuras 10a a 10c a) Se coloca una férula termoplástica a medida a los dos días, con extensión de las articulaciones interfalángicas proximal y distal para evitar déficits de extensión. b, c) A las 2 semanas, se colocan férulas para el ejercicio que permiten un arco de movilidad limitado y controlado.
Tabla 1 Plan de tratamiento tras artroplastia interfalángica proximal.
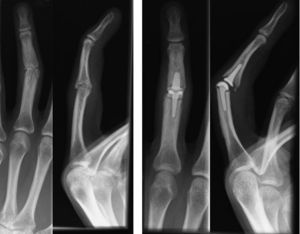
Figuras 11a y 11b Radiografías de un paciente de 40 años de edad con artritis postraumática de la articulación interfalángica proximal: a) Imágenes preoperatorias. b) Imágenes en el control de seguimiento a los 21 meses.
Errores, incidencias, complicaciones- Infección superficial de la herida: revisión precoz ydesbridamiento con tratamiento antibiótico.
- Infección del lecho del implante: retirada de la próte-sis, desbridamiento, y colocación de un espaciador-libera-dor de antibiótico y tratamiento antibiótico sistémico en caso de ser necesario, estabilización con un fijador externo, tratamiento final mediante artrodesis.
- Aflojamiento protésico aséptico: cambio de los com-ponentes o conversión a artrodesis.
- Luxación de los componentes: si se debe a la incom-petencia de las partes blandas, se indica la revisión. Si es posible, se estabilizan la placa palmar y los ligamentos colaterales; si no es posible, se extrae la prótesis y se realiza a continuación una artrodesis.
- Adherencias tendinosas: fisioterapia intensiva y trata-miento con férulas. Si fuese necesario, tenolisis.
- Aflojamiento y/o migración de los componentes pro-tésicos: cambio de los componentes, retirada y artrodesis.
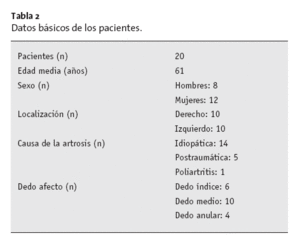
Revisamos retrospectivamente 20 pacientes (8 hombres, 12 mujeres) a los que se les habían implantado 24 prótesis articulares IFP de carbón pirolítico. El período de seguimiento medio era de 15 meses (6-30 meses). Se excluyeron 3 dedos en los resultados funcionales por las complicaciones que habían presentado (una infección, dos luxaciones), y en el momento de la revisión las prótesis ya habían sido retiradas. Sin embargo, estos casos se incluyeron en la estadística de las complicaciones. Los pacientes tenían un promedio de 61 años de edad (35-80 años).
Este tipo de prótesis se utilizó en 14 casos para tratar artritis idiopáticas. La artritis era postraumática en cinco casos, y secundaria a poliartritis en un caso. Se colocaron seis prótesis IFP en dedos índice, diez en el dedo medio, y cuatro en el dedo anular (tabla 2).
Tabla 2 Datos básicos de los pacientes.
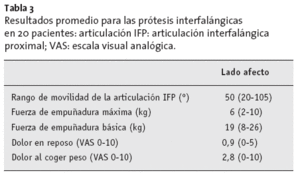
Se obtuvieron dedos completamente libres de dolor en reposo en 13 de las 21 prótesis, medido mediante la escala visual analógica (VAS: 0-10 puntos). El resto de los pacientes tenían dolor leve (VAS: 1-3). El arco de movilidad promedio obtenido fue de 50º (20-105º) con una flexo-ex-tensión de 0-12-71º (tabla 3). El déficit de extensión mínimo y máximo oscilaba entre –15º y 50º, con una flexión posible entre 40º y 90º.
Tabla 3 Resultados promedio para las prótesis interfalángicas en 20 pacientes: articulación IFP: articulación interfalángica proximal; VAS: escala visual analógica.
Para evaluar el grado de satisfacción de los pacientes se les preguntó si se someterían de nuevo al mismo tipo de tratamiento. 16 de los 20 pacientes estaban satisfechos con el resultado y se habrían sometido de nuevo a la misma intervención.
El estudio radiográfico realizado en dos proyecciones reveló una subluxación, dos casos de quistes periprostéticos, y osteofitos en tres pacientes (dos palmares, uno posterior). Las radiografías mostraban cinco casos de aflojamiento del componente distal y cinco casos de aflojamiento proximal, mostrando una falta de osteointegración.
La complicación menor pero de alguna manera molesta de ruidos no dolorosos, especialmente de “chirrido”, se presentó en nueve de 21 prótesis (43%). De manera similar, la migración de la prótesis no se ha acompañado de ningún déficit funcional hasta la fecha. Sin embargo, los efectos a largo plazo de estas observaciones están por definir.
En dos casos, se produjeron adherencias del aparato extensor, y se trataron con tenolisis quirúrgica y unos ejercicios específicos de la mano. También se presentaron las tres complicaciones previamente mencionadas que condicionaron la retirada de la prótesis.
CorrespondenciaDr. Reinhard Meier Unfallchirurgische KlinikMedizinische Hochschule Hannover (MHH)D-30625 Hannover Tel.: (+49/511) 532-2026; Fax: -5877Correo electrónico: reinhard.meier@handchirurg.org
Klinik für HandchirurgieSalzburger Leite 1D-97616 Bad Neustadt Tel.: (+49/9771) 66-2800