Objetivo. Tratamiento de la infección tardía, que requiere siempre un recambio completo de todo el material externo.
Indicaciones. Cualquier infección que persiste durante más de cuatro semanas con identificación de gérmenes y/o claros síntomas de infección.
Contraindicaciones. Ausencia de operabilidad, infección aguda con sepsis y riesgo de bacteremia que puede poner en riesgo la vida del paciente, defectos de tejidos sin posibilidad de efectuar una cirugía de recubrimiento mediante colgajo.
Técnica quirúrgica. Artrotomía, sinovectomía, extracción de todo el material externo inclusive todos los restos de cemento, lavado con chorro de agua, inserción de un espaciador, cierre de la herida o cierre temporal de la herida asistido por vacío.
Tratamiento postoperatorio. Reposo en cama con férula de inmovilización y drenaje hasta la reducción de la cantidad de secreción < 50 ml; a continuación, movilización mediante ortesis sin carga. Antibiosis sistémica durante cuatro semanas; después de dos semanas sin antibióticos se puncionará la rodilla, y a continuación se realizará la incubación del líquido puncionado durante dos semanas. En caso de no identificar patógeno alguno, se realizará la reimplantación de una endoprótesis total de rodilla de revisión y, en caso necesario, se efectuará con cirugía de recubrimiento con colgajo (colgajo del gastrocnemio). Si existe identificación de patógenos, se realizará una nueva revisión con recambio del espaciador.
Resultados. La literatura reporta unas tasas de éxito entre 80-95% tanto para la cirugía de recambio en uno como en dos tiempos. Nuestras tasas de éxito entre este colectivo de pacientes tan heterogéneo es del 81% aproximadamente.
Redacción
K. Dresing, Göttingen
Ilustraciones
R. Himmelhan, Heidelberg
Introducción
Para realizar una intervención quirúrgica como tratamiento de una prótesis total de rodilla (PTR) se tienen que cumplir dos requisitos diferentes:
1. Se trata de una infección temprana, es decir, en el caso de una infección bacteriana del implante difundida por vía hematógena, la sintomatología persiste como máximo hace cuatro semanas y/o la complicación de la infección aparece en un período cuatro semanas postoperatorias como máximo8. Estas dos clasificaciones normales de las infecciones de endoprótesis se corresponden con los grupos II y III según Tsukayama y I y II según McPherson1,13.
2. Existe una infección tardía o crónica del PTR, que, según anamnesis y diagnóstico clínico, persiste como mínimo desde hace más de cuatro semanas (Tsukayama IV y/o McPherson III1,13).
Actualmente, en el caso de la primera situación hay consenso internacional de que no solo es razonable intentar preservar el PTR, sino que se debería hacer lo posible para conseguirlo2,8,11,12. La técnica quirúrgica para lograrlo se ha descrito en la primera parte del artículo (DOI 10.1007/s00064-012-0212-5), en el que se examinan también los detalles importantes y de las fuentes de error.
En cuanto a la segunda variante crónica de la infección de PTR, existe un amplio consenso sobre la necesidad de explantar todo el material extraño para poder dominar la infección3,5,7,8,10. Actualmente existen varios conceptos sobre el tratamiento posterior y el momento de la reimplantación que compiten entre sí y todos ellos gozan del mismo grado de reconocimiento. En esta segunda parte del artículo presentamos el concepto con los pasos quirúrgicos importantes y examinamos las fuentes de error y las particularidades técnicas.
Explicar las fases quirúrgicas para la implantación de una endoprótesis de rodilla de revisión sobrepasaría el marco de este artículo, por lo que no las abordamos; además, estas no difieren de la técnica de reimplante después de un aflojamiento aséptico.
Principio y objetivo de la intervención
En la infección crónica de una prótesis de rodilla se ha completado la formación de biofilm y hay un implante infectado in situ. En la mayoría de los casos existe también una osteomielitis7.
La curación de la infección es el máximo objetivo del tratamiento; incluso la función medida en relación con el rango de movimiento permanece en este caso en un segundo plano. El objetivo es conseguir una articulación libre de infección y de dolor, una «restitutio ad integrum» no será posible. Puesto que los implantes están recubiertos con un biofilm, este se debería extraer completamente. La extracción de esta capa de biofilm supondrá la eliminación de todos los materiales extraños (implantes, restos de cemento), así como la realización de un desbridamiento consecuente del tejido de partes blandas infectado, tejido óseo y fragmentos óseos avitales (necróticos) para prevenir la formación de secuestros. Otras medidas quirúrgicas son el cierre del espacio muerto mediante el empleo de espaciadores, la antibioterapia local mediante administración antibiótica según antibiograma añadida al cemento óseo, la estabilización de la rodilla mediante una férula externa, un espaciador intramedular en caso de gran pérdida ósea o cerclajes en fisuras o fracturas de la diáfisis (iatrógenas).
La conservación del aparato extensor es un requisito indispensable para la implantación de una prótesis artificial de rodilla. No obstante, la extracción radical de todo el tejido infectado tiene prioridad absoluta. Si después del desbridamiento ya no es posible reconstruir el aparato extensor, entonces se deberá planificar la artrodesis de la rodilla como procedimiento siguiente.
Ventajas
- Este procedimiento radical resulta fundamental para curar con éxito la infección y, además, abre la posibilidad de efectuar un nuevo tratamiento endoprotésico.
- Con el sellado del espacio muerto mediante un espaciador, las partes blandas se mantienen con la suficiente tensión longitudinal y se reduce la hemorragia.
- Con la inmovilización de la rodilla, las partes blandas tienen el reposo necesario para su consolidación, sobre todo en el lado extensor más delgado.
- El procedimiento en dos tiempos aumenta la seguridad ante infecciones de recidiva, sobre todo en el caso de patógenos multirresistentes.
- Por lo general, el cierre de la herida se puede garantizar en la primera intervención eligiendo un espaciador del tamaño adecuado, de modo que es posible evitar tener que realizar una cirugía con colgajo muscular para su reconstrucción.
- El procedimiento en dos tiempos brinda la oportunidad de decidir junto con el paciente sobre las consecuencias terapéuticas de la pérdida de hueso y de partes blandas observadas durante la fase intraoperatoria, sobre todo en el caso de ser necesaria una artrodesis o incluso una amputación definitiva.
Desventajas
- Imposibilidad de realizar ejercicios fisioterapéuticos con un espaciador monobloc y posibilidad limitada con un espaciador articulado, hecho que puede limitar el rango de movimiento de la nueva prótesis3,5,9,10.
- La reducción de la superficie limita la liberación de antibióticos del espaciador, por ejemplo, de cadenas de antibióticos.
- El procedimiento en dos tiempos conlleva un aumento del riesgo debido a la aplicación de la doble anestesia.
- Por regla general, no suele ser posible una hospitalización del paciente durante todo el periodo comprendido entre la intervención de explantación y la reimplantación, hecho que requiere un tratamiento provisional del paciente con medios auxiliares en su domicilio o en centros de asistencia (en estos casos suelen ir asociados a un coste económico para el paciente).
Indicaciones
- Cualquier infección detectada de una PTR con sintomatología durante más de cuatro semanas, independientemente del momento de la implantación.
- Cualquier dehiscencia de la herida con endoprótesis suelta durante más de dos semanas.
- Todos los pacientes que puedan ser sometidos a una cirugía quirúrgica en dos tiempos.
- Identificación segura de gérmenes multirresistentes en la articulación.
Contraindicaciones
- En el caso de pacientes de grado C según McPherson1, la cirugía de recambio supone más inconvenientes que ventajas para su salud y suele ser útil la colocación de una fístula controlada.
- La proliferación de gérmenes puede constituir un serio riesgo para la vida de los pacientes con sepsis grave. En estos casos se indica la realización de una intervención de descompresión. Una vez estabilizada, se puede extraer la prótesis sin ningún riesgo.
- En el caso de pacientes con partes blandas extensas y, por ejemplo, con una enfermedad arterial periférica u otras comorbilidades, que no pueden ser sometidos a una intervención plástica de reconstrucción con recubrimiento mediante colgajos, se deberá decidir sobre la necesidad de amputar el muslo.
Información para el paciente
- Riesgos quirúrgicos generales
- Pérdida del hueso/fractura
- Hemorragia
- Transfusión de sangre
- Extracción del cemento con apertura de ventanas en el fémur y/o en la tibia
- Inserción de cerclajes
- Inserción de espaciadores y/o cadenas de PMMA
- Luxación del espaciador
- Acortamiento de la pierna
- Limitación de la movilidad de la rodilla
- Lesiones del nervio peroneo
- Lesiones del nervio tibial
- Lesión de la arteria poplítea
- Recidiva de la infección
- Trombosis
- Amputación del muslo como consecuencia
Preparación de la intervención
- Radiografía de la rodilla en dos planos (plano longitudinal, con proyección completa de la prótesis); en caso de endoprótesis de cadera ipsilateral, radiografías actuales de la cadera (con proyección completa de la prótesis).
- Poner a disposición suficientes reservas de sangre.
- Documentación sobre el diagnóstico clínico-neurológico, sobre todo de la función del nervio peroneo.
- Para todos los tipos de prótesis, presentar el pasaporte de implantes o, preferiblemente, el informe quirúrgico de la implantación, con indicación del tipo de prótesis.
- Para todas las prótesis semi-articuladas o de bisagra, solicitar el instrumental para su extracción.
Instrumental
- Instrumental básico.
- Instrumental adicional del fabricante de la prótesis.
- Cincel y extractor de clavos retrógrados para la extracción del cemento.
- Si es preciso, broca para cavidad intramedular.
- Lavado con chorro de agua.
- Si es preciso, juego de cerclajes.
- Cemento PMMA para la fabricación del espaciador.
- Instrumental para complicaciones intraoperatorias.
Anestesia y posición del paciente
- Anestesia total o espinal.
- Isquemia de muslo.
- Posición de decúbito supino, pierna sana en posición ligeramente hacia abajo.
- Posición del muslo sobre rodillo móvil a la altura de la isquemia (no en el hueco poplíteo, tener precaución con el nervio peroneo, nervio tibial, vena poplítea).
- Posicionar la pierna de modo que tenga completa libertad de movimientos y cubrirla para la fluoroscopia con arco en C del fémur en proyección lateral mediante elevación.
- Previo acuerdo con el anestesista, planificar un catéter para el dolor en caso de requerir analgesia de larga duración local postoperatoria.
Técnicas quirúrgicas
(Figs. 1-10)
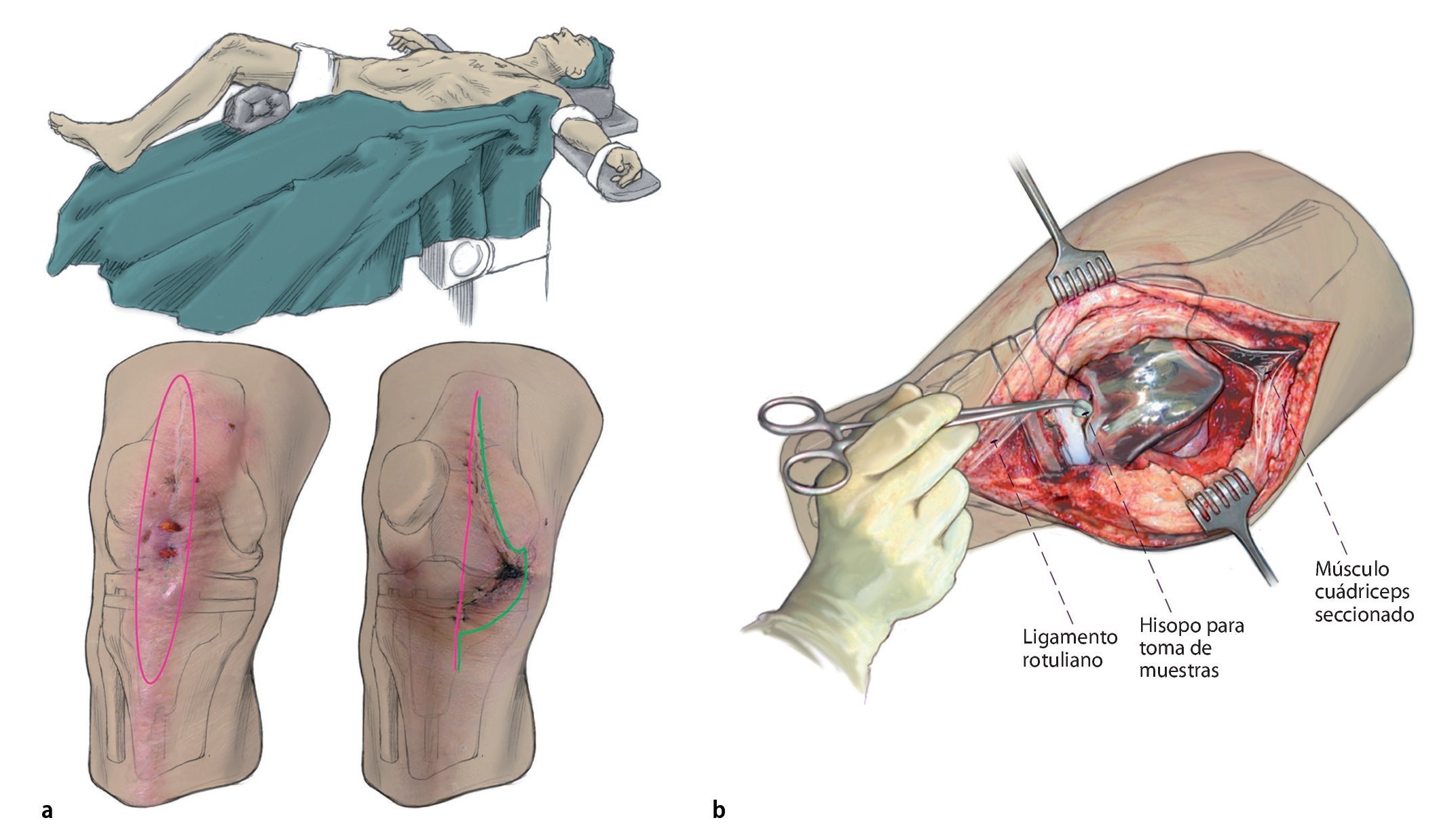
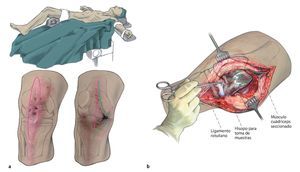
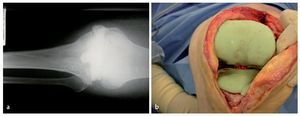
Fig. 1 La sección cutánea se tiene que realizar sobre la antigua cicatriz de abordaje o, como mínimo, debe tener la misma longitud que en el primer abordaje (a). Las fístulas y las dehiscencias de la herida que aparezcan en la zona de la cicatriz/herida se seccionarán longitudinalmente de forma ovalada (forma de piedra de afilar). Las fístulas que se encuentren fuera del abordaje a la articulación se reseccionarán solo con un puente cutáneo suficiente y, si es preciso, se pueden curetear. Además, durante la extracción de la prótesis también se realizará en primer lugar la sinovectomía completa en la zona ventral y en el receso lateral. Se pondrá atención de no dañar el aparato extensor en la zona de la inserción del ligamento rotuliano a pesar de tener que realizar el desbridamiento durante la lateralización de la rodilla. Si la rodilla se encuentra contracturada, se recomienda seccionar el tendón del cuádriceps en el tercio medial (b). En el paso siguiente se extrae el polietileno y se desacopla la prótesis; a continuación, se completa la sinovectomía en el receso posterior. Se extraerá una toma de muestras con tejido sinovial.
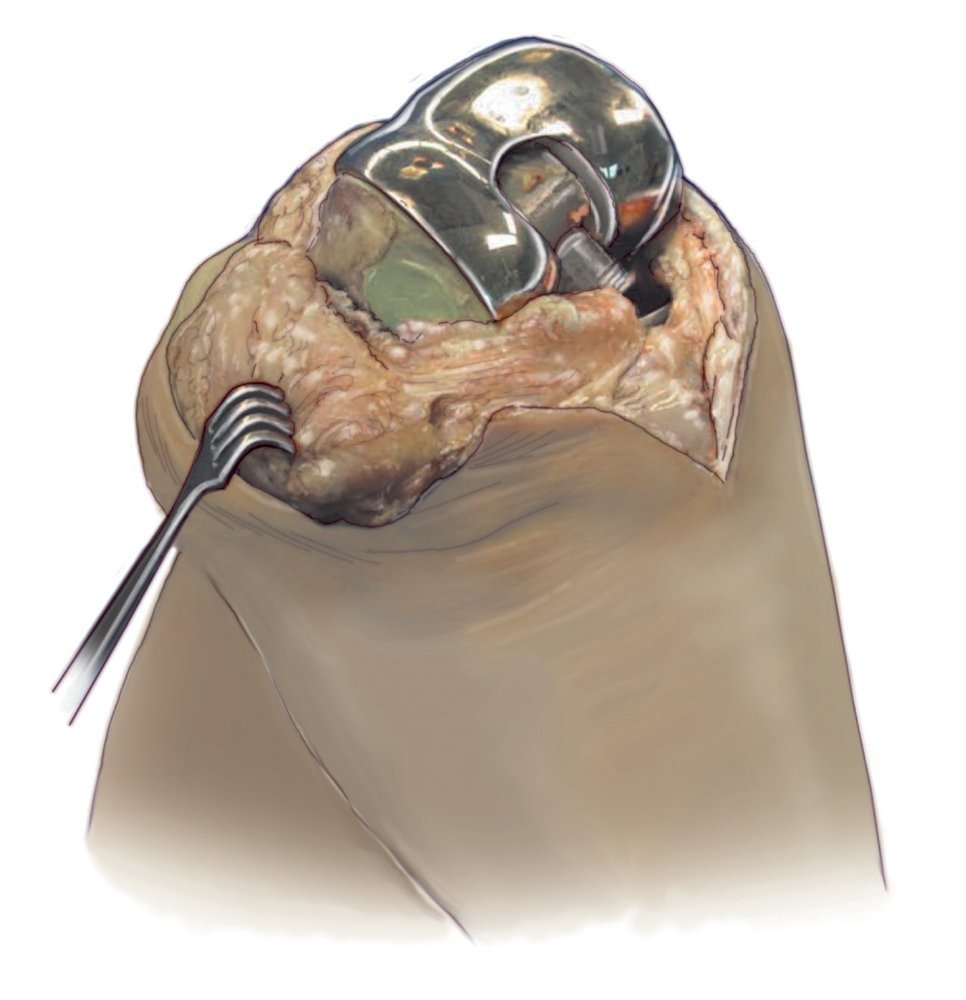
Fig. 2 Liberar suficientemente los cóndilos femorales medial y lateral de modo que se garantice una flexión máxima de la rodilla. La posición de flexión se puede mantener con el rodillo móvil como soporte para el posicionamiento del paciente.
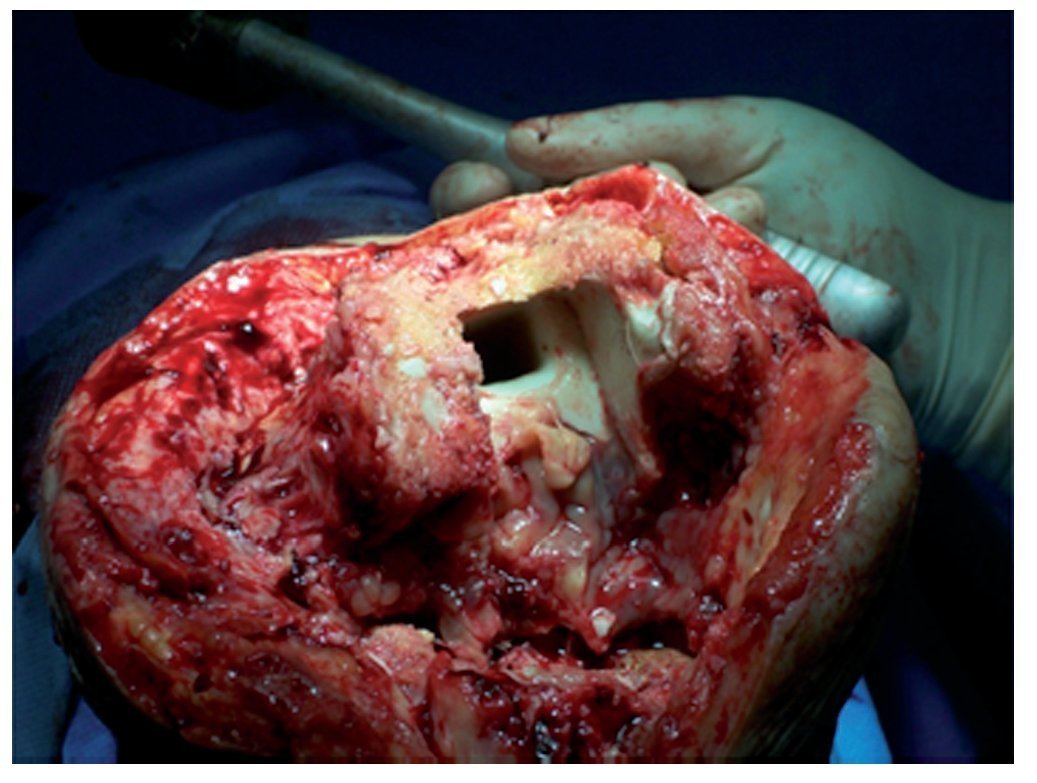
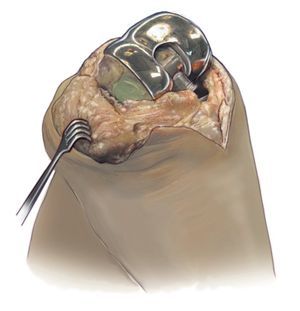
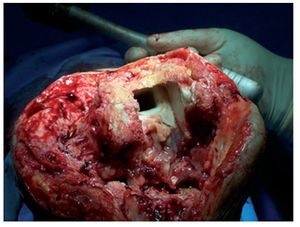
Fig. 3 Sitio intraoperatorio después de la extracción del vástago protésico. En la cavidad medular se puede reconocer el soporte de cemento remanente. Diagnosis después de la extracción de la prótesis. Si se cincela con cuidado, se puede reducir la pérdida ósea; generalmente se suelta primero la interface metal cemento.
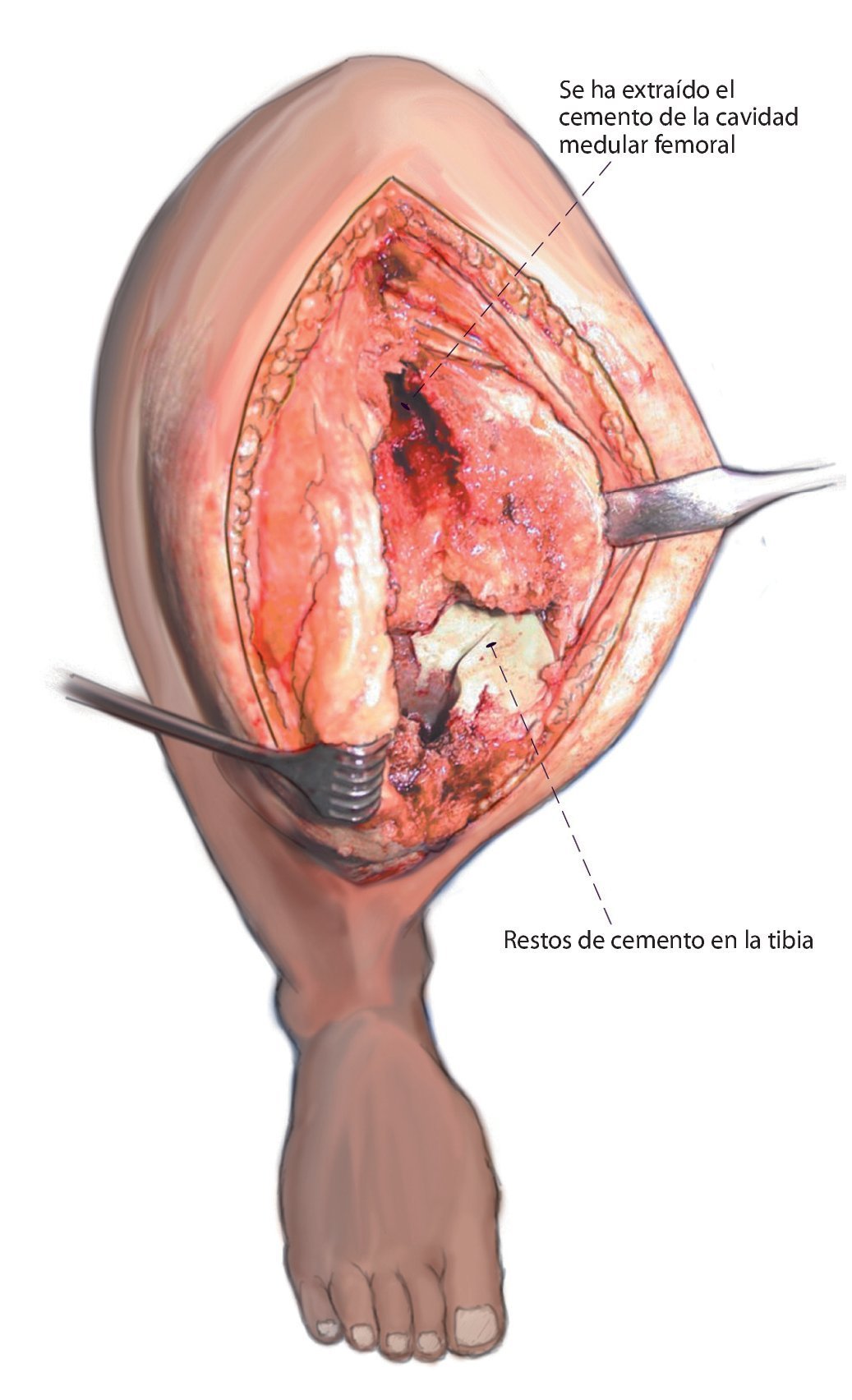
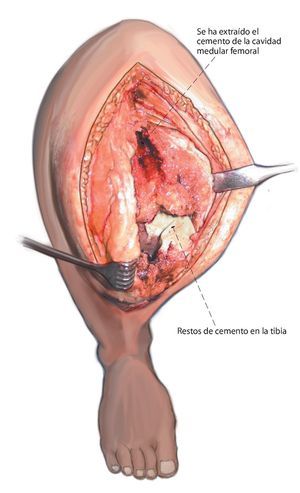
Fig. 4 Se ha extraído el cemento del espacio de la médula ósea. Los restos de cemento se pueden reconocer con facilidad en la tibia.
Fig. 5 Instrumentos de extracción diversos.
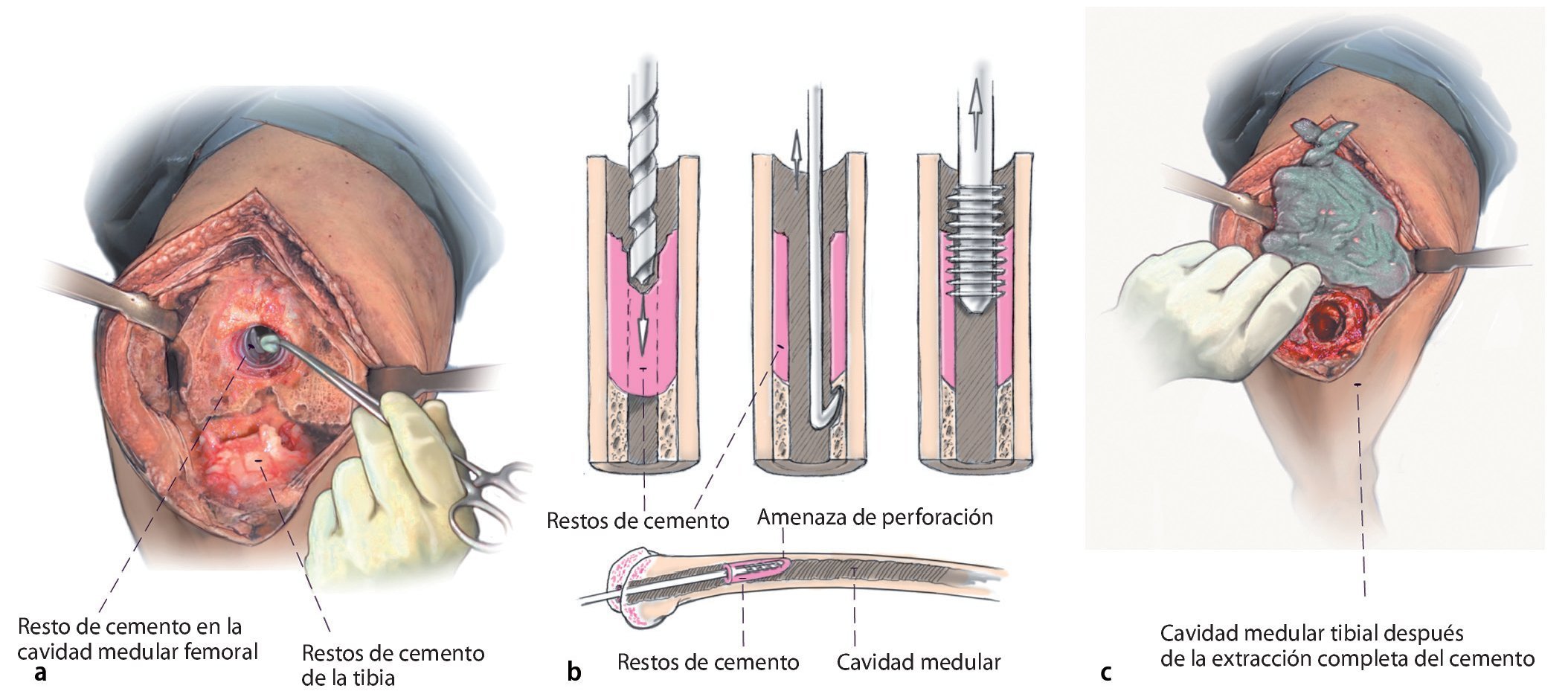
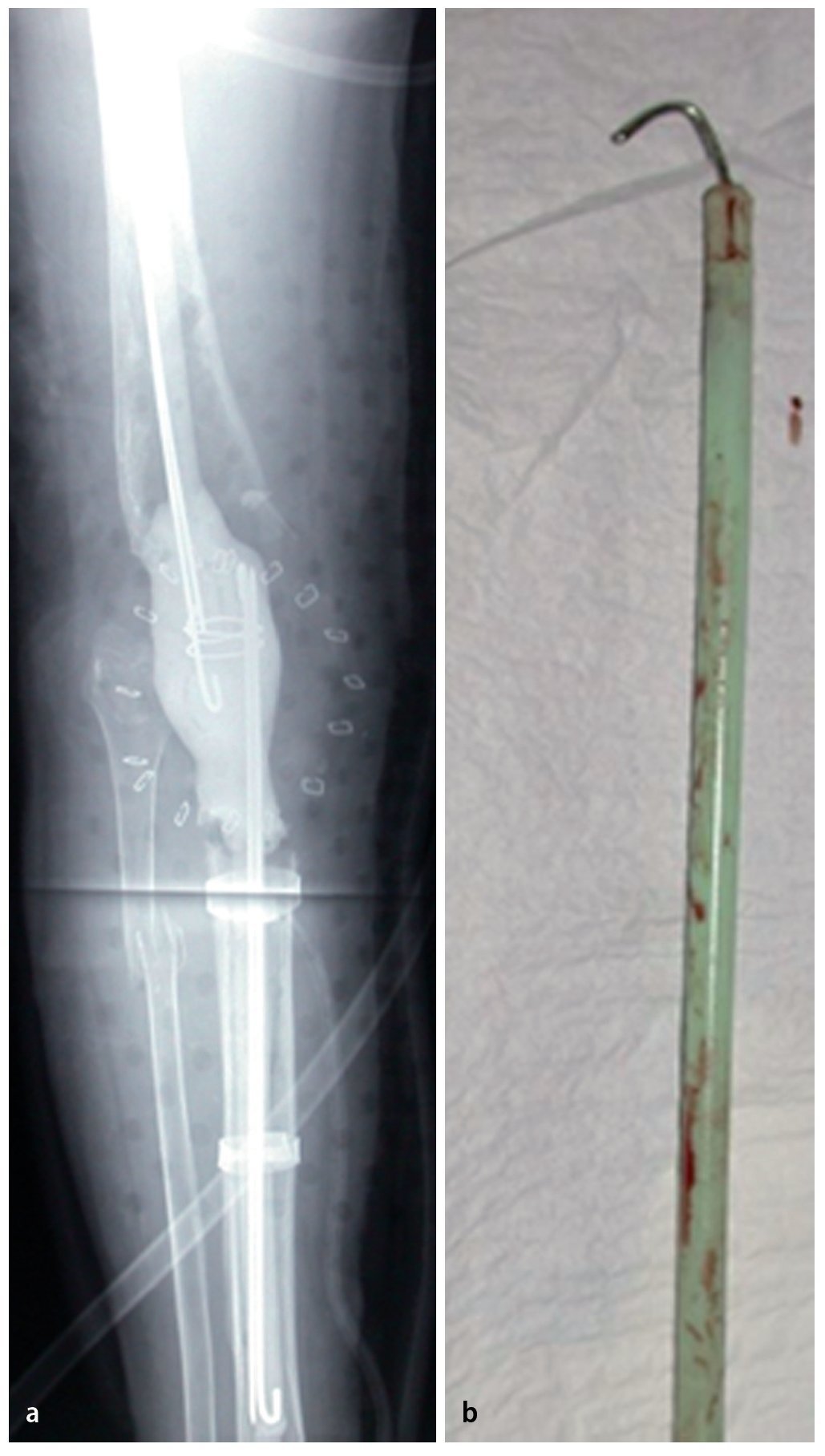
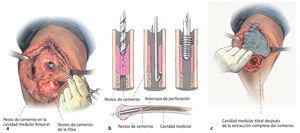
Fig. 6 Se extraen todos los restos de cemento y todas las membranas de la cavidad medular femoral. En el mercado existen diferentes instrumentos de extracción. De forma rutinaria se efectúa una segunda toma de muestras de la cavidad medular. Se deberán extraer con sumo cuidado todos los restos de cemento de la cavidad medular. Se realizará un control minucioso para garantizar la completa extracción de todos los restos de cemento. a) Resto de cemento en la cavidad medular proximal. b) El soporte de cemento cerrado proximal se debería perforar por el centro. Generalmente, con el extractor de clavos y el cincel retrógrado es posible extraer todos los restos de cemento. Extracción de soportes de cemento cerrados mediante perforación e inserción de un extractor de clavos, agujas roscadas o similar. Atención: es posible la realización de una vía falsa sobre todo en la antecurvatura del fémur (defecto óseo ventral). c) En el paso siguiente se realiza la extracción del componente tibial con la misma extracción de cemento como en femoral. También en este caso se efectúa una tercera toma de muestras.
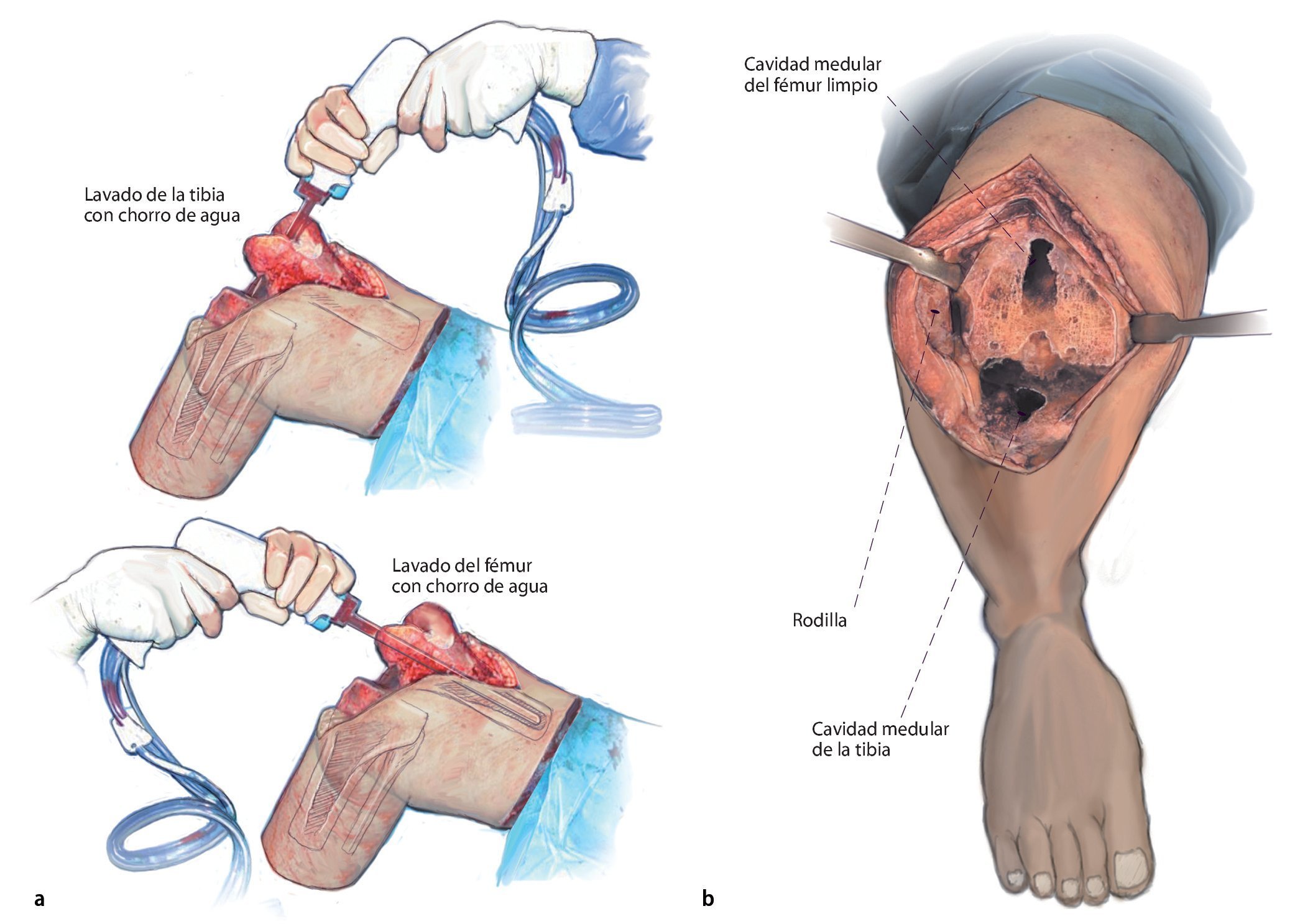
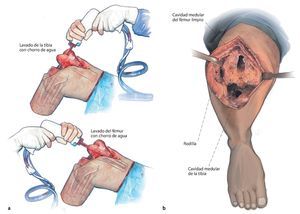
Fig. 7 a) A continuación se realiza un lavado minucioso con chorro de agua. Las cavidades medulares se pueden limpiar mecánicamente con el cepillo para médula ósea y a continuación se lava con una tobera larga. Después se debe colocar un nuevo paño quirúrgico, cambiar los guantes de todo el equipo y sustituir también el succionador. Por último, hay que extraer todo el material extraño, todo el tejido granular y todos los restos óseos. b) Estado después del lavado con chorro de agua. A continuación de esta fase se abre la isquemia, se introduce una compresa quirúrgica o, mejor, unas cuantas compresas en la cavidad medular de la tibia y del fémur y se espera a que se produzca la fase hiperémica bajo compresión durante tres minutos. A continuación se realiza la hemostasia.
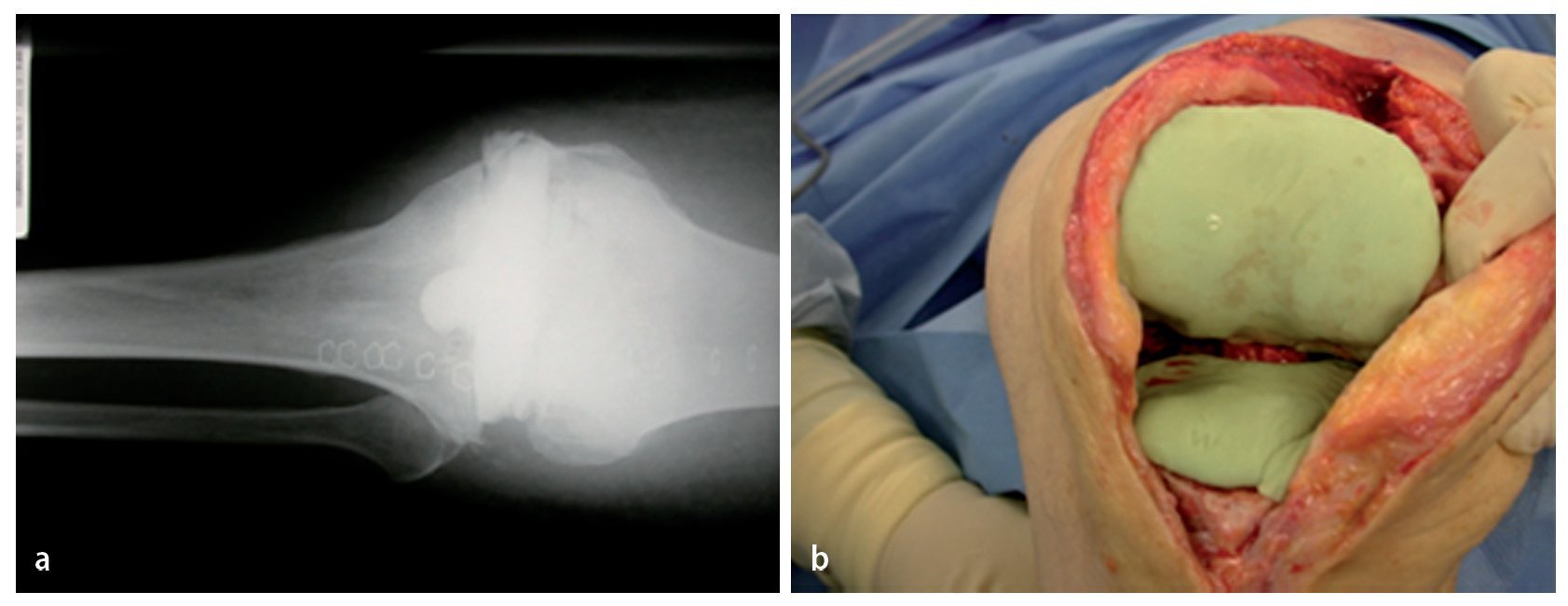
Fig. 8 Desde el punto de vista facultativo, ahora se puede conformar un espaciador monobloc (a) o un espaciador articulado para el macizo condíleo y el platillo tibial (b) formado por cemento de polimetilmetacrilato, que rellena el espacio hueco del surco articular ensanchado y que cierra a ras las superficies óseas que suelen sangrar fuertemente. El cemento debe contener gentamicina y clindamicina, que se complementan sinérgicamente cuando son liberadas. En caso de ser necesario según antibiograma, se puede añadir vancomicina y colistina. a) Radiografía de un espaciador monobloc in situ. b) Espaciador articulado «hecho a medida» in situ.
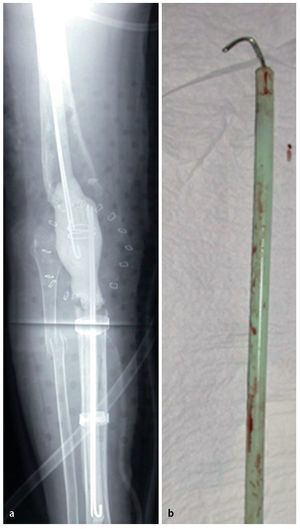
Fig. 9 a) Radiografía de un espaciador para el puenteo de defectos con fijación de la cavidad medular. b) Detalle del clavo de cemento integrado en el cemento PMMA (agujas de perforación revestidas con cemento PMMA). El espaciador se dimensionará delgado, de modo que sea posible el cierre de la herida libre de tensiones por encima del drenaje. La existencia de grandes partes de defectos óseos comporta una inestabilidad absoluta de la pierna, que no se puede estabilizar con ortesis. Es posible aplicar un fijador externo; sin embargo, tiene el inconveniente de crear una unión permanente con la cavidad medular desde fuera («pin track»). Por otra parte, aumenta el riesgo de infección para la futura prótesis. Estas franjas de defectos se pueden puentear con espaciadores para médula espinal fabricados de PMMA.
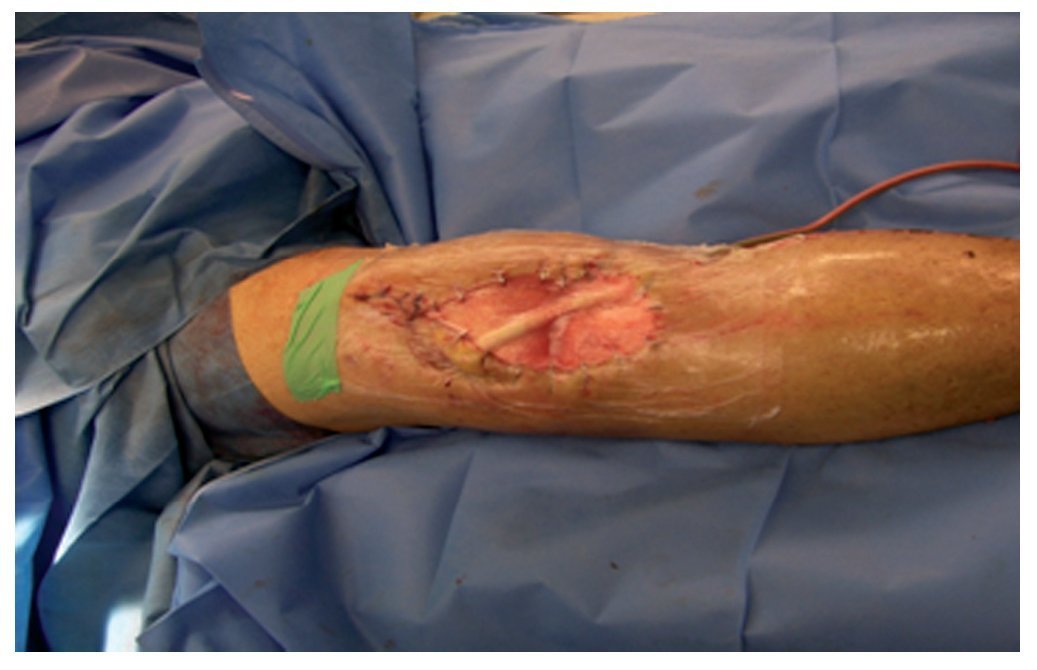
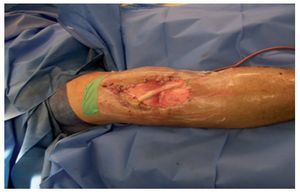
Fig. 10 Si no es posible cerrar la herida a pesar del pequeño tamaño del espaciador, se recomienda realizar un sellado al vacío de la herida. El recubrimiento de defectos mediante cirugía de colgajo de gastrocnemio no se debería realizar hasta la reimplantación de la PTR, puesto que el colgajo puede cicatrizar sobre el espaciador, de modo que sea demasiado pequeño para cubrir la prótesis definitiva. Después del vendaje y de un almohadillado de algodón se pondrá la pierna en reposo en una férula dorsal en la rodilla en ligera posición en flexión.
Tratamiento postoperatorio
- Férula de fijación y reposo en cama durante tres días. Después, movilización con la férula sin carga de la pierna.
- El drenaje debería dejarse hasta que la cantidad diaria de secreción disminuya por debajo de 50 ml, a fin de prevenir punciones de hematomas innecesarias.
- Ocho semanas hasta la reimplantación de la PTR.
- Antibiosis
• Terapia antibiótica sistémica durante cuatro semanas según antibiograma
• Dos semanas de pausa de la terapia antibiótica
• A continuación, punción de la rodilla ambulante con dos semanas de incubación del frasco con el líquido obtenido en la punción.
Errores, riesgos y complicaciones
- Irritaciones o lesiones permanentes del nervio peroneo debido a una fuerte presión lateral, especialmente si la rodilla está contracturada.
- Debilitamiento o rotura del aparato extensor en caso de estructuras contracturadas en la zona de inserción a la tuberosidad tibial.
- Fisuras y fracturas durante la extracción del cemento en huesos con pérdida de densidad en la interface hueso-cemento.
• En la convexidad de la antecurvación femoral, precisamente, se pueden producir defectos óseos desapercibidos.
• Es posible conservar un soporte óseo estable mediante la aplicación de procedimientos realizados por pasos, que suelen ser laboriosos y que se deben efectuar con cuidado.
• Se prestará atención a las fisuras longitudinales; se estabilizarán con cerclajes para hacer posible la reimplantación.
• Se recomienda realizar controles radiológicos intraoperatorios.
- Gran pérdida de sangre por las cavidades medulares abiertas.
• La comunicación entre el cirujano y el anestesista es muy importante, sobre todo si ya no existe oclusión vascular.
• No sobrepasar el tiempo de isquemia de dos horas continuas.
Conclusiones para la práctica
- La intervención de recambio en dos tiempos es el procedimiento más utilizado tanto en Europa como en los EE. UU. ante una infección de endoprótesis total de rodilla; en los EE. UU. es considerada incluso el tratamiento de elección o «Gold standard».
- Sin embargo, actualmente la intervención de recambio en un tiempo como alternativa es tema de debate, puesto que presenta resultados igual de buenos3,5,9,10.
- Por último, se trata de elaborar un régimen terapéutico a medida para cada paciente, que se corresponda exactamente a su situación individual y que persiga un único objetivo: la eliminación permanente de la infección bajo preservación de la pierna afectada.
- La base es un desbridamiento suficientemente radical durante la primera intervención de revisión6,12.
- La terapia antibacteriana adyuvante es necesaria para seguir reduciendo las tasas de recidiva. El espectro de patógenos no solo requiere un dominio total de la rutina quirúrgica, sino también una colaboración multidisciplinaria con infectólogos y microbiólogos4.
- Con los datos actuales, no consideramos procedente declarar apodíctico ninguno de los procedimientos de recambio en uno o en dos tiempos. Se dará prioridad a un concepto establecido acordado conjuntamente con todas las disciplinas que participan en el tratamiento.
Conflicto de intereses. El autor del presente trabajo declara que no existe ningún conflicto de intereses para él ni para los co-autores.
Correspondencia
Dr. P. Herrmann
Abteilung Unfall-, Wirbelsäulen- und Gelenkchirurgie,
Asklepios-Südpfalzklinik Kandel
Luitpoldstr. 14, 76870 Kandel (Alemania)
pe.herrmann@asklepios.com