Alivio del dolor, recuperación de la función y rango de movilidad activos.
Indicaciones
Prótesis de hombro en fracturas fallidas con manguito rotador insuficiente, pseudoparálisis, inestabilidad crónica, anquilosis severa.
Contraindicaciones
Destrucción glenoidea avanzada. Lesiones severas del deltoides (> 50%) y parálisis del nervio axilar. Infección florida.
Técnica quirúrgica
Abordaje deltopectoral. Exposición del implante aflojado, retirada mediante fenestración en el húmero. Liberación periarticular con preservación de estructuras neurovasculares. Exposición de la glenoides, fijación no cementada de la placa base (metaglena) y colocación de la bola glenoidea (glenoesfera). Fenestración de la diáfisis humeral, extracción del cemento, colocación de cerclajes de sutura y alámbricos, y cementación del componente humeral (vástago de revisión largo) con un ángulo de retroversión de 10-30º tomando como referencia el eje longitudinal del antebrazo. Reconstrucción anatómica de las partes blandas con preservación de los rotadores externos (reinserción de las tuberosidades desplazadas, y en caso de ser necesario, transposición del latissimus dorsi y teres major según la técnica de LEpiscopo).
Manejo postoperatorio
Férula de abducción y ejercicios pasivos y activosasistidos incluyendo movilidad pasiva continua (Ormed, Friburgo, Alemania) durante 6 semanas tras la intervención.
Resultados
Entre los años 2000 y 2005, se llevaron a cabo 84 cirugías de revisión de hombro con prótesis invertida a través de una ventana ósea en el húmero, de las cuales 34 eran revisiones de fracasos de hemiartroplastias en fracturas (cinco hombres, 29 mujeres). En 25 de los pacientes se realizó un seguimiento que alcanzó los 59 meses postoperatorios; otros nueve pacientes fueron entrevistados telefónicamente o por escrito (n = 34, edad media 68 años [59-82 años], seguimiento medio 31,5 años [12-59 meses]). La puntuación de la escala de Constant ponderada por edad y género fue de 17,5% y mejoró hasta alcanzar el 63% en el postoperatorio. El arco de movilidad para la flexión activa y la rotación interna mejoró sustancialmente (flexión media preoperatoria 48%, postoperatoria 125%). Todos los pacientes obtuvieron el alivio del dolor. La función estaba relacionada a la magnitud de la lesión de partes blandas. Catorce pacientes estaban muy satisfechos con el resultado quirúrgico, 16 estaban satisfechos y cuatro insatisfechos. En total había ocho complicaciones.
Notas preliminares
La principal indicación para colocar una prótesis invertida8 es la pseudoparálisis dolorosa con artropatía por déficit del manguito de los rotadores en pacientes de edad avanzada. La experiencia en otras indicaciones es limitada, especialmente en reprótesis, por tanto hay pocos casos publicados en la literatura científica6. La indicación principal para una prótesis invertida como implante de revisión es una hemiartroplastia por fractura fallida con pseudoparálisis dolorosa4, y con menor frecuencia, inestabilidades. Los resultados de la hemiartroplastia para fracturas son peores que en el tratamiento de la artrosis primaria de la articulación del hombro12,15. En el año 2001, Boileau et al3 presentaron un estudio multicéntrico, con una muestra de 71 prótesis en fracturas y publicaron resultados muy buenos en 16%, buenos en 26%, satisfactorios en 25%, y malos en 33%, especialmente en fracturas antiguas, y alertaron sobre la osteotomía de las tuberosidades, que se identificó como factor de riesgo especialmente dando lugar a resultados especialmente malos o impredecibles. Sin embargo, el análisis de 30 hombros con fracaso de prótesis colocada por fractura desplazada del húmero proximal indicó múltiples causas del fracaso del sistema de fractura1: los resultados estaban primariamente influenciados por una reducción anatómica y una fijación de las tuberosidades insuficientes10, desplazamiento secundario y migración, e insuficiencia consecuente del manguito de los rotadores. Dado que la retracción del manguito de los rotadores con la subsiguiente fibrosis, atrofia e infiltración grasa es irreversible, el éxito de los procedimientos sobre las partes blandas o de los implantes anatómicos como alternativa es limitado.
La complejidad de la cirugía de revisión protésica del hombro se refleja así, en forma de resultados claramente inferiores comparados con la sustitución protésica articular primaria. No se puede predecir el éxito como seguro, y el alivio del dolor tan sólo se obtiene en el 60% de los pacientes11, la mejoría funcional es rara, si hay insuficiencia del manguito de los rotadores. La insuficiencia del músculo subescapular con migración anterosuperior, subluxación o incluso luxación es un hallazgo frecuente en este contexto.
Nuestros propios resultados para 17 casos de revisión con sistema de prótesis total invertida tras colocación en casos postraumáticos primarios revelan unos resultados muy descorazonadores con una mejoría de la función ponderada por edad en la Escala de Constant del 20% al 69% al año de seguimiento7.
Debido a la patología subyacente asociada a la cirugía de revisión, los siguientes factores son importantes para el resultado funcional:
- Retirada del implante previo a través de una ventana ósea en el húmero con mínima pérdida de hueso y preservación de la vascularidad de los fragmentos14.
- Anclaje seguro del implante de revisión con restauración de la longitud humeral.
- La centralización de la articulación glenohumeral proporciona al músculo deltoides un nuevo fulcro y un brazo de palanca mejorado.
- Intento de reconstrucción parcial del manguito de los rotadores, especialmente para recuperar la función de los rotadores externos. Si ya no hay sustancia adecuada disponible, se puede valorar la posibilidad de realizar una transposición del latissimus dorsi o del teres major. Sin embargo, esto compromete aún más la rotación interna ya de por sí limitada y la vascularidad del hueso residual.
- La preservación definitiva de la función del pectoralis major ya que esto tendrá un efecto favorable en la flexión, especialmente en los frecuentes casos de defectos en la porción anterior del músculo deltoides.
- La movilización y la reinserción de las tuberosidades5 proporciona remanentes del manguito de los rotadores (los signos de infiltración grasa en la TC son importantes, la RNM no suele ser posible debido a los artefactos metálicos).
- Liberación periarticular para movilizar las tuberosidades desplazadas, incluyendo la resección de adherencias y tejido cicatricial.
La revisión precisa un análisis preoperatorio cuidadoso individualizado de los casos, teniendo en cuenta los siguientes factores:
- Cicatrices de heridas previas.
- Situación de las partes blandas, especialmente del músculo deltoides.
- Situación neurológica (nervio axilar, plexo).
- Osificaciones heterotópicas periarticulares.
- Desplazamiento de las tuberosidades.
- Stock óseo de la glenoides y del húmero (osteoporosis, destrucción).
- Análisis del fracaso de la prótesis previa: aflojamiento, malalineación, anclaje, implantación cementada o no cementada, tapón endomedular, reconstrucción de la altura humeral (medición del húmero en proyección antero-posterior [AP] de los lados afecto y contralateral).
- Diagnóstico para la infección de bajo grado (hallazgos preoperatorios, serología, curso clínico, biopsias intraoperatorias, y en caso de duda, aspiración preoperatoria de la cavidad articular).
Principios quirúrgicos y objetivos
Recuperación de la función del hombro, y si es posible, libre de dolor, mediante revisión con un implante que proporciona al músculo deltoides un nuevo fulcro, un centro de rotación medializado con una pretensión adecuada de manera que el defecto del manguito de los rotadores queda compensado.
Ventajas
Restitución de una función del hombro satisfactoria en comparación con la artrodesis o la artroplastia de resección tras la retirada de una hemiartroplastia.
Procedimiento de salvamento para una hemiartroplastia postraumática fallida.
Inconvenientes
Aún no se dispone de resultados a largo plazo.
La rotación externa activa no se puede mejorar en la mayoría de los casos.
Tasa de complicaciones más elevada que en la artroplastia primaria.
Técnica quirúrgica difícil.
Indicaciones
Sustitución protésica postraumática primaria del hombro fallida en pacientes de edad avanzada en los cuales no hay manguito de los rotadores o éste es insuficiente.
Relativas
Anquilosis moderadamente dolorosa o inestabilidad crónica de una hemipótesis.
Contraindicaciones
Lesión avanzada del músculo deltoides con parálisis o atrofia muscular irreversible, que conduce a la pérdida de > 50% de la masa muscular.
Destrucción extensa de hueso glenoideo de manera que no hay anclaje para la placa base (metaglena).
Relativas
Destrucción glenoidea que se puede manejar con colocación de un implante de revisión (metaglena con un tetón central largo o con aletas) y/o posibilidad de injerto corticoesponjoso (procedimiento en dos tiempos).
Paciente con edad < 70 años.
Información para el paciente
Riesgos quirúrgicos generales.
Lesiones neurovasculares, especialmente parestesia de los nervios axilar o radial y del plexo braquial.
Limitación funcional permanente.
Aflojamiento/fallo mecánico de los componentes protésicos (p. e., desacoplamiento de los componentes).
Limitaciones funcionales residuales, p. e., restauración insuficiente de la rotación externa activa y reducción de la rotación interna (con frecuencia la mano sólo puede alcanzar la parte posterior de las nalgas).
Fallo por fatiga de la espina de la escápula y del acromion, fractura periprotésica del húmero por una caída.
Fractura intraoperatoria del húmero con riesgo de pseudoartrosis y salida del cemento dentro de las partes blandas.
Inmovilización del brazo en una ortesis de abducción durante 6 semanas con ejercicios pasivos y activos-asistidos.
Resultados a largo plazo de > 15 años desconocidos para las prótesis invertidas de hombro.
Planificación preoperatoria
Inspección del estado de las partes blandas, incluyendo los abordajes quirúrgicos previos.
Investigación serológica para descartar infección de bajo grado (recuento celular, PCR, VSG).
Aspiración de la efusión, y en caso de ser necesario, análisis microbiológico del aspirado sinovial.
Examen neurológico con análisis de la función de cada una de las tres partes del deltoides (parte espinal, acromial, y clavicular), valoración de los signos deficitarios "lag signs" como parámetros sensibles de la parálisis del músculo deltoides.
Registro del arco de movilidad activo y pasivo y análisis de las inestabilidades funcionales.
Radiografías del hombro en los tres planos (AP = "glenoidea verdadera", axial, "outlet" torácico), con aparato de escopia para inestabilidades dinámicas, según se precise.
Para la destrucción ósea: imágenes de TC de alta resolución con reducción de artefactos, especialmente para valorar el stock óseo glenoideo.
Análisis radiológico de la situación del hueso y de las partes blandas para una planificación preoperatoria adecuada. Las medidas se marcan en la proyección AP del húmero afecto y del contralateral con medición con plantilla y con cabeza femoral metálica (diámetro de 28 mm) a nivel del hueso para determinar el tamaño y la longitud humeral adecuados.
Esquemas de planificación (digital o plantillas) y decisión del tamaño de los componentes y de la longitud del vástago.
Instrumental quirúrgico e implantes
Equipo de extracción de prótesis articular total, en particular, brocas y fresas de diámetro creciente, escoplos de hoja recambiable.
Equipo estándar de hombro con separadores de Roux y separadores automáticos.
Rotadores musculares de Rowe y separadores de valva de Kölbel (Link Co., Hamburgo, Alemania) y separadores en anillo de Fukuda de los tamaños apropiados.
Sierra oscilante de alta frecuencia y/o cortador de hueso de alta frecuencia (para sacar el cemento).
Conjunto de implantes de revisión modulares (preferentemente de Tornier Co., Burscheid, Alemania, ya que esta compañía ofrece vástagos de longitud hasta 210 mm, alternativamente DePuy Co., Kirskel-Limbach, Alemania). Instrumental de extracción universal (p. e., DePuy Co.).
Caja de instrumental específico para prótesis e implantes de prueba para prótesis invertida de hombro (p. e. los de Tornier y DePuy) con vástagos de revisión largos especiales (150 mm, 180 mm, y 210 mm). La compañía Tornier ofrece diáfisis de revisión con tornillos de bloqueo para bloquear el componente humeral proximal.
Anestesia y colocación
Posición de silla de playa con brazo tallado libre.
Anestesia general, posiblemente en combinación con bloqueo interescalénico del plexo braquial.
Técnica quirúrgica
Figuras 1 a 9
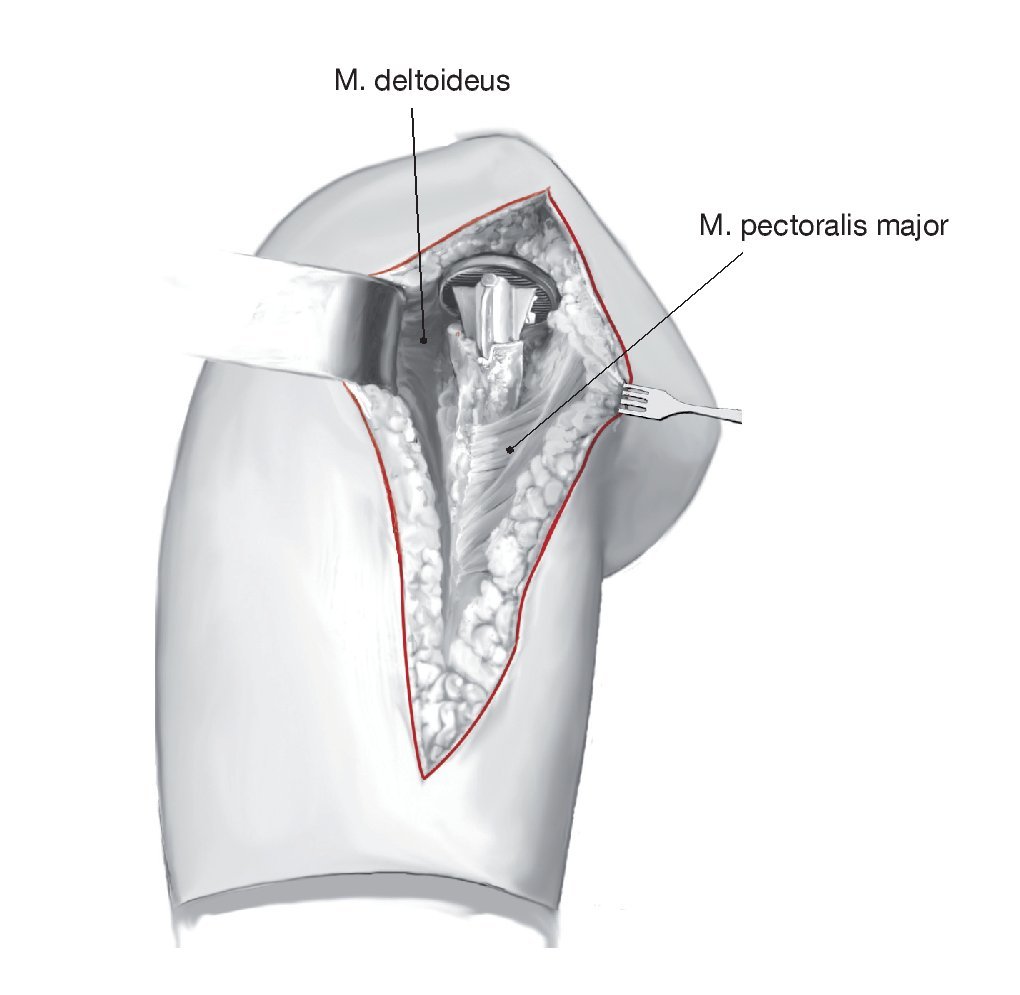
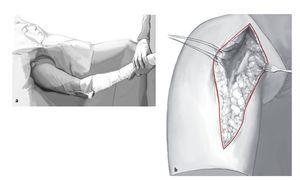
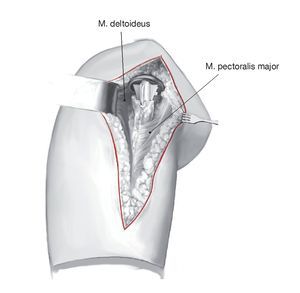
Figuras 1a y 1b. Colocación del paciente y abordaje. Posición de silla de playa estándar para cirugía del hombro de manera que el brazo pueda moverse libremente en el borde de la mesa de operaciones (a). El brazo se venda con una venda elástica hasta el nivel del codo para dejar sitio para una posible extensión distal de la incisión en caso de fractura humeral distal. En este último caso, es necesario exponer el nervio radial y se separa con una lazada. Se ha demostrado que impregnar la envoltura de la incisión con yodo es útil para la profilaxis de la infección, pero no se puede realizar si el paciente tiene alergias conocidas (3-M Co., Neuss, Alemania). Abordaje deltopectoral del hombro utilizando la línea de la cicatriz previa (b). La incisión cutánea sobre el surco deltopectoral empieza en la clavícula, discurre medial desde la apófisis coracoides en sentido distal sobre la cara anterior del brazo. División del tejido celular subcutáneo, identificación del surco deltopectoral y de la vena cefálica. Si la vena todavía está presente, se diseca y se separa lateralmente. Disección cuidadosa con liberación del tejido cicatricial y exposición del origen del tendón conjunto en la apófisis coracoides. Lateralmente, disección hasta el húmero con liberación subacromial cuidadosa y exposición de los restos del manguito de los rotadores, posiblemente con fragmentos de hueso adheridos. Se moviliza el músculo deltoides subperiósticamente preservando los nervios axilares circunflejos.
Figura 2 Luxación del húmero proximal con hemiartroplastia in situ: ausencia de tuberosidades y de manguito rotador. Siempre que sea posible, conservar los restos del manguito de los rotadores (el teres minor con frecuencia permanece intacto), y se movilizan los restos de tuberosidades utilizando suturas de tracción. Tenodesis del tendón de la porción larga del bíceps (si está presente) con suturas reabsorbibles (1-0) in situ. Exposición subperióstica del húmero distalmente siguiendo el surco intertuberositario, conservando la inserción del pectoral mayor. Disección roma alrededor del músculo pectoral y colocación de una cinta de material sintético suave a través del mismo. Exposición anterior del húmero mediante rotación externa del brazo, y en caso de implantes modulares, extracción del componente protésico de la cabeza. Extracción del cemento accesible por debajo de la cabeza de la prótesis y de la metáfisis. Disección con pequeños escoplos a lo largo del implante proximal en el intersticio y aflojamiento cuidadoso. Si la prótesis de hombro no se puede extraer, se realiza una ventana humeral anterior. El primer corte de la ventana se realiza lateralmente a la inserción del pectoral mayor con la sierra oscilante y a continuación, tras el corte medial, se moviliza con escoplos.
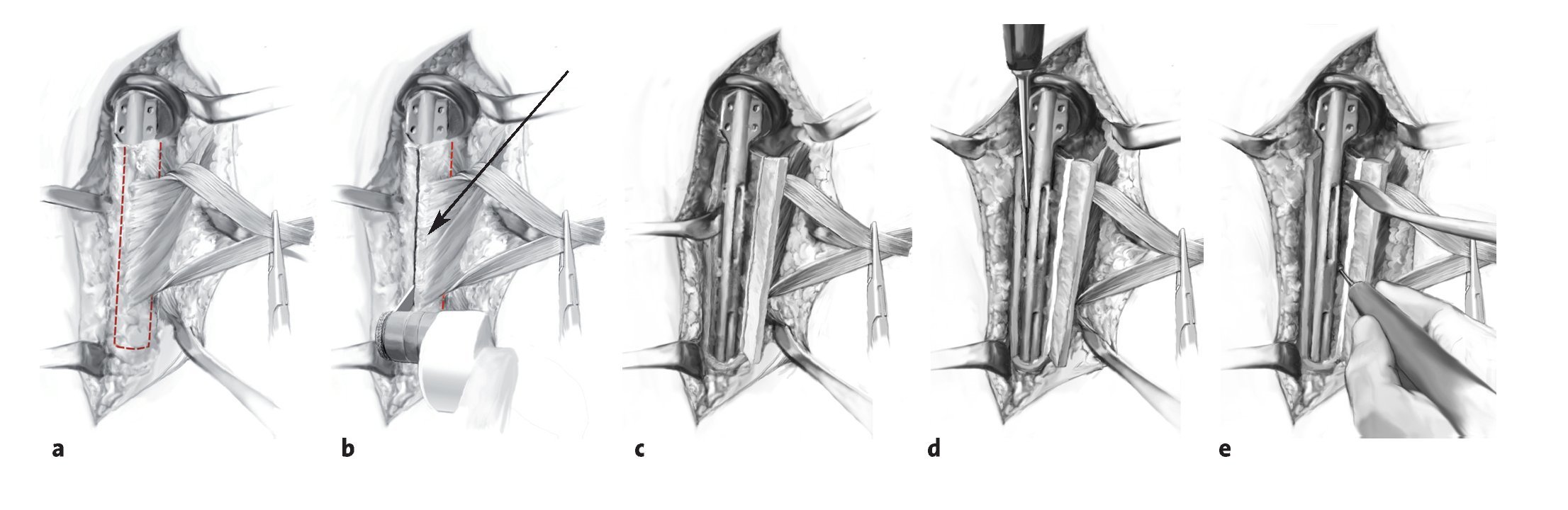
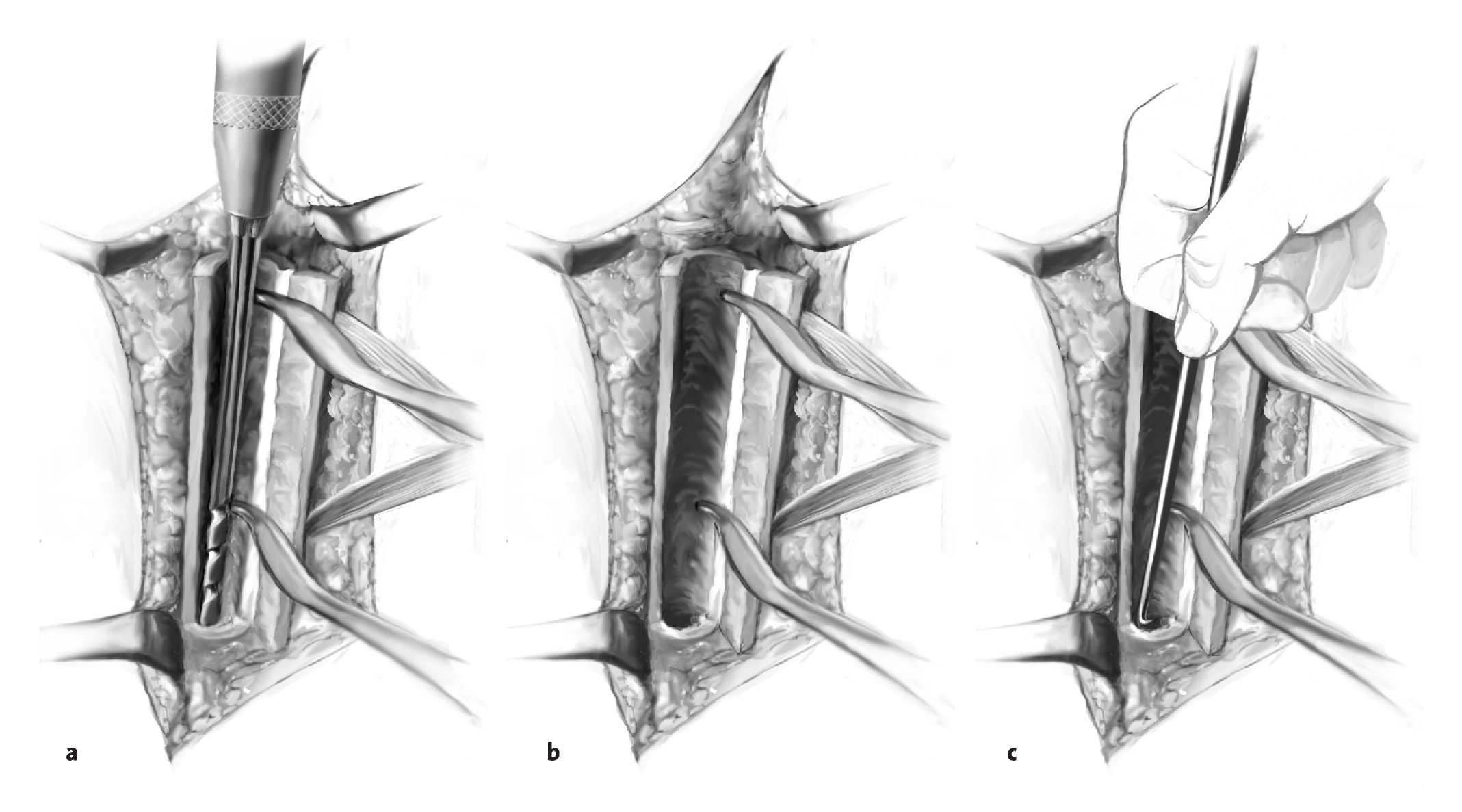
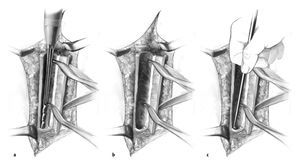
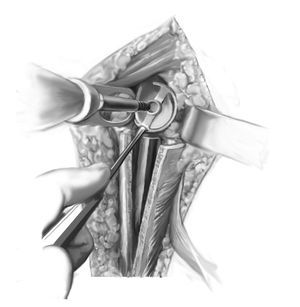
Figuras 3a a 3e. Exposición del húmero proximal y preparación para la ventana ósea. Se abre una ventana ósea pediculada al pectoral mayor con una sierra oscilante y se abre en sentido medial (a-c). Se libera la prótesis cuidadosamente utilizando escoplos pequeños y se saca (d, e). La planificación de la ventana ósea y del pectoral mayor tiene en cuenta los siguientes factores: preservación de la inserción del músculo deltoides, la longitud mínima requerida de la ventana para extraer la prótesis y el tapón distal de cemento, y conservación de una longitud suficiente de anclaje distal humeral. Se moviliza medialmente la ventana humeral pediculada. Se va aflojando el cemento trozo a trozo y se va extrayendo hasta que se pueda sacar toda la prótesis. Deberá extraerse cualquier trozo de cemento que quede sobre el hueso, con ayuda de la fresa de alta frecuencia, especialmente si está adherido a fragmentos corticales muy finos. También se puede usar la fresa para avanzar distalmente en el tapón de cemento remanente. Se pasa una cinta deslizante por debajo de la inserción del pectoral mayor (flecha en los bordes proximal y distal, b), cerca del húmero proximal. Si hay cemento residual en la región diafisaria por debajo de la ventana ósea, se puede abrir la diáfisis con una broca o con un extractor de ultrasonidos y se puede ensanchar progresivamente de manera que se pueda extraer el cemento con un pequeño gancho.
Figuras 4a a 4c. Extracción del tapón residual de cemento. Si el tapón de cemento continúa distal a la punta de la prótesis, se debe ensanchar la zona mediante fresas de tamaño creciente y se extrae poco a poco con pequeños ganchos (a-c). Si el tapón de cemento se extiende muy lejos distalmente y se adhiere muy firmemente a la cortical ósea fina y osteoporótica, se pueden realizar dos procedimientos: 1. Extensión de la incisión cutánea distalmente, exposición del nervio radial y ampliación de la ventana ósea; 2. Fresado del tapón de cemento como mínimo hasta los 8 mm y colocación de componente vástago de 6 mm en el tapón de cemento remanente. Para crear un buen anclaje para el implante, se amplía cuidadosamente la diáfisis humeral utilizando fresas de diámetro creciente hasta que se haya alcanzado la cortical distalmente. Tras el fresado, se determina la longitud del implante. En una situación de revisión, suele ser necesario utilizar vástagos de 150-210 mm de longitud. En general, la continuidad de la metáfisis humeral está con frecuencia interrumpida, de manera que no es necesario disecar más como en las cirugías primarias. En estos casos, es especialmente importante recuperar la altura humeral para lograr una retroversión correcta de la prótesis. Se debe lograr un balance entre, por un lado, lograr un cierre con estabilidad suficiente (al menos 20º de retrovesión con respecto al eje longitudinal del antebrazo, que corresponde aproximadamente a unos 10º de retroversión anatómica), el choque con el reborde glenoideo antero (inferior y postero/superior en los extremos de las rotaciones) y por otro lado, las necesidades funcionales del paciente (más rotación interna a expensas de rotación externa cuando hay daño añadido de las articulaciones adyacentes, p. e., artritis reumatoide). En caso de duda, cuando hay riesgo de luxación debido a contracturas o defectos musculares, es preferible aumentar la retroversión; en los casos en que se da prioridad a la rotación interna, es mejor colocar la prótesis en posición neutra. Se debe reconstruir tanto como sea posible el húmero proximal utilizando los restos de hueso y de partes blandas. Esto incluye movilizar los restos de las tuberosidades y realizar una fijación circunferencial segura con suturas o con cerclajes alámbricos (de 1,0-1,2 mm). Después de preparar el húmero, se coloca el vástago en la diáfisis sin anclarlo definitivamente, con el fin de proteger el húmero restante durante la siguiente disección. Se colocan los alambres de cerclaje, o como alternativa, suturas de Fiber-wire alrededor del húmero proximal preparados para la fijación posterior de la ventana humeral.
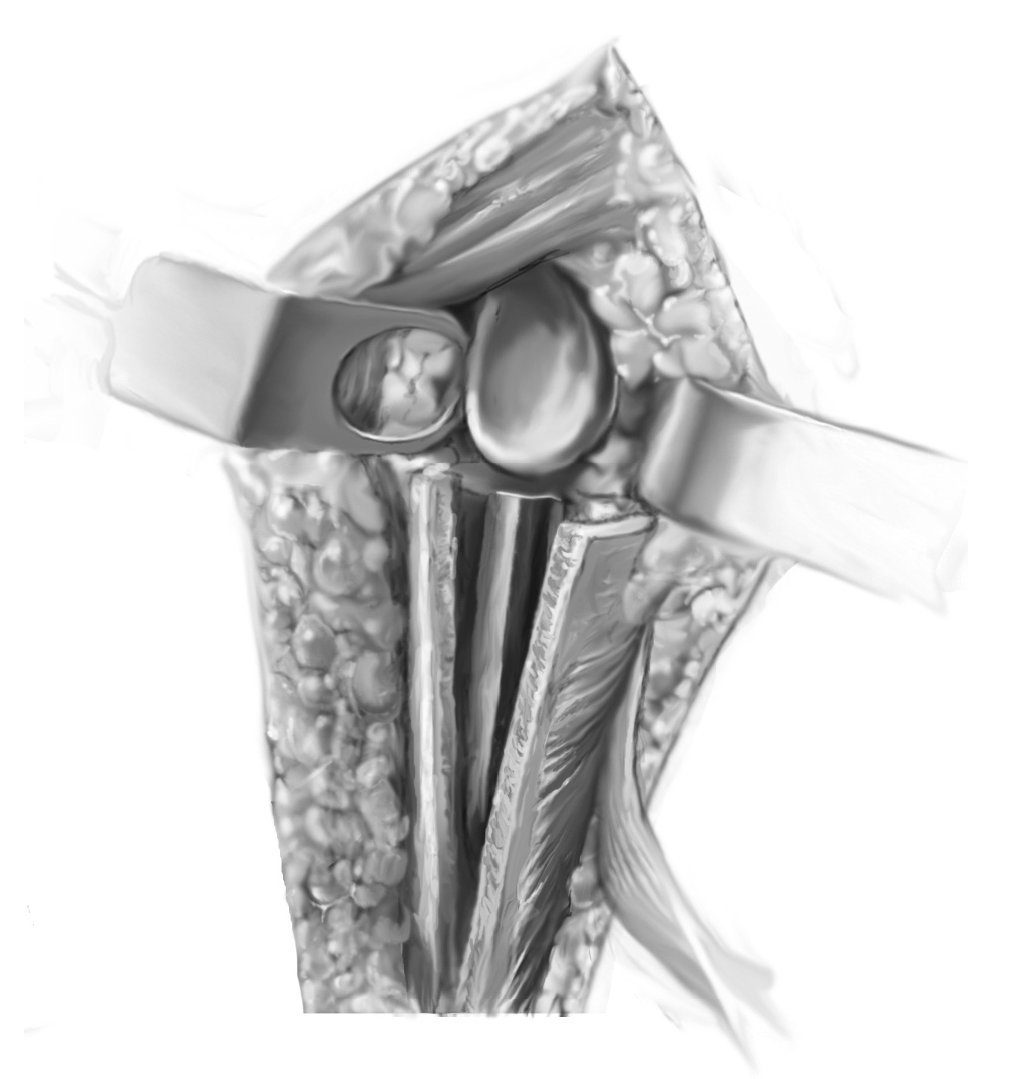
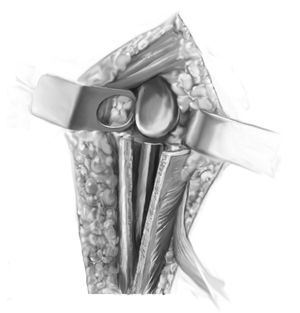
Figura 5. Preparación de la glena. Se coloca un separador humeral en el borde posterior de la glenoides. Previamente, se liberan los tejidos blandos y las adherencias con una raspa de hueso trabajando subperiósticamente a lo largo del cuello de la glenoides hasta que se pueda colocar un separador de Rowe en la parte anterior del cuello glenoideo. A continuación se realiza una liberación periglenoidea subperiósticamente paso a paso. Se coloca un separador de Hohmann o un separador bífido en posición inferior para proteger el nervio axilar. Si hay adherencias u osificaciones heterotópicas extensas, en estos raros casos está indicado realizar una revisión completa de la cápsula articular, así como identificar el nervio axilar y una neurolisis apropiada. Tras la liberación y resección del tejido cicatricial, se expone circunferencialmente la glenoides y se evalúan la cantidad de stock óseo, la calidad del mismo, y la versión glenoidea. Si la glenoides está intacta, se puede colocar una aguja guía exactamente en el centro de la glenoides con una ligera inclinación de 10º hacia inferior. La alineación de la placa base (metaglena) con el borde inferior de la glenoides previenen la muesca inferior (pinzamiento del componente humeral contra el reborde glenoideo inferior con la consiguiente osteolisis, causada por el desgaste y los restos del componente de polietileno [PE]).
Figura 6 Fresado con la fresa cónica sobre la aguja guía (p. e., Tornier Co.). La superficie de contacto se prepara para recibir la placa base (metaglena) con una fresa plana introducida a través de una aguja guía central. Para defectos óseos más grandes, se puede ampliar la glenoides colocando injerto óseo autólogo, lo que suele precisar extracción de hueso de la cresta ilíaca. La colocación de la metaglena con la aleta de reconstrucción (p. e. provisto por DePuy) sólo es útil en defectos marginales. Con frecuencia el stock óseo de la glenoides está tan severamente mermado debido a la osteoporosis y la falta de carga compresiva de la superficie articular como resultado de la migración superior que el procedimiento debe realizarse con el máximo cuidado. El orificio central preparado para el tetón central se rellena con harina de huesos; de manera optativa se puede recubrir la superficie posterior de la metaglena con chips de hueso esponjoso impactado ya que la fijación es no cementada. Se fija la metaglena con cuatro tornillos de esponjosa, los tornillos bloqueados superior e inferior se sitúan en la mejor posición con fijación bicortical a aproximadamente 30º al plano de la glenoides. La alineación de los tornillos anterior y posterior se ajusta para adaptarse al stock óseo. Los tornillos generalmente encuentran un buen anclaje anterior en la base de la coracoides (fresando desde el orificio anterior en dirección superior y posterior, dirigido ligeramente craneal hacia la posición horaria de las 12 empezando desde el agujero superior) y en el margen lateral de la escápula (desde el orificio inferior hacia la posición horaria de las 6) palpando la superficie anteroinferior de la escápula.
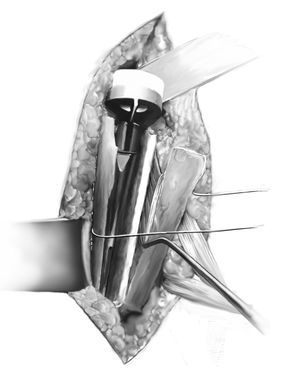
Figura 7. Fijación de la metaglena colocada. Tras colocar la metaglena, se introduce la glenosfera y se fija con el tornillo central de bloqueo. Se vuelve a exponer la diáfisis humeral y se introduce el implante de prueba del tamaño adecuado. Esto debe recuperar la longitud humeral apropiada. Una vez realizada la reducción de prueba, debería ser necesario aplicar una tracción moderada sobre el húmero para poder luxar. Se puede utilizar una referencia aproximada, con el brazo en abducción de 40º se aplica tracción en dirección axial: no debe observarse una distracción mayor a la anchura del dedo meñique. Básicamente, son ciertas las siguientes afirmaciones: cuanto mayor sea el defecto de partes blandas y la pérdida de hueso metafisario, más tensas deben quedar las partes blandas. Si se ha logrado una posición estable, se pueden marcar en la prótesis la retroversión adecuada y el nivel de anclaje con un rotulador, posiblemente la distancia entre la parte más alta del último vástago colocado y el hueso residual. Se coloca un tapón intramedular reabsorbible dentro del húmero distal a la altura predeterminada. Se ensambla el implante humeral para corresponder a la longitud del implante de prueba y se introduce en el húmero distal.
Figura 8 Nueva introducción del componente humeral después de cementar, y colocación del polietileno. Antes de la colocación definitiva, se prepara el cerclaje alámbrico dejándolo listo para estabilizar la ventana ósea. El recubrimiento del componente humeral con cemento óseo es útil para obtener una distribución uniforme del cemento en lo que habitualmente es una cavidad medular muy estrecha. Los implantes de revisión sin bloqueo de la modularidad (de DePuy) se pueden bloquear modelando el cemento en la parte proximal del componente humeral. Colocación del implante humeral con la altura y retroversión previstas. No se cierra la ventana ósea hasta que el cemento de la cavidad medular distal se ha endurecido. Después de valorar de nuevo la estabilidad articular con los componentes de prueba y después de colocar el polietileno definitivo de la altura requerida (3-12 mm, dependiendo de la casa comercial), se recoloca la ventana ósea utilizando los cerclajes previamente preparados y/o pinzas de reducción. La fijación de la ventana ósea se puede reforzar mediante un segundo recubrimiento de cemento en el vástago proximal.
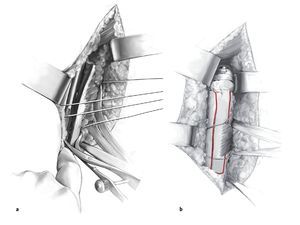
Figuras 9a y 9b. Reducción de la ventana ósea pediculada al pectoral mayor y fijación del húmero proximal mediante cerclaje. Como último test de tensión se coloca de nuevo el componente de prueba. Si queda demasiado laxo, se puede atornillar una extensión humeral (+ 9 mm). Se estabilizan los restos de manguito de los rotadores y de tuberosidades tal y como se había preparado previamente, suturas no reabsorbibles de alta resistencia a la tensión (p. e., Fiber-wire N.º 2 Arthrex Co., Karlsfeld/Múnich, Alemania, Orthocord, Mitek Co., Kirkel-Limbach, Alemania, o Ethibond N. º 3-5, Ethicon Co., Norderstedt, Alemania; a). Los cerclajes de sutura previamente preparados se doblan hacia la prótesis hasta alcanzar la reducción más anatómica posible y la fijación del húmero proximal (b). Si falta rotación externa, se puede considerar la posibilidad de realizar una transferencia muscular de latissimus dorsi o teres major según técnica de L'Episcopo9. Finalmente, se valoran de nuevo el arco de movilidad y la estabilidad del implante. Drenaje de aspiración y cierre de la herida con suturas de adaptación en el surco deltopectoral.
Manejo postoperatorio
Colocación e inmovilización con el brazo en una férula de abducción durante 6 semanas. Este tratamiento proporciona un alivio temporal para el arco coracoacromial debilitado que asegura la integración ósea de la metaglena. Un soporte alternativo es el vendaje tipo Gilchrist, si no se tolera el cojín de abducción.
La antibioticoterapia perioperatoria debe prolongarse como mínimo hasta obtener el resultado de los cultivos anaeróbicos, porque la experiencia ha demostrado que es muy frecuente demostrar contaminación en forma de una infección de bajo grado clínicamente silente por Staphilococcus epidermidis, propioni- o corynebacterias.
Cambio del vendaje y retirada de los drenajes aspirativos el día 3 postoperatorio.
Ejercicios activos asistidos con limitación de la flexión, abducción y rotación interna hasta la semana 6 post-operatoria. Intraoperatoriamente se comprueba la rotación externa posible; postoperatoria, se pueden permitir 20º menos. Ejercicios isométricos del deltoides.
A partir de la 6.ª semana postoperatoria y tras una evaluación radiológica, autorizamos los ejercicios activos con potenciación del deltoides pero con una carga máxima de 2 kg en la mano durante las primeras 12 semanas.
Evaluación radiológica el 3.er día postoperatorio, al alta, a las 6 semanas, a los 3, 6 y 12 meses postoperatorios, y cada 1-2 años.
Errores, riesgos, complicaciones
Artrolisis insuficiente: limitación persistente de la movilidad, irritación del plexo braquial, luxación de la epífisis humeral debido a cicatrices voluminosas, restos de tuberosidades, u osificaciones.
La disección demasiado extensa de las partes blandas aumenta la tasa de complicaciones, especialmente las lesiones vasculares, hematoma postoperatorio, y lesión del plexo braquial.
Lesiones preoperatorias del nervio axilar como consecuencia de compresión cicatricial: exposición intraoperatoria y neurolisis.
Pérdida de elementos contráctiles del músculo deltoides y atrofia asimétrica: aumento del pretensado mediante incremento de la longitud del implante.
Longitud excesiva: riesgo de parestesia del plexo braquial y nervios periféricos (nervio radial), afectación funcional, distrofia refleja.
Extravasación del cemento óseo del húmero fenestrado: cierre cuidadoso de la ventana ósea, inspección exhaustiva del lugar tras la implantación y la extracción del cemento óseo.
Pseudoartrosis de la ventana ósea: cierre cuidadoso del sarcófago de hueso, si es clínicamente relevante, revisión e injerto óseo tras el cerclaje.
Reabsorción progresiva de los fragmentos óseos como resultado de la devascularización debido al arrancamiento completo de las inserciones de partes blandas (p. e., músculo pectoral). Esto está asociado con el riesgo de aflojamiento prematuro y fracaso por fatiga del implante.
Inestabilidad/luxación de la prótesis: revisión y cambio del componente de polietileno, y si fuera necesario, un suplemento humeral adicional para aumentar longitud. Si hay volumen articular suficiente, revisión a un componente glenoideo mayor (diámetro de 42 mm). Colocación de un componente humeral proximal de talla 42 mm o glenoesfera produce mayor estabilidad en los casos en los que hay unas partes blandas laxas periarticulares. Sin embargo, este procedimiento es más probable que conlleve una tendencia a la luxación anterior debido a la formación de una cicatriz tirante o contractura de las partes blandas posteriores. De manera adicional, se puede aumentar el riesgo de "notching" o muesca inferior por el choque del componente humeral. Nota bene: los componentes articulares más grandes pueden tener un efecto opuesto, si hay un proceso cicatricial severo.
Fractura humeral intraoperatoria: antes de retirar el implante, es importante prestar especial atención a lograr el aflojamiento adecuado del implante y a la fenestración del húmero. En casos de fractura, osteosíntesis mediante cerclaje alámbrico, es posible extender el abordaje distalmente.
Disociación del componente protésico humeral (especialmente en sistemas sin mecanismo de seguridad que previene el desacoplamiento y en ausencia de hueso metafisario): capa de cemento adecuada en la zona de anclaje.
Acromion móvil: refijación primaria o refuerzo mediante banda de tensión y aporte de injerto corticoesponjoso de cresta ilíaca para prevenir una fractura por fatiga secundaria del acromion por inclinación, luxación y pérdida de pretensión del deltoides. En contraste con otras fracturas más mediales por fatiga de la espina de la escápula, una inclinación leve a moderada con frecuencia se tolera sin pérdida severa de la función.
Fragmentos óseos residuales/osificaciones subacromiales: puede haber una limitación de la movilidad. Si es clínicamente relevante, cirugía de revisión y extracción, o reducción del tamaño del fragmento.
Stock óseo glenoideo insuficiente: mejoría intraoperatoria de la reserva ósea mediante injerto óseo de cresta ilíaca fijado con tornillos, posiblemente con inserción de una metaglena de revisión. En casos de defectos glenoideos severos cuyo tamaño no se hubiera identificado preoperatoriamente: colocar primero sólo el componente humeral de la longitud adecuada como hemiartroplastia y en segundo tiempo convertirlo a invertida.
Colocación incorrecta de la metaglena: movilidad post-operatoria limitada y aumento de la muesca glenoidea inferior. Orientación intraoperatoria exacta de la guía central y colocación de la metaglena con una leve inclinación caudal y cobertura marginal del borde inferior de la glenoides por la metaglena.
Aflojamiento postoperatorio de la metaglena: revisión y, en caso necesario, conversión a hemiprótesis con injerto óseo simultáneo para reconstruir la glenoides. Tras la curación de la glenoides es posible realizar una conversión secundaria a una prótesis invertida.
Infección aguda de la herida: revisión precoz con desbridamiento y cambio del componente de polietileno así como retirada de la glenoesfera con el fin de irrigar el tercer espacio dentro del mismo.
Infección crónica: extracción de la prótesis y colocación de un espaciador biarticulado con antibióticos suplementarios según el antibiograma.
Resultados
En el período comprendido entre los años 2000 y 2005, llevamos a cabo 84 cirugías de revisión de hombro utilizando una prótesis Grammont para reemplazar una prótesis previa. La mayoría estaba compuesta por una serie de 34 pacientes (cinco hombres, 29 mujeres, edad media 68 años en el momento de la cirugía) con hemiartroplastias postraumáticas fracasadas. En estos casos la artroplastia de revisión se realizó a través de una ventana ósea con pedículo en el pectoral mayor. En 14 pacientes con manguito rotador previamente insuficiente se retiró la hemiartroplastia y se realizó revisión a prótesis de hombro invertida. En cinco casos, se revisaron prótesis bipolares a prótesis invertidas. En siete pacientes, se colocó una prótesis invertida después de retirar la hemiartroplastia infectada y colocar un espaciador articulado. El número de cirugías previas para las prótesis en fracturas fue de 2,3 de promedio (1-7).
Preoperatoriamente, 24 pacientes presentaban una pérdida significativa de la porción anterior del músculo deltoides y/o denervación parcial del deltoides confirmada en EMG como consecuencia de intervenciones previas. En 28 pacientes había migración anterosuperior estática de la cabeza humeral o subluxación. En todos estos pacientes se diagnosticó una pseudoparálisis como consecuencia de la insuficiencia del manguito de los rotadores. En ocho pacientes, las biopsias intraoperatorias eran positivas sin signos clínicos aparentes de infección.
Método
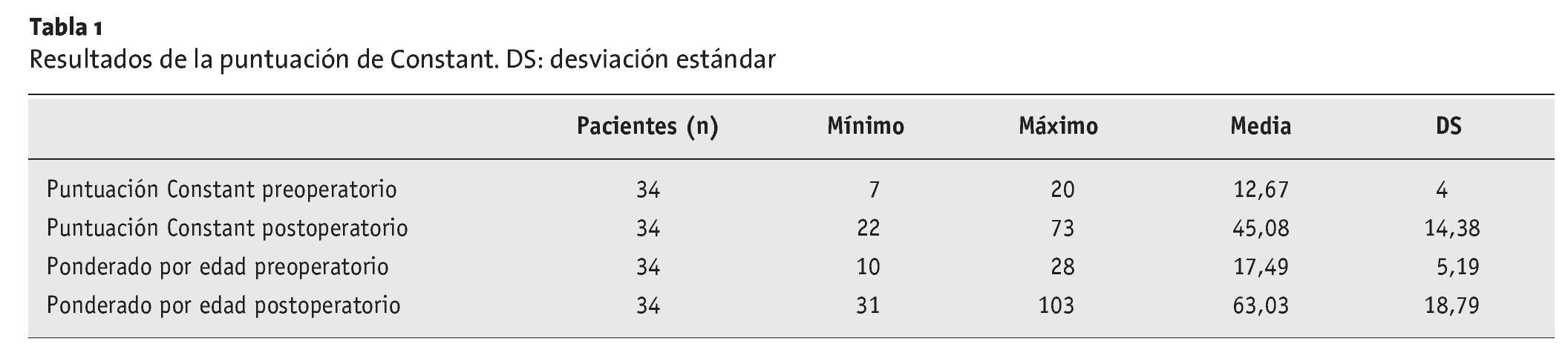
Los pacientes acudieron a evaluación de seguimiento prospectivamente a los 3 meses de la intervención, y a los 6, 12, y hasta los 59 meses. Se valoró la escala de Constant preoperatoriamente y en seguimiento final (tabla 1). Los pacientes fueron interrogados acerca de su evaluación subjetiva y el nivel de satisfacción; preoperatoriamente, el hombro afecto había sido examinado radiológicamente, en algunos casos, mediante tomografía computerizada. Se obtuvieron radiografías en dos proyecciones en el seguimiento, de los 34 pacientes, 25 estaban disponibles para evaluación clínica de seguimiento, nueve fueron entrevistados telefónicamente o por escrito y recibieron un cuestionario validado mediante correo para registrar la Escala de Constant2. El tiempo medio desde la cirugía hasta la evaluación final fue de 31,5 meses (12-59 meses).
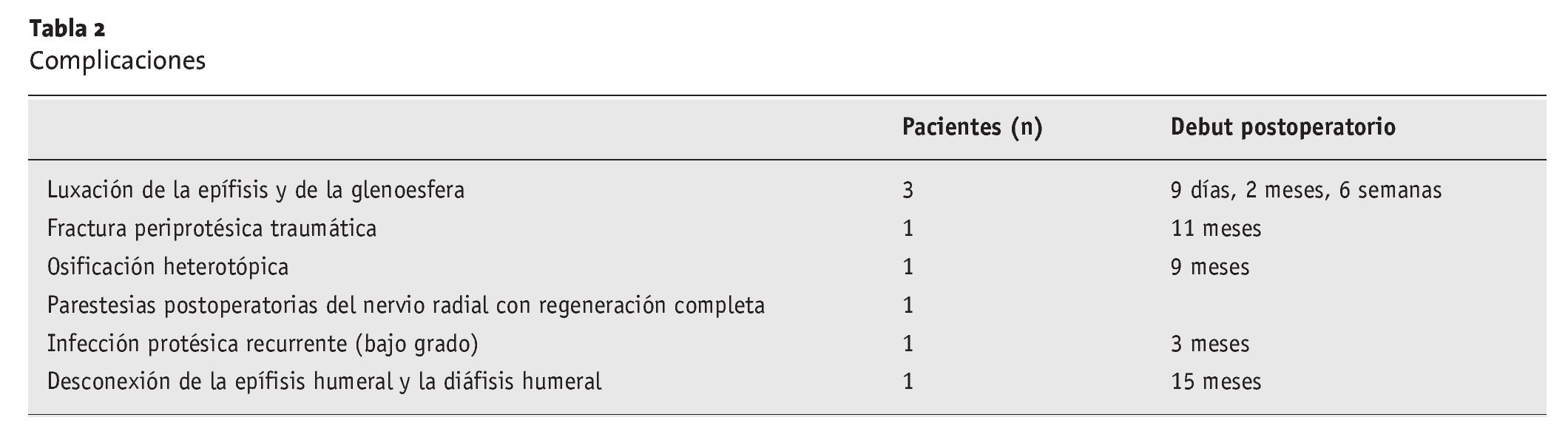
Se observaron complicaciones en ocho pacientes (tabla 2). Tres pacientes sufrieron luxación de la prótesis que requirió revisión. Las luxaciones fueron revisadas mediante cirugía abierta, se aumentó la altura del componente de polietileno y/o se añadió un alargador humeral. El caso con disociación precisó una cirugía de revisión con recambio del vástago con colocación de cemento óseo para prevenir la rotación y el desacoplamiento. En un paciente, se tuvo que practicar la exéresis de osificaciones heterotópicas y del alambre de cerclaje que protuía para aliviar un pinzamiento doloroso. En otro paciente, se produjo la recidiva de una infección de bajo grado (patógeno: Stafilococo aureus); 3 meses tras la intervención, fue necesaria una cirugía de revisión en dos tiempos con un espaciador articular añadiendo vancomicina y gentamicina.
En un paciente, el tapón de cemento preoperatorio se extendió a la región supracondílea del húmero distal y no se pudo retirar en la primera intervención. Este paciente se cayó a los 11 meses de la cirugía y sufrió una fractura periprotésica con una paresia transitoria del nervio radial. En la revisión, se colocó una placa preconformada y un injerto de peroné con un cerclaje. El cemento de la primera operación se retiró completamente y se sustituyó por injerto óseo esponjoso.
En el momento de la última revisión, el 88% de los pacientes estaban satisfechos con el resultado de la intervención. Había una disminución clara del dolor en todos los casos y una mejoría en el arco de movilidad en 30 casos; lo que es más importante, habían recuperado la capacidad de realizar las actividades de la vida diaria.
Todos los pacientes habrían consentido de nuevo la intervención.
Debido a la pérdida de los rotadores externos, doce de los 25 pacientes acusaban una limitación significativa de la rotación externa a 90º de abducción.
Preoperatoriamente, la rotación interna estaba limitada al sacro en todos los pacientes. La mejoría postoperatoria en dos pacientes alcanzó el nivel de T12 y en cinco pacientes alcanzaban el nivel de L3. La flexión se incrementó desde un valor preoperatorio de 48º a una media post-operatoria de 125º.
La puntuación en la escala de Constant postoperatoria alcanzó exactamente los 45 puntos y 63% ponderado por edad y sexo. De media, la elevación activa fue de 110º y la abducción de 95º. No se observaron casos de pseudoartrosis ni de fracturas diafisarias en ningún paciente como resultado de la fenestración del húmero.
El resultado postoperatorio mostraba una tendencia a decrecer en relación con el número de cirugías previas (media de 2,3), la falta y/o insuficiencia del manguito de los rotadores con atrofia grasa, y la resorción completa de las tuberosidades (17 pacientes).
En el momento del control final, el análisis radiológico no reveló ningún aflojamiento del implante. Se detectó "notching" inferior en 4 pacientes (11,8%; uno IIº, tres Iº según Sirveaux et al13).
Un paciente desarrolló osificaciones heterotópicas con el tiempo que le provocaron clínica de pinzamiento por lo que fueron resecadas en cirugía de revisión.
Tras una hemiartroplastia fallida por fractura, la revisión mediante prótesis invertida es una buena opción para los pacientes en una situación aparentemente desesperada con una pérdida de movilidad del hombro casi completa. A pesar de una situación inicial muy difícil y de una técnica quirúrgica muy compleja, se ha logrado una recuperación satisfactoria de la función del hombro en nuestra cohorte de pacientes sin haber tenido que recurrir a tratamientos alternativos menos prometedores, tales como la artrodesis de hombro o la artroplastia de resección. Esta técnica quirúrgica aún debe ser prerrogativa de aquellos cirujanos que tengan una buena formación quirúrgica y experiencia en prótesis total primaria de hombro.
Características de los casos (figs. 10 a 12)
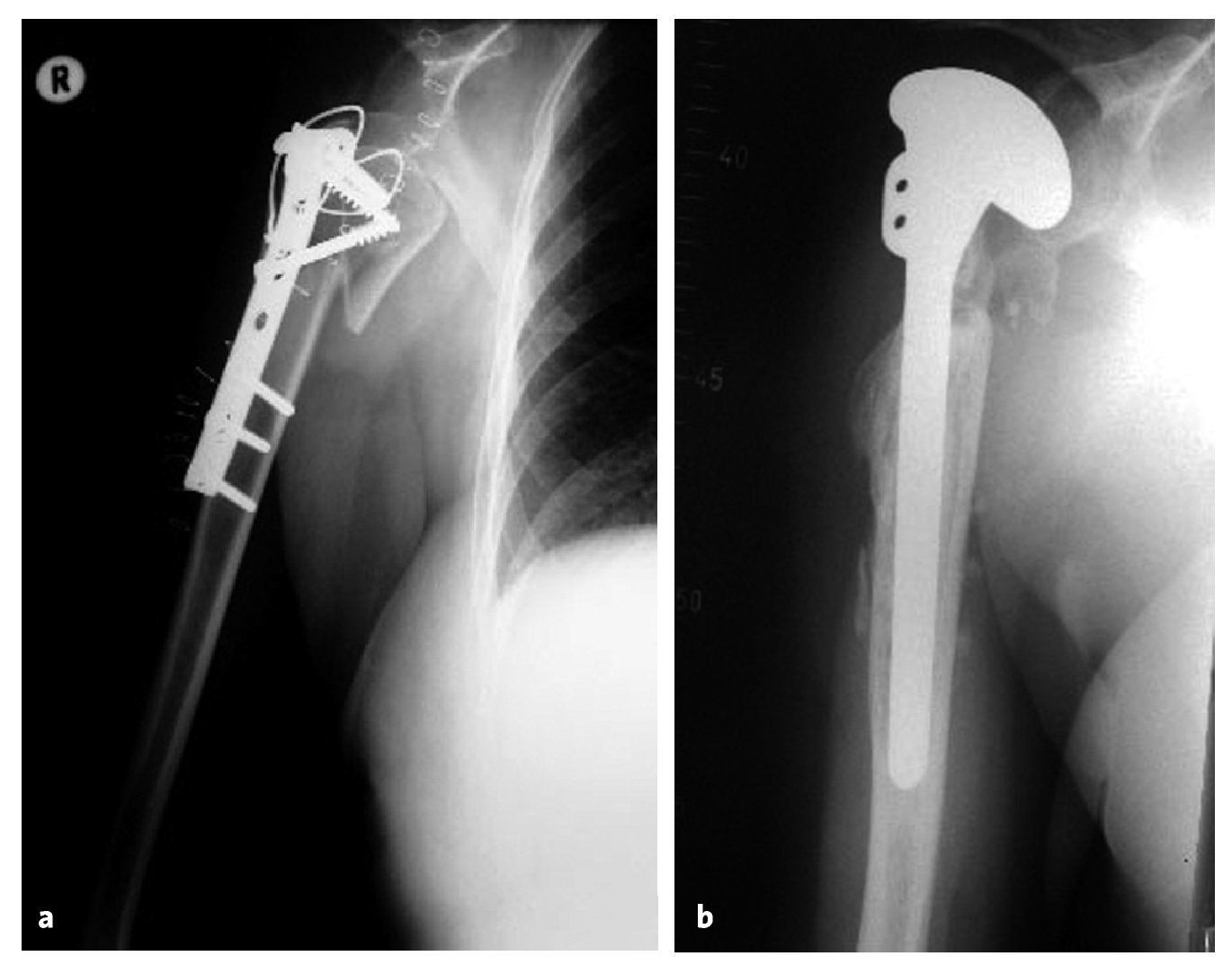
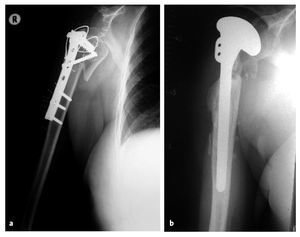
Figuras 10a y 10b. a) Mujer de 63 años con placa de osteosíntesis en el húmero proximal para fijar una fractura conminuta colocada en otro centro en agosto de 2002. b) Revisión a hemiartroplastia (Neer II) en septiembre de 2002 en otro hospital para resolver una luxación de la placa y malalineación persistente de los fragmentos de la fractura. El paciente se presentó en nuestras consultas externas en septiembre de 2003. La puntuación de la Escala de Constant era de 16 con dolor y limitación de la movilidad (flexión 70º, abducción 70º). La hemiartroplastia habría migrado anterosuperiormente debido a la insuficiencia del manguito de los rotadores. El paciente fue ingresado para cirugía de revisión protésica del hombro.
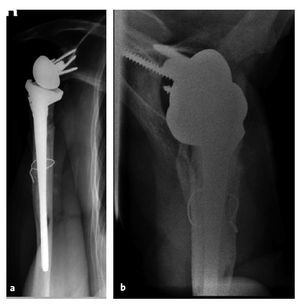
Figuras 11a y 11b. Radiografías del hombro derecho (a: AP, b: proyección axial) 25 meses tras la cirugía. Se colocó una prótesis invertida de vástago largo. Ventana ósea quirúrgica fijada con un cerclaje alámbrico.
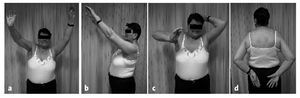
Figuras 12a a 12d. Movilidad a los 25 meses de la operación. Flexión activa 140º y abducción 100º. Existe un déficit residual evidente en la rotación externa activa con el brazo en abducción. La puntuación del Constant mejoró hasta 58,6 puntos (83,7% ponderado por edad). La paciente no tenía dolor y estaba muy satisfecha con el resultado quirúrgico.
Correspondencia
Prof. Dr. Frank Gohlke
Orthopädische Klinik Konig-Ludwig-Haus Lehrstuhl für Orthopädie
Brettreichstrasse 11
D-97074 Würzburg (Alemania)
Tel.: (+49/931) 803-0; fax: -1129
Correo electrónico: f-gohlke.klh@mail.uni-wuerzburg.de