Notas preliminares
En el recambio de un componente acetabular aflojado se disponen de varias opciones. Una posibilidad es la utilización de cótilos no cementados pressfit.
Por regla general en la bibliografía se recoge que los componentes acetabulares pressfit están más bien diseñados en defectos con reborde cotiloideo conservado (defectos "contained") o en pequeños defectos segmentarios. Por el contrario, se recoge como contraindicacion para cótilos pressfit los defectos acetabulares de > 50%1,8,9,13,17,18.
Sin embargo, Della Valle et al5 describen buenos resultados en grandes defectos acetabulares con el acetábulo Miller-Galante I. Hallaron una tasa de supervivencia a los 15 años del 81% en recambios por causa séptica y del 96% en recambios por aflojamiento aséptico, en los cuales 30 de 138 cótilos mostraban grandes defectos5. En estos casos se utilizó el cótilo pressfit de pared gruesa Miller-Galante I (Zimmer, Warsaw, IL, EE. UU.) "line to line", es decir, que se introduce sin pressfit y con abundantes tornillos de esponjosa (de tres a seis) para fijarlo5.
En el siguiente trabajo se describiría la técnica quirúrgica para la utilización de un cótilo de pared delgada con un pressfit aumentado de 4 mm en una indicación límite de recambio de componente acetabular en grandes defectos cotiloideos. La experiencia vivida con componentes acetabulares de pared gruesa sobre aparición de fracturas de acetábulo con aumento del pressfit a 4 mm12 no disminuyó al utilizar componentes de pared acetabular fina.
El cótilo utilizado en este trabajo es el AllofitSTM, que consiste en un componente acetabular pressfit de Protasul-Titan que se caracteriza por una pared de sólo 3 mm. Mediante un aumento a nivel ecuatorial de 2 mm y una disminución del diámetro a nivel polar de un mm, se obtiene el principio de pressfit según Morscher14,15 (fig. 1).
Figura 1. Cótilo AllofitSTM con exposición del aplanamiento polar y del pressfit ecuatorial de 2 mm.
La superficie del cótilo dispone de unos 1.200 punchones en disposición radial de 1 mm que aumentan la superficie de contacto hasta un 80%. En el borde del cótilo se hallan hasta seis anclajes para asegurar la estabilidad rotacional en el hueso. Estos anclajes salen perpendiculares y se reparten hacia la periferia (fig. 1), lo cual facilita un mejor asentamiento al colocar el implante. Con cada golpe el cótilo progresivamente se ancla más hasta el pressfit necesario. Nosotros utilizamos el implante AllofitSTM en cirugía de revisión con un pressfit de 4 mm, con lo cual elegimos el implante de una talla superior a la última fresa.
El cótilo AllofitSTM se presenta aquí como ejemplo. Otros cótilos alternativos de grosor pequeño de pared son el cótilo fitmore o el cótilo estandar Wagner (Zimmer GmbH, Winterthur, Suiza), el cótilo Trident AD (casa Stryker Howmedica Osteonics, Allendale, NJ, EE. UU.) y el cótilo Cerafit (Casa Ceraver Osteal, Roisssy, Francia).
Principios quirúrgicos y objetivos
Reimplantación de un cótilo no cementado pressfit incluso en defectos grandes para la reconstrucción de una extremidad sin dolor y capaz de carga.
Ventajas
Posibilidad de anclaje óseo incluso en grandes defectos óseos.
Técnica quirúrgica con disección del músculo glúteo medio (al contrario de la alternativa en otros cótilos).
Renuncia a trasplantes de hueso heterólogo.
Implante de revisión de coste razonable.
Desventajas
Técnica exigente.
Ocasionalmente compromiso con la estabilidad ósea primaria a costa de colocación del componente en una excesiva anteversión o verticalidad que puede comportar una luxación.
Indicaciones
Componente acetabular protésico aflojado.
Reconstrucción de un cótilo protésico en situaciones de Girdlstone o de presencia de espaciador a causa de una infección periprotésica.
Contraindicaciones
Grandes defectos segmentarios del acetábulo que no permitirían una fijación en tres superficies y con ello un pressfit suficiente.
Infección local persistente.
Riesgos quirúrgicos generales y especiales que puedan implicar riesgo vital.
Información al paciente
Riesgos quirúrgicos generales, como trombosis, infección, hemorragias y lesiones nerviosas.
Migración y/o aflojamiento del cótilo.
Fractura del acetábulo.
Luxación articular.
Carga parcial de la extremidad intervenida por regla general durante al menos tres meses.
Preparación preoperatoria
Mejora del estado general y de los posibles riesgos quirúrgicos, así como información al paciente.
Punción preoperatoria de la cadera y valoración microbiológica para descartar una infección como causa de aflojamiento.
Preparación de un recuperador de sangre (p. ej., Haemonetics GmbH Deutschland, Wolfrathauser strasse 84, 81379 Múnich, Alemania). Autotransfusión.
Profilaxis antibiótica peroperatoria; p. ej., administración de 250 mg de cefuroxima en una sola dosis: en caso de tiempos quirúrgicos superiores a 2 h se administran antibióticos durante 24 h (p. ej., 3 ´ 250 mg de cefuroxima).
Rasurado de la pierna desde la cresta iliaca hasta por debajo de la rodilla inmediatamente antes de la intervención11.
Radiología de la cadera con una distancia foco al chasis de 115 cm en dos planos.
Instrumental e implantes
Instrumental estándar para la implantación.
Intrumental de la caja de implantes, en este caso del cótilo pressfit AllofitSTM (Zimmer Germany GmbH, Merzhauser strasse 112, 79100 Friburgo, Alemania).
Preparación del recuperador de sangre.
Anestesia y posición del paciente
Anestesia general o raquianestesia.
Paciente en posición decúbito lateral con soportes pélvicos blandos anterior y posterior.
En ocasiones es necesario colocar al paciente en decúbito supino.
Entallado de la zona operatoria dejando libre la extremidad.
Técnica quirúrgica
Figuras 2 a 13
Figura 2. Abordaje longitudinal posterolateral de unos 15-20 cm en dirección de las fibras del glúteo mayor hasta el trocánter mayor y después unos centímetros distales en dirección del muslo.
Figura 3. Disección del tejido subcutáneo y de la fascia lata en la misma dirección. Disección roma del glúteo mayor en dirección de las fibras.
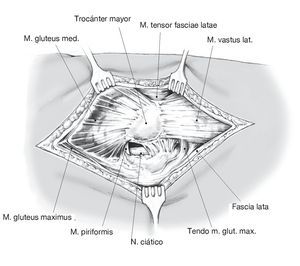
Figuras 4a y 4b. Sección cercana al hueso y ligadura de los rotadores externos a nivel de su inserción. Identificación y disección del nervio ciático (a). Resección de la así denominada neocápsula y del tejido cicatricial para exposición de la articulación (b). Luxación de la articulación, retirada de la antigua cabeza protésica. En caso de un aflojamiento más extenso, retirada también del vástago de la prótesis.
Figura 5. Exposición del acetábulo con un separador de Hohmann angulado a través del posicionamiento anterior del fémur. Liberación de todo el reborde del componente protésico acetabular. Retirada del espaciador de polietileno en componentes no cementados. Se trabaja con escoplo alrededor del componente acetabular con un escoplo curvo.
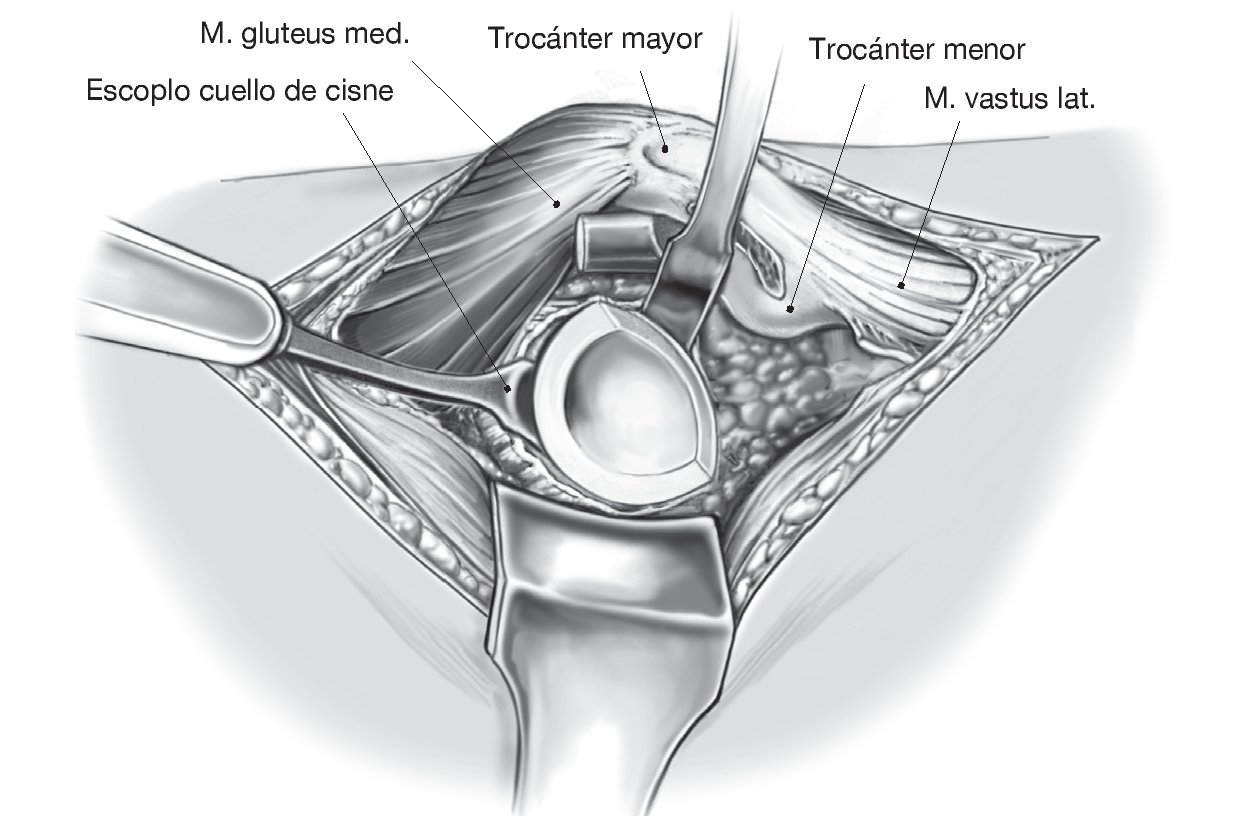
Figura 6. Se continúa el trabajo con escoplo alrededor del componente acetabular con escoplo curvo angulado, como el "escoplo cuello de cisne" (casa Waldemar Link, Nordestedt, Alemania), o con los escoplos angulados de la caja de escoplos acetabulares de la casa Smith & Nephew (Schenefeld, Alemania). Retirada del componente acetabular.
Figura 7. Limpieza del suelo acetabular de las membranas de aflojamiento con cucharas. Se remiten dichas membranas a Microbiología y a Anatomía Patológica para descartar una infección periprotésica.
Figura 8. Fresado del centro acetabular con una fresa significativamente más pequeña que el componente retirado para obtener un nuevo centro acetabular. Para garantizar un mejor contacto de los bordes óseos con la prótesis acetabular en caso de un defecto segmentario, puede ser necesaria una medialización del centro acetabular obteniendo o aumentando un defecto acetabular central. Retirada del material fresado. Zona de contacto óseo para una fijación de tres superficies.
Figura 9. Se continúa el fresado de tamaño progresivo central sin presión hasta obtener una superficie ósea suficiente del acetábulo. Consejo: a menudo es necesario aumentar un defecto segmentario central a través de un fresado cuidadoso en profundidad con tal de obtener al final un soporte periférico suficiente a nivel del borde acetabular. En caso de defectos segmentarios se ha de tener en cuenta que se obtenga en tres zonas el suficiente contacto óseo para conseguir el anclaje press-fit (por regla general, inferior a nivel de la incisura acetabuli, anterior o anterosuperior, y posterior o posterosuperior). Para asegurar una suficiente superficie triplanar, en ocasiones es necesario debilitar el reborde preexistente para preservar el aspecto posterior.
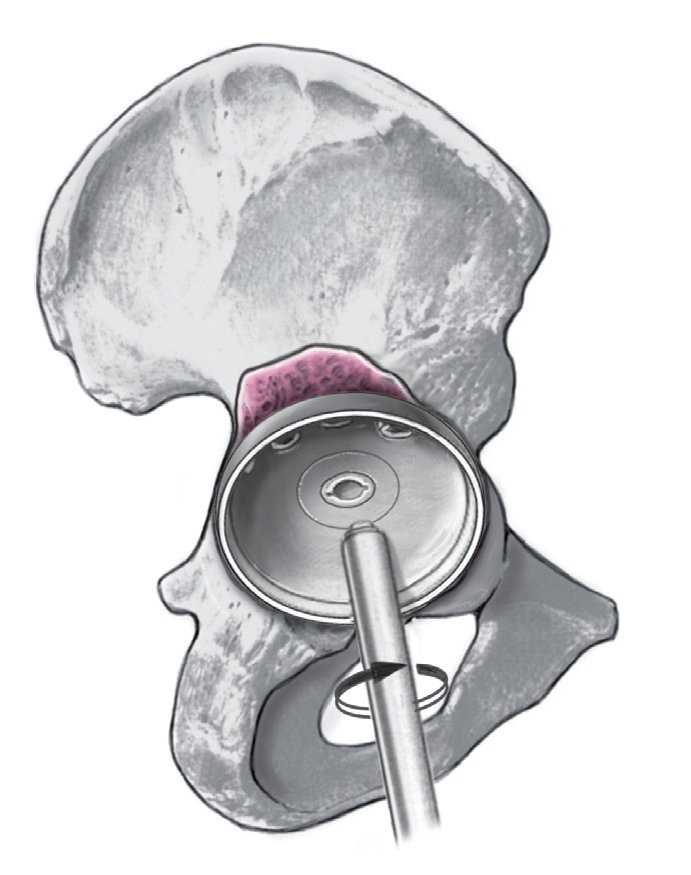
Figura 10. Colocación del hueso fresado en el suelo acetabular y ocasionalmente en el defecto acetabular preexistente (lo último a menudo no es necesario). Introducción de un componente acetabular de pared fina de una talla superior a la de la última fresa, con lo cual se obtiene en las superficies de contacto un pressfit de 4 mm.
Figura 11. Introducción del cierre central polar del componente AllofitSTM.
Figuras 12a a 12c. Fijación complementaria a través de la colocación de dos a tres tornillos de esponjosa en el hueso ilion (a). Colocación de los tornillos a ser posible en la dirección de las líneas de fuerza en la cadera (b, c).
Figura 13. Introducción del polietileno (a ser posible con los rebordes elevados); para obtener el mejor press-fit, es conveniente una ligera anterversión (5-10º) en la implantación. A continuación, cierre cuidadoso de la herida y colocación de un vendaje de compresión envolviendo toda la pierna y cadera.
Tratamiento postoperatorio
Documentación radiográfica.
Retirada del drenaje de redon a las 48 h, como máximo a las 72 h.
A partir del primer día postoperatorio, ejercicios de marcha con 10 kg. De carga parcial de la extremidad intervenida con bastones de antebrazo.
El progreso de la carga se decidirá en función de la calidad ósea, la edad del paciente, y la percepción intraoperatoria de la calidad del anclaje pressfit. Por regla general se realiza carga parcial de 10 kg durante seis semanas. La sensación de carga se ha de entrenar con una báscula de baño. A continuación, control radiológico de la cadera con visión profunda de la articulación coxal en dos proyecciones. Carga progresiva con 10 kg por semana.
Hasta la carga completa, profilaxis de la trombosis con heparina de bajo peso molecular.
Errores, riesgos y complicaciones
Hematoma de la herida a través del sangrado óseo: el aspirado de la zona de la herida con ayuda de un recuperador durante al menos 6 h disminuye el riesgo de un hematoma. Los drenajes de redon deben entonces retirarse al tercer día. El drenaje linfático postoperatorio favorece la reabsorción del hematoma.
Alteraciones de cicatrización de la herida: revisión precoz. En caso de sospecha clínica de una infección, además del desbridamiento, el cambio de polietileno y de cabeza, la toma de al menos cinco muestras histológicas para valoración microbiológica, se debe realizar un lavado suficiente con solución antiséptica (por ejemplo, Octenisept® Schülke & Mayr GmbH, 22480, Norderstedt, Alemania) y una antibioterapia sistémica (por ejemplo, levofloxacino [Tavanic] y rifampicina).
La lesión del nervio ciático o del nervio femoral normalmente se da por la tracción de los separadores o por hiperpresión o por un aumento de la tensión de partes blandas en la elongación de la extremidad. Por regla general es reversible. En caso de avance de la lesión nerviosa es recomendable una revisión con neurolisis.
Fisura o fractura del acetábulo al introducir el cótilo pressfit: según el desplazamiento y la extensión de la inestabilidad osteosíntesis con placas de reconstrucción y tratamiento con implantes especiales (por ejemplo, jaula con garfios de Ganz o la malla de apoyo de Burch Schneider [Zimmer GmbH, Winterthur, Suiza]).
Fijación pressfit insuficiente del componente acetabular AllofitSTM debido a un escaso contacto óseo o a una mala calidad ósea: cambio de procedimiento hacia un implante especial (por ejemplo, la malla de apoyo de Burch Schneider).
Tendencia intraoperatoria a la luxación: utilización de una cabeza con offset además de un polietileno de ceja alta (por ejemplo, Bio-Fall, casa Merete, 12247, Berlín, Alemania) o una cabeza más grande con un polietileno más grande (por ejemplo, Durasul, Zimmer Germany GmbH). En caso de no controlar la inestabilidad, se cambia el procedimiento hacia un implante especial (por ejemplo, la malla de apoyo de Burch Schneider).
Resultados
El procedimiento arriba descrito se realizó entre noviembre del 2002 a febrero del 2005 en 52 pacientes con un cambio de cótilo a un cótilo AllofitSTM: se trata de 25 recambios de cótilo y de 37 recambios de toda la prótesis completa de 20 cótilos cementados y de 32 cótilos no cementados en 27 mujeres y 25 hombres a una edad de 70,4 ± 9,1 (53-89 años). En 33 pacientes se trataba del primer recambio de cótilo, en diez del segundo, en seis del tercero, y en tres del cuarto. Los diagnósticos primarios de base comprendían coxartrosis (n = 38), artritis reumatoide (n = 5), fracturas de cuello de fémur (n =4), necrosis de cabeza femoral idiopática (n = 4) y espondiloartritis seronegativa (n= 1). En 36 casos se trataba de un aflojamiento aséptico y en 16 casos se trata de un aflojamiento séptico. En caso de una infección periprotésica se plantea un recambio en dos tiempos: tras la retirada de la prótesis y la colocación de un espaciador de cemento, se realizaba a las seis semanas la reimplantación de una prótesis no cementada. De forma intraoperatoria y previo a la implantación del cótilo AllofitSTM se clasifica el defecto óseo según Paprosky18. Se hallaron ocho defectos tipo 2A, once del tipo 2B, 19 del tipo 2C, doce del tipo 3A y dos del tipo 3B.
Todos los pacientes se siguieron de forma prospectiva durante el primer año postoperatorio, todos a los 3 meses y a los 6 meses de manera clínica y radiográfica. En el análisis de las radiografías y siguiendo los criterios de Dominikus et al7, se tomaron dos proyecciones digitalizadas de pelvis anteroposterior con las referencias claramente identificables (a las dos semanas postoperatorias y en la última exploración). Aquí se obtuvo una exploración en la radiografía en busca de radiolucencias en las zonas I, II y III según DeLee y Charnley4. Siguiendo las recomendaciones de Cordero-Ampuero et al3, se valoraron las radiolucencias > 2 mm como signos de aflojamiento. Los posibles cambios a nivel acetabular se analizaron según el método de Nunn et al16 (figs. 14a a 14c), con lo cual las mediciones que pueden variar con respecto a la distancia del paciente al chasis y variaciones de la anatomía de la pelvis se corrigieron según las recomendaciones de Nunn et al16. Las alteraciones de ≥ 3 mm en dirección horizontal o vertical2,16 y/o las variaciones del ángulo de inclinación a partir de 5º3,16 se aceptaron como migración definitiva. El promedio de seguimiento fue de 35,8 ± 8,8 meses (26-53 meses).
Figuras 14a a 14c. Exposición del análisis de aflojamiento según Nunn et al16 a propósito de la evolución del caso de una paciente de 78 años con un recambio de prótesis de cadera derecha con un defecto acetabular del tipo Paprosky 2C con un defecto de la ceja posterior. t: figura de la lágrima; x: punto de corte entre la línea que une las dos lágrimas y la perpendicular del centro de la cabeza; z: centro de la cabeza. Las alteraciones del segmento zx explican una migración vertical; las alteraciones del segmento tx se refieren a una migración horizontal, y la variación del ángulo a implica una variación del ángulo de inclinación. a) Visión de la radiografía de pelvis anteroposterior preoperatoria con identificación del cótilo aflojado y del vástago cementado. b) Radiografía anteroposterior de pelvis a las cuatro semanas postoperatorias de un recambio colocando un cótilo AllofitSTM y con un vástago de revisión modular Revitan curvado (Zimmer GmbH, Winterthur, Suiza). c) Radiografía anteroposterior de pelvis a los 30 meses postoperatorios.
La escala de valoración de la cadera de Harris10 aumentó de 46,4 ± 15,5 puntos de forma continua a 87,3 ± 15,0 puntos a los 24 meses postoperatorios (tabla 1). Ninguno de los cótilos mostraron signos radiológicos de aflojamiento; sin embargo, dos cótilos presentaron criterios radiológicos de migración (desplazamiento horizontal o vertical de 3 mm o un cambio de ángulo de al menos 5º2,3,6,16). En un paciente de 75 años con artritis reumatoide y con un defecto óseo del tipo Paprosky 2C se dio a los seis meses postoperatorios un aplanamiento del ángulo de inclinación de 5º, y en un paciente de 56 años con una necrosis de cabeza femoral de base y un defecto de tipo 3A de Paprosky se presentó a los seis meses postoperatorios un aplanamiento del ángulo de inclinación de 6º en combinación con un desplazamiento vertical de unos 3 mm. Ambos pacientes no se quejaron de dolor. En un caso se dio una luxación (un mes de postoperatorio) que se pudo tratar de forma conservadora.
Para asegurar el éxito del procedimiento presentado parece ser más decisivo no tanto el tipo exacto de defecto, sino la posibilidad de obtener el suficiente pressfit en al menos tres superficies óseas para obtener una fijación en tres áreas óseas. Para ello será decisivo el grosor de las paredes óseas y con esto la calidad ósea de las áreas óseas preexistente.
Dado que se trata de resultados precoces, todo y los resultados prometedores, todavía es pronto para hacer juicios definitivos. Se trata sobre todo de esperar si los dos casos con migración significativa aunque asintomática terminan en un aflojamiento.
Correspondencia
Prof. Dr. Bernd Fink
Klinik für Endoprothetik, Allgemeine und Rheumorthopädie Orthopädische Klinik Markgröningen Kurt-Lindemann-Weg 10
71706 Markgröningen (Alemania)
Tel.: (+49/7145) 912-201; fax: -292
Correo electrónico: b.fink@okm.de