A pesar del aumento del número de casos atendidos por consumo de cocaína, la dependencia de opiáceos continúa siendo el trastorno adictivo más prevalente en los servicios específicos de atención a las drogodependencias en nuestra área. Los programas de tratamiento con metadona (PTM), cuya eficacia y efectividad están ampliamente documentadas1, continúan siendo la principal opción para este grupo de pacientes. No obstante, los resultados de estos programas pueden variar en función de distintos factores, uno de los cuales viene dado por la heterogeneidad del perfil de los pacientes al inicio del mismo2-6. La posibilidad de disponer de distintos sustitutivos opiáceos (metadona, buprenorfina o diacetilmorfina) permitiría asignar determinados subgrupos de pacientes a cada uno de estos programas. De esta forma, se aumentaría la efectividad relativa del tratamiento para cada tipología de pacientes y, como consecuencia de ello, la efectividad global del servicio asistencial7.
La buprenorfina es un fármaco agonista parcial de los receptores opioides μ indicado para el tratamiento de pacientes con dependencia de opiáceos, existiendo una sólida evidencia sobre su efectividad8-10. Actualmente se utiliza de forma habitual y normalizada en muchos países. No obstante, el preparado comercial de buprenorfinal (Subutex®) no está disponible para su empleo clínico en España. Por ello, hasta el momento, sólo hay experiencias clínicas en nuestro país en el contexto de estudios de investigación11,12.
La investigación clínica no ha aportado aún evidencias suficientes sobre el perfil de pacientes que mejor responde al tratamiento con buprenorfina frente a los que siguen tratamiento con metadona13. Los ensayos clínicos que han comparado la eficacia de estos dos fármacos indican que, en dosis equivalentes, ambos son igualmente eficaces en términos de retención en el programa y en reducción del consumo de heroína9,13. Sin embargo, la propiedad de la metadona como agonista completo de los receptores opioides μ hace que este fármaco continúe siendo la primera opción a considerar en el tratamiento de los pacientes con dependencia a opiáceos, sobre todo en sujetos con elevados consumos de heroína previos y un alto nivel de neuroadaptación.
A pesar de ello, tanto la experiencia clínica acumulada, como los datos aportados por estudios realizados con diseños de tipo observacional señalan algunas situaciones que aconsejan el tratamiento con buprenorfina14, como por ejemplo la aparición de efectos secundarios con metadona, metabolizadores rápidos, interacciones farmacológicas, desarrollo de anticuerpos anti-metadona, rechazo de dosis eficaces, prejuicios hacia el programa de metadona asociados al mal cumplimiento, percepción del programa de buprenorfina como menos estigmatizante, expectativas y curiosidad por un nuevo opiáceo, mayor facilidad de retirada del programa de metadona a través de la toma de buprenorfina.
Con relación a esta última indicación, se ha demostrado la utilidad de la buprenorfina en pacientes que desean abandonar el programa de mantenimiento con metadona15. El tratamiento con buprenorfina se inicia con una pauta de inducción que tiene como primer objetivo reducir la sintomatología de la abstinencia de opiáceos. La buprenorfina puede producir una amplia variedad de efectos farmacodinámicos (por ejemplo efecto «tipo agonista» o efecto «tipo antagonista») dependiendo de distintos factores, tales como el nivel de dependencia física subyacente (neuroadaptación), el tipo de opiáceo que el paciente viene consumiendo (en este caso la metadona), el tiempo transcurrido desde la última dosis de metadona y la primera dosis de buprenorfina, así como la primera dosis de prueba de buprenorfina16.
Se ha demostrado que la buprenorfina tiene la capacidad de reducir y suprimir significativamente la sintomatología de abstinencia de opiáceos, tanto frente a placebo como frente a agonistas 2 adrenérgicos como la clonidina17. Para que esto sea posible, las dosis de metadona previas han de ser bajas o moderadas (más exactamente, sus niveles plasmáticos). Por el contrario, si la dosis previa de metadona es alta o bien si ha transcurrido relativamente poco tiempo desde la última dosis de metadona hasta la toma de la primera dosis de buprenorfina, el paciente experimentaría un síndrome de abstinencia «inducido»18.
La mayoría de los estudios que describen esta fase de inducción se han realizado en centros ambulatorios o bien en régimen de hospitalización, bajo condiciones experimentales. Tradicionalmente, las comunidades terapéuticas (CT) han sido consideradas como programas libres de drogas y, aunque más recientemente se están incorporando los tratamientos con me-tadona19,20, aún son muy escasos los estudios que han evaluado la utilidad de buprenorfina21. Pensamos que resultaría interesante evaluar la utilidad de buprenorfina en el tratamiento de adictos a opiáceos en régimen de CT, ya que en nuestro ámbito asistencial de Andalucía las CT no son recursos finalistas, sino que constituyen un eslabón más dentro de una amplia red coordinada de servicios.
El objetivo de este trabajo es la descripción y la evaluación clínica del proceso de inducción a buprenorfina, en el contexto de una CT, en pacientes que venían tomando metadona. Este trabajo forma parte de otro estudio más amplio22.
Pacientes y métodosDiseño y procedimientos de muestreoSe trata de un estudio observacional (descriptivo), longitudinal prospectivo y abierto (diseño antes-des-pués). Se utilizó un procedimiento de muestreo consecutivo no probabilístico. Los sujetos que cumplían los criterios de selección y eran elegibles firmaron el consentimiento informado. El protocolo del estudio fue aprobado por el Comité Autonómico de Ensayos Clínicos de Andalucía y se ha realizado de acuerdo a la Declaración de Helsinki.
Marco asistencialEl estudio fue realizado en un total de cinco CT residenciales públicas dependientes del Plan Andaluz Sobre Drogas y otras Adicciones de la Junta de Andalucía. Estas CT forman parte de una red asistencial coordinada, de modo que los pacientes que acceden a ellas proceden de centros específicos de atención a las drogodependencias de carácter público y ambulatorio. Cuando el paciente es dado de alta en la CT puede continuar el tratamiento desde su centro ambulatorio de referencia, o bien es derivado a recursos de media estancia. En las CT de Andalucía pueden ingresar pacientes en tratamiento con metadona. El perfil general de estos sujetos suele ser el de un paciente que venía consumiendo heroína a pesar del tratamiento con metadona, tiene una o más adicciones concomitantes (sobre todo abuso de cocaína, alcohol y benzodiacepinas), tiene un grado variable de comorbilidad psiquiátrica y es de difícil manejo en régimen ambulatorio.
Dentro de las CT, estos pacientes pueden seguir dos rutas terapéuticas: a) estabilización clínica y mantenimiento con metadona durante todo el tiempo que dure el ingreso, continuando posteriormente el tratamiento con este opiáceo en régimen ambulatorio, b) estabilización clínica y reducción progresiva de las dosis de metadona hasta su retirada completa antes del alta terapéutica. Este segundo grupo es la población diana seleccionada para evaluar el proceso de transferencia de metadona a buprenorfina.
SujetosEl tratamiento con buprenorfina se ofreció a todos aquellos pacientes que ingresaban en la CT con una dosis menor o igual a 80 mg/día de metadona y en los que se valoró clínicamente la posibilidad de iniciar una retirada paulatina de este fármaco durante su ingreso. La dosis al ingreso era mantenida sin cambios durante un mínimo de una semana, durante la cual se evaluaban los criterios de selección. Todos los pacientes fueron sometidos a un proceso de evaluación médica, psicológica y social por los procedimientos habituales durante la fase de «admisión» en CT. En esta valoración se tuvieron en cuenta las opiniones y los deseos de los usuarios del programa de metadona.
Aquellos pacientes con dosis de metadona inferiores o iguales a 40 mg/día pudieron acceder directamente a la fase de inducción de buprenorfina tras la primera semana. Si las dosis de metadona estaban entre 40 y 80 mg/día, el paciente pasaba por una fase previa de reducción flexible e individualizada de las mismas hasta alcanzar los 40 mg/día como máximo.
Los criterios de inclusión fueron los siguientes: a) diagnóstico de «dependencia de opiáceos en terapéutica con agonistas» según criterios DSM-IV-TR actualmente en programa de tratamiento con metadona en su centro derivador de referencia, b) tomar una dosis máxima diaria de metadona de 40 mg/día durante una semana antes de la inducción a buprenorfina, c) paciente que vaya a iniciar o que actualmente se encuentre en «fase de retirada» del programa de tratamiento con metadona, valorado mediante juicio clínico (tabla 1), y d) firmar el consentimiento informado.
Tabla 1. Criterios propuestos para definir las fases del tratamiento con agonistas opiáceos
Los criterios de exclusión fueron: a) sujetos con cargos judiciales pendientes y con expectativas de iniciar el cumplimiento de la pena en los próximos 6 meses, b) mujeres embarazadas o en período de lactancia, y c) dosis de metadona superiores a 80 mg/día.
Procedimiento de inducciónPara la organización de las distintas fases del tratamiento farmacológico con buprenorfina (inducción, mantenimiento, retirada, registro de efectos adversos, interacciones, etc.), adoptamos los criterios propuestos por la Guía clínica para el tratamiento con buprenorfina de la dependencia de heroína del Departamento de Salud de Australia16. Se administró buprenorfina (Subutex®) en comprimidos sublinguales de 2 y 8 mg.
Los pacientes que accedieron a ser transferidos desde el programa con metadona al de buprenorfina recibieron una extensa información en dos momentos: a) antes de firmar el consentimiento informado, y b) días antes de la administración de la primera dosis de buprenorfina. Tal como constaba en el consentimiento informado, los pacientes podían consultar cualquier duda sobre la medicación y retirarse del tratamiento en cualquier momento.
El primer día de inducción a buprenorfina comienza 24 horas después de la toma del último comprimido de metadona. A partir de este momento se invitaba al paciente a esperar algún tiempo hasta que comenzaran a aparecer algunos síntomas de abstinencia. Este proceso fue supervisado por personal médico y enfermero, registrándose periódicamente estos síntomas mediante las escalas Subjective Opiate Withdrawal Scale (SOWS) y Objective Opiate Withdrawal Scale (OOWS) de Handelsman et al23. Los pacientes podían esperar realizando alguna de las actividades propias de la CT y tenían la posibilidad de recibir apoyo psicológico.
Los últimos registros en las escalas SOWS y OOWS, evaluados antes de la administración de la primera dosis de buprenorfina, fueron codificados para su análisis estadístico. Se volvió a realizar otro registro con estas escalas una hora después de la toma de buprenorfina para evaluar la respuesta a la misma. Si los pacientes presentaban síntomas de abstinencia a pesar del tratamiento con buprenorfina se les administraba medicación sintomática (AINE, clonidina o benzodiacepinas). Durante los cinco primeros días de inducción, se evaluaron los síntomas de abstinencia (antes/después) de la toma de la buprenorfina. La pauta de dosificación fue flexible e individualizada, con modificación de dosis en función de las necesidades de los pacientes.
Procedimiento de reducción y seguimientoLos pacientes acudían diariamente a la consulta médica de la CT para la toma de la dosis de buprenorfina. El programa de intervención psicosocial que acompaña al tratamiento farmacológico con buprenorfina siguió las mismas pautas del empleado en el programa de metadona durante la fase de retirada del mismo24.
Tras la fase de inducción, el paciente recibía una dosis individualizada que se mantenía durante un tiempo que oscilaba entre 1 y 4 meses. Cuando se consideraba oportuno, y de acuerdo con el paciente, se procedía a una pauta de reducción progresiva (reducciones no superiores a 2 mg/semana) hasta reducir a 0 mg dentro de un período de 16 semanas. Tras una evaluación basal, previa a la inducción a buprenorfina, se realizan entrevistas de seguimiento al mes y a los tres meses de iniciado el tratamiento. Los datos de seguimiento han sido publicados en otro trabajo22.
Medidas de resultadosLa OOWS23 -SAO objetivo- es una escala que evalúa la presencia y la severidad de los síntomas objetivos de la abstinencia de opiáceos mediante 13 signos físicos observables. Un clínico puntúa cada uno de los síntomas como ausentes (0) o presentes (1). La puntuación máxima, por lo tanto, es 13.
La SOWS23 -SAO subjetivo- es una lista de síntomas de 16 ítems que mide la presencia de síntomas subjetivos de la abstinencia a opiáceos. Cada paciente puntúa cada ítem dentro de una escala que va de 0 (nada en absoluto) a 4 (extremadamente). Las puntuaciones totales tienen un rango que va de 0 a 64.
El Test para la Evaluación de la Calidad de Vida en Adictos a Sustancias Psicoactivas (TECVASP)25 tiene como objetivo conocer cómo repercute la adicción a sustancias sobre el desarrollo de la vida diaria de las personas, evaluando los componentes de la salud física, psicológica y social. Se trata de un instrumento de calidad de vida específico para población drogodependiente y se fundamenta en el concepto biaxial de la adicción de Edwards et al26. Según este concepto, la adicción vendría definida por dos ejes; uno de ellos estaría constituido por la dependencia propiamente dicha y el otro por los «problemas» o las consecuencias médicas, psicológicas y sociales ocasionadas por aquella. La TECVASP es una escala autoadministrada compuesta por 22 ítems codificados mediante una escala tipo Lickert de 5 grados. Las puntuaciones bajas en esta escala se corresponden con una peor calidad de vida y las puntuaciones altas con una alta calidad de vida.
El Opiate Treatment Index (OTI)27 es una entrevista clínica semiestructurada, cuyo propósito es la evaluación de la gravedad de los problemas relacionados con el consumo de drogas. Consta de seis subescalas, cuyas puntuaciones totales proporcionan una medida de la gravedad de cada uno de estos problemas. Cada una de estas subescalas puede aplicarse de manera independiente. En este estudio se administró la escala de «estado general de salud», que comprende una valoración médica general, problemas relacionados con la inyección, valoración neurológica, cardiorespiratoria, genitourinaria, musculoesquelética y gastrointestinal. Las puntuaciones bajas en esta escala representan un buen estado de salud. Hemos utilizado la versión española del OTI, adaptada y validada en nuestro medio28.
El General Health Questionnaire (GHQ-28)29 es una escala de síntomas que realiza una aproximación al grado de ajuste o distrés psicológico. Los ítem de sus diferentes subescalas se refieren a síntomas subjetivos de manifestaciones somáticas asociadas a ansiedad y depresión, así como a dificultades de relación y de adecuación a los papeles sociales y familiares. Las puntuaciones más bajas en esta escala representan un mejor ajuste psicológico. Por otro lado, el GHQ-28 sigue un modelo de evaluación categorial que permitiría la detección (screening) de «probables casos psiquiátricos». Para ello, hemos empleado el punto de corte general (puntuación total igual o superior a 5).
La gravedad de la dependencia de opiáceos se ha medido mediante la Sección 12 de la entrevista clínica Schedules for Clinical Assessment in Neuropsychiatry (SCAN)30. El sistema CATEGO-5 es una aplicación informática que permite generar los diagnósticos clínicos según criterios ICD-10 a partir de las puntuaciones obtenidas en la entrevista. Asimismo, permite estimar una puntuación de gravedad para un determinado trastorno (en este caso, dependencia de sustancias) denominado índice de definición (ID). Este parámetro es el que empleamos como indicador de respuesta de la gravedad de la dependencia.
Finalmente, mediante un cuaderno de recogida de datos (CRD) se registraron variables sociodemográficas, variables sobre el consumo reciente e historia de consumo, tratamientos previos y determinación de parámetros bioquímicos y serológicos.
Análisis estadísticoLos datos descriptivos se presentan como medias ± desviación estándar (DE) o porcentajes. Las pruebas de contraste de hipótesis empleadas son la «t» de Student para la comparación de medias y ji cuadrado para la comparación de porcentajes. Para el análisis estadístico se utilizó el programa SPSS v.11.
ResultadosDescripción de la muestraUn total de 119 pacientes cumplieron los criterios de selección durante la fase de reclutamiento. De éstos, 46 pacientes (38,7%) fueron transferidos del tratamiento con metadona al de buprenorfina, mientras que los 73 restantes (61,3%) decidieron permanecer en tratamiento con metadona. A pesar de que este último grupo no participó en el estudio, se registró información basal sobre el mismo con propósitos comparativos.
El 93,5% de los pacientes que iniciaron tratamiento con buprenorfina eran varones, siendo la media de edad de 36,9 años (DE: 6,8). Como puede verse en la tabla 2, la mayoría de ellos no tiene estudios primarios, su nivel de incorporación laboral es muy bajo y casi la mitad de la muestra tiene o ha tenido incidencias legales. En la tabla 2 vemos también que el perfil sociodemográfico de ambos grupos es similar. Sólo se observan diferencias estadísticamente significativas en la variable «nivel de estudios».
Tabla 2. Información sociodemográfica
Entre los pacientes del grupo de buprenorfina la media de años transcurridos desde el inicio del consumo de opiáceos y cocaína supera los 15 años. Estos períodos de tiempo son superiores a los observados en los pacientes del grupo de metadona, si bien las diferencias no son estadísticamente significativas (tabla 3).
Tabla 3. Información relacionada con el consumo y su tratamiento
En el grupo que continúa con el tratamiento con metadona se observa un mayor consumo de cocaína en el mes previo al ingreso. Para el resto de sustancias, las diferencias observadas son escasas. El número medio de tratamientos previos es 1,3; siendo éste igual para los pacientes que iniciaron tratamiento con buprenorfina y para los pacientes que permanecieron con metadona. En cambio, el tiempo medio que han permanecido en el último PTM hasta el momento de la entrevista es casi el doble entre quienes se encuentran en tratamiento con buprenorfina. A pesar de esta diferencia, en términos estadísticos no se encuentra significatividad. El tiempo total de permanencia en PTM es superior entre quienes inician el tratamiento con buprenorfina, aunque la diferencia observada no es estadísticamente significativa. Como puede observarse en la tabla 3, la dosis media de metadona con la que ingresaron en la comunidad es discretamente superior en el grupo que decide permanecer en PTM.
La prevalencia de infección por el virus de la inmunodeficiencia humana (VIH) fue baja en el grupo de buprenorfina (6,5%), siendo casi tres veces superior en el grupo que permanece en tratamiento con meta-dona (17,3%), a pesar de lo cual no se encuentra significación estadística. La prevalencia de infección por el virus de la hepatitis B (VHB) y C (VHC) también fue algo mayor en el grupo de metadona, tal como puede observarse en la tabla 4. No se observan diferencias significativas entre ambos grupos en relación al tipo de fármacos que venían tomando.
Tabla 4. Información relacionada con enfermedades y su tratamiento
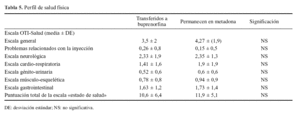
El examen del estado de salud física de los pacientes se analizó mediante la escala de salud del OTI. Como se observa en la tabla 5, en todas las subescalas de salud analizadas se observan puntuaciones semejantes en ambos grupos. En términos globales, si consideramos la puntuación total de la escala del estado de salud, la gravedad de los distintos problemas enumerados en el OTI es ligeramente inferior en el grupo tratado con buprenorfina.
Tabla 5. Perfil de salud física
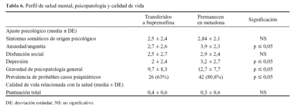
El perfil de salud mental difiere en ambos grupos. Como se observa en la tabla 6, el perfil de gravedad psicopatológica es más severo entre los pacientes que continúan en tratamiento con metadona. En este grupo, se observa una mayor puntuación general en la escala GHQ-28 y un mayor porcentaje de pacientes que son categorizados como «probables casos psiquiátricos». Se observan diferencias estadísticamente significativas entre ambos grupos en las escalas de «ansiedad/angustia» y «depresión». En relación con la calidad de vida, se aprecia una discreta mejor puntuación en el grupo de tratamiento con buprenorfina, si bien las diferencias no son estadísticamente significativas.
Tabla 6. Perfil de salud mental, psicopatología y calidad de vida
La dosis media (± DE) de buprenorfina empleada durante el período de tratamiento fue de 4,8 ± 1,02 mg/día.
Reducción de las dosis de metadonaComo hemos comentado, los pacientes que iniciaron tratamiento con buprenorfina en la CT (n = 46) procedían de un PTM en su centro ambulatorio de referencia. De éstos, 18 pacientes ingresaron con una dosis de metadona menor o igual a 40 mg/día, por lo que, tras una semana de estabilización con estas dosis, iniciaron el proceso de inducción directamente. Los 28 pacientes restantes, tras la primera semana, comienzan un proceso de reducción paulatina de sus dosis de metadona antes de pasar a la inducción con buprenorfina. En la figura 1 puede observarse la pauta promedio de reducción de la dosis de metadona (dosis media en cada período y duración media de cada uno de ellos). En términos generales se realizaron reducciones semanales de un porcentaje determinado de la dosis inicial de metadona. La mayoría de ellos, tras tres semanas de reducción, pudieron acceder al tratamiento con buprenorfina. Durante este período los pacientes no refirieron síntomas de abstinencia intolerables. En la semana previa al inicio de la inducción con buprenorfina se mantuvo constante la dosis de meta-dona (generalmente 30 o 40 mg/día).
Figura 1. Proceso de reducción de las dosis de metadona previamente a la inducción a buprenorfina.
Primer día de inducciónEl primer día de inducción a buprenorfina comienza a las 24 horas de la última toma de metadona. A partir de este momento, el paciente, previamente informado de las características de este proceso, aceptaba retrasar la primera toma de buprenorfina hasta experimentar algunos síntomas de abstinencia. Se trataba de un período de espera activo, en el que el sujeto podía participar en alguna de las actividades propias de la CT, al tiempo que recibía apoyo profesional. Como hemos comentado en el apartado anterior, con periodicidad se evaluaba su sintomatología de abstinencia. Comprobamos que este período podía variar mucho de unos pacientes a otros, a pesar de partir de dosis previas de metadona muy similares. Así, el tiempo medio (± DE) transcurrido desde que se cumplieron las 24 horas desde la última toma de metadona es de 35 ± 16,8 horas, variando entre pacientes que tomaron la primera dosis de buprenorfina una hora después de cumplirse las 24 horas establecidas, y otros pacientes que incluso retrasaron la primera dosis más de dos días. En la tabla 7 se muestra la distribución de las dosis iniciales de buprenorfina administradas según las dosis previas de metadona.
Tabla 7. Relación entre las dosis de buprenorfina administradas el primer día y la dosis de metadona previa. Número de pacientes que recibieron las distintas dosis de buprenorfina
Como puede observarse, la mayoría de los pacientes parten de dosis previas de metadona de 30-40 mg/día y comienzan con 4 mg de buprenorfina (bien con medio comprimido de Subutex® de 8 mg o con dos comprimidos de Subutex® de 2 mg).
Una hora después de la toma del primer comprimido de buprenorfina se evaluó la sintomatología de abstinencia a opiáceos (objetiva y subjetiva) mediante las escalas de Handelsman et al23, SOWS y OOWS, y se comparó con la última evaluación de la misma justo antes de la toma. Como puede verse en la tabla 8, se observa una reducción de casi dos tercios en las puntuaciones de estas escalas entre ambos momentos de la evaluación. Esta diferencia es estadísticamente significativa tanto en la de SAO objetivo —OOWS— (t = 4,679; g.l. = 44; p < 0,000) como en la de SAO subjetivo –SOWS— (t = 4,886; g.l. = 44; p < 0,000).
Tabla 8. Evolución de las puntuaciones de las escalas de SAO objetivo y subjetivo
A pesar de que los pacientes de la muestra, como promedio, experimentaron una clara disminución de los síntomas de abstinencia, el 33,3% de ellos requirió medicación adicional para mitigar algunos síntomas residuales. De estos casos que necesitaron medicación, un 68,4% recibió benzodiacepinas y el resto recibió AINE y/o clonidina.
Para conocer por qué estos pacientes requirieron más medicación, analizamos tres variables: el SAO antes y después de la toma, la dosis de metadona que tomaban antes de la inducción de buprenorfina, y, finalmente, el índice de masa corporal (IMC) (tabla 9). En primer lugar, observamos que la reducción de los síntomas de abstinencia tras la toma de buprenorfina era mayor en el grupo que no necesitó más medicación, aunque estas diferencias no son estadísticamente significativas. En relación con la segunda variable analizada, encontramos que en el grupo de pacientes que requirió medicación adicional las dosis de meta-dona previas eran significativamente mayores. Finalmente, no observamos diferencias estadísticamente significativas entre los valores del índice de masa corporal entre ambos grupos de pacientes.
Tabla 9. Necesidad de medicación adicional
Segundo a quinto día de inducciónEn la tabla 8 se muestra la evolución de las puntuaciones en las escalas de SAO objetivo y subjetivo durante los cinco primeros días de la inducción. Como puede observarse, a medida que se incrementan día a día las dosis medias de Subutex® (tabla 10) los síntomas de abstinencia disminuyen durante los tres primeros días y, a partir del cuarto día, el SAO prácticamente ha desaparecido (tabla 8). En todo momento, las puntuaciones medias en la escala de SAO subjetivo fueron superiores a las del SAO objetivo (una vez corregido el efecto de la diferente escala).
Tabla 10. Dosis medias de buprenorfina administradas durante los primeros días de la inducción
Efectividad del tratamiento (seguimiento al mes y a los tres meses)Evaluamos la efectividad del tratamiento con buprenorfina medida en términos de calidad de vida relacionada con la salud, así como en términos de reducción de la gravedad de la dependencia y de los problemas de salud física y psíquica. En este sentido, hemos observado una mejoría en todos estos indicado-res tanto al mes como a los tres meses de iniciado el tratamiento. Estos datos han sido publicados en otro trabajo y pueden consultarse22.
DiscusiónLos datos de este trabajo aportan más evidencias sobre la efectividad farmacológica, la seguridad y la comodidad del proceso de transferencia del tratamiento con metadona a buprenorfina. Hasta el momento actual sólo contábamos con la metadona como el agonista de referencia para el tratamiento de los pacientes con dependencia de opiáceos. Aunque este fármaco seguirá siendo la principal alternativa para la mayoría de estos sujetos, la buprenorfina se presenta como una opción útil para un determinado perfil de pacientes.
Aunque dicho perfil no está definitivamente establecido, las características farmacológicas de la buprenorfina como agonista parcial de los receptores opioides μ apoyan dos indicaciones fundamentales: a) como tratamiento de mantenimiento de primera elección para pacientes consumidores de heroína con una historia de abuso relativamente corta, con un nivel de consumo bajo-moderado y con un perfil moderado de problemas psicosociales relacionados, y b) como una opción a considerar para pacientes en tratamiento con metadona con una evolución relativamente buena y que deseen cambiar de opiáceo, bien por preferencias personales (para seguir en régimen de «mantenimiento») o bien como paso previo para dejar el programa de tratamiento con opiáceos y pasar a otro «libre de drogas».
Para interpretar adecuadamente los resultados de este estudio, han de tenerse en cuenta tres hechos fundamentales. En primer lugar, se trata básicamente de un trabajo de evaluación descriptiva de nuestra primera experiencia en el uso de este fármaco. Esto nos ha llevado probablemente a un «exceso de cautela» en algunos de los procedimientos empleados (dosis de buprenorfina, tiempo de espera hasta la primera dosis, etc.) que, con más experiencia, probablemente realizaríamos de otro modo. En segundo lugar, también se trataba de una «experiencia nueva» para los pacientes que accedieron a este tratamiento. En este sentido, el paciente tenía que llegar a comprender y, sobre todo, aceptar, que para acceder al tratamiento con buprenorfina desde el programa de metadona no debía tomar más de 40 mg/día de este fármaco, que tenía que esperar más de 24 horas desde la última dosis de metadona hasta la primera de buprenorfina y tolerar algunos síntomas de abstinencia antes de tomar la primera dosis de ésta. Finalmente, los resultados de este trabajo se han realizado en régimen de CT y no en un centro ambulatorio, lo que condiciona las dosis de buprenorfina empleadas (inferiores a las inducidas en régimen ambulatorio) y la continuidad de cuidados.
Por todo esto, nunca se insistirá lo suficiente en la importancia de informar adecuadamente al paciente antes de iniciar la inducción. Hemos de transmitir información sobre las características de la buprenorfina como agonista parcial y su diferencia con la metadona, así como señalar las peculiaridades del procedimiento de inducción. En nuestra experiencia, si el paciente candidato está bien seleccionado y suficientemente informado, y la inducción se lleva a cabo de forma adecuada, hemos superado la fase «clave» del tratamiento. A partir de este momento, el manejo clínico de la buprenorfina no presenta más dificultades que las del tratamiento con metadona.
En la muestra estudiada, los pacientes seleccionados que venían tomando una dosis de metadona inferior o igual a 40 mg/día pudieron acceder directamente al tratamiento con buprenorfina tras una semana de estabilización. Aquellos con dosis entre 80 y 40 mg/día de metadona pasaron por una fase previa de descenso paulatino de las mismas. Este proceso se realizó de manera individualizada y resultó cómoda para los pacientes, no presentando ninguna incidencia destacable. Lógicamente, aquellos pacientes con dosis más altas tardaron algo más en alcanzar el «umbral» de 40 mg/día.
Existe bastante consenso entre las distintas guías clínicas existentes16,30-32 en considerar esta dosis de metadona como la máxima aconsejable y, salvo excepciones, es la que habitualmente se emplea en la clínica (algunos defienden un máximo de 30 mg/día). El establecimiento de esta dosis de metadona se debe a las características farmacológicas de la buprenorfina como agonista parcial de los receptores opioides μ. Por ello, la transferencia desde un agonista completo de vida media larga como la metadona debe hacerse cuando los niveles plasmáticos de ésta sean bajos, correspondiéndose con un bajo nivel de ocupación de los receptores μ (generalmente con dosis iguales o inferiores a 40 mg/día).
En estas condiciones, la administración de buprenorfina produce un efecto «agonista» y el paciente percibe una disminución de los síntomas de abstinencia. Por el contrario, si las dosis de metadona previas son superiores, la administración de buprenorfina podría desencadenar un síndrome de abstinencia al que se ha denominado «SAO inducido»12. Se postula que, a nivel farmacodinámico, se produciría un «desplazamiento» de las moléculas de metadona por parte de las de buprenorfina. Estas últimas presentan una mayor afinidad por el receptor μ, pero una menor actividad intrínseca (agonismo parcial).
En este contexto, la dosis máxima de metadona aconsejable antes de la inducción a buprenorfina nos da una idea del perfil del sujeto susceptible de tratamiento con este fármaco. Así, un paciente con un nivel de neuroadaptación correspondiente a una dosis alta de metadona no resultará ser un buen candidato inicial. Algunos autores señalan una cierta «equivalencia» entre dosis de 16-24 mg/día de buprenorfina y 60-100 mg/día de metadona18. Estamos hablando aquí de dosis de buprenorfina de «mantenimiento» y no precisamente de las que empleamos los primeros días de inducción (más bajas). Con esto no queremos decir que un paciente que toma más de 100 mg/día de meta-dona no pueda acceder en ningún momento a un programa de buprenorfina. Esto será posible cuando el nivel de neuroadaptación disminuya progresivamente como consecuencia de una reducción paulatina de las dosis de metadona o, dicho de otra forma, de una retirada «natural», y cuando el paciente esté «maduro». No creemos conveniente «forzar» al sujeto a una reducción más o menos rápida de las dosis de metadona con objeto de iniciar en breve un tratamiento con buprenorfina.
Hay que tener en cuenta que no todos los pacientes van a aceptar esta reducción y no todos van a tolerar los efectos subjetivos «agonistas parciales» de la buprenorfina. Por ejemplo, algunos pacientes transferidos nos referían que cuando estaban en tratamiento con metadona «notaban el puntito» del efecto de la misma (es decir, un mínimo efecto se-dante/euforizante como reforzador positivo, además del reforzador negativo), pero cuando pasaron a tomar buprenorfina dejaron de notar este «punto». Estos pacientes comentaban «estar más despiertos», «tener la mente más despejada», «como si no tomara nada pero sin tener mono», haber mejorado «el contacto con las cosas», incluso haber aumentado la intensidad de los estímulos sensoriales (incluido el del tacto, presión y dolor). Por tanto, el efecto subjetivo «agonista parcial» de la buprenorfina vendría determinado por un moderado efecto reforzador positivo (sedante/euforizante) y un adecuado efecto reforzador negativo (disminución de los síntomas de abstinencia).
Evidentemente, estos efectos percibidos no son igualmente aceptados y tolerados por todos los sujetos en tratamiento. Nuestra impresión clínica ha sido que el pronóstico a medio plazo del tratamiento con buprenorfina vendría determinado, al menos en parte, por esta percepción subjetiva inicial. Así, aquellos pacientes que durante las dos primeras semanas del tratamiento perciben estos efectos de forma positiva (por ejemplo, la sensación de «estar más despejados pero sin mono») serán probablemente los que tengan más adherencia al mismo y, por tanto, los que definan el perfil idóneo para este fármaco. Por otro lado, aquellos pacientes que «añoren el puntito de la meta-dona», que perciban sensaciones del tipo «esto es muy flojo» o «esto es como no tomar nada, no me hace efecto», probablemente acabarían dejando el tratamiento con buprenorfina y volviendo al programa de metadona, es decir, los que definan el perfil para este otro fármaco. En ambos casos, existiría un correlato neurobiológico que traduciría un diferente nivel de neuroadaptación. En relación a esto último, insistimos en que estamos hablando de impresiones clínicas o de hipótesis sugeridas por la observación de nuestros pacientes, y que deberán ser contrastadas en ulteriores estudios.
Además de la relación existente entre la dosis previa de metadona y la primera de buprenorfina, otro de los factores que determinan la aparición o no de un SAO inducido es el tiempo transcurrido entre ambas tomas. En nuestro estudio, el período de tiempo de espera registrado entre las 24 horas tras la última dosis de meta-dona y la primera de buprenorfina es superior a los encontrados en la literatura16. Nosotros interpretamos este dato como fruto de nuestra inexperiencia en el uso de la buprenorfina. Como ya hemos comentado, optamos por evaluar el proceso de inducción desde el primer paciente, sin esperar a tener una experiencia previa en el manejo del fármaco (aunque sí partíamos de una formación específica por parte de clínicos expertos y contábamos con su asesoramiento). Nuestro temor fundamental era generar un SAO inducido debido a un tiempo de espera excesivamente corto. Al mismo tiempo pretendíamos asegurar que la «primera experiencia» del paciente con la buprenorfina fuese la de percibir una reducción de los síntomas de abstinencia y, así, aumentar la satisfacción con el fármaco y evitar su rechazo.
Tras la experiencia acumulada en el tratamiento de estos pacientes en CT, así como por la de una pequeña muestra tratada en régimen ambulatorio (datos no publicados), creemos que el tiempo entre ambas tomas puede reducirse sensiblemente. Coincidiendo con la experiencia de otros autores, pensamos que este momento llegaría cuando el paciente comience a experimentar los primeros síntomas de abstinencia asociados a la disminución de los niveles plasmáticos de metadona, lo que se ha denominado «SAO esperado»12.
También observamos que los pacientes inducidos en CT tenían más tolerabilidad a los síntomas de abstinencia que los que iniciaban el tratamiento en régimen ambulatorio (datos no publicados). Encontramos que este hecho tiene cierta lógica, ya que los pacientes en CT permanecen en un entorno asistencial, no tienen prisa por desplazarse a otros lugares y pueden esperar con la certeza de ser atendidos en cualquier momento durante el tiempo necesario.
Los datos del estudio muestran que la buprenorfina se ha mostrado muy eficaz en la reducción de la sintomatología de la abstinencia (disminución de más de dos tercios en las puntuaciones del SAO objetivo y subjetivo), de forma similar a los datos observados por otros autores15. Aún así, algunos pacientes necesitaron medicación adicional para reducir estos síntomas.
En los pacientes que siguen presentando síntomas de abstinencia tras la toma de buprenorfina no siempre es fácil diferenciar en qué medida estos síntomas son atribuibles al SAO inducido o bien al SAO esperado insuficientemente cubierto. Por esto, es importante en el primer día de inducción evaluar bien los síntomas de SAO antes de la toma de buprenorfina, y una o dos horas después de la misma. Si los síntomas de SAO han disminuido globalmente, pero aun así persisten de forma intolerable, podemos plantearnos administrar una segunda dosis de buprenorfina si la primera ha sido muy pequeña (por ejemplo, 2 mg). Por el contrario, si tras la primera dosis, los síntomas no han disminuido en absoluto o incluso han aumentado, estaríamos ante un SAO inducido, lo que contraindica una segunda dosis en el primer día.
La administración de dos dosis de buprenorfina durante el primer día es un procedimiento habitual por parte de muchos clínicos y, aunque aumenta la probabilidad de desencadenar un SAO, en manos expertas no constituye problema alguno; es una simple cuestión de considerar globalmente un conjunto de datos (dosis de metadona previa, primera dosis de buprenorfina, peso del paciente, tiempo de espera entre ambos opiáceos y monitorización de la abstinencia tras la primera dosis de buprenorfina).
En nuestro trabajo no hemos empleado en ningún paciente una segunda dosis de buprenorfina durante el primer día de inducción. Si tras la primera dosis, el paciente presentaba síntomas de abstinencia, optábamos por administrar medicación adicional hasta el día siguiente. Estas prescripciones se hicieron, por lo general, durante uno o dos días (en algún caso excepcional, durante tres días). Observamos que los pacientes que necesitaron medicación adicional puntuaban más alto en las escalas de SAO y su índice de masa corporal era algo superior que el de los pacientes que no necesitaron más medicación. Este dato también fue observado por el grupo de Baño et al12 y podría atribuirse, en parte, a que los niveles plasmáticos de metadona permanecerían más altos en los pacientes más obesos a igualdad de dosis, tras un mismo tiempo de espera desde la última dosis de aquella (debido a la existencia de un reservorio de metadona en «tercer espacio»).
Las dosis medias de buprenorfina fueron aumentando durante los cinco días de la inducción, ajustándose progresivamente según las necesidades. Los síntomas de abstinencia fueron disminuyendo durante la inducción a medida que aumentaban las dosis medias de buprenorfina. Los síntomas objetivos de la abstinencia disminuyeron más rápidamente que los subjetivos, de modo que a los 5 días de iniciar el tratamiento con bu-prenorfina-Subutex® ya no se observan síntomas de SAO medibles con las escalas utilizadas. Este comportamiento apoya la eficacia de este fármaco en el control de los síntomas de abstinencia y se sitúa en la línea de estudios similares15.
En términos generales, la muestra en la que hemos observado estos resultados tiene un perfil de severidad de la adicción medio-bajo, en relación al de los pacientes que deciden permanecer en PTM. Más concretamente, los pacientes transferidos a buprenorfina tienen al ingreso menor consumo de cocaína y menor severidad psicopatológica. Estas diferencias en los perfiles de severidad también han sido observadas en estudios que tratan de comparar la eficacia a largo plazo de los programas de buprenorfina con los de meta-dona, medida en términos de calidad de vida relacionada con la salud33,34.
Tal como exponemos en el apartado de pacientes y métodos, el tratamiento con buprenorfina se ofertó a todos los pacientes que ingresaban en la CT con una dosis igual o inferior a 80 mg/día. De los 119 pacientes que cumplían los criterios de selección, 46 aceptaron el tratamiento con buprenorfina y los 73 restantes lo rechazaron. Se trata, por tanto, de un proceso de autoselección. La casi totalidad de pacientes que rechazaron la buprenorfina argumentaron razones de temor e incertidumbre ante un fármaco desconocido para ellos. Esto es comprensible, ya que hay que tener en cuenta que el tratamiento con buprenorfina sublingual (Subutex®) aún no está comercializada en nuestro país, y que éste es un estudio de tipo experimental. Así, algunos pacientes referían temor a «probar» una sustancia nueva, mientras que los más veteranos tenían algunas experiencias negativas con el abuso de buprenorfina en dosis analgésicas (Buprex®). Como vemos, son los pacientes que tienen un perfil de severidad de la adicción más grave, los que más recelan de los beneficios que la buprenorfina podría reportarles.
Una de las limitaciones de nuestro trabajo viene dada por el limitado tamaño de la muestra, lo que redunda en una menor potencia estadística y en una menor representatividad de los resultados. Por otro lado y, como ya hemos indicado, ha de tenerse en cuenta que ésta ha sido nuestra primera experiencia en el manejo de este fármaco. Probablemente, la posibilidad de atender a un mayor número de pacientes nos permitirá un mejor ajuste de los procedimientos de inducción. Otro elemento a tener en cuenta es que hemos empleado buprenorfina sublingual (Subutex®). Muy posiblemente, el fármaco que vaya a ser comercializado no será éste, sino Suboxone®, es decir, una combinación de buprenorfina y naloxona (también sublingual). La ventaja añadida de este fármaco es la seguridad del mismo frente a un eventual abuso por vía endovenosa. En este caso, el efecto antagonista de la naloxona impediría el efecto de la buprenorfina. Debido a la no absorción sublingual de la naloxona, la administración de un comprimido sublingual de Suboxone® tiene el mismo efecto que un comprimido de la misma dosis de Subutex® , siendo el manejo de ambos fármacos superponible35.
Los resultados de este trabajo aconsejan extender los programas de tratamiento con buprenorfina a la población drogodependiente con el perfil adecuado. Lamentable y sorprendentemente, en España aún no disponemos de este fármaco en las mismas condiciones de equidad que la metadona, debido, en parte, a que aún no se ha decidido su financiación por parte del Servicio Nacional de Salud. Es nuestro deseo que esta situación no persista indefinidamente. Estamos de acuerdo en que exista más de un antidepresivo financiado y más de un antipsicótico financiado, pero ¿por qué sólo un opiáceo para el tratamiento de una población tan heterogénea como la de los adictos a heroína?
La buprenorfina no va a sustituir a los tratamientos con metadona. Más bien, va a ocupar el «espacio» existente entre los programas de metadona y los denominados «programas libres de drogas». En un estudio reciente que hemos realizado en la provincia de Cádiz sobre una muestra aleatoria de 300 pacientes en PTM36, el 42,8% del total toma dosis comprendidas entre 50 y 100 mg/día y el 37,7% del total dosis inferiores a 50 mg/día. De todos estos pacientes, algunos estarán en la fase de incremento (proceso de estabilización), otros en fase de mantenimiento (la mayoría) y, finalmente, otro grupo ha iniciado una fase más o menos lenta de retirada del programa. A aquellos pacientes que estén en fase de mantenimiento con dosis inferiores a 60 mg/día o bien a los pacientes en fase de retirada, podemos plantearles la opción de ser transferidos a un programa con buprenorfina. En nuestra muestra, este grupo de candidatos potenciales podría representar, aproximadamente, un 30% del total de pacientes en tratamiento con metadona. Habrá que pensar que algunos de ellos no aceptarán la propuesta de cambiar de opiáceo. Estas cifras se aproximan mucho al porcentaje de pacientes atendidos con buprenorfina en la mayoría de los países en que está disponible; aproximadamente un 20% del total de pacientes en tratamiento con sustitutivos opiáceos14. En Andalucía, con aproximadamente 18.000 pacientes en PTM, esta cifra supondría un total de 3.600 candidatos al tratamiento con buprenorfina. Como vemos, la metadona seguirá siendo la principal alternativa de tratamiento para esta población, pero la posibilidad de disponer de otra alternativa útil, como es la buprenorfina sublingual, para un determinado grupo de pacientes, nos abre la posibilidad de ampliar el arsenal terapéutico de nuestra especialidad, lo que redundaría en una mejoría de la calidad de la atención a nuestros usuarios.
AgradecimientosEste estudio ha sido íntegramente financiado con fondos públicos por la Dirección General para las Drogodependencias y otras Adicciones de la Junta de Andalucía. No ha sido realizado por ningún tipo de incentivación por parte de la Industria Farmacéutica, ni por intereses políticos por parte de la Administración Pública. Los autores de este trabajo declaran su deseo de que los tratamientos con buprenorfina puedan estar definitivamente disponibles en España al mismo nivel de equidad y accesibilidad que los tratamientos con metadona.
Queremos agradecer de forma muy especial el asesoramiento de la Dra. M.ª Dolores Baño Rodrigo, así como su estímulo intelectual, su integridad profesional y sus cualidades personales. Desde aquí nuestro apoyo incondicional en su nueva trayectoria profesional.
Los autores declaran que no existe conflicto de interés.
Correspondencia:
F. GONZÁLEZ-SAIZFundación Andaluza para la Atención a las Drogodependencias e Incorporación Social (FADAIS). Avda. Hytasa, edificio Toledo II, Plt. 3.ª Ofic. n.º 1 41006 Sevilla. España. Correo electrónico: pacogonzalez@comcadiz.com
Recibido: 17-10-2007 Aceptado para su publicación: 09-01-2008