El objetivo de este estudio es analizar el uso, la efectividad, la seguridad y los costes de la prevención de ictus en fibrilación auricular (FA) no valvular en pacientes que inician tratamiento con dabigatrán o antagonistas de la vitamina K (AVK).
EmplazamientoAtención Primaria (AP) del Instituto Catalán de la Salud (ICS), en Cataluña, durante el período 2011-2013.
ParticipantesTodos los pacientes atendidos en los centros de AP del ICS con diagnóstico de FA que inician dabigatrán o AVK.
IntervencionesNo aplica (estudio observacional).
Mediciones principalesNúmero de prescripciones y facturaciones de dabigatrán y AVK, incidencia de ictus y eventos tromboembólicos, incidencia de hemorragias mayores, incidencia de muertes durante el seguimiento, número de bajas laborales y medida de los costes asociados a estas variables.
ResultadosSe incluyó a 14.930 pacientes en el estudio; el 94,6% inició AVK y el 5,4%, dabigatrán. Estos últimos eran pacientes más jóvenes y con menos comorbilidades asociadas. No hubo diferencias estadísticamente significativas entre AVK y dabigatrán en el riesgo de ictus, hemorragias y mortalidad. Los costes asociados al manejo de la FA eran mayores para visitas de AP en el grupo de AVK y mayores para laboratorio, y farmacia en el grupo de dabigatrán, aunque los costes totales no fueron estadísticamente diferentes.
ConclusionesLa mayoría de los pacientes iniciaron AVK. No hubo diferencias entre AVK y dabigatrán en el riesgo de ictus, hemorragias y mortalidad.
To analyze the use, effectiveness, safety and costs of stroke prevention in non-valvular atrial fibrillation (AF) in patients initiating treatment with dabigatran or vitamin K antagonists (VKA).
SettingPrimary Care (PC) at the Catalan Health Institute (ICS) in Catalonia, during 2011-2013.
ParticipantsPatients attended in ICS PC centres with a registered diagnosis of AF who initiate dabigatran or VKA.
InterventionsNot applicable
Main measurementsNumber of prescriptions and reimbursements of dabigatran and VKA, incidence of stroke and haemorrhages, incidence of mortatlity, number of sickness leave, and costs associated to all the previous variables.
Results14,930 patients were included; 94.6% initiated VKA and 5.4%, dabigatran. Dabigatran patients were younger and with less comorbidity. There were no statistically significant differences between VKA and dabigatran in the risk of stroke, haemorrhages or death. The costs associated to AF management were higher for PC visits in the VKA group, and higher for laboratory and pharmacy in the dabigatran group, although overall costs were not statistically different.
ConclusionsMost patients initiated VKA. We found no differences between VKA and dabigatran in the risk of stroke, haemorrhages or mortality.
La fibrilación auricular (FA) es la arritmia crónica más frecuente, cuya prevalencia en la población general en Europa y Norteamérica es del 1,5-2% y aumenta progresivamente con la edad1–3. La FA representa una carga importante para el sistema sanitario debido a la población cada vez más envejecida2. En España se ha descrito una prevalencia superior al 17% en población de más de 80 años4,5.
La FA se asocia con varias enfermedades cardiovasculares, como hipertensión, diabetes, insuficiencia cardíaca o ictus. Aumenta al doble la tasa de mortalidad y la tasa de ictus en 5veces. De hecho, uno de cada 5ictus se atribuye a la FA6.
Los fármacos dirigidos a reducir el riesgo de ictus y eventos tromboembólicos en FA son los anticoagulantes orales (ACO). Los antagonistas de la vitamina K (AVK), acenocumarol y warfarina eran la única opción terapéutica disponible hasta la autorización de los ACO directos (ACOD) en la prevención tromboembólica en FA no valvular (dabigatrán en 2011, rivaroxabán en 2012, apixabán en 2013 y edoxabán en 2016 en España). Por ello, los ACOD se utilizan cada vez más en el manejo de la FA7.
En España existe un proceso de evaluación y autorización de nuevos medicamentos para determinar su reembolso en el Sistema Nacional de Salud. Esta evaluación se lleva a cabo a través del informe de posicionamiento terapéutico (IPT). El IPT que establece los criterios para la prescripción de ACOD para prevención de ictus en FA los posiciona como segunda línea de tratamiento para aquellos pacientes en que se inicia la anticoagulación8. Sin embargo, los ACOD se prescriben como primera opción terapéutica en la mayoría de países europeos y por este motivo el uso de ACOD en España es generalmente bajo7,9,10, aunque en aumento progresivo (datos internos aún no publicados).
El estudio ESC-FA analizaba el uso de fármacos disponibles en aquel momento para la prevención del ictus en FA en nuestro ámbito, AVK y antiagregantes plaquetarios11. También se analizaron la efectividad y la seguridad de estos fármacos en condiciones de práctica clínica habitual utilizando datos de la historia clínica electrónica de atención primaria (AP)12. Posteriormente, se estimaron los costes atribuidos al manejo de la FA en esta población13.
Finalmente, dentro del estudio ESC-FA se analizó el número de pacientes que iniciaban dabigatrán o AVK tras el diagnóstico de FA no valvular en nuestro territorio durante el período 2011-2013 y se describieron los factores asociados a la prescripción de estas 2alternativas terapéuticas14. Siguiendo la línea trazada por estos estudios anteriores, el objetivo del presente estudio es evaluar la efectividad, la seguridad y los costes en condiciones de práctica clínica habitual mediante datos procedentes de la base de datos Sistema de Información para el Desarrollo de la Investigación en Atención Primaria (SIDIAP)15.
Material y métodosDiseñoEstudio observacional de cohortes de base poblacional.
Fuente de datosLa fuente principal de datos es SIDIAP15, que contiene información clínica anonimizada procedente de todos los centros de AP del Instituto Catalán de la Salud (ICS), principal proveedor de servicios de salud en Cataluña, con una cobertura de 279 centros de AP, con una población de referencia de 5,8 millones de ciudadanos (aproximadamente el 80% de la población catalana o el 12% de la población española). La información de SIDIAP procede de estación clínica de atención primaria (ECAP™, Institut Català de la Salut [ICS], Barcelona, España) (historia clínica electrónica utilizada en los centros de AP en Cataluña) e incluye características sociodemográficas, problemas de salud registrados mediante códigos CIE-1016, parámetros clínicos y de laboratorio, hábitos tóxicos, prescripciones de AP y sus correspondientes datos de facturación en oficinas de farmacia. SIDIAP se puede cruzar con la base de datos de conjunto mínimo básico de datos de hospitalizaciones de agudos (CMBD-HA)17, que contiene diagnósticos al alta hospitalaria registrados mediante códigos CIE-918 de todos los hospitales de Cataluña.
Población de estudioLa población estudiada estaba formada por todos los adultos con un nuevo diagnóstico de FA no valvular registrado en ECAP que iniciaron tratamiento anticoagulante con AVK o dabigatrán en el período 2011-2013, que no tenían prescripciones previas de ningún ACO. Los criterios de exclusión fueron: FA valvular, inicio de ACO más de 6 meses antes del diagnóstico de FA, tener una única facturación de farmacia de ACO, tener facturación de otros ACO que no fueran AVK o dabigatrán, rivaroxabán o apixabán, ya que había pocos pacientes tratados con estos 2últimos fármacos. Los pacientes se siguieron desde el momento de entrada en la cohorte hasta la ocurrencia del primero de los siguientes eventos: final del período de estudio, pérdida de seguimiento o muerte.
Variables de estudioLas variables analizadas en el momento de entrada a la cohorte fueron: características sociodemográficas, riesgo de ictus y hemorragia mediante escalas CHA2D2VASc y HAS-BLED, comorbilidades de interés (antecedentes de infarto, hipertensión, diabetes, insuficiencia cardíaca, enfermedad renal crónica, arteriopatía periférica), ictus y hemorragias previas, datos de laboratorio y exposición a ACO, y comedicaciones (antiinflamatorios no esteroideos, inhibidores de la bomba de protones, antiagregantes, β-bloqueantes, inhibidores del enzima conversor de angiotensina, antagonistas del receptor de angiotensina ii, digoxina, verapamilo, diltiazem y antiarrítmicos). Las variables analizadas durante el seguimiento fueron: ictus, hemorragias, muertes por cualquier causa, exposición a los fármacos dabigatrán y AVK, y costes de las siguientes variables: visitas de AP (incluyendo visitas a médico de familia y enfermera, en el centro o en el domicilio), admisiones hospitalarias, eventos relacionados con la FA que requirieron ingreso hospitalario (ictus y hemorragias), derivaciones a especialistas hospitalarios, determinaciones de international normalized ratio (INR) en AP y tratamientos farmacológicos como costes directos, e incapacidad laboral temporal (ILT) (definida como el período de días de baja debido a enfermedad, disponible en SIDIAP codificada como CIE-10, con data de inicio y fin, y médico de familia responsable) como costes indirectos.
La variable principal de efectividad eran los ictus y eventos tromboembólicos. La variable principal de seguridad eran las hemorragias mayores, específicamente cerebrales y gastrointestinales. Todos los eventos de interés se identificaron tanto en la base de datos SIDIAP como en la de CMBD-HA.
Las muertes por cualquier causa se identificaron en SIDIAP, donde teníamos acceso a la fecha de muerte pero no a la causa.
Obtuvimos información sobre la exposición a fármacos del registro de facturación de farmacia, donde se identificaban los fármacos mediante códigos ATC19. La discontinuación del tratamiento se definió como > 2 meses consecutivos sin registro de facturación del ACO correspondiente.
Para calcular los costes de visitas de AP, derivaciones y determinaciones de INR se utilizaron los precios establecidos en el Boletín Oficial de la Generalitat de Catalunya (DOGC) para 201220. Para la estimación de costes del tratamiento farmacológico se usaron los precios de venta al público basados en datos de facturación de farmacia. Los costes de las incapacidades laborales (ILT) se calcularon mediante la aproximación del «capital humano»21 y se obtuvieron de la encuesta trimestral de coste laboral del 2012 para Cataluña del Instituto Nacional de Estadística22. Los costes de las admisiones hospitalarias se obtuvieron del sistema de clasificación de grupos relacionados por el diagnóstico (GRD) publicados en el DOGC, ponderados según complejidad del hospital. Los GRD incluidos fueron: 014, hemorragia intracraneal (HIC) e ictus con infarto; 015, oclusión precerebral sin infarto, y 174, 175, hemorragias gastrointestinales. Todos los costes se expresan en euros del 2012. El análisis de costes se realiza desde la perspectiva de la sociedad.
Análisis estadísticoSe utilizaron técnicas de estadística descriptiva para resumir las variables analizadas. Las variables categóricas se expresan como frecuencias (%) y las continuas como media, desviación estándar (DE) o mediana (rango intercuartílico). Los test utilizados para comparar variables entre grupos fueron el test de chi al cuadrado o el test exacto de Fisher para las categóricas y el test de t de Student o el de Mann-Whitney para las continuas.
Para el manejo de datos faltantes se utilizaron imputaciones múltiples con 10 conjuntos de datos imputados, incluyendo en el modelo de imputación todos los potenciales confusores. Las variables imputadas fueron índice de masa corporal (IMC), hábito tabáquico y hábito alcohólico.
Debido a la distribución no aleatoria de los tratamientos, se utilizó un modelo logístico basado en variables confusoras para calcular la puntuación de propensión o Propensity score (PS). Los grupos se aparearon 1:2 (dabigatrán:AVK). La adecuación del apareamiento se analizó estimando las diferencias estandarizadas entre usuarios de AVK y de dabigatrán para todas las variables. Las variables de apareamiento fueron: sexo, edad, IMC, hábito alcohólico y tabáquico, CHA2D2VASc, HASBLED, ictus previo, hemorragia cerebral y gastrointestinal previas, comorbilidades y comedicaciones.
Se definió el tiempo de seguimiento aquel que transcurría entre la entrada a la cohorte y el evento. Los pacientes se siguieron hasta la discontinuación del tratamiento ACO, ocurrencia de un evento, muerte, pérdida de seguimiento o fin del período de estudio.
Las hazard ratios (HR) de dabigatrán vs. AVK se calcularon para las variables de resultado mediante modelos de regresión proporcional de Cox. El modelo final de regresión de Cox se ajustó utilizando los conjuntos de datos de imputación múltiple mediante las reglas de Rubin para combinar las estimaciones de efectos y los errores estándar a fin de tener en cuenta la incertidumbre relacionada con los datos faltantes.
Se usaron modelos lineales generalizados para estudiar el efecto del tratamiento sobre el coste total anual y los factores asociados con el aumento de costes13,23. Los contrastes fueron bilaterales y se aceptó un nivel de significación estadística p ≤ 0,05. El análisis estadístico se llevó a cabo mediante el software R versión 3.3.2 (R Core Team, 2013. R: A language and environment for statistical computing. R Foundation for Statistical Computing, Viena, Austria. http://www.R-project.org/).
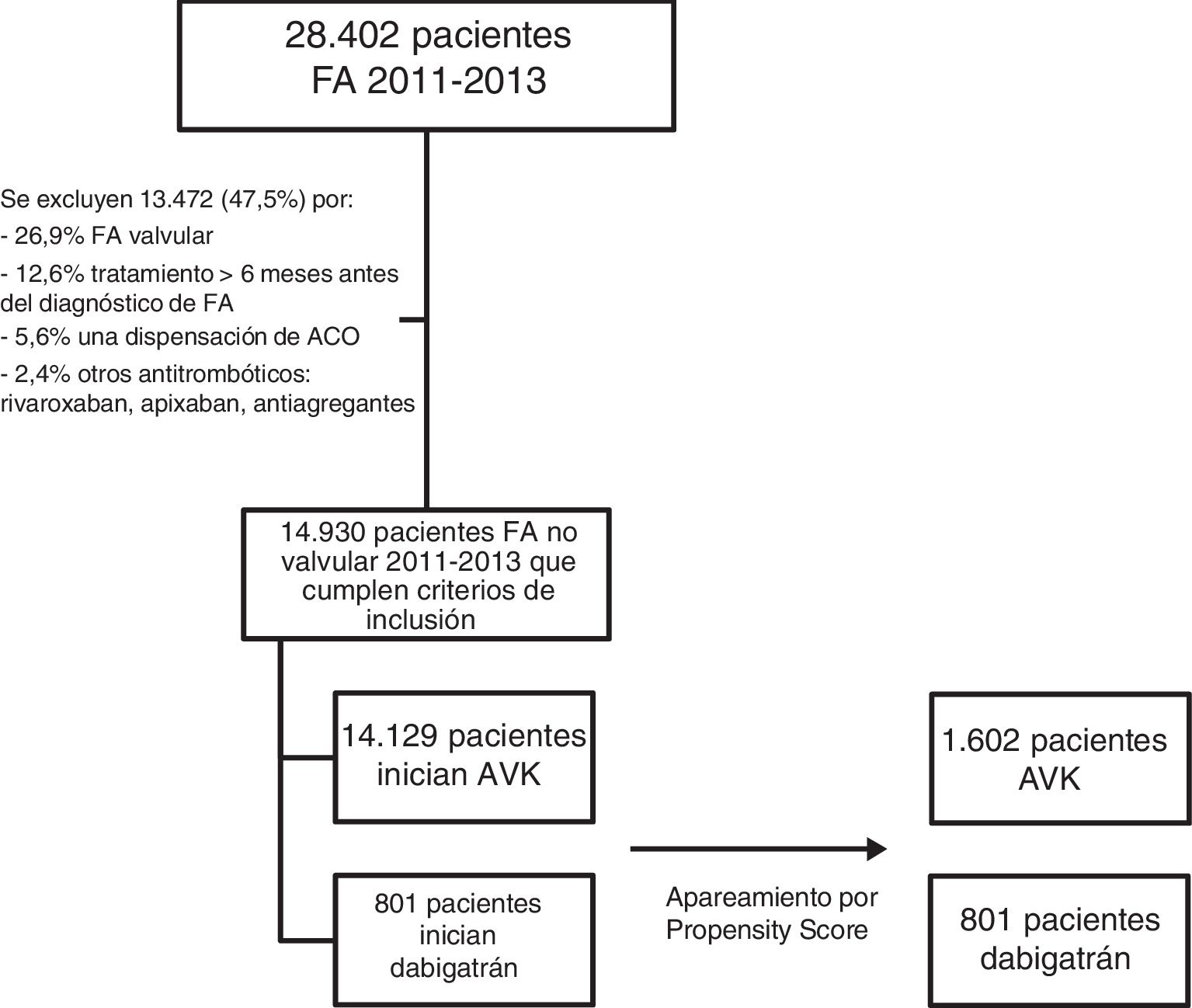
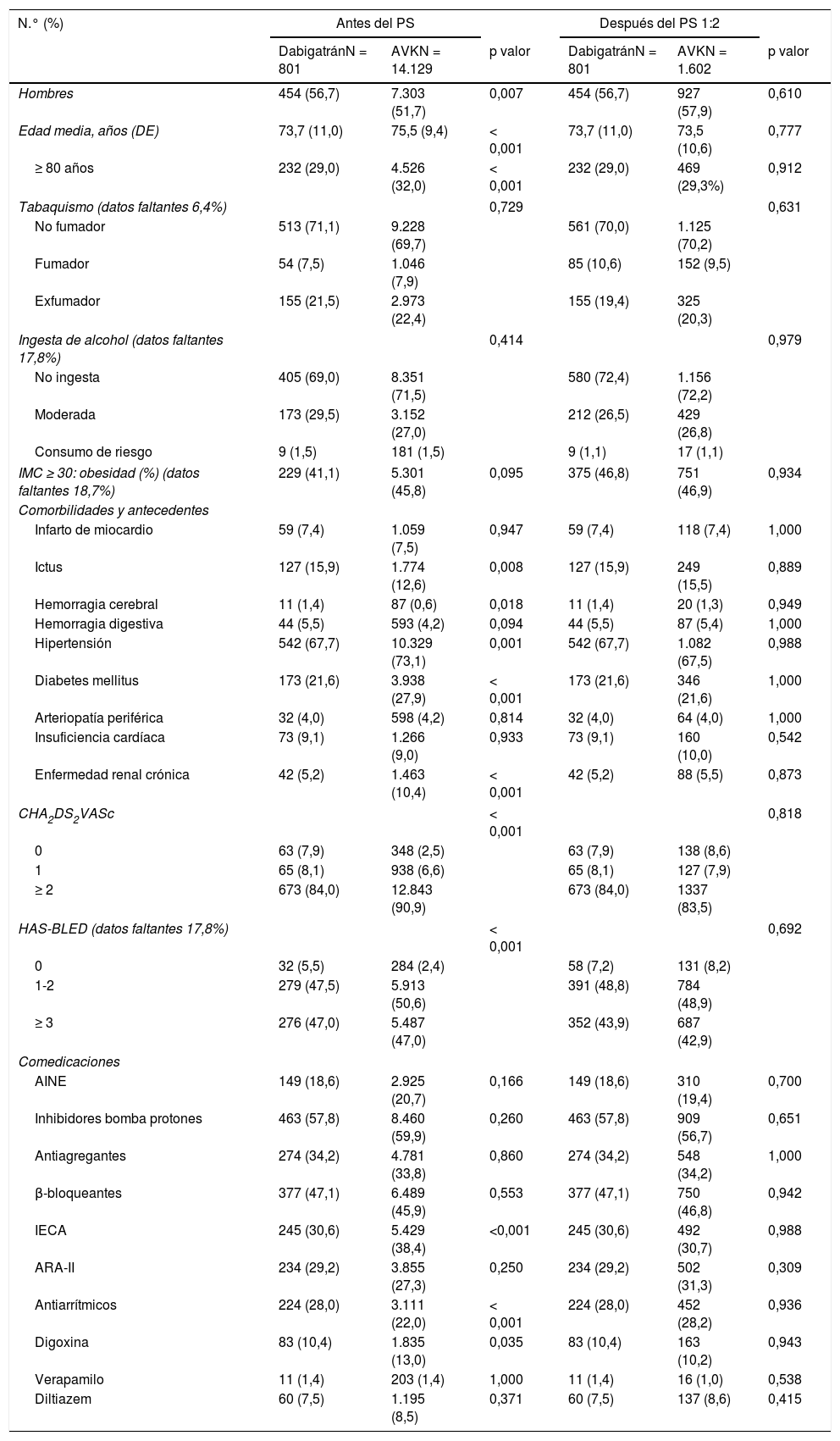
ResultadosUn total de 14.930 pacientes cumplieron criterios de inclusión en el estudio; 14.129 (94,6%) iniciaron AVK y 801 (5,4%) iniciaron dabigatrán (fig. 1). Los pacientes eran diferentes en el momento de inicio del estudio en algunas de sus características sociodemográficas y clínicas (tabla 1): aquellos tratados con dabigatrán eran más jóvenes que los que iniciaban AVK, había más hombres en el grupo de dabigatrán y menos pacientes con hipertensión y diabetes que en el grupo de AVK. Los que recibían dabigatrán tenían menor riesgo de ictus (CHA2D2VASc ≥ 2; 84% vs. 90,9%) y había más pacientes con antecedentes de ictus y hemorragias cerebrales que en el grupo de AVK. Después del apareamiento por PS (n = 2,403), las características sociodemográficas y clínicas iniciales quedaron balanceadas entre los 2grupos (tabla 1).
Características basales de los pacientes antes y después del apareamiento mediante PS
| N.° (%) | Antes del PS | Después del PS 1:2 | ||||
|---|---|---|---|---|---|---|
| DabigatránN = 801 | AVKN = 14.129 | p valor | DabigatránN = 801 | AVKN = 1.602 | p valor | |
| Hombres | 454 (56,7) | 7.303 (51,7) | 0,007 | 454 (56,7) | 927 (57,9) | 0,610 |
| Edad media, años (DE) | 73,7 (11,0) | 75,5 (9,4) | < 0,001 | 73,7 (11,0) | 73,5 (10,6) | 0,777 |
| ≥ 80 años | 232 (29,0) | 4.526 (32,0) | < 0,001 | 232 (29,0) | 469 (29,3%) | 0,912 |
| Tabaquismo (datos faltantes 6,4%) | 0,729 | 0,631 | ||||
| No fumador | 513 (71,1) | 9.228 (69,7) | 561 (70,0) | 1.125 (70,2) | ||
| Fumador | 54 (7,5) | 1.046 (7,9) | 85 (10,6) | 152 (9,5) | ||
| Exfumador | 155 (21,5) | 2.973 (22,4) | 155 (19,4) | 325 (20,3) | ||
| Ingesta de alcohol (datos faltantes 17,8%) | 0,414 | 0,979 | ||||
| No ingesta | 405 (69,0) | 8.351 (71,5) | 580 (72,4) | 1.156 (72,2) | ||
| Moderada | 173 (29,5) | 3.152 (27,0) | 212 (26,5) | 429 (26,8) | ||
| Consumo de riesgo | 9 (1,5) | 181 (1,5) | 9 (1,1) | 17 (1,1) | ||
| IMC ≥ 30: obesidad (%) (datos faltantes 18,7%) | 229 (41,1) | 5.301 (45,8) | 0,095 | 375 (46,8) | 751 (46,9) | 0,934 |
| Comorbilidades y antecedentes | ||||||
| Infarto de miocardio | 59 (7,4) | 1.059 (7,5) | 0,947 | 59 (7,4) | 118 (7,4) | 1,000 |
| Ictus | 127 (15,9) | 1.774 (12,6) | 0,008 | 127 (15,9) | 249 (15,5) | 0,889 |
| Hemorragia cerebral | 11 (1,4) | 87 (0,6) | 0,018 | 11 (1,4) | 20 (1,3) | 0,949 |
| Hemorragia digestiva | 44 (5,5) | 593 (4,2) | 0,094 | 44 (5,5) | 87 (5,4) | 1,000 |
| Hipertensión | 542 (67,7) | 10.329 (73,1) | 0,001 | 542 (67,7) | 1.082 (67,5) | 0,988 |
| Diabetes mellitus | 173 (21,6) | 3.938 (27,9) | < 0,001 | 173 (21,6) | 346 (21,6) | 1,000 |
| Arteriopatía periférica | 32 (4,0) | 598 (4,2) | 0,814 | 32 (4,0) | 64 (4,0) | 1,000 |
| Insuficiencia cardíaca | 73 (9,1) | 1.266 (9,0) | 0,933 | 73 (9,1) | 160 (10,0) | 0,542 |
| Enfermedad renal crónica | 42 (5,2) | 1.463 (10,4) | < 0,001 | 42 (5,2) | 88 (5,5) | 0,873 |
| CHA2DS2VASc | < 0,001 | 0,818 | ||||
| 0 | 63 (7,9) | 348 (2,5) | 63 (7,9) | 138 (8,6) | ||
| 1 | 65 (8,1) | 938 (6,6) | 65 (8,1) | 127 (7,9) | ||
| ≥ 2 | 673 (84,0) | 12.843 (90,9) | 673 (84,0) | 1337 (83,5) | ||
| HAS-BLED (datos faltantes 17,8%) | < 0,001 | 0,692 | ||||
| 0 | 32 (5,5) | 284 (2,4) | 58 (7,2) | 131 (8,2) | ||
| 1-2 | 279 (47,5) | 5.913 (50,6) | 391 (48,8) | 784 (48,9) | ||
| ≥ 3 | 276 (47,0) | 5.487 (47,0) | 352 (43,9) | 687 (42,9) | ||
| Comedicaciones | ||||||
| AINE | 149 (18,6) | 2.925 (20,7) | 0,166 | 149 (18,6) | 310 (19,4) | 0,700 |
| Inhibidores bomba protones | 463 (57,8) | 8.460 (59,9) | 0,260 | 463 (57,8) | 909 (56,7) | 0,651 |
| Antiagregantes | 274 (34,2) | 4.781 (33,8) | 0,860 | 274 (34,2) | 548 (34,2) | 1,000 |
| β-bloqueantes | 377 (47,1) | 6.489 (45,9) | 0,553 | 377 (47,1) | 750 (46,8) | 0,942 |
| IECA | 245 (30,6) | 5.429 (38,4) | <0,001 | 245 (30,6) | 492 (30,7) | 0,988 |
| ARA-II | 234 (29,2) | 3.855 (27,3) | 0,250 | 234 (29,2) | 502 (31,3) | 0,309 |
| Antiarrítmicos | 224 (28,0) | 3.111 (22,0) | < 0,001 | 224 (28,0) | 452 (28,2) | 0,936 |
| Digoxina | 83 (10,4) | 1.835 (13,0) | 0,035 | 83 (10,4) | 163 (10,2) | 0,943 |
| Verapamilo | 11 (1,4) | 203 (1,4) | 1,000 | 11 (1,4) | 16 (1,0) | 0,538 |
| Diltiazem | 60 (7,5) | 1.195 (8,5) | 0,371 | 60 (7,5) | 137 (8,6) | 0,415 |
AINE: antiinflamatorios no esteroideos; ARA-II: antagonistas del receptor de angiotensina II; AVK: antagonistas de vitamina K; DE: desviación estándar; IMC: índice de masa corporal; IECA: inhibidores de la enzima conversora de angiotensina; PS: Propensity score.
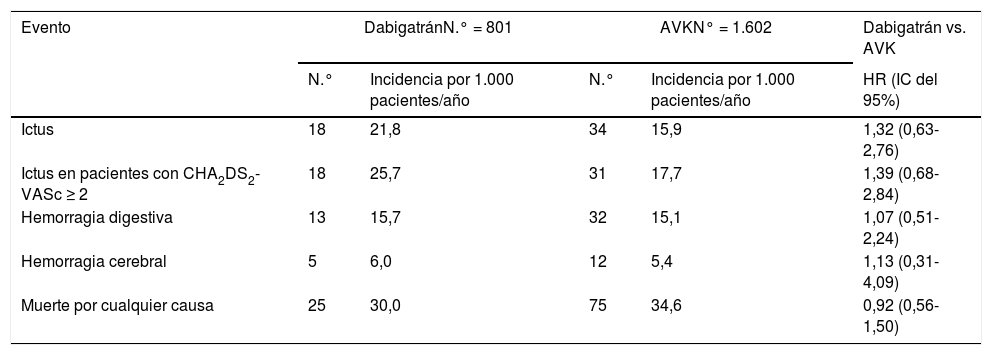
La tabla 2 muestra las tasas de incidencia y los HR ajustados en el análisis que censuraba a los pacientes cuando discontinuaban el tratamiento anticoagulante. Dabigatrán mostró un riesgo superior de ictus, aunque no fue estadísticamente significativo. Tampoco hubo diferencias estadísticas entre los grupos en el riesgo de hemorragia y mortalidad por cualquier causa.
Eventos tromboembólicos y hemorrágicos durante el seguimiento
| Evento | DabigatránN.° = 801 | AVKN° = 1.602 | Dabigatrán vs. AVK | ||
|---|---|---|---|---|---|
| N.° | Incidencia por 1.000 pacientes/año | N.° | Incidencia por 1.000 pacientes/año | HR (IC del 95%) | |
| Ictus | 18 | 21,8 | 34 | 15,9 | 1,32 (0,63-2,76) |
| Ictus en pacientes con CHA2DS2-VASc ≥ 2 | 18 | 25,7 | 31 | 17,7 | 1,39 (0,68-2,84) |
| Hemorragia digestiva | 13 | 15,7 | 32 | 15,1 | 1,07 (0,51-2,24) |
| Hemorragia cerebral | 5 | 6,0 | 12 | 5,4 | 1,13 (0,31-4,09) |
| Muerte por cualquier causa | 25 | 30,0 | 75 | 34,6 | 0,92 (0,56-1,50) |
AVK: antagonistas de vitamina K; IC: intervalo de confianza; HR: hazard ratio.
En la tabla 3 se muestran el consumo de recursos y los costes para el año 2013 asociados al manejo clínico de los pacientes incluidos en el estudio. La media de visitas a AP fue de 19,5 (DE 18,9) en el grupo de dabigatrán y de 36,1 (DE 31,6) en el de AVK. La estancia hospitalaria fue de 2,7 (DE 7,6) y 3,6 días (DE 9,7) para dabigatrán y AVK, respectivamente.
Consumo de recursos sanitarios y costes asociados al manejo de la fibrilación auricular en los pacientes incluidos en el estudio en 2013
| N.° recursos, media (DE) | Grupo con dabigatrán(n = 801) | Grupo con AVK(n = 1.602) | Total(n = 2.403) |
|---|---|---|---|
| Visitas Atención Primaria | 19,5 (18,9) | 36,1 (31,6) | 30,5 (18,9) |
| Días de hospitalización | 2,7 (7,6) | 3,6 (9,7) | 3,3 (7,6) |
| Fármacos FAa, envases por paciente | 6,2 (7,0) | 6,1 (5,9) | 6,1 (7,0) |
| Fármacos concomitantes, envases por paciente | 4,2 (6,5) | 3,6 (6,1) | 3,8 (6,5) |
| Costes (€), media (IC del 95%) | Grupo con dabigatrán(n = 801) | Grupo con AVK(n = 1.602) | Total(n = 2.403) | p valor |
|---|---|---|---|---|
| Visitas Atención Primaria | 842,5 (791,9-893,0) | 1.474,1 (1.418,3-1.529,8) | 1.263,5 (1.221,1-1.306,0) | < 0,001 |
| Hospitalizaciones según GRDb | 1.640,3 (1.341,1-1.939,6) | 2.104,8 (1.632,6-2.576,9) | 1.949,9 (1.619,8-2.280,1) | 0,194 |
| Incapacidad laboral temporal | 230,5 (122,8-338,2) | 195,2 (124,3-266,1) | 207,0 (147,7-266,3) | 0,582 |
| Laboratorio | 64,1 (57,6-70,6) | 47,2 (44,1-50,3) | 52,8 (49,8-55,8) | < 0,001 |
| Fármacos FAa | 752,3 (719,5-785,2) | 103,5 (92,3-114,6) | 319,8 (301,8-337,8) | < 0,001 |
| Fármacos concomitantes | 545,8 (499,7-592,0) | 526,7 (493,6-559,8) | 533,1 (506,2-559,9) | 0,511 |
| Coste total | 4075,6 (3725,6-4425,5) | 4551,4 (3.962,8-4.940,6) | 4326,1 (3.979,8-4.672,4) | 0,315 |
AVK: antagonistas de vitamina; FA: fibrilación auricular; IC: intervalo de confianza; GRD: grupos relacionados por el diagnóstico.
Los costes en visitas de AP y en hospitalizaciones fueron superiores en el grupo de AVK respecto al grupo de dabigatrán, aunque solo la diferencia de costes en visitas a AP fue estadísticamente significativa. Los costes en ILT y laboratorio fueron superiores en el grupo de dabigatrán, siendo solo significativa la diferencia en los últimos. En cuanto al coste de fármacos, los que se utilizan en el manejo de la FA incluyen antitrombóticos y agentes para control de ritmo y frecuencia cardíaca, y es significativamente superior para el grupo de dabigatrán. El resto de los fármacos son los que se utilizan en el tratamiento de las enfermedades concomitantes y los costes son ligeramente superiores, aunque no de manera significativa, para dabigatrán. El coste total del manejo de la FA en 2013 no presentó diferencias entre grupos, siendo de 4.075,60 € en el grupo tratado con dabigatrán y de 4.551,40 € en el grupo de AVK.
En conclusión, dabigatrán mostró un riesgo de ictus y hemorragias superior a AVK pero no estadísticamente significativo. Los costes totales del manejo de la FA fueron superiores en el grupo de pacientes tratados con AVK respecto a los que recibían dabigatrán, aunque las diferencias no fueron estadísticamente significativas.
DiscusiónEn nuestro estudio solo el 5,4% de los diagnosticados de FA iniciaron tratamiento con dabigatrán en 2011-2013. Los pacientes tratados con este fármaco eran en su mayoría hombres, más jóvenes y con menor puntuación de riesgo de ictus, aunque presentaban antecedentes de ictus y hemorragia cerebral con mayor frecuencia que aquellos que iniciaban AVK. En comparación con estudios similares, en el nuestro hubo menos pacientes que iniciaban dabigatrán después del diagnóstico de FA. Algunos de estos estudios de cohortes encontraron diferencias en la tasa de ictus entre dabigatrán y AVK, mientras que algunos no mostraron diferencias significativas. La incidencia de hemorragias también fue diferente según los estudios.
Larsen et al.24 llevaron a cabo un estudio de cohortes con la base de datos danesa en 2011-2015, en el cual se incluyó a 61.678 pacientes naïve a ACO; el 57% inició a warfarina, el 21% dabigatrán, el 12% rivaroxabán y el 10% apixabán. La proporción de pacientes que iniciaban ACOD en aquel momento era claramente superior a la de nuestro estudio, aunque actualmente ya disponemos de datos en nuestro ámbito que muestran un mayor número de pacientes que inician ACOD como primera línea de tratamiento para prevención del ictus en FA no valvular7. En el estudio de Larsen et al. no se encontraron diferencias estadísticamente significativas entre los pacientes tratados con ACOD y los tratados con AVK en la variable de efectividad; ictus isquémico. Sin embargo, cuando analizaron los fármacos por separado, rivaroxabán mostró un riesgo inferior de ictus y dabigatrán y apixabán mostraron menores tasas de sangrado y de mortalidad en comparación con warfarina. Los autores analizaron datos hasta final del 2015, por lo que la experiencia en el uso de ACOD era más amplia que la de nuestro estudio, en el que se analizó un período en el que solo dabigatrán y rivaroxabán estaban disponibles, y apixabán solo durante los últimos meses del período, aunque en nuestro estudio estos 2últimos fármacos no se incluyeron.
En un estudio de cohortes apareado mediante PS llevado a cabo en los Holanda en 2010-201225 se incluyó a 920 pacientes; el 48% inició dabigatrán y el 52%, acenocumarol. La proporción de uso de dabigatrán es superior a la de nuestro estudio. No se encontraron diferencias en incidencia de ictus entre los 2fármacos y se vio un menor riesgo de sangrado mayor con dabigatrán respecto a acenocumarol.
En un estudio que se realizó en EE. UU. en 2010-2012 con apareamiento PS26 cumplían criterios de inclusión 64.935 pacientes; el 32,5% iniciaba dabigatrán y el 67,5%, warfarina. Dabigatrán mostró un riesgo inferior de ictus isquémico y hemorrágico e infarto de miocardio por separado, y mayor riesgo de hemorragia digestiva.
En otro estudió en EE. UU. llevado a cabo por Graham et al.27 en 2010-2012, el 19,8% de los pacientes iniciaban dabigatrán y el 80,2%, warfarina. También se hizo apareamiento por PS y se analizaron la efectividad y la seguridad, mostrando dabigatrán 150mg/12h un menor riesgo de ictus isquémico, infarto de miocardio, HIC y muerte, y mayor riesgo de sangrado digestivo. No se encontraron diferencias con dabigatrán 75mg/12h, excepto menor riesgo de HIC respecto a warfarina. Esta dosis no tiene autorizada la indicación en FA no valvular en Europa.
En otro estudio apareado 1:2 por PS en Dinamarca, el 27,4% de los pacientes iniciaban dabigatrán y el 72,6%, warfarina. La incidencia de ictus y embolias no fue diferente entre grupos. Las tasas de mortalidad, HIC e infarto ajustadas fueron inferiores con las 2dosis de dabigatrán respecto a warfarina, y la de hemorragia gastrointestinal fue inferior solo para la dosis de 110mg/12h28.
Como ya se ha comentado anteriormente, el uso de ACOD en nuestro país es menor que en otros países14,29,30, principalmente debido a las condiciones de prescripción más restrictivas que se incluyen en el IPT, que recomienda prescribir los ACOD solo en pacientes con antecedentes de HIC o alto riesgo de presentarla y en pacientes con dificultades para mantener valores de INR dentro del margen terapéutico8,31.
Por otro lado, en nuestro estudio también calculamos los costes derivados del manejo de la FA durante el año 2013 en las 2cohortes. El mayor coste en visitas de AP en el grupo de AVK podría ser debido al mayor número de visitas respecto a los tratados con dabigatrán, y estas visitas pueden ser en gran parte debidas a la monitorización de INR, que en nuestro ámbito se ha estimado que tiene un coste de entre 305 y 714 € anuales por paciente. Las tasas de eventos relacionados con la FA que requirieron hospitalización fueron superiores, aunque no estadísticamente significativas, en el grupo de dabigatrán, posiblemente por la mayor estancia hospitalaria del grupo de AVK. En cuanto a los costes de las ILT, estos fueron superiores, aunque la diferencia estadística no fue significativa, en el grupo de dabigatrán, lo que podría explicarse por la menor media de edad de estos pacientes, que todavía serían población activa, mientras que los que reciben AVK son mayores y, por tanto, jubilados. Los costes mayores en la partida de laboratorio para el grupo de dabigatrán podrían explicarse por la necesidad de la monitorización de la función renal frecuente, puesto que el fármaco se elimina principalmente por vía renal. Por último, los costes superiores en fármacos para el grupo de dabigatrán son evidentemente debidos al mayor precio del fármaco. En cuanto a los costes totales, fueron superiores para el grupo de pacientes que recibían AVK, sobre todo por el mayor peso de las partidas debidas a visitas de AP y a hospitalizaciones por ictus y hemorragias, pero las diferencias con el grupo de dabigatrán no fueron estadísticamente significativas.
En cuanto a los estudios sobre costes del manejo de la FA, la mayoría son estudios de coste-efectividad que comparan AVK con ACOD, pero hay poca bibliografía sobre costes atribuidos a la FA y su manejo desde la AP de salud. El estudio de Ringborg et al. estimó los costes de la FA en 5países europeos. En España se describieron costes de 6.360 € asociados a ingresos hospitalarios, que incluían también diagnósticos, intervenciones, tratamiento farmacológico y pérdida de productividad durante el ingreso hospitalario. En nuestro caso, no podemos calcular estos costes intrahospitalarios puesto que no tenemos acceso a estos datos.
En el estudio de Desai et al. se calculó el uso de recursos sanitarios, como el número de fármacos, hospitalizaciones y días de estancia hospitalaria, y visitas a AP, cardiología y neurología. En los pacientes que recibían AVK había más hospitalizaciones y mayor número de días de estancia hospitalaria, así como mayor número de visitas a AP, igual que en nuestro estudio. También describieron un menor número de visitas a cardiología en comparación con los pacientes que recibían ACOD.
En nuestro estudio no encontramos diferencias significativas entre dabigatrán y AVK en ninguna de las variables de efectividad y seguridad, lo que podría ser debido al reducido tamaño de muestra. Por tanto, necesitamos llevar a cabo otros estudios que incluyan grandes muestras de pacientes anticoagulados, también con otros fármacos, para poder conseguir una mayor potencia estadística.
El uso, la efectividad y la seguridad de los ACOD en nuestro ámbito necesitaba ser analizado, puesto que este grupo de fármacos se utilizan cada vez más para la prevención del ictus en FA no valvular. Algunas de las fortalezas de nuestro estudio son la completitud de datos sociodemográficos y clínicos de vida real. Entre las limitaciones incluimos los posibles datos faltantes, cuyo efecto puede ser minimizado mediante técnicas de imputación múltiple, los efectos de los posibles confusores, que se han minimizado mediante modelos ajustados de regresión de Cox para las características sociodemográficas y posibles factores confusores y predictores, tal y como se describe en el análisis estadístico, y el no disponer de datos más actualizados, puesto que dentro del estudio ESC-FA solo se nos autorizó la extracción de datos hasta final de 2013. Las limitaciones específicas del bajo uso de ACOD en el período de estudio son inherentes al estudio, puesto que las recomendaciones del IPT los posicionan como terapia de segunda línea en pacientes recién diagnosticados de FA. Sobre el tamaño de muestra, actualmente estamos llevando a cabo una serie de estudios sobre el uso de ACO en FA, con lo que próximamente tendremos resultados actualizados y asimismo podremos estimar los resultados en salud derivados del uso de este grupo de fármacos.
ConclusionesLa mayoría de los pacientes recién diagnosticados de FA iniciaban AVK durante el período de nuestro estudio.
El bajo uso de ACOD, específicamente dabigatrán, es debido a las recomendaciones del IPT de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) para la prescripción de estos fármacos, que se reservan para terapia anticoagulante de segunda línea.
Los pacientes que iniciaron dabigatrán eran más jóvenes, con menos comorbilidades y menor puntuación en la escala de riesgo de ictus, con una mayor frecuencia de historia de HIC en comparación con aquellos que iniciaron AVK.
No encontramos diferencias en la incidencia de ictus y hemorragias entre los usuarios de dabigatrán y AVK durante el período de seguimiento.
Los costes totales del manejo de la FA son superiores en el grupo de pacientes que recibían AVK, aunque no mostraron diferencias significativas respecto a los costes del grupo de pacientes que recibían dabigatrán.
El tratamiento anticoagulante oral para la prevención de ictus en fibrilación auricular no valvular más prescrito en nuestro ámbito siguen siendo los antagonistas de la vitamina K (AVK).
Los anticoagulantes orales directos se reservan para terapia anticoagulante de segunda línea debido a las recomendaciones establecidas por la Agencia Española de Medicamentos y Productos Sanitarios.
Qué aporta este estudioEn este estudio de cohortes con datos de vida real no encontramos diferencias en la incidencia de ictus y hemorragias entre los usuarios de dabigatrán y AVK durante el período de seguimiento.
Los costes totales del manejo de la fibrilación auricular fueron superiores en el grupo de pacientes que recibían AVK, principalmente debido a mayores costes de visitas de atención primaria y hospitalizaciones.
El «Estudio ESC-FA, estudio en diferentes fases sobre la efectividad, seguridad y costes de la prevención tromboembólica en pacientes con fibrilación auricular no valvular» es un proyecto financiado por el Instituto de Salud Carlos III en la convocatoria correspondiente al año 2011 mediante los Proyectos para la traslación de la aplicación terapéutica de medicamentos de uso humano, huérfanos y terapias avanzadas, con el código expediente EC11-251.
Aspectos éticos y de confidencialidad de datosEl presente estudio sigue las directrices nacionales e internacionales: Declaración de Helsinki y principios de Buenas Prácticas en Investigación.
El Comité Ético de Investigación del IDIAP Jordi Gol, institución de referencia para la investigación en Atención Primaria del ICS aprobó el protocolo de estudio en diciembre del 2011.
De acuerdo con la legislación española y europea sobre confidencialidad y protección de datos (Ley 3/2018 de Protección de Datos de Carácter Personal), los datos incluidos en la base de datos SIDIAP están siempre anonimizados e identificados mediante un código único encriptado que imposibilita la identificación de las personas. Por ello, no es necesario solicitar consentimiento informado a los participantes.
Para el cruce de las bases de datos de SIDIAP con CMBD-HA (u otras), SIDIAP utiliza un tercero para asegurar la confidencialidad, el cual no tiene acceso a la información clínica, únicamente a códigos e identificadores.
Depósito y enlace de datosApéndice técnico, código estadístico y conjunto de datos disponibles mediante solicitud a autora de correspondencia.
Conflicto de interesesLos autores no declaran ningún conflicto de interés.