El pronóstico de la estenosis aórtica es sombrío cuando asocia fracaso ventricular. Sin embargo, los resultados son favorables con cirugía. Nuestro objetivo es valorar la evolución de pacientes con estenosis aórtica y disfunción ventricular izquierda sometidos a sustitución valvular aórtica.
MétodosVeintiocho pacientes con estenosis aórtica severa y fracción de eyección menor o igual al 50% fueron sometidos a sustitución valvular aórtica entre 2003 y 2012. Excluimos a aquellos con regurgitación aórtica o enfermedad coronaria asociadas.
ResultadosEdad media 70,6 años; 19 hombres (67,9%) y 9 mujeres (32,1%). El 92,8% en clase funcional de la New York Heart Association III-IV, con fracción de eyección media 38,93% (el 82,1% presentaba disfunción ventricular moderada y el 17,9% disfunción severa). Al 66,7% se le implantó una prótesis mecánica y al 33,3% una biológica; 4 pacientes (14,3%) necesitaron marcapasos definitivo. Uno (3,6%) presentó complicaciones graves (taponamiento cardíaco y mediastinitis). Mortalidad hospitalaria: 7,1% (2 pacientes). Ningún enfermo falleció durante el seguimiento (29,9±73 meses). Incremento postoperatorio del 16,38% en la fracción de eyección, pasando todos (100%) a una clase funcional I. Supervivencia global: 92,9%.
ConclusionesLa sustitución valvular aórtica es una opción segura, eficaz y duradera en pacientes con disfunción ventricular izquierda. Se asocia a una mejoría en la clase funcional y fracción de eyección, con una perspectiva de futuro excelente.
Aortic stenosis has a dismal prognosis when associated with ventricular dysfunction. In contrast, outcomes become favourable with surgery. Our objective is to evaluate the outcome of patients with aortic stenosis and left ventricular dysfunction undergoing aortic valve replacement.
Methods28 patients with severe aortic stenosis and an ejection fraction less than 50% or equal underwent aortic valve replacement between 2003 and 2012. We excluded those with associated aortic regurgitation or coronary artery disease.
ResultsMean age was 70,61 years. 19 males (67,9%), 9 females (32,1%). 92,8% were in New York Heart Association functional class III-IV, with a mean ejection fraction of 38,93% (82,1% had moderate left ventricular dysfunction, 17,9% had severe dysfunction). 66,7% received a mechanical valve, in 33,3% a biological one was implanted. 4 patients (14,3%) required a permanent pacemaker. 1 patient (3,6%) had severe complications (cardiac tamponade and mediastinitis). Hospital mortality was 7,1% (2 patients). There were no late deaths during follow-up (29,9±73 months). Postoperatively, mean ejection fraction showed an increase of 16,38%, all patients (100%) were in functional class I. Overall survival was 92,9%.
ConclusionsAortic valve replacement is a safe, effective and durable option in patients with left ventricular dysfunction. It is associated with an improvement in functional class and ejection fraction, with an excellent outlook.
La estenosis aórtica (EAO) es, tras la enfermedad coronaria y la hipertensión arterial, la tercera forma más común de enfermedad cardiovascular en el mundo occidental1,2, siendo también la valvulopatía más frecuente en países desarrollados3,4 y la principal causa de recambio valvular en Europa y Estados Unidos1,4-6. Su prevalencia aumenta con la edad, siendo del 8% en pacientes con edades comprendidas entre 65-79 años y del 16% en octogenarios7.
El número de sustituciones valvulares aórticas (SVAO) anuales se ha incrementado, constituyendo la EAO una creciente carga de salud. Esto puede explicarse, por un lado, por el incremento en la esperanza de vida de la población (se espera que esta tendencia continúe, estando previsto que el número de SVAO se doble en 20201), pero, por otro lado, dicho incremento también refleja un cambio en el umbral quirúrgico: la cirugía se lleva a cabo actualmente tanto en pacientes considerados no lo suficientemente sintomáticos (o asintomáticos), como en aquellos previamente considerados demasiado enfermos para indicar el proceso quirúrgico8. Así, los pacientes acuden con comorbilidades tales como edad avanzada, enfermedad pulmonar, insuficiencia renal, enfermedad coronaria asociada y disfunción ventricular izquierda (DVI) significativa.
Ante la aparición de la DVI es necesaria una corrección quirúrgica rápida, ya que el pronóstico se vuelve sombrío, con una supervivencia media de alrededor de 2 años9,10 y un elevado riesgo de muerte súbita2.
La SVAO se recomienda como un procedimiento quirúrgico estándar11, pues mejora los síntomas y la supervivencia5, todo ello con una baja morbimortalidad perioperatoria y resultados favorables, incluso en pacientes con DVI6,11.
En la literatura, la mayoría de los estudios que evalúan el efecto de la cirugía en enfermos con EAO y DVI incluyen a pacientes con enfermedad coronaria y diversos grados de regurgitación aórtica. Ambas patologías influyen en la aparición del fracaso ventricular y, además, afectan a los resultados quirúrgicos, haciéndose difíciles de interpretar9.
El objetivo de este estudio es valorar la evolución de pacientes con EAO aislada pura y DVI sometidos a SVAO.
MétodosSe trata de un estudio observacional, descriptivo y transversal de pacientes intervenidos de SVAO aislada entre 2003 y 2012, con criterios de inclusión: 1) EAO de válvula nativa, pura (es decir, sin ningún grado de regurgitación asociado) y severa, definida como área valvular aórtica<1 cm2, gradiente de presión transaórtico medio>40mmHg y velocidad máxima del jet aórtico>4m/s. En los pacientes con EAO severa de bajo gradiente, la inclusión se estableció con área valvular aórtica<1 cm2 con velocidad máxima del jet aórtico<4m/s o gradiente de presión transaórtico medio<40mmHg, y que con ecocardiografía de estrés con dobutamina tuvieran un área valvular aórtica<1 cm2 y velocidad máxima del jet aórtico>4m/s a cualquier flujo, y 2) que estuviera asociada a DVI al menos moderada (la función ventricular se clasificó según lo establecido en la escala de riesgo EUROSCORE I), considerando DVI ligera (fracción de eyección [FE] 51-65%), DVI moderada (FE 30-50%) y DVI severa (FE < 30%), y con arterias coronarias sin lesiones angiográficamente significativas (ausencia de lesiones ≥ 50% en cualquiera de las arterias coronarias epicárdicas).
Se excluyó a los pacientes sometidos de forma concomitante a otras intervenciones valvulares (distintas de la SVAO) así como las reintervenciones.
Se analizan las variables: edad, sexo, talla, peso, índice de masa corporal, superficie corporal, enfermedad pulmonar obstructiva crónica (pacientes en tratamiento prolongado con broncodilatadores y/o corticoides o con espirometría preoperatoria con obstrucción severa), insuficiencia renal crónica (moderada con aclaramiento creatinina 50-85 ml por minuto, severa con aclaramiento creatinina < 50 ml por minuto no dializados y pacientes en diálisis), insuficiencia mitral y/o tricúspide ligera/moderada, ritmo cardíaco, clase funcional de la New York Heart Association, área valvular aórtica, gradiente de presión transaórtico máximo y medio, velocidad máxima del flujo aórtico, diámetro diastólico del ventrículo izquierdo (VI), dilatación ventricular izquierda (ligera con diámetro ventricular 55-60mm, moderada 61-70mm y severa > 70mm), hipertrofia ventricular izquierda (HVI) (ligera con grosor septo interventricular 10-15mm, moderada 16-20mm, severa > 20mm), FE, tipo y tamaño de prótesis implantada, complicaciones, días de hospitalización, tiempo de seguimiento y mortalidad.
En cuanto a la técnica quirúrgica, la vía de abordaje en todos los pacientes fue la esternotomía media completa. La cirugía se llevó a cabo en circulación extracorpórea monocava y en hipotermia ligera (32 °C). La dosis inicial de cardioplejía fría hemática fue por vía anterógrada (aplicando también suero frío epicárdico), repitiéndose las dosis de mantenimiento cada 20 min por vía retrógrada. No se utilizó termómetro septal para control de la temperatura. Tras aortotomía transversalizada, se procedió a explante de válvula aórtica nativa e implante de prótesis aórtica con puntos apoyados en teflón en cara ventricular. La prótesis seleccionada (mecánica o biológica) fue a criterio del cirujano responsable y el paciente intervenido. En ningún caso fue necesario realizar ampliación de la raíz aórtica, pues la prótesis más pequeña implantada fue de 19 mm de diámetro.
Para el análisis de datos se ha utilizado el programa estadístico SPSS 19. Para variables cuantitativas se obtuvieron las medidas de tendencia central y de dispersión (media y desviación estándar (DE), respectivamente). Para variables cualitativas se calcularon frecuencias absolutas y relativas. Los test de contraste de hipótesis utilizados fueron la t de Student y la chi al cuadrado para variables cualitativas.
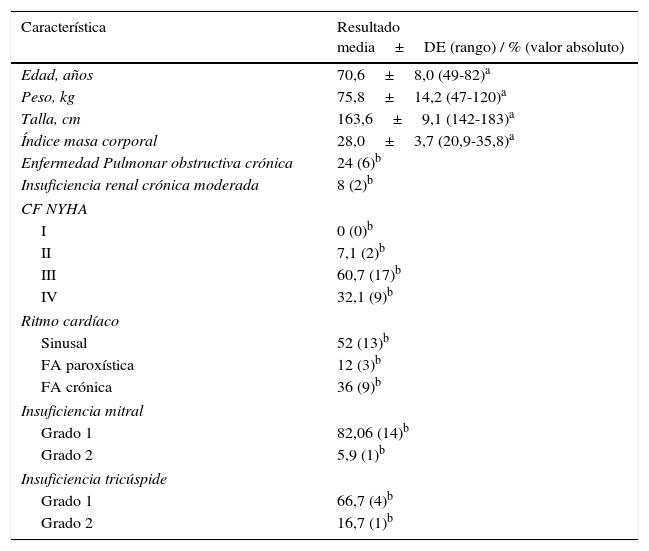
ResultadosSe estudió a 28 pacientes. Los hombres representaban el 67,9% (19) y las mujeres el 32,1% (9). Las características demográficas y clínicas se muestran en la tabla 1.
Características demográficas y clínicas preoperatorias
| Característica | Resultado media±DE (rango) / % (valor absoluto) |
|---|---|
| Edad, años | 70,6±8,0 (49-82)a |
| Peso, kg | 75,8±14,2 (47-120)a |
| Talla, cm | 163,6±9,1 (142-183)a |
| Índice masa corporal | 28,0±3,7 (20,9-35,8)a |
| Enfermedad Pulmonar obstructiva crónica | 24 (6)b |
| Insuficiencia renal crónica moderada | 8 (2)b |
| CF NYHA | |
| I | 0 (0)b |
| II | 7,1 (2)b |
| III | 60,7 (17)b |
| IV | 32,1 (9)b |
| Ritmo cardíaco | |
| Sinusal | 52 (13)b |
| FA paroxística | 12 (3)b |
| FA crónica | 36 (9)b |
| Insuficiencia mitral | |
| Grado 1 | 82,06 (14)b |
| Grado 2 | 5,9 (1)b |
| Insuficiencia tricúspide | |
| Grado 1 | 66,7 (4)b |
| Grado 2 | 16,7 (1)b |
CF NYHA: clase funcional de la New York Heart Association; cm: centímetros; DE: desviación estándar; FA: fibrilación auricular; kg: kilogramos.
El 24% (6) presentaba enfermedad pulmonar obstructiva crónica y el 8% (2) tenía una función renal moderadamente deprimida.
El 82,1% de los pacientes tenía una DVI moderada, mientras que el 17,9% restante presentaba una DVI severa.
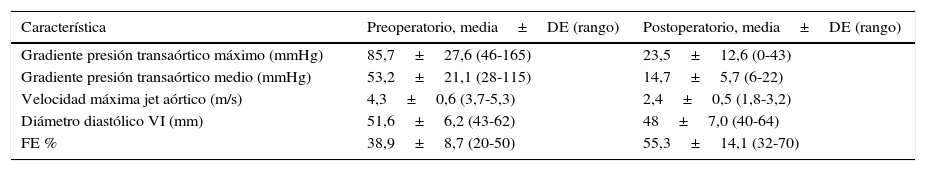
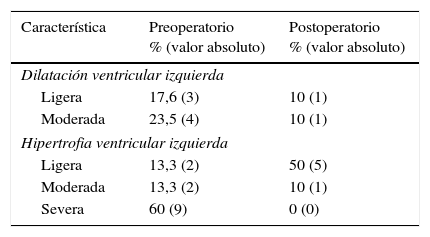
La tabla 2 muestra los parámetros ecocardiográficos pre y postoperatorios. El gradiente máximo de presión transaórtico y la velocidad máxima del flujo aórtico experimentaron una reducción media de 62,2mmHg y 1,9m/s, respectivamente. El gradiente medio de presión transaórtico se redujo una media de 38,5mmHg. El diámetro diastólico del VI disminuyó 3,6mm de media. La FE mostró un incremento del 16,4% tras la cirugía. En la tabla 3 se recoge el porcentaje de pacientes que presentaba dilatación e hipertrofia ventricular izquierdas durante el pre y postoperatorio, así como sus grados.
Datos ecocardiográficos pre y postoperatorios
| Característica | Preoperatorio, media±DE (rango) | Postoperatorio, media±DE (rango) |
|---|---|---|
| Gradiente presión transaórtico máximo (mmHg) | 85,7±27,6 (46-165) | 23,5±12,6 (0-43) |
| Gradiente presión transaórtico medio (mmHg) | 53,2±21,1 (28-115) | 14,7±5,7 (6-22) |
| Velocidad máxima jet aórtico (m/s) | 4,3±0,6 (3,7-5,3) | 2,4±0,5 (1,8-3,2) |
| Diámetro diastólico VI (mm) | 51,6±6,2 (43-62) | 48±7,0 (40-64) |
| FE % | 38,9±8,7 (20-50) | 55,3±14,1 (32-70) |
DE: desviación estándar; FE: fracción de eyección; mm: milímetros; mmHg: milímetros de mercurio; m/s: metros/segundo; VI: ventrículo izquierdo.
Dilatación e hipertrofia ventricular izquierda pre y postoperatorias
| Característica | Preoperatorio % (valor absoluto) | Postoperatorio % (valor absoluto) |
|---|---|---|
| Dilatación ventricular izquierda | ||
| Ligera | 17,6 (3) | 10 (1) |
| Moderada | 23,5 (4) | 10 (1) |
| Hipertrofia ventricular izquierda | ||
| Ligera | 13,3 (2) | 50 (5) |
| Moderada | 13,3 (2) | 10 (1) |
| Severa | 60 (9) | 0 (0) |
En cuanto a las características de las prótesis aórticas y su relación con la superficie corporal, el área valvular efectiva media protésica fue de 1,7 cm2. Al 66,7% de los pacientes se le implantó una prótesis mecánica. La más frecuentemente implantada fue la prótesis de St. Jude Medical Regent® (Saint Jude Medical Inc, Saint Paul, Minnesota, EE. UU.) de 23mm de diámetro (que representa el 22,2% del total de casos), seguida de la CarboMedics Top Hat® (CarboMedics Inc, Austin, EE. UU.) de 25mm (14,8% del total). Al 33,3% restante se le implantó una prótesis biológica, siendo la más frecuente la prótesis de Carpentier Edwards Magna® (Edwards Lifesciences, Irvine, EE. UU.) de 23mm de diámetro (que representa el 18,5% del total de casos), seguida de la Carpentier Edwards Magna® (Edwards Lifesciences, Irvine, EE. UU.) de 21mm (11,1% del total). En el 46,4% de los casos existe desproporción prótesis-paciente (definida como ligera-moderada si el área del orificio efectivo indexada es mayor o igual a 0,85 cm2/m2 y severa si es menor o igual a 0,65 cm2/m2). Tan solo uno de los pacientes de este subgrupo (7,7%) presentaba una desproporción severa, el resto (92,3%) fue de grado ligero-moderado.
El tiempo medio ± DE de hospitalización fue de 21,8 ± 26,9 días, con un mínimo de 7 días y un máximo de 143. La mortalidad hospitalaria fue del 7,1% (2 pacientes).
Durante el postoperatorio, 4 pacientes (14,3%) necesitaron el implante de un marcapasos definitivo: 2 (7,2%) de forma inmediata por la aparición de un bloqueo aurículo-ventricular completo posquirúrgico y los 2 restantes (7,2%) durante el seguimiento por fibrilación auricular lenta. Solo un 3,6% (un enfermo) presentó otras complicaciones graves postoperatorias, concretamente un taponamiento cardíaco y una posterior dehiscencia esternal por mediastinitis que precisó recerclaje.
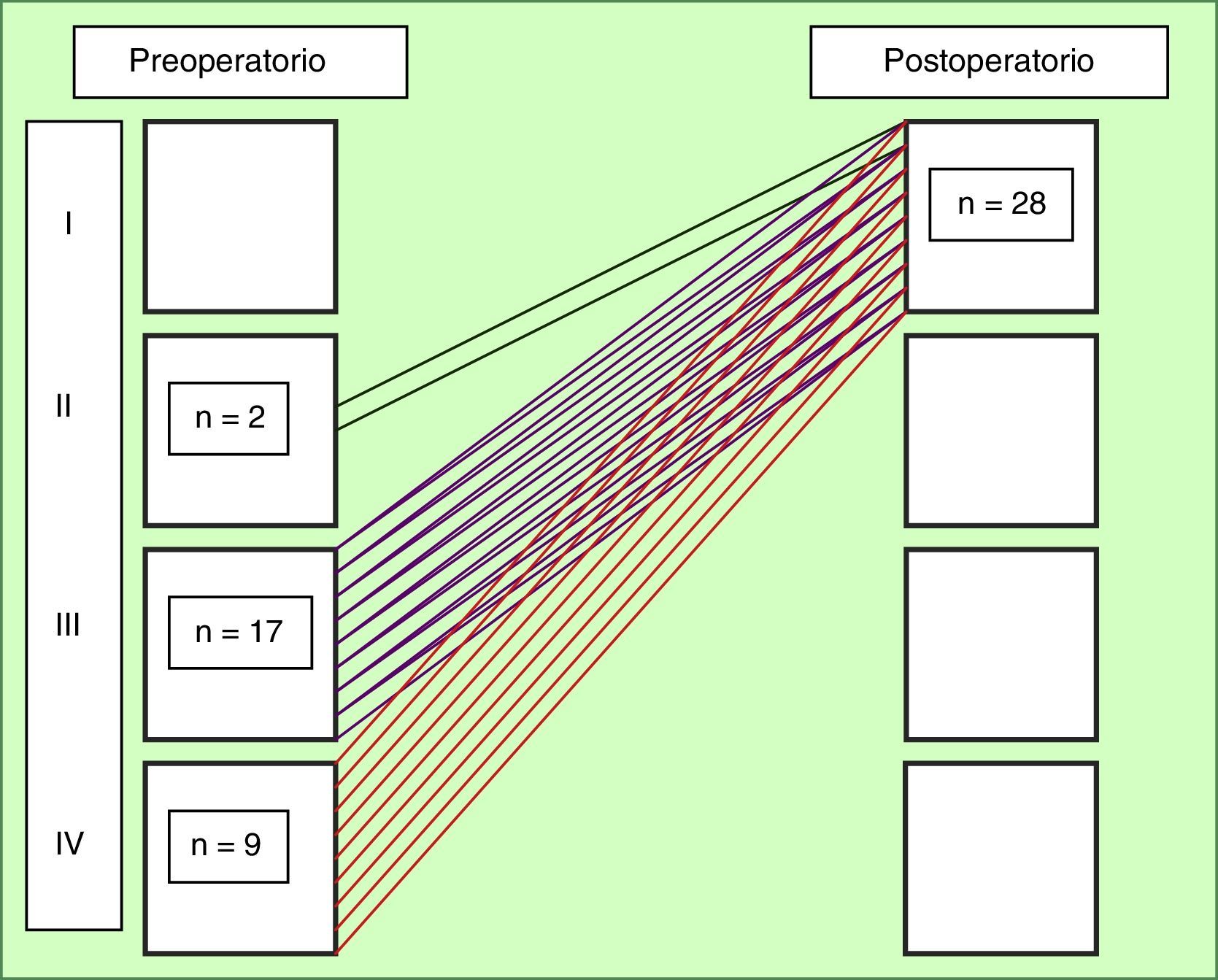
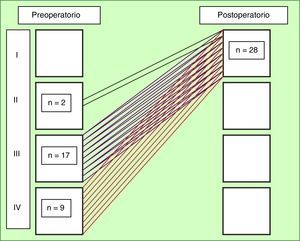
Durante el seguimiento, cuya duración media ± DE fue de 29,9 ± 36,5 meses, rango entre 0 y 114, un paciente falleció a causa de una neoplasia pélvica. Todos los enfermos de la serie (100%) pasaron a una clase funcional I de la New York Heart Association durante el postoperatorio (fig. 1). La supervivencia global fue del 92,9%.
DiscusiónLa EAO supone un desajuste de poscarga para el VI, que incrementa la tensión de su pared con la consecuente HVI, dilatación y eventual fracaso2,3,12-16. El desarrollo de la HVI es un mecanismo compensatorio que constituye un determinante crítico en el funcionamiento ventricular de los pacientes con EAO2. En nuestro estudio el 86,6% de los pacientes tenía algún grado de HVI (que fue severa en el 60% de los casos). Cuando la EAO empeora y este mecanismo compensatorio fracasa, el VI se dilata12. El 41,1% de nuestros enfermos presentaba ya algún grado de dilatación ventricular, que fue catalogada de moderada en el 23,5% de los mismos. Dicha dilatación incrementa el estrés sistólico de la pared, aumentando el consumo miocárdico de oxígeno y disminuyendo progresivamente la función sistólica12.
La SVAO es el tratamiento de elección en estos pacientes3,17,18. Mejora dramáticamente los síntomas de fracaso cardíaco8,10 y la clase funcional. Todos nuestros pacientes pasaron a una clase funcional de la New York Heart Association I tras la intervención, con evidentes resultados también en términos hemodinámicos (todas las variables estudiadas experimentaron una clara mejoría después de la cirugía, destacando un incremento del 16,4% en la FE junto a una disminución de la HVI).
La mejoría está en relación directa con el aumento en el área valvular aórtica conseguido por la SVAO. Nuestros pacientes pasaron de tener un área valvular aórtica media de 0,7 cm2 a tener un área valvular efectiva protésica media de 1,7 cm2. Ello subraya la importancia de implantar prótesis con unas características hemodinámicas adecuadas al índice de masa corporal de cada paciente, que permitan optimizar el incremento posterior del área valvular aórtica, y así, evitar cualquier estenosis residual que sería muy perjudicial en el contexto de un VI disfuncionante.
Numerosos estudios han identificado la desproporción prótesis-paciente como un factor de riesgo que afecta a la supervivencia tras la SVAO. Del mismo modo, el remodelado ventricular puede retrasarse con el implante de prótesis pequeñas que dejan gradiente residual1,17. En nuestro estudio, el 46,4% de los pacientes presentó desproporción prótesis-paciente. Sin embargo, tan solo uno de ellos (7,7%) presentaba una desproporción severa, el resto (92,3%) fue de grado ligero-moderado. Ninguno de estos pacientes presentó posteriormente clínica indicativa de estenosis residual.
En pacientes con EAO y DVI, la SVAO prolonga la supervivencia3,5, ya que cambia drásticamente la evolución natural de la enfermedad, devolviéndolos a una situación basal en la que su esperanza de vida no se verá truncada en un máximo de 2 años, sino que será comparable con la de la población general homóloga7, lo que supone un beneficio claro, con el subsiguiente impacto sociológico, económico y personal.
Aunque diversos estudios señalan una correlación entre baja FE preoperatoria y mayor riesgo de mortalidad tras SVAO5,8,11,17,19 (algunos incluso han sugerido que esta no debería considerarse en este subgrupo de pacientes), múltiples estudios han demostrado una supervivencia favorable en estos pacientes.
En ellos, la evidencia científica actual pone de manifiesto que deberían someterse a SVAO (salvo contraindicación), porque esta les ofrece unos resultados excelentes a corto y medio plazo en comparación con la historia natural de la enfermedad, con una morbimortalidad perioperatoria aceptable11,12. Los resultados obtenidos en nuestro estudio apoyan esta idea, con mortalidad del 7,1% (similar a la publicada, entre el 8-33%1,3,9) y una supervivencia global del 92,9%, con un porcentaje bajo de complicaciones.
Se debe recordar que las series más antiguas mostraban resultados desfavorables, pero en la actualidad las técnicas, particularmente en relación con la preservación miocárdica, el manejo quirúrgico y anestésico y la tecnología protésica con materiales y hemodinámica mejorados, han contribuido a minimizar los riesgos asociados a la SVAO con disfunción ventricular asociada1,5,8,9,11.
ConclusionesLa SVAO presenta una baja morbimortalidad asociada y proporciona excelentes resultados en el tratamiento de pacientes con EAO severa y DVI. Esta técnica quirúrgica ofrece un cambio drástico en la evolución natural de la enfermedad, mejorando la supervivencia.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes y que todos los pacientes incluidos en el estudio han recibido información suficiente y han dado su consentimiento informado por escrito para participar en dicho estudio.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.