La hemorragia digestiva alta (HDA) es una potencial complicación tras la cirugía bariátrica, con una incidencia entre el 2 y el 4%. El objetivo de este estudio es presentar nuestra incidencia de HDA tras cirugía bariátrica, su forma de presentación y su manejo mediante un algoritmo terapéutico.
Pacientes y métodoEstudio observacional prospectivo de una serie de 300 cirugías bariátricas por laparoscopia de manera consecutiva, desde enero del 2004 hasta diciembre del 2012. Se recogen datos demográficos, forma de presentación, diagnóstico y tratamiento de la HDA. En 280 pacientes se practicó bypass gástrico según la técnica de Wittgrove modificada, con anastomosis circular en 265 y anastomosis longitudinal en 15. En 20 pacientes se practicó gastrectomía vertical.
ResultadosAparecieron 27 casos (9%) de HDA tratados con: cirugía en un caso por inestabilidad hemodinámica; con gastroscopia diagnóstica-terapéutica en 13 casos (en 2 casos, 2 veces); en 10 de ellos, apareció de forma precoz (1-6 días) cuyo origen fue la línea de sutura de la anastomosis gastroyeyunal (GY) y en 3 de forma tardía, a los 15-20 días, siendo su origen una úlcera en la boca anastomótica. En el resto (13 pacientes), el manejo fue de forma conservadora.
ConclusionesAunque el manejo conservador de la HDA resuelve la mayoría de los casos, la clínica y la forma de presentación deben alertarnos, por lo que, en casos graves de sangrado, se requerirá de una endoscopia urgente. Es importante un equipo multidisciplinar y una comunicación estrecha entre cirujanos y endoscopistas para el manejo de esta seria complicación.
Gastrointestinal bleeding (GB) is a potential complication after bariatric surgery and its frequency is around 2-4% according to the literature. The aim of this study is to present our experience with GB after bariatric surgery, its presentation and possible treatment options by means of an algorithm.
Patients and methodFrom January 2004 to December 2012, we performed 300 consecutive laparoscopic bariatric surgeries. A total of 280 patients underwent a laparoscopic Roux en Y gastric bypass with creation of a gastrojejunal anastomosis using a circular stapler type CEAA No 21 in 265 patients and with a linear stapler in 15 patients. Demographics, clinical presentation, diagnostic evaluation and treatment were reviewed. A total of 20 patients underwent a sleeve gastrectomy.
ResultsTwenty-seven cases (9%) developed GB. Diagnosis and therapeutic endoscopy was required in 13 patients. The onset of bleeding occurred between the 1st-6th postop days in 10 patients, and the origin was at the gastrojejunostomy staple-lines, and 3 patients had bleeding from an anastomotic ulcer 15-20 days after surgery. All other patients were managed non-operatively.
ConclusionConservative management of gastrointestinal bleeding is effective in most cases, but endoscopy with therapeutic intent should be considered in patients with severe or recurrent bleeding. Multidisciplinary postoperative follow- up is very important for early detention and treatment of this complication.
La obesidad se ha convertido en la epidemia del siglo XXI, por lo que el número de procedimientos quirúrgicos ha crecido exponencialmente. El bypass gástrico en Y de Roux laparoscópico se ha convertido en la técnica quirúrgica gold estándar para el tratamiento de la obesidad mórbida1. Según los criterios de Fobi-Baltasar que definen un buen tratamiento de la obesidad, existe acuerdo en que la técnica debe ser: segura (mortalidad < 1% y morbilidad < 10%) reproducible, ofrecer una buena calidad de vida, requerir pocas revisiones (<2%), tener mínimos efectos secundarios y ser fácilmente reversible2–4.
La hemorragia digestiva alta precoz (definida como aquella que ocurre antes de las 2 semanas tras la cirugía bariátrica) presenta una incidencia variable, entre 0,6 y 4% y es una de las complicaciones más frecuentes asociadas al bypass gástrico en comparación con otras técnicas como sleeve o la banda gástrica y generalmente su origen se encuentra en la anastomosis gastroyeyunal1,5.
No es fácil precisar la causa y evolución del sangrado, por lo que en determinados casos se requiere de una endoscopia que permita localizar y tratar el origen del sangrado, siendo su uso, en el postoperatorio inmediato, controvertido y complejo por el riesgo de dehiscencia o perforación de la anastomosis, con unos estudios publicados muy limitados y dispares5.
El objetivo de este estudio es presentar nuestra incidencia de hemorragia digestiva alta postoperatoria, su forma de presentación y su manejo en 300 pacientes tratados mediante cirugía bariátrica laparoscópica.
Material y métodosEn el periodo comprendido desde enero del 2004 hasta diciembre del 2012, 300 pacientes fueron intervenidos mediante cirugía bariátrica. Se distribuyeron en 123 varones y 177 mujeres con una edad media de 49 años (rango 25-60). Las indicaciones fueron IMC igual o superior a 40kg/m2, o IMC de 35 si se asociaban a comorbilidades mayores, tras una valoración por endocrinología, psiquiatría y ginecología. Algunos con IMC>60 y enfermedad severa se remitieron para colocación de balón intragástrico transitorio. Tras la valoración del riesgo quirúrgico por el anestesista, fueron intervenidos por el mismo grupo de cirujanos dedicados a la cirugía bariátrica.
En cuanto a la técnica quirúrgica, en 280 pacientes, se realizó bypass gástrico en Y de Roux laparoscópico según la técnica de Wittgrove modificada. Para la confección del reservorio gástrico, se realizó una sección horizontal y 2 o 3 verticales con grapadora de carga azul y la sección del asa yeyunal se seccionó con grapadora con carga vascular. En 265 pacientes se practicó una anastomosis gastroyeyunal circular terminolateral con material de autosutura tipo CEAA n.° 21 y en 15 pacientes fue una anastomosis terminolateral longitudinal mediante sutura mecánica lineal de 45mm de carga azul (grapas de 3,5mm) y se cerró con sutura manual sobre una sonda calibradora. Se revisó la anastomosis y, tras comprobar la estanqueidad anastomótica, se dieron 2 o 3 puntos tipo Hoffmeister a cada lado y en el centro de la anastomosis. La anastomosis del pie de asa se realizó laterolateral con endograpadora de 45mm carga vascular (grapas de 2,8mm) y posteriormente se cerró el orificio de forma manual.
En 20 pacientes se realizó gastrectomía vertical (gastroplastia tubular), seccionando el estómago con endograpadora de cargas azules.
Como profilaxis antitrombótica se utilizó heparina (5.000 unidades subcutáneas) el día previo a la intervención y los días posteriores. Se usaron medias de compresión neumática intermitente en la cirugía y el primer día postoperatorio con movilización precoz, tras su retirada. Como rutina se administró como profilaxis antibiótica una dosis única de cefazolina 2 g en la inducción anestésica. En todos los casos, tras la cirugía se realizó control postoperatorio en la Unidad de Cuidados Intensivos durante las primeras 24 h. El seguimiento diario del procedimiento, tanto desde el punto de vista médico como de enfermería y nutrición, fue realizado según nuestra vía clínica6.
Los pacientes fueron revisados en consultas externas de cirugía al primer mes postoperatorio y después, periódicamente, cada 3 meses.
El seguimiento se realizó de forma prospectiva. Se recogieron las siguientes variables: datos sociodemográficos y antecedentes personales, IMC, tipo de técnica quirúrgica, aparición y forma de hemorragia digestiva alta, realización de endoscopia diagnóstica-terapéutica (tipo de procedimiento hemostático), estancia hospitalaria, tasas de reintervención, mortalidad y sus causas. El estudio estadístico es simplemente descriptivo.
ResultadosEntre enero de 2004 y abril de 2013, 300 pacientes fueron intervenidos mediante cirugía bariátrica en nuestro Servicio de Cirugía. Todos los pacientes fueron seguidos durante el periodo de estudio con una media de 89 meses (rango: 3-108 meses). Un paciente falleció por tromboembolismo pulmonar masivo en el postoperatorio inmediato tras reintervención por necrosis parcial del remanente gástrico.
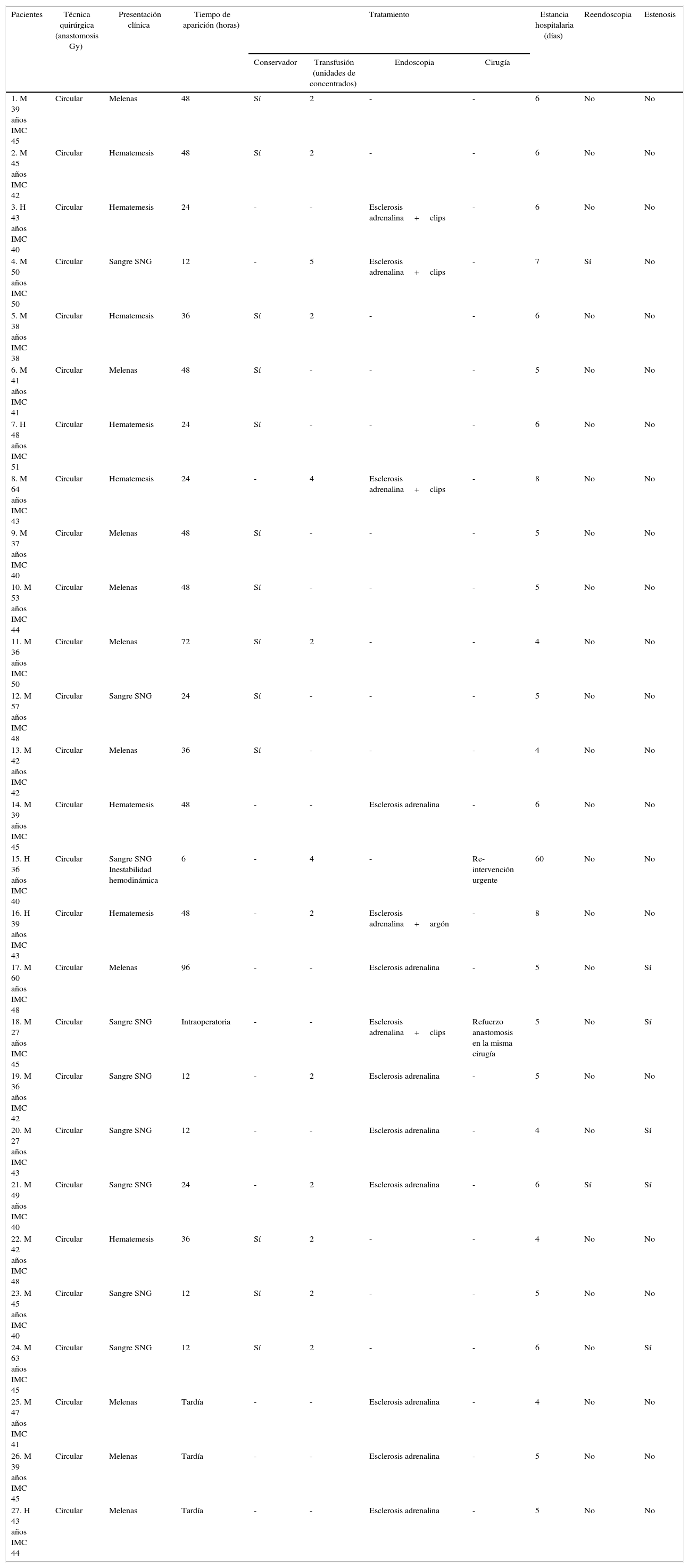
En 27 casos (9%) apareció una hemorragia digestiva alta (tabla 1). La forma de presentación fue de aparición precoz entre el 1.° y 6.° días, en forma de hematemesis o salida de sangre por sonda nasogástrica en 24 pacientes y en 3 de forma tardía, a los 15-20 días en forma de melenas.
Presentación clínica y tratamiento de la hemorragia digestiva tras cirugía bariatrica
| Pacientes | Técnica quirúrgica (anastomosis Gy) | Presentación clínica | Tiempo de aparición (horas) | Tratamiento | Estancia hospitalaria (días) | Reendoscopia | Estenosis | |||
|---|---|---|---|---|---|---|---|---|---|---|
| Conservador | Transfusión (unidades de concentrados) | Endoscopia | Cirugía | |||||||
| 1. M 39 años IMC 45 | Circular | Melenas | 48 | Sí | 2 | - | - | 6 | No | No |
| 2. M 45 años IMC 42 | Circular | Hematemesis | 48 | Sí | 2 | - | - | 6 | No | No |
| 3. H 43 años IMC 40 | Circular | Hematemesis | 24 | - | - | Esclerosis adrenalina+clips | - | 6 | No | No |
| 4. M 50 años IMC 50 | Circular | Sangre SNG | 12 | - | 5 | Esclerosis adrenalina+clips | - | 7 | Sí | No |
| 5. M 38 años IMC 38 | Circular | Hematemesis | 36 | Sí | 2 | - | - | 6 | No | No |
| 6. M 41 años IMC 41 | Circular | Melenas | 48 | Sí | - | - | - | 5 | No | No |
| 7. H 48 años IMC 51 | Circular | Hematemesis | 24 | Sí | - | - | - | 6 | No | No |
| 8. M 64 años IMC 43 | Circular | Hematemesis | 24 | - | 4 | Esclerosis adrenalina+clips | - | 8 | No | No |
| 9. M 37 años IMC 40 | Circular | Melenas | 48 | Sí | - | - | - | 5 | No | No |
| 10. M 53 años IMC 44 | Circular | Melenas | 48 | Sí | - | - | - | 5 | No | No |
| 11. M 36 años IMC 50 | Circular | Melenas | 72 | Sí | 2 | - | - | 4 | No | No |
| 12. M 57 años IMC 48 | Circular | Sangre SNG | 24 | Sí | - | - | - | 5 | No | No |
| 13. M 42 años IMC 42 | Circular | Melenas | 36 | Sí | - | - | - | 4 | No | No |
| 14. M 39 años IMC 45 | Circular | Hematemesis | 48 | - | - | Esclerosis adrenalina | - | 6 | No | No |
| 15. H 36 años IMC 40 | Circular | Sangre SNG Inestabilidad hemodinámica | 6 | - | 4 | - | Re- intervención urgente | 60 | No | No |
| 16. H 39 años IMC 43 | Circular | Hematemesis | 48 | - | 2 | Esclerosis adrenalina+argón | - | 8 | No | No |
| 17. M 60 años IMC 48 | Circular | Melenas | 96 | - | - | Esclerosis adrenalina | - | 5 | No | Sí |
| 18. M 27 años IMC 45 | Circular | Sangre SNG | Intraoperatoria | - | - | Esclerosis adrenalina+clips | Refuerzo anastomosis en la misma cirugía | 5 | No | Sí |
| 19. M 36 años IMC 42 | Circular | Sangre SNG | 12 | - | 2 | Esclerosis adrenalina | - | 5 | No | No |
| 20. M 27 años IMC 43 | Circular | Sangre SNG | 12 | - | - | Esclerosis adrenalina | - | 4 | No | Sí |
| 21. M 49 años IMC 40 | Circular | Sangre SNG | 24 | - | 2 | Esclerosis adrenalina | - | 6 | Sí | Sí |
| 22. M 42 años IMC 48 | Circular | Hematemesis | 36 | Sí | 2 | - | - | 4 | No | No |
| 23. M 45 años IMC 40 | Circular | Sangre SNG | 12 | Sí | 2 | - | - | 5 | No | No |
| 24. M 63 años IMC 45 | Circular | Sangre SNG | 12 | Sí | 2 | - | - | 6 | No | Sí |
| 25. M 47 años IMC 41 | Circular | Melenas | Tardía | - | - | Esclerosis adrenalina | - | 4 | No | No |
| 26. M 39 años IMC 45 | Circular | Melenas | Tardía | - | - | Esclerosis adrenalina | - | 5 | No | No |
| 27. H 43 años IMC 44 | Circular | Melenas | Tardía | - | - | Esclerosis adrenalina | - | 5 | No | No |
IMC: índice de masa corporal (kg/m2); H: hombre; M: mujer; SNG: sonda nasogástrica.
Solo un paciente fue tratado con cirugía directa, por inestabilidad hemodinámica en el postoperatorio inmediato. Inicialmente el abordaje fue laparoscópico, teniendo que reconvertir a laparotomía, donde se rehizo una nueva anastomosis de forma manual. Este paciente desarrolló un postoperatorio tórpido, con ingreso prolongado en la Unidad de Cuidados Intensivos por sepsis del catéter. Los 26 restantes no precisaron reintervención quirúrgica. De estos, en 13 pacientes la hemorragia digestiva alta (de aparición precoz en 10 y tardía en 3) fue lo suficientemente importante para indicar gastroscopia diagnóstica-terapéutica, comprobándose el origen del sangrado en la línea de sutura de la anastomosis GY, y en una úlcera en la boca anastomótica en 3 casos. Todas las endoscopias se realizaron con sedación profunda sin necesidad de intubación endotraqueal, salvo en el caso que se objetivó en el mismo acto quirúrgico, en este caso el manejo endoscópico se realizó simultáneamente con visión directa laparoscópica y se reforzó la sutura con puntos sueltos de seda. En uno de los pacientes no se encontró el origen de la hemorragia tras la gastroscopia por lo que se realizó una enteroscopia doble balón que objetivó una úlcera en el remanente gástrico excluido. A todos ellos se les realizó esclerosis con 2cc de adrenalina al 1/10.000; además, en 4 casos se colocaron endoclips (Resolution Clip, Boston Scientific, Natick, MA, EE. UU.) y en uno, se realizó coagulación con argón. En 6 pacientes hubo que transfundir concentrados de hematíes. Dos de ellos sufrieron recidiva del sangrado y requirieron de nueva gastroscopia terapéutica, al 2.° y 6.° días. En 13 pacientes el manejo fue de forma conservadora con observación, monitorización, control analítico y fluidoterapia, siendo necesaria transfusión de concentrados de hematíes en 7 casos.
En cuanto al tratamiento antitromboembólico, solo se retiró la heparina a 9 pacientes inicialmente, restaurándola tras el procedimiento endoscópico aproximadamente a las 24 h si no existían signos de resangrado ni anemización. Se incentivó la movilización precoz y la deambulación desde el primer día postoperatorio.
La tolerancia oral de la mayoría de los casos fue a las 24 h tras la endoscopia. En un caso de resangrado, se realizó nueva endoscopia sin hallazgos, por lo que se pidió TC abdominal que mostró un cuadro suboclusivo por coágulo intraluminal que se resolvió de forma conservadora, por lo que se demoró la tolerancia 2 días más. En 3 casos la tolerancia se empezó a las 48h tras la prueba.
La estancia media de estos pacientes fue 5,52 días frente a 4,1 días de los pacientes que no desarrollaron esta complicación.
De todos ellos y con posterioridad, 5 pacientes (1,7%) desarrollaron estenosis de la anastomosis GY. En el grupo al que no se le realizó endoscopia diagnóstico-terapéutica aparecieron 15 casos de estenosis (5,3%). En todos estos casos la anastomosis fue circular.
En el seguimiento ambulatorio posterior, todos los pacientes tuvieron tratamiento con heparina y esomeprazol 40 mg/día durante el primer mes. No se realizaron endoscopias de control, salvo en un paciente que a los 2 meses de alta tuvo un episodio de hematemesis con reingreso y endoscopia, siendo diagnosticado de un síndrome de Mallory-Weiss y permanecía en tratamiento con inhibidores de la bomba de protones, y otro paciente que presentó anemia persistente.
DiscusiónLa hemorragia digestiva alta precoz tras realizar un bypass gástrico en Y de Roux presenta una incidencia que oscila entre el 0,6 y el 4%. Supone un serio problema clínico y logístico que conlleva un aumento de la morbilidad y una potencial reintervención5.
Suele presentarse en las primeras 24-48 h del postoperatorio, aunque algunos casos pueden ocurrir pasados unos días. Se manifiesta como hematemesis o melenas o sangre fresca por la sonda nasogástrica. En los casos graves se presenta como taquicardia, hipotensión y descenso de hemoglobina5,7.
Habitualmente se atribuye como sitio probable de sangrado la línea de sutura mecánica de la anastomosis gastroyeyunal e influye la técnica empleada para la realización de la anastomosis. Existen sin embargo muchos lugares probables del origen del sangrado en estos casos como la anastomosis yeyuno-yeyunal o el remanente gástrico. Estudios en los que se compara técnica abierta y laparoscópica han demostrado que la hemorragia digestiva ocurre con más frecuencia en el bypass gástrico laparoscópico que en la cirugía abierta o en otras técnicas de cirugía bariátrica. Lo anterior se atribuye al hecho de que en la cirugía abierta es más frecuente la sutura manual o refuerzo de anastomosis1,7,8.
Se han propuesto distintos métodos de prevención del sangrado en la línea de grapas. Se recomienda el uso de endograpadoras con menor altura (2,5mm) ya que proporcionan mayor compresión de los tejidos y, por tanto, mejor hemostasia. Otros métodos de prevención serían el refuerzo de la anastomosis o el uso de pegamentos biológicos7,8.
El uso de heparinas y clopidogrel se consideran factores predisponentes. Su uso aumenta el riesgo de sangrado postoperatorio, por lo que se recomienda su suspensión si aparece hemorragia digestiva. La obesidad es un factor de riesgo independiente de tromboembolismo venoso. El riesgo de un evento tromboembólico, incluyendo la trombosis venosa profunda o el tromboembolismo pulmonar, está aumentado en pacientes intervenidos mediante cirugía bariátrica1, por lo que se recomienda su administración de forma profiláctica además de medias de compresión neumática y deambulación precoz como medidas preventivas, al igual que realizamos nosotros según nuestra vía clínica6. Tras individualizar cada caso, en nuestra serie se consideró la retirada de la antiagregación en 9 pacientes que, además, requirieron transfusión sanguínea. Se reintrodujo lo antes posible si no existían signos de sangrado o anemización, y se mantetuvo durante el primer mes del postoperatorio.
En cuanto al tratamiento, el manejo inicial consiste en medidas de resucitación, fluidoterapia, transfusión sanguínea, monitorización y establecer la severidad del sangrado que depende de la clínica y el tiempo de presentación. Es importante descartar sangrado extraluminal1,5,9,10. Hematemesis o sangre fresca por el recto sugieren un sangrado activo. Hipotensión, taquicardia, palidez y vasoconstricción requieren reintervención urgente. Si el sangrado es antes de las 6h y va acompañado de descenso de hematocrito también requerirá reintervención, mientras que si la hemorragia se presenta tras 48h sin cambios en hematocrito, no requerirá cirugía5.
No es fácil precisar, con exactitud, el punto de origen del sangrado. La falta de respuesta adecuada al tratamiento médico obliga a realizar algún procedimiento que permita tener una localización y causa del lugar del sangrado y planificar su tratamiento. El seguimiento postoperatorio estrecho y multidisciplinar es muy importante para la detección y tratamiento precoz de las complicaciones6,11. Una endoscopia alta permite realizar una evaluación diagnóstica y tratamiento en casos de sangrado de la bolsa gástrica o de la anastomosis gastroyeyunal y se usa con relativa frecuencia en el sangrado del postoperatorio tardío. Sin embargo, existe controversia en su uso en el postoperatorio inmediato ya que no está exenta de riesgos, dada la sutura reciente de la neobolsa gástrica, por lo que aumenta el riesgo de dehiscencia y perforación. La mayoría de sangrados son leves y limitados y la endoscopia ha de ser considerada cuando hay un resangrado tras el manejo conservador, cuando haya inestabilidad hemodinámica o cuando la caída de hemoglobina ≥ 2 g. A pesar de ello, el tratamiento conservador resuelve la mayoría de sangrados agudos, y es rara la necesidad de reintervención5,12. En los casos en los que no se localice el origen del sangrado, que se sospeche en la yeyunostomía o en el estómago excluido se puede realizar una endoscopia doble balón, con el consenso del equipo y realizada en quirófano con extrema precaución, ya que tiene mayor riesgo de dehiscencia de anastomosis en el postoperatorio inmediato13,14. En nuestra serie un paciente se benefició de esta técnica, que pudo localizar como origen del sangrado una úlcera en el estómago excluido.
La hemostasia se realizó con inyección de epinefrina en todos los casos, asociada en 4 de ellos al uso de clip y en uno a cauterización con argón. Con una tasa de resangrado del 7,4% (2 pacientes). Uno de los pacientes requirió tratamiento quirúrgico urgente por inestabilidad hemodinámica. A medio-largo plazo estas técnicas de hemostasia pueden favorecer la estenosis gastroyeyunal, que apareció en 5 de nuestros pacientes (1,7%) y necesitaron dilatación endoscópica posterior. La esclerosis endoscópica podría ser un factor de riesgo para la estenosis posterior como consecuencia de la reacción inflamatoria-cicatricial secundaria. Esta asociación no ha sido descrita en la literatura y serían necesarios más estudios para llegar a sólidas conclusiones. En el grupo al que no se le realizó endoscopia, fueron 15 pacientes con estenosis (5,3%). En todos los casos la anastomosis fue mecánica circular.
Algunos estudios prefieren el uso de endoclips cuando sean técnicamente accesibles ya que, a diferencia de las inyecciones esclerosantes o la coagulación térmica, los endoclips no producen daño adicional del tejido y pueden usarse concomitantemente para el tratamiento de fugas anastomóticas o perforaciones iatrogénicas y pueden reducir el riesgo de estenosis de la anastomosis gastroyeyunal15–19.
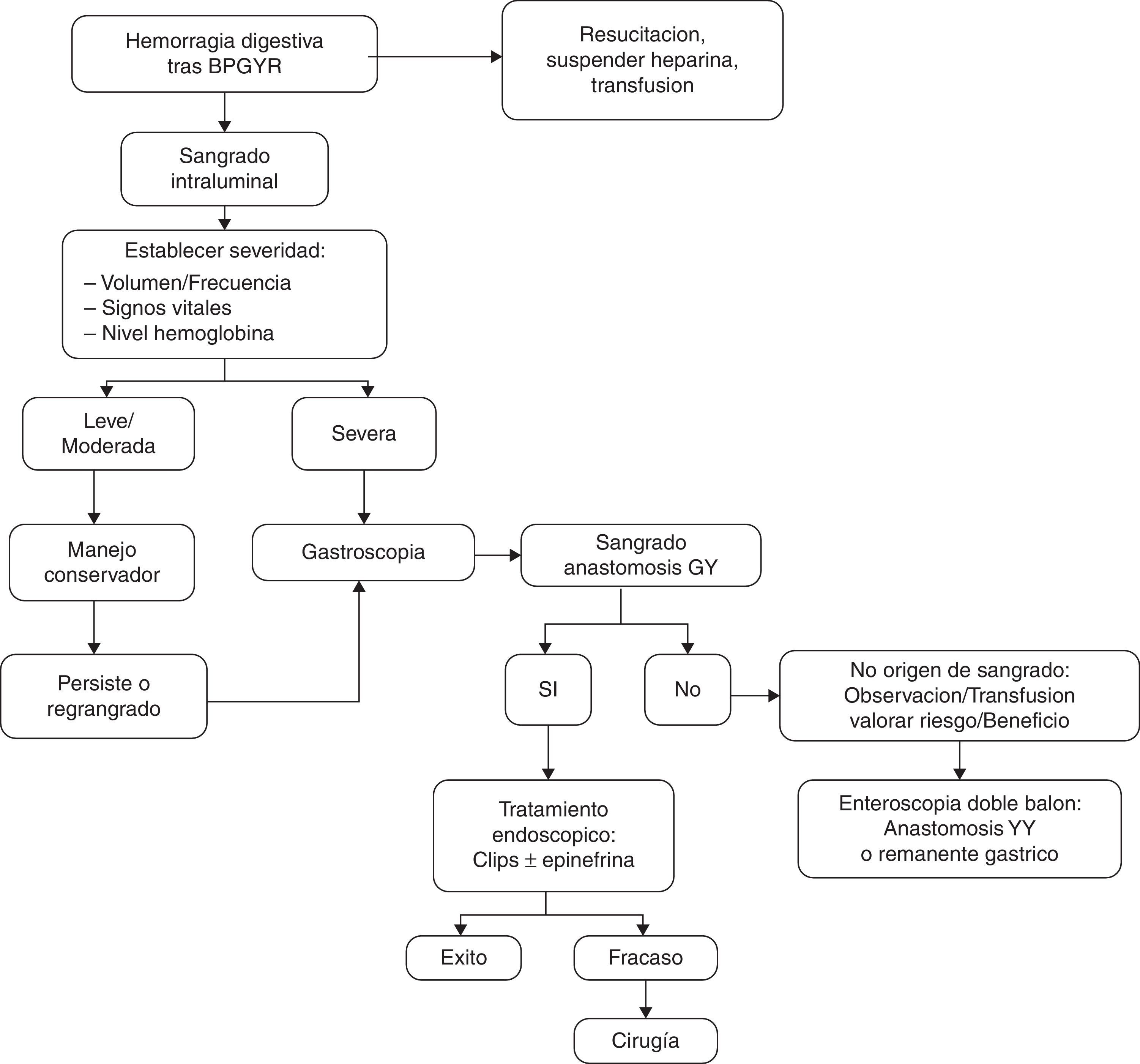
En el manejo de la hemorragia digestiva proponemos el algoritmo de la fig. 1. La gastroscopia urgente debe ser recomendada y realizada por endoscopistas experimentados en técnicas hemostáticas, especialmente en uso de endoclips. La revisión por endoscopia con mínima insuflación de aire durante la endoscopia, rápida y con precaución, se recomienda en estos casos5.
La estancia media de estos pacientes fue 5,52 días, ligeramente superior a los pacientes que no desarrollaron esta complicación (4,1 días).
La tolerancia oral no se demora cuando aparece este tipo de complicación, se suele comenzar antes de las primeras 24 h tras el procedimiento endoscópico.
En cuanto al seguimiento en consulta, no se recomiendan endoscopias de control sistemáticamente, solo en el caso de anemia persistente o clínica de sangrado, como ocurrió en 2 de nuestros casos. El uso de inhibidores de la bomba de protones se recomienda durante los 2 primeros meses.
Como conclusión, la hemorragia digestiva alta es una complicación frecuente tras bypass gástrico laparoscópico. El origen más común es la anastomosis gastroyeyunal. Existen, sin embargo, muchos lugares probables de origen del sangrado en estos casos por lo que una endoscopia permite realizar una evaluación diagnóstica y fijar un tratamiento. Aunque el manejo conservador expectante resuelve la mayoría de los casos, la clínica y la forma de presentación deben alertarnos, por lo que en casos graves de sangrado se requerirá de una endoscopia urgente. Sin embargo, no está exenta de riesgos en el postoperatorio inmediato, dada la sutura reciente de la neobolsa gástrica, ni a mediano-largo plazo, como la estenosis gastroyeyunal, por lo que es importante un equipo multidisciplinar y una comunicación estrecha entre cirujanos y endoscopistas para el manejo de esta seria complicación.
FinanciaciónArtículo financiado en parte por la Fundación para la Formación e Investigación Sanitaria (FFIS) de la Región de Murcia, España, Group FFIS-008.
Conflicto de interesesLos autores declaramos que no hay ningún conflicto de interés.