Este artículo pretende realizar una breve revisión de los principales conceptos en los que se basan las medidas de prevención y control de la infección. La antisepsia comprende el conjunto de técnicas destinadas a la eliminación total (esterilización) o mayoritaria (desinfección) de los gérmenes que contaminan un medio. Ambos procedimientos deben ir precedidos de una limpieza del medio donde se vayan a aplicar.
La desinfección se lleva a cabo por medio de biocidas o germicidas, sustancias químicas antimicrobianas cuyos mecanismos de acción y resistencia son muy similares a los de los antibióticos. Esta similitud está generando inquietud por la posibilidad de cruce de información genética que agrave el problema de las resistencias bacterianas. La mayoría de los biocidas pueden actuar como antisépticos, aplicados sobre piel y tejidos, o desinfectantes, sobre materiales inanimados. El espectro de acción de los germicidas depende de las características propias del producto y de factores externos controlables: temperatura, concentración, tiempo de exposición, etc.
Las técnicas de esterilización son fundamentalmente de carácter físico, a través de autoclaves que exponen el material a vapor o gas esterilizante. Los mayores avances están en las exposiciones a bajas temperaturas con tiempos más cortos de exposición, en paralelo con los avances tecnológicos de instrumentación con materiales que no soportan temperaturas elevadas y con rotaciones de uso altas, por la presión asistencial.
This article aims to provide a brief review of the main concepts on which the prevention and control of infection are based. Antisepsis comprises a set of techniques aimed at the total sterilization, or at most, disinfection, removing germs that contaminate an environment. Both procedures must be preceded by an environmental cleanup in the location in which they intend to be applied.
The disinfection is carried out using biocides or germicides. Antimicrobial chemicals, that have mechanisms of action and resistances very similar to antibiotics, are generating concern due to the possibility of crossing genetic information that aggravates the problem of bacterial resistance. Most biocides can act as antiseptics, and applied to skin tissue, or disinfectants on inanimate materials. The spectrum of action of germicides depends on the product itself and external controllable factors: temperature, concentration, exposure time, etc.
Sterilization techniques are primarily physical, by exposing the material to steam, or sterilizing gas, using autoclaves. Major advances are the use of low temperatures with shorter exposure times, in parallel with technological advances in instrumentation in order to avoid high temperatures and high use rotations due to workload.
Históricamente la prevención y el control de las enfermedades transmisibles estaban íntimamente unidos a procedimientos como el salazón, el ahumado, la ebullición, etc., incluso sin comprender los mecanismos por los cuales estas actividades evitaban la transmisión de infecciones. Con el descubrimiento de los microbios se comprendieron la causa de las enfermedades infecciosas y sus mecanismos de transmisión, y de forma paulatina fueron surgiendo nuevos métodos para impedir dicha transferencia. El cirujano inglés Joseph Lister fue el primero en percatarse de la importancia de la asepsia en el ámbito quirúrgico, y desarrolló por primera vez la idea de prevenir las infecciones de herida quirúrgica con el uso de métodos antisépticos1.
El concepto de asepsia hace referencia a la utilización de procedimientos que impidan el acceso de microorganismos patógenos a un medio libre de ellos, por ejemplo mediante el lavado de manos, la instauración de técnicas de barrera o la limpieza habitual. Antisepsia es el conjunto de procedimientos o actividades destinados a inhibir o destruir los microorganismos potencialmente patógenos. Para la implementación de la antisepsia se usan los biocidas, tanto en piel y tejido humanos (antisépticos) como en objetos, superficies o ambiente (desinfectantes). La revolución terapéutica que supuso el descubrimiento de los antibióticos hizo que los biocidas pasaran a un segundo plano. La emergencia del grave problema de la multirresistencia bacteriana, que nos sitúa en una «era preantibiótica», hizo que volvieran a adquirir importancia.
La esterilización, otra piedra angular de la antisepsia, tiene como objetivo la eliminación de cualquier microorganismo, nocivo o no.
BiocidasBiocidas son aquellas sustancias que por medios bien químicos o bien biológicos pueden destruir, contrarrestar, neutralizar, impedir la acción o ejercer un efecto de control sobre cualquier organismo nocivo2. Recientemente se ha propuesto una definición más simple y clara según la cual un biocida es una molécula química activa en un producto para inhibir o destruir bacterias. La actividad antimicrobiana es el efecto letal o inhibitorio, tanto de un producto biocida como de un antibiótico3.
La evaluación de la actividad antimicrobiana ofrece dificultad por el amplio número de ensayos disponibles para evaluar la eficacia de los biocidas y por la ausencia de consenso para la estandarización de métodos para algunas fases de los estudios. En Europa, el European Committee for Standardization (CEN) creó el comité técnico 216 (TC216) para la estandarización de las pruebas de evaluación de eficacia de los antisépticos y desinfectantes4. Los países miembros deben adaptar sus estándares nacionales, las normas UNE-EN en el caso de España, a las normas europeas. A pesar de los intentos de armonización, existen lagunas; por ejemplo, actualmente no hay normas europeas para el ensayo de desinfectantes contra biofilms para aplicaciones de cuidado de la salud3.
Los biocidas de uso sanitario deben atenerse a la legislación aplicable en cada país. En España los desinfectantes que se utilizan específicamente con los dispositivos médicos se consideran productos sanitarios clase IIA y deben llevar el marcado CE5, precisando la intervención de un organismo notificado que inspeccione y verifique la calidad del producto antes de otorgarle la marca CE. Los desinfectantes de ambientes y superficies, así como los antisépticos para piel sana o intacta utilizados en los ámbitos clínicos o quirúrgicos, no se consideran producto sanitario, pero requieren autorización sanitaria como desinfectantes otorgada por la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) y deberán exhibir en su etiquetado el número de autorización «n.°-DES» que corresponda a dicha autorización. Los desinfectantes destinados a aplicarse sobre heridas, mucosas o piel dañada son considerados especialidades farmacéuticas y deben poseer la correspondiente autorización de comercialización como medicamento otorgada por la AEMPS.
Espectro y mecanismo de acciónLos mecanismos de acción de los biocidas se centran en alterar la estructura del microorganismo, bien sea impidiendo la entrada y salida de elementos vitales para el microorganismo o alterando estructuras. Las dianas se sitúan en la pared celular, en la membrana citoplasmática o en el citoplasma6.
Para la selección de un biocida hay que tener en consideración diversos factores del biocida, del germen y de la exposición, ya que de ellos dependerá su efectividad (tabla 1). La concentración del biocida y el tiempo de contacto son cruciales, y su efecto combinado se determina con el parámetro CT (contact time), que se expresa como mg·min/l y determina cómo afecta un desinfectante a un tipo de microorganismo y bajo unas condiciones específicas. El CT se utiliza para comparar la efectividad de diferentes biocidas. Otros factores importantes son la estabilidad de los compuestos activos de los biocidas en el medio ambiente, la temperatura del medio ambiente (a temperaturas bajas la efectividad es menor) o la presencia de sustancias interferentes, como proteínas o materia orgánica, así como la presencia de biofilms3,7.
Factores que influyen en las interacciones entre biocida y germen
| Factores que determinan la efectividad de un biocida | ||
| Dependientes del biocida | Dependientes de la exposición | Dependientes del germen |
| • Composición química• Concentración• Modo de acción | • Tiempo• Temperatura• pH• Sustancias interferentes | • Concentración de los microorganismos en la mezcla de reacción• Grado de agregación• Tamaño del germen• Afinidad por lípidos |
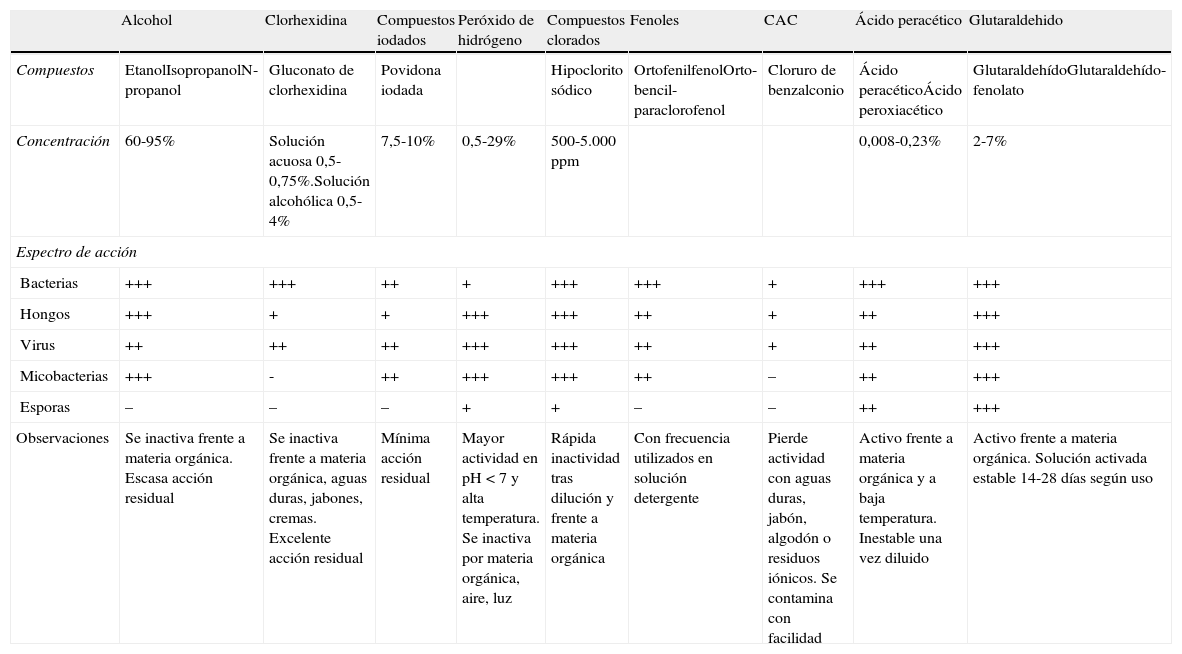
En la tabla 2 se muestran las características más destacables de los biocidas más frecuentemente usados como antisépticos y/o desinfectantes.
Características de los biocidas más frecuentemente utilizados
| Alcohol | Clorhexidina | Compuestos iodados | Peróxido de hidrógeno | Compuestos clorados | Fenoles | CAC | Ácido peracético | Glutaraldehido | |
| Compuestos | EtanolIsopropanolN-propanol | Gluconato de clorhexidina | Povidona iodada | Hipoclorito sódico | OrtofenilfenolOrto-bencil-paraclorofenol | Cloruro de benzalconio | Ácido peracéticoÁcido peroxiacético | GlutaraldehídoGlutaraldehído-fenolato | |
| Concentración | 60-95% | Solución acuosa 0,5-0,75%.Solución alcohólica 0,5-4% | 7,5-10% | 0,5-29% | 500-5.000ppm | 0,008-0,23% | 2-7% | ||
| Espectro de acción | |||||||||
| Bacterias | +++ | +++ | ++ | + | +++ | +++ | + | +++ | +++ |
| Hongos | +++ | + | + | +++ | +++ | ++ | + | ++ | +++ |
| Virus | ++ | ++ | ++ | +++ | +++ | ++ | + | ++ | +++ |
| Micobacterias | +++ | - | ++ | +++ | +++ | ++ | – | ++ | +++ |
| Esporas | – | – | – | + | + | – | – | ++ | +++ |
| Observaciones | Se inactiva frente a materia orgánica. Escasa acción residual | Se inactiva frente a materia orgánica, aguas duras, jabones, cremas. Excelente acción residual | Mínima acción residual | Mayor actividad en pH<7 y alta temperatura. Se inactiva por materia orgánica, aire, luz | Rápida inactividad tras dilución y frente a materia orgánica | Con frecuencia utilizados en solución detergente | Pierde actividad con aguas duras, jabón, algodón o residuos iónicos. Se contamina con facilidad | Activo frente a materia orgánica y a baja temperatura. Inestable una vez diluido | Activo frente a materia orgánica. Solución activada estable 14-28 días según uso |
CAC: Compuestos de amonios cuaternarios.
El interés por las resistencias bacterianas a los biocidas es proporcional al incremento de uso de estos productos ante la emergencia de las resistencias bacterianas a antimicrobianos. Los primeros estudios que hicieron referencia a esta problemática describían situaciones de emergencia de resistencias bacterianas a los biocidas como resultado de un mal uso o defectuoso almacenamiento (y posterior contaminación) de los mismos8,9. Estudios más recientes han descrito la falta de efectividad de los biocidas utilizados en hospitales sobre aquellos microorganismos que crecen y se multiplican en los biofilms de superficies y dispositivos médicos, lo que conlleva un fracaso en el control de estos reservorios para la prevención de infecciones relacionadas con la asistencia sanitaria (IRAS)10,11. De cualquier forma, la mayor parte de la evidencia sobre resistencia a los biocidas proviene de los ensayos de laboratorio.
La concentración de los biocidas es considerado el factor más relevante para la definición de resistencia bacteriana a los mismos. Muchos de los estudios sobre resistencia a biocidas basan sus hallazgos en la concentración mínima inhibitoria (CMI). El uso de este parámetro para dicho objetivo es discutible, ya que en la práctica se utilizan concentraciones mucho más elevadas y es improbable que no se logre una reducción del número de bacterias como resultado de una elevada CMI. Por ello actualmente se considera la concentración bactericida mínima (CBM) como el mejor parámetro de resultado de eficacia de un biocida, ya que permite comparar la letalidad entre una cepa estándar y la estudiada. Por otra parte, la determinación de la letalidad de un biocida con la concentración de uso indicará si la cepa bacteriana es o no susceptible (resistencia intrínseca o natural) o resistente al compararla con el estándar3.
El tándem resistencias bacterianas y biocidas tiene 2 vertientes definidas; por una parte, la resistencia bacteriana a las sustancias químicas biocidas, y por otra, el papel del biocida en la inducción de resistencia bacteriana a antibióticos.
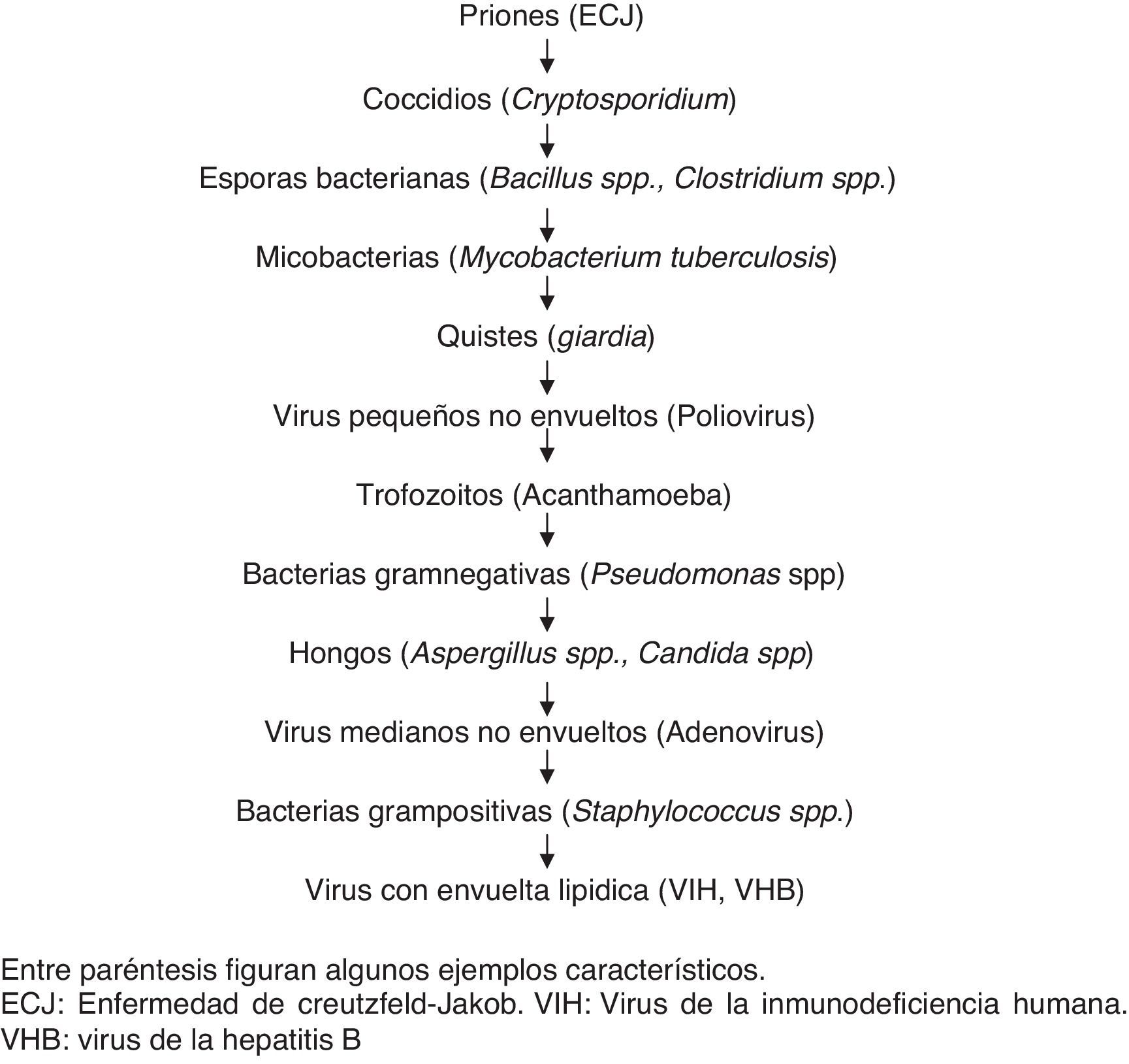
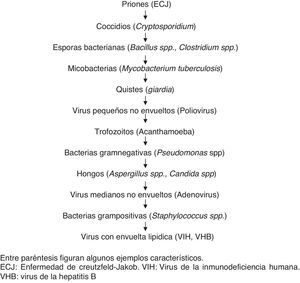
La resistencia de un microorganismo a un determinado biocida puede ser una propiedad natural (intrínseca o innata), y entonces se habla de no susceptibilidad, o una resistencia adquirida. En términos globales, el mecanismo de resistencia innata más frecuentemente descrito reside en las características de la membrana celular; la naturaleza y la composición de la misma dependen del tipo de organismo y puede actuar como una barrera en la que puede haber una absorción reducida. Esta circunstancia puede tener relevancia práctica en esporas bacterianas, en concreto de algunas especies como el Clostridium difficile3,6,12,13. En la figura 1 se muestran diferentes microorganismos ordenados en función de su nivel de resistencia natural a los desinfectantes.
Principales agentes causales de enfermedades infecciosas en orden decreciente de resistencia a los desinfectantes. Entre paréntesis figuran algunos ejemplos característicos.
ECJ: enfermedad de Creutzfeld-Jakob. VHB: virus de la hepatitis B. VIH: virus de la inmunodeficiencia humana.
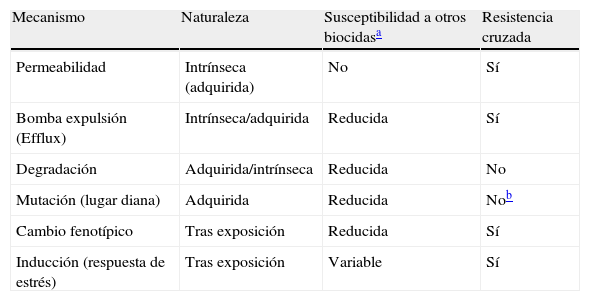
Como en los antibióticos, la resistencia también puede ser adquirida, y los mecanismos en ambos casos son muy semejantes. Puede surgir por mutación o por la adquisición de material genético en forma de plásmidos o transposones. Aunque la adquisición de genes de resistencia ha sido documentada, la información disponible sobre el efecto de los biocidas en la transferencia de los determinantes genéticos es escasa y a veces con resultados opuestos según el biocida estudiado. Por ejemplo, al estudiar el efecto del uso de biocidas a concentraciones subinhibitorias el resultado en unos casos puede ser inhibitorio y en otros potenciador sobre la transferencia de resistencia3,14. La tabla 3 resume los principales mecanismos bacterianos de resistencia a los biocidas.
Mecanismos bacterianos de resistencia a los biocidas
| Mecanismo | Naturaleza | Susceptibilidad a otros biocidasa | Resistencia cruzada |
| Permeabilidad | Intrínseca (adquirida) | No | Sí |
| Bomba expulsión (Efflux) | Intrínseca/adquirida | Reducida | Sí |
| Degradación | Adquirida/intrínseca | Reducida | No |
| Mutación (lugar diana) | Adquirida | Reducida | Nob |
| Cambio fenotípico | Tras exposición | Reducida | Sí |
| Inducción (respuesta de estrés) | Tras exposición | Variable | Sí |
Fuente: SCENIHR Assessment of the Antibiotic Resistance Effects of Biocides 2009.
Otro punto de interés es la resistencia cruzada entre biocidas y antibióticos. El proyecto «Confronting the clinical relevance of biocide induced antibiotic resistance» (BIOHYPO), financiado con fondos europeos, investigó la asociación entre el uso extendido de biocidas y la resistencia a antibióticos en patógenos humanos. Para ello, se analizaron 4 biocidas sobre patógenos humanos: cloruro de benzalconio, clorhexidina, triclosán e hipoclorito sódico. Estas pruebas han determinado los puntos de corte ecológico (ECOFF) de CMI y CBM de los biocidas14-16. En líneas generales, y excepto en casos muy puntuales, no se ha observado una relación significativa entre la baja sensibilidad de los patógenos a los biocidas y la resistencia a antibióticos. No obstante, los investigadores prevén cambios en un futuro y será imprescindible estar alerta al progreso de la evidencia disponible15,16.
Desde un punto de vista práctico, aunque la resistencia bacteriana se ha descrito en casi todos los biocidas, la repercusión clínica se considera irrelevante, apoyados en el hecho de que las concentraciones usadas en la práctica son sustancialmente superiores a las CMI de las cepas con susceptibilidad reducida3,16–18.
Antisepsia sobre piel, mucosas y tejidosLos antisépticos son una de las armas más poderosas en el control de la infección. La disponibilidad de los mismos está limitada por la toxicidad de algunos o por la fácil contaminación de otros. Los antisépticos más frecuentes en cuidados sanitarios son la clorhexidina, el alcohol y la povidona iodada. La selección de uno u otro, así como la concentración y solución, dependerán del objetivo de aplicación.
Piel intactaLa povidona iodada como tal carece de actividad hasta que se va liberando el iodo, verdadero agente de la actividad antiséptica. Se utiliza a concentraciones del 1, 7,5 y 10%, puede causar hipersensibilidad en algunas personas con alergia al iodo y no debe usarse en embarazadas, neonatos o personas con bocio. La clorhexidina actúa rápidamente y posee gran actividad bactericida. Se aplica a una concentración de 0,5%. El alcohol al 70% es un bactericida de acción rápida, llegando a eliminar el 90% de las bacterias de la piel en 2min si se permite secar al aire; el frotado con algodón destruye un máximo del 75%19.
En los últimos años ha surgido una amplia producción científica, en general con resultados favorables a la clorhexidina, aunque muchos de ellos esconden una sobrevaloración del alcohol incorporado a la solución20,21. En general, cuando se requiere un efecto prolongado se prefiere la clorhexidina, y cuando se busca un efecto inmediato, mejor povidona iodada22. El paquete de medidas (bundle) descrito por el Institute for Healthcare Improvement (IHI) para la prevención de las infecciones relacionadas con catéter establece la recomendación de antisepsia del sitio de inserción con clorhexidina al 2% en solución alcohólica. Otras guías son menos restrictivas en la recomendación, considerando que cuando el catéter es venoso periférico puede usarse con la misma eficacia cualquiera de los 3 antisépticos, y en los catéteres venosos centrales o arteriales periféricos hay que usar clorhexidina alcohólica en concentración superior al 0,5%23,24. De los estudios sobre preparación de piel para la incisión quirúrgica no parece desprenderse ningún resultado concluyente sobre la superioridad de un antiséptico sobre otro, aunque sí parece apreciarse una ventaja en la utilización de antisépticos en solución alcohólica, incluso a concentraciones elevadas21,25,26. El uso de estas soluciones debe recibir una correcta aplicación, ya que son inflamables y pueden dar lugar a eventos adversos con dispositivos eléctricos. Respecto a la ducha o baño previo a la intervención, como prevención de infecciones del sitio quirúrgico, los resultados no encuentran diferencias entre antisépticos, e incluso entre estos y el empleo de agua y jabón neutro27. Entre las medidas para el control de epidemias por Staphylococcus aureus resistente a meticilina (SARM) y de Enterococcus sp. resistente a vancomicina (ERV) en instituciones sanitarias, se describió la utilidad del uso de descolonización con higiene corporal con solución jabonosa de clorhexidina al 2%28, y la recomendación se ha extendido a otros gérmenes multirresistentes (GMR)29.
Piel no intactaEn general, sobre las heridas no se aconseja el uso de antisépticos por ser citotóxicos, retrasar la curación y ser más perjudiciales que beneficiosos cuando no se usan en las concentraciones apropiadas. Sin embargo, el uso de antisépticos a concentraciones adecuadas es efectivo y bien tolerado, recomendando su cese de uso cuando los primeros signos clínicos de mejoría comienzan a detectarse. Como recomendación general, las soluciones empleadas son las acuosas. La povidona iodada es a concentraciones del 2,5%, o del 10% si es en apósitos impregnados. En la clorhexidina para descontaminación, la concentración es del 0,5%. En un reciente estudio sobre úlceras venosas crónicas la única evidencia disponible propone el uso de cadexómero yodado al 0,9%, que es un producto consistente en la unión de un dextranómero, agente potenciador del desbridamiento químico, e iodo30. Algunos gérmenes que actualmente invaden nuestras instituciones, como Pseudomonas sp., con perfiles de resistencia cada vez más amplios y que por otra parte son causa frecuente de colonización e infección de heridas, pueden verse beneficiados de alternativas antisépticas no muy comunes, como el ácido acético en concentraciones iguales o superiores al 0,5% en solución salina para irrigación o sobre compresa empapada31.
MucosasSobre mucosas, 2 indicaciones básicas. La higiene oral con clorhexidina al 0,12% o al 0,2% disminuye la incidencia de neumonía asociada a ventilador32, por lo que ha entrado a formar parte básica de los bundles de prevención con diana en este tipo de infección. Otra aplicación es la preparación vaginal antes de una cesárea con soluciones de povidona iodada que reduce el riesgo de endometritis posterior33.
Desinfección sobre instrumental, superficies y ambienteLa limpieza, como paso previo cronológicamente a la desinfección, constituye un factor de importancia prioritaria. Una limpieza incorrecta o defectuosa repercutirá de forma negativa en las sucesivas etapas del proceso de antisepsia/desinfección o esterilización. El proceso de desinfección, a diferencia de la esterilización, solo es capaz de eliminar la mayor parte de los gérmenes patógenos (pero no todos). Además, por las características del procedimiento, el material desinfectado pierde rápidamente esta propiedad por carecer del factor de empaquetado que lo proteja de contaminaciones. El espectro de gérmenes sobre los que es efectivo un desinfectante varía de uno a otro, o en un mismo desinfectante en dependencia de sus concentraciones y su tiempo de exposición. Según el nivel de cobertura alcanzado por un desinfectante, se puede clasificar como de nivel alto cuando incluye esporas bacterianas, de nivel intermedio cuando incluye micobacterias pero no esporas, o de nivel bajo cuando no incluye ni micobacterias ni esporas7.
Los criterios de elección de procesado del material de uso sanitario con desinfección, en sus diferentes niveles, o con esterilización, lo esquematizó Spaulding en 1968, y permanece en vigor la clasificación que realizó de dispositivos, según el nivel de riesgo que dichos materiales tuviesen de desarrollar infección7,34. Las 3 categorías que describió son:
- •
Crítico: todo material contaminado por cualquier germen que tenga un alto riesgo de desarrollar infección. Incluye todo material que entra en contacto con cavidades estériles o sistema vascular.
- •
Semicrítico: material que entra en contacto con mucosas o piel no intacta. Estos dispositivos deberían estar libres de microorganismos, aunque pueden estar permitido un pequeño número de esporas bacterianas, ya que las membranas mucosas (pulmonar, gastrointestinal, etc.) tienen generalmente resistencia a la infección por esporas bacterianas comunes.
- •
No crítico: material que se utiliza sobre piel intacta.
El material crítico debe ser sometido a esterilización antes de su uso.
El material semicrítico debe ser sometido a desinfección de alto nivel antes de su uso. Es en la práctica el de mayor riesgo, ya que con ellos se han detectado más infecciones asociadas a cuidados sanitarios que con los críticos o no críticos. Los primeros porque se les somete a esterilización, y los segundos por su escaso riesgo intrínseco. El glutaraldehído, el peróxido de hidrógeno, el ortofenilaldehído (OPA), el ácido peracético, el peróxido de hidrógeno y el cloro son considerados desinfectantes de alto nivel. El reprocesado de material sanitario semicrítico para su desinfección tiene lugar a través de contacto con líquido desinfectante y puede ser manual o automático. El tiempo de contacto oscila entre 8 y 45min a temperaturas entre 20 y 25°C. El reprocesado automático mediante máquinas desinfectadoras minimiza los errores humanos, evita contacto de los profesionales con sustancias tóxicas y no requiere de sistemas de ventilación especiales35,36.
Dentro de la categoría de material semicrítico, mención especial merece el procesado del material endoscópico. Los endoscopios flexibles, por el tipo de cavidad en la que penetran, adquieren alta carga microbiana, y aunque se han publicado numerosas guías y recomendaciones para el reprocesado de endoscopios, la adherencia a las mismas tiene importantes áreas de mejora. En este contexto ha adquirido mucha relevancia la introducción de nueva tecnología, tanto en los desinfectantes como en las mejoras de los procesadores automáticos. Sobre estos últimos, todos los modelos tienen ciclos de desinfección y aclarado, y algunos también limpieza con detergente, vaporización de alcohol y/o ciclos de secado forzado con aire; no obstante, no todos son compatibles con todos los desinfectantes de alto nivel o con todos los fabricantes de endoscopios del mercado, por lo que en la selección habrá que tenerlo en cuenta. Por la repercusión que los procedimientos con este tipo de material endoscópico tienen en la seguridad del paciente, está muy debatida actualmente la necesidad de controles microbiológicos en la monitorización de este material. Un método de control nuevo es el basado en la bioluminiscencia de adenosín-trifosfato (ATP) para la monitorización de la limpieza, principal causa de fallo del proceso efectivo de desinfección36–38.
El material no crítico, a diferencia del material crítico y semicrítico, requiere desinfección de nivel medio o bajo. Aunque en sí mismo no supone un riesgo, pueden actuar como fómite en la transmisión, por contaminación a través de manos o piel colonizada. Los productos más frecuentemente usados como desinfectantes de nivel medio son los fenoles y los compuestos de cloro con un tiempo de contacto de al menos un minuto. Entre los de nivel bajo, encontramos añadidos a los anteriores los compuestos de amonio cuaternarios, con el mismo tiempo de contacto recomendado35,36.
SuperficiesEl papel de las superficies contaminadas está teniendo un creciente protagonismo con la emergencia de los GMR. La persistencia de estos organismos en objetos y materiales del entorno del paciente ha conllevado el rescate de la limpieza y desinfección de las mismas como uno de los mecanismos de control y prevención básicos en la transmisión de infecciones por GMR. En la mayoría de los casos el biocida más eficaz es el hipoclorito sódico a concentraciones de 1.000ppm39,40.
AmbienteAl igual que en las superficies, la emergencia de GMR y su demostrada persistencia en el medio ambiente han supuesto una actualización de métodos desechados hace tiempo, como por ejemplo la fumigación de habitaciones. La tecnología ha modernizado la vaporización ambiental de un desinfectante, en este caso el peróxido de hidrógeno, más inocuo que los usados tiempo atrás. Se ha demostrado efectivo para Staphylococcus aureus resistente a meticilina, Clostridium difficile, Serratia sp., Acinetobacter sp. y otros34,41.
EsterilizaciónLa esterilización se define como el proceso mediante el cual se destruyen todos los microorganismos viables presentes en un objeto o superficie, incluidas las esporas bacterianas. El concepto de esterilidad expresa una condición absoluta: un determinado objeto o superficie está estéril o no está estéril. Puesto que la esterilidad no puede demostrarse de manera absoluta sin causar la destrucción completa de todas las unidades esterilizadas, se define la esterilidad en términos probabilísticas y se considera que un producto crítico es estéril cuando la probabilidad de que una unidad estéril contenga algún microorganismo en forma activa o latente es igual o menor de 1 entre un millón (SAL [sterility assurance level] o coeficiente de seguridad de esterilidad de 10−6)42.
El paso previo e imprescindible para una correcta esterilización es la limpieza exhaustiva del material a esterilizar. A través de un proceso mecánico se elimina, por arrastre, la suciedad visible y la materia orgánica de una superficie u objeto, reduciendo el número de microorganismos y protegiendo los instrumentos contra la corrosión y el desgaste.
El empaquetado tiene como objetivo mantener el instrumental aislado de toda fuente de contaminación, conservando la esterilidad conseguida en el proceso de esterilización. El embalaje debe ser adecuado para permitir la penetración del agente esterilizante según el método de esterilización escogido, en función de las características y el uso que se vaya a dar a los materiales a esterilizar y del tiempo de esterilidad requerido43.
Esterilización de dispositivos médicos y quirúrgicosAunque una gran mayoría de los dispositivos médicos y quirúrgicos utilizados en el ámbito sanitario son resistentes al calor, desde los años cincuenta ha habido una tendencia creciente a utilizar dispositivos médicos e instrumental quirúrgico fabricados con materiales sensibles al calor, lo que ha hecho necesario desarrollar tecnologías de esterilización a baja temperatura como son el óxido de etileno, el plasma o el vapor de peróxido de hidrógeno, el ozono, etc.7.
La elección de un método u otro de esterilización no es arbitraria, sino que según el RD 1591/2009 el fabricante debe especificar en ficha técnica si un determinado material es o no reprocesable, así como el método y las condiciones para el correcto reprocesamiento del mismo.
En la tabla 4 se refieren los distintos métodos de esterilización más ampliamente utilizados en el ámbito hospitalario, con sus ventajas e inconvenientes44.
Ventajas e inconvenientes de los diferentes métodos de esterilización
| Método esterilización | Ventajas | Inconvenientes |
| Vapor | No tóxico para paciente, personal o medio ambienteCiclo fácilmente monitorizableRápido efecto microbiocidaSistema menos afectado por los restos orgánicos o inorgánicosRapidez del cicloMuy buena penetración en empaquetados médicos y en dispositivos con lúmenes | No apto para material termosensiblePor la exposición repetida puede dañar el material (p.ej., algún instrumentos de microcirugía)Puede dejar instrumental húmedo, con el riesgo de oxidación del mismoPosibilidad de quemaduras |
| Peróxido de hidrógeno gas plasma | Seguro para el medio ambiente, no deja residuos tóxicos y no precisa aireaciónPermite esterilizar material sensible a temperatura (<50°C) y humedad, tanto metálicos como no metálicosDuración del ciclo estándar 47minFacilidad de manejar y monitorizar los ciclosInstalación simple, solo precisa toma eléctricaCompatible con gran cantidad de instrumental y dispositivos médicos | No permite procesar celulosa, tela o líquidosLimitaciones para procesar dispositivos en función del diámetro de la luz y la longitudMuy sensible a la presencia de humedad en la cámaraRequiere envolturas Tyvek y contenedores especialesEl peróxido de hidrógeno puede ser tóxico a niveles mayores de 1ppm TWA |
| Peróxido de hidrógeno vapor | Seguro para trabajadores y el medio ambienteNo deja residuos tóxicos y no precisa aireaciónDuración del ciclo 28min (ciclo sin lúmenes), 55min (ciclo con lúmenes)Permite esterilizar material sensible a temperatura (<50°C) y humedadFacilidad de manejar y monitorizar los ciclosFácil instalación | No permite procesar celulosa, tela o líquidosLimitaciones para procesar dispositivos en función del diámetro de la luz y la longitud (p.ej., lúmenes de acero inoxidable de <de 1mm de diámetro o más de 125mm de longitud).Precisa catalizadorRequiere envolturas Tyvek y contenedores especialesEl peróxido de hidrógeno puede ser tóxico a niveles mayores de 1ppm TWA |
| Óxido de etileno | Alta eficacia microbiocidaBuena difusión y penetrabilidad en embalajes y lúmenesEl uso de cartuchos individuales y cámaras de presión negativa minimiza la posibilidad de fuga y exposición a OEFacilidad de manejar y monitorizar los ciclosCompatible con gran cantidad de instrumental y dispositivos médicos | El envasado puede realizarse en bolsa de papel mixto y en bolsa de papel Tyvek y contenedores especialesEs absorbido por muchos materiales y requiere un tiempo de aireación para eliminar los residuos del OELimitaciones dependiendo de la longitud y del diámetro de la luz, presencia de sales inorgánicas o materia orgánicaOE es tóxico, carcinogénico, inflamablePrecisa usar catalizadores para transformar el residuo en CO2 y H2OLos cartuchos deben guardarse en armarios para líquidos inflamablesDuración del cicloIncompatibilidad con algunos metales (p.ej., Al, Sn, Mg, Zn), puede fijarse a algunos materialesIncapacidad para inactivar priones |
| Ozono | Permite esterilizar material sensible a temperatura (<50°C) y humedadNo tóxico (se genera a partir de oxígeno y agua), no precisa aireaciónAprobado por la FDA para los instrumentos de metal y de plástico, incluso algunos instrumentos con lúmenesDuración ciclo ≥46min | Uso limitado clínica (no hay datos publicados sobre la compatibilidad/penetrabilidad/resistencia de la materia orgánica de materiales) y los datos de eficacia microbicida sin limitados |
Adaptado de Rutala y Weber44.
La esterilización por vapor es el método que presenta el mayor margen de seguridad por su fiabilidad, consistencia y letalidad. El vapor destruye los microorganismos por coagulación irreversible y desnaturalización de las enzimas y proteínas estructurales. El principio básico de la esterilización en autoclaves de vapor es la exposición del material a la temperatura requerida a una presión determinada durante un tiempo especificado. Para lograr la penetración y la difusión del vapor dentro de la cámara es necesario eliminar previamente el aire de la cámara. Esto se puede conseguir de forma pasiva, por gravedad (autoclaves gravitatorios), o de forma activa, mediante pulsos de vapor y extracción por una bomba de vacío, que es la que utilizan de forma habitual los autoclaves en el ámbito hospitalario. Para detectar fugas de aire o extracción insuficiente del aire de la cámara que originarían ciclos de esterilización no efectivos se utiliza la prueba de Bowie&Dick. Las temperaturas más comúnmente utilizadas para la esterilización por vapor son 121 y 132-134°C. La presión debe ser mayor para alcanzar temperaturas más altas (por ejemplo, 1,05bar para 121°C y 2bar para 134°C). Desde el punto de vista de la duración de los ciclos para alcanzar la esterilización, a mayor temperatura es necesario menor tiempo de exposición (a 121°C el tiempo de exposición necesario es de 20min y a 134°C, de 3,5min), y a temperaturas constantes, los tiempos de exposición van a variar dependiendo del tipo de material, de si el material está envuelto o no y del tipo de esterilizador. Con objeto de minimizar la duración de los ciclos y poder utilizar el material en el menor tiempo posible, se definieron los ciclos «Flash». Este tipo de esterilización es una modificación de la esterilización a vapor convencional en el que el material a esterilizar se coloca sin envolver en una bandeja abierta o en un recipiente o envoltura especialmente diseñados para permitir una rápida penetración del vapor de agua7.
Para reprocesar material crítico sensible al calor o a la humedad deben usarse métodos de esterilización a baja temperatura. Estos métodos provocan la muerte de los microorganismos por la acción de agentes químicos, bien por oxidación química (mecanismo utilizado por los peróxidos, el ácido peracético o el gas plasma de peróxido de hidrógeno), bien por alquilación (mecanismo utilizado por el óxido de etileno o el formaldehído).
El óxido de etileno se utiliza desde los años cincuenta como agente esterilizante a baja temperatura. Tiene una excelente actividad microbiocida, gran poder de difusión y penetrabilidad, y es relativamente económico. Los rangos operativos son concentración de gas (450-1.200mg/l), temperatura entre 37-63°C, humedad relativa 40-80% y tiempo de exposición de 1-6h. Dentro de ciertas limitaciones, el aumento de la temperatura y de la concentración del gas puede reducir el tiempo de exposición necesario para lograr la esterilización7.
El peróxido hidrógeno gas plasma es una tecnología que se empezó a comercializar en 1993. Su mecanismo de acción se basa en una primera fase de difusión de gas de peróxido de hidrógeno y la posterior generación en una cámara de vacío, mediante radiofrecuencia o energía de microondas, de radicales libres que son capaces de interactuar con los componentes esenciales de las células (enzimas, ácidos nucleicos) inactivando los microorganismos7,44,45.
El mecanismo de acción del peróxido hidrógeno vaporizado se basa en la difusión del peróxido de hidrógeno en fase vapor seco. No precisa necesariamente de cámara de vacío44,45.
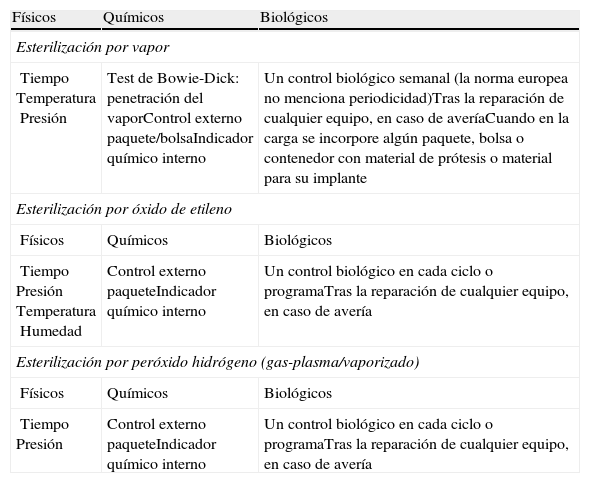
Control del proceso de esterilizaciónPara garantizar el proceso de esterilización es necesario comprobar los parámetros físicos del ciclo (controles físicos), verificar los parámetros críticos en el interior de los envases (controles químicos) y certificar la capacidad letal del ciclo de esterilización (controles biológicos). En la tabla 5 se especifican los controles indicados para cada tipo de esterilización46.
Controles de calidad del proceso de esterilización
| Físicos | Químicos | Biológicos |
| Esterilización por vapor | ||
| TiempoTemperaturaPresión | Test de Bowie-Dick: penetración del vaporControl externo paquete/bolsaIndicador químico interno | Un control biológico semanal (la norma europea no menciona periodicidad)Tras la reparación de cualquier equipo, en caso de averíaCuando en la carga se incorpore algún paquete, bolsa o contenedor con material de prótesis o material para su implante |
| Esterilización por óxido de etileno | ||
| Físicos | Químicos | Biológicos |
| TiempoPresiónTemperaturaHumedad | Control externo paqueteIndicador químico interno | Un control biológico en cada ciclo o programaTras la reparación de cualquier equipo, en caso de avería |
| Esterilización por peróxido hidrógeno (gas-plasma/vaporizado) | ||
| Físicos | Químicos | Biológicos |
| TiempoPresión | Control externo paqueteIndicador químico interno | Un control biológico en cada ciclo o programaTras la reparación de cualquier equipo, en caso de avería |
La enfermedad de Creutzfeldt-Jakob (ECJ) es una enfermedad neurodegenerativa que se puede propagar a través de los instrumentos contaminados utilizados previamente en un paciente infectado. Solo se han registrado 4 casos en todo el mundo que implican instrumentos neuroquirúrgicos, pero la detección de proteína priónica anormal en otros tejidos orgánicos ha extendido el riesgo de contaminación a una amplia variedad de procedimientos médicos y quirúrgicos. Los métodos convencionales de esterilización y desinfección son insuficientes en la reducción de la infectividad de priones, y las recomendaciones de la Organización Mundial de la Salud son a menudo poco prácticas. A través de modelos matemáticos se ha establecido que después de 6 ciclos de limpieza y desinfección convencional la transmisión es improbable. Las estrategias de prevención básicas incluyen la utilización de instrumentos desechables cuando sea posible y poner en cuarentena a los instrumentos no desechables hasta que se compruebe el diagnóstico, y el uso de métodos especiales para reprocesar instrumentos ante sospecha de ECJ47,48.
La elección de un procesado de material por desinfección o esterilización dependerá de 3 factores: riesgo del paciente de padecer la enfermedad (pacientes con diagnóstico confirmado o de sospecha elevada), la infectividad del tejido implicado en la instrumentación (cerebro, médula espinal, ojo y pituitaria) y el uso previsto del material.
Los instrumentos deben mantenerse húmedos después de su uso y hasta que se inicie la descontaminación, que será tan pronto como sea posible después de su uso. La alta resistencia de los priones a los métodos estándar obliga a procedimientos especiales (tabla 6) tanto en esterilización para dispositivos críticos o desinfección para los semicríticos que han tenido contacto con tejidos de alto riesgo de los pacientes de alto riesgo49.
Desinfectantes y esterilizantes eficaces sobre priones
| Desinfectantes | Esterilizantes |
| Eficaz (reducción >3 log10 en 1h a 20-55°C) | Eficaz (reducción >3 log10 de 18min a 3h) |
| Formulación específica de detergente alcalino | Autoclave 121C-132°C 1h (autoclaves de desplazamiento de gravedad) |
| Formulación específica de detergente enzimático | Autoclave 121°C 30min (autoclaves de vacío previo) |
| Clorina >1.000ppm | Autoclave 134°C 18min (autoclaves de vacío previo) |
| Cobre 0,5mmol/l y H2O2 100mmol/l | Autoclave 134°C 18min sumergido en agua |
| Tiocionato de guanidina >3M | Gas plasma H2O2 Sterrad® NX |
| H2O2 59% | Gas plasma radiofrecuencia |
| Ácido peracético 0,2% | Sulfato de sodio 2%+ácido acético 1%+autoclave 121°C 15-30min |
| Formulación específica desinfectante fenólico >0,9% | NaOH 0,09N o 0,9N 2h+autoclave a 121°C 1h (autoclaves de desplazamiento de gravedad) |
| Formulación específica CAC | H2O2 vaporizado 1,5-2mg/l |
| Sulfato de sodio 2%+ácido acético 1% | |
| NaOH ≥ 1N | |
| Metaperiodato sódico 0,01M |
CAC: compuestos de amonio cuaternario; H2O2: peróxido de hidrógeno; M: molar; N: normal; NaOH: hidróxido de sódio.
Adaptado de Rutala y Weber49.
Los autores declaran no tener ningún conflicto de intereses.
Sección acreditada por el Consell Català de Formació Continuada de les Professions Sanitàries. Consultar preguntas de cada artículo en: http://www.eslevier.es/eimc/formacion