La dispepsia funcional es un trastorno muy frecuente, cuyos mecanismos fisiopatológicos todavía no son bien conocidos y sobre la que los procinéticos parecen tener utilidad. El objetivo del presente estudio fue evaluar el efecto procinético de cinitaprida en pacientes con dispepsia funcional tipo dismotilidad y enlentecimiento del vaciamiento gástrico.
MétodosDe forma aleatoria, 19 pacientes recibieron 1mg de una solución oral de cinitaprida t.i.d. o placebo durante 4 semanas en dos periodos consecutivos, según un diseño cruzado y a doble ciego. La variable principal fue la media del cambio en el tiempo de vaciamiento gástrico a la mitad respecto al valor basal tras ingesta líquida, a las 4 semanas de tratamiento, cuantificado mediante ecografía de alta resolución en tiempo real.
ResultadosAl finalizar el tratamiento, la media del tiempo de vaciamiento gástrico a la mitad disminuyó para ambos tratamientos, sin diferencias estadísticamente significativas entre ellos (p=0,8720). Esta disminución resultó mayor para cinitaprida respecto a placebo (p=0,0169) cuando se analizó a los pacientes con un vaciamiento de leve a moderadamente enlentecido. Para este grupo de pacientes, cinitaprida resultó estadísticamente superior a placebo en el área bajo la curva porcentual del área antral y en el porcentaje de días libres de náuseas. La administración de cinitaprida fue bien tolerada, con un perfil de seguridad comparable a placebo.
ConclusionesCinitaprida oral es segura, facilita el vaciamiento gástrico y mejora la sintomatología clínica en pacientes con dispepsia funcional tipo dismotilidad y enlentecimiento del vaciamiento gástrico leve-moderado.
Functional dyspepsia is a highly common disorder. The physiopathological mechanisms of this entity are not yet completely known and prokinetic drugs seem to be useful. The aim of this study was to evaluate the prokinetic effect of cinitapride in patients with dysmotility-like dyspepsia and delayed gastric emptying.
MethodsNineteen patients were randomized to receive 1mg of an oral solution of cinitapride t.i.d or placebo for 4 weeks in two consecutive periods, following a crossover and double-blind design. The main variable was the mean change from baseline after 4 weeks of treatment in gastric-emptying half-time after a liquid test meal, measured by real-time ultrasonography.
ResultsAt the end of treatment, the mean gastric-emptying half-time decreased with both treatments, with no statistically significant differences between them (ANOVA, p=0.8720). This decrease was greater for cinitapride than for placebo (ANOVA, p=0.0169) in patients with mild-to-moderate delayed gastric emptying. In this group of patients, cinitapride was also superior to placebo in the percentage AUC of the antral area and the percentage of days free of nausea. Cinitapride was well tolerated, with a safety profile comparable to that of placebo.
ConclusionsOral cinitapride is safe and effective in improving gastric emptying and symptoms in patients with dysmotility-like dyspepsia and mild-to-moderate delayed gastric emptying.
En general, con el término dispepsia se engloba un conjunto de síntomas originados en el tracto digestivo superior y que incluyen plenitud posprandial que produce molestia, dolor epigástrico, ardor epigástrico y saciedad precoz. Estos síntomas pueden ser continuos o intermitentes, y estar relacionados o no con la ingesta. La prevalencia de esta patología en la población general llega hasta el 40% y representa un motivo frecuente de consulta médica1. La dispepsia funcional es un diagnóstico de exclusión, una vez realizada una endoscopia digestiva alta que descarte una causa orgánica subyacente. Esta afección es el diagnóstico más prevalente entre los pacientes dispépticos que acuden a las consultas de atención primaria. Las causas y los mecanismos fisiopatológicos de la dispepsia funcional probablemente sean múltiples, y todavía son poco conocidos, e incluyen: alteraciones de la motilidad digestiva, la regulación autonómica y la sensibilidad visceral y alteraciones psicológicas, como ansiedad y estrés2. En función de que el síntoma predominante sea el dolor o el malestar (disconfort), los llamados criterios de Roma II clasifican la dispepsia funcional en dispepsia tipo ulcerosa y dispepsia tipo dismotilidad3. En los recientemente publicados criterios de Roma III2, se ha establecido una nueva clasificación diagnóstica: síndrome de dolor epigástrico y síndrome de molestia posprandial, asimilables a la dispepsia tipo ulceroso y dispepsia tipo dismotilidad, respectivamente.
En cuanto al tratamiento de la dispepsia funcional, una reciente revisión sistemática concluye que los antagonistas H2, los inhibidores de la bomba de protones y los procinéticos son más eficaces que el placebo en el alivio o la remisión de los síntomas4. Los fármacos procinéticos se han utilizado mucho en el tratamiento de la dispepsia funcional a partir de la evidencia del subgrupo de pacientes con hipomotilidad del estómago y vaciamiento gástrico enlentecido. Además, desde un punto de vista teórico, los síntomas inducidos por la distensión gástrica (secundaria a la hipersensibilidad visceral del estómago) podrían beneficiarse de un vaciamiento gástrico más rápido. Los resultados publicados con domperidona o cisaprida son muy variables. En un metaanálisis5, se concluyó la eficacia de ambos fármacos en relación con placebo, aunque estos datos deben tomarse con cautela. El uso de cisaprida, además, actualmente está suspendido en muchos países debido a efectos adversos en la repolarización cardíaca6. La utilidad de los procinéticos parece ser mayor en la dispepsia funcional tipo dismotilidad que en la de tipo ulceroso7. Así, algunos autores han considerado su uso en este tipo de dispepsia como grado de recomendación B (hay moderada evidencia según investigaciones para apoyar la recomendación)8.
La cinitaprida es un fármaco agonista selectivo de los receptores serotonérgicos 5-HT4 y antagonista de los receptores 5-HT2 y dopaminérgicos D29. Su efecto terapéutico está en su capacidad de aumentar el tono del esfínter esofágico inferior y de su potente actividad gastrocinética, lo que produce aumentos significativos en el vaciamiento gástrico. La farmacocinética de cinitaprida, así como su perfil de eficacia y seguridad, se ha revisado ampliamente10. Cinitaprida, comercializada en España desde 1990, actualmente está aprobada para el tratamiento de la dispepsia tipo dismotilidad leve-moderada y como tratamiento coadyuvante del reflujo gastroesofágico en pacientes en quienes los inhibidores de la bomba de protones se hayan mostrado insuficientes. La incidencia de efectos adversos con la pauta posológica de 1mg t.i.d. recogida durante los casi 15 años de experiencia clínica ha sido muy baja y no muy distinta de placebo en los estudios comparativos realizados. A diferencia de la cisaprida, la administración de cinitaprida se ha asociado a la aparición de trastornos de la repolarzación cardíaca9.
El objetivo del presente estudio fue evaluar el efecto procinético de cinitaprida en pacientes con dispepsia funcional tipo dismotilidad y enlentecimiento del vaciamiento gástrico.
Pacientes y métodosPacientesEste ensayo clínico, aleatorizado, cruzado, a doble ciego y controlado con placebo, incluyó a 19 pacientes de ambos sexos con dispepsia tipo dismotilidad y vaciamiento gástrico enlentecido tras ingesta líquida, objetivado mediante ecografía de alta resolución en tiempo real. Siguiendo los criterios de Roma II, los pacientes debían presentar, como síntoma principal, molestias (no dolor) localizadas en la parte alta del abdomen, de intensidad leve o moderada, y de duración ≥ 2 días a la semana durante, al menos, los 6 meses previos a la inclusión en el estudio. Otros criterios de inclusión fueron la ausencia de hallazgos físicos y/o de laboratorio clínicamente relevantes en la visita de selección y constantes vitales y electrocardiograma (ECG) dentro de los límites de la normalidad. Los criterios de exclusión fueron los siguientes: historia de cualquier condición clínica relevante que desaconsejase la participación en el estudio a juicio del investigador; historia de abuso de drogas y/o alcohol o consumo actual de alcohol > 50g/día; fumadores de más de 20 cigarrillos al día; consumo excesivo de café, te y/o chocolate; presentar lesiones en la endoscopia de selección; acidez y/o regurgitación, gastroparesia diabética o gastroparesia grave; síndrome del intestino irritable; evidencia de hernia de hiato >3cm, o historia de cirugía esofágica, gástrica o intestinal; consumo de cualquier fármaco en investigación en los 3 meses anteriores a la primera administración del fármaco; consumo de inhibidores de la bomba de protones, antagonistas de los receptores H2, prostaglandinas o sucralfato en las 2 semanas previas a la inclusión en el estudio; consumo de antiinflamatorios no esteroideos (AINE), corticoides o bisfosfonatos en las 4 semanas previas a la inclusión en el estudio y consumo de antieméticos, fármacos adrenérgicos, anticolinérgicos, antagonistas del calcio, eritromicina o procinéticos en los 7 días anteriores a la inclusión en el estudio; necesidad de tratamiento con ketoconazol, itraconazol, miconazol o macrólidos; mujeres embarazadas, en periodo de lactancia, o mujeres sexualmente activas que no utilizasen un método anticonceptivo de barrera o anticonceptivos de tipo hormonal de forma estable durante los últimos 6 meses. El estudio, realizado en el Departamento de Medicina Interna y Salud Pública de la Universidad de Bari (Italia) entre enero de 2003 y noviembre de 2005, siguió lo establecido en la Declaración de Helsinki y las normas de buena práctica clínica y fue aprobado por el Comité Ético del centro y por las autoridades reguladoras pertinentes. Todos los participantes dieron su consentimiento por escrito antes de su participación en el estudio.
TratamientosLos pacientes recibieron cinitaprida (Cidine® 0,2mg/ml, solución oral) y placebo durante 4 semanas, en 2 periodos consecutivos siguiendo un diseño cruzado. Así, de los 19 pacientes incluidos en el estudio, se asignó aleatoriamente a 10 pacientes a la secuencia placebo-cinitaprida y 9, a la secuencia cinitaprida-placebo, con un periodo de blanqueo de 1 semana entre ambos tratamientos. Los pacientes recibieron cinitaprida 1mg t.i.d. en forma de 5ml de solución oral y placebo (t.i.d.) en forma de una solución oral de aspecto galénico idéntico para asegurar el doble ciego. Los días en que se realizaba la ecografía en tiempo real, el tratamiento se administraba a las 8.00 de la mañana en ayunas bajo supervisión del equipo investigador. Se instruyó a los pacientes a tomar el tratamiento 15min antes del desayuno, la comida y la cena los días en que lo tomaban de forma ambulatoria.
Procedimientos del estudioEn la visita de selección, realizada como máximo 2 semanas antes del inicio del primer periodo de tratamiento, se realizó la historia clínica y la exploración física, determinaciones analíticas (hematología, bioquímica, análisis de orina y test de embarazo en mujeres), ECG y registro de la medicación concomitante. Además, se realizó la ecografía en tiempo real tras ingesta líquida y se utilizó una escala verbal tipo Likert de 4 categorías (0=ausente, 1=leve, 2=moderado, 3=intenso) para evaluar la intensidad de los síntomas propios de la dispepsia. Tanto la ecografía como la escala verbal se consideraron como evaluaciones basales del primer periodo. Posteriormente, se realizaron dos visitas (una visita basal y otra a las 4 semanas de tratamiento) en ambos periodos de tratamiento. En la visita basal de cada periodo, se registró el posible consumo de medicación concomitante y acontecimientos adversos, se entregó al paciente la medicación del estudio y el diario para anotar diariamente los síntomas y, en el segundo periodo, se realizó la ecografía y la evaluación de los síntomas. En la visita después del tratamiento de cada periodo, además de lo especificado para la visita basal, se realizaron exploración física, medición de constantes vitales, ECG, determinaciones analíticas y revisión del diario del paciente.
Mediciones ecográficasPara realizar el estudio del vaciamiento gástrico tras ingesta líquida se realizó una ecografía de alta resolución en tiempo real con un ecógrafo (Tosbee, Toshiba Inc., Tokyo) con un transductor convexo de 3,75MHz de frecuencia. Todas las exploraciones fueron realizadas tras ayuno durante la noche por la misma persona y registradas en vídeo. Las mediciones se realizaron del siguiente modo: la anchura en relajación del antro se midió en dos cortes, uno sagital en el que se visualizaban simultáneamente el antro, la vena mesentérica superior y la aorta, y otro longitudinal que incluía el píloro y la zona media del antro a una distancia, como máximo, de 5cm del píloro. Las mediciones así definidas se realizaron a los tiempos establecidos en el protocolo del estudio, entre la consecución de dos ondas peristálticas. Luego, se midió también una contracción antral, definida ecográficamente como un adelgazamiento de la pared del músculo antral acompañado de la máxima reducción del área antral, seguido de la relajación de la pared muscular y el aumento del área antral. A partir de este concepto, se definió la frecuencia de contracción antral como el número de contracciones antrales observadas visualmente durante 2min. El tiempo de vaciamiento gástrico a la mitad se calculó en relación con la ingesta de un preparado comercial (Nutridrink®, 200ml) y se definió como el tiempo en minutos en que el área antral vuelve a la mitad de su valor basal (50%) tras la ingesta del preparado.
Variables de eficaciaComo variable principal del estudio se definió la media del cambio en el tiempo de vaciamiento gástrico a la mitad respecto al valor basal tras ingesta líquida, a las 4 semanas de tratamiento. Las variables secundarias fueron las siguientes: media del cambio respecto al valor basal a las 4 semanas de tratamiento del área antral mínima, del área bajo la curva (AUC) porcentual del área antral sobre el área máxima (AUC% del área antral) y la frecuencia de contracción del área antral. También se realizó la evaluación diaria de los síntomas propios de la dispepsia (plenitud abdominal, saciedad precoz, distensión abdominal, náusea) (mediante la cumplimentación por parte del paciente de la escala verbal descrita en el apartado de procedimientos) y la media de consumo de antiácidos para cada grupo de tratamiento.
SeguridadSe evaluaron la tolerabilidad y la seguridad de los tratamientos, mediante la recogida de los acontecimientos adversos (AA), y las constantes vitales, exploración física, ECG (frecuencia cardíaca e intervalos PQ, RR, QRS, QT y QTC calculado mediante la fórmula de Bazet: QT/RR1/2) y determinaciones de laboratorio (hematología, bioquímica, análisis de orina).
EstadísticaSegún los resultados de un estudio similar11, se consideró que la inclusión de 20 pacientes sería suficiente para detectar una diferencia de 6min entre cinitaprida y placebo en el vaciamiento gástrico respecto al valor basal, asumiendo una desviación estándar de las diferencias de 7,35min y considerando un error tipo I del 5% bilateral, un poder del 80% y una tasa de pérdidas del 30%. En cuanto a la estadística descriptiva, las variables continuas se presentan mediante la media y la desviación estándar o mediana e intervalo; se utiliza el intervalo de confianza del 95% para indicar la precisión del estadístico. Las variables categóricas se presentan en números absolutos y porcentajes.
El análisis de la variable principal y las variables secundarias se realizó mediante un modelo ANOVA para diseños cruzados. Se estableció como nivel de significación estadística un valor de p<0,05. Todos los análisis de eficacia se realizaron por protocolo (pacientes aleatorizados, que cumplían los criterios de selección, recibieron la medicación del estudio, completaron ambos periodos de tratamiento y no presentaron desviaciones mayores del protocolo). Adicionalmente, se realizó un análisis atendiendo a la clasificación de los pacientes según el tipo de enlentecimiento del vaciamiento gástrico (leve-moderadamente enlentecido y muy enlentecido), así como un análisis para intentar establecer una posible relación entre los síntomas y el vaciamiento gástrico, tanto en situación basal como en respuesta a cinitaprida o placebo. Todos los análisis se realizaron con el paquete estadístico SAS (The Statistical Analysis Systems Institute, Carey, NC) (versión 8.0).
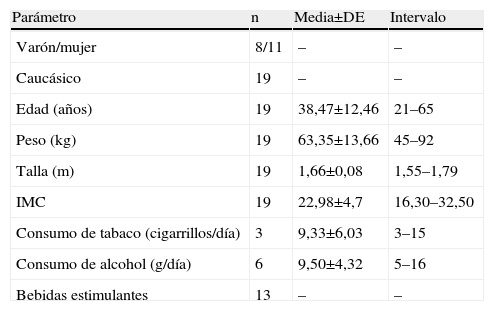
ResultadosSe incluyó un total de 19 pacientes (8 varones y 11 mujeres). Todos ellos completaron el estudio y se los analizó para seguridad, mientras que a 18, para eficacia. Las características basales fueron comparables entre ambas secuencias de tratamiento (CTP-placebo y placebo-CTP) y no se detectaron anormalidades clínicamente relevantes ni alteraciones electrocardiográficas ni en las constantes vitales en ninguno de los pacientes. Por lo que respecta al enlentecimiento en el vaciamiento gástrico, en 8 pacientes fue leve-moderadamente enlentecido (tiempo de vaciamiento gástrico a la mitad >35 y<60min) y en 10 pacientes fue muy enlentecido (tiempo de vaciamiento gástrico a la mitad ≥60min). Casi el 90% de los pacientes presentaban síntomas diariamente y éstos eran de intensidad moderada en el 79% de los casos. La tabla 1 resume las principales características basales de los pacientes.
Características demográficas basales. Población total
| Parámetro | n | Media±DE | Intervalo |
| Varón/mujer | 8/11 | – | – |
| Caucásico | 19 | – | – |
| Edad (años) | 19 | 38,47±12,46 | 21–65 |
| Peso (kg) | 19 | 63,35±13,66 | 45–92 |
| Talla (m) | 19 | 1,66±0,08 | 1,55–1,79 |
| IMC | 19 | 22,98±4,7 | 16,30–32,50 |
| Consumo de tabaco (cigarrillos/día) | 3 | 9,33±6,03 | 3–15 |
| Consumo de alcohol (g/día) | 6 | 9,50±4,32 | 5–16 |
| Bebidas estimulantes | 13 | – | – |
DE: desviación estándar; IMC: índice de masa corporal.
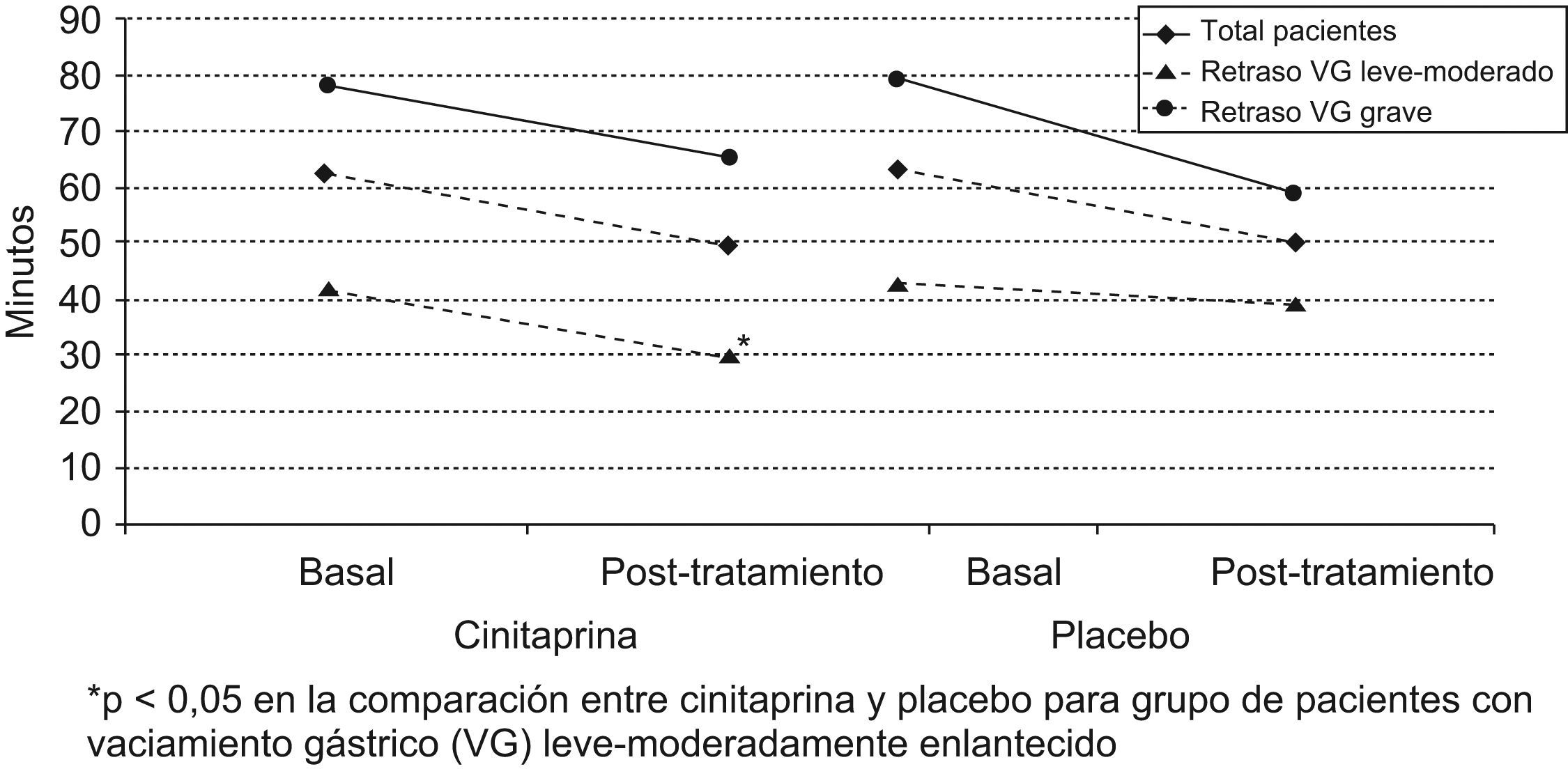
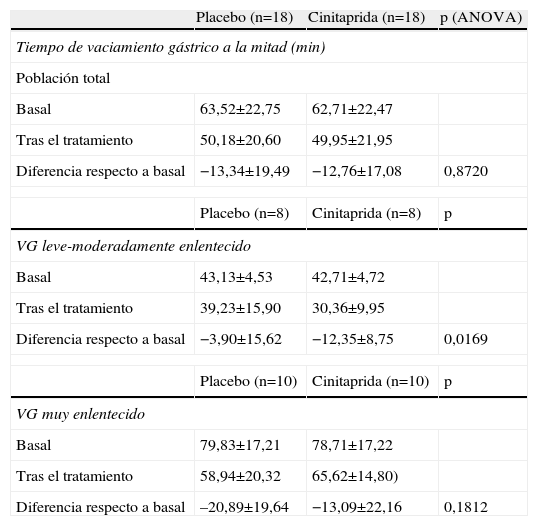
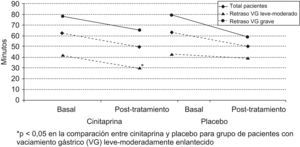
Respecto a la variable principal, considerando la totalidad de los pacientes, tras 4 semanas de tratamiento se observó una disminución de la media del tiempo de vaciamiento gástrico a la mitad respecto al valor basal para ambos tratamientos (cinitaprida y placebo), sin diferencias estadísticamente significativas entre ellos (ANOVA, p=0,8720). Cuando se analizó esta variable según la intensidad del enlentecimiento, se detectaron diferencias estadísticamente significativas favorables a cinitaprida respecto a placebo en los pacientes con vaciamiento de leve a moderadamente enlentecido (ANOVA, p=0,0169). Finalmente, el mismo análisis realizado en los pacientes con vaciamiento muy enlentecido mostró una disminución en la media de tiempo de vaciamiento gástrico a la mitad para ambos grupos respecto al valor basal, sin diferencias estadísticamente significativas entre ellos (ANOVA, p=0,1812) (tabla 2, fig. 1).
Media del tiempo de vaciamiento gástrico a la mitad por grupo de tratamiento. Población total y según intensidad del retraso
| Placebo (n=18) | Cinitaprida (n=18) | p (ANOVA) | |
| Tiempo de vaciamiento gástrico a la mitad (min) | |||
| Población total | |||
| Basal | 63,52±22,75 | 62,71±22,47 | |
| Tras el tratamiento | 50,18±20,60 | 49,95±21,95 | |
| Diferencia respecto a basal | −13,34±19,49 | −12,76±17,08 | 0,8720 |
| Placebo (n=8) | Cinitaprida (n=8) | p | |
| VG leve-moderadamente enlentecido | |||
| Basal | 43,13±4,53 | 42,71±4,72 | |
| Tras el tratamiento | 39,23±15,90 | 30,36±9,95 | |
| Diferencia respecto a basal | −3,90±15,62 | −12,35±8,75 | 0,0169 |
| Placebo (n=10) | Cinitaprida (n=10) | p | |
| VG muy enlentecido | |||
| Basal | 79,83±17,21 | 78,71±17,22 | |
| Tras el tratamiento | 58,94±20,32 | 65,62±14,80) | |
| Diferencia respecto a basal | –20,89±19,64 | −13,09±22,16 | 0,1812 |
VG: vaciamiento gástrico.Los datos expresan media±desviación estándar.
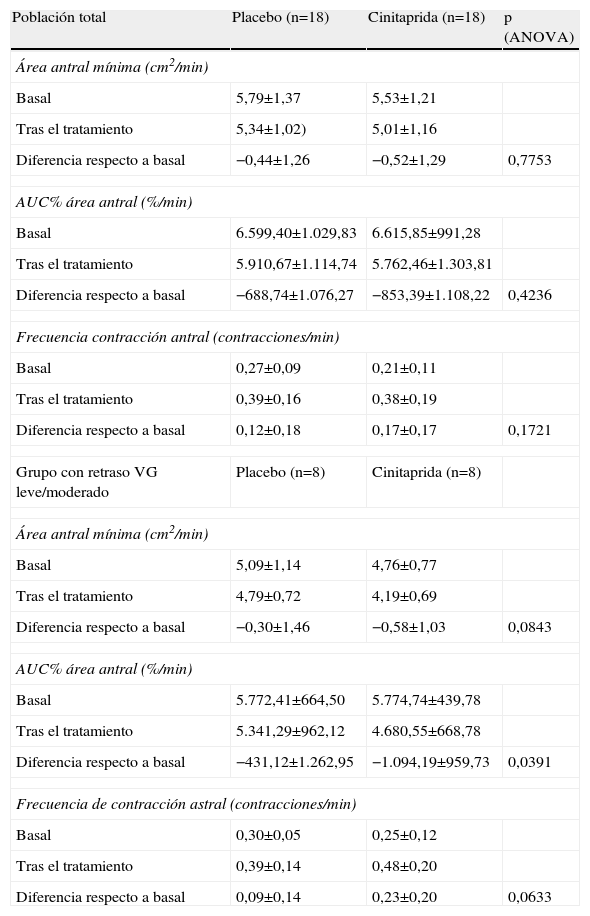
En cuanto a las variables secundarias referentes al vaciamiento gástrico (área antral mínima, AUC% del área antral y frecuencia de contracción del área antral), no se observaron diferencias estadísticamente significativas entre los dos tratamientos cuando se analizó el total de la población. En el grupo de pacientes con vaciamiento gástrico leve-moderadamente enlentecido se observaron diferencias favorables a cinitaprida, que resultaron estadísticamente significativas respecto a placebo para la disminución del AUC% del área antral (ANOVA, p=0,0391) y que mostraron una tendencia hacia una mejor respuesta para el área antral mínima (ANOVA, p=0,0843) y frecuencia de contracción antral (ANOVA, p=0,0633) (tabla 3).
Media de los valores de las variables secundarias derivadas de la ecografía
| Población total | Placebo (n=18) | Cinitaprida (n=18) | p (ANOVA) |
| Área antral mínima (cm2/min) | |||
| Basal | 5,79±1,37 | 5,53±1,21 | |
| Tras el tratamiento | 5,34±1,02) | 5,01±1,16 | |
| Diferencia respecto a basal | −0,44±1,26 | −0,52±1,29 | 0,7753 |
| AUC% área antral (%/min) | |||
| Basal | 6.599,40±1.029,83 | 6.615,85±991,28 | |
| Tras el tratamiento | 5.910,67±1.114,74 | 5.762,46±1.303,81 | |
| Diferencia respecto a basal | −688,74±1.076,27 | −853,39±1.108,22 | 0,4236 |
| Frecuencia contracción antral (contracciones/min) | |||
| Basal | 0,27±0,09 | 0,21±0,11 | |
| Tras el tratamiento | 0,39±0,16 | 0,38±0,19 | |
| Diferencia respecto a basal | 0,12±0,18 | 0,17±0,17 | 0,1721 |
| Grupo con retraso VG leve/moderado | Placebo (n=8) | Cinitaprida (n=8) | |
| Área antral mínima (cm2/min) | |||
| Basal | 5,09±1,14 | 4,76±0,77 | |
| Tras el tratamiento | 4,79±0,72 | 4,19±0,69 | |
| Diferencia respecto a basal | −0,30±1,46 | −0,58±1,03 | 0,0843 |
| AUC% área antral (%/min) | |||
| Basal | 5.772,41±664,50 | 5.774,74±439,78 | |
| Tras el tratamiento | 5.341,29±962,12 | 4.680,55±668,78 | |
| Diferencia respecto a basal | −431,12±1.262,95 | −1.094,19±959,73 | 0,0391 |
| Frecuencia de contracción astral (contracciones/min) | |||
| Basal | 0,30±0,05 | 0,25±0,12 | |
| Tras el tratamiento | 0,39±0,14 | 0,48±0,20 | |
| Diferencia respecto a basal | 0,09±0,14 | 0,23±0,20 | 0,0633 |
AUC: área bajo la curva; VG: vaciamiento gástrico.
Los datos expresan media±desviación estándar.
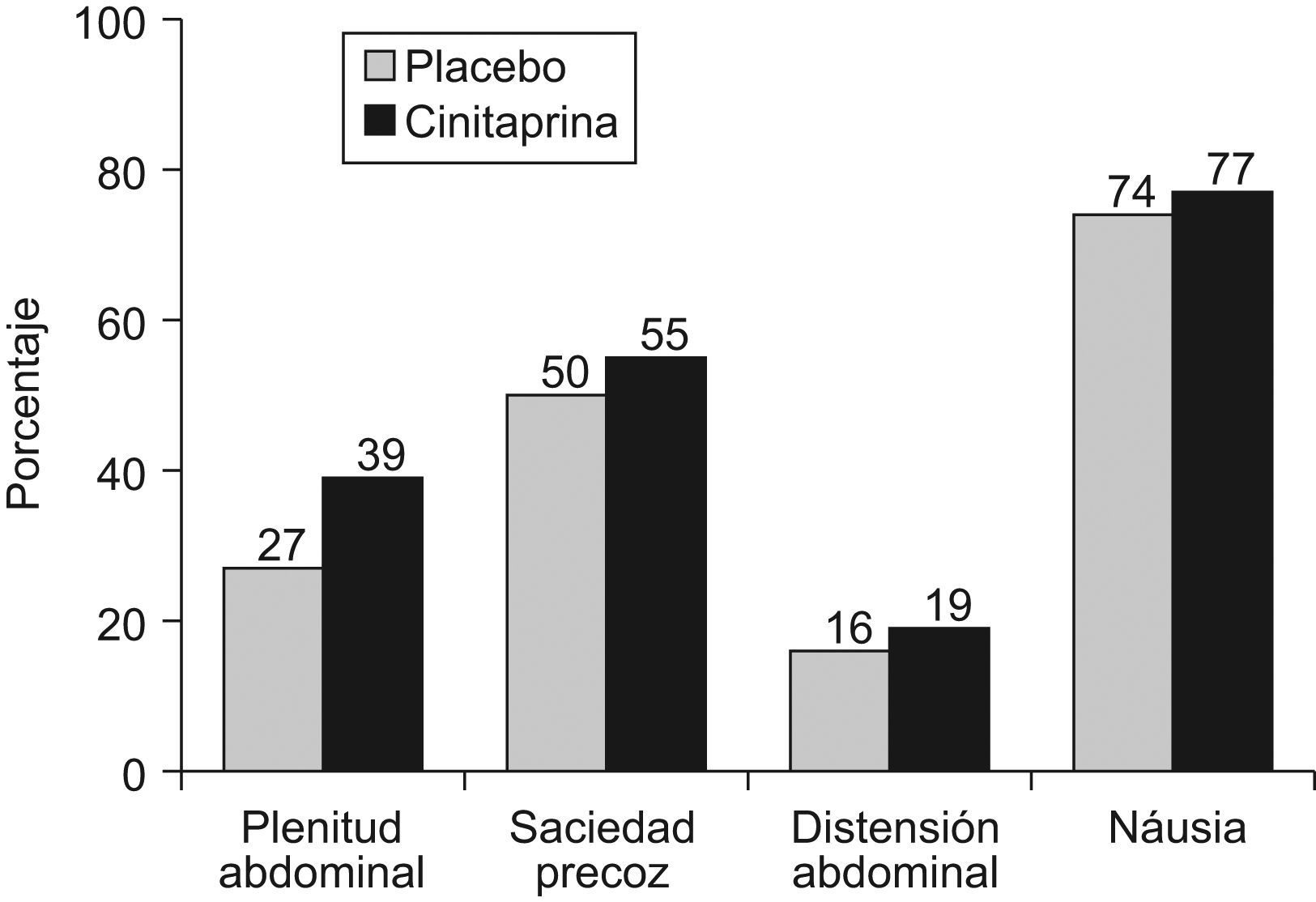
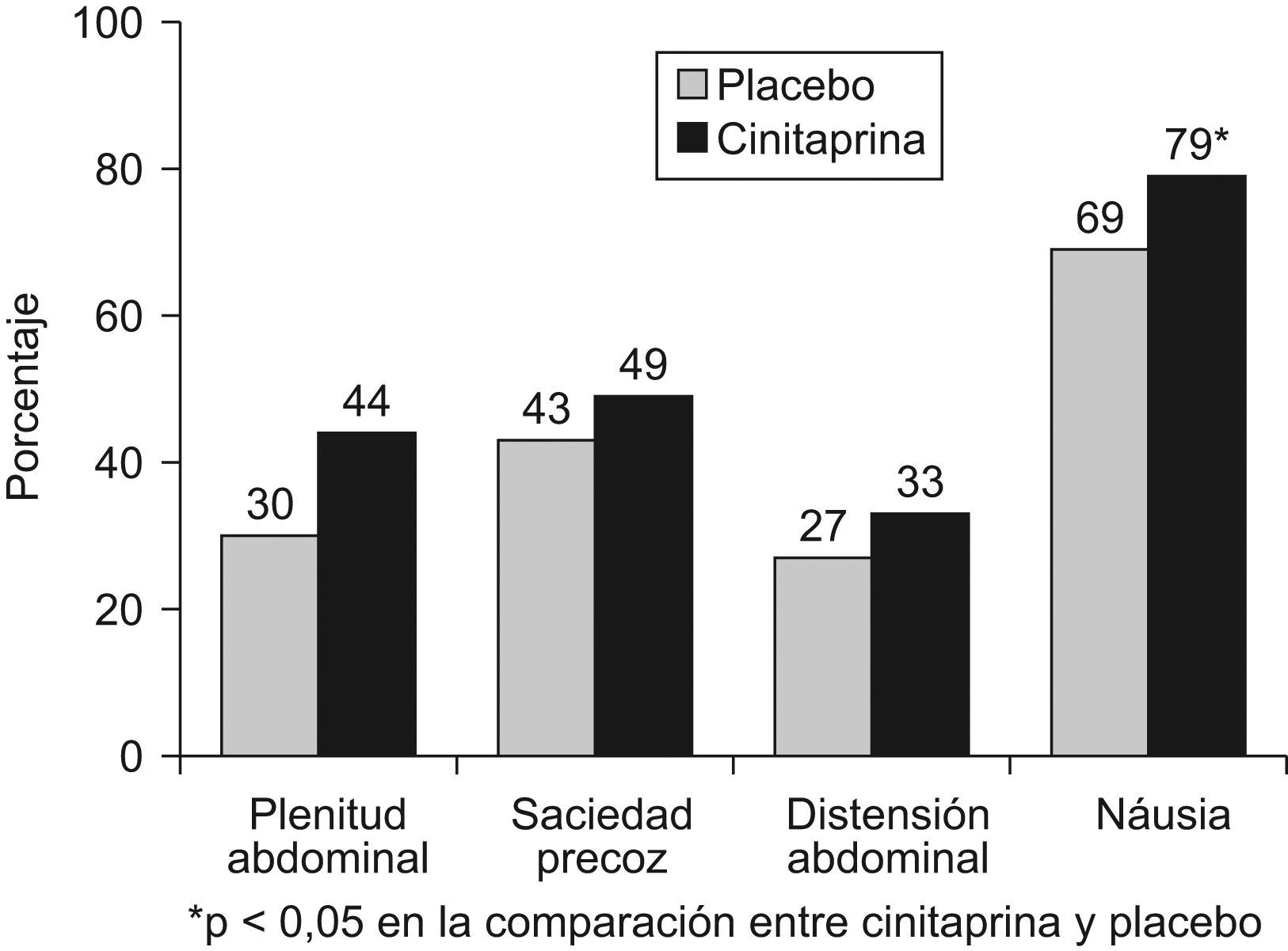
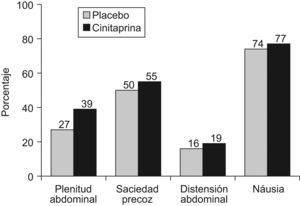
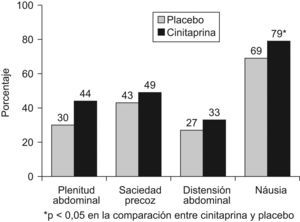
Los resultados de la evaluación diaria de los síntomas (plenitud abdominal, saciedad precoz, distensión abdominal, náusea) se muestran en las figuras 2 y 3 para el total de la población y para el grupo de pacientes con enlentecimiento leve-moderado, respectivamente. En este último grupo, cinitaprida mostró un porcentaje de días libres de síntomas significativamente mayor que placebo para las náuseas (p=0,05). Además, se observó una tendencia favorable a cinitaprida para la plenitud abdominal en las dos poblaciones analizadas (p=0,07 y 0,08 para la población total y con enlentecimiento leve-moderado, respectivamente). No se observaron diferencias entre ambos grupos de tratamiento en la media de consumo de antiácidos, que fue muy baja en ambos grupos (valor medio<0,5 dosis/día).
En cuanto al análisis para intentar establecer la relación entre los síntomas y el vaciamiento gástrico, en primer lugar se realizó una tabla de contingencia con los datos en situación basal, en la que se distribuyó a los pacientes según sus síntomas fueran leves o moderados (los ausentes y graves no podían ser incluidos en el estudio), en función de que su vaciamiento gástrico fuera leve-moderadamente enlentecido o muy enlentecido. El análisis estadístico no mostró relación entre la gravedad de los síntomas y el grado de vaciamiento gástrico en situación basal (p=0,5765, test exacto de Fisher). Este análisis se repitió con los datos obtenidos al final del estudio, sin encontrar relación entre la gravedad de los síntomas y el grado de enlentecimiento para ninguno de los dos grupos de tratamiento (p=0,2913 y p=0,7009 para placebo y cinitaprida, respectivamente; test exacto de Fisher).
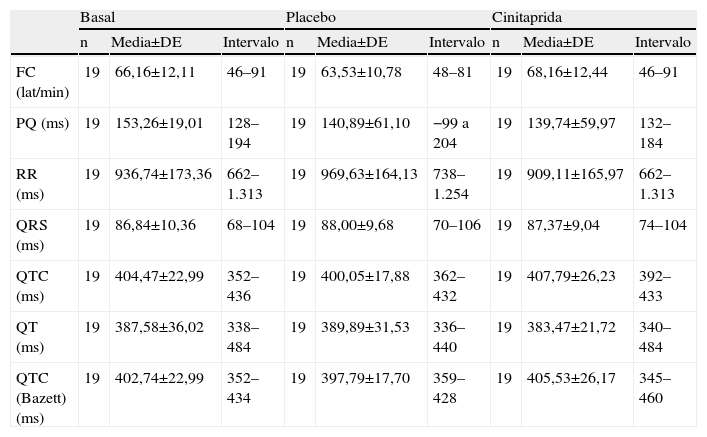
En relación con la seguridad, durante el estudio se comunicó un total de 62 AA. De ellos, 43 ocurrieron en 13 pacientes en tratamiento con cinitaprida y 28 en 11 pacientes en el grupo placebo. En cuanto a su naturaleza, los descritos con más frecuencia fueron cefalea (9 episodios en 4 pacientes en el grupo cinitaprida y 13 episodios en 4 pacientes en el grupo placebo) y faringitis (2 episodios en 2 pacientes en el grupo cinitaprida y 3 episodios en 3 pacientes en el grupo placebo). No hubo abandonos por AA ni se comunicaron AA graves durante el estudio. Al final de ambos periodos de tratamiento no se detectaron alteraciones clínicas relevantes ni alteraciones en los parámetros de laboratorio, constantes vitales ni registro electrocardiográfico. Concretamente, en referencia al análisis del ECG, al final del estudio no se observaron diferencias respecto a los valores basales para ninguno de los parámetros del ECG analizados ni alteraciones morfológicas compatibles con trastornos de conducción, ritmo, isquémicos o aparición de onda U (tabla 4).
Parámetros del electrocardiograma basales y por grupo de tratamiento
| Basal | Placebo | Cinitaprida | |||||||
| n | Media±DE | Intervalo | n | Media±DE | Intervalo | n | Media±DE | Intervalo | |
| FC (lat/min) | 19 | 66,16±12,11 | 46–91 | 19 | 63,53±10,78 | 48–81 | 19 | 68,16±12,44 | 46–91 |
| PQ (ms) | 19 | 153,26±19,01 | 128–194 | 19 | 140,89±61,10 | −99 a 204 | 19 | 139,74±59,97 | 132–184 |
| RR (ms) | 19 | 936,74±173,36 | 662–1.313 | 19 | 969,63±164,13 | 738–1.254 | 19 | 909,11±165,97 | 662–1.313 |
| QRS (ms) | 19 | 86,84±10,36 | 68–104 | 19 | 88,00±9,68 | 70–106 | 19 | 87,37±9,04 | 74–104 |
| QTC (ms) | 19 | 404,47±22,99 | 352–436 | 19 | 400,05±17,88 | 362–432 | 19 | 407,79±26,23 | 392–433 |
| QT (ms) | 19 | 387,58±36,02 | 338–484 | 19 | 389,89±31,53 | 336–440 | 19 | 383,47±21,72 | 340–484 |
| QTC (Bazett) (ms) | 19 | 402,74±22,99 | 352–434 | 19 | 397,79±17,70 | 359–428 | 19 | 405,53±26,17 | 345–460 |
DE: desviación estándar; FC: frecuencia cardíaca; PQ: duración en milisegundos desde el inicio de la onda P hasta el inicio de la despolarización ventricular (Q y R); QRS: duración en milisegundos del complejo QRS; QTC: intervalo QT corregido por la frecuencia cardíaca; QT: duración en milisegundos desde el inicio de la onda Q hasta el final de la onda T; RR: duración en milisegundos entre dos picos de la onda R de dos complejos QRS consecutivos.
Las causas y los mecanismos fisiopatológicos de la dispepsia funcional todavía son poco conocidos. Entre los que parecen tener un papel preponderante destacan las alteraciones en la motilidad gastrointestinal y la función sensorial12,13. Además se han descrito otros mecanismos fundamentales en la génesis de la dispepsia funcional entre los que cabe mencionar la inadecuada relajación del fundus gástrico tras la ingesta14.
Este estudio se diseñó con el objetivo de evaluar la actividad de cinitaprida en dosis de 1mg t.i.d., respecto a placebo, en el vaciamiento gástrico y sintomatología clínica en pacientes con dispepsia funcional tipo dismotilidad con enlentecimiento del vaciamiento gástrico.
Los resultados del estudio muestran un efecto procinético de cinitaprida en el grupo de pacientes con enlentecimiento del vaciamiento gástrico leve-moderado, en el que la administración de cinitaprida ha demostrado un efecto clínica y estadísticamente significativo en relación con placebo en la evaluación de la variable principal (tiempo de vaciamiento gástrico a la mitad) y en el AUC% del área antral, así como una tendencia hacia una mejor respuesta para el área antral mínima y frecuencia del área antral. Respecto a la valoración del porcentaje de días libres de síntomas, se observó una diferencia estadísticamente significativa favorable a cinitaprida respecto a placebo para las náuseas y una tendencia favorable a cinitaprida en la plenitud abdominal. El análisis realizado a posteriori no mostró una relación estadísticamente significativa entre la gravedad de los síntomas y el grado de enlentecimiento en el vaciamiento gástrico, ni el momento basal ni después del tratamiento, para ninguno de los tratamientos administrados. Este hecho no es nuevo y ha sido constatado por diversos investigadores. Así, en un estudio realizado en 551 pacientes con dispepsia funcional el tipo y la gravedad de los síntomas fueron semejantes en los que tenían o no el vaciamiento gástrico enlentecido15.
Las limitaciones metodológicas de algunos de los estudios realizados previamente en esta indicación han sido motivo de crítica y han contribuido a la controversia respecto a la validez de los mismos16. En este sentido, el presente estudio fue diseñado según los estándares de calidad desde el punto de vista metodológico. Así, el estudio se realizó mediante un diseño aleatorizado, a doble ciego, controlado con placebo y con un tamaño muestral adecuadamente estimado a partir de estudios previos publicados. La inclusión de los pacientes se realizó según los criterios de Roma II, que eran los que estaban en vigor en el momento de realizar el estudio. Respecto al uso de la ecografía para evaluar el vaciamiento gástrico, es bien reconocida su utilidad como técnica no invasiva, relativamente fácil de realizar, validada y reproducible, especialmente en investigación17, que constituye un método versátil y válido para evaluar el vaciamiento gástrico y la contractilidad antral18.
En el presente estudio, el efecto de cinitaprida se determinó mediante la evaluación del vaciamiento gástrico y la sintomatología clínica. El hecho de que los resultados hayan sido consistentes en ambas evaluaciones les confiere una mayor robustez y refuerza tanto el grado de recomendación B conferido a la cinitaprida por algunos autores8 como la eficacia atribuida a los procinéticos en la dispepsia funcional19. Por otro lado, el hecho de que no se haya encontrado una asociación entre la gravedad de los síntomas y el grado de enlentecimiento del vaciamiento gástrico ni en el momento basal ni tras el tratamiento podría explicarse por la influencia de otros mecanismos fisiopatológicos en la aparición de la dispepsia, tal como la relajación inadecuada del fundus gástrico. De hecho, otros procinéticos con acción serotoninérgica semejante a la cinitaprida, como la cisaprida, han demostrado tener un efecto positivo en la relajación del estómago proximal14. Aún más, no incluir en nuestro estudio a los pacientes con dispepsia muy leve o muy grave es posible que haya dificultado encontrar diferencias en la variable del vaciamiento gástrico.
Ensayos realizados con otros procinéticos, incluyendo la cisaprida, domperidona y levosulpirida, también han demostrado la falta de correlación entre la mejoría sintomática y su efecto en el vaciamiento gástrico20,21.
La administración de cinitaprida fue bien tolerada. No hubo abandonos a causa de AA ni se comunicaron AA graves, alteraciones analíticas o electrocardiográficas durante el estudio, lo que corrobora los resultados publicados recientemente por Robert et al9 en un estudio de coadministración de cinitaprida y ketoconazol.
En resumen, la administración de cinitaprida oral a dosis de 1mg t.i.d. es segura, facilita el vaciamiento gástrico y mejora la sintomatología clínica en pacientes con dispepsia funcional tipo dismotilidad y enlentecimiento del vaciamiento gástrico leve-moderado.
Conflictos de interesesJoan Heras, Marta Robert y M. Josep Plazas son empleados de Laboratorios Amirall, SA. Marta Mas (Trial Form Support) ha coordinado y colaborado en la redacción del manuscrito por encargo de Laboratorios Almirall, S.A. Piero Portincasa y Fermín Mearin no poseen ningún conflicto de intereses en relación con este artículo.
Los autores agradecen la colaboración de Emma Albacar (Trial Form Support) en la realización del análisis estadístico.